一种基于氮硫共掺杂石墨烯负载合金纳米线复合材料电化学传感器的建构及其应用的制作方法
本发明涉及一种氮硫共掺杂石墨烯负载合金纳米线复合材料,以及所述复合材料构建的电化学传感器,所述复合材料电化学传感器可用于双氯芬酸类物质的检测。
背景技术:
双氯芬酸(diclofenac,dcf)是一种衍生于苯乙酸类的非甾体抗炎药,在医药行业中被广泛使用,它通过人或动物直接排放、排泄及医疗护理等进入水体中。因双氯芬酸在污水处理厂的降解并不完全,所以在不同水环境中(包括污水处理厂出水、河水、湖水和地下水)被频繁检测出来。也有报道表明,长时间暴露在有双氯芬酸的环境下,会导致鱼类的肾脏损害,并改变鱼鳍,从而导致鱼类的总体健康受损。因此,双氯芬酸被认为是一种新兴的污染物,逐渐得到了国内外环保工作者的广泛关注。
迄今为止,已采用多种方法测定双氯芬酸,如气相色谱-质谱法、液相色谱法、液相色谱-质谱联用质谱法、分光光度法、比色法、分光荧光法、伏安法等。与其它方法相比,电化学方法由于其操作简便、快速响应、灵敏度高,经济等优点被广泛研究。实验结果表明,基于纳米复合材料修饰电极构建电化学传感器,可以大大提高裸电极的电催化活性、增大其比表面积,有利于待测物的富集及催化,使所构建的电化学传感器具有选择性好、灵敏度高、检出限低等优点。金属纳米线因易制备、比表面积大,表面反应活性高,具有较高的催化效率以及较强的吸附能力等特性,在电化学反应中可以作为优良的电子传递媒介。然而,纳米线因尺寸较小,稳定较差,长期放置易团聚,易从电极表面脱附,影响到传感材料电化学性能的提高。故需引入其它物质作为载体,被广泛使用的载体有石墨烯、活性碳、碳纳米管、二氧化钛等。石墨烯具有超大的比表面积和卓越的机械性能,同时还具有高导电性且吸附能力强,当吸附一些其它纳米材料后,石墨烯的导电能力会有所变化,因此石墨烯基纳米复合材料可以作为构建电化学传感器的优良界面材料。但石墨烯作为载体时存在些缺点,石墨烯既不亲水又不亲油,这就增加了金属纳米材料负载到石墨烯上面的难度,因此需对石墨烯进行化学改性。
技术实现要素:
本发明针对上述现有的问题,提供了一种电化学性能和稳定性优异的氮硫共掺杂石墨烯负载合金纳米线复合材料,并将其用于修饰裸玻碳电极,构建基于氮硫共掺杂石墨烯负载合金纳米线复合材料的电化学传感器,用于制品中双氯芬酸类物质的快速检测。
本发明提出如下技术方案:
本发明提供了一种合金纳米线的制备方法,包括以下步骤:
1)室温下将含有第一金属的盐溶液加入到阳离子表面活性剂溶液中,混合均匀;
2)向步骤1)中获得的混合溶液中加入无机还原剂,室温下搅拌,静置,得到第一金属的纳米晶种;
3)按步骤1)配置混合溶液,加入含有第二金属的盐溶液和银盐溶液,混合均匀后再加入抗坏血酸混合均匀;
4)向步骤3)中获得的混合溶液中加入甲苯,搅拌均匀后加入步骤1)中所制得的第一金属的纳米晶种,恒温下反应,离心分离后得到所述合金纳米线。
较佳地,所述阳离子型表面活性剂包括十六烷基三甲基溴化铵、十六烷基三甲基氯化铵、十八烷基三甲基溴化铵和/或十八烷基三甲基氯化铵;所述无机还原剂为硼氢化钠。
较佳地,所述第一金属为金,第二金属为镍;所述第一金属的盐溶液包括haucl4·3h2o或haucl4.4h2o溶液;所述第二金属的盐溶液包括氯化镍和/或硝酸镍溶液;进一步地,所述金镍比为1:1。
较佳地,所述银盐为硝酸银。
较佳地,所述加入第一金属盐溶液:第二金属盐溶液:甲苯体积比为50:2.5:(0.8~1.5)。
较佳地,所述步骤4)中的反应温度不超过30℃。
本发明还提供了一种氮硫共掺杂石墨烯负载合金纳米线复合材料的制备方法,包括以下步骤:
1)按质量比为1:1称取氧化石墨烯和硫氰酸铵配置成溶液,混合后超声分散;
2)将步骤(1)中分散后得到的溶液置于高压反应釜中进行恒温水热反应,反应结束后冷却至室温;
3)将步骤(2)中冷却后的反应产物移出,超声分散,清洗后得到氮硫共掺杂石墨烯;
4)向清洗后的氮硫共掺杂石墨烯中加入合金纳米线,于旋涡混合器上震荡,得到氮硫共掺杂石墨烯负载合金纳米线复合材料。
较佳地,所述合金纳米线为金镍合金纳米线。
较佳地,所述氧化石墨烯和硫氰酸铵质量比为1:1。
较佳地,所述恒温水热反应的反应温度为160-200℃。
本发明还提供了一种基于氮硫共掺杂石墨烯负载合金纳米线复合材料建构的电化学传感器,包括:由氮硫共掺杂石墨烯负载合金纳米线复合材料修饰裸玻碳电极;所述基于氮硫共掺杂石墨烯负载合金纳米线复合材料构建的电化学传感器应用于双氯芬酸类物质的检测中。
本发明还提供了一种基于氮硫共掺杂石墨烯负载合金纳米线复合材料建构的电化学传感器用于双氯芬酸类物质的检测方法,包括:
向磷酸盐缓冲溶液(pbs)中加入待测样品,搅拌均匀,用计时电流法富集后,进行差分脉冲伏安法测定。
较佳地,所述pbs缓冲溶液的ph值为4~7,更优选地,ph值为5。
较佳地,所述富集电位为0~0.4v,更优选地,富集电位为0.2v;富集时间为0~140s,更优选地,富集时间为120s。
较佳地,所述差分脉冲伏安法测定的扫描速度为40~280mv/s,更优选地,扫描速度为50mv/s。
较佳地,所述差分脉冲伏安法测定的扫描范围为0~1.0v。
较佳地,修饰电极对双氯芬酸的检测限为0.3μm,线性范围为3~130μm。
本发明的有益效果是:
(1)本发明以金属纳米粒子作为晶种,采用种子生长法制备得到金属纳米棒,再以金属纳米棒作种子,使纳米棒长成纳米线,该方法相比传统的制备金属纳米线的方法(如模板法,电化学沉积法等),制备过程简单,设备简化,并具有产量高,成本低等优点;
(2)双金属合金纳米线能够克服单一纳米线金属修饰电极存在电催化活性易受干扰,易失活等不足;
(3)经氮硫原子掺杂的石墨烯,其结构特性及化学敏感度得到优化,具有更高的化学活性及稳定性,同时,掺杂了氮硫的石墨烯其表面附着金属纳米材料的能力大大增强,使得氮硫共掺杂石墨烯成为金镍合金纳米线的优良载体;
(4)采用氮硫共掺杂石墨烯负载合金纳米线复合材料构建的电化学传感器对双氯芬酸进行检测,其电催化性能良好,灵敏度高,检测误差小,检测结果具有良好的重现性。
附图说明
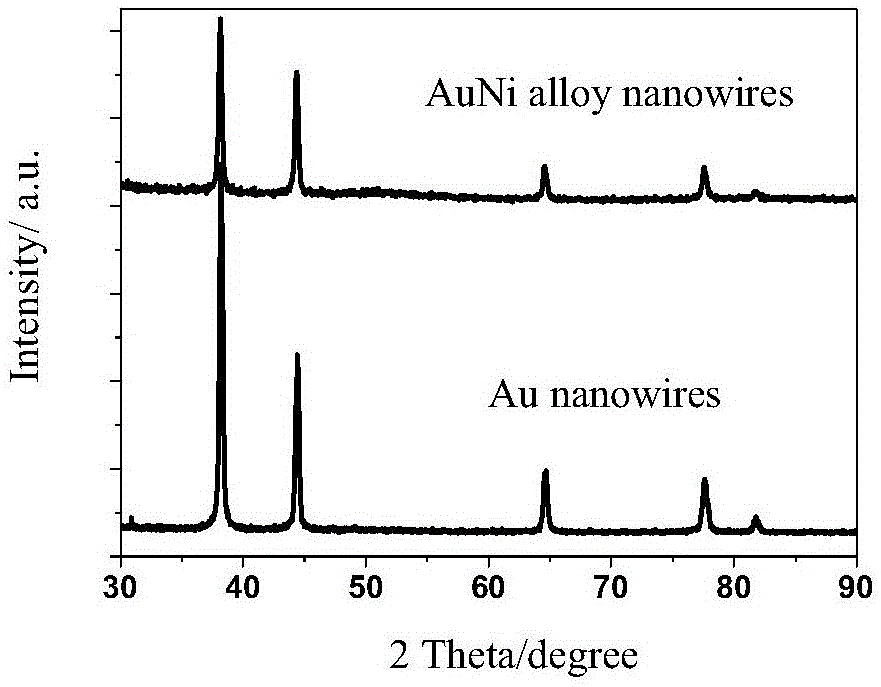
图1制备的金属纳米线的xrd图
图2gce(a),n,s-g/gce(b),n,s-g/auninws/gce(c)在含有0.5mkcl溶液与10mmfe(cn)63-溶液中的cv图
图3gce(a),n,s-g/gce(b),n,s-g/auninws/gce(c)在含有0.1mkcl溶液与5mmfe(cn)63-/4-溶液中的eis图
图4是采用本发明n,s-g/auninws复合材料修饰电极在含浓度为5×10-5m双氯芬酸的磷酸盐缓冲溶液(pbs)中(b)与空白实验(a)的cv对比图
图5n,s-g/auninws/gce在浓度为5×10-5m的双氯芬酸(0.1mpbs、ph=5)中扫第1圈(a)、第2圈(b)、第3圈(c)、第4圈(d)的cv图
图6gce(a),b-s,n-g/gce(b),n,s-g/auninws/gce(c)在浓度为5×10-5m的双氯芬酸溶液(0.1mpbs、ph=5)的cv图
图7修饰电极在5×10-5m的双氯芬酸溶液中的电流响应值与pbs缓冲溶液ph的关系图
图8双氯芬酸的电流响应值与富集时间关系图
图9双氯芬酸电流响应值与富集电位关系图
图10第二个氧化峰电流与扫描速率线性拟合图
图11不同浓度双氯芬酸的dpv图
图12双氯芬酸电流响应值(第二个氧化峰电流)与浓度的线性拟合图
图13在相同条件下,5次构建的电化学传感器重复性检测双氯芬酸的cv图
具体实施方式
下面结合附图对本发明作进一步详细说明。
实施例1auni纳米线的制备
(1)au纳米晶种的制备
在恒温下(25℃),首先将5.0ml、0.20m的十六烷基三甲基溴化铵(ctab)溶液与5.0ml、0.0005m的氯金酸(haucl4)溶液混合均匀;然后向上述混合液中加入0.6ml、0.010m冰水硼氢化钠(nabh4)溶液,搅拌2min,反应体系避光静置2h。
(2)auni纳米线的制备
向5.0ml、0.20m的ctab溶液中加入5.0ml、0.0010m的haucl4溶液混合均匀,然后加入0.2ml、0.0040m的硝酸银(agno3)溶液和250μl氯化镍溶液,混合均匀后,加入2ml、0.08m抗坏血酸;继续加入100μl甲苯,搅拌10min,加入80μlau纳米晶种。将反应体系在恒温25℃下避光静止24h,制得auni纳米线(aunws)。
将制备好的auni纳米线放入冰箱冷藏10min后,经多次离心分离,去除多余的ctab,再用蒸馏水稀释成10ml,冷藏,备用。
对比例au纳米线的制备
向5.0ml、0.20m的ctab溶液中加入5.0ml、0.0010m的haucl4溶液,混合均匀,然后加入0.2ml、0.0040m的硝酸银(agno3)溶液混合均匀,再加入70μl、0.08m抗坏血酸混合均匀;向溶液里加入100μl甲苯,搅拌10min,加入80μlau纳米晶种。将反应体系在恒温25℃下避光静止24h。
图1中的xrd衍射谱图显示auninws的2θ值相比于aunws向右移,且没有分裂成单峰,表明了auni纳米线制备成功且是以合金的形式存在。
实施例2氮硫共掺杂石墨烯负载auni纳米线复合材料(n,s-g/auninws)的制备
(1)取35ml浓度为0.5mg/ml氧化石墨烯,按氧化石墨烯与硫氰酸铵的质量比为1:1称取后配置成溶液,并在超声清洗器中混合超声30min;
(2)将超声后的溶液装入反应釜聚四氟乙烯内衬里,旋紧反应釜,把反应釜放入温度稳定在180℃的集热式恒温加热磁力搅拌器,恒温水热反应10小时后自然冷却至室温;
(3)取出反应釜内衬中的产物,超声分散,将上述超声分散好的产物置于离心机中离心清洗,直至多余的硫氰酸铵被洗脱干净,得到氮硫共掺杂石墨烯载体(n,s-g);
(4)取4ml上述制备好的载体于离心管中超声30min后,加入1ml实施例一中制备的auninws,于旋涡混合器上震荡,即可得到n,s-g/auninws复合材料。
实施例3n,s-g/auninws复合材料电化学传感器的构建及其电化学性能研究
先将玻碳电极(gce,直径3mm)用0.05μm的al2o3在麂皮上抛光成镜面,冲洗干净,晾干。用移液枪分别取5μl制备好的复合材料滴涂在裸玻碳电极表面,自然晾干。
分别以fe(cn)63-和fe(cn)63-/4-作为氧化还原探针,采用cv和eis对比不同修饰电极分别在含有0.5mkcl溶液的10mmfe(cn)63-溶液中和在含有0.1mkcl溶液与5mmfe(cn)63-/4-溶液中的电化学行为。
从图2中可以看出,与裸玻碳电极(a)相比,所有修饰电极的氧化还原峰均增大,其中n,s-g/auninws/gce(c)的氧化还原峰最大。从图3的阻抗分析图中可以得出n,s-g/auninws/gce(c)的电阻很小,几乎为零。这说明修饰n,s-g/auninws复合材料能够提供更大的比表面积,加速溶液中fe(cn)63-/4-在修饰电极表面发生电子转移,结果表明n,s-g/auninws复合材料可明显提高修饰电极的导电性。
实施例4n,s-g/auninws复合材料电化学传感器(n,s-g/auninws/gce)对双氯芬酸的检测
采用本发明n,s-g/auninws复合材料电化学传感器在含浓度为5×10-5m双氯芬酸的磷酸盐缓冲溶液(pbs)中进行cv检测,并与不含双氯芬酸的磷酸盐缓冲溶液(空白)的cv图进行对比(图5);进一步地,该复合材料修饰电极在浓度为5×10-5m的双氯芬酸(0.1mpbs、ph=5)中扫描4圈记录cv图(图6);扫描速度为50mv/s,扫描范围在0.0~1.0v。
从图4可以看出,与空白溶液相比,加入双氯芬酸后,n,s-g/auninws/gce在0.795v、0.537v、0.507v处有峰值,说明n,s-g/auninws复合材料电化学传感器对双氯芬酸具有良好的电化学响应。
由图5可以看出,扫描第1圈仅有0.795v、0.507v处有一对氧化还原峰,而扫第2、3、4圈时0.795v处氧化峰电流下降,同时在0.537v增加第二个氧化峰。这是由于双氯芬酸的电化学氧化是一个两个电子和两个质子转移的电化学机制,且属不可逆氧化反应。这是由于再次(第二圈)向正电位扫描时,由于双氯芬酸的氧化产物具有电化学活性,其可逆的氧化电势在较低的电位下形成,致使0.537v处出现第二个氧化峰。
相同条件下,与裸玻碳电极和未负载合金纳米线的氮硫共掺杂石墨烯修饰电极对双氯芬酸样品检测进行对比,由图6可知n,s-g/auninws/gce(曲线c)背景电流明显大于其它电极,这表明裸玻碳电极gce(a)和未负载合金纳米线的氮硫共掺杂石墨烯修饰电极s,n-g/gce(b)相比,n,s-g/auninws复合材料电化学传感器明显具有较高有效活性表面,是电化学测定双氯芬酸的最佳材料。
实施例5检测条件的优化
图7-10分别考察了pbs缓冲溶液ph值、富集时间,富集电位以及扫描速度对检测结果的影响,较佳地,所述pbs缓冲溶液的ph值为4~7,更优选地,ph值为5;较佳地,所述富集电位为0~0.4v,更优选地,富集电位为0.2v;富集时间为0~140s,更优选地,富集时间为120s;较佳地,所述差分脉冲伏安法测定的扫描速度为50mv/s;较佳地,所述差分脉冲伏安法测定的扫描范围为0~1.0v。且由,第二个氧化峰电流ip与扫描速度υ关系知(图10),在40~280mv/s扫描范围内,第二个氧化峰电流ip与扫描速度υ成线性关系,其线性回归方程为ip=0.0528υ+3.889,r2=0.993,说明n,s-g/auninws复合材料电化学传感器对双氯芬酸在该扫描速度范围内为吸附控制。
图11为不同浓度的双氯芬酸dpv图,随着双氯芬酸浓度的增大,其氧化峰电流也逐渐增大,且峰电位稍微向右移动。
图12为不同浓度双氯芬酸与第二个氧化峰电流的线性拟合图,根据图中的第二个氧化峰电流线性回归方程为ip=0.047c-6.899,r2=0.997,可以得出该电化学传感器对双氯芬酸的检测限为0.3μm,线性范围为3~130μm。
实施例6检测重复性考察
图13是5次制备的n,s-g/auninws复合材料电化学传感器检测同一浓度双氯芬酸的cv图,从图中可以看到,5次不同的n,s-g/auninws复合材料电化学传感器对双氯芬酸的测量峰电流、峰电位基本一致,说明采用n,s-g/auninws复合材料修饰玻碳电极来构建双氯芬酸电化学传感器具有良好的重现性。
实施例7实际样品的检测
称取50mg研磨好的双氯芬酸钠缓释胶囊,超声处理使其溶于适量的水中,然后转入50ml容量瓶中,定容到刻度。取ph=5的pbs缓冲溶液5ml于洁净的小烧杯中做底液,加入5ml该实际样品溶液,用计时电流法,在富集电位为0.2v、富集时间120s的条件下富集,再采用dpv进行测定,扫描范围为0.0~1.0v。平行测定3次,其检测结果见表1。
表1双氯芬酸钠缓释胶囊中双氯芬酸的测定
以上所述的仅是本发明的一些实施方式。对于本领域的普通技术人员来说,在不脱离本发明创造构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!