牙周疾病检测试剂盒及使用方法与流程
本发明涉及一种生物检测领域的试剂盒,特别是一种涉及牙周疾病检测试剂盒及其使用方法。
背景技术:
目前牙科在临床上对于牙周疾病的检查方法是由医师综合临床症状、口腔探诊和牙周组织检查(比如出血、口臭、牙龈外观肿胀、测定牙菌斑附着状况、牙周袋的深度、出血或牙齿的松动度)及x光图像等多种结果,进行牙周疾病的评估和诊断,都需从病理型态上观察和判断病情。
牙周疾病的早期症状通常不明显,其中牙龈炎为牙周炎的早期阶段,患者经常不自觉或往往忽视初期牙龈炎,当患者因剧烈疼痛或牙龈出血等症状到医院就诊时,病情多半已经严重,甚至有些患者盲目吃消炎药,不及时就医,导致其他口腔疾病的发生,比如智齿冠周炎、牙周炎、牙龈乳头炎等等。在牙科临床现场,也经常可见到患者的牙龈明显退缩、牙齿松动,严重者则出现牙槽骨大量吸收甚至感染,最后可能必须拔牙无法保留牙齿或牙齿脱落,严重影响患者的生活质量。因此,早期发现牙周疾病和及时治疗更显得十分重要。
然而,现有牙周疾病检查方式包括以下缺陷:主要由医生判断,而医生诊治经验丰富程度有别,无法排除主观因素,在病情的判断上仍有不够客观的疑虑;现有检测牙龈炎方式,弱点是医生只能通过临床症状诊断,导致疾病发现晚;目前尚无成熟技术及指标,判断牙周炎是否处于进展期,因此牙周炎往往错最佳控制的时机,导致其恶化到不可控制的程度。此外,就患者自身居家的口腔卫生管理而言,若是有可供患者自行检测的工具,有助于患者在家自检,及早预防牙周疾病或及时就诊治疗。
因此,在牙周疾病的检测领域里,急需开发操作简单且容易判别的试剂盒及检测方法,可供医生在临床现场快速检测,取得客观的证据判断病情;另一方面,也能让患者在家自检使用,及早察觉牙周的异常并就诊治疗。
此外,在牙周疾病的检测上,由于每个人对于疾病的病征表现可能不同,而且因为牙周炎进展期的临床炎性症状不明显,临床检测很难判断进展程度,所以用需要利用精确的分子检测,以直观反映牙周的免疫反应,防止炎症发生进一步侵染。
技术实现要素:
综合上述现有技术的缺陷,本发明提供一种试剂盒与其使用方法,以解决前述的技术问题。本发明提出的试剂盒及其使用方法,除了判断是否存在牙周疾病之外,还可以检测牙周炎是否在进展期,提供了代表性的临床证据,操作简便、快速且精确,从而提升临床预防与早期干预治疗牙周疾病的效果。
为解决上述技术问题,本发明采用的技术方案是提供一种牙周疾病检测试剂盒,包括:白细胞介素-1β特异抗体、白细胞介素-18特异抗体及至少一种固相载体。
本发明的另一目的在于提供可靠且精确的牙周疾病检测与区别牙周疾病疾病进展的试剂盒。
根据上述目的,本发明涉及一种牙周疾病检测试剂盒,其特征是:白细胞介素-1β特异抗体及白细胞介素-18特异抗体分别固定于具有不同粒径的固相载体。其中,固相载体为微米级聚苯乙烯小珠,白细胞介素-1β特异抗体及白细胞介素-18特异抗体分别与微米级聚苯乙烯小珠共价连接。此外,试剂盒进一步包括生物素耦联检测抗体及荧光素标记的链霉亲和素。
根据上述目的,本发明还提供了上述牙周疾病检测试剂盒的使用方法,包括如下步骤:将生物样本加入共价连接白细胞介素-1β特异抗体及白细胞介素-18特异抗体的微米级聚苯乙烯小珠混合,以形成第一溶液;将生物素耦联检测抗体加入第一溶液并予以混合,以形成第二溶液;将荧光素标记的链霉亲和素加入第二溶液予以混合,以形成第三溶液;通过流式细胞仪区分第三溶液中的微米级聚苯乙烯小珠;以及,依据第三溶液中的荧光强度以定量分析的方式分别得到生物样本中的白细胞介素-1β及白细胞介素-18的浓度来进行牙周病的评估及诊断。
根据本发明以细胞因子浓度判断牙周疾病程度的目的,本发明在测得白细胞介素-1β和白细胞介素-18的浓度范围后,进一步以下列定义范围判断牙周疾病的病程:当白细胞介素-1β浓度大于1000pg/ml,则判断属于牙龈炎;当白细胞介素-18浓度小于70pg/ml,且所述白细胞介素-18浓度除以所述白细胞介素-1β的比值小于0.3,则判断属于牙周炎进展期;或是当白细胞介素-18浓度小于70pg/ml,且所述白细胞介素-18浓度除以所述白细胞介素-1β浓度的比值大于0.3且小于0.5,则判断属于牙周炎的炎症期。
本发明的再一目的在于提供可靠、操作简易方便又快速的牙周疾病检测与区别牙周疾病疾病进展的试剂盒。
根据上述目的,本发明涉及一种牙周疾病检测试剂盒,其特征是:其中的固相载体为硝酸纤维膜。其中,牙周疾病检测试剂盒进一步包括胶体金标记白细胞介素-1β抗体与胶体金标记白细胞介素-18抗体;白细胞介素-1β特异抗体及白细胞介素-18特异抗体分别固定在硝酸纤维膜的不同位置。
根据上述目的,本发明还提供了上述牙周疾病检测试剂盒的使用方法,包括如下步骤:(1)制备胶体金标记白细胞介素-1β抗体;(2)制备胶体金标记白细胞介素-18抗体;(3)将生物样本接触胶体金标记白细胞介素-1β抗体与胶体金标记白细胞介素-18抗体,使生物样本中的白细胞介素-1β或白细胞介素-18分别与胶体金标记白细胞介素-1β抗体与胶体金标记白细胞介素-18抗体结合,形成样品液;(4)将样品液接触作为固相载体的硝酸纤维膜,使已结合胶体金标记白细胞介素-1β抗体的白细胞介素-1β及已结合胶体金标记白细胞介素-18抗体的白细胞介素-18,分别与硝酸纤维膜上固定的白细胞介素-1β特异抗体及白细胞介素-18特异抗体结合,从而显示对应的颜色;以及(5)依据颜色的深浅,分别确定白细胞介素-1β及白细胞介素-18的浓度范围。
附图说明
图1表示本案第一实施例的流程示意图。
图2表示本案第一实施例流式细胞仪检测的数据示意图。
图3表示本案第一实施例检测牙周炎患者治疗前后唾液中il-18变化。
图4表示本案第二实施例的流程示意图。
图5表示本案第二实施例的检测试纸条配置示意图。
图6表示本案第二实施例检测试纸条检测结果的类型示意图。
具体实施方式
为了使本发明的目的、技术特征及优点,能更为相关技术领域人员所了解,并得以实施本发明,在此配合所附的附图、具体阐明本发明的技术特征与实施方式,并列举较佳实施例进一步说明。以下文中所对照的附图,为表达与本发明特征有关的示意,并未亦不需要依据实际情形完整绘制。而关于本案实施方式的说明中涉及本领域技术人员所熟知的技术内容,亦不再加以陈述。
本发明提供一种检测牙周疾病的试剂盒及对应的使用方式,通过免疫学方法检测唾液中的两种细胞因子:白细胞介素-1β(interleukin-1beta、interleukin-1β;以下简称il-1β)及白细胞介素-18(interleukin-18,以下简称il-18)的浓度,据此可以判别牙龈炎或其他牙周疾病;同时根据检测到的两种细胞因子的浓度范围,可以进一步判别牙龈炎或牙周炎进展及被控制程度。本发明的检测牙周疾病的试剂盒可依需求应用于临床诊断或病人居家自检。
本发明所指的牙周病主要包括但不限于牙龈炎和牙周炎。牙周炎病人的龈沟液(gingivalcrevicularfluid,gcf)样本中可检测出il-1β(参考文献:journalofperiodontalresearch25(3):156-63),并且和健康对照龈沟液样本相比有显着上升(参考文献:kaohsiungjmedsci.13(10):609-17、jclinperiodontol.35(6):507-13、jclinperiodontol.200229(1):48-53)。牙周炎病人的唾液样本中,il-1β比健康对照组亦显着升高,具有统计学意义。il-18浓度和牙周炎进展显示有显着正相关(参考文献:jperiodontol.76(5):785-90、joralsci.51(2):261-6)。
依据本发明的概念,分别对三个组别的试验对象进行检测,包括:健康人对照(7例)、牙龈炎病人(5例)及牙周炎病人(7例),对这些试验对象同时收集了龈沟液及唾液进行检测。具体而言,用多重生物因子的定量免疫分析检测(multiplex)方法,同时检测了13种细胞因子。分析结果显示,在唾液样本中,牙龈炎患者对比健康人,il-1β显著升高,具有统计学意义,且其离析度最大。牙周炎患者对比健康人,只有il-18显著降低,而其它细胞因子(包括il-1β)则无显着变化。由此显示,il-1β及il-18联用,可以区别牙龈炎和牙周炎,也验证了本发明联用il-1β及il-18两种细胞因子作为生物标记的代表性。
牙龈炎,即牙周表面软组织炎症进展爆发期,单独靠il-1β即可诊断。患者及健康人对照具体结果如下:
为了实例证明本发明使用il-18和il-1β浓度合理且可靠,尤其是il-18浓度以及il-18/il-1β比值用于牙周炎(即牙周炎症进展到深层硬组织)的意义,已针对7位患者的牙周疾病进行实际分析,将他们接受检测的实测结果得到的il-18浓度以及il-18/il-1β的比值,比对医生现场诊断的结果,详如下表。
值得一提的是,上表患者5,il-18/il-1β比值0.44,介于0.3与0.5之间,依本发明定义属于牙周炎的炎症期,怀疑牙周炎发展,接着经由医生的临床检测,探测到局部牙槽骨呈角性吸收,属于牙龈炎发展成牙周炎的阶段,显示本发明对于判断牙周疾病准确且有代表性。
本发明优选使用的免疫学方法包括但不限于:基于流式细胞仪的酶联免疫方法及免疫层析法,此等免疫检测方法相关的基本原理与操作方法应当为本领域技术人员所熟知,若非必须,则不再加以详述。
由于本发明适用广泛的免疫学检测方法,因此适合针对牙科临床现场的诊治需求,采用酶联免疫方法制作试剂盒,让医院、诊所能够使用流式细胞仪进行检测,提供精确的定量分析证据,供诊治参考。同时,本发明也同样适合依据病人的自检需求或医疗院所的快检需求,采用免疫层析法,制作试纸型态的试剂盒;此种试剂盒操作简易且无侵入性,检测结果容易判读,使患者在任何地方都能使用,提高对牙周疾病的警觉性,整体提升牙周疾病的预防或及时治疗效果。
第一实施例:
本发明的一种优选实施例,是提供一种牙周疾病的检测试剂盒,其中包括:il-1β特异抗体、il-18特异抗体及至少一种固相载体,透过基于流式细胞仪的酶联免疫方法检测生物样本中il-1β和il-18,用以诊断牙周疾病(优选为牙龈炎及牙周炎),并对应判别疾病的进展程度或被控制程度。
具体而言,根据此一实施例,试剂盒中的il-1β特异抗体是固定在一种固相载体上,il-18特异抗体则另行固定在粒径大小不同的固相载体上,用于辨认并捕捉生物样本中的il-1β和il-18这两种细胞因子,以供后续检测之用。优选地,本发明il-1β特异抗体及il-18特异抗体是以共价连接的方式固定到固相载体上;且其中的固相载体优选为微米级聚苯乙烯小珠;在微米级聚苯乙烯小珠选择上,il-1β特异抗体固定在粒径5微米的聚苯乙烯小珠上,il-18特异抗体则固定在粒径7微米的聚苯乙烯小珠上。
根据此实施方式,本发明的试剂盒进一步包括生物素耦联检测抗体及荧光素标记的链霉亲和素(streptavidin)。其中,生物素耦联检测抗体是用来结合il-1β特异抗体及il-18特异抗体捕捉到的il-1β和il-18。本发明对于生物素耦联检测抗体并无特殊限制,可依需求选用市售或自制适用于流式细胞仪分析、可辨认微珠或磁珠特性的生物素耦联检测抗体。
依据本发明的优选的实施方式,第一实施例优选使用市售的微珠、抗体和标准品如下表所示。
此外,本发明对于荧光素标记的链霉亲和素亦无特殊限制,可依需求选用市售或自制适用于流式细胞仪分析、具有优良荧光讯号特性的荧光素标记的链霉亲和素,优选地,本发明适合选用藻红蛋白(phycoerythrin,简称pe)耦联链霉亲和素。除了pe,也可选用fitc或其他的荧光标记或探针,例如:apc、cy3、cy5、rhodaminered、tritc、pacificblue、所有alexafluor系列荧光标记,及上述荧光探针组合成的偶联荧光探针。
根据本发明第一实施例,以下具体说明试剂盒的使用方法,但须先言明,以下相关步骤为本领域技术人员可轻易理解的免疫学检测方法,因此使用者可依其检测当时所处的环境和检测条件,在不影响检测可靠性的基础上,适当加以调整或增减相关步骤。首先,请参考图1,步骤s11是将生物样本加入与il-1β特异抗体及il-18特异抗体共价连接的微米级聚苯乙烯小珠,使生物样本与小珠充分混合与反应,使il-1β特异抗体及il-18特异抗体能分别捕捉生物样本中的il-1β及il-18,以形成第一溶液。接着,步骤s12是将生物素耦联检测抗体加入第一溶液中,充分混合,使生物素耦联检测抗体结合到捕捉到的il-1β及il-18,以形成第二溶液。再接着,步骤s13是将荧光pe耦联链霉亲和素加入第二溶液,充分混合,使pe耦联链霉亲和素结合到生物素耦联检测抗体,以形成第三溶液。最后,步骤s14是将第三溶液通过流式细胞仪,流式细胞仪以前向角散射(forwardscatter,fsc)及侧面散射(sidescatter,ssc)区分第三溶液中的两种粒径不同的微米级聚苯乙烯小珠,步骤s15是并依据第三溶液中的荧光强度,定量分析生物样本中的il-1β及il-18。依此方法,即可精确检测生物样本中il-1β及il-18的浓度。优选地,基于本发明检测口腔疾病的应用,前述生物样本为唾液。
本发明再举一实验例详细说明第一实施例的操作步骤,详述如下。
1、准备混合微珠
1)、取il-18及il-1β捕获微珠(13×),超声1分钟;而后涡旋(vortex)30秒。
2)、计算所需微珠体积。每管反应需要25微升混合微珠,另需算入因使用排枪损失的体积。比如,50管反应需要1.5毫升混合微珠;96管反应需要3毫升混合微珠;以此类推。
3)、以准备1.5毫升混合微珠为例:吸取115微升il-18及il-1β捕获微珠(13×)置于一个干净的1.5毫升塑料管,再加入1.27毫升缓冲液组合(biolegend740368)中的实验缓冲液(assaybuffer)。
2、准备洗液
1)、平衡缓冲液组合中的20倍洗液(washbuffer)到室温,充分混合令所有溶质溶解。
2)、用475毫升去离子水稀释25毫升20倍洗液。该1倍洗液可放置于2-8℃,保持1个月。
3、准备标准品
1)、用250微升实验缓冲液溶解冻干的炎症因子标准品,在室温放置10分钟。
2)、而后转移至1.5毫升试管,此管为最高浓度标准品(c7)。
3)、另取6个试管,分别标记c6,c5,c4,c3,c2及c1。
4)、移取75微升实验缓冲液至此六管。从c7中取25微升标准品加入c6管中获得1:4稀释标准品,充分混匀后即得到c6标准品。
5)、以此类推,用此连续稀释法制备c5,c4,c3,c2及c1标准品。用实验缓冲液做0pg/ml标准品(c0)。标准品具体浓度如下表所示:
4、实验流程
1)、开始实验以前,所有试剂平衡至室温(20℃-25℃),避光备用。为保证结果可靠性,所有标准品和样品都要做复管。计算所需微孔数目。
2)、加入25微升实验缓冲液至所有微孔(v底96孔板)。
3)、加入25微升标准品至对应微孔(注意保持复孔平行性)。
4)、加入25微升样品至对应微孔(注意保持复孔平行性)。
5)、加入25微升混合微珠至所有微孔(加入微珠以前,充分摇晃试管保证均一性)。
6)、加入25微升检测抗体至所有微孔。
7)、用铝箔包裹96孔板避光。室温下,将96孔板置于孔板震荡器震荡(约600转每分钟)2小时。
8)、之后,每孔直接加入25微升缓冲液组合中的sa-pe。
9)、用铝箔包裹96孔板避光。室温下,将96孔板置于孔板震荡器继续震荡(约600转每分钟)30分钟。
10)、离心96孔板(1000g,5分钟)。
11)、用排枪吸去上清,小心不要扰动底部微珠。
12)、每孔加入200微升1x洗液,将96孔板置于孔板震荡器震荡(约600转每分钟)1分钟以充分混匀。之后离心96孔板(1000g,5分钟)。移去上清。
13)、每孔加入200微升1x洗液,排枪吹打混匀。
14)、在流式细胞仪上检测样品,读取数据。
15)、根据微珠大小区分il-1β(5微米)及il-18(7微米)。根据相应标准曲线,算出il-1β及il-18浓度。
根据上述实验例,由流式细胞仪检测的结果示意如图2,利用流式细胞仪侧面散射光通道(sidescatter,ssc-a)及正前方散射通道(forwardscatter,fsc-a),两种大小的微珠聚集在两个不同的群落里,可以明显的被区分开。较小的微珠(5微米)用来标记il-1β,位于左下方;较大的微珠(7微米)用来标记il-18,位于右上方。
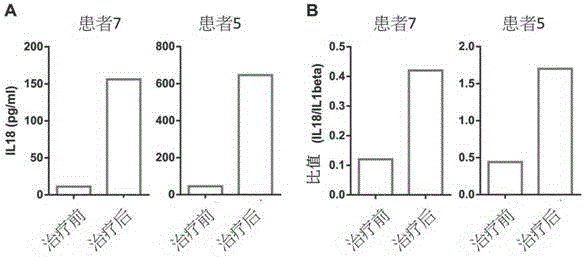
为了进一步确认以本发明以特异抗体结合微珠检测il-18作为牙周炎标记物的灵敏性,延续比较两名牙周炎患者(即前文曾列表说明的患者5及患者7)治疗前后的情况(唾液样本分别取于治疗前一周及治疗后一周)。如图3所示,实施相应牙周炎治疗(改良gracey刮治术)后,两名患者的il-18均有显着上升(a),由低于70pg/ml(患者7为11.10pg/ml;患者5为44.95pg/ml),升至高于100pg/ml(患者7为155.99pg/ml;患者5为645.99pg/ml)。不仅如此,il-18/il-1β比值也有显着升高(b)。
第二实施例:
本发明的另一种优选实施例,是提供一种牙周疾病的检测试剂盒,其中包括:il-1β特异抗体、il-18特异抗体及至少一种固相载体,透过基于免疫层析法的使用方法检测生物样本中il-1β和il-18,用以诊断牙周疾病(优选为牙龈炎及牙周炎),并对应判别疾病的进展程度或被控制程度。
具体而言,根据此一实施例,试剂盒中的il-1β特异抗体和il-18特异抗体,il-1β特异抗体是固定在一种固相载体上,il-18特异抗体则是固定在同一个固相载体上的不同位置。其中,固相载体优选为硝酸纤维膜。关于固定位置的选择,可将两种特异抗体用点状、条带状、区块的方式固定在固相载体的不同位置上,不加以特别限制。更具体而言,本发明于实施时,适合因应试剂盒的用途和改良,广泛用于各式免疫层析方法适用的固定方式,比如条带状的固定适合用于试纸检测,点状或区块状的固定适合用于芯片或陈列式分析等等。优选地,为了便于解释本发明精神,此实施例先以条带状的固定方式为例,继续说明。
在此实施例中,使用的免疫层析方法优选为胶体金免疫层析方法,也就是使用胶体金(colloidalgold)原理显色,以显示生物样本中il-1β和和il-18的侦测结果。基于此原理,试剂盒中进一步包括标记不同粒径胶体金颗粒的il-1β抗体与il-18抗体,以下分别称为:胶体金标记il-1β抗体及胶体金标记il-18抗体。优选地,前述il-1β抗体标记的胶体金粒径为40纳米,il-18抗体标记的胶体金粒径为150纳米。胶体金标记il-1β抗体及胶体金标记il-18抗体可在制造时用吸附的方式固定在硝酸纤维膜上形成结合垫供生物样本滴入反应,也可以采用溶液试剂的方式依需求在现场制备,本发明优选实验例使用溶液试剂的方式制备胶体金标记il-1β抗体及胶体金标记il-18抗体。
依据本发明优选的实施方式,第二实施例优选使用市售的抗体、胶体金和相关试剂、耗材如下表所示。
1、制备胶体金标记il-1β抗体
1)、将edc和sulfo-nhs加去离子水配成10毫克/毫升溶液。
2)、移取1)中配好的20微升edc溶液,加入1毫升40纳米胶体金悬液中。
3)、在此混合液中加入1)中配好的40微升sulfo-nhs溶液
4)、涡旋混合后,在室温旋转孵育30分钟。
5)、3800转/分钟离心10分钟。
6)、移弃上清,底部沉淀的胶体金颗粒团用1毫升试剂盒所附反应缓冲液重悬。
7)、涡旋保证胶体金颗粒充分重悬。
8)、加入50微克il1β捕获抗体,涡旋混匀。
9)、室温旋转孵育1小时。
10)、加入10微升试剂盒所附quencher封闭,室温旋转孵育10分钟。
11)、3800转/分钟离心10分钟。移弃上清,底部沉淀的胶体金颗粒团用1毫升试剂盒所附反应缓冲液重悬,涡旋充分混匀。
12)、重复11)以去除所有未反应抗体。
13)、3800转/分钟离心10分钟。移弃上清,底部沉淀的胶体金颗粒团用1毫升试剂盒所附复合物稀释液重悬,涡旋充分混匀。
14)、放置于4℃备用。
2、制备胶体金标记il-18抗体
1)、将edc和sulfo-nhs加去离子水配成10毫克/毫升溶液。
2)、移取1)中配好的8微升edc溶液,加入1毫升150纳米胶体金悬液中。
3)、在此混合液中加入1)中配好的16微升sulfo-nhs溶液
4)、涡旋混合后,在室温旋转孵育30分钟。
5)、2000转/分钟离心5分钟。
6)、移弃上清,底部沉淀的胶体金颗粒团用1毫升试剂盒所附反应缓冲液重悬。
7)、涡旋保证胶体金颗粒充分重悬。
8)、加入25微克il18捕获抗体,涡旋混匀。
9)、室温旋转孵育1小时。
10)、加入5微升试剂盒所附quencher封闭,室温旋转孵育10分钟。
11)、2000转/分钟离心5分钟。移弃上清,底部沉淀的胶体金颗粒团用1毫升试剂盒所附反应缓冲液重悬,涡旋充分混匀。
12)、重复11)以去除所有未反应抗体。
13)、3800转/分钟离心10分钟。移弃上清,底部沉淀的胶体金颗粒团用1毫升试剂盒所附复合物稀释液重悬,涡旋充分混匀。
14)、放置于4℃备用。
3、检测唾液中il1β及il18
1)、100微升唾液与10微升il1β胶体金抗体及10微升il-18胶体金抗体混合。室温轻柔摇动,反应5分钟。
2)、检测试纸条样品垫一端伸入上述混合液中。由于毛细效应,20分钟后胶体金迁移完成。
3)、检测结果包多种类型,条带有无和深浅的显示,示意如图6。其中,类型10表示检测结果正常、类型11表示检测出牙龈炎、类型12表示检测出牙龈炎及牙周炎倾向、类型13表示检测出牙周炎、类型14无任何条带显示,表示检测失效,必须重新检测。
此实施例的试剂盒的制备,优选适合选用一般的胶体金免疫层析产品制程,亦可依需求调整,以提高检测的可靠性并节省制造成本。简言之,不同粒径的胶体金标记il-1β抗体与胶体金标记il-18抗体,可吸附在硝酸纤维膜上,并且与前述固定有il-1β特异抗体与il-18特异抗体的硝酸纤维膜组装成检测试纸条型态如图5,供简便检测之用。
关于优选的检测试纸条100的具体制备方式请参考图5。检测试纸条100由三部分构成:样品垫d、硝酸纤维膜及吸水垫a。在硝酸纤维膜上,按顺序以1微升/厘米的距离均匀以特定抗体打上检测线,其中检测线1为il-18检测线(il-18特异抗体);检测线2为il-18控制线(羊抗兔igg抗体);检测线3为il-1β检测线(il-1β特异抗体);检测线为il-1β控制线(羊抗鼠igg抗体)。静置晾干后,装上样品垫d及吸水垫a后,即成为检测试纸条100,可供检测唾液之用。
根据本发明第二实施例,以下具体说明试剂盒的使用方法,但须先言明,以下相关步骤为本领域技术人员可轻易理解的免疫学检测方法,因此使用者可依其检测当时所处的环境和检测条件,在不影响检测可靠性的基础上,适当加以调整或增减相关步骤。请参考图4,本实施例的牙周疾病检测试剂盒的使用方法包括的步骤为:步骤s41是制备胶体金标记il-1β抗体;步骤s42是制备胶体金标记il-18抗体;步骤s43是将生物样本接触胶体金标记il-1β抗体与胶体金标记il-18抗体,使生物样本中的il-1β或il-18分别与胶体金标记il-1β抗体与胶体金标记il-18抗体结合,形成样品液;步骤s44是将样品液接触硝酸纤维膜,使已结合胶体金标记il-1β抗体的il-1β及已结合胶体金标记il-18抗体的il-18,分别与硝酸纤维膜上固定的il-1β特异抗体及il-18特异抗体结合,从而显示对应的颜色;步骤s45是依据颜色的深浅,分别确定il-1β及il-18的浓度范围。
其中,所谓接触是指将生物样本用各种方式进入样品垫的吸收孔隙中进行毛细作用而移动,优选的生物样本是液体生物样本,因此可依照使用者操作方便,将生物样本倒入或沾湿样品垫,或用各式吸管工具转移滴到样品垫上,也可将样品垫浸入液体样本中。
将生物样本接触样品垫后,其中已结合胶体金标记il-1β抗体的il-1β及已结合胶体金标记il-18抗体的il-18,会透过毛细作用移动,并且分别对应与预先以条带方式固定在硝酸纤维膜上不同位置的il-1β特异抗体及il-18特异抗体辨识与结合,从而使胶体金富集,产生显色的作用,在特定的条带位置显示对应的颜色,条带处显示的颜色分别代表il-1β及il-18,即可用以评估和判别牙周疾病的进展。
由第二实施例的使用方法可知,本发明的操作简单,可随时随地进行,并可快速得到结果。
基于上述的两个实施例可知,本发明的试剂盒适合应用在各种免疫检测方法,同步检测il-1β及il-18的浓度范围,做为临床诊治或自检的证据
此外,基于本发明针对的细胞因子il-1β与il-18,主要用途是检测牙周疾病,因此,前述的生物样本泛指人体内部或分泌的各种血液、体液,其中包括但不限于从口腔采检的体液样本,优选为唾液。
由于特异抗体的搭配和选择可能影响试剂盒的可靠性及灵敏度,关于细胞因子特异抗体的来源选用有不同考虑。本发明对于il-1β特异抗体与il-18特异抗体,或是胶体金标记il-1β抗体与胶体金标记il-18抗体所选用的抗体,并无特殊限制。根据以上第一、第二实施例,本发明可依据制造者的实际制造需求和产品的性能表现选用适合的抗体。比如,il-1β特异抗体与il-18特异抗体可选用市售的细胞因子特异抗体,或是自制的细胞因子特异抗体;胶体金标记il-1β抗体与胶体金标记il-18抗体亦可选用市售已标记的胶体金标记细胞因子抗体,或是自制的胶体金标记细胞因子抗体。只要抗体的特异性符合辨识细胞因子的特异性需求,即适用于本发明。
根据本发明另一实施例,若是在临床现场采检,则可进一步先处理生物样本,提升定量分析的精确效果和可靠性。优选地,若以唾液样本为例,取得待测的唾液后,进行冷冻保存-20℃待分析时再取出备用,在唾液样本分析前,进行离心处理,随后再进行特定细胞因子检测取得结果。
根据本发明另一实施例,以唾液、牙龈炎和牙周炎进展程度为例,根据实证资料,病人唾液中细胞因子的浓度分布代表了不同并成的牙龈炎、牙周炎,优选的界定方式之一为采用细胞流式仪微珠法,病人在治疗前测得的il-1β及il-18的浓度特征界定如下:
(1)il-1β>1000pg/ml,为牙周软组织炎症进展爆发期,判断属于牙龈炎。(2)il-18<70pg/ml且il-18/il-1β<0.3,为牙周硬组织炎症进展期(侵袭骨组织牙周炎),判断属于牙周炎进展期。(3)il-18<70pg/ml且0.3<il-18/il-1β<0.5,疑似牙周组织炎症发展倾向,判断属于牙周炎的炎症期,建议进一步检查。
当病人接受治疗后,再用本发明提出的试剂盒和方法检测,以判读病人的病情控制情况,浓度特征界定如下:
接受治疗后,il-1β<1000pg/ml,视为牙龈炎被控制(临床治愈);接受治疗后,il-18>100pg/ml,为牙周炎被控制(临床治愈)。
另一优选的界定方式之一为采用胶体金层析法,病人在治疗前测得的il-1β及il-18的浓度特征请参考图6,以代表il-1β及il-18条带的有无和深浅界定,结果10为正常;结果11为牙龈炎;结果12为牙龈炎及牙周炎倾向;结果13为牙周炎;结果14上无条带代表试剂和失效,需要重新检测。
从以上说明可知,本发明突破性的运用科学检验的方法,对于牙周疾病的进展程度进行识别,为临床提供证据。
以上所述仅为本发明之较佳实施例,并非用以限定本发明之权利范围;同时以上的描述,对于相关技术领域之专门人士应可明了及实施,因此其他未脱离本发明所揭示之精神下所完成的等效改变或修饰,均应包含在申请专利范围中。
- 还没有人留言评论。精彩留言会获得点赞!