一种FGF23检测试剂盒及其制备方法与流程
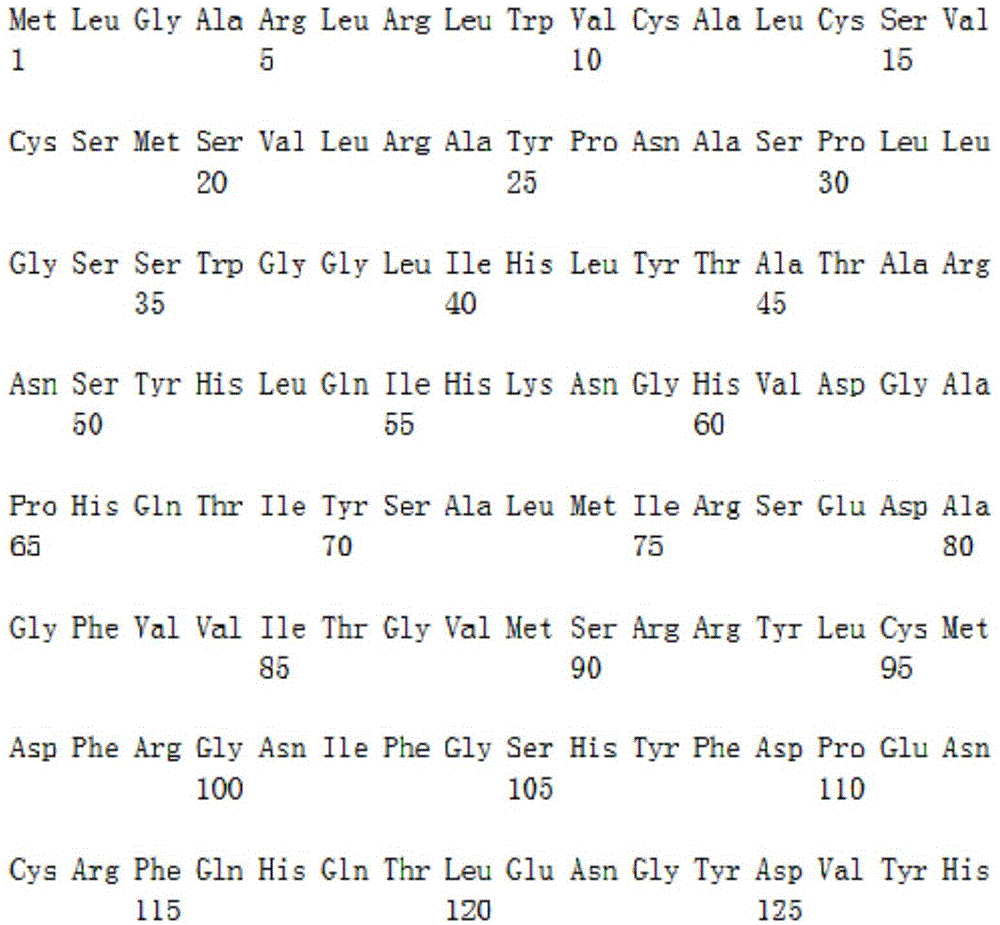
本发明属于试剂盒技术领域,尤其涉及一种fgf23检测试剂盒及其制备方法。
背景技术:
fgf23(成纤维样细胞生长因子23)是一个功能蛋白分子,含251个氨基酸残基,分子量32kda,在蛋白分子179位精氨酸和180位丝氨酸之间经蛋白酶水解成n-末端和c-末端两个片段。它主要是由分泌细胞分泌,用于调节磷酸盐和1,25(oh)2d代谢。
fgf23是最近发现的相关蛋白大家族中的新成员,其基因编码一个含250个氨基酸残基的蛋白。fgf23的n-末端(aa1-24)是疏水的且很可能作为其进入血液循环的信号肽;它的c-末端(aa180-251)与fgf蛋白家族的其它成员仅有有限的同源性。fgf23与fgf21(~24%为同源序列)和fgf19(~22%为同源序列)最接近。
肾磷酸盐流失可导致低血磷症,是骨骼矿化和生长板发展缺陷的原因之一。常染色体显性低血磷性佝偻病(adhr,一种罕见遗传疾病)患者体内携带一种fgf23突变子,该突变子可使蛋白质免受水解断裂。而且,并发瘤原性骨软化(oom)的肿瘤患者被证实有过量的fgf23mrna表达,似乎表明血液中fgf23浓度的上升是导致这类病人磷酸盐流失的原因。对啮齿动物应用重组fgf23后发现尿中磷的排泄量增加进而导致低血鳞症和骨软化/佝偻病也印证了这一结论。总之,现有文献表明fgf23直接或间接地与磷酸盐动态平衡的调节有关。
测定人体血液循环中的全段fgf23水平可能为以下不同程度的血磷酸盐流失障碍患者的实验室评估提供重要的诊断工具:瘤原性骨软化,x-链锁低血磷性佝偻病和常染色体遗传性低血磷性佝偻病。此外,对fgf23的灵敏测定可能为骨骼调节和矿化动态提供新的见解。
技术实现要素:
本发明提供一种fgf23检测试剂盒及其制备方法,目的在于测定人血清和血浆中成纤维细胞生长因子23的含量。
本发明是这样实现的,一种fgf23检测试剂盒,其特征在于,包括微孔板、fgf23校准品制剂、fgf23质控品制剂和生物素标记的兔抗fgf23多克隆抗体,所述微孔板上包被有鼠抗fgf23单克隆抗体,所述fgf23校准品制剂包括7种不同浓度的重组fgf23多肽的溶液,所述fgf23质控品制剂具有两种标定浓度的重组fgf23多肽溶液,所述生物素标记的兔抗fgf23多克隆抗体具有指定效价,该效价范围为1:4550-5050,且所述微孔板上包被的鼠抗fgf23单克隆抗体也具有指定效价,效价范围为1:950-1:1050,所述鼠抗fgf23单克隆抗体与所述兔抗fgf23多克隆抗体的用量比相同。
优选的,所述fgf23检测试剂盒内还包括检测缓冲液、终止液、清洗液和底物溶液。
优选的,所述fgf23检测试剂盒还包含有酶结合物,所述酶结合物的工作浓度为1.0-2.0μg/ml,且优选为1.5μg/ml。
优选的,所述生物素标记的兔抗fgf23多克隆抗体的具体效价优选为1:5000。
优选的,所述微孔板上包被的鼠抗fgf23单克隆抗体的具体效价优选为1:1000。
本发明是这样实现的,一种fgf23检测试剂盒的制备方法,其特征在于,主要包括以下步骤:
s1、制备fgf23多肽;
s2、制备鼠抗fgf23单克隆抗体;
s3、制备兔抗fgf23多克隆抗体;
s4、制备酶结合物溶液;
s5、制备fgf23校准品制剂;
s6、制备fgf23质控品制剂;
s7、制备包被有鼠抗fgf23单克隆抗体的微孔板。
优选的,制备所述fgf23校准品制剂或所述fgf23质控品制剂的重组fgf23多肽的氨基酸序列组成如seqidno.1所示。
优选的,所述酶结合物溶液的制备过程中包含有链霉亲和素标记的hrp,用tris缓冲液和edta的混合液将链霉亲和素标记的hrp稀释为1.0-2.0μg/ml。
优选的,所述包被有鼠抗fgf23单克隆抗体的微孔板的制备包括以下步骤:
1)取fgf23单克隆抗体,用10mmol/l的tris缓冲液(含25mol/ledta)稀释;
2)稀释后所得抗体溶液效价约为1:1000,然后向微孔板各孔中加入100ul抗体溶液,室温过夜,然后移至干燥间抽干。
与现有技术相比,本发明的有益效果是:本发明是一种fgf23检测试剂盒,采用双抗体夹心酶联免疫法,本发明的制备方法制备出的fgf23检测试剂盒使用时具有特异性、灵敏度和精密度都非常好的优点。
应当理解的是,以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围。
附图说明
图1为本发明重组fgf23多肽氨基酸的序列seqidno.1之一;
图2为本发明重组fgf23多肽氨基酸的序列seqidno.1之二;
图3为本发明实施例2中实施例2中检测方法的标准曲线图;
图4为本发明实施例2中各类健康人样本的平均值表格图;
图5为本发明实施例3中批次间差异检测结果表格图;
图6为本发明实施例3中批间检测结果表格图;
图7为本发明实施例3中稀释/线性检测结果表格图;
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
在本发明的描述中,需要理解的是,术语“长度”、“宽度”、“上”、“下”、“前”、“后”、“左”、“右”、“竖直”、“水平”、“顶”、“底”、“内”、“外”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本发明和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。此外,在本发明的描述中,“多个”的含义是两个或两个以上,除非另有明确具体的限定。
实施例1
(一)本实施例所述的fgf23检测试剂盒的主要组成成份如下:
1.微孔板
鼠抗fgf23单克隆抗体预包被的条形微孔板(12条×8孔),置于框架中,且微孔板由ps(聚苯乙烯)制作而成,具有强度高、耐疲劳性、尺寸稳定、蠕变小等优点;
2.fgf23校准品
fgf23校准品是溶于人工血清中的重组fgf23多肽溶液,其7种浓度分别为0、0.2、0.6、1.8、5、10、20pmol/l,分别标号1-7,且该fgf23校准品为冻干粉,每种浓度分装为一瓶,共有7瓶;
3.fgf23质控品
fgf23质控品是溶于人工血清中的重组fgf23多肽溶液,共设置有两种指定浓度,浓度分别为1.50pmol/l和4.50pmol/l,分别标号1和2,每种浓度分装为一瓶,共有2瓶;
4.检测缓冲液
可以直接使用的10mmol/l的tris缓冲液,共1瓶,为保证溶液可足够检测所需,检测缓冲液每瓶至少20.0ml;
5.生物素标记的兔抗fgf23多克隆抗体
可直接使用的生物素标记的兔抗fgf23多克隆抗体,共1瓶,为保证溶液可足够检测所需,生物素标记的兔抗fgf23多克隆抗体溶液每瓶至少6.0ml;
6.酶结合物
酶结合物是链霉亲和素标记的hrp(溶于含去污剂、防腐剂的tris缓冲溶液中),共1瓶,为保证溶液可足够检测所需,每瓶至少13.0ml;
7.底物溶液
可直接使用的含有四甲基联苯胺(tmb)的底物溶液,共1瓶,为保证溶液可足够检测所需,每瓶至少13.0ml;
8.终止液
可直接使用的0.18m硫酸溶液,共1瓶,为保证溶液可足够检测所需,每瓶至少7.0ml;
9.清洗液
含有去污剂和防腐剂的浓缩清洗缓冲液,共1瓶,为保证溶液可足够检测所需,每瓶至少50.0ml;
10.封板膜
孵育时密封微孔板的粘性薄膜。
所述试剂盒的制备如下:
(二)、本实施例所述的fgf23检测试剂盒的制备方法过程如下:
s1、制备fgf23多肽
fgf23多肽的氨基酸组成如seqidno:1所示,其可以通过诱导表达得到,也可以通过合成得到;
fgf23多肽通过诱导表达参照常规方法制备:获得编码fgf23的dna片段,将该片段插入pet质粒载体中,然后转化入大肠杆菌中构建重组表达菌株(pet-fgf23/bl21),再利用iptg进行诱导表达,通过ni-nta亲和层析法分离纯化融合蛋白,得到氨基酸组成如seqidno:1所示的fgf23多肽,纯度鉴定合格后即可用作抗原免疫动物;
s2、制备鼠抗fgf23单克隆抗体:
1)、对小鼠采用皮下注射方式,对其进行免疫接种,初次免疫注射1mg/ml浓度的上述fgf23抗原0.2ml/只,第3周、第4周及第5周分别注射浓度为1mg/mlfgf23抗原与不完全弗氏佐剂等体积混合溶液;免疫达到预期效果后拉颈处死小鼠,收集血液,适量分装后保存(小鼠血液,可分离血清,其中含有鼠抗fgf23多抗);
2)、同时,在生物安全柜中解剖小鼠,取其脾脏筛选淋巴b细胞,完成后与外购的骨髓瘤细胞融合,通过有限稀释法挑选目标克隆融合细胞,最后接种培养以生产单克隆抗体;
3)、取鼠抗fgf23单克隆抗体,用10mmol/l的tris缓冲液与25mol/ledta混合,得到抗体工作液,所述鼠抗fgf23单克隆抗体工作液效价为1:1000;
s3、制备兔抗fgf23多克隆抗体:
1)、取家兔采用皮下注射方式,对其进行免疫接种,初次免疫注射1mg/ml浓度的上述fgf23抗原0.2ml/只,第3周、第4周及第5周分别注射浓度为1mg/mlfgf23抗原与不完全弗氏佐剂等体积混合溶液;免疫达到预期效果后处死家兔,动脉采血,然后采用辛酸-硫酸铵法纯化即得兔抗fgf23多克隆抗体。
2)、用10mmol/l的tris缓冲液稀释兔抗fgf23多克隆抗体至浓度约1.0mg/ml,取浓度为1.25mg/ml的活化生物素(n-羟基琥珀酰亚胺生物素),按抗体稀释液:生物素=10:1体积比混合,通过化学反应将生物素与兔抗fgf23多克隆抗体交联;取制备后的生物素标记fgf23抗体,加入1%的bsa和0.018%的bronidoxl做为稳定剂和防腐剂,4℃密封保存,所述兔抗fgf23多克隆抗体工作液的效价为1:5000;
s4、制备酶结合物溶液:
1)、取链霉亲和素冻干粉0.1g,加入到10ml10mmol/ltris缓冲液中溶解混匀;
2)、取hrp固体用去离子水稀释为5mg/ml,采用简易过碘酸钠法将hrp与链霉亲和素交联。取制备后的链霉亲和素标记hrp,再加入1%的bsa、0.1%的tween20和0.0075%的bronidoxl做为稳定剂和防腐剂,取12ml分装,4℃密封保存,所述酶结合物的工作浓度为1.5μg/ml;
s5、制备fgf23校准品制剂:
取fgf23多肽,分别用10mmol/l的tris缓冲液稀释至fgf23浓度为0pmol/l,0.20pmol/l,0.60pmol/l,1.80pmol/l,5.00pmol/l,10.00pmol/l和20.00pmol/l,各取0.4ml分装,冻干后4℃密封保存;
s6、制备fgf23质控品制剂:
用10mmol/l的tris缓冲液稀释fgf23多肽,质控品1中fgf23浓度约为1.50pmol/l,质控品2中fgf23浓度约为4.50pmol/l,并加入1%的bsa和0.018%的bronidox5l做为稳定剂和防腐剂,各取0.4ml分装,冻干后4℃密封保存;
s7、制备包被有鼠抗fgf23单克隆抗体的微孔板:
取鼠抗fgf23单克隆抗体,用10mmol/l的tris缓冲液(含25mol/ledta)稀释,所得抗体溶液效价约为1:1000;然后向微孔板各孔中加入100ul抗体溶液,室温过夜,然后移至干燥间抽干,可以理解的是,此步骤须在洁净环境中完成。
(三)、其他
微孔板、底物溶液、终止液和清洗液均由其他商业公司提供。
实施例2:运用实施例1所述的试剂盒对fgf23检测
本发明所述试剂盒采用双抗体夹心酶联免疫法,是基于一种fgf23片段对包被于微孔板上的单克隆抗体结合,再与生物素标记的fgf23抗体结合的方法。
首先,加入的标本/质控品/校准品中的fgf23与微孔板中的固相抗体(鼠抗fgf23单克隆抗体)结合,然后加入生物素标记的兔抗fgf23多克隆抗体选择性结合目标物fgf23,生物素再与加入的链霉亲和素标记的hrp结合,形成酶标记的夹心复合物,经过洗涤后加入底物溶液,tmb在酶催化下显色,最后加入终止液终止反应。颜色的深浅和标本中的fgf23呈正相关。在酶标仪450nm(参考波长630nm)下测定吸光度od值。
1、使用前,将所有溶液平衡至室温(18-25℃),确定实验所需微孔板数量,每一样本设两个平行孔,另外,每轮实验共需要18孔用于校准品和质控品,将适当数量的微孔板置于塑料框架上,将未使用的微孔板条与干燥剂一起密封于铝箔袋中。具体包括以下步骤:
1)一次孵育
向适当的孔中加入50μlfgf23校准品(1-7),质控品或待测样本,再加入50μl生物素标记抗体溶液,用封口膜密封微孔板,室温孵育过夜(18-24小时)。
2)清洗
清洗缓冲溶液以浓缩缓冲溶液:蒸馏水=1:19的比例进行体积稀释,手工清洗微孔板5次,若使用自动洗板机,通常清洗5次,确保每次手工或自动清洗后将微孔中的溶液倒干净,进入下一步前,在吸水纸上拍干,弃去残余液体。
3)二次孵育
向各孔加入100μl酶结合物溶液,用封口膜密封微孔板,室温下避光孵育60±5分钟。
4)清洗
清洗缓冲溶液以浓缩缓冲溶液:蒸馏水=1:19的比例进行体积稀释,手工清洗微孔板5次,若使用自动洗板机,通常清洗5次,确保每次手工或自动清洗后将微孔中的溶液倒干净,进入下一步前,在吸水纸上拍干,弃去残余液体。
5)与生色底物溶液孵育
向各孔加入100μl底物溶液,用封口膜密封,室温下避光孵育20-30分钟。
6)终止显色反应
向各孔加入50μl终止溶液。
7)测定吸光度
在30min内以630nm为参照,测定450nm下的吸光度。
2、检测范围
如果待测样本的吸光度高于校准品7,建议将样本做1:11稀释(1+10,如10μl样本+100μl检测缓冲液)后重新检测。
3、质量控制
【参考值(参考范围)】
各类健康人样本的平均值举例如图4所示。
【检验结果的解释】
结果处理
450nm波长(参考630nm波长)读取吸光度(od值)。可以使用软件或坐标纸根据校准品的吸光度数值建立标准曲线(参见图1)。可以从这个标准曲线上获得样本的浓度。检测结果使用4参数曲线回归拟合。不同的曲线拟合方法需要用户自己评价。计算样本的最终浓度还应该考虑各自的稀释倍数。
实施例3:试剂盒质量分析
一、批次间差异:<7.0%
批次间差异:4个不同操作员使用2个不同批次的试剂盒(该试剂盒的制备和组成,使用方法如实施例1和2所示,以下实验中的用到试剂盒也同上)检测2个已知浓度fgf23参考品10次,检测结果如图5所示。
二、检测限:0.08pmol/l
检测限为0.08pmol/l,此值为20个校准品0吸光度测定平均值加两倍标准差所对应的浓度。
三、精确度≤12%
批内检测:1个操作员使用一个批次的试剂盒检测2个已知浓度fgf23参考品6次。
批间检测:4个不同操作员使用2个不同批次的试剂盒检测2个已知浓度fgf23参考品10次,检测结果如图6所示。
四、稀释/线性:回收率=96%
用本试剂盒检测筛选样本,分别挑取阳性样本血清、edta血浆、肝素血浆、枸缘酸钠血浆各一份,阴性样本血清、血浆各一份,然后用阴性血清分别以比例1:1、1:3、1:7稀释阳性样本血清,用阴性血浆分别以比例1:1、1:3、1:7稀释阳性样本edta血浆、肝素血浆、枸缘酸钠血浆,每个稀释样本作2次平行测试,计算其平均值,平均回收率=(稀释理论值-稀释测试均值)/稀释理论值(稀释理论值=原样本测试值/稀释倍数),如图7所示。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种用于检测犬副流感病毒试剂盒的制造方法与工艺
- 腹泻相关病毒多重基因检测体系及其试剂盒和应用的制造方法与工艺
- 基于POCKIT Micro荧光PCR平台的禽流感病毒H7亚型检测试剂及应用的制造方法与工艺
- 一种流行性乙型脑炎的重组酶常温扩增核酸(RT‑RPA)试纸条检测试剂盒及应用的制造方法与工艺
- 一种腺苷高半胱氨酸酶基因启动子区甲基化程度检测试剂盒及测定方法与流程
- 一种检测心肌梗死的试剂及其应用的制造方法与工艺
- 用于检测CDKN2B基因变异的试剂盒及CDKN2B基因变异率的定量检测方法与流程
- 一种CYP2C19*3基因型检测试剂盒及其检测方法与流程
- 一种CYP2C19*2基因型检测试剂盒及其检测方法与流程
- 基于高通量测序法的人类多基因突变检测试剂盒的制造方法与工艺