一种检测银杏叶提取物制剂中山梨醇和甲硫氨酸含量的方法与流程
本发明涉及药物成分检测
技术领域:
,尤其涉及一种检测银杏叶提取物制剂中山梨醇和甲硫氨酸含量的方法。
背景技术:
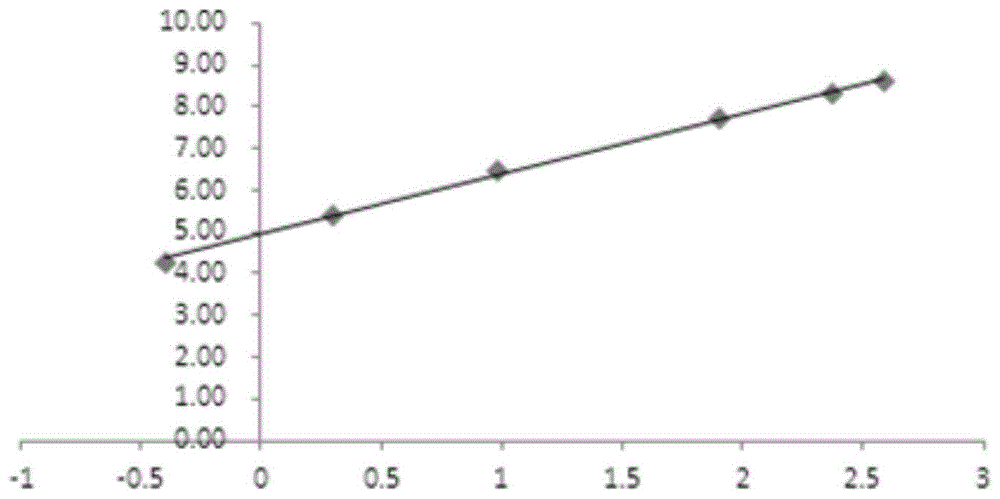
:银杏叶提取物或其制剂(例如舒血宁注射液)具有扩张血管、改善微循环的作用,常用于缺血性心脑血管疾病,冠心病,心绞痛,脑栓塞,脑血管痉挛疾病的治疗。其中舒血宁注射液作为一种银杏叶提取物制剂,其主要成分为银杏叶提取物,辅料为甲硫氨酸、山梨醇和乙醇,每1ml舒血宁注射液折合银杏叶提取物为3.5mg,其中含总黄酮醇苷0.84mg,含银杏内酯0.14mg,舒血宁注射液中的黄酮类和银杏内酯等成分含量占总固体量的大部分,但辅料的含量也需要检测和控制,以确保辅料的合理使用,增加舒血宁注射液的稳定性并降低毒副作用。银杏叶提取物制剂中的山梨醇和甲硫氨酸分别在制剂中起到助溶和抗氧化的作用,2015年版药典中采用高碘酸钠氧化-硫代硫酸钠滴定法检测山梨醇纯品,而对于含山梨醇的药材或制剂多采用紫外分光光度法和示差折光-hplc法来检测;2015年版药典中采用电位滴定法检测甲硫氨酸纯品,而对于含甲硫氨酸的制剂多采用uv-hplc法来检测;银杏叶提取物制剂中含有复杂的中药成分,采用两种检测手段分别检测甲硫氨酸和山梨醇,存在操作繁琐,周期长、检测仪器要求高以及检测成本高的问题技术实现要素:针对现有银杏叶提取物制剂中山梨醇和甲硫氨酸含量的方法存在操作繁琐,周期长、检测仪器要求高以及检测成本高的问题,本发明提供一种检测银杏叶提取物制剂中山梨醇和甲硫氨酸含量的方法。为达到上述发明目的,本发明实施例采用了如下的技术方案:一种银杏叶提取物制剂中山梨醇和甲硫氨酸含量的检测方法,所述检测方法为hplc-uv-elsd法,其中hplc的条件为:色谱柱:十八烷基硅烷键合硅胶柱;流动相:体积比为90-100:5的水-甲醇溶液;流速:0.7-0.9ml/min;洗脱方式:等度洗脱;所述uv的条件为:检测波长为200-210nm;所述elsd的条件为:漂移管温度:40-45℃;气体流量:1-1.5l/min。相对于现有技术,本发明提供的银杏叶提取物制剂中山梨醇和甲硫氨酸含量的检测方法,采用hplc-uv-elsd(液相色谱—紫外检测器—蒸发光检测器)的检测方法,通过选择上述色谱条件,可实现对成分复杂的银杏叶提取物制剂中的山梨醇及甲硫氨酸辅料同时进行定量检测,山梨醇和甲硫氨酸为分子结构和性质完全不同的两种物质,甲硫氨酸有紫外吸收现象,现有比较简便易行的检测方法为高相液色谱紫外检测法;而山梨醇是一种糖醇,无紫外吸收,虽然现有山梨醇含量的检测方法很多,但应用在测定银杏叶提取物制剂中山梨醇含量时,存在着专属性不强、操作复杂等问题,在银杏叶提取物制剂(舒血宁注射液或其它含有山梨醇和甲硫氨酸的银杏叶提取物制剂)中两者很难同时进行检测,但本发明提供的色谱条件及紫外检测器和蒸发光检测器的条件,可实现对银杏叶提取物制剂中的山梨醇及甲硫氨酸的同时定量检测,简化了检验过程,节约了分析时间,且检测的精密度和准确度高、重现性和稳定性好,可用于银杏叶提取物制剂的质量控制及综合评价,为提高和控制银杏叶提取物制剂的质量提供了可靠保障。优选的,所述流动相为体积比为95:5的水-甲醇溶液。上述优选的流动相比例,能够更好地分离杂质,利于有山梨醇和甲硫氨酸的检出,可有效改善峰形,使检测结果的准确度及精密度更高。优选的,柱温为30-40℃。优选的,所述柱温为35℃。优选的,所述流速为0.7ml/min。优选的,进样体积为10-20μl。优选的,所述等度洗脱时间为8-12min。优选的,所述uv的检测波长为205nm。优选的,所述elsd的气体流量为1.5l/min,漂移管温度为45℃。上述优选的色谱及检测器条件有利于进一步提高对山梨醇和甲硫酸氨检测的灵敏度。优选的,所述检测方法的对照品溶液中,甲硫氨酸的浓度为50μg/ml,山梨醇的浓度为1mg/ml;供试品溶液中银杏叶提取物的浓度为0.03-0.04mg/ml。上述优选的供试品溶液的浓度有利于对供试品中山梨醇和甲硫氨酸的有效分离,以及对其含量进行更准确的计算。附图说明图1是本发明实施例2中检测得到的山梨醇浓度与峰面积之间的线性关系标准曲线;图2是本发明实施例2中检测得到的甲硫氨酸浓度与峰面积之间的线性关系标准曲线;图3是本发明实施例3对舒血宁注射液中山梨醇和甲硫氨酸含量进行检测的色谱图;图4是本发明实施例4对舒血宁注射液中山梨醇和甲硫氨酸含量进行检测的色谱图;图5是本发明实施例5对舒血宁注射液中山梨醇和甲硫氨酸含量进行检测的色谱图;图6是本发明实施例6对舒血宁注射液中山梨醇和甲硫氨酸含量进行检测的色谱图;图7是本发明实施例7对舒血宁注射液中山梨醇和甲硫氨酸含量进行检测的色谱图。具体实施方式为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。为了更好的说明本发明实施例提供的检测方法,下面通过实施例做进一步的举例说明。实施例1材料与方法:仪器:agilent1100高效液相色谱仪,dikmasedex85蒸发光检测器,milli-qadvantangea10纯化水机;试剂:色谱纯甲醇,纯化水,山梨醇(中国药品生物制品检定所),甲硫氨酸(中国药品生物制品检定所);样品:舒血宁注射液(神威药业集团有限公司生产);溶液的配制对照品溶液的制备:分别取甲硫氨酸和山梨醇,精密称定,加水制成每1ml溶液含50μg甲硫氨酸和1mg山梨醇的混合溶液,即得。供试品溶液的制备:取12批次的舒血宁注射液各1ml置100ml容量瓶,加水定容,摇匀,即得。舒血宁注射液中山梨醇和甲硫氨酸含量的检测方法:分别精密吸取上述对照品溶液及供试品溶液各20μl,注入液相色谱仪,进行检测分析;具体检测条件为:色谱柱:十八烷基硅烷键合硅胶柱;流动相:体积比为95:5的水-甲醇溶液;流速:0.7ml/min;柱温:35℃;洗脱方式:等度洗脱10min;检测波长:205nm;漂移管温度:45℃;气体流量:1.5l/min。检测分析和计算得到山梨醇和甲硫氨酸含量如表1和表2所示:表1山梨醇含量检测分析结果其中,所述样品浓度为供试品溶液中山梨醇的浓度;成品浓度为舒血宁注射液中山梨醇的浓度;总固体浓度为舒血宁注射液中的总固体浓度;百分含量为舒血宁注射液中山梨醇的浓度占总固体浓度的百分比值。表1甲硫氨酸含量检测分析结果其中,所述样品浓度为供试品溶液中甲硫酸铵的浓度;成品浓度为舒血宁注射液中甲硫酸铵的浓度;总固体浓度为舒血宁注射液中的总固体浓度;百分含量为舒血宁注射液中甲硫酸铵的浓度占总固体浓度的百分比值。实施例2方法学验证与结果:线性关系考察:将对照品溶液与水分别稀释至2倍、2.5倍、5倍、10倍、20倍及40倍体积,分别精密吸取上述溶液20μl注入液相色谱仪,记录峰面积。以山梨醇进样量(μg)的常用对数为横坐标(x),峰面积的常用对数为纵坐标(y),绘制标准曲线,山梨醇的回归方程为:y=1.4397x+4.9372,r2=0.9981(n=6)。结果表明山梨醇在0.670-13.390mg范围内呈良好的线性关系,结果如表3所示,绘制得到的标准曲线如图1所示。表3山梨醇线性关系考察浓度(mg/ml)进样量(ug)峰面积0.0330.67071.20.0671.339221.300.1342.678634.000.3356.6952267.300.53610.7124113.100.67013.3905461.30以甲硫氨酸进样量(μg)为横坐标(x),峰面积为纵坐标(y),绘制标准曲线,甲硫氨酸的回归方程为:y=972.17x-0.1399,r2=1(n=6)。结果表明甲硫氨酸在0.025-0.508mg范围内呈良好的线性关系,结果如表4所示,绘制得到的标准曲线如图2所示。表4甲硫氨酸线性关系考察浓度(mg/ml)进样量(ug)峰面积0.0010.02524.40.0030.05149.500.0050.10298.400.0130.254246.700.0200.406395.700.0250.508493.20精密度试验:将稀释至5倍的对照品溶液连续进样6次,每次进样20μl,测定峰面积,测定结果见表5和表6.表5山梨醇精密度试验结果表6甲硫氨酸精密度试验结果以上结果表明,山梨醇精密度试验和甲硫氨酸精密度试验的rsd均小于2%,说明本检测方法精密度良好。重复性:取批号为170731111的舒血宁注射液6份,按照供试品溶液的制备方法制备成待测溶液,精密吸取20μl注入色谱仪,记录峰面积。计算舒血宁注射液中山梨醇和甲硫氨酸的含量,结果见表7至8。表7舒血宁注射液中山梨醇含量测定重复性试验结果表8舒血宁注射液甲硫氨酸含量测定重复性试验结果以上结果表明,山梨醇和甲硫氨酸重复性试验的rsd均小于1%,说明本检测方法的重复性良好。稳定性:重复性试验项下的舒血宁注射液(批号17073111)样品1,分别于0、0.5、1、2、4、6小时进样20μl分析,记录峰面积,结果见表9和表10。表9山梨醇稳定性试验结果表10甲硫氨酸稳定性试验结果以上结果表明,山梨醇和甲硫氨酸稳定性试验的rsd均小于2%,说明本检测方法的稳定性良好。准确度:准备对照品溶液备用;取重复性试验项下的舒血宁注射液(批号17073111)样品6,精密量取5.0ml至10ml容量瓶中,平行9份。其中,3份加入上述对照品溶液0.7ml,加水定容,作为低浓度组供试品溶液;3份加入上述对照品溶液1.4ml,加水定容,作为中浓度组供试品溶液;3份加入上述对照品溶液2.1ml,加水定容,作为高浓度组供试品溶液。分别进样上述9份供试品溶液20μl,记录峰面积,计算山梨醇和甲硫氨酸在舒血宁注射液中的加样回收率(加样回收率=实际测得量/实际加入量×100%),试验结果见表11和表12。表11山梨醇加样回收率试验结果表12甲硫氨酸加样回收率试验结果以上结果表明,山梨醇和甲硫氨酸在各浓度下的回收率均在95-105%的范围内,rsd值均小于4%,说明本检测方法准确度较好。实施例3一种舒血宁注射液中山梨醇和甲硫氨酸含量的检测方法,所述检测方法为hplc-uv-elsd法,检测条件为:色谱柱:十八烷基硅烷键合硅胶柱;流动相:体积比为95:5的水-甲醇溶液;流速:0.7ml/min;柱温:35℃;洗脱方式:等度洗脱10min;检测波长:205nm;漂移管温度:45℃;气体流量:1.5l/min。对照品溶液中,甲硫氨酸的浓度为50μg/ml,山梨醇的浓度为1mg/ml;供试品溶液为稀释100倍的舒血宁注射液(批号17080211);精密量取对照品溶液、供试品溶液各20μl,分别注入液相色谱仪,按上述高效液相色谱条件进样测定,得到的色谱图,如图3所示,具有较好的分离度。实施例4一种舒血宁注射液中山梨醇和甲硫氨酸含量的检测方法,所述检测方法为hplc-uv-elsd法,检测条件为:色谱柱:十八烷基硅烷键合硅胶柱;流动相:体积比为95:5的水-甲醇溶液;流速:0.8ml/min;柱温:35℃;洗脱方式:等度洗脱10min;检测波长:205nm;漂移管温度:45℃;气体流量:1.5l/min。对照品溶液中,甲硫氨酸的浓度为50μg/ml,山梨醇的浓度为1mg/ml;供试品溶液为稀释100倍的舒血宁注射液(批号17080211);精密量取对照品溶液、供试品溶液各20μl,分别注入液相色谱仪,按上述高效液相色谱条件进样测定,得到的色谱图,如图4所示,具有较好的分离度。实施例5一种舒血宁注射液中山梨醇和甲硫氨酸含量的检测方法,所述检测方法为hplc-uv-elsd法,检测条件为:色谱柱:十八烷基硅烷键合硅胶柱;流动相:体积比为95:5的水-甲醇溶液;流速:0.9ml/min;柱温:35℃;洗脱方式:等度洗脱10min;检测波长:205nm;漂移管温度:45℃;气体流量:1.5l/min。对照品溶液中,甲硫氨酸的浓度为50μg/ml,山梨醇的浓度为1mg/ml;供试品溶液为稀释100倍的舒血宁注射液(批号17080211);精密量取对照品溶液、供试品溶液各20μl,分别注入液相色谱仪,按上述高效液相色谱条件进样测定,得到的色谱图,如图5所示,具有较好的分离度。实施例6一种舒血宁注射液中山梨醇和甲硫氨酸含量的检测方法,所述检测方法为hplc-uv-elsd法,检测条件为:色谱柱:十八烷基硅烷键合硅胶柱;流动相:体积比为90:5的水-甲醇溶液;流速:0.7ml/min;柱温:30℃;洗脱方式:等度洗脱10min;检测波长:205nm;漂移管温度:45℃;气体流量:1.5l/min。对照品溶液中,甲硫氨酸的浓度为50μg/ml,山梨醇的浓度为1mg/ml;供试品溶液为稀释100倍的舒血宁注射液(批号17080211);精密量取对照品溶液、供试品溶液各20μl,分别注入液相色谱仪,按上述高效液相色谱条件进样测定,得到的色谱图,如图6所示,具有较好的分离度。实施例7一种舒血宁注射液中山梨醇和甲硫氨酸含量的检测方法,所述检测方法为hplc-uv-elsd法,检测条件为:色谱柱:十八烷基硅烷键合硅胶柱;流动相:体积比为100:5的水-甲醇溶液;流速:0.7ml/min;柱温:40℃;洗脱方式:等度洗脱10min;检测波长:205nm;漂移管温度:45℃;气体流量:1.5l/min。对照品溶液中,甲硫氨酸的浓度为50μg/ml,山梨醇的浓度为1mg/ml;供试品溶液为稀释100倍的舒血宁注射液(批号17080211);精密量取对照品溶液、供试品溶液各20μl,分别注入液相色谱仪,按上述高效液相色谱条件进样测定,得到的色谱图,如图7所示,具有较好的分离度。利用实施例3的检测方法对含有山梨醇和甲硫氨酸的其它银杏叶提取物制剂进行检测,检测结果与实施例3中检测的舒血宁注射液的检测效果相当。以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换或改进等,均应包含在本发明的保护范围之内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1