有机电解液和使用该电解液的锂电池的制作方法
本发明构思涉及有机电解液和包括该有机电解液的锂电池。
背景技术:
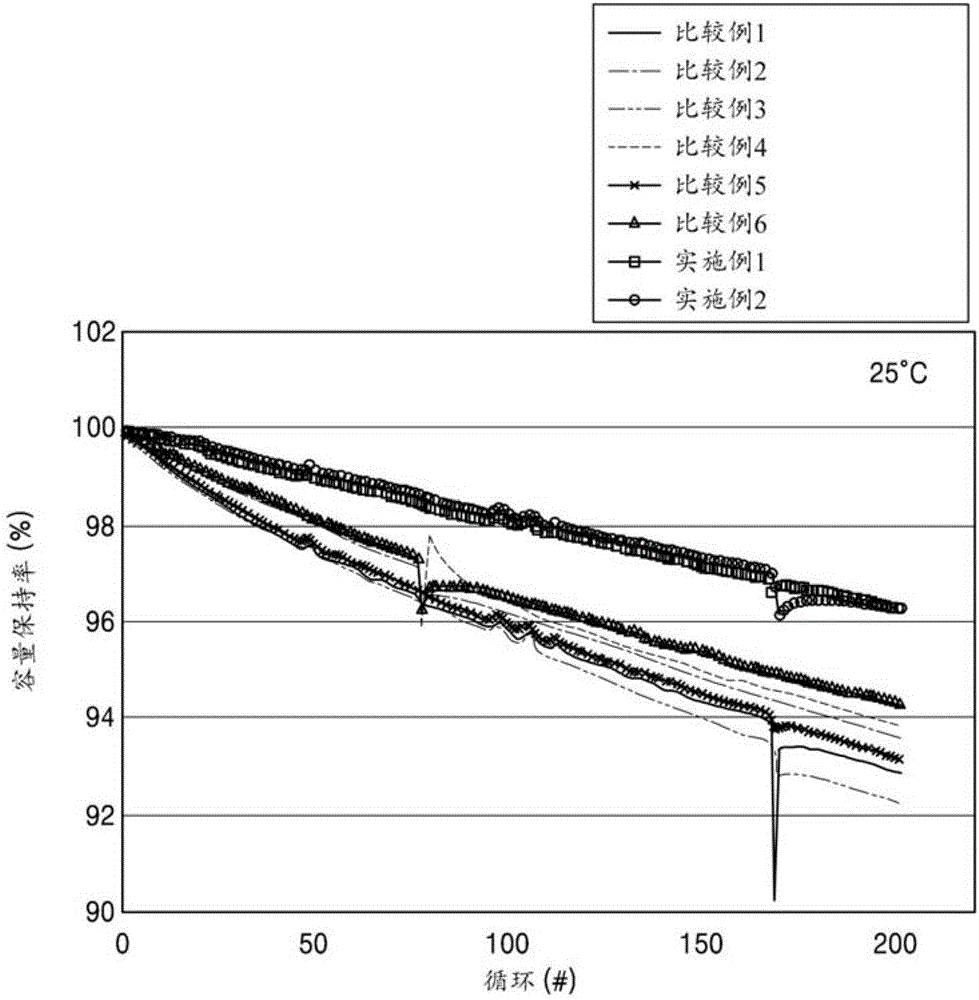
:锂电池用作便携式电子装置如摄录机、移动电话和笔记本电脑的驱动电源。可再充电锂二次电池具有的每单位重量的能量密度是常规铅-酸电池、镍-镉电池、镍-氢电池和镍-锌电池的三倍或更高,并且能够高速充电。锂电池在高驱动电压下运作,并且因而不能使用对锂高度反应性的水性电解液。大体上,将有机电解液用于锂电池中。通过将锂盐溶解于有机溶剂中制备有机电解液。具有高离子电导率、高介电常数和低粘度、同时也在高电压下稳定的有机溶剂是优选的。当碳酸盐类极性非水性溶剂用于锂电池时,在初始充电过程中可发生可逆反应,其中由于阴极/阳极和电解液之间的副反应,过量电荷被消耗。由于可逆反应,钝化层如固体电解质界面(下文称“SEI”)可形成于阳极表面上。在充电和放电过程中,锂盐与有机溶剂在电解液中反应,并且消耗有机溶剂,产生气体,以及形成具有高阻抗的固体电解质界面,并且从而降低锂电池的寿命特性。因此,需要能够抑制气体产生和形成具有低阻抗的固体电解质界面的有机固体电解液,以防止锂电池的寿命特性劣化。发明详述技术问题本发明构思提供新型有机电解液。本发明构思提供包括该有机电解液的锂电池。技术方案根据本发明构思的一方面,提供了有机电解液,其包括:有机溶剂;锂盐;由以下式1表示的硼酸盐化合物;和由以下式2表示的离子金属络合物:其中,在以上式1和2中,R1、R2和R3可各自独立地是氢;用卤素取代或未取代的C1-C5烷基基团;或用卤素取代或未取代的C1-C5氰烷基基团,其中R1、R2和R3中的至少一个可包括氰烷基基团,Me可以是选自由过渡金属和元素周期表13至15族元素组成的组的元素,M可以是金属离子,a可以是1至3的整数,b可以是1至3的整数,s=b/a,p可以是0至8的整数,q可以是0或1,r可以是1至4的整数,X1和X2可各自独立地是O、S或NR6,R4和R6可各自独立地是卤素、用卤素取代或未取代的C1-C5烷基基团、或用卤素取代或未取代的C1-C5芳基基团,以及R5可以是用卤素取代或未取代的C1-C5亚烷基基团或用卤素取代或未取代的C4-C10亚芳基基团。根据本发明构思的另一方面,提供了锂电池,其包括:阴极;阳极;和有机电解液。有利效果根据本发明构思的方面,当使用具有新型组合物的有机电解液时,可改善锂电池的寿命特性。附图描述图1a是显示在室温(25℃)下实施例1和2以及比较例1至6中制备的锂电池的寿命特性的图;图1b是显示在室温(25℃)下实施例7和8以及比较例1和7中制备的锂电池的寿命特性的图;图1c是显示在高温(45℃)下实施例7和8以及比较例1和7中制备的锂电池的寿命特性的图;和图2是根据示例实施方式的锂电池的示意图。<对附图主要部分的符号说明>1:锂电池2:阳极3:阴极4:隔板5:电池壳体6:盖组件最佳模式下文中,将参照示例实施方式详细描述有机电解液和包括该有机电解液的锂电池。根据示例实施方式,有机电解液可包括有机溶剂;锂盐;由以下式1表示的硼酸盐化合物;和由以下式2表示的离子金属络合物:在以上式1和2中,R1、R2和R3可各自独立地是氢;用卤素取代或未取代的C1-C5烷基基团;或用卤素取代或未取代的C1-C5氰烷基基团,其中R1、R2和R3中的至少一个可包括氰烷基基团,Me可以是选自由过渡金属和元素周期表中13-15族元素组成的组中的元素,M可以是金属离子,a可以是1至3的整数,b可以是1至3的整数,s=b/a,p可以是0至8的整数,q可以是0或1,r可以是1至4的整数,X1和X2可各自独立地是O、S或NR6,R4和R6可各自独立地是卤素、用卤素取代或未取代的C1-C5烷基基团、或用卤素取代或未取代的C1-C5芳基基团,R5可以是用卤素取代或未取代的C1-C5亚烷基基团或用卤素取代或未取代的C4-C10亚芳基基团。例如,M可以是碱金属离子或碱土金属离子。有机电解液可抑制气体产生且固体电解质界面具有高阻抗,并且因此,其可防止电池性能如锂电池的寿命特性的劣化。有机电解液改善锂电池性能的原理将被详细解释,但是该解释仅被提供以帮助理解本发明构思,并且不限制对本发明构思的范围。例如,硼酸盐化合物可提供促进锂盐溶解的阴离子,并且因而可改善有机电解液的离子电导率。而且,在上述式2中的离子金属络合物中,由X1和X2表示的杂原子可形成环并且连接至表示为Me的中心原子,并且因而可形成化学稳定结构。因此,除了改善离子电导率,包括离子金属络合物的有机电解液可具有改善的耐热性、化学稳定性和耐水解性。就此方面,当有机电解液同时包括硼酸盐化合物和离子化合物时,可同时提供高离子电导率、改善的耐热性和耐水解性。因此,包括有机电解液的锂电池可具有改善的稳定性和寿命特性。例如,在有机电解液中,硼酸盐化合物可由以下式3表示:<式3>B(OR10)3在以上式3中,R10可以是用卤素取代或未取代的C1-C5氰烷基基团。例如,在有机电解液中,硼酸盐化合物可以是三氰甲基硼酸盐、三氰乙基硼酸盐(三(2-氰乙基)硼酸盐)、三氰丙基硼酸盐或三氰丁基硼酸盐,但是实施方式不限于此,并且可使用是路易斯酸和能够提供阴离子的任何硼酸盐化合物。例如,在有机电解液中,离子金属络合物可由下式4表示:<式4>在上述式4中,Ma可以是Al、B或P,M可以是金属离子,p可以是0至8的整数,q可以是0或1,r可以是1至4的整数,X3和X4可各自独立地是O或S,R7可以是卤素,并且R8可以是用卤素取代或未取代的C1-C5亚烷基基团或用卤素取代或未取代的C4-C10亚芳基基团。例如,在有机电解液中,离子金属络合物可由以下式5或6表示:在以上式5和6中,Ma可以是Al、B或P,p可以是0至8的整数,r可以是1至4的整数,R7可以是卤素,R9可以是用卤素取代或未取代的C1-C5亚烷基基团。例如,在有机电解液中,离子金属络合物可由以下式7至12中的一个表示。在有机电解液中,硼酸盐化合物的量可以是基于有机电解液总重量的约0.1wt%至约10wt%,但是该量不限于此,并且可根据需要调整至合适。例如,在有机电解液中,硼酸盐化合物的量可以是基于有机电解液总重量的约0.1wt%至约7wt%。例如,在有机电解液中,硼酸盐化合物的量可以是基于有机电解液总重量的约0.1wt%至约5wt%。例如,在有机电解液中,硼酸盐化合物的量可以是基于有机电解液总重量的约0.1wt%至约3wt%。当硼酸盐化合物的量在上述范围内时,可获得进一步改善的电池特性。在有机电解液中,离子金属络合物的量可以是基于有机电解液总重量的约0.1wt%至约10wt%,但是该量不限于此,并且可根据需要调整至合适。例如,在有机电解液中,离子金属络合物的量可以是基于有机电解液总重量的约0.1wt%至约7wt%。例如,在有机电解液中,离子金属络合物的量可以是基于有机电解液总重量的约0.1wt%至约5wt%。例如,在有机电解液中,离子金属络合物的量可以是基于有机电解液总重量的约0.1wt%至约3wt%。当离子金属络合物的量在上述范围内时,可获得进一步改善的电池特性。有机电解液可进一步包括由以下式13表示的氟类化合物:<式13>在上述式13中,X1和X2可各自独立地是氢;卤素;用卤素取代或未取代的C1-C2烷基基团,其中X1和X2中的至少一个可包括氟原子。当有机电解液包括另外的氟类化合物时,有机电解液的粘度可降低。当有机电解液的粘度降低时,可改善有机电解液的浸渍特性和离子电导率。在有机电解液中,氟类化合物可由式14和15之一表示:在有机电解液中,氟类化合物的量可以是基于有机电解液总量的约0.1wt%至约10wt%,但是该量并不限于此,并且可根据需要调整至适当量。例如,在有机电解液中,氟类化合物的量可以是基于有机电解液总量的约0.1wt%至约7wt%。例如,在有机电解液中,氟化合物的量可以是基于有机电解液总量的约0.1wt%至约5wt%。例如,在有机电解液中,氟化合物的量可以是基于有机电解液总量的约0.1wt%至约3wt%。当氟化合物的量在上述范围内,锂电池可具有改善的电池特性。在有机电解液中,硼酸盐化合物、离子金属络合物和氟类化合物的比率可以是基于100重量份的硼酸盐化合物的约20重量份至约500重量份的离子金属络合物和约20重量份至约500重量份的氟化合物,但是该比率不限于此,并且可在不抑制本发明构思的效果的范围内调整。例如,在有机电解液中,硼酸盐化合物、离子金属络合物和氟类化合物的比率可以是基于100重量份的硼酸盐化合物的约20重量份至约400重量份的离子金属络合物和约20重量份至约400重量份的氟化合物。例如,在有机电解液中,硼酸盐化合物、离子金属络合物和氟类化合物的比率可以是基于100重量份的硼酸盐化合物的约20重量份至约300重量份的离子金属络合物和约20重量份至约300重量份的氟化合物。在有机电解液中,有机溶剂可包括低沸点溶剂。低沸点溶剂指在约25℃的温度下和约1atm的压力下具有约200℃或更低沸点的溶剂。例如,有机溶剂可包括选自由碳酸二烷基酯、环碳酸酯、线型或环状酯、线型或环状酰胺、脂族腈、线型或环状醚及其衍生物组成的组中的一种或多种。具体的,有机溶剂可包括选自由以下组成的组中的一种或多种:碳酸二甲酯(DMC)、碳酸甲乙酯(EMC)、碳酸甲丙酯、碳酸乙丙酯、碳酸二乙酯(DEC)、碳酸二丙酯、碳酸丙二酯(PC)、碳酸乙二酯(EC)、碳酸丁二酯、丙酸乙酯、丁酸乙酯、乙腈、琥珀腈(SN)、二甲亚砜、二甲基甲酰胺、二甲基乙酰胺、γ-戊内酯、γ-丁内酯和四氢呋喃,但是实施方式不限于此,并且可使用在本领域中作为低沸点溶剂可得的任何材料。在有机电解液中,锂盐的浓度可以是约0.01M至约2.0M,但是实施方式不限于此并且可根据需使用任何合适的量。当锂盐的浓度在该范围内,锂电池可具有改善的电池特性。有机电解液中使用的锂盐不被特别限制,并且可使用本领域中作为锂盐可得的任何材料。例如,可使用LiPF6、LiBF4、LiSbF6、LiAsF6、LiClO4、LiCF3SO3、Li(CF3SO2)2N、LiC4F9SO3、LiAlO2、LiAlCl4、LiN(CxF2x+1SO2)(CyF2y+1SO2)(其中x和y选自1至20)、LiCl、LiI或其混合物。例如,在有机电解液中,锂盐可以是LiPF6。有机电解液可以是液体或凝胶。有机电解液可通过将上述硼酸盐化合物、离子金属络合物和锂盐添加至有机溶剂来制备。根据另一示例实施方式的锂电池可包括阴极、阳极和上述有机电解液。锂电池在结构上不特别受限制,并且锂电池可以是锂二次电池如锂离子电池、锂离子聚合物电池、锂硫电池以及锂一次电池。例如,在以上锂电池中,阴极可包括镍。例如,阴极的正极活性材料可以是包括镍的锂过渡金属氧化物。例如,阴极的正极活性材料可以是在过渡金属中具有最高量镍的富镍-锂过渡金属氧化物。例如,在锂电池中,阳极可包括石墨作为负极活性材料。同样,锂电池可具有约4.8V或更高的高压。在一种或多种示例实施方式中,锂电池可以由下列方式制造。首先,制备阴极。例如,将阴极活性材料、导电剂、粘合剂和溶剂混合以制备阴极活性材料组合物。在一些示例实施方式中,阴极活性材料组合物可直接涂覆在金属集电器上,以制备阴极板。在一些示例实施方式中,阴极活性材料组合物可被浇铸在单独的载体上以形成阴极活性材料膜,其然后可从载体上分离并被层压在金属集电器上,以制备阴极板。阴极不限于上述实例,并且可以是各种类型之一。阴极活性材料可以是现有技术中可得的任何阴极活性材料,例如,可以是含锂的金属氧化物。在一些示例实施方式中,阴极活性材料可以是锂与选自Co、Mn、Ni及其组合的金属的至少一种复合氧化物。在一些示例实施方式中,阴极活性材料可以是由下式之一表示的化合物:LiaA1-bB'bD'2(其中0.90≤a≤1.8和0≤b≤0.5);LiaE1-bB'bO2-cD'c(其中0.90≤a≤1.8,0≤b≤0.5,和0≤c≤0.05);LiE2-bB'bO4-cD'c(其中0≤b≤0.5和0≤c≤0.05);LiaNi1-b-cCobB'cD'α(其中0.90≤a≤1.8,0≤b≤0.5,0≤c≤0.05,和0<α≤2);LiaNi1-b-cCobB'cO2-αF'α(其中0.90≤a≤1.8,0≤b≤0.5,0≤c≤0.05,和0<α<2);LiaNi1-b-cCobB'cO2-αF'2(其中0.90≤a≤1.8,0≤b≤0.5,0≤c≤0.05,和0<α<2);LiaNi1-b-cMnbB'cD'α(其中0.90≤a≤1.8,0≤b≤0.5,0≤c≤0.05,和0<α≤2);LiaNi1-b-cMnbB'cO2-αF'α(其中0.90≤a≤1.8,0≤b≤0.5,0≤c≤0.05,和0<α<2);LiaNi1-b-cMnbB'cO2-αF'2(其中0.90≤a≤1.8,0≤b≤0.5,0≤c≤0.05,和0<α<2);LiaNibEcGdO2(其中0.90≤a≤1.8,0≤b≤0.9,0≤c≤0.5,和0.001≤d≤0.1);LiaNibCocMndGeO2(其中0.90≤a≤1.8,0≤b≤0.9,0≤c≤0.5,0≤d≤0.5,和0.001≤e≤0.1);LiaNiGbO2(其中0.90≤a≤1.8和0.001≤b≤0.1);LiaCoGbO2(其中0.90≤a≤1.8和0.001≤b≤0.1);LiaMnGbO2(其中0.90≤a≤1.8和0.001≤b≤0.1);LiaMn2GbO4(其中0.90≤a≤1.8和0.001≤b≤0.1);QO2;QS2;LiQS2;V2O5;LiV2O5;LiI'O2;LiNiVO4;Li(3-f)J2(PO4)3(其中0≤f≤2);Li(3-f)Fe2(PO4)3(其中0≤f≤2);和LiFePO4。在上述式中、A可选自镍(Ni)、钴(Co)、锰(Mn)及其组合;B'可选自铝(Al)、镍(Ni)、钴(Co)、锰(Mn)、铬(Cr)、铁(Fe)、镁(Mg)、锶(Sr)、钒(V)、稀土元素及其组合;D'可选自氧(O)、氟(F)、硫(S)、磷(P)及其组合;E可选自钴(Co)、锰(Mn)及其组合;F'可选自氟(F)、硫(S)、磷(P)及其组合;G可选自铝(Al)、铬(Cr)、锰(Mn)、铁(Fe)、镁(Mg)、镧(La)、铈(Ce)、锶(Sr)、钒(V)及其组合;Q选自钛(Ti)、钼(Mo)、锰(Mn)及其组合;I'可选自铬(Cr)、钒(V)、铁(Fe)、钪(Sc)、钇(Y)及其组合;并且J可选自钒(V)、铬(Cr)、锰(Mn)、钴(Co)、镍(Ni)、铜(Cu)及其组合。在一些示例实施方式中,阴极活性材料可以是LiCoO2、LiMnxO2x(其中x=1或2)、LiNi1-xMnxO2x(其中0<x<1)、LiNi1-x-yCoxMnyO2(其中0≤x≤0.5,0≤y≤0.5,和1-x-y>0.5)或LiFePO4。以上作为阴极活性材料列出的化合物可具有表面涂层(下文也称作“涂层”)。可选地,可使用没有涂层的化合物和具有涂层的化合物的混合物,化合物选自以上列出的化合物。在一些示例实施方式中,涂层可包括选自由以下组成的组中的至少一种涂覆元素的化合物:涂覆元素的氧化物、氢氧化物、氧基氢氧化合物、氧基碳酸盐和羟基碳酸盐。在一些示例实施方式中,用于涂层的化合物可以是无定形或结晶的。在一些示例实施方式中,用于涂层的涂覆元素可以是镁(Mg)、铝(Al)、钴(Co)、钾(K)、钠(Na)、钙(Ca)、硅(Si)、钛(Ti)、钒(V)、锡(Sn)、锗(Ge)、镓(Ga)、硼(B)、砷(As)、锆(Zr)或其混合物。在一些示例实施方式中,当使用涂覆元素的化合物时,可使用不会不利地影响阴极活性材料的物理性质的任何方法形成涂层。例如,可使用喷涂方法或浸渍方法形成涂层。涂覆方法可被本领域普通技术人员很好地理解,并且因而将省去其详细描述。在一些示例实施方式中,导电剂可以是炭黑或石墨颗粒,但是示例实施方式不限于此。可使用本领域中作为导电剂可得的任何材料。粘合剂的实例是偏二氟乙烯/六氟丙烯共聚物、聚偏二氟乙烯(PVDF)、聚丙烯腈、聚甲基丙烯酸甲酯、聚四氟乙烯、其混合物和苯乙烯-丁二烯橡胶聚合物,但是示例实施方式不限于此。可使用本领域中作为粘合剂可得任何材料。溶剂的实例是N-甲基吡咯烷酮、丙酮和水,但是示例实施方式不限于此。可使用在本领域中作为溶剂可得的任何材料。阴极活性材料、导电剂、粘合剂和溶剂的量可以在通常用于锂电池中的范围内。导电剂、粘合剂和溶剂中的至少一个可根据锂电池的用途和结构被省去。接下来,制备阳极。例如,将阳极活性材料、导电剂、粘合剂和溶剂混合以制备阳极活性材料组合物。在一些示例实施方式中,阳极活性材料组合物可直接涂覆在金属集电器上并且干燥以制备阳极板。在一些示例实施方式中,阳极活性材料组合物可被浇铸在单独的载体上以形成阳极活性材料膜,其然后可从载体上分离并且层压在金属集电器上以制备阳极板。在一些示例实施方式中,阳极活性材料可以是用于现有技术中可得的锂电池的任何阳极活性材料。例如,阳极活性材料可包括选自锂金属、与锂可成合金的金属、过渡金属氧化物、非过渡金属氧化物和含碳物质的至少一种。与锂可成合金的金属的实例是Si、Sn、Al、Ge、Pb、Bi、Sb、Si-Y合金(其中Y是碱金属、碱土金属、XIII族元素、XIV族元素、过渡金属、稀土元素或其组合,并且Y不是Si)和Sn-Y合金(其中Y是碱金属、碱土金属、XIII族元素、XIV族元素、过渡金属、稀土元素或其组合,并且Y不是Sn)。在一些示例实施方式中,Y可以是镁(Mg)、钙(Ca)、锶(Sr)、钡(Ba)、镭(Ra)、钪(Sc)、钇(Y)、钛(Ti)、锆(Zr)、铪(Hf)、鈩(Rf)、钒(V)、铌(Nb)、钽(Ta)、(Db)、铬(Cr)、钼(Mo)、钨(W)、(Sg)、锝(Tc)、铼(Re)、(Bh)、铁(Fe)、铅(Pb)、钌(Ru)、锇(Os)、(Hs)、铑(Rh)、铱(Ir)、钯(Pd)、铂(Pt)、铜(Cu)、银(Ag)、金(Au)、锌(Zn)、镉(Cd)、硼(B)、铝(Al)、镓(Ga)、锡(Sn)、铟(In)、钛(Ti)、锗(Ge)、磷(P)、砷(As)、锑(Sb)、铋(Bi)、硫(S)、硒(Se)、碲(Te)、钋(Po)或其组合。过渡金属氧化物的实例包括锂钛氧化物、钒氧化物和锂钒氧化物。非过渡金属氧化物的实例包括SnO2和SiOx(其中0<x<2)。含碳物质的实例是结晶碳、无定形碳和其混合物。结晶碳的实例是石墨,如以无形状、板、片、球形或纤维形式的天然石墨或人工石墨。无定形碳的实例是软质炭黑(在低温烧结的碳)、硬碳、中间相沥青碳化物和烧结焦炭。在一些示例实施方式中,用于阳极活性材料组合物的导电剂、粘合剂和溶剂可以与用于阴极活性材料组合物的那些相同。阳极活性材料、导电剂、粘合剂和溶剂的量可与用于锂电池的本领域中通常使用的那些相同。导电剂、粘合剂和溶剂中的至少一个可根据锂电池的用途和结构被省去。接下来,制备待置于阴极和阳极之间的隔板。用于锂电池的隔板可以是通常用于锂电池中的任何隔板。在一些示例实施方式中,隔板可对于电解液中的离子迁移具有低阻抗并且具有卓越的电解液-保持能力。隔板的实例是玻璃纤维、聚酯、特氟龙、聚乙烯、聚丙烯、聚四氟乙烯(PTFE)和其组合,其每一种可以是无纺织物或织物。例如,包括聚乙烯或聚丙烯的可卷隔板可用于锂离子电池。具有良好有机电解液保持能力的隔板可用于锂离子聚合物电池。例如,隔板可以以下述方式制造。在一些示例实施方式中,可将聚合物树脂、填料和溶剂混合在一起,以制备隔板组合物。然后,可直接将隔板组合物涂覆在电极上,并且然后干燥以形成隔板。在一些示例实施方式中,隔板组合物可被铸造在载体上并且然后被干燥以形成隔板膜,其然后可从载体上分离并被层压在电极上以形成隔板。用于制造隔板的聚合物树脂可以是通常用作电极板的粘合剂的任何材料。聚合物树脂的实例是偏二氟乙烯/六氟丙烯共聚物、聚偏二氟乙烯(PVDF)、聚丙烯腈、聚甲基丙烯酸甲酯和其混合物。接下来,制备有机电解液。参照图2,锂电池1包括阴极3、阳极2和隔板4。在一些示例实施方式中,阴极3、阳极2和隔板4可被缠绕或折叠,并且然后密封在电池壳体5中。在一些示例实施方式中,电池壳体5可被填充有有机电解液并且用盖组件6密封,从而完成锂电池1的制造。在一些示例实施方式中,电池壳体5可以是圆柱形类型、矩形类型或薄膜类型。例如,锂电池1可以是薄膜类型电池。在一些示例实施方式中,锂电池1可以是锂离子电池。在一些示例实施方式中,隔板可以置于阴极和阳极之间以形成电池组件。在一些示例实施方式中,电池组件可以是双电池结构堆叠并且用有机电解液浸渍。在一些示例实施方式中,所得组件可放入袋内并且气密密封,从而完成锂离子聚合物电池的制造。在一种或多种示例实施方式中,多个电池组件可被堆叠以形成电池组,其可用于需要高容量和高输出的任何设备中。例如,电池组可用于便携式计算机、智能电话或电动车辆。锂电池可具有改善的寿命特性和高率特性,并且因而可用于电动车辆(EV)。例如,锂电池可用于混合驱动汽车如插入式混合驱动汽车(PHEV)中。锂电池可以应用于大功率储存场。例如,锂电池可用于电瓶车或电动工具。本发明构思的模式下文中,本发明构思将在以下通过实施例和比较例进一步详细描述。但是,这些实施例仅用于阐释的目的并且不限制本发明构思的范围。(有机电解液的制备)实施例1:LDFOP(1%)+TCEB(1%)通过如下制备有机电解液:使用1.15M的LiPF6作为锂盐,添加相对于有机电解液总重的1wt%的二氟双(草酸根)合磷酸锂(LDFOP)——其是由以下式8表示的金属盐、和1wt%的由以下式16表示的三(2-氰乙基)硼酸酯(TCEB)至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。实施例2:LDFOP(1%)+TCEB(1%)+FEC(1%)通过如下制备有机电解液:使用1.15M的LiPF6作为锂盐,添加相对于有机电解液总重的1wt%的由以下式8表示的金属盐、1wt%的由以下式16表示的三(2-氰乙基)硼酸酯和1wt%的由以下式14表示的氟代碳酸乙二酯至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。实施例3:LDFOP(1%)+TCEB(0.5%)+FEC(1%)以与实施例2中相同的方式制备有机电解液,除了将1wt%的由式8表示的金属盐、0.5wt%的由式16表示的三(2-氰乙基)硼酸酯和1wt%的由式14表示的氟代碳酸二乙酯添加至混合溶剂。实施例4:LDFOP(1%)+TCEB(0.25%)+FEC(1%)以与实施例2中相同的方式制备有机电解液,除了将1wt%的由8式表示的金属盐、0.25wt%的由式16表示的三(2-氰乙基)硼酸酯和1wt%的由式14表示的氟代碳酸二乙酯添加至混合溶剂。实施例5:LDFOP(1%)+TCEB(0.5%)+FEC(3%)以与实施例2中相同的方式制备有机电解液,除了将1wt%的由式8表示的金属盐、0.5wt%的由式16表示的三(2-氰乙基)硼酸酯和3wt%的由式14表示的氟代碳酸二乙酯添加至混合溶剂。实施例6:LDFOP(1%)+TCEB(0.5%)+FEC(0.5%)以与实施例2中相同的方式制备有机电解液,除了将1wt%的由式8表示的金属盐、0.5wt%的由式16表示的三(2-氰乙基)硼酸酯和0.5wt%的由式14表示的氟代碳酸二乙酯添加至混合溶剂。实施例7:LiFOB(1%)+TCEB(0.5%)通过如下制备有机电解液:使用1.15M的LiPF6作为锂盐,添加相对于有机电解液总重的1wt%的由以下式10表示的金属盐和0.5wt%的由以下式16表示的三(2-氰乙基)硼酸酯至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。实施例8:LiFOB(1%)+TCEB(0.5%)+FEC(3%)通过如下制备有机电解液:使用1.15M的LiPF6作为锂盐,添加相对于有机电解液总重的1wt%的由以下式8表示的金属盐、0.5wt%的由以下式16表示的三(2-氰乙基)硼酸酯和3wt%的由以下式14表示的氟代碳酸二乙酯至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。比较例1:无添加剂通过如下制备有机电解液:添加1.15M作为锂盐的LiPF6至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。比较例2:仅LDFOP(1%)通过如下制备有机电解液:使用1.15M的LiPF6作为锂盐,添加相对于有机电解液总重的1wt%的由以下式8表示的金属盐至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。<式8>比较例3:仅TCEB(1%)通过如下制备有机电解液:使用1.15M的LiPF6作为锂盐,添加相对于有机电解液总重的1wt%的由以下式16表示的三(2-氰乙基)硼酸酯至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。<式16>比较例4:仅FEC(1%)通过如下制备有机电解液:使用1.15M的LiPF6作为锂盐,添加相对于有机电解液总重的1wt%的由以下式14表示的氟代碳酸二乙酯至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。<式14>比较例5:LDFOP(1%)+FEC(1%)通过如下制备有机电解液:使用1.15M的LiPF6作为锂盐,添加相对于有机电解液总重的1wt%的由以下式8表示的金属盐和1wt%的由以下式14表示的氟代碳酸二乙酯至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。比较例6:TCEB(1%)+FEC(1%)通过如下制备有机电解液:使用1.15M的LiPF6作为锂盐,添加相对于有机电解液总重的1wt%的由以下式16表示的三(2-氰乙基)硼酸酯和1wt%的由以下式14表示的氟代碳酸二乙酯至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。比较例7:LDFOP(1%)+VEC(0.5%)通过如下制备有机电解液:使用1.15M的LiPF6作为锂盐,添加相对于有机电解液总重的1wt%的由以下式8表示的金属盐和0.5wt%的碳酸乙烯亚乙酯(VEC)至以2:4:4体积比的碳酸二乙酯(EC)、碳酸甲乙酯(EMC)和碳酸二甲酯(DMC)的混合溶剂。<式8>(锂电池的制备)实施例9(阳极的制备)将97wt%的石墨颗粒(MC20,由MitsubishiChemicalCorporation制造)、1.5wt%的作为导体的BM408(由DaicelCorporation制造)和1.5wt%的作为粘合剂的BM400-B(由ZeonCorporation制造)混合,添加至蒸馏水,并且然后通过使用机械搅拌器搅拌60分钟,以制备负极活性材料浆料。该浆料通过使用刮片以约60μm的厚度施加至具有约10μm厚度的铜集电器上,通过使用热风干燥器在约100℃的温度下干燥约0.5小时,再在约120℃的温度下在真空中干燥约4小时,并且然后进行辊压以制备阳极板。阳极具有约1.55g/cc的混合物密度(E/D)和约14.36mg/cm2的负载水平(L/L)。(阴极的制备)将94wt%的Zr-涂覆的LiNi0.65Co0.20Mn0.15O2(NCM65,由SamsungSDI制造)、3.0wt%的作为导体的Denka黑和3wt%的作为粘合剂的PVDF(Solef6020,由Solvay制造)混合,添加至N-甲基-2-吡咯烷酮溶剂,并且然后通过机械搅拌器搅拌30分钟,以制备正极活性材料浆料。将浆料通过使用刮片以约60μm的厚度施加至具有约20μm厚度的铝集电器上,通过使用热风干燥器在约100℃的温度下干燥约0.5小时,再在约120℃的温度下在真空中干燥约4小时,并且然后进行辊压,以制备阴极板。阴极具有约3.15g/cc的混合物密度(E/D)和约27.05mg/cm2的负载水平(L/L)。(电池组件)将具有约16μm厚度的陶瓷涂覆的聚乙烯隔板(由SKInnovationCo.,Ltd.制造)用作隔板,并且将以上实施例1中制备的有机电解液用于制造袋型锂电池。实施例10至16以与实施例9中相同的方式制造锂电池,除了使用实施例2至8中制备的每种有机电解液代替实施例1中制备的电解液。比较例8至14以与实施例9中相同的方式制造锂电池,除了使用比较例1至7中制备的每种有机电解液代替实施例1中制备的电解液。评估例1:测量粘度测量实施例1至8和比较例1至6中制备的有机电解液的粘度,并且一些结果显示在表1中。通过使用粘度计SV-1A(A&DCompany;Vibroviscometer)测量粘度。[表1]如上表1中所显示的,与比较例2至6中制备的有机电解液的粘度相比,实施例2中制备的有机电解液的粘度显著降低。评估例2:评估在室温(25℃)下的充电和放电特性将实施例9-16和比较例8至14中制造的锂电池在室温(25℃)下以约0.5C倍率的恒定电流充电,直至电压达到4.20V(vs.Li),并且然后在约0.05C倍率的电流水平停止,同时维持约4.20V的恒定电压。其后,将锂电池以约0.5C倍率的恒定电流放电,直至电压达到2.80V(vs.Li)(形成过程,第一循环)。将经历形成过程的锂电池在约25℃的温度和以约0.5C倍率的恒定电流充电,直至电压达到4.20V(vs.Li),并且然后以约0.05C倍率的电流停止,同时维持约4.20V的恒定电压。其后,重复其中将锂电池以约1.5C倍率以恒定电流放电直至电压达到2.80V(vs.Li)的循环,直至第200个循环。一些上述充电和放电评估结果显示在以下表2中。通过以下方程1定义在第200个循环的容量保持率。<方程1>容量保持率=[在第200个循环的放电容量/在第一个循环的放电容量]×100评估例3:评估在高温(45℃)下的充电和放电特性以与评估例2中相同的方式将锂电池充电和放电,除了将充电和放电温度改变至约45℃。充电和放电评估结果的一些结果显示于以下表2中。[表2]如表2和图1A至1C中显示的,与不包括本发明构思的有机电解液的比较例8至13中制备的锂电池相比较,包括本发明构思的有机电解液的实施例9至16中制备的锂电池显示了改善的在室温(25℃)和高温(45℃)下的寿命特性。评估例4:评估在高温(45℃)下的直流阻抗(DCIR)通过下述方法测量锂电池的直流阻抗(DCIR)。在第一循环将实施例9至16和比较例8至14中制备的锂电池在高温(45℃)下以0.5C倍率的电流充电,直至电压达到SOC的50%,以0.02C的倍率停止,在相同条件下维持10分钟,以0.5C倍率的恒定电流放电30秒,在相同条件下维持30秒,以0.5C倍率的恒定电流放电30秒,在相同条件下维持10分钟,以1.0C倍率的恒定电流放电30秒,在相同条件下维持30秒,以0.5C倍率的恒定电流水平放电1分钟,在相同条件下维持10分钟,以2.0C倍率的恒定电流放电30秒,在相同条件下维持30秒,以0.5C倍率的恒定电流放电2分钟,在相同条件下维持10分钟,以3.0C倍率的恒定电流放电30秒,在相同条件下维持30秒,以0.5C倍率的恒定电流放电2分钟,并且然后在相同条件下维持10分钟。对于10秒的每个C-倍率的平均压降是直流电压。一些直流阻抗值显示在以下表3中。[表3]如以上表3中显示的,与比较例8至13中制备的并且不包括本发明中的有机电解液的锂电池相比较,包括本发明构思的有机电解液的实施例9至16中制备的锂电池显示在高温(45℃)下直流阻抗的显著更低的增加率。因此,可得出结论,已经在实施例中制备的锂电池中抑制了固体电解质界面的产生。评估例4:评估在60℃高温下的稳定性在第一个循环期间,将实施例9至16和比较例8至13中制造的锂电池在室温(25℃)下和以约0.5C倍率的恒定电流充电,直至电压达到4.20V,在4.20V的恒定电压下充电,直至电流达到0.05C,并且然后以0.5C倍率的恒定电流放电,直至电压达到2.75V。在第二个循环期间,将锂电池以约0.5C倍率的恒定电流充电,直至电压达到4.20V,在4.20V的恒定电压下充电,直至电流达到0.05C,并且然后以0.2C倍率的恒定电流放电,直至电压达到2.80V。在第三个循环期间,将锂电池以约0.5C倍率的恒定电流充电,直至电压达到4.20V,在4.20V的恒定电压下充电,直至电流达到0.05C,并且然后以0.2C倍率的恒定电流放电,直至电压达到2.80V。在第三个循环中的放电容量被视作标准容量。在第四个循环期间,将锂电池以约0.5C的倍率充电,直至电压达到4.20V,在4.20V的恒定电压下充电,直至电流达到0.05C,在60℃烤箱中储存60天,并且然后将电池取出并以0.1C的倍率经受第四次放电循环,直至电压达到2.75V。一些充电和放电结果显示于以下表4中。在高温储存后的容量保持率可通过以下方程2定义。<方程2>在高温储存后的容量保持率[%]=[在第四次循环中在高温暴露后的放电容量/标准容量]×100(标准容量是在第三次循环中的放电容量)[表4]在储存60天后的容量保持率[%]实施例986.78实施例1086.28实施例1186.74实施例1287.09实施例1386.27实施例1488.08实施例1588.46实施例1689.72比较例883.22比较例984.59比较例1083.43比较例1185.20比较例1285.60比较例1385.98如以上表4中显示的,与比较例8至13中制造的并且不包括本发明构思的有机电解液的锂电池相比较,包括本发明构思的有机电解液的实施例9至16中制造的锂电池显示显著增加的在高温下的稳定性。评估例5:所产生气体的量的评估关于实施例9至16和比较例8至14中制造的锂电池,在评估在高温(45℃)下的寿命特性期间,测量所产生气体的量,并且一些评估结果显示于以下表5中。将已经完成寿命特性评估的电池置于夹具中,敲击(popped),并且然后将夹具的内部气体压力的变化转化为体积,以测量所产生气体的量。[表5]如以上表5中显示的,与比较例14中制造的并且不包括本发明构思的有机电解液的锂电池相比较,包括本发明构思的有机电解液的实施例13中制备的锂电池显示显著更低的所产生气体的量。尽管已经参照其示例实施方式具体显示和描述了本发明构思,但是将理解可进行其中形式和细节的各种改变,而不脱离本发明权利要求的精神和范围。工业应用可通过使用新型组合物的有机电解液改善锂电池的寿命特性。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1