多酚的纯化的制作方法
本发明涉及一种纯化来自原料的多酚的方法。具体地讲,本发明涉及富集能从植物材料获得的多酚的特别是绿原酸(CGA)的级分,其中与原料相比,富集级分的异构体平衡基本上得到保持。
背景技术:
饮料(诸如咖啡)的一项重要性质是持久的泡沫(也称为“奶泡(crema)”)和浓郁的香味,它们被认为是重要的质量指标。奶泡的体积、质地、细腻度、颜色和稳定性是吸引消费者的独特特性。奶泡的产生来源于对表面活性咖啡组分的提取,这些表面活性咖啡组分会包覆用加压热水喷射捣实的意式浓缩咖啡(espresso)基质而产生的气泡并使其稳定。
咖啡香味也是一项重要的性质,因为咖啡香味的浓郁程度是消费者所感受到的第一感官体验。当嗅闻咖啡时,香味可以帮助你评价咖啡的风味和咖啡的亮度。在烘焙期间,许多芳族化合物自咖啡豆基质中形成或释放,并且影响人们对于咖啡的感受(香味和风味)。芳族化合物最重要的前体之一是绿原酸,特别是咖啡酰奎尼酸。
因此,人们已有兴趣从许多不同种类的植物材料,例如,浆果、葡萄、柑橘、蔬菜、谷物、草药、茶、咖啡、可可中分离富集多酚的级分。具体地讲,人们已有兴趣分离富集绿原酸化合物并具有类似于原始植物材料的绿原酸化合物异构体平衡的多酚的级分,以给食物和饮料产品增添例如香味和风味。
此外,已报道多酚具有抗微生物、抗病毒、抗诱变、抗癌、抗增殖和血管扩张效果。多酚可具有抗菌活性,其可用于对抗由变形链球菌(Streptococcus mutans)引起的蛀牙。多酚被列为益智药,据说可改善脑力功能,诸如认知、记忆、智力、积极性、注意力和专注力。
然而,食物立法中加强了健康声明的规则,制造商必须确保活性成分的一致水平,并且要提供所制造产品达标的科学证据。
因此,需要一种提供富集多酚的级分(特别是包含绿原酸(CGA)的级分)的方法,该级分中绿原酸平衡类似于最初存在于植物材料中的绿原酸平衡。随后,该富集级分可用于确保食物产品的活性成分具有恒定水平,以及确保在干预研究中具有恒定水平以证明摄入多酚(诸如来自咖啡的多酚)与给定的声称效果之间的因果关系。
因此,在行业中需要一种用于提供富集多酚(特别是绿原酸)的级分的方法,该级分相对于其来源的植物材料具有最本真的特性,该级分可用于增强食物或饮料的性质。
技术实现要素:
因此,本发明描述了一种纯化多酚的新方法,其中多酚平衡得到保持或基本上得到保持。此外,本发明的方法可导致在该方法期间形成有限的衍生物或者不会形成衍生物,例如多酚的乙酯。因为乙酯不具有与植物材料中天然存在的天然多酚相同的性质,所以它们是不期望的。此外,相对于原始产物而言,乙酯会改变富集级分的多酚平衡。
因此,本发明的一个方面涉及一种从原料提供富集多酚的级分的方法,该方法包括以下步骤:
(i)将原料溶解于含水溶剂中;
(ii)将pH调节至pH 3以下;
(iii)使原料与色谱树脂接触;
(iv)从色谱树脂解吸多酚,以提供包含多酚的洗脱物;
(v)将洗脱物的pH调节至pH 3.5以上;以及
(vi)将洗脱物与被洗脱的多酚分离,以获得富集多酚的级分。
本发明的另一方面涉及能从根据本发明的方法获得的富集多酚的级分。
本发明的又一方面是提供一种食物成分,其包含根据本发明的富集多酚的级分。
本发明的又一方面是提供一种食物产品,其包含根据本发明的富集多酚的级分和/或根据本发明的食物成分。
另一方面涉及根据本发明的富集多酚的级分和/或根据本发明的食物成分作为产生香味、风味和/或发泡的前体的用途。
另一方面涉及一种药物组合物,其包含根据本发明的富集多酚的级分以及药学上可接受的载体。
附图说明
图1示出了本发明的多酚的非限制性实施例。图中(*)标记表示R1的连接点。
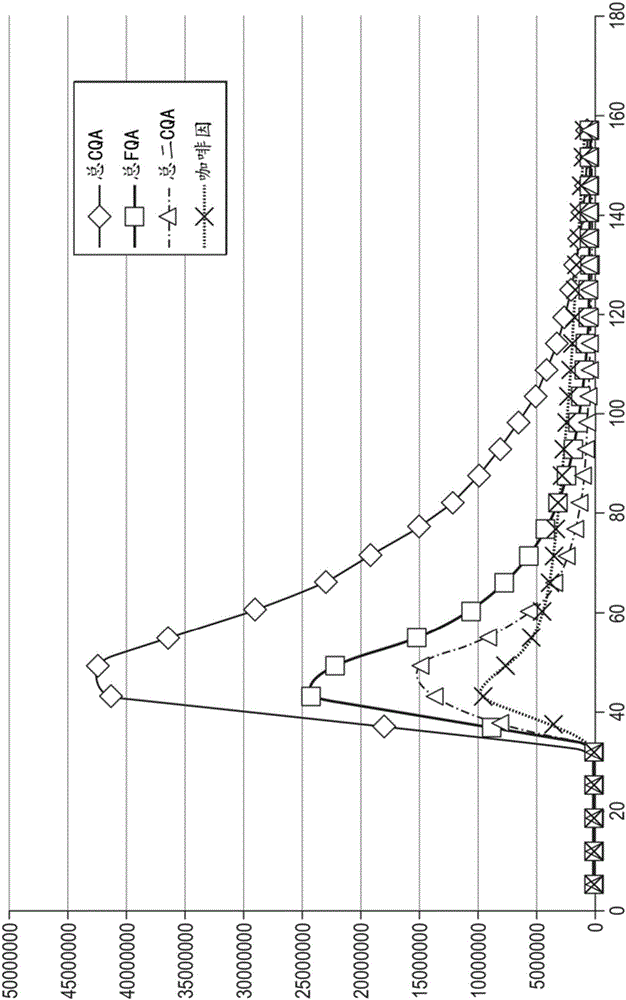
图2示出了用90%乙醇解吸CQA、FQA、二CQA和咖啡因的解吸动力学。
图3示出了实验室规模的根据本发明的纯化方法的具体实施方案。
图4示出了富集多酚的生咖啡级分与初始咖啡的总体组成的比较。
图5示出了富集多酚的生咖啡级分与初始咖啡的CGA组成的比较。
图6示出了5-CQA在75%乙醇中,在pH 1、pH 2、pH 7.4和pH 12的条件下2小时后的降解情况。
图7示出了在t=室温、50℃和80℃下,5-CQA转化成其乙酯的情况。
图8示出了(a)在50℃下3小时内和(b)在室温下36小时内形成5-CQA酯的情况。
图9示出了用于生产规模的改良纯化方案。
图10示出了用于临床研究的,脱咖啡因的富集多酚的生咖啡级分与初始咖啡的总体组成的比较。
图11示出了脱咖啡因的富集级分与初始咖啡的详细CGA组成的比较。
图12示出了用于临床研究的,含咖啡因的富集多酚的生咖啡级分与初始咖啡的总体组成的比较。
图13示出了含咖啡因的富集级分与初始咖啡的详细CGA组成的比较。
图14示出了采用连续解吸步骤,在解吸混合物中乙醇比率渐增(1)20%、(2)50%、(3)80%的条件下,对绿原酸进行纯化的方案。
图15示出了在初始咖啡以及通过乙醇梯度解吸获得的三个级分中,CGA的相对组成。
图16示出了三种不同乙醇梯度解吸级分的HPLC色谱图。
现将在下文中更详细地描述本发明。
具体实施方式
本发明描述了一种使用色谱树脂提供富集多酚的级分的新方法。从本发明得到的富集级分可以提供改善的性质,特别是香味、风味和发泡性质,这是因为富集级分中存在的多酚(例如绿原酸化合物)的异构体平衡基本上得到保持,并且类似于最初存在于植物材料中的多酚(例如绿原酸化合物)的异构体平衡。此外,根据本发明的提供富集多酚的级分的方法还提供了具有高纯度和/或良好性质(产物性能)的富集级分。
在本发明的一个实施方案中,富集级分的绿原酸化合物含量为至少40%(w/w),诸如至少50%(w/w),例如至少60%(w/w),例如至少70%(w/w)。
与其他纯化方法相比,本发明的方法可以具有若干优点。本发明的一个优点可在于,富集级分的多酚(特别是绿原酸化合物)异构体平衡可得到保持。另一个优点可在于,该方法产生有限的多酚的乙酯,或者不产生多酚的乙酯。本发明另外的优点可在于,可获得高水平的纯度(即,>60%)。
根据本发明的方法的示意性细节示于图3、图9和图14中。每个方案代表着根据本发明的方法的具体实施方案。
因此,本发明的一个方面涉及一种从原料提供富集多酚的级分的方法,该方法包括以下步骤:
(i)将原料溶解于含水溶剂中;
(ii)将pH调节至pH 3以下;
(iii)使原料与色谱树脂接触;
(iv)从色谱树脂解吸多酚,以提供包含多酚的洗脱物;
(v)将洗脱物的pH调节至pH 3.5以上;以及
(vi)将洗脱物与被洗脱的多酚分离,以获得富集多酚的级分。
该方法是基于多酚化合物,例如图1中所述多酚化合物的化学和物理性质而开发的。最重要的多酚之一是绿原酸(CGA),它是存在于咖啡以及许多其他植物材料中的最主要的多酚。绿原酸(CGA)的具体(非限制性)示例为,3-咖啡酰奎尼酸(3CQA)、4-咖啡酰奎尼酸(4CQA)、5-咖啡酰奎尼酸(5CQA)、3,4-二咖啡酰奎尼酸(3,4二CQA)、3,5-二咖啡酰奎尼酸(3,5二CQA)、4,5-二咖啡酰奎尼酸(4,5二CQA)、3-阿魏酰奎尼酸(3FQA)、4-阿魏酰奎尼酸(4FQA)、5-阿魏酰奎尼酸(5FQA)和咖啡酸。
绿原酸是低分子量化合物,其分子量总体上在600g/mol以下。绿原酸具有一个或几个芳族基团(即酚部分)。可在含有这些芳族部分的化合物之间建立非共价芳族相互作用,也称为π-π堆积相互作用。该性质用于将绿原酸特异性地吸附到具有芳族基团的基质。
绿原酸具有赋予酸碱性质的奎尼酸基团(pKa=3.2)。在pH低于pKa时,绿原酸被质子化。此时分子不带电荷,并且因此它是相当疏水的。在pH高于pKa时,酸官能团为羧酸酯形式,这意味着整个分子由于电荷而更为亲水。该性质可用于调节分子的疏水性,进而用于纯化目的。
包含多酚的原料可来自不同来源。在一个实施方案中,原料是植物材料。在另一实施方案中,植物材料选自:咖啡(诸如生咖啡、含咖啡因的咖啡、脱咖啡因的咖啡和脱咖啡因的生咖啡)、麦芽、可可、茶、浆果、葡萄、蔬菜、柑橘、草药和谷物。原料最初可以溶解在例如沸水中。可能有利的是,在开始上述纯化过程之前,先进行所溶解原料的初始沉淀步骤,以便除去高分子量(HMW)化合物,如蛋白质类、类黑精和多糖类,例如阿拉伯半乳聚糖。因此,在一个实施方案中,在进行步骤(ii)中的pH调节之前,在步骤(i)中获得的所溶解原料可例如用醇(优选地乙醇)进行沉淀以提供固相和液相。在另一实施方案中,在进行步骤(ii)中的pH调节之前,可经由过滤、离心和/或倾析将固相与液相分离。在该任选的分离步骤之后,并且在进行步骤(ii)中的pH调节之前,可对液相进行蒸发处理,以从液相除去用于使HMW沉淀的醇。
富集多酚的级分可以是不同形式的。因此,在一个实施方案中,富集多酚的级分可以是液体形式或干燥形式。在另一实施方案中,富集多酚的级分是冷冻干燥的。
下文的实施例1公开了一个具体示例,其中所溶解的原料用80%的醇进行沉淀。因此,在一个实施方案中,醇为乙醇。在另一实施方案中,醇(诸如乙醇)的浓度在50%至99%(w/w)的范围内,诸如60%至99%(w/w),诸如60%至90%(w/w),诸如70%至90%(w/w),诸如75%至85%(w/w)。
根据本发明的方法包括在将原料加载到树脂柱上之前将其酸化至pH 3以下。在本发明的一个实施方案中,步骤(ii)中的pH调节是指调节至在pH2.5以下,优选地在pH 2以下,更优选地在pH 1.5以下,或者甚至更优选地至约pH 1。在另一实施方案中,所用的酸选自强酸,例如盐酸、硫酸和磷酸。之所以采用相对较低的pH,是因为纯水和/或使用更高的pH值可能导致CGA从树脂解吸。另一方面,在酸性条件下,由于绿原酸保持其质子化和疏水形式,所以保持与树脂的相互作用。
下文所示的实施例2证明了在将原料加载到色谱树脂上之前将pH降低至pH 1的效果。在pH调节后,并且在将原料加载到色谱树脂上之前,可将材料过滤,除去较大的碎片。还可以在施加待纯化的原料之前,用酸对色谱树脂进行预调理。因此,在一个实施方案中,用pH在3以下的酸对色谱树脂进行预调理,优选在pH 2以下,更优选在pH 1.5以下,或甚至更优选低至约pH 1。在另一实施方案中,用于对柱进行预调理的酸选自盐酸、硫酸和磷酸。酸的精确浓度可变。因此,在一个实施方案中,酸的浓度在0.001M至1M的范围内,优选地在0.001M至0.5M的范围内,或者甚至更优选地在0.05M至0.3M的范围内。
在将原料加载到色谱树脂上之后,可能是有利的是,漂洗色谱树脂以除去未结合的材料。因此,在一个实施方案中,可以在使多酚解吸之前用漂洗溶液处理色谱树脂。优选地,漂洗溶液具有在pH 3以下的pH值,优选地在pH 2以下,更优选地在pH 1.5以下,甚至更优选地约pH 1。在一个实施方案中,洗涤溶液包含酸,诸如盐酸、硫酸或磷酸。由于酸的精确浓度可变,因此在本发明的一个实施方案中,漂洗溶液中的酸浓度在0.001M至1M的范围内,优选地在0.001M至0.5M的范围内,或者甚至更优选地在0.05M至0.3M的范围内。
实施例3示出了用0.1M HCl对柱进行漂洗的效果,其结果是,与不包括漂洗步骤时相比,最终级分的纯度从50%增加到66%。因此,可以得出结论,在解吸之前对柱进行漂洗可以进一步提高最终级分的纯度。
原料和色谱材料之间的比例可影响纯化产物的量。柱过载可能导致柱饱和,这会导致有价值的多酚化合物分离不充分,因为所溶解的原料的级分可能未被吸附到柱上。因此,在本发明的一个实施方案中,原料与色谱材料之间的比例可以为从2:1至1:4(基于重量:重量),诸如从1:1至1:3(基于重量:基于重量),例如约1:2(基于重量:重量)。
在本发明的上下文中,术语“色谱树脂”涉及到存在于色谱柱中并且负责原料的分离的色谱介质。在本发明的一个实施方案中,色谱树脂可以填充在填充床中或膨胀床中。可使用不同类型的色谱树脂。因此,在本发明的一个实施方案中,步骤(iii)可涉及在聚合物树脂和/或技术人员已知的任何其他色谱介质上进行吸附色谱法。
对于解吸而言,必须削弱色谱树脂与多酚的酚化合物之间的相互作用。不同的参数可影响本发明的解吸步骤。
本发明的发明人发现,在存在羟基组分(例如乙醇)的情况下,温度可能是对多酚的乙酯的不期望的形成具有显著影响的参数。
因此,在本发明的一个实施方案中,解吸期间的温度可在70℃以下,诸如在60℃以下,诸如在50℃以下,诸如在40℃以下。在另一实施方案中,该温度在10℃至40℃的范围内,诸如在25℃至35℃的范围内,例如为约30℃。实施例7证明了保持温度低以避免CGA形成乙酯的优点。因此,通常可能有利的是,在该方法的每个步骤期间保持尽可能低的温度。然而,人们往往需要在测定速度(例如,蒸发和/或解吸步骤期间)和避免产生乙酯之间进行折中。
可影响解吸过程的另一参数是解吸洗脱液的组成。解吸洗脱液可包含可改善多酚的解吸的不同成分。在本发明的一个实施方案中,解吸洗脱液可包含羟基组分,优选地该羟基组分是乙醇。其他醇类或醇类的组合也可用作解吸洗脱液。
本发明的发明人还发现,在存在羟基化合物(例如乙醇)的情况下,洗脱物和解吸洗脱液的pH可对该方法中多酚的乙酯的不期望的形成具有显著影响。在本发明的一个实施方案中,洗脱物和/或解吸洗脱液的pH可在pH 3以上,诸如pH 3.5以上,优选地约pH 4,或甚至更优选地在4至5的pH范围内。在高pH值下,例如在pH 12的强碱性条件下,可以减少不期望地形成绿原酸的乙酯的现象,但是可能引起多酚的其他不期望的反应。
在本发明的另一实施方案中,解吸洗脱液可包含羟基组分(优选地为乙醇)与碱性水溶液的组合,该碱性水溶液可优选地为KOH。
在本发明的一个实施方案中,解吸洗脱液可包含至少20%的羟基组分,例如至少30%的羟基组分,诸如至少40%的羟基组分,诸如至少50%的羟基组分,例如至少60%的羟基组分,诸如至少70%的羟基组分,例如至少80%的羟基组分和至多20%的碱性水溶液,诸如至少90%的羟基组分和至多10%的碱性水溶液,或其逐级式的组合。
由于富集多酚的级分可包含许多不同的多酚化合物和绿原酸化合物,因此可以使用逐级洗脱。因此,在本发明的一个实施方案中,解吸洗脱液可包含:
(i)在10%-30%范围内的羟基组分,诸如15%-25%,诸如17%-23%或诸如19%-21%,或者
(ii)在40%-60%范围内的羟基组分,诸如45%-55%,诸如47%-53%或诸如49%-51%,或者
(iii)在70%-90%范围内的羟基组分,诸如75%-85%、诸如77%-83%或诸如79%-81%。
在本发明的另一实施方案中,解吸步骤可以是逐级洗脱,其包括(i)、(ii)或(iii)中提及的解吸洗脱液羟基组分浓度中的两者或更多者的组合,诸如所有三者的逐步组合。通过在解吸期间添加羟基组分的浓度梯度进行洗脱,从而获得包含不同多酚化合物的解吸洗脱液,也可以是有利的。因此,在本发明的一个实施方案中,可以在解吸期间以从最多100%至最小1%的梯度提供羟基组分,诸如从最多90%至最少15%,诸如从最多90%至最少70%,诸如从最多60%至最少40%,诸如从最多30%至最少10%。在上述实施方案中,羟基组分最初具有高浓度,然而,自低浓度过渡到高浓度可能是有利的。因此,在本发明的另一实施方案中,可以在解吸期间以从至少1%到至多100%的梯度提供羟基组分,诸如从至少15%到至多90%,诸如从至少10%到至多30%,诸如从至少40%到至多60%,诸如从至少70%到至多90%。在另一实施方案中,解吸步骤作为根据本发明的任何梯度范围的逐级组合来提供。通过进行逐级洗脱,收集多种洗脱物(每种洗脱物具有不同多酚的不同含量),随后可以混合两种或更多种所收集的洗脱物以获得这样的最终产物,该最终产物的多酚特别是绿原酸的异构体平衡更精确地类似于原料中存在的多酚特别是绿原酸的异构体平衡。如果只收集到一种洗脱物,则也许不可能达到上述效果。
如此前所提到的,温度影响乙酯的形成。因此,在本发明的一个实施方案中,解吸可在80℃以下的温度下进行,诸如在75℃以下,诸如在50℃以下,诸如在35℃以下,或诸如在20℃至30℃的范围内。然而,由于解吸的速度在较高温度下较快,这又得进行折中。
在解吸之后,可以有利的是,进一步调节洗脱物的pH以避免形成乙酯。因此,在一个实施方案中,在解吸后将pH调节至3.5-6的范围内,诸如3.5-5,诸如3.5-4.5,诸如4-5,或诸如约4或5的pH。
所获得的洗脱物包含羟基组分,并且为了进一步提高洗脱物中多酚的浓度,可将羟基组分与多酚分离。
洗脱后的分离步骤,以及任选的pH调节,可按不同的方式进行。在本发明的一个实施方案中,可以通过蒸发来进行步骤(vi)中的分离。由于温度也影响乙酯的形成,因此洗脱物的蒸发在80℃以下的温度下进行,诸如在75℃以下,在60℃以下,诸如在40℃至60℃的范围内,或诸如45℃至5℃的范围内,优选地约50℃。然而,由于解吸的速度在升高的温度下更快,这又得进行折中。在蒸发之后,得到包含羟基组分的蒸发相和包含多酚的冷凝相。
优选地,残余相中存在的羟基组分的含量小于5%(w/w),更优选地小于1%(w/w),甚至更优选地小于0.1%(w/w),更优选地小于0.01%(w/w)。
应当理解,pH调节可以在羟基组分的分离(诸如蒸发)之前或在羟基组分的分离(诸如蒸发)之后进行。此外,pH调节可以在羟基组分的分离之前和之后进行。因此,在本发明的一个实施方案中,解吸洗脱液的pH可被调节到在3.5至6范围内,诸如3.5至5,诸如3.5至4.5,诸如4至5或诸如约4或5的pH。在本发明的一个实施方案中,分离步骤(诸如蒸发)在分离之前进行、在分离之后进行或在分离之前和之后进行。在分离步骤之后,解吸洗脱液可以存在于酸性溶液中,其中多酚可以其疏水及显著不溶的形式存在。为了更好地溶解多酚,如上所述地进行pH调节可以是有利的。
为了使纯化方案具有工业实用性,处理时间可以是重要的。因此,在本发明的一个实施方案中,处理时间可为36小时或更少,诸如30小时或更少,例如25小时或更少,诸如20小时或更少,例如18小时或更少,诸如15小时或更少,例如12小时或更少,诸如10小时或更少,例如5小时或更少。在本发明的上下文中,处理时间涉及以下过程的时段:从原料溶解,直到洗脱物已经分离成包含羟基组分的相和包含多酚的残余相,从而获得根据本发明的富集多酚的级分。
富集多酚的级分可进一步纯化。因此,在本发明的一个实施方案中,富集多酚的级分可通过色谱、超滤、纳滤、微滤、反渗透或其任何组合来进一步纯化。最终产物还可冷冻干燥。
除了涉及纯化方法之外,本发明还涉及能通过这种方法获得的产物。因此,本发明的另一方面涉及能从根据本发明的方法获得的富集多酚的级分。此类产物可能是非常独特的,因为它们具有与原始存在于原材料中的多酚平衡相类似的多酚平衡,特别是绿原酸的平衡。
在本发明的一个实施方案中,富集多酚的级分的多酚含量基于干物质计可为至少35%(w/w),诸如至少45%,诸如至少55%,诸如至少65%或诸如至少75%。因此,在本发明的一个实施方案中,富集多酚的级分中多酚乙酯的含量基于干物质计并且相对于多酚总含量而言可为在20%(w/w)以下,诸如在15%(w/w)以下,例如在10%(w/w)以下,诸如在5%(w/w)以下,例如在1%(w/w)以下,诸如在0.1%至20%(w/w)的范围内,诸如在0.1%至10%的范围内,诸如在0.1%至5%的范围内,诸如在0.1%至4%的范围内,诸如在0.1%至3%的范围内,诸如在0.1%至2%的范围内,或诸如在0.1%至1%的范围内。在本发明的一个更具体的实施方案中,富集多酚的级分中,基于干物质计,多酚含量可为至少35%(w/w),并且基于干物质计和相对于总多酚的含量,多酚的乙酯可为在20%(w/w)以下,诸如介于0.1%至20%(w/w)之间。
因此,在本发明的一个实施方案中,多酚可为绿原酸(CGA)、咖啡酸或它们的组合。在本发明的另一实施方案中,绿原酸(CGA)可选自:3-咖啡酰奎尼酸(3CQA)、4-咖啡酰奎尼酸(4CQA)、5-咖啡酰奎尼酸(5CQA)、3,4-二咖啡酰奎尼酸(3,4二CQA)、3,5-二咖啡酰奎尼酸(3,5二CQA)、4,5-二咖啡酰奎尼酸(4,5二CQA)、3-阿魏酰奎尼酸(3FQA)、4-阿魏酰奎尼酸(4FQA)、5-阿魏酰奎尼酸(5FQA)、咖啡酸和其任何组合。
在本发明的另一实施方案中,富集多酚的级分可包含3-咖啡酰奎尼酸(3CQA)、4-咖啡酰奎尼酸(4CQA)、5-咖啡酰奎尼酸(5CQA)、3,4-二咖啡酰奎尼酸(3,4二CQA)、3,5-二咖啡酰奎尼酸(3,5二CQA)、4,5-二咖啡酰奎尼酸(4,5二CQA)、3-阿魏酰奎尼酸(3FQA)、4-阿魏酰奎尼酸(4FQA)、5-阿魏酰奎尼酸(5FQA)和咖啡酸。
在本发明的另一实施方案中,相对于原料中存在的含量而言,富集级分中3-咖啡酰奎尼酸(3CQA)、4-咖啡酰奎尼酸(4CQA)、5-咖啡酰奎尼酸(5CQA)、3,4-二咖啡酰奎尼酸(3,4二CQA)、3,5-二咖啡酰奎尼酸(3,5二CQA)、4,5-二咖啡酰奎尼酸(4,5二CQA)、3-阿魏酰奎尼酸(3FQA)、4-阿魏酰奎尼酸(4FQA)和5-阿魏酰奎尼酸(5FQA)各者的含量至多偏离30%(w/w),诸如至多25%(w/w);例如至多20%(w/w),诸如至多15%(w/w);例如至多10%(w/w)。
在本发明的另一实施方案中,绿原酸(CGA)可包含至少50%(w/w)单-咖啡酰奎尼酸,和/或至多25%(w/w)二-咖啡酰奎尼酸。在另一相似的实施方案中,富集多酚的级分包含基于干物质计至少12%(w/w)的3-咖啡酰奎尼酸(3CQA)、4-咖啡酰奎尼酸(4CQA)或5-咖啡酰奎尼酸(5CQA)中的至少一种,诸如所述化合物中的至少两种,优选地所述化合物中的全部三种。
在本发明的另一实施方案中,富集多酚的级分可包含基于干物质计小于12%(w/w)的3,4-二咖啡酰奎尼酸(3,4二CQA)、3,5-二咖啡酰奎尼酸(3,5二CQA)或4,5-二咖啡酰奎尼酸(4,5二CQA)中的至少一种,诸如所述化合物中的至少两种,优选地所述化合物中的全部三种。
在本发明的又另一个实施方案中,富集多酚的级分可包含基于干物质计小于12%(w/w)的3-阿魏酰奎尼酸(3FQA)、4-阿魏酰奎尼酸(4FQA)或5-阿魏酰奎尼酸(5FQA)中的至少一种,优选地包含全部三种。
富集多酚的级分可以直接用作食物成分或形成食物成分的一部分。因此,本发明的另一方面涉及一种食物成分,其包含根据本发明的富集多酚的级分。在本发明的一个实施方案中,食物成分可包含相对于食物成分中多酚的总量而言介于0.1%至20%(w/w)之间的多酚乙酯,诸如在0.1%至10%的范围内,诸如在0.1%至5%的范围内,诸如在0.1%至4%的范围内,诸如在0.1%至3%的范围内,诸如在0.1%至2%的范围内,或诸如在0.1%至1%的范围内。
该富集多酚的级分或该食物成分可用于食物产品。因此,本发明的又一方面涉及包含根据本发明的富集多酚的级分和/或食物成分的食物产品。在一个实施方案中,食物产品包含相对于食物产品中的多酚的总量而言介于0.1%至20%(w/w)之间的多酚乙酯,诸如在0.1%至5%的范围内,诸如在0.1%至10%的范围内,诸如在0.1%至4%的范围内,诸如在0.1%至3%的范围内,诸如在0.1%至2%的范围内,或诸如在0.1%至1%的范围内。
多酚可用于不同的目的,以改善食物产品。因此,本发明的一个方面涉及根据本发明的富集多酚的级分和/或根据本发明的食物成分作为产生香味、风味和/或发泡的前体的用途。
在又另一方面,本发明涉及一种药物组合物,其包含根据本发明的富集多酚的级分以及药学上可接受的载体。由于多酚可以在体内表现出生物活性,例如抗氧化剂、酶的活化剂/抑制剂及受体,因此多酚可被认为是药物组合物中的相关组分。
应当注意,在本发明的其中一个方面的上下文中描述的实施方案和特征也适用于本发明的其他方面。
现将在下面的非限制性实施例中进一步详细描述本发明。
方法
级分
生咖啡级分由纯的或脱咖啡因的生罗布斯塔(Robusta)咖啡豆制成。
树脂
Amberlite FPX66(CAS N°9003-69-4)是商业食品级树脂,其化学结构由大网状芳族聚合物(即苯乙烯)组成。由于苯乙烯环不是官能化的,所以该基质是相当疏水的。
实验室规模的实验的纯化设置
-柱:带热护套的XK 50/30玻璃柱(通用医疗(GE Healthcare))
工作台规模的纯化设置
-柱:带热护套的XK 50/100玻璃柱(通用医疗(GE healthcare))
通过HPLC-UV分析绿原酸
通过HPLC-UV使用以下设置进行绿原酸(CGA)的分析:
-系统-HPLC为Ultimate 3000,由提供。它配备了四元泵、进样器、UV检测器和Chromeleon软件。
-样品制备-样品是粉末或级分。将粉末以2mg/mL的浓度溶解于甲醇:水(80:20)中。将级分在甲醇:水(80:20)中稀释,使得被分析物的范围在0.2mg/mL以下。
-HPLC方法-色谱分离在环境温度下在Spherisorb ODS-1柱,5μm,250×4.6mm(沃特世公司(Waters))上实现。应用A/B(A:92%水/8%乙腈/1mL/L正磷酸,B:50%水/50%乙腈/2mL/L正磷酸)的二元梯度。进样体积为20μL。绿原酸分析的波长设定在325nm,咖啡因分析的波长设定在275nm。
-绿原酸异构体-所使用的方法能够在45分钟内测定咖啡因和九种主要的绿原酸:3种咖啡酰奎尼酸(CQA)、3种阿魏酰奎尼酸(FQA)和3种二-咖啡酰奎尼酸(二-CQA)的浓度。
-校准-使用外标执行校准。使用在甲醇:水(80:20)中浓度为0.2mg/mL的两种标准品(5-CQA和咖啡因)。使用来自成都普瑞法科技开发有限公司(Biopurify)的纯标准品测定绿原酸异构体的换算系数。
根据以下公式,其他CQA的以克/100克表示的浓度由5-CQA的浓度确定:
-式中:
-W是以每100克新鲜产品的克数计的被分析物浓度。
-AS是测试样品溶液中被分析物的峰面积。
-C0是以毫克/毫升计的标准品中被分析物的浓度,(5-CQA,如果被分析物不在标准品溶液中)。
-P是当纯度小于0.95时标准品中被分析物的纯度(如果纯度≥0.95,P=1)。
-Vs是测试溶液的体积,单位为毫升
-D是稀释系数(10或1)。
-F是允许由5-CQA标准品计算其他绿原酸异构体的校正系数。
用于解吸研究和级分组成的LC-MS分析
通过LC-UV-MS/MS如下对咖啡级分进行表征:
-系统:使用1200SL、DAD检测器(安捷伦科技有限公司(Agilent))和QToF 6520(安捷伦科技有限公司(Agilent))进行分析
-样品制备:直接进样
-HPLC方法:在联接到QToF 6520(安捷伦科技有限公司(Agilent))的Kinetex C18柱,2.6μm,100×2.1mm(美国菲罗门公司(Phenomenex))上实现色谱分离。应用A/B(A:0.1%甲酸,B:0.1%甲酸的MeOH溶液)的二元梯度。
-柱温度保持在30℃。样品在水中的浓度为约10mg/mL。进样体积为3μL。波长设定在325nm,参照设定在385nm,并且对于两者,带宽均为2nm。
-MS参数:质谱仪QTOF 6520(安捷伦科技有限公司(Agilent))在正负ESI模式下使用,并且在MS模式下操作以跟踪绿原酸的解吸并在自动MS/MS模式操作进行化合物鉴定。
实施例1-沉淀
在沸水中以50%TC(干物质含量)制备生咖啡提取物(即,含咖啡因的/脱咖啡因的),没有任何问题。
由于未处理的提取物会导致柱的堵塞,所以通过在80%乙醇(V/V)中沉淀生咖啡提取物的高分子量(HMW)化合物(即蛋白质、类黑精、阿拉伯半乳聚糖)将这类化合物去除。通过在布氏(Büchner)过滤器(孔隙度等级1)上过滤除去沉淀。进一步蒸发乙醇。之后,在处理之前和之后通过HPLC-UV评估CGA(绿原酸)的浓度。主要结果为:
-在沉淀HMW化合物后没有观察到柱的堵塞。
-80%乙醇处理不影响CGA溶解度。
-CGA中的损失低并且大多包埋在沉淀物中。
总之,醇类(诸如乙醇)在根据本发明的方法中尤其的有用。
实施例2-吸附
首先原样使用由实施例1获得的咖啡溶液评定吸附。其显示吸附速率较差。然后,将由实施例1获得的咖啡溶液酸化至pH 1,以增强CGA物质和树脂的芳族聚合物之间的疏水相互作用的强度。通过HPLC-UV分析CGA显示:
-没有酸化的提取物保留较差(11%)。
-酸化至pH 1显著改善多酚的保留。与咖啡提取物的天然pH(即pH 4至7)相比,采用酸化步骤时吸附速率几乎加倍。最终吸附速率增加至约19%。随后通过优化咖啡/树脂的比例进一步改善该值。
-在酸性条件下,仅CGA和其他疏水性化合物被柱保留,而亲水性分子(例如矿物质和糖)通过。
总之,酸性环境改进了本公开的方案的吸附步骤。
实施例3-柱漂洗
为了除去未保留但仍存在于柱的死体积中的化合物,用水和0.1M HCl进行漂洗。之后,检查洗涤水的CGA。作为主要发现,发现了:
-纯水倾向于解吸CGA。
-在酸性条件下,由于绿原酸保持其质子化和疏水形式,所以保持与树脂的相互作用。CGA在用0.1M HCl漂洗柱时不被解吸。
-当包括洗涤步骤时,最终富集级分的纯度由50%增加至66%。
总之,洗涤步骤提高了最终产物的纯度。
实施例4-解吸
对于CGA解吸,必须削弱树脂和酚化合物之间的疏水相互作用。考虑到食品级纯化级分,选择乙醇作为有机溶剂。加入KOH(10-4M)以便提高解吸溶液的pH。将该乙醇/KOH混合物(90/10V/V)用作解吸溶液并且与纯乙醇或乙醇/水混合物进行比较。发现了:
-当使用乙醇/水时,CGA不完全解吸。
-通过将解吸介质的pH升高至5,可显著提高解吸效率。通过使用乙醇/KOH,CGA为部分去质子化的,即它们对树脂具有较小的亲和力,并且因此观察到100%的解吸。
-温度升高至70℃降低30%的解吸持续时间。
为了确保纯化级分中CGA的组成保持与初始咖啡相同,至关重要的是了解不同异构体的解吸动力学以及含咖啡因样品的咖啡因的解吸动力学。因此,在解吸期间收集一系列级分。如图2所示,本研究显示:
-使用90%乙醇时,CQA、FQA和二-CQA在相同的时间间隔内被洗脱,从而可以同时解吸所有异构体。
-对于单一异构体,解吸的最大值也在较小时间范围内(数据未示出)。
-咖啡因开始与CGA一起洗脱,但比CGA解吸更缓慢。
实施例5-咖啡/树脂比例
为了优化咖啡/树脂比例,在吸附阶段期间在柱的出口处进行级分收集。通过UV在325nm(CGA的特征波长)处分析每种级分。最佳比例对应于CGA开始再次从柱中洗脱出来时的咖啡溶液的体积。由该溶液体积计算通过柱的咖啡固形物的相应质量。最佳咖啡/树脂比例被确定为约0.55g咖啡对应1g树脂。然而,由于从一种类型的咖啡到另一种类型的咖啡以及在相同种类的咖啡中,绿原酸的含量可能变化很大,所以该比例可变。
实施例6-实验室规模下纯化之前和之后的组成
在已经完成根据图3的纯化方案后,将组分与原料的含量进行比较。分析冷冻干燥的粉末的组成,以评估在纯化CGA期间出现的其他化合物的变化。如图4所示,主要变化如下:
-主要变化涉及CGA。其水平在富集的纯化级分中高出约2倍;
-碳水化合物和有机酸由于其高极性而显著降低(含量分别降为原来的1/12和1/10);
-氨基酸也降低,但幅度小于碳水化合物和有机酸;
-咖啡因存在并且经历富集高达1.2%(3倍多),虽然初始咖啡是脱咖啡因的咖啡;
-在“其他”类别中列出的未鉴定化合物的比例变为2.2倍。造成这种增加的化合物可具有与CGA相同的疏水性,并且因此在该过程中也被吸附。
进一步评估了富集的多酚级分的详细组成。CGA分布的分析显示如图5所示的以下结果。
-在实验室规模的纯化方案下,CGA水平从33%增加到56%。在富集的纯化级分中仍保持CGA异构体的初始平衡;
-FQA平衡保持不变。
-CQA的相对含量略有降低,特别是3-CQA的相对含量。该异构体的较高极性可解释其在树脂上的较差吸附。
-二-CQA(主要是3,5-二-CQA和4,5-二-CQA)的含量增加。两种咖啡酸残基可赋予这些异构体对树脂更高的亲和力(对于FQA和CQA为两种相互作用而不是一种),使其能够更有效地纯化。
-游离咖啡酸的比例显著增加(含量变为5倍),可能是由于在纯化过程中CQA的水解。
总体来说,异构体平衡可认为接近初始提取物的异构体平衡。
在所有纯化步骤的连续优化之后,可获得纯度为约70%的CGA级分和保留的CGA平衡。富集系数总体上约为2。该过程的关键步骤为:
-通过高分子量化合物在80%乙醇中沉淀进行的预纯化。
-在疏水树脂(即Amberlite FPX66)上的吸附阶段,该阶段通过在吸收之前酸化提取物至pH1来进行优化。
-用乙醇/KOH 10-4M(90/10)在70℃下进行的解吸阶段。
-pH调节为5,以维持蒸发期间CGA的溶解度并且改进冷冻干燥时级分的性能。
-富集级分也类似地富集其他含有芳族部分的疏水化合物类,诸如较少的CGA、NPPA、DKP和咖啡因。
实施例7-实验室规模下纯化之前和之后的纯可溶咖啡组成
由实施例6的实验室规模研究的发现,将如图9所示的优化方案应用于纯可溶咖啡。在本实施例中,应用以下条件:
-使用纯可溶咖啡作为原料
-用实验室规模的柱进行多酚富集级分生产。
结果是:
-在实验室规模的纯化方案下,被分级富集的CGA含量由10%增加到24%。在富集的纯化级分中仍保持CGA异构体的初始平衡;
-在实验室规模的纯化方案下,CGA水平从33%增加到56%。在富集的纯化级分中仍保持CGA异构体的初始平衡;
-该优化的方案可应用于纯可溶咖啡
实施例8-避免由CGA形成乙酯
研究了有利于由CGA不期望地形成乙酯的过程条件。随后在模型研究中研究了CGA降解的动力学和分别的CGA酯的形成。在该过程中,可形成CGA的乙酯。然而,这是不期望的,因为它可显著影响CGA平衡和富集级分的性质。
以下方案显示了产生乙酯的酯化的一般反应机理。酸和醇之间的反应通过质子转移催化,使得反应速率为pH依赖性的。作为第二关键参数,温度应该影响降解速率,因为这是化学反应的通常情况。评价两个参数以便确定避免CGA的乙基化的理想条件。
在实验期间,通过改变以下参数pH、温度和时间,在乙醇(75%乙醇溶液)存在下储存5-CQA。
该过程在以下条件下使用5-CQA酯化作为模型进行。
对于每次试验,将10mg的5-CQA溶解于40mL的75%乙醇溶液中。
-pH研究:用盐酸(32%)将pH调节至pH 1、pH 2.7和pH 4,使用NaOH溶液(4N)将pH调节至pH 12,并且将所有样品保持在80℃温度的实验室烘箱中2小时。
-温度研究:将CQA溶液用盐酸(32%)调节至pH 1,并且在实验室烘箱中在室温、50℃或80℃下保持2小时。
-时间研究:将5-CQA溶液调节至pH 1并且在室温或50℃下保持1小时、2小时、3小时和36小时(仅室温)。
-系统:使用具有DAD检测器(美国菲尼根质谱公司(Thermo Finnigan))和Rheos HPLC系统(美国菲尼根质谱公司(Thermo Finnigan))的LCQ Deca质谱仪(美国菲尼根质谱公司(Thermo Finnigan))在LC-DAD-MS系统上进行分析。
-样品制备:对于每个参数,将溶液的等分试样以1:10稀释,并且直接用于LC/MS-DAD分析。
-HPLC方法:在环境温度下在Zorbax Eclipse C18柱,5μm,150×3mm(安捷伦科技有限公司(Agilent))上进行分离。应用A/B(A:0.1%甲酸,B:甲醇)的二元梯度。
-MS参数:所使用的质谱仪是以FullScan和数据依赖的MS/MS模式(m/z 100-1000)操作的LCQ-Deca,用于化合物鉴定。
pH
通过LC/MS-DAD监测5-CQA的降解和相应乙酯的形成。图6显示在75%乙醇溶液中在不同pH下储存2小时的5-CQA的色谱图。pH研究显示:
-在pH 1时,在2小时内观察到5-CQA快速转化成其酯。
-在pH 2.7时,5-CQA酯化显著降低。
-在pH 4下,5-CQA在2小时后几乎不降解。
-强碱性条件(pH 12)引起完全不同的反应方案,包括水解5-CQA产生咖啡酸和奎尼酸。此外,碱性条件有利于通过3-CQA和4-CQA的出现观察到的5-CQA的异构化。
总之,在乙醇存在的条件下,富集级分的pH应该为约4,诸如4至5。因此,对于图6所示的根据本发明的方法中的步骤(v),约4至5的pH可能是最优的,其中可以看出,在较低的pH(pH 2.7及以下)下发生乙酯形成,而在较高的pH(pH 12)下,发生5-CQA水解产生咖啡酸和奎尼酸。此外,碱性条件有利于通过3-CQA和4-CQA的出现观察到的5-CQA的异构化。
温度
在下一步骤中,评价了温度的影响。为了模拟最坏情况,选择pH 1。实际上,其对应于前面实验中最关键的pH,并且其目前反映了纯化方案的条件。2小时后,通过LC/MS-DAD监测保持在三个温度即环境温度(室温)、50℃和80℃下的5-CQA的降解(图7)。温度研究显示:
-在室温下,仅少量的5-CQA转化成其乙酯。
-在50℃下,酯化速率升高。与天然5-CQA相比,高达40%的酯是可检测的。
-在80℃下,5-CQA至其乙酯的酯化进一步加速,得到与5-CQA相比相同量的酯。
总之,在乙醇存在的情况下,咖啡提取物和富集级分的温度应该降低,特别是在酸性条件下。
时间
虽然pH和温度与纯化装置的尺寸无关,但停留时间随着放大而明显增加。因此,下一项研究评估了在给定pH和温度下5-CQA转化成其乙酯的酯化动力学。该研究在pH 1下在室温和50℃下进行(图8)。时间研究显示:
-在50℃下,5-CQA在第一个3小时内稳定地转化成其乙酯。在对应于放大方案的当前解吸持续时间的时间段之后,形成30%的酯。
-在室温下,5-CQA的稳定性高得多。3小时后仅形成3%的酯。36小时后增加至14%。
总之,乙酯的形成取决于解吸步骤的pH和温度。
实施例9-大规模下纯化之前和之后的脱咖啡因咖啡组成
由实施例6的实验室规模研究的发现,将优化的方案(图9)放大以用于更大量地生产富集级分而不降解CGA。在本实施例中,应用以下条件:
-使用脱咖啡因的生咖啡提取物作为原料
-用1m柱进行多酚富集级分的生产。
生产5批以便评估纯化过程的可重复性。
进行脱咖啡因级分的完全表征,结果显示在图10中。
-脱咖啡因的分级富集的CGA含量从33%增加到63%。
-纯化后组成的变化与实验室规模制备期间观察到的变化相似(参见实施例6)。
-与实验室规模制备相比,其他化合物的群组较少富集(9.4%对18.8%)。
-与实验室规模相比,咖啡因的富集较低(0.8%对1.2%)。
CGA的详细组成示于图11中。
如在实验室规模条件下已经看到的,CGA平衡保持得相当好(实施例6)。
-主要变化涉及作为CGA中极性最高的化合物的3-CQA,其在纯化后不太丰富。
-相反地,更多的非极性二-CQA和FQA在纯化时被富集。
此外,评估了更新的方案(图9)的性能。
-总体回收率为24%。
-CGA的回收率为46%。
-与初始量相比,CGA富集系数为1.9。
此外,使用HPLC-UV/MS对最终产物中CGA及其酯的分析显示了:
-乙酯的转化大大降低
-酯的最终浓度不超过天然CGA浓度的1%
因此,确实可以在工业上适用的规模下针对脱咖啡因组合物进行根据本发明的方法,而不会大大影响多酚平衡或产生大量乙酯。
实施例10-大规模下纯化之前和之后的含咖啡因咖啡组成
对于含咖啡因的多酚富集级分,还按以下条件应用更新的方案(图9):
-使用含咖啡因的生咖啡提取物作为原料
-并行使用两个60cm柱进行多酚富集级分生产以减少停留时间。
-生产10批以便评估纯化过程的可重复性。
进行含咖啡因的级分的完全表征,结果可见于图12中。
-含咖啡因的分级富集的CGA含量从33%增加到53%。
-咖啡因的量从9.7%增加一倍以上至19.9%。
-碳水化合物和有机酸由于其高极性而大大降低。
-其他化合物略有增加。
-这些变化与脱咖啡因的富集级分观察到的变化相似。
富集的含咖啡因的级分中CGA的详细组成示于图13中。
-与脱咖啡因的富集级分相反,3-CQA浓度几乎保持不变。
-主要变化涉及5-CQA,其在纯化后不太丰富。
-总体而言,脱咖啡因的富集级分的组成变化较不明显,并且分布保持与初始咖啡非常相似。
对于含咖啡因的富集级分,分别分析十个批次以评价批次与批次之间的性能。
-发现总体回收率为34%,因此相对于脱咖啡因的富集级分(24%)更高。
-相较于脱咖啡因的富集级分的46%的回收率,CGA的回收率为55%。
-相较于脱咖啡因的富集级分的1.9的富集系数,CGA富集系数为1.6。
还进行HPLC-UV/MS以控制含咖啡因的富集级分中CGA及其酯的含量。数据未示出。
-酯的最终浓度不超过天然CGA浓度的1%
-如对于脱咖啡因的富集级分已经看到的,该形成不可完全避免。
因此,确实可以在工业上适用的规模下针对含咖啡因的组合物进行根据本发明的方法,而不会大大影响多酚平衡或产生大量乙酯。
实施例11-脱咖啡因的富集级分和含咖啡因的富集级分的制备的性能比较。
结论:
-使用图9中显示的方案,对于脱咖啡因的咖啡,可获得63%纯度的级分,而对于含咖啡因的咖啡,可获得53%纯度的级分。
-脱咖啡因的级分的更好性能可能是由于咖啡因的存在/不存在。由于咖啡因以2的系数被富集,所以对于含咖啡因的级分,咖啡因达到几乎20%的浓度,这同时降低CGA的相对浓度。
-对于其他化合物,在纯化后没有观察到脱咖啡因的级分和含咖啡因的级分之间的具体差异。
-脱咖啡因的级分和含咖啡因的级分之间,3-CQA、4-CQA和5-CQA的比例不同。这是由于在脱咖啡因过程中已经发生的异构化。与初始分布相比,纯化过程对富集级分中CGA的组成几乎没有影响,因此在整个过程中维持多酚的异构体平衡。
-在这两种情况下,酯的浓度不超过天然CGA浓度的1%。
-由于在该方法期间存在大量的CGA和乙醇,所以在不完全改变方案的情况下不可完全避免酯形成。因此,对于CGA富集级分的食品级制备物,小于1%的酯的量必须被认为是技术上不可避免的。
-批次与批次之间的可重现性非常好,相对标准偏差小于10%。因此,该方案适于从一个批次向另一批次递送富集CGA的级分,该级分具有指定量的CGA和众所周知的单一异构体平衡。
实施例12-乙醇浓度的优化
在前面的实施例中已经描述了纯化咖啡多酚的食品级方案,其中咖啡多酚吸附到疏水性树脂上。在等度条件下使用90%的含水乙醇进行解吸,在最终富集级分中多酚的纯度为60%至70%。
考虑到生产更具体的多酚产物,研究了纯化的咖啡多酚异构体的制备。为了这一目的,采用具有递减极性的溶剂(即含水乙醇20/80、50/50、80/20)的连续解吸步骤。
在解吸混合物中在乙醇比例递增的三个连续步骤中进行解吸。方案示出于图14中。如下获得三种纯化的富集级分:
步骤1-用乙醇/水/KOH 20/70/10(v/v/v)解吸;
步骤2-用乙醇/水/KOH 50/40/10(v/v/v)解吸;
步骤3-用乙醇/水/KOH 80/10/10(v/v/v)解吸。
通过应用梯度从食品级树脂进行解吸,获得三种不同的富集级分。然后通过HPLC-UV评估这些富集级分的绿原酸组成。图15示出了CGA的三个主要类别的相对贡献。图16示出了三种不同富集级分的HPLC色谱图。
主要发现:
-与先前所示的初始提取物的多酚相比,所有富集级分含有约两倍的多酚(即65-85%对33%);
-用20%乙醇解吸产生含有70.7%绿原酸的富集级分,该绿原酸中97%是单CQA并且2.4%是单FQA。因此,在低乙醇比例(即20/80)下获得几乎仅含有CQA的富集级分;
-用50%乙醇解吸产生含有85.7%绿原酸的富集级分,该绿原酸具有接近初始生咖啡提取物的分布。因此,在中间乙醇比例(即50/50)下获得具有CQA、FQA和二CQA的混合组成的富集级分;
-用80%乙醇解吸产生含有65.1%绿原酸的富集级分,该绿原酸中65%为较低极性的二-CQA。因此,在高乙醇比例(即80/20)下获得富集非极性二-CGA的级分。
这种梯度应用在期望改进各种形式的绿原酸化合物类的解吸的情况下可能是有帮助的,并且之后可将富集级分组合以提供与最初在咖啡中的CGA异构体平衡类似的CGA异构体平衡。在需要更具体的组成的情况下,梯度解吸也可以是有用的。
- 还没有人留言评论。精彩留言会获得点赞!