包括动物双歧杆菌亚种乳酸菌LMGP‑28149的组合物的制作方法
本发明涉及一种基于至少一种益生菌的组合物,该组合物用于痊愈性治疗超重人类的体重增加,和/或预防性治疗超重或曾经超重的人类的体重增加。
背景技术:
术语“超重”在本发明中指人类具有主要为腹部脂肪的体脂的异常或过多的堆积,这对他/她的健康有风险。在本发明的范围内,术语“超重”还包括人类的肥胖状况的特定且极端的情况。
术语“曾经超重”在本发明中应被理解为这个人已经进行了减肥,并且在3至5年的时段内具有被认为是正常(基于BMI或腰围/臀围的比率)的体重。
简单指数允许在一组给定人群的水平上,测量超重和肥胖,详细阐述该简单指数却是困难的。例如,因为儿童和青少年的身体经历与他们的生长相关的一定数量的生理学变化,因此用于衡量儿童和青少年中的超重和肥胖指数的比例与成人中所使用的比例不同。所以,依赖于年龄,WHO(世界卫生组织)向公众提供了不同的、用于依赖于个体的年龄或个体样品的平均年龄来衡量体重的方法。
作为例子,可在体重指数(BMI)的基础上评价成人中的超重,与目前用于估计成人超重和肥胖的尺寸相比,这代表了对体重的简单测量。它对应于体重除以尺寸的平方,以kg/m2来表示。
BMI的优点在于应用于两种性别,并且应用于所有的成人年龄区间。因此,BMI应被认为是近似指示,因为它不一定对应于依赖于个体的脂肪量的相同的百分比。
在本上下文中,WHO定义了在BMI的基础上的以下阈值用于确定成人是否是超重或肥胖:
-正常体重状况对应于介于20至25之间的BMI;
-超重状况对应于介于25至30之间的BMI;以及
-肥胖状况对应于等于或大于30的BMI。
但是,应当注意到,BMI没有给出相对于皮下脂肪,腹部脂肪分布的任何指示。
即使该指数具有对成人个体的所有年龄区间和两种性别进行一致分类的优点,但优选可与另一指标(可例如是测量个体的腰围)一起来补充解释该指数。
因此,腰围大于100cm的男性成人个体被认为是超重的。该阈值在成人女性中是88cm。
通过测量腰围(A)/臀围(H)的比率,可将该参数推广至所有年龄区间。
在男性个体中大于1的比率和在女性个体中大于0.85的比率被认为是超重。
一旦人类中的超重,尤其是人类肥胖被WHO认为是疾病,就在本发明的范围内应用术语“治疗”。
术语“痊愈性”在本发明中应被理解为,目的在于降低超重人类的体重和/或降低超重人类的体重增加的作用。因此,痊愈性治疗暗示了具有以下目的的作用:优选在饮食过程中和/或在饮食之后,达到在人类中被认为是正常的体重,即,对健康有较小的风险,在预定值的范围内,例如基于BMI其包含介于20至25之间、优选等于22。
术语“对健康有较小风险”在本发明范围内应被理解为在体重被认为正常时,发展成代谢综合征的风险是可以忽略的。
具体地,痊愈性作用主要的目的在于降低个体中的腹部脂肪或至少降低腹部脂肪的堆积。
术语“预防性”在本发明中应指具有以下目的的作用:稳定超重或曾经超重(即已经减肥了)的人类的体重,并因此在饮食过程中和/或饮食之后,预防或限制超重或曾经超重的人类的体重增加。预防性治疗还暗示具有以下目的的作用:优选在饮食过程中和/或饮食之后,维持稳定的体重,该体重优选在人类中被认为是正常的体重,在基于例如BMI(作为提醒,在20~25之间)的预定值的恒定范围内,但按照A/H比率正常体重也可被理解为在女性个体中小于0.85,且在男性个体中小于1.00。
目前,在全球范围内,相对于体重不足,超重和肥胖导致(因为相关疾病,如II型糖尿病或心血管疾病)更多的死亡。
具体地,体重和肥胖的比例已在全球范围内流行(考虑到每年超过至少3百万人的死亡在病理学上与他们的超重或肥胖相关),并且不再限于所谓的富有国家,现在体重和肥胖也影响低收入或中等收入的国家。
进一步地,证明了高BMI,有时与高A/H比率一起,在一个方面是促进代谢综合征的因素,其在本发明的范围内被定义为健康的风险因素的联合:动脉高血压、高甘油三酯血症、低HDL胆固醇水平和类固醇肥胖病症(例如腹部脂肪的堆积)和血糖增加。这些指标实际上形成对于以下三种主要已知定义所共有的定义基础:WHO的定义(公开于1998年,于1999年进行了修订),2001年公开的国家胆固醇教育计划(NCEP-ATPIII)的定义,以及2005年公开的国际糖尿病联盟的定义。
在实践中,以下指标以非详尽的方式表示了代谢综合征:异常高的胰岛素水平;II型糖尿病;高胆固醇血症(与低水平的“好”胆固醇HDL相关);高血压;体重增加随着时间显著增加;尤其如果是腹部肥胖;高甘油三酯血症;肝脂肪变性;系统性炎症病症的发展;以及,脂肪细胞肥大。
此外,以下指标以非详尽的方式表示了慢性疾病的风险:肌肉-骨骼障碍,尤其是关节病;或者,某些类型的癌症。
因此,导致人类超重的不受控制的体重增加的问题,被证明是在全球水平上对健康具有不可忽视的影响的社会问题。
从这个角度上,WHO在它的预防体重过度增加的全球策略中,提出了关于食物和体育运动的建议。由2004年世界卫生大会(WHA)所采用的此策略阐述了鼓励群众遵循健康饮食和规律运动所需的步骤。
但是,如果这一策略是基于预防体重增加的建议,则它对于超重或曾经超重的个体和具有再次增加体重风险的个体体重增加的痊愈性和预防性治疗没有提出任何指示。实际上,目前不受控制的体重增加的问题不再集中于具有正常体重(即具有正常的BMI和/或正常腰围)、但可能增加体重的个体,而是特别集中于从WHO指出近14亿超过20岁的人已显示出超重的那一刻起,已经超重的个体。在后者中,超过2亿男性和近3亿女性是肥胖的,并且在世界上,在10个成年人中超过1个成年人是肥胖的。
因此,非常需要一种治疗方法,能够降低或预防超重人类的超重或肥胖。优选地,该治疗方法应当不是非常强制性的,因为意识到与超重和肥胖相关的主要原因是缺乏努力遵循与治疗方法(有时可能是严格的)相关联的特定饮食。
具体地,本发明是已知因果关系的一部分,该已知因果关系使肠道微生物区与肥胖发展相关联(Ley et al.,2006.Nature,444:1022-1023;Nadal et al.,2008.Int J.Obes.,33(7):758-67)。
在这种情况下进行了很多研究,并且提供了包括大量文献的现有技术,其中文献提到在超重和肥胖的范围内使用基于益生菌的治疗方法。
具体地,已经示出微生物区有助于使宿主维持良好的健康状态。实际上,微生物区的平衡状态有助于调节肠道稳态和免疫平衡,从而微生物区的任何失衡都被解释为参与了代谢综合征的发展,尤其在发展该综合征的遗传易感性的个体中参与代谢综合征的发展(Parks et al.,Cell Metab,2012)。
对微生物区——体重增加的关系的鉴定曾是大量研究的推动力,是各专利申请的主题,下面对相关度最高的专利申请进行评述。
首先,应当提到国际专利申请WO2007043933,其中提出以发酵奶的形式使用干酪乳杆菌(Lactobacillus casei)F19和嗜酸乳杆菌(L.acidophilus)NCFB 1748,以及乳双歧杆菌(Bifidobacterium lactis)Bb12的菌株,来降低食欲以及脂肪在特定组织中的堆积,从而控制人类的体重。但是,该申请中所声称的效果似乎主要起源于钙和乳蛋白的共同作用,而不是上述细菌菌株的存在。此外,该效果仅靶向与小肠代谢相关的基因表达,因此不涉及参与体重增加的其它器官和组织。
其次,文献US20100061967A1也提出使用细菌组合物来调整调节饱足机制的肽的表达,该调整仅发生在胃肠道中。
国际专利申请WO2009153662公开了基于双歧杆菌(Bifidobacteriesa)和乳酸杆菌(Lactobacilli)的组合物在治疗糖尿病中的应用,该应用仅基于这些微生物降低周围组织的炎症的能力,而这些微生物并不作用于中枢神经系统,因此例如不作用于饱足的中枢调节机制,其中糖尿病是与超重或肥胖诱导的代谢综合征相关的指示疾病列表下的一种疾病。
此外,文献US20100150890提供了以下信息:组合物中的益生菌在刺激交感神经系统的功能中的应用,以便刺激代谢,因此刺激能量消耗。但是,示出交感紧张在某些肥胖个体中也是活跃的,因此它的活化在治疗超重和肥胖的范围内不是可靠的选择方案。
专利申请US20100111915显示了益生菌的组合物作为在预防儿童肥胖的范围内的选择方案的一般应用。按照US20100111915记载的内容,这一应用基于益生菌的双歧效果,但该文献没有给出任何具体的根据,其给出证实肠道中的双歧杆菌的数量增加可能是预防儿童出现肥胖的作用的起因。
文献US20050112112提出微生物的组合物从存在于胃肠道中的单糖和二糖生成不能被人类消化的糖聚合物的应用,从而实际上降低糖在体内的吸收。
最后,文献JP10306028也给出了以下信息:使用双歧杆菌与壳聚糖的组合,对胆固醇被身体的吸收具有抑制作用。
不幸的是,即使现有技术中的组合物能降低超重和肥胖,并且能降低与代谢综合征相关的症状(例如,这被称为缓解),使用现有技术中的组合物也不能持续3至5年以上(例如,这被称为痊愈),使体重长期维持在期望的正常水平(即对应于例如介于20至25之间的BMI)。
技术实现要素:
在本发明的范围内,应当将缓解与痊愈区分开。如果一个体在体检过程(体重、腰围测量等)中不再检测到超重,则该个体被称为处于缓解状态。但仅在特定的额外时间间隔之后,才称为痊愈,其中特定的额外时间间隔取决于超重类型。通常,当缓解持续3年或5年时,才被认为痊愈了。
本发明的目标是通过提供在开始所述的组合物来克服现有技术的不足,该组合物的特征在于,所述益生菌是动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149。
按照布达佩斯条约,根据本发明的菌株于2014年1月27日保藏于BCCM(比利时微生物保藏中心,Belgian Coordinated Collections of Micro-organisms)和LMG(微生物细菌实验室,Laboratorium voor Microbiologie- ),保藏编号为LMG P-28149。
在本发明的范围内,上述组合物优选包括在存活条件下的益生菌动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149。术语“在存活条件下”指存活细菌在上述组合物中的浓度介于108CFU/g组合物和1013CFU/g组合物之间。
在本发明的范围内,观察到该特定益生菌的菌株对饱足,以及与限制体重增加相关的肠道微生物区的恢复都具有显著的积极作用。
明显观察到动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149的存在对肠道中的阿克曼菌(Akkermansia muciniphila)重新定殖具有作用,其中阿克曼菌(Akkermansia muciniphila)是因其在防止人类肥胖中的作用而闻名的一种细菌,它的水平在超重或肥胖个体中大大降低。
进一步地,还令人惊奇地观察到根据本发明的菌株的抗炎和免疫调节作用,这与转录因子PPARγ的表达的恢复相关,该转录因子PPARγ参与调节白色脂肪组织的T淋巴细胞的功能。
因此,根据本发明的组合物明显能够在超重人类中,痊愈性或预防性治疗肠道微生物区障碍和与该障碍相关的炎性疾病。
因此,本发明有利地旨在于痊愈性或预防性治疗与人类超重相关的代谢综合征。
因此,根据本发明,证明了基于动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149的组合物对身体明显具有以下效果,该效果优选在饮食过程中和/或在饮食之后,伴随在富含脂肪的饮食下体重增加降低,或伴随体重的稳定:改善胰岛素敏感性;降低腹部和皮下脂肪量的发展;减小脂肪细胞的大小;尤其通过促炎性巨噬细胞,降低白色脂肪组织的细胞浸润;减少炎性标记物;限制肝脂肪变性;以及,限制或降低“坏”的胆固醇水平。
可以看出,根据本发明的至少包括益生菌动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149的组合物作用于与超重相关的各种因素。
在本发明的范围内,还证明了不仅处于或不处于存活条件下的具体动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149菌株,而且来源于该菌株的化合物,都具有对体重增加的预防性和痊愈性作用,并且对超重人类的代谢综合征也有作用。
在本上下文中,根据本发明的组合物可进一步包括至少一种益生菌成分或至少两种益生菌成分的组合,各成分都来源于动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149,并且选自由细胞壁的成分、细胞器的组分、核酸、细胞膜的成分和细胞代谢物所组成的组。
作为例示而不用作限制,上述细胞壁的成分选自由肽聚糖、蛋白、多糖、磷壁酸,或它们的组合所组成的组。
作为例示而不用作限制,上述代谢物选自由有机酸、无机酸、蛋白、肽、氨基酸、酶、脂质、碳水化合物、糖脂、糖蛋白、维生素、盐、金属或它们的组合所组成的组。
在具体实施方式中,根据本发明的组合物包括:丁酸盐,或至少一种它的衍生物;和/或,丙酸盐,或至少一种它的衍生物;通过动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149来促进该丁酸盐和/或丙酸盐的诱导
或者,根据本发明的组合物包括至少一种额外的益生菌,所述额外的益生菌选自由以下益生菌组成的组:古生菌(Archaea)、厚壁菌(Firmicutes)、拟杆菌(Bacteroidetes)、变形菌(Proteobacteria)、放线菌(Actinobacteria)、疣微菌(Verrucomicrobia)、梭杆菌(Fusobacteria)、产甲烷菌(Metanobacteria)、螺旋菌(Spirochaetes)、丝状杆菌(Fibrobacters)、脱铁杆菌(Deferribacteres)、异常球菌(Deinococcus)、栖热菌(Thermus)、蓝细菌(Cyanobacteria)、甲烷短杆菌(Methanobrevibacterium)、乳杆菌(Lactobacillus)、消化链球菌(Peptostreptococcus)、瘤胃球菌(Ruminococcus)、粪球菌(Coprococcus)、萨博得林氏菌(Subdolingranulum)、多尔氏菌(Dorea)、布雷第菌(Bulleidia)、厌氧菌(Anaerofustis)、孪生球菌(Gemella)、罗氏菌(Roseburia)、凯特妮菌(Catenibacterium)、小杆菌(Dialister)、安罗仓科斯菌(Anaerotruncus)、葡萄球菌(Staphylococcus)、微球菌(Micrococcus)、丙酸杆菌(Propionibacterium)、肠杆菌(Enterobacteriaceae)(非致病性)、霍氏杆菌(Faecalibacterium)、拟杆菌(Bacteroides)、普拉菌(Parabacteroides)、普氏菌(Prevotella)、真杆菌(Eubacterium)、阿克曼菌(Akkermansia)、芽胞杆菌(Bacillus)、丁酸弧菌(Butyrivibrio)和梭菌(Clostridium),或它们的组合。
优选地,根据本发明的组合物可进一步包括至少一种真菌和/或酵母菌株,所述菌株选自由酵母(Saccharomyces)、念珠菌(Candida)、毕赤酵母(Pichia)、德巴利氏酵母(Debaryomyces)、球拟酵母(Torulopsis)、曲霉菌(Aspergillus)、根霉菌(Rhizopus)、毛霉菌(Mucor)和青霉菌(Penicillium)所组成的组。
优选地,根据本发明的组合物包括用于封装益生菌的载体,其中,上述动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149和可选的上述至少一种额外的益生菌被封装在该载体中。
有利地,上述真菌和/或上述酵母也被封装在上述载体中。
或者,上述封装载体包括选自由藻酸盐、壳聚糖、果胶、普鲁兰多糖、明胶、角叉菜胶、琼脂凝胶或它们的组合所组成的组中的至少一种物质。
优选地,上述至少一种物质是水胶体。
有利地,根据本发明的组合物包括选自由单糖、多糖、氨基酸、肽、蛋白、维生素、酵母提取物、卤盐、碱金属或碱土金属、抗氧化剂、甘油、乙酸锌、氯化锌、乳酸锌、抗坏血酸、柠檬酸、植物油、乳脂或它们的组合所组成的组中的至少一种食物源。
在具体实施方式中,根据本发明的组合物是包括至少一种益生元的共生组合物。
优选地,所述至少一种益生元以非限制性的方式选自由低聚糖、低聚果糖、低聚半乳糖、低聚木糖、菊粉或它的衍生物、乳果糖或它的衍生物、低聚甘露糖,或它们的组合所组成的组。
优选地,根据本发明的组合物包括覆盖上述动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149和可选的上述至少一种额外的益生菌的第一肠溶包衣。具体的,该第一肠溶包衣选自由乙基纤维素、羟丙基纤维素、羧甲基纤维素、聚合物(诸如)或它们的组合所组成的组。
或者,上述组合物进一步包括选自由藻酸盐、壳聚糖、果胶、普鲁兰多糖、明胶、角叉菜胶、琼脂凝胶、纤维素、半纤维素、乙基纤维素、羧甲基纤维素或它们的组合所组成的组中的第二外包衣。
在另一可选实施方式中,根据本发明的组合物包括一种或几种生物相容性赋形剂。
根据本发明的组合物可用于在怀孕女性或生完孩子的女性中,或在处于“拟娩”仪式或曾经处于“拟娩”仪式的男性中,痊愈性或预防性治疗过度的体重增加(即,普遍超过伴随怀孕所发生的体重增加)。
根据本发明,上述组合物可表现为基于该组合物的食物,或进一步包含(优选处于存活条件下的)动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149的食物补充物的食物组合物。
在本发明的意义上,术语“食物组合物”应当指在食品市场上普遍存在的组合物(例如零食、即食食品、饮料等)。
在本发明的意义上,术语“食物补充物”应被理解为食料,它的目的是提供具有营养学和/或生理学效果的营养物或物质的补充。
根据本发明,可提供上述组合物以经由口或舌下途径来使用和摄入,但也可经由呼吸,优选经由鼻或支气管,或进一步经由直肠来使用和摄入。
上述组合物也可是至少基于来自上述益生菌的成分的可注射的液体组合物,并且用于皮下注射。
优选地,根据本发明的组合物可被调制为片剂、丸剂、胶囊、颗粒剂、粉末、流体、液体、乳膏或喷雾剂。
根据本发明,上述组合物可用于在怀孕女性或生完孩子的女性中,或在处于“拟娩”仪式或曾经处于“拟娩”仪式的男性中,痊愈性或预防性治疗过度的体重增加(即,普遍超过伴随怀孕所发生的体重增加)。
在所附的权利要求书中,给出了根据本发明的治疗组合物的其它实施方式和应用。
本发明还涉及包括至少一种益生菌的组合物在超重或曾经超重的人类中的非治疗性美容应用,该益生菌是动物双歧杆菌亚种乳酸菌Bifidobacterium animalis ssp.Lactis编号LMG P-28149。
优选地,用于非治疗性美容应用的上述组合物包括选自由以下益生菌所组成的组中的至少一种额外的益生菌:古生菌(Archaea)、厚壁菌(Firmicutes)、拟杆菌(Bacteroidetes)、变形菌(Proteobacteria)、放线菌(Actinobacteria)、疣微菌(Verrucomicrobia)、梭杆菌(Fusobacteria)、产甲烷菌(Metanobacteria)、螺旋菌(Spirochaetes)、丝状杆菌(Fibrobacters)、脱铁杆菌(Deferribacteres)、异常球菌(Deinococcus)、栖热菌(Thermus)、蓝细菌(Cyanobacteria)、甲烷短杆菌(Methanobrevibacterium)、乳杆菌(Lactobacillus)、消化链球菌(Peptostreptococcus)、瘤胃球菌(Ruminococcus)、粪球菌(Coprococcus)、萨博得林氏菌(Subdolingranulum)、多尔氏菌(Dorea)、布雷第菌(Bulleidia)、厌氧菌(Anaerofustis)、孪生球菌(Gemella)、罗氏菌(Roseburia)、凯特妮菌(Catenibacterium)、小杆菌(Dialister)、安罗仓科斯菌(Anaerotruncus)、葡萄球菌(Staphylococcus)、微球菌(Micrococcus)、丙酸杆菌(Propionibacterium)、肠杆菌(Enterobacteriaceae)(非致病性)、霍氏杆菌(Faecalibacterium)、拟杆菌(Bacteroides)、普拉菌(Parabacteroides)、普氏菌(Prevotella)、真杆菌(Eubacterium)、阿克曼菌(Akkermansia)、芽胞杆菌(Bacillus)、丁酸弧菌(Butyrivibrio)和梭菌(Clostridium),或它们的组合。
有利地,用于非治疗性美容应用的上述组合物包括选自由酵母(Saccharomyces)、念珠菌(Candida)、毕赤酵母(Pichia)、德巴利氏酵母(Debaryomyces)、球拟酵母(Torulopsis)、曲霉菌(Aspergillus)、根霉菌(Rhizopus)、毛霉菌(Mucor)和青霉菌(Penicillium)所组成的组中的真菌和/或酵母菌株。
优选地,在用于非治疗性美容应用的上述组合物中,上述动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149和可选的上述至少一种额外的益生菌被封装在封装载体中。
有利地,在用于非治疗性美容应用的上述组合物中,上述封装载体包括选自由藻酸盐、壳聚糖、果胶、普鲁兰多糖、明胶、角叉菜胶、琼脂凝胶和它们的组合所组成的组中的至少一种物质。
有利地,用于非治疗性美容应用的上述组合物包括选自由单糖、多糖、氨基酸、肽、蛋白、维生素、酵母提取物、碱金属或碱土金属的卤盐、抗氧化剂、甘油、乙酸锌、氯化锌、乳酸锌、抗坏血酸、柠檬酸、植物油、乳脂或它们的组合所组成的组中的至少一种食物源。
优选地,用于非治疗性美容应用的上述组合物进一步包括至少一种益生元,从而形成共生组合物。
优选地,用于非治疗性美容应用的上述组合物包括覆盖上述动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149和可选的上述至少一种额外的益生菌的第一肠溶包衣。
有利地,在用于非治疗性美容应用的上述组合物中,上述第一肠溶包衣选自由乙基纤维素、羟丙基纤维素、羧甲基纤维素、或它们的组合所组成的组。
优选地,用于非治疗性美容应用的上述组合物包括选自由藻酸盐、壳聚糖、果胶、普鲁兰多糖、明胶、角叉菜胶、琼脂凝胶、纤维素、半纤维素、乙基纤维素、羧甲基纤维素或它们的组合所组成的组中的第二外包衣。
有利地,用于非治疗性美容应用的上述组合物进一步包括一种或几种生物相容性赋形剂。
在所附的权利要求中示出了根据本发明的组合物的用于非治疗性美容应用的其它形式。
本发明还涉及益生菌动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149的培养基,该培养基包括至少一种蛋白源和至少一种碳水化合物源,该培养基的特征在于它进一步包括谷胱甘肽。
谷胱甘肽是三肽,参与维持细胞的细胞质的氧化还原电位,以及一定数目的活性氧类的解毒和去除反应。
令人惊奇地是,示出在本发明的范围内,这样的包括谷胱甘肽的培养基优化益生菌动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149菌株的效能,对此,观察到对超重或曾经超重人类中的体重增加的痊愈性或预防性作用。
优选地,根据本发明的培养基包括浓度介于20g/l培养基至30g/l培养基之间的谷胱甘肽。
有利地,根据本发明,上述培养基的蛋白源选自由乳清蛋白胨、酪蛋白胨、植物或细菌蛋白胨,和它们的组合所组成的组。
优选地,根据本发明,上述培养基的碳水化合物源包括至少一种糖或多种糖的混合物,所述糖选自由乳糖、葡萄糖、半乳糖、果糖、麦芽糊精、淀粉、海藻糖、麦芽三糖和它们的组合所组成的组。
优选地,根据本发明,上述培养基进一步包括至少一种氨基糖,例如氨基葡萄糖或氨基半乳糖。
优选地,根据本发明,上述培养基进一步包括至少一种酵母提取物。
优选地,根据本发明,上述培养基进一步包括至少一种蛋提取物。
在所附的权利要求书中示出了根据本发明的培养基的其它实施方式。
本发明还涉及通过发酵来制造益生菌动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149的方法,该方法包括用于在根据本发明的培养基中培养该益生菌的至少一个步骤。
在所附的权利要求书中示出了根据本发明的方法的其它实施方式。
以非限制性方法并且参考下面所述的实施例,本发明的其它特征和优点从下面的说明中将变得明显。
这些实施例重复了在小鼠中获得的结果其包括从人血液中分离的免疫细胞中体外获得的结果。
尽管在下面的实施例1至实施例4中重复测试的结果是在小鼠中获得的,但是应理解在人类中也能获得类似的结果。
具体地,在本发明的范围内证明了上述菌株对哺乳动物,尤其是啮齿动物中的体重增加的特定效果。
实际上,益生菌动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149菌株的单独给药或与至少一种其它益生菌的联合给药,在超重(包括胰岛素抗性)的哺乳动物,尤其是啮齿动物中的诱导了体重增加的降低以及炎性和代谢参数的改善。
具体地,在本发明的范围内证明了,基于根据本发明的益生菌菌株的组合物的代谢保护效果,该代谢保护效果还与脂肪组织内的PPARγ的表达和细胞重建的恢复,以及对肝脂肪变性的防护效果的恢复相关。
基于根据本发明的菌株的组合物还能调整与脂肪酸运输相关的受体的表达,尤其能恢复与G蛋白(GPR41和GPR43)耦联的参与短链脂肪酸(SCFA)运输的受体,其中短链脂肪酸(SCFA)是在由营养物吸收所诱导的饱足机制中的重要作用因子。
实际上,证明了根据本发明的菌株对脂肪细胞的大小,以及对促炎性细胞因子和趋化因子(MCP-1、IL-6、TNF-α等)的产生的积极作用,其中一些是导致胰岛素抗性的直接原因。
观察到,根据本发明的菌株还能重建哺乳动物中的血脂谱以及葡萄糖的代谢,预防发展成与代谢综合征直接相关的疾病,如血脂异常(以及由此导致的II型糖尿病)和高血糖症的风险。
最后,证明了摄取根据本发明的益生菌菌株与阿克曼菌(Akkermansia)在肠道中的重新定殖之间的关系,其中阿克曼菌(Akkermansia)是因其在预防人类肥胖中的作用以及在超重或肥胖个体中大大降低而闻名的细菌。
附图说明
图1示出了小鼠中,在超重以及然后的肥胖发展过程中,Ls33对以下方面的作用:(A)体重增加(%)随时间的变化,(B)对葡萄糖(GT)的耐受性,(C)附睾脂肪组织(EWAT)的重(量),和(D)皮下脂肪组织(SCWAT)的重(量)。数据被表示为平均值(每组10至15只小鼠)±平均值标准误差(SEM)。**p<0.01;***p<0.001。*对应于在相同介入性治疗下,富含脂肪的饮食(HFD)与对照饮食(LFD)之间的对比(饮食效果的测量)。
图2示出了小鼠中,在超重以及然后的肥胖发展过程中,混合物(Mix)对以下方面的作用:(A)体重增加(%)随时间的变化,(B)食物的累积摄入(克/天/小鼠),(C)对胰岛素的耐受性(IT),和(D)GT。数据被表示为平均值(每组5至14只小鼠)±平均值标准误差(SEM)。**p<0.01;***p<0.001;#p<0.05;##p>0.01;###p<0.001。*对应于在相同介入性治疗下,HFD饮食与LFD饮食之间的对比(饮食效果的测量)。#对应于在相同的饮食下,Mix与磷酸盐缓冲液(PBS)之间的对比(根据本发明的益生菌或益生菌的混合物的效果的测量)。
图3示出了小鼠中,在超重以及然后的肥胖发展过程中,混合物(Mix)对以下方面的作用:(A)EWAT的重量(量),(B)SCWAT的重量(量),(C)血液中的瘦素的量(ng/ml),(D)血液中的脂联素的量(μg/ml),(E)EWAT的组织学(各实验组的代表性切片),和(F)EWAT中的脂肪细胞的大小分布。数据被表示为平均值(每组10至15只小鼠)±平均值标准误差(SEM)。**p<0.01;***p<0.001;#p<0.05;##p<0.01;###p<0.001。*对应于在相同介入性治疗下,HFD饮食与LFD饮食之间的对比(饮食效果的测量)。#对应于在相同的饮食下,Mix与PBS之间的对比(根据本发明的益生菌或益生菌的混合物的效果的测量)。
图4示出了小鼠中,在超重以及然后的肥胖发展过程中,混合物(Mix)对以下方面的作用:(A)EWAT的细胞组成(分析单核细胞/巨噬细胞的特定基因(F4/80、CD68、CD11b、CD11c)的表达,调节T淋巴细胞(FoxP3)和趋化因子MCP-1),(B)巨噬细胞在EWAT中的存在(对F4/80特异性的免疫荧光标记和按照积分密度[IntDen]进行量化),(C)EWAT的炎症(分析促炎性细胞因子Tnfα、IL-1a、IL-6和IL-17的基因的表达),和(D)PPAR伽马(PPARγ)在信使RNA(左,基因表达)和蛋白(中左,Western印记和量化[任意单位:A.U.])水平的表达。数据被表示为平均值(每组5至14只小鼠)±平均值标准误差(SEM)。**p<0.01;***p<0.001;##p<0.01;###p<0.001。*对应于在相同介入性治疗下,HFD饮食与LFD饮食之间的对比(饮食效果的测量)。#对应于在相同的饮食下,Mix与PBS之间的对比(益生菌或益生菌的混合物的效果的测量)。
图5示出了小鼠中,在超重以及然后的肥胖发展过程中,混合物(Mix)对以下方面的作用:(A)脂质代谢中必需的因子(分析基因FABP1、APO CII和CD36的表达),(B)短链脂肪酸的受体(SCFA),通过分析基因GPR41和GPR43的表达)。数据被表示为平均值(每组5至14只小鼠)±平均值标准误差(SEM)。**p<0.01;***p<0.001;##p<0.01;###p<0.001。*对应于在相同介入性治疗下,HFD(高脂肪饮食)与LFD(低脂肪饮食)之间的对比(饮食效果的测量)。#对应于在相同的饮食下,Mix与PBS之间的对比(益生菌或益生菌的混合物的效果的测量)。
图5(C)示出了在体外模拟肠道生态系统的模型(SHIME)中,在与益生菌混合物Mix孵育24h和48h之后,总SCFA的产生水平(左),以及乙酸盐、丁酸盐和丙酸盐的成比例的水平。***与时间0相比。
图6示出了小鼠中,在超重和肥胖发展过程中,混合物(Mix)对(A)肠道微生物区的组合物,尤其是对双歧杆菌(Bifidobacteria)和阿克曼菌(Akkermansia muciniphila)的种群的作用。(B)通过TGGE对5只小鼠(代表HFD-PBS组和HFD-Mix组)进行分析,确定在经Mix或未经Mix治疗的HFD小鼠中,检测到的双歧杆菌(Bifidobacterium)物种。标记物M1或M2对应于所指示菌株的混合物。*p<0.05;**p<0.01;#p<0.05;##p<0.01。*对应于使用相同介入性治疗,HFD饮食与LFD饮食之间的对比(饮食效果的测量)。#对应于在相同的饮食下,Mix与PBS之间的对比(根据本发明的益生菌或益生菌的混合物的效果的测量)。
图7示出了小鼠中,在超重以及然后的肥胖发展过程中,混合物(Mix)对以下方面的作用:(A)胰腺、肝脏和脾脏的重量(量),(B)脂滴的堆积(脂肪变性,参见代表各实验组的组织切片),和(C)炎症或在脂质代谢暗含的或应答于胰岛素的不同的标记物(分析基因mcp-1、IL-6、TNFα、IL-10、IL-17、srebp-1c、APOCII Fabp1和IRS2的表达)。数据被表示为平均值(每组5至14只小鼠)±平均值标准误差(SEM)。**p<0.01;***p<0.001;##p<0.01;###p<0.001;####p>0.0001。*对应于使用相同介入性治疗,HFD饮食与LFD饮食之间的对比(饮食效果的测量)。#对应于在相同的饮食下,Mix与PBS之间的对比(根据本发明的益生菌或益生菌的混合物的效果的测量)。
图8a和图8b示出了根据本发明的益生菌动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149随时间对体重增加的影响,这取决于该益生菌是否在根据本发明的培养基中培养(图8a)或不在根据本发明的培养基中培养(图8b)。LFD=低脂肪饮食;HFD=高脂肪饮食;HFD B.lactis=当该益生菌在谷胱甘肽(图8a)的存在下或没有谷胱甘肽(图b)的情况下进行培养时,与摄取根据本发明的组合物相关的高脂肪饮食。
具体实施方式
观察了下面的程序,用于收集在下面的实施例1~4中所讨论的体内结果。
体内程序
小鼠、细菌菌株和饮食
在实验开始时,对5周龄雄性小鼠C57BL/6J进行测试。
唾液乳杆菌(Lactobacillus L.salivarius)Ls33菌株由丹尼斯克(Danisco)(Madison,WI,USA)提供。
益生菌的混合物(在下面的实施例中被称为Mix)包括CFU(菌落形成单位)比率为1:1(总109CFU)的两种不同的菌株:鼠李糖乳杆菌(L.rhamnosus)LMG S-28148的菌株和动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149的菌株。给予小鼠的饮食被分成具有低脂肪含量的第一饮食(LFD:D12450B;脂肪含10%kcal)和具有高脂肪水平的第二饮食(HFD:D12492,脂肪含60%kcal)。上述饮食由Research Diet公司提供。
动物的治疗程序
每周连续持续5天,每只小鼠经口给予:在无菌水(H2O)中的30μL Ls33-109CFU(菌落形成单位或在口服组合物中存在的菌落形成单位的数目)(Ls33-H2O组);无菌水(H2O组);或,在磷酸盐缓冲液(PBS)中的益生菌的混合物(混合物组;5×108CFU/菌株)(混合物-PBS组或PBS组)。
在治疗一周之后,向经Ls33、水、混合物或PBS治疗的小鼠随机分配LFD饮食(n=5/组)或HFD饮食(n=15/组)。每周记录体重和食物摄取。
当处死动物时,收集血液、附睾白色脂肪组织(EWAT)和皮下白色脂肪组织(SCWAT)、肝脏、脾脏、小肠和胰腺。
测试对胰岛素和葡萄糖的耐受性
在分别进行12周和14周饮食之后,进行了葡萄糖耐受性(GTT)测试和胰岛素耐受性(ITT)测试。对动物禁食6小时时段,然后接受腹膜内(IP)给予葡萄糖(D-葡萄糖,1g/kg体重)(GTT)或胰岛素(0.75UI/kg体重)(ITT)。在注射葡萄糖(GTT)或胰岛素(ITT)之前,以及在注射了葡萄糖(GTT)或胰岛素(ITT)之后的不同时间,使用市场上可购买到的自动血糖仪(例如 performa)对从尾巴采集的血液样品,测量血液中的葡萄糖水平。
血液分析
使用市场上销售的ELISA试剂盒,测量瘦素、脂联素、MCP-1和胰岛素的血浆水平。使用市场可购买到的分析试剂盒(例如由英国的Cambridge开发的Abcam试剂盒),确定非酯化脂肪酸(NEFA)、甘油三酯、甘油、HDL胆固醇和LDL胆固醇的水平。
组织学分析和免疫组化分析
使肝脏和白色脂肪组织(EWAT)的样品处于4%的对聚甲醛溶液中,然后包埋在石蜡中,最后进行切片,并且放置在载玻片上,然后使用苏木素-伊红(H&E)进行染色。使用成像程序Image J(NIH image,国家生物技术信息中心(National Center for Biotechnology Information)),进行白色脂肪组织(EWAT)的形态学分析,其中每个切片至少10个视野(代表约100个脂肪细胞)。
分析基因的表达
(按照本领域技术人员已知的方法)提取肝脏和肠的白色脂肪组织的总RNA,然后进行逆转录(对于上述组织类别的每一种,使用1μg的量进行逆转录)。按照本领域技术人员已知的方法,进行定量实时PCR(聚合酶链式反应)(RT-qPCR)。
统计学分析
数据被表示为平均值±平均值标准误差(SEM)。使用克鲁斯卡尔-沃利斯(Kruskal Wallis)检验,然后使用惠曼(Mann-Whitney)U检验,来进行统计学分析。当p值小于0.05时,实验组之间的差异被认为在统计学上是显著的
观察了下面的程序,用于收集在实施例5和6中所讨论的体外结果。
体外程序
人类微生物生态系统的模拟装置–SHIME模型
按照本领域技术人员熟知的程序,将模拟人胃肠道的SHIME反应器设置在适当位置。
将Mix添加到反应器中,并且在厌氧气氛下,在37℃孵育t=0、t=24h和t=48h的时间点,测量短链脂肪酸产物(SCFA)。
评价动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149菌株对人类血细胞的抗炎性效果
将从四位健康供体获得的新鲜人类血液以1:1的比率稀释在PBS-Ca(GIBCO)中,沉积在聚蔗糖(Ficoll)(GIBCO)层上,并且在20℃在400G下离心30分钟。
在离心后,从血液中分离出外周血单个核细胞(PBMC),使用PBS-Ca悬浮在50ml的终体积中,然后在20℃在750G下离心10分钟进行冲洗,重复三次。然后,将PBMC重悬在补充有10%(v/v)灭活的小牛血清(在56℃孵育30分钟的血清)、1%(w/v)L-谷氨酰胺(GIBCO)和庆大霉素(30μg/ml)(GIBCO)的RPMI培养基(GIBCO)中。对PBMC进行计数,将它们的数目调节为2×106细胞/ml。将制备物分配(1ml)在24孔培养板中。
实施例1:Ls33与混合物
本实施例示出了Ls33对小鼠的超重和肥胖发展的影响。
图1示出了对于在Ls33或水和具有低脂肪水平(LFD)或高脂肪水平(HFD)的食物饮食中治疗15周,以下指示:
(A)体重增加随时间的变化,表示为相对于在d=0天测量的体重的百分比;
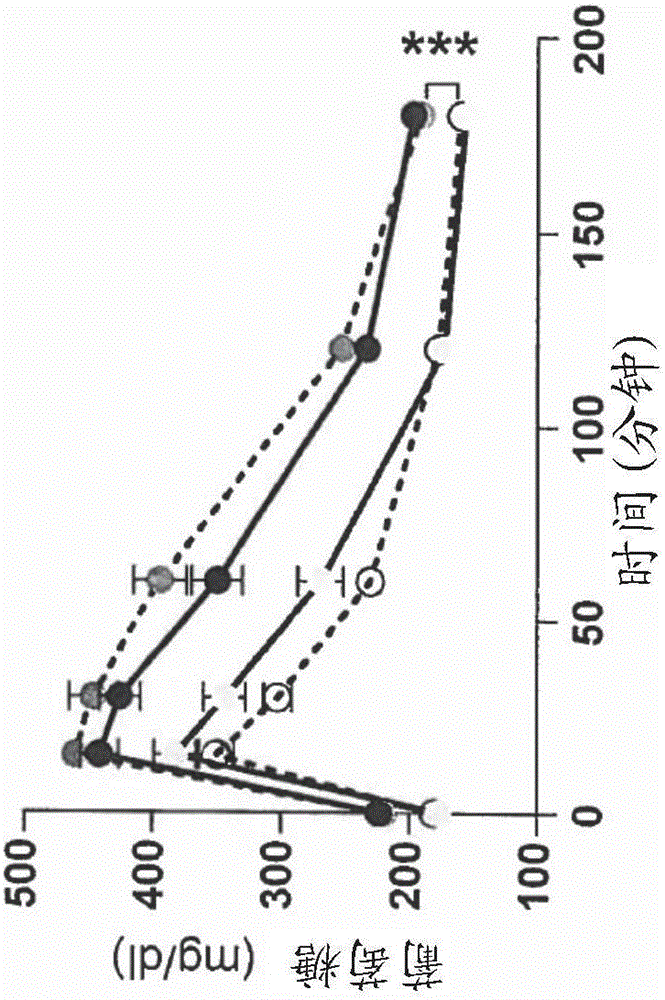
(B)在饮食12周之后进行的葡萄糖耐受性测试(GTT)。在6小时禁食时段之后、在图上指示的时间t(分钟)时、在腹膜内注射(IP)葡萄糖之后(对应于时间t=0),测量小鼠的葡萄糖水平(mg/dl)。
(C)在15周饮食(在处死过程中称重)之后,附睾脂肪组织(EWAT)的重量(量)(g);
(D)在15周饮食(在处死过程中称重)之后,皮下脂肪组织(SCWAT)的重量(量)(g)。
如该图所显示的结果,尽管在其它病理学模型中(即肠炎)证明了菌株Ls33具有体外抗炎性活性,但菌株Ls33没有示出对各指示A至D的任何(阳性或阴性)效果。
相反地,给予混合物Mix示出显著的保护效果。这些结果示于图2中。
该图示出在使用益生菌混合物(Mix)或PBS治疗,并且食用低脂肪水平(LFD)或高脂肪水平(HFD)的饮食17周之后的对应结果:
(A)体重增加随时间的变化(表示为相对于在d=0天测量的体重的百分比);
(B)每只小鼠每天的累积食物摄入(g/天/小鼠);
(C)在起始饮食后14周进行胰岛素耐受性测试(ITT):在腹膜内注射(IP)胰岛素之后测量血液中的葡萄糖水平。结果示出标准化水平(相对于注射前测量的葡萄糖水平的%)±SEM,和在注射胰岛素之后的各标准化葡萄糖水平的曲线下面积(AUC)的值的平均值±SEM;
(D)在饮食12周之后进行的葡萄糖耐受性测试(GTT)。测量IP注射葡萄糖之后的小鼠中的葡萄糖水平(mg/dl),并且计算AUC值。
与HFD-PBS组中获得的体重增加(113.51%±4.89%的增加)相比,在HFD-Mix小鼠组中观察到显著性较小的体重增加(80.97%±4.96%的增加)(参见图2A)。
如图2B所示,经益生菌混合物Mix治疗的HFD组的小鼠具有降低的累积食物摄入(食物摄入,FI)。有趣的是,对于体重增加和FI指数所观察到的有益效果在起始治疗之后(从第四周)快速显现出来。
如下面表1中较少的葡萄糖和胰岛素水平所示,给予Mix混合物改善了HFD组的葡萄糖的内稳态:
表1
该表的数据表示为平均值±平均值标准误差(SEM)(对应于每组5至14只小鼠)。*p<0.05;***p<0.001;#p<0.05;##p<0.01;###p<0.001。*对应于在相同介入性治疗下,HFD饮食与LFD饮食之间的对比(饮食效果的测量)。#对应于在相同的饮食下,Mix与PBS之间的对比(益生菌或益生菌的混合物的效果的测量)。
此外,如表1所示,如果Mix的效果维持局限于NEFA、甘油和甘油三酯的水平,则当它与总胆固醇水平的减少和HDL胆固醇减少相关时,证明了Mix具有降胆固醇作用。
进一步地,如通过胰岛素耐受性测试的结果所证明的(参见图2C),与对照组相比,HOMA-IR指数((禁食胰岛素/禁食葡萄糖水平)/22.5的水平)在HDF-Mix组的小鼠中显著降低(32.04±5.86比81.57±19.63;p<0.01),这表明胰岛素敏感性得到改善。
另外,经Mix治疗的小鼠对葡萄糖注射的耐受性更低(参见图2D)。
实施例2:Mix对白色脂肪组织的炎症的作用
图3示出了Mix对以下方面的效果:
(A)EWAT的重量(量)(g);
(B)SCWAT的重量(量)(g);
(C)如在提前禁食6小时的小鼠的血清中通过ELISA法(酶联免疫检验法)测量的,血液中的瘦素的量(ng/ml);
(D)如在提前禁食6小时的小鼠的血清中通过ELISA法测量的,血液中的脂联素的量(μg/ml);
(E)附睾白色脂肪组织的组织学(呈现了代表各实验组的经苏木精和伊红染色的切片)。比例尺为100μm。黑色箭头指示细胞浸润的存在;和
(F)EWAT中的脂肪细胞的大小分布。结果以每一大小等级的脂肪细胞的%表示(0~20μm,20~40等)。同时,图7示出Mix对以下方面的作用:
(A)胰腺、肝脏和脾脏的重量(量)(g);
(B)肝脏(呈现了代表各实验组的经H&E染色的切片)中的脂滴的堆积(即脂肪变性)。比例尺为100μm;和
(C)肝脏中,编码促炎性细胞因子和抗炎性细胞因子,以及参与脂质运输和代谢的受体的基因的表达。
与对照组HFD相比,HFD-Mix组的EWAT和SCWAT的脂肪量明显降低(参见图3A和图3B)。
另外,在HFD-Mix组的个体中,还观察到胰腺、肝脏和脾脏的重量(量)的明显降低(参见图7A)。
进一步地,尽管受控的HFD组小鼠发展成肝脂肪变性,但给予益生菌混合物Mix可以限制组织中的脂滴的存在(参见图7B)。
与白色脂肪组织质量的减少一致,证明血液瘦素水平显著低于HFD-Mix组中的血液瘦素水平(参见图3C),同时脂联素水平趋于较高(参见图3D)。
附睾脂肪组织的组织学示出,在HFD-Mix组的小鼠中具有较高密度的小脂肪细胞(参见图3E和图3F)。
应注意,如果在对照组的小鼠中,围绕脂肪细胞的细胞(由图3E中的箭头所示)明显浸润到脂肪组织中,则在接受了益生菌Mix的组的小鼠中采集的组织样品标记的这种浸润较少。
在肥胖发展过程中,巨噬细胞被招募到白色脂肪组织中,同时调节T细胞FoxP3+CD4+离开这些组织。
图4示出了在超重小鼠中,Mix对脂肪组织的炎症的作用。
如图4A所示,与对照组LFD相比,几种单核细胞/巨噬细胞的特异性标记物(F4/80、Cd68、Cd11b和Cd11c)的表达水平在HFD组小鼠中升高,同时与标记物Foxp3相关的水平降低。
给予益生菌混合物Mix显著降低了由HFD饮食诱导的单核细胞/巨噬细胞标记物的表达,并且使标记物Foxp3的表达水平升高。
Mix混合物,即根据本发明的益生菌菌株对巨噬细胞被招募到脂肪组织中的影响得到了图4B所示的结果的支持。
如Il6、Tnfα、Il-1α和Il-17的特异性信使RNA的表达水平降低(参见图4C)所证明的,根据巨噬细胞的招募降低,同时抗炎性Treg淋巴细胞积累增加,本实施例示出经Mix混合物治疗的小鼠中,附睾脂肪组织具有比对照组织低的炎性水平。
进一步地,示出了基于Mix混合物的治疗限制了HFD饮食诱导的PPARγ(在信使RNA水平和蛋白水平上)的降低(参见图4D)。
实施例3:Mix对小肠的脂质代谢和短链脂肪酸(SCFA)的产生的作用
本实施例中示出,负责短链脂肪酸(Short-Chain Fatty Acid,SCFA)运输的基因(GPR41和GPR43)的表达水平在进行HFD饮食的小鼠的小肠中降低,这表明在HFD组中,当后者较少被检出时,SCFA能够在较小程度上起积极作用,同时基因(GPR41和GPR43)在HFD饮食下在经Mix混合物治疗的动物中显著增加(参见图5B)
反过来,给予Mix具有限制在脂肪食物饮食诱导的脂质代谢中必需的基因增加的效果(参见图5A)。
实施例4:Mix对微生物区和阿克曼菌(Akkermansia muciniphila)的集落水平的作用
通过定量PCR(qPCR)对来自小鼠盲肠内容物的微生物区的特定细菌进行分析,其中小鼠在给予或没有给予Mix的同时食用HFD饮食,在另一方面小鼠在给予或没有给予Mix的同时食用LFD饮食。
图6中示出的结果示出了HFD-Mix小鼠的微生物区的组成的变化,特别是在食用HFD饮食且经根据本发明的益生菌菌株或益生菌混合物治疗的小鼠中阿克曼菌(Akkermansia muciniphila)集落的恢复。
实施例5:Mix对SFCA的产生的作用;SHIME模型的使用
在本实施例中,使用了体外模拟肠道的动态模型,旨于再现人类肠道的微生物生态系统。
如该模拟的结果所示(参见图5C),使用益生菌动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149菌株能在接种后48h时段内增加SFCA的产生,促进肠道中丁酸盐和丙酸盐的产生,其中丁酸盐和丙酸盐在人类中促进由营养物摄取所诱导的饱足的两种代谢物。在表2中重复了,在根据本发明的Mix混合物孵育之前(T0)和之后(T24h和T48h),与SHIME反应器相关联的升结肠中产生的丁酸盐和丙酸盐水平。这些数据表示为mmol/L±SED。
表2
证明在动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149菌株的培养基中的谷胱甘肽的重要性
图8a和图8b示出了根据本发明的益生菌动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149随时间对体重增加的影响,这取决于上述益生菌是否培养在(图8a)或没有培养在(图8b)根据本发明的培养基中。
如通过对比图8a和图8b所看到的,更具体地如通过HFD B.lactis曲线所看到的,当富含脂肪的食物饮食与摄入根据本发明的组合物相关联时,其中通过在含谷胱甘肽的培养基中培养来获得益生菌动物双歧杆菌亚种乳酸菌(Bifidobacterium animalis ssp.Lactis)编号LMG P-28149,观察到体重增加随时间显著降低(图8a);而当给予根据本发明的组合物,其中根据本发明的组合物包括在不含谷胱甘肽的培养基中培养获得的益生菌,则不是这种情况(图8b)。
很容易理解,本发明并不收到上述实施方式的限制,可以在不偏离所附权利要求的范围的情况下,对其进行很多改变。
缩写词列表
SCFA:短链脂肪酸
EWAT:附睾白色脂肪组织
GT(T):葡萄糖耐受性(测试)
HDL:高密度脂质
H&E:苏木精和伊红
HFD:富含脂肪的饮食
BMI:体重指数
(HOMA)-IR:用于估计胰岛素抗性的(稳态模型)
IT(T):胰岛素耐受性(测试)
(V)LDL:(极)低密度脂质
LFD:低脂肪饮食
NEFA:非酯化脂肪酸
PBS:磷酸盐缓冲液
PBMC:外周血单个核细胞
SCWAT:皮下白色脂肪组织
SEM:平均值标准误差
SHIME:人肠道微生物生态系统的模拟装置
WAT:白色脂肪组织
PCT/RO/134表
- 还没有人留言评论。精彩留言会获得点赞!