使用BRAF抑制剂的伤口愈合的制作方法
本申请要求于2014年5月6日提交的美国临时申请系列号61/989,398的优先权,其通过引用被并入本文。
政府利益的声明
本发明根据各自由美国国立卫生研究院(the National Institute of Health;NIH)授予的P01CA168585、CA-16042和AI-28697,在政府支持下做出。政府在本发明中具有一定权利。
领域
本公开内容涉及包含BRAF抑制剂的组合物和使用包含BRAF抑制剂的组合物治疗伤口的领域。
背景
丝氨酸/苏氨酸蛋白激酶B-Raf(“B-Raf”或“BRAF”)是信号转导蛋白激酶,其参与调节MAP激酶/ERK信号传导通路,影响细胞分化、分裂和分泌。BRAFV600E是常见的致癌BRAF突变,其通过丝裂原活化蛋白激酶(MAPK)通路诱导组成型信号传导,刺激癌细胞增殖和存活。阻断BRAF激酶的活性构象的致癌BRAF的抑制剂的临床开发,当与标准化学疗法相比时,已引起高比率的目标肿瘤反应和总存活率的改善。然而,非黑素瘤性皮肤癌(例如,高分化皮肤鳞状细胞癌和角化棘皮瘤)在约15%至30%的用BRAF抑制剂诸如维罗非尼(vemurafenib)和达拉菲尼(dabrafenib)(GSK-2118436)治疗的患者中发展。
针对细胞培养物、动物模型和人类中的BRAFV600E–突变细胞的BRAF抑制剂诸如维罗非尼的抗肿瘤活性,与致癌MAPK信号传导的抑制相关,如由磷酸化的ERK(pERK)的抑制证明的,所述磷酸化的ERK(pERK)是BRAF的下游效应物,其当被磷酸化时是有活性的。然而,BRAF抑制剂在具有野生型BRAF的细胞系中诱导相反的作用——即,增加pERK,所述具有野生型BRAF的细胞系具有上游通路的激活,诸如致癌RAS或上调的受体酪氨酸激酶。BRAF野生型细胞中MAPK信号传导的该RAF抑制剂依赖性激活称为“特殊MAPK通路激活(paradoxical MAPK-pathway acitvation)”,并且受到RAF二聚体的形成驱动,其通过CRAF和随后的MAPK通路超活化引起信号传导。通过诱导特殊(paradoxical)MAPK激活来抑制非癌环境中BRAF抑制剂的这些皮肤增殖性副作用以加速皮肤伤口愈合将是期望的。
概述
根据本文描述的实施方案,提供了用于治疗伤口的方法。此类方法包括使伤口与有效量的BRAF抑制剂接触来刺激伤口愈合的步骤。BRAF抑制剂可以是抑制BRAF的活性的任何合适的剂,除了其他剂以外包括:AMG542、ARQ197、ARQ736、AZ628、CEP-32496、GDC-0879、GSK1120212、GSK2118436(达拉菲尼(dabrafenib),)、LGX818(encorafenib)、NMS-P186、NMS-P349、NMS-P383、NMS-P396、NMS-P730、PLX3603(RO5212054)、PLX4032(维罗非尼(vemurafenib),)、PLX4720(二氟苯基-磺胺(Difluorophenyl-sulfonamine))、PF-04880594、PLX4734、RAF265(CHIR-265)、RO4987655、SB590885、索拉非尼(sorafenib)、索拉非尼甲苯磺酸盐和XL281(BMS-908662)。
在一些方面,BRAF抑制剂可以是药物组合物的部分。在此类情况中,药物组合物可包含有效量的BRAF抑制剂和药学上可接受的载体。在某些方面,药物组合物是局部用剂(topoical agent),包括软膏、乳状液体(cream liquid)、凝胶、水凝胶或喷雾。
此外,在一些实施方案中,BRAF抑制剂或其药物组合物可以是用于在治疗伤口中使用的伤口敷料的部分。在该情况中,伤口敷料可以用BRAF抑制剂或其药物组合物浸渍或涂覆。可以在根据本文描述的实施方案中使用的合适的伤口敷料包括藻酸盐敷料、抗微生物敷料、绷带、生物合成的敷料、生物敷料、胶原敷料、复合敷料(composite dressing)、压缩敷料(compression dressing)、接触层敷料、泡沫敷料、纱布敷料、水胶体敷料、水凝胶敷料、皮肤密封剂或液体皮肤敷料、专用吸收性敷料、透明薄膜式敷料或伤口填充物。
附图简述
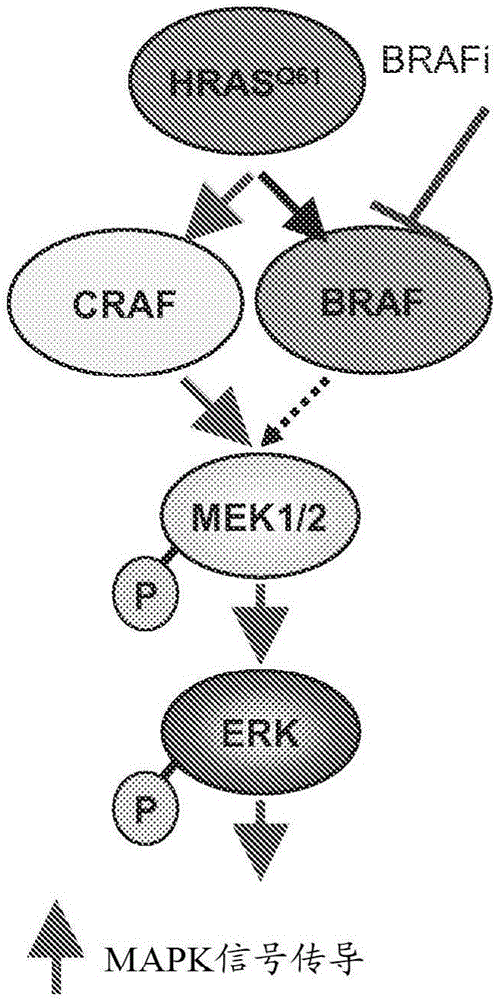
图1是图解了在BRAFV600E突变的黑素瘤中的BRAF抑制(图1A)、在发展HRAS突变来源的皮肤鳞状细胞癌和角化棘皮瘤(cuSCC/KAs)的黑素瘤患者中的BRAF野生型细胞中的BRAF抑制(图1B)和在健康受试者中的BRAF和RAS野生型细胞中的BRAF抑制(图1C)的差异作用的示意图。
图2图解了BRAF抑制在人类角化细胞中诱导特殊MAPK激活,引起增加的增殖。图2A是通过自动化显微镜分析仪进行的增殖和刮伤愈合作为在维罗非尼的存在或不存在下的HEKa的重复培养物中在不同时间点的细胞的相对伤口密度百分比的定量分析。通过t-检验的P值<0.0044。在图3A中显示了代表性图像。图2B显示了在0小时(基线)和24小时在维罗非尼的存在或不存在下人类成人上皮角化细胞(HEKa)的细胞增殖伤口愈合测定的代表性图像。图2C图解了在暴露于或未暴露于维罗非尼的软琼脂中生长的HEKa和M249细胞的集落定量的倍数变化展示。在图3B中显示了代表性图像。图2D显示暴露于或未暴露于维罗非尼的HEKa集落的平均斑点尺寸的增加。图2E显示具有和不具有维罗非尼和/或曲美替尼的HEKa集落的平均数目。图2F是与BRAFV600E突变的黑素瘤细胞系M249相比,HEKa中的pERK的蛋白印迹分析和Ki67的表达水平。图2G是当用维罗非尼、曲美替尼或维罗非尼和曲美替尼的组合处理时,与BRAFV600E突变的黑素瘤细胞系M249相比,HEKa细胞中的pERK和pMEK的蛋白印迹分析。图2H是用媒介物或VEM(2μM)处理并用pERK和Ki67染色的HEKa和M249细胞的磷酸化流式细胞术(phosphoflow cytometry)分析。左边显示HEKa和M249中单独的pERK和Ki67表达的直方图。pERK和Ki67的共表达水平显示在图的中部,且定量的和代表性的倍数变化显示在左边。
图3显示了图2中描述的实验的代表性结果。图3A显示了在维罗非尼的存在或不存在下人类成人上皮角化细胞(HEKa)的细胞增殖刮伤测定的时间进程图像。增殖的定量分析展现在图2A中。图3B显示了用DMSO或VEM处理的M249和HEKa的3D培养物图像。
图4显示了代表性磷酸化流式细胞术图像,显示产生图2H中展现的数据的门控策略。图4A显示M249细胞的磷酸化流式细胞术图像;图4B显示HEKa细胞的磷酸化流式细胞术图像。
图5图解了BRAF抑制加速了小鼠中的伤口愈合。图5A是根据一些实施方案在CH3小鼠中进行的伤口愈合测定的示意图。图5B显示在第2、6和14天,PBS治疗的和VEM治疗的小鼠的代表性图像。图5C显示了图解在三次重复实验中(媒介物(DMSO/生理盐水)和VEM;实验#1-3)和在使用维罗非尼(VEM)和/或曲美替尼(TRAME)以及DMSO/生理盐水作为媒介物/对照的单独的实验(实验#4)中的伤口牵张强度(WTS)的一组图,所述三次重复实验的每次实验具有8只小鼠/组。WTS展示为克力(gf)(对于所有三次实验通过t-检验的p<0.0001)。
图6是在治疗后第1天(D1)、第2天(D2)和第6天(D6)的伤口愈合的病理分析的示意图。图6A显示在维罗非尼(VEM)、曲美替尼(TRAME)或组合(VEM+TRAME)的存在和不存在下的代表性显微照片H&E图像(200X)。在每组中,切割的伤口的愈合包括相同的标准过程。伤口邻近的表皮经历增生和增殖,并且来自该过程的表皮细胞向中央迁移以封闭切割的表皮缺损。切口的空间最初被纤维蛋白填充,然后其被成纤维细胞、巨噬细胞、多形核细胞和新的毛细血管占据。在维罗非尼的存在下(图V1、V2、V6),愈合过程加速。相比于对照样本(图C2),在维罗非尼组(图V2)中在切割后第2天伤口邻近的表皮增生更广泛。皮肤表面完整性以表皮下纤维化开始在6天中重建(图V6),而此时,对照组中的再上皮化不完全并且不存在真皮修复性纤维化(图C6)。仅用曲美替尼治疗的组在第2天显示轻微的损伤周围的增生(图M2),并且到第6天未显示修复的迹象(图M6)。在维罗非尼加曲美替尼组合的组(图VM1、VM2、VM6)中,在第2天,损伤周围的增生(图VM2)低于用维罗非尼治疗的组(图V2),但高于单独的曲美替尼(图M2)。此外,在第6天不存在再上皮化(图VM6)。图6B显示在用媒介物、维罗非尼、曲美替尼或组合治疗后第1天、第2天和第6天,从伤口的右侧和左侧的表皮增生的长度的定量。每个条包括来自4个样品的数据。
图7显示在暴露于或未暴露于维罗非尼的小鼠中,愈合皮肤伤口的基因表达谱分析。上图显示BRAF特征基因的热图,和其使用基因集合变异分析(Gene Set Variation Analysis;GVSA)计算的总体富集得分;下图显示伤口愈合特征基因的热图和总体GVSA得分。
详述
本文提供了使用BRAF抑制剂用于治疗伤口的方法、药物组合物和伤口敷料。根据本文描述的实施方案,BRAF抑制剂可以单独地、作为药物组合物的部分、或作为伤口敷料的部分使用以加速伤口愈合。
目前,BRAF抑制剂被用于在诸如癌症的疾病和状况中利用其涉及BRAF的突变的形式的抗增殖活性(图1A)。然而,尽管BRAF抑制剂对BRAF的突变的形式的抗增殖效果,已观察到,用BRAF抑制剂治疗癌症诸如黑素瘤的患者发展二次增殖性状况。
特殊MAPK激活是用BRAF抑制剂治疗的患者中这些二次增殖性状况(例如,浸润性鳞状细胞癌和角化棘皮瘤)的发展背后的致病基础(Su等2012;Oberholzer等2012)。在这些二次皮肤损伤中的非突变的BRAF上游的RAS突变的频繁存在导致强烈的RAS-GTP激活,其引起ERK的特殊地增加的磷酸化、增加的MAPK通路输出和增强的细胞增殖(图1B)。特殊MAPK激活是RAF抑制剂的特性(Hall-Jackson等1999),其中与BRAF启动子的优先结合在强烈的上游RAS-GTP信号传导的环境中引起其CRAF异二聚体配偶体的反式激活(Heidorn等2010;Poulikakos等2010;Holderfield等2013)。因此,经BRAF抑制剂治疗的患有BRAF突变的转移性黑素瘤的患者发展多种其他皮肤增殖性状况(Belum等2013),其中的大多数当伴随施用MEK抑制剂时被改善(Flaherty等2012),所述MEK抑制剂阻断特殊RAF激活的下游作用(Su等2012;Escuin-Ordinas等2013)。在下面的实施例中,表明在癌症治疗中BRAF抑制剂的皮肤增殖性副作用的该机制理解可以在另外的健康受试者(即,野生型(wt)RAS和BRAF)中被利用以通过在野生型细胞中诱导特殊MAPK激活加速皮肤伤口愈合(图1C)。
BRAF抑制剂
可根据本文描述的实施方案使用的BRAF抑制剂可以包括选择性地抑制野生型BRAF或BRAF的突变形式(例如,BRAFV600E、BRAFV600K、BRAFV600D、BRAFV600L、BRAFV600R)的至少一部分生物活性(例如,信号转导活性)的任何剂。在一些方面,BRAF抑制剂可以是单独的BRAF选择性的,或可以具有针对在RAF/MEK/ERK通路中的一种或更多种另外的靶的抑制活性。例如在一方面,BRAF抑制剂可以是RAF激酶抑制剂,即,抑制剂可以具有针对除了BRAF之外的RAF激酶诸如ARAF、CRAF或二者的抑制活性。在某些实施方案中,选择BRAF抑制剂以具有增加的特殊MAPK激活活性。如此,根据本文描述的实施方案使用的BRAF抑制剂可以充当MAPK特殊激活物,意味着,BRAF抑制剂引起MAPK信号传导的增加。在一些方面,MAPK特殊激活物是当靶BRAF激酶是野生型BRAF激酶时呈现增加的MAPK信号传导的BRAF抑制剂。
本领域已描述了若干BRAF激酶抑制剂,其中的任何一个可以适合用于在本文描述的方法、敷料和组合物中使用。合适的BRAF抑制剂可包括但不限于1,2-二-环基取代的炔化合物或衍生物;1-甲基-5-(2-(5-(三氟甲基)-1H-咪唑-2-基)吡啶-4-基氧基)-N-(4-(三氟甲基)苯基)-1H-苯并[d]咪唑-2-胺);2,6-二取代的喹唑啉、喹喔啉、喹啉和异喹啉化合物或衍生物;4-氨基-5-氧络-8-苯基-5H-吡啶并-[2,3-D]-嘧啶化合物或衍生物;4-氨基-噻吩并[3,2-C]吡啶-7-羧酸化合物或衍生物;5-(4-氨基苯基)-异喹啉化合物或衍生物;苯磺胺噻唑化合物或衍生物;苯并咪唑化合物或衍生物;双环化合物或衍生物;吡唑并[1,5-a]嘧啶化合物或衍生物的桥接、双环杂环或螺旋双环杂环衍生物;肉桂酰胺和氢-肉桂酰胺化合物或衍生物;二-取代的咪唑化合物或衍生物;稠合的三环吡唑并[1,5-a]嘧啶化合物或衍生物;杂芳基化合物或衍生物;杂环化合物或衍生物;1H-苯并[D]咪唑化合物或衍生物;咪唑并[4,5-B]吡啶化合物或衍生物;N-(6-氨基吡啶-3-基)-3-(亚磺酰氨基)苯甲酰胺化合物或衍生物;N-[3-(1-氨基-5,6,7,8-四氢-2,4,4B-三氮杂芴-9-基)-苯基]苯甲酰胺化合物或衍生物;含氮的双环杂芳基化合物或衍生物;杂环取代的二芳基脲化合物或衍生物的N-氧化物;omega-羧基芳基取代的二苯基脲化合物或衍生物;噁唑化合物或衍生物;苯乙胺化合物或衍生物;苯基磺酰胺取代的、吡唑并[1,5-a]嘧啶化合物或衍生物;苯基三唑化合物或衍生物;杂环化合物或衍生物;1h-吡唑并[3,4-b]吡啶化合物或衍生物;嘌呤化合物或衍生物;吡唑[3,4-B]吡啶化合物或衍生物;吡唑化合物或衍生物;吡唑啉化合物或衍生物;吡唑并[3,4-b]吡啶、吡咯并[2,3-b]吡啶化合物或衍生物;吡唑并[3,4-d]嘧啶化合物或衍生物;吡唑并[5,1-c][1,2,4]三嗪化合物或衍生物;吡唑基化合物或衍生物;嘧啶化合物或衍生物;吡咯化合物或衍生物;吡咯并[2,3-B]吡啶化合物或衍生物;取代的6-苯基-吡啶并[2,3-D]嘧啶-7-酮化合物或衍生物;取代的氮茚化合物或衍生物;取代的苯并咪唑化合物或衍生物;取代的二芳基-脲化合物或衍生物;噻吩并吡啶化合物或衍生物;噻吩并嘧啶、噻吩并吡啶或吡咯并嘧啶化合物或衍生物;噻吩酰胺化合物或衍生物、和任何其他合适的芳基和/或杂芳基化合物或衍生物。在一些方面,本文描述的合适的BRAF抑制剂可以包括化合物或衍生物本身,或可以是其药学上可接受的盐或溶剂化物。
若干专利和专利申请公开了可根据本文描述的实施方案使用的范例BRAF抑制剂,包括但不限于国际专利申请公布号WO2011117381、WO2011119894、WO2011117381、WO2011097594、WO2011097526、WO2011085269、WO2011090738、WO2011025968、WO2011025927、WO2011023773、WO2011028540、WO2010111527、WO2010104973、WO2010100127、WO2010078408、WO2010065893、WO2010032986、WO2009115572、WO2009108838、WO2009111277、WO2009111278、WO2009111279、WO2009111280、WO2009108827、WO2009111260、WO2009100536、WO2009059272、WO2009039387、WO2009021869、WO2009006404、WO2009006389、WO2008140850、WO2008079277、WO2008055842、WO2008034008、WO2008115263、WO2008030448、WO2008028141、WO2007123892、WO2007115670、WO2007090141、WO2007076092、WO2007067444、WO2007056625、WO2007031428、WO2007027855、WO2007002433、WO2007002325、WO2006125101、WO2006124874、WO2006124780、WO2006102079、WO2006108482、WO2006105844、WO2006084015、WO2006076706、WO2006050800、WO2006040569、WO2005112932、WO2005075425、WO2005049603、WO2005037285、WO2005037273、WO2005032548;和美国专利号US8642759、US8557830、US8504758、US7863288、US7491829、US7482367和US7235576;其所有的说明书在此通过引用被并入,如同在本文充分陈述。
在某些实施方案中,BRAF抑制剂可以从选自以下的一组分子中选择:AMG542、ARQ197、ARQ736、AZ628、CEP-32496、GDC-0879、GSK1120212、GSK2118436(达拉菲尼,)、LGX818(encorafenib)、NMS-P186、NMS-P349、NMS-P383、NMS-P396、NMS-P730、PLX3603(RO5212054)、PLX4032(维罗非尼,)、PLX4720(二氟苯基-磺胺)、PF-04880594、PLX4734、RAF265(CHIR-265)、RO4987655、SB590885、索拉非尼、索拉非尼甲苯磺酸盐或XL281(BMS-908662)。
在一些实施方案中,BRAF抑制剂具有式(I)或式(II)的结构或其药学上可接受的盐:
其中:
R1是H、任选地用氰基取代的C3-C6环烷基、任选地用氰基取代的C1-C3烷基、-C(O)NH2、羟基、-X1NHC(O)OR1a、-X1NHC(O)NHR1a,其中X1是任选地用1至3个基团取代的C1-C4亚烃基,所述基团的每个独立地选自卤素、C1-C4烷基或卤素取代的C1-C4烷基,并且R1a是H、C1-C4烷基或卤素取代的C1-C4烷基;
R1b是H或甲基;
R2是H或卤素;
R3是H、卤素、C1-C4烷氧基、C1-C4烷基、卤素取代的C1-C4烷氧基、或卤素取代的C1-C4烷基;
R4是卤素、H或C1-C4烷基;
R5是C1-C6烷基、C3-C6环烷基、C3-C8支链烷基、卤素取代的C1-C6烷基、卤素取代的C3-C8支链烷基、C3-C6环烷基-(C1-C3)-亚烃基、或苯基,其中所述苯基任选地用1至3个取代基取代,所述取代基的每个独立地选自卤素、CH3或CF3;
R6是H、C1-C4烷基或卤素;并且
R7是H、C1-C6烷基、C3-C6环烷基、1-甲基-(C3-C6)-环烷基、1-(卤素取代的-甲基)-(C3-C6)-环烷基、C3-C8支链烷基、卤素取代的C1-C6烷基、卤素取代的C3-C8支链烷基、或苯基,其中所述苯基任选地用1至3个取代基取代,所述取代基选自卤素、C1-C4烷基或卤素取代的C1-C4烷基,优选地其中R7是H、C1-C6烷基、C3-C6环烷基、1-甲基-(C3-C6)-环烷基、C3-C8支链烷基或苯基,其中所述苯基任选地用1至3个取代基取代,所述取代基选自卤素、C1-C4烷基或卤素取代的C1-C4烷基。
在式(I)的化合物或其药学上可接受的盐的一个特定的实施方案中,R1是任选地用氰基取代的C1-C3烷基、-C(O)NH2、羟基、-X1NHC(O)OR1a,其中X1是任选地用1至3个基团取代的C1-C4亚烃基,所述基团的每个独立地选自卤素、C1-C4烷基或卤素取代的C1-C4烷基,并且R1a是H、C1-C4烷基或卤素取代的C1-C4烷基;
R2是H或卤素;
R3是H、卤素、C1-C4烷氧基、C1-C4烷基、卤素取代的C1-C4烷氧基、或卤素取代的C1-C4烷基;
R4是卤素、H或C1-C4烷基;
R5是C1-C6烷基、C3-C6环烷基、C3-C8支链烷基、卤素取代的C1-C6烷基或卤素取代的C3-C8支链烷基;
R6是H、C1-C4烷基或卤素;并且
R7是H、C1-C6烷基、C3-C6环烷基、1-甲基-(C3-C6)-环烷基、1-(卤素取代的-甲基)-(C3-C6)-环烷基、C3-C8支链烷基、卤素取代的C1-C6烷基、或卤素取代的C3-C8支链烷基、或苯基,其中所述苯基任选地用1至3个取代基取代,所述取代基选自卤素、C1-C4烷基或卤素取代的C1-C4烷基,优选地其中R7是H、C1-C6烷基、C3-C6环烷基、1-甲基-(C3-C6)-环烷基、或苯基,其中所述苯基任选地用1至3个取代基取代,所述取代基选自卤素、C1-C4烷基或卤素取代的C1-C4烷基。
在优选的实施方案中,提供了式(II)的化合物或其药学上可接受的盐(本文还被称作“LGX818”或“encorafenib”),其中
R1是–CH2-(S)-CH(CH3)NHC(O)OCH3;
R1b是H;
R2是H;
R3是Cl;
R4是H;
R5是CH3;
R6是F;并且
R7是异丙基。
在另一个实施方案中,提供了式(II)的化合物或其药学上可接受的盐,其中
R2是H或F;
R3是H、卤素、C1-C2烷氧基、C1-C2烷基、卤素取代的C1-C2烷氧基、或卤素取代的C1-C2烷基;
R4是H或甲基;
R5是C1-C4烷基、C3-C6环烷基、C3-C5支链烷基、卤素取代的C1-C4烷基、卤素取代的C3-C6支链烷基或C3-C6环烷基-(C1-C3)-亚烃基;
R6是H、C1-C2烷基或卤素;并且
R7是C3-C6环烷基、1-甲基-(C3-C6)-环烷基或C3-C6支链烷基。
在另一个实施方案中,提供了式(II)的化合物或其药学上可接受的盐,其中
R2是H;
R3是H、Cl、F、甲氧基、甲基或二氟甲氧基;
R4是H;
R5是甲基、环丙基、乙基、丙基、异丙基、仲丁基、异丁基、三氟甲基或3,3,3-三氟丙基;
R6是H、甲基、F或Cl;并且
R7是叔丁基、环丙基或1-甲基环丙基。
在一些实施方案中,BRAF抑制剂是式(III)的化合物或其药学上可接受的盐:
其中:
a为0、1、2或3;
每个R1是相同的或不同的,并且独立地选自卤素、烷基、卤代烷基、–OR6、–CO2R6、–NR6R7和–CN;
环A选自C3-C6环烷基、苯基、5-6元杂环和5-6元杂芳基,所述杂环和所述杂芳基每个具有1或2个选自N、O和S的杂原子;
Q1、Q2、Q3和Q4中的每个是CH、CR2或N,其中Q1、Q2、Q3和Q4中不超过一个是N;
每个R2是相同的或不同的,并且独立地选自卤素、烷基、卤代烷基和–OR6;
W选自–O–和–S–;
R3选自H、烷基、卤代烷基-、-亚烃基-OH、–NR5R7、–C3-C6环烷基、-亚烃基-C(O)-OH、-亚烃基-NH2和Het;
其中当R3是C3-C6环烷基时,所述C3-C6环烷基任选地用1或2个取代基取代,所述取代基是相同的或不同的,并且独立地选自卤素、C1-C3烷基、卤代-(C1-C3)-烷基、OH、O-(C1-C3)-烷基、氧络、S-(C1-C3)-烷基)、SO2、NH2、N(H)(C1-C3)-烷基和N(C1-C3烷基)2;
Het是具有1或2个选自N、O和S的杂原子的5-6元杂环,并且任选地用1或2个取代基取代,所述取代基是相同的或不同的,并且每个独立地选自卤素、C1-C3烷基、卤代-(C1-C3)-烷基、O-(C1-C3)-烷基、C1-C3亚烃基-O-(C1-C3)-烷基、OH、C1-C3亚烃基-OH、氧络、SO2((C1-C3)-烷基)、C1-C3亚烃基-SO2((C1-C3)-烷基)、NH2、N(H)((C1-C3)-烷基)、N(C1-C3烷基)2、CN和–CH2CN;
R4选自H、烷基、卤代烷基、烯基、–OR6、–R5-OR6、–R5-CO2R6、–R5-SO2R6、–R5-Het、–R5-C(O)-Het、–N(H)R8、–N(CH3)R8和–R5-NR6R7;每个R5是相同的或不同的,并且独立地是C1-C4亚烃基;
每个R6和每个R7是相同的或不同的,并且独立地选自H、烷基、卤代烷基、–OR6–C(O)-烷基和–C(O)-环烷基;
R8选自H、烷基(任选地被–OH取代)、卤代烷基、C3-C6环烷基、–R5-(C3-C6)-环烷基、Het2、–R5-Het2、–R5-OR6、–R5-O-R5-OR6、–R5-C(O)2R6、–R5-C(O)NR6R7、–R5-N(H)C(O)-R6、–R5-N(H)C(O)-R5-OR6、–R5-N(H)C(O)2-R5-R5-NR5R7、–R5-S(O)2R6、–R5-CN和–R5-N(H)S(O)2R6;
其中当R8是C3-C6环烷基时,所述C3-C6环烷基任选地用1或2个取代基取代,所述取代基是相同的或不同的,并且独立地选自卤素、C1-C3烷基、卤素-(C1-C3)-烷基、OH、O-(C1-C3)-烷基、氧络、S-(C1-C3)-烷基、SO2(C1-C3烷基)、NH2、N(H)-(C1-C3)-烷基和N(C1-C3烷基)2、和N(H)SO2-(C1-C3)-烷基;并且
Het2是具有1或2个选自N、O和S的杂原子的4-6元杂环,并且任选地用1、2、3、4或5个C1-C3烷基或1或2个取代基取代,所述取代基是相同的或不同的,并且每个独立地选自卤素、C1-C3烷基、卤代-(C1-C3)-烷基、O-(C1-C3)-烷基、C1-C3亚烃基-O-(C1-C3烷基)、OH、C1-C3亚烃基-OH、氧络、SO2(C1-C3烷基)、C1-C3亚烃基-SO2(C1-C3烷基)、NH2、N(H)-(C1-C3烷基)、N(C1-C3烷基)2、N(H)SO2-(C1-C3烷基)、C(O)(C1-C3烷基)、CO2(C1-C4烷基)、CN和–CH2CN;
并且R9和R10独立地选自H和烷基。
在优选的实施方案中,提供了式(III)的化合物或其药学上可接受的盐,其中
a是2;
R1是F;
每个R2是F;
R3是叔丁基;
R4是N(H)R8;
R8是H;并且
W是S(在本文称为“GSK2118436”、“达拉菲尼”或)。
在某些实施方案中,BRAF抑制剂是式(IV)的化合物:
其中:
R2、R4、R5和R6独立地选自由以下组成的组:氢、卤素、任选地取代的低级烷基、任选地取代的低级烯基、任选地取代的低级炔基、任选地取代的环烷基、任选地取代的杂环烷基、任选地取代的芳基、任选地取代的杂芳基、-CN、-NO2、-CRaRbR26和-LR26;
R3选自由以下组成的组:氢、卤素,任选地取代的低级烷基、任选地取代的低级烯基、任选地取代的低级炔基、任选地取代的环烷基、任选地取代的杂环烷基、任选地取代的芳基、任选地取代的杂芳基、-CN、-NO2、-CRaRbR26、-LR26和-A-Ar-L1-R24;
A选自由以下组成的组:-O-、-S-、-CRaRb-、-NR1-、-C(O)-、-C(S)-、-S(O)-和-S(O)2-;
R1选自由以下组成的组:氢、低级烷基、环烷基、杂环烷基、芳基、杂芳基、-C(O)R7、-C(S)R7、-S(O)2R7、-C(O)NHR7、-C(S)NHR7和-S(O)2NHR7,其中低级烷基任选地用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:氟、-OH、-NH2、低级烷氧基、低级烷硫基、单烷氨基、二烷氨基和-NR8R9,其中低级烷氧基、低级烷硫基、单烷氨基或二烷氨基的烷基链任选地用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:氟、-OH、-NH2、低级烷氧基、氟取代的低级烷氧基、低级烷硫基、氟取代的低级烷硫基、单烷氨基、二烷氨基和环烷氨基,然而,条件是,结合到烷氧基的O、硫代烷基的S或单或二烷氨基的N的烷基链碳的任何取代是氟,然而,另外条件是,当R1是低级烷基时,结合到-NR1-的N的低级烷基碳上的任何取代是氟,并且其中环烷基、杂环烷基、芳基或杂芳基任选地用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:卤素、-OH、-NH2、低级烷基、氟取代的低级烷基、低级烷氧基、氟取代的低级烷氧基、低级烷硫基、氟取代的低级烷硫基、单烷氨基、二烷氨基和环烷氨基;R7选自由以下组成的组:低级烷基、环烷基、杂环烷基、芳基和杂芳基,其中低级烷基任选用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:氟、-OH、-NH2、低级烷氧基、低级烷基硫、单烷氨基、二烷氨基和-KR8R9,然而,条件是,结合到-C(O)NHR7、-C(S)NHR7或-S(O)2NHR7的N的烷基碳的任何取代是氟,其中低级烷氧基、低级烷硫基、单烷氨基或二烷氨基的烷基链任选地用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:氟、-OH、-NH2、低级烷氧基、氟取代的低级烷氧基、低级烷硫基、氟取代的低级烷硫基、单烷氨基、二烷氨基和环烷氨基,然而,条件是,结合到烷氧基的O、硫代烷基的S或单或二烷氨基的N的烷基链碳的任何取代是氟,并且其中环烷基、杂环烷基、芳基和杂芳基任选地用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:卤素、-OH、-NH2、低级烷基、氟取代的低级烷基、低级烷氧基、氟取代的低级烷氧基、低级烷硫基、氟取代的低级烷硫基、单烷氨基、二烷氨基和环烷氨基;
Ar选自由任选地取代的亚芳基和任选地取代的杂亚芳基组成的组;
在每次出现时,L独立地选自由以下组成的组:-(alk)a-S-(alk)b-、-(alk)a-O-(alk)b-、-(alk)a-NR25-(alk)b-、-(alk)a~C(O)-(alk)b-、-(alk)a-C(S)-(alk)b-、-(aUc)a-S(O)-(alk)b-、-(alk)a-S(O)2-(alk)b-、-(alk)a-OC(O)-(alk)b-、-(alk)a-C(O)O-(alk)b-、-(alk)a-OC(S)-(alk)b-、-(alk)a-C(S)O-(alk)b-、-(alk)a-C(O)NR25-(alk)b-、-(alk)a-C(S)NR25-(alk)b-、-(alk)a-S(O)2NR25-(alk)b-、-(alk)a-NR25C(O)-(alk)b-、-(alk)a-NR25C(S)-(alk)b-、-(alk)a-NR25S(O)2-(alk)b-、-(alk)a-NR25C(O)O-(alk)b-、-(alk)a-NR25C(S)O-(alk)b-、-(alk)a-OC(O)NR25-(alk)b-、-(alk)a-OC(S)NR25-(alk)b-、-(alk)a-NR25C(O)NR25-(alk)b-、-(alk)a-NR25C(S)NR25-(alk)b-和-(alk)a-NR25S(O)2NR25-(alk)b-;a和b独立地是0或1;alk是C1-C3亚烃基或用一个或更多个取代基取代的C1-C3亚烃基,所述一个或更多个取代基选自由以下组成的组:氟、-OH、-NH2、低级烷基、低级烷氧基、低级烷硫基、单烷氨基、二烷氨基和-NR8R9,其中低级烷基或低级烷氧基、低级烷硫基、单烷氨基或二烷氨基的烷基链任选地用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:氟、-OH、-NH2、低级烷氧基、氟取代的低级烷氧基、低级烷硫基、氟取代的低级烷硫基、单烷氨基、二烷氨基和环烷氨基,然而,条件是,与烷氧基的O、烷硫基的S或单或二烷氨基的N结合的烷基链碳的任何取代是氟;
L1是-(CRaRb)v-或L,其中v是1、2或3;其中在每次出现时Ra和Rb独立地选自由以下组成的组:氢、氟、-OH、-NH2、低级烷基、低级烷氧基、低级烷硫基、单烷氨基、二烷氨基和-NR8R9,其中低级烷基、低级烷氧基、低级烷硫基、单烷氨基或二烷氨基的烷基链任选地用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:氟、-OH、-NH2、低级烷氧基、氟取代的低级烷氧基、低级烷硫基、氟取代的低级烷硫基、单烷氨基、二烷氨基和环烷氨基,然而,条件是,结合到烷氧基的O、硫代烷基的S或单或二烷氨基的N的烷基链碳的任何取代是氟;或在相同或不同碳上的Ra和Rb中的任何两个组合以形成3-7元单环环烷基或5-7元单环杂环烷基,并且Ra和Rb的任何其他的独立地选自由以下组成的组:氢、氟、-OH、-NH2、低级烷基、低级烷氧基、低级烷硫基、单烷氨基、二烷氨基和-NR8R9,其中低级烷基、低级烷氧基、低级烷硫基、单烷氨基或二烷氨基的烷基链任选地用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:氟、-OH、-NH2、低级烷氧基、氟取代的低级烷氧基、低级烷硫基、氟取代的低级烷硫基、单烷氨基、二烷氨基和环烷氨基,然而,条件是,结合到烷氧基的O、硫代烷基的S或单或二烷氨基的N的烷基链碳的任何取代是氟,并且其中3-7元单环环烷基或5-7元单环杂环烷基任选地用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:卤素、-OH、-NH2、低级烷基、氟取代的低级烷基、低级烷氧基、氟取代的低级烷氧基、低级烷硫基、氟取代的低级烷硫基、单烷氨基、二烷氨基和环烷氨基;
R8和R9与其附接的N组合以形成5-7元杂环烷基,所述5-7元杂环烷基任选地用一个或更多个取代基取代,所述一个或更多个取代基选自由以下组成的组:氟、-OH、-NH2、低级烷基、氟取代的低级烷基、低级烷氧基、氟取代的低级烷氧基、低级烷硫基和氟取代的低级烷硫基;
在每次出现时R25独立地选自由以下组成的组:氢、任选地取代的低级烷基、任选地取代的环烷基、任选地取代的杂环烷基、任选地取代的芳基和任选地取代的杂芳基;和
在每次出现时R24和R26独立地选自由以下组成的组:氢,然而,条件是,氢不与L或Li的S(O)、S(O)2、C(O)或C(S)中的任何一个结合;任选地取代的低级烷基;任选地取代的低级烯基,然而,条件是,当R24或R26是任选地取代的低级烯基时,其烯烃碳不结合到L或L1的N、S、O、S(O)、S(O)2、C(O)或C(S);任选地取代的低级炔基,然而,条件是,当R24或R26是任选地取代的低级炔基时,其炔烃碳不结合到L或L1的N、S、O、S(O)、S(O)2、C(O)或C(S);任选地取代的环烷基;任选地取代的杂环烷基;任选地取代的芳基和任选地取代的杂芳基。
在优选的实施方案中,提供了式(III)的化合物或其药学上可接受的盐,其中:
R2是H;
R3是-A-Ar-L1-R24;
A是-C(O)-;
Ar是2,4-二氟苯基;
L1是-SO2-;
R4是H;
R5是4-氯苯基;
R6是H;
R24是正丙基(本文称为“PLX4032”、“维罗非尼”或)。
在其他实施方案中,本领域技术人员可使用体外、体内、计算机模拟或本领域已知的其他筛选方法产生或鉴定出新型BRAF抑制剂。例如,可以使用用于检测在MAPK信号传导级联中BRAF的下游分子(例如,MEK和/或ERK)的磷酸化的测定,从小分子、肽或核酸的训练集鉴定野生型BRAF的BRAF抑制剂。BRAF抑制剂可以发挥阻遏(suppress)或抑制(inhibit)BRAF表达和/或信号传导功能的作用,从而降低MEK和ERK的磷酸化。可以在此类实施方案中使用的若干磷酸化测定是可得的,包括但不限于激酶活性测定(例如,由R&DLife 销售的那些);用于与免疫测定诸如蛋白印迹、酶联免疫吸附测定(ELISA)、流式细胞术、免疫细胞化学、免疫组织化学一起使用的磷酸化特异性抗体;质谱、蛋白质组学和磷酸化-蛋白多重测定。在某些实施方案中,可以使用测量候选抑制剂激活MAPK通路的能力的筛选方法鉴定用于在本文描述的实施方案中使用的BRAF抑制剂。可以通过反式激活CRAF实现MAPK通路的这一激活。与用于在治疗癌症和与异常的BRAF表达相关的其他疾病中使用的典型的BRAF抑制剂筛选不同,以此方式鉴定的BRAF抑制剂(本文还被称作MAPK特殊激活物)可被使用以利用特殊MAPK激活通过诱导皮肤细胞的增加的增殖来加速皮肤伤口愈合。
如本文使用的,术语“药学上可接受的盐”意指本发明的化合物的对于在受试者中应用是安全并且有效的,并且具有所需的生物活性的那些盐。药学上可接受的盐包括存在于本发明的化合物中的酸或碱基团的盐。药学上可接受的盐包括但不限于氢氟酸盐、盐酸盐、氢溴酸盐、氢碘酸盐、硝酸盐、硫酸盐、硫酸氢盐、磷酸盐、酸性磷酸盐、异烟酸盐、醋酸盐、乳酸盐、水杨酸盐、柠檬酸盐、酒石酸盐、泛酸盐、酒石酸氢盐、抗坏血酸盐、琥珀酸盐、马来酸、龙胆酸盐、延胡索酸盐、葡糖酸盐、葡萄糖醛酸盐、糖酸盐、甲酸盐、苯甲酸盐、谷氨酸盐、甲磺酸盐、乙磺酸盐、苯磺酸盐、对-甲苯磺酸盐和双羟萘酸盐(即,1,11-亚甲基-二-(2-羟基-3-萘甲酸盐))、铝、钙、锂、镁、钾、钠、锌和二乙醇胺盐。本发明的某些化合物可以与多种氨基酸形成药学上可接受的盐。对于药学上可接受的盐的综述,参见Berge等,66J.Pharm.Sci.1-19(1977),其通过引用并入本文。
药物组合物
在一些实施方案中,以上描述的一种或更多种BRAF抑制剂可以是药物组合物的部分。在一些方面,药物组合物包括至少一种BRAF抑制剂和药学上可接受的载体。如本文使用的术语“药学上可接受的载体”意指参与将BRAF抑制剂从一个位置、体液、组织、器官(内部或外部)、或身体的部分携带或运输到另一位置、体液、组织、器官或身体的部分的药学上可接受的材料、组合物或媒介物,诸如液体或固体填充物、稀释剂、赋形剂、溶剂或封装材料。
在一些实施方案中,药物组合物包含药学上可接受的载体和与式(I)或式(II)或其药学上可接受的盐一致的BRAF抑制剂。在一些实施方案中,BRAF抑制剂是LGX818(encorafenib)或其盐或衍生物。
在一些实施方案中,药物组合物包含药学上可接受的载体和与式(III)或其药学上可接受的盐一致的BRAF抑制剂。在一些实施方案中,BRAF抑制剂是GSK2118436(达拉菲尼,)或其盐或衍生物。
在一些实施方案中,药物组合物包含药学上可接受的载体和与式(IV)或其药学上可接受的盐一致的BRAF抑制剂。在一些实施方案中,BRAF抑制剂是PLX4032(维罗非尼,)或其盐或衍生物。
从与制剂的其他成分例如BRAF抑制剂是相容的并且适合用于在与生物系统的组织或器官接触中使用而无过度的毒性、刺激、过敏反应、免疫原性或其他问题或并发症,与合理的效益/风险比相称的意义上而言,每种载体是“药学上可接受的”。
可以用作药学上可接受的载体的材料的一些实例包括:(1)糖,诸如乳糖、葡萄糖和蔗糖;(2)淀粉,诸如玉米淀粉和马铃薯淀粉;(3)纤维素和其衍生物,诸如羧甲基纤维素钠、乙基纤维素和醋酸纤维素;(4)粉末化的黄芪胶;(5)麦芽;(6)明胶;(7)滑石;(8)赋形剂,诸如可可脂和栓剂蜡;(9)油,诸如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;(10)乙二醇,诸如丙二醇;(11)多元醇,诸如甘油、山梨醇、甘露醇和聚乙二醇;(12)酯,诸如油酸乙酯和月桂酸乙酯;(13)琼脂;(14)缓冲剂,诸如氢氧化镁和氢氧化铝;(15)藻酸;(16)无热原的水;(17)等渗的生理盐水;(18)林格氏溶液;(19)醇,诸如乙醇和丙烷醇;(20)磷酸盐缓冲溶液;和(21)在药物制剂中采用的其他无毒相容的物质诸如丙酮。
药物组合物可根据需要包含药学上可接受的辅助物质以接近生理条件,所述药学上可接受的辅助物质诸如pH调节剂和缓冲剂、毒性调节剂等等,例如,乙酸钠、氯化钠、氯化钾、氯化钙、乳酸钠等等。另外,用于药物组合物的制剂还可包括润湿剂、着色剂、脱模剂(release agent)、包衣剂、芳香剂、防腐剂、抗氧化剂或其他辅助成分。
在一个实施方案中,药学上可接受的载体是水性载体,例如缓冲的生理盐水等等。在某些实施方案中,药学上可接受的载体是极性溶剂,例如丙酮和醇。在某些方面,药学上可接受的载体是合适的材料,所述合适的材料允许、促进或增强经皮、局部、雾化吸入、可吸入或任何其他合适的施用方式,诸如在下面详细描述的那些施用途径。
在这些制剂中的BRAF抑制剂的浓度可以广泛不同,并且将主要基于流体体积、粘度、体重等等,根据选择的特定施用方式和生物系统的需要被选择。通常,存在于药物组合物中的一种或更多种BRAF抑制剂的量将是将产生治疗效果的量。例如,在一些实施方案中,药物组合物中的一种或更多种BRAF抑制剂的重量/体积(w/v)或重量百分比(wt%)浓度可以是在约0.001%到100%、0.001%到90%、0.001%到80%、0.001%到70%、0.001%到60%、0.001%到50%、0.001%到40%、0.001%到30%、0.001%到20%、0.001%到10%、0.001%到1%、0.01%到100%、0.01%到90%、0.01%到80%、0.01%到70%、0.01%到60%、0.01%到50%、0.01%到40%、0.01%到30%、0.01%到20%、0.01%到10%、0.01%到1%、0.1%到100%、0.1%到90%、0.1%到80%、0.1%到70%、0.1%到60%、0.1%到50%、0.1%到40%、0.1%到30%、0.1%到20%、0.1%到10%、0.1%到1%、1%到100%、1%到90%、1%到80%、1%到70%、1%到60%、1%到50%、1%到40%、1%到30%、1%到20%、1%到10%、1%到5%、1%到4%、1%到3%、1%到2%、0.1%到0.9%、0.1%到0.8%、0.1%到0.7%、0.1%到0.6%、0.1%到0.5%、0.1%到0.4%、0.1%到0.3%、0.1%到0.2%、0.2%到1%、0.3%到1%、0.4%到1%、0.5%到1%、0.6%到1%、0.7%到1%、0.8%到1%或0.9%到1%之间。
在其他实施方案中,药物组合物中的一种或更多种BRAF抑制剂的浓度可以是约1nM、2nM、3nM、4nM、5nM、6nM、7nM、8nM、9nM、10nM、20nM、30nM、40nM、50nM、60nM、70nM、80nM、90nM、100nM、200nM、300nM、400nM、500nM、600nM、700nM、800nM、900nM、1μM、2μM、3μM、4μM、5μM、6μM、7μM、8μM、9μM、10μM、20μM、30μM、40μM、50μM、60μM、70μM、80μM、90μM、100μM、200μM、300μM、400μM、500μM、600μM、700μM、800μM、900μM、1mM、2mM、3mM、4mM、5mM、6mM、7mM、8mM、9mM、10mM、20mM、30mM、40mM、50mM、60mM、70mM、80mM、90mM、100mM、200mM、300mM、400mM、500mM、600mM、700mM、800mM、900mM或1M。在一些方面,BRAF抑制剂在受试者(例如,人类或其他哺乳动物)中产生治疗效果的浓度(摩尔浓度或wt%)可以从体外或体内数据、从细胞培养物和/或动物实验诸如以下实施例中描述的那些来推断。
在一些方面,药物组合物还包含至少一种另外的治疗剂。除了一种或更多种BRAF抑制剂之外,可以作为药物组合物的部分被包含的合适的治疗剂包括但不限于,伤口治疗剂诸如生长因子(例如,重组血小板来源的生长因子(PDGF;/贝卡普勒明凝胶))、基于鱼皮的MariGen Omega3组织再生技术、糖、抗酸药、维生素A、维生素D、抗微生物剂和防腐剂(例如,醋酸、酸化亚硝酸盐、acticoat 7、aquacel-Ag、抗微生物肽、杆菌肽、BCTP纳米乳剂、卡地姆碘、碘、西曲溴铵、氯己定、精油、flammacerium、FPQC、夫西地酸、庆大霉素、葡糖酸盐、六氯酚、蜂蜜、碘化合物、碘酊、脂质体碘、醋酸磺胺米隆、甲硝唑、莫匹罗星、莫匹罗星钙、硫酸新霉素、新孢霉素(neosporin)、硝基糠腙、制霉菌素、噬菌体疗法、木瓜、益生素、多粘菌素B、聚维酮碘、瑞他帕林、次氯酸钠、过氧化氢、银、silvercel、银羊膜、硝酸银、银敷料、银泡沫、磺胺嘧啶银、磺胺醋酰Na+和超氧水);和止痛剂诸如发红剂(例如,水杨酸盐、烟酸盐、辣椒素、辣椒提取物)、NSAID(例如,布洛芬、双氯芬酸、联苯乙酸、酮洛芬、吡罗昔康、萘普生、氟比洛芬)、氢化可的松、苯扎氯铵、苄达明、多磺酸粘多糖、水杨酰胺、苯酚、冷却喷雾、炉甘石和局部麻醉剂(例如,利多卡因、利诺卡因、丙胺卡因、苯佐卡因、普莫卡因、地布卡因)。
伤口敷料
本文描述的BRAF抑制剂和其药物组合物可以与一种或更多种伤口敷料组合或联合使用。在某些实施方案中,一种或更多种BRAF抑制剂或其药物组合物被用于浸渍或涂覆伤口敷料。任何伤口敷料,诸如下面描述的那些,可以用一种或更多种BRAF抑制剂或包含一种或更多种BRAF抑制剂的药物组合物来浸渍或涂覆。上文详细描述了此类药物组合物。
在一个实施方案中,用包含一种或更多种BRAF抑制剂的药物组合物浸渍或涂覆的伤口敷料可以作为单一的伤口愈合敷料或一组独立包装的伤口愈合敷料出售。在此类情况中,当应用于伤口时,在单一的敷料单元中一起供应的敷料和BRAF抑制剂不但起作用以赋予典型的敷料的伤口愈合特性(例如,停止出血、减轻疼痛、保护免受进一步伤害或损伤、保护免受感染),还行使增强和/或加速伤口愈合的功能。
若干合适的伤口敷料是已知的并且在本领域中被使用以促进伤口愈合、保护开放的伤口、提供疼痛缓解和防止感染和/或污染,其中的任何一个可以根据本文描述的实施方案使用。合适的伤口敷料的实例包括但不限于藻酸盐、抗微生物剂、绷带、生物合成制品、生物制品、胶原、复合敷料、压缩绷带、接触层、泡沫、纱布、水胶体、水凝胶、皮肤密封剂/液体皮肤敷料、专用吸收性敷料、透明薄膜式敷料、伤口填充物。在一些方面,可以在伤口上使用用一种或更多种BRAF抑制剂浸渍或涂覆的多于一种伤口敷料。在其他方面,伤口敷料可以与局部用软膏、凝胶、喷雾、糊剂、液体或其他制剂组合使用,其中的每一个可以包含一种或更多种BRAF抑制剂或其组合物。
根据一些实施方案,用单独的或作为药物组合物的部分的一种或更多种以上描述的BRAF抑制剂浸渍或涂覆伤口敷料。在某些方面中,可以用于浸渍或涂覆伤口敷料的一种或更多种BRAF抑制剂选自以下的一种或更多种:AMG542、ARQ197、ARQ736、AZ628、CEP-32496、GDC-0879、GSK1120212、GSK2118436(达拉菲尼,)、LGX818(encorafenib)、NMS-P186、NMS-P349、NMS-P383、NMS-P396、NMS-P730、PLX3603(RO5212054)、PLX4032(维罗非尼,)、PLX4720(二氟苯基-磺胺)、PF-04880594、PLX4734、RAF265(CHIR-265)、RO4987655、SB590885、索拉非尼、索拉非尼甲苯磺酸盐和XL281(BMS-908662)。浸渍的或涂覆的伤口敷料可以直接地应用到伤口,使得敷料向伤口提供一种或更多种BRAF抑制剂的治疗作用。
在一些实施方案中,伤口敷料用单独的或作为药物组合物的部分的与式(I)或式(II)或其药学上可接受的盐一致的BRAF抑制剂浸渍或涂覆。在一些实施方案中,BRAF抑制剂是LGX818(encorafenib)或其盐或衍生物。
在一些实施方案中,伤口敷料用单独的或作为药物组合物的部分的与式(III)或其药学上可接受的盐一致的BRAF抑制剂浸渍或涂覆。在一些实施方案中,BRAF抑制剂是GSK2118436(达拉菲尼,)或其盐或衍生物。
在一些实施方案中,伤口敷料用单独的或作为药物组合物的部分的与式(IV)或其药学上可接受的盐一致的BRAF抑制剂浸渍或涂覆。在一些实施方案中,BRAF抑制剂是PLX4032(维罗非尼,)或其盐或衍生物。
使用方法
在一些实施方案中,单独的或作为药物组合物的部分的以上描述的BRAF抑制剂可以在用于治疗受试者伤口的方法中使用。本文描述的此类方法可以用于治疗任何类型的伤口,包括但不限于急性非穿透性伤口(例如,擦伤、撕裂伤、挫伤)、急性穿透性伤口(例如,戳伤、表面切口、刮伤或撕裂伤、手术切口和伤口、枪伤)、热伤口(例如,烧伤、晒伤和冻伤)、溃疡(例如,慢性糖尿病性溃疡、压迫性溃疡/褥疮)、化学伤口、动物或昆虫咬伤和蜇伤、和电伤口。
用于治疗伤口的方法可以包括使伤口与有效量的一种或更多种BRAF抑制剂接触以加速伤口愈合的步骤。可以根据本文描述的方法使用的合适的BRAF抑制剂包括但不限于以上描述的那些。在某些方面中,一种或更多种BRAF抑制剂可以选自以下的一种或更多种:AMG542、ARQ197、ARQ736、AZ628、CEP-32496、GDC-0879、GSK1120212、GSK2118436(达拉菲尼,)、LGX818(encorafenib)、NMS-P186、NMS-P349、NMS-P383、NMS-P396、NMS-P730、PLX3603(RO5212054)、PLX4032(维罗非尼,)、PLX4720(二氟苯基-磺胺)、PF-04880594、PLX4734、RAF265(CHIR-265)、RO4987655、SB590885、索拉非尼、索拉非尼甲苯磺酸盐和XL281(BMS-908662)。
在一些实施方案中,可以根据本文描述的方法使用的BRAF抑制剂与式(I)或式(II)或其药学上可接受的盐一致。在一些实施方案中,BRAF抑制剂是LGX818(encorafenib)或其盐或衍生物。
在一些实施方案中,可以根据本文描述的方法使用的BRAF抑制剂与式(III)或其药学上可接受的盐一致。在一些实施方案中,BRAF抑制剂是GSK2118436(达拉菲尼,)或其盐或衍生物。
在一些实施方案中,可以根据本文描述的方法使用的BRAF抑制剂与式(IV)或其药学上可接受的盐一致。在一些实施方案中,BRAF抑制剂是PLX4032(维罗非尼,)或其盐或衍生物。
根据本文描述的方法,使伤口与一种或更多种BRAF抑制剂或其药物组合物接触可通过任何合适的递送或施用途径实现。为了治疗伤口,BRAF抑制剂或其药物组合物可通过本领域已知的任何施用途径递送或施用,包括但不限于,口服、经鼻、局部、雾化吸入、经粘膜、表皮、经皮、皮肤、眼、肺、皮下和/或吸入。取决于施用方法,药物组合物可以以多种单位剂型施用。例如,适合于经皮施用的单位剂型包括经浸渍的或涂覆的贴剂、绷带、纱布或本文描述的任何其他敷料。
根据一些实施方案,BRAF抑制剂或其药用组合物可以以适合每种施用途径的制剂或制品的形式给予受试者。可用于本发明的方法中的制剂可以包含一种或更多种BRAF抑制剂、一种或更多种用于其的药学上可接受的载体和任选地一种或更多种另外的治疗剂或成分。制剂可以呈单位剂型方便地呈现,并且可通过药学领域熟知的任何方法制备。取决于待被治疗的受试者和特定的施用方式,可以与载体材料组合以产生单一剂型的活性成分的量将不同。可以与载体材料组合以产生药学上有效剂量的BRAF抑制剂的量通常将是产生治疗效果的BRAF抑制剂的量。
在一些实施方案中,制剂可以适合于口服施用,以用于治疗口腔伤口或疮。在此类实施方案中,制剂可以呈固体剂型(例如,胶囊、扁囊剂、丸剂、片剂、锭剂(使用风味基础,通常是蔗糖和阿拉伯树胶或黄芪胶)、散剂、颗粒剂),或呈液体剂型(例如,作为在水性或非水性液体中的溶液或悬浮液、作为水包油或油包水液体乳剂或微乳剂、作为酏剂或糖浆、作为糖果锭剂(使用惰性基质,诸如明胶和甘油、或蔗糖和阿拉伯树胶)和/或作为漱口剂等等),每种含有预定量的BRAF抑制剂作为活性成分。
在用于口服施用的固体剂型(例如,胶囊、片剂、丸剂、糖衣丸、散剂、颗粒剂等等)中,BRAF抑制剂可以与一种或更多种药学上可接受的载体诸如柠檬酸钠或磷酸氢钙和/或以下的任何一种混合:1)填充物(filler)或填充剂(extender),诸如淀粉、乳糖、蔗糖、葡萄糖、甘露醇和/或硅酸;2)粘合剂,诸如,例如,羧甲基纤维素、藻酸盐、明胶、聚乙烯吡咯烷酮、蔗糖和/或阿拉伯树胶;3)保湿剂,诸如甘油;4)崩解剂,诸如琼脂-琼脂、碳酸钙、马铃薯或木薯淀粉、藻酸、某些硅酸盐和碳酸钠;5)溶液阻滞剂,诸如石蜡;6)吸收加速剂,诸如季铵化合物;7)润湿剂,诸如,例如,乙酰基醇和单硬脂酸甘油酯;8)吸收剂,诸如高岭土和膨润土;9)润滑剂,诸如滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、月桂基硫酸钠、以及其混合物;和10)着色剂。在胶囊、片剂和丸剂的情况下,药物组合物还可以包含缓冲剂。相似类型的固体组合物也可以被采用作为在使用诸如乳糖(lactose)或乳糖(milk sugar)以及高分子量聚乙二醇等等的赋形剂的软填充和硬填充的明胶胶囊中的填充物。
在液体剂型中,BRAF抑制剂可以与本领域中通常使用的惰性稀释剂混合,诸如,例如,水或其他溶剂、增溶剂和乳化剂,诸如乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苄醇、苯甲酸苄酯、丙二醇、1,3-丁二醇、油(特别地,棉籽油、花生油、玉米油、胚芽油、橄榄油、蓖麻油和芝麻油)、甘油、四氢糠醇、聚乙二醇和脱水山梨醇的脂肪酸酯、以及其混合物。除惰性稀释剂之外,口服组合物还可以包含佐剂,诸如润湿剂、乳化剂和助悬剂、甜味剂、调味剂、着色剂、香味剂和防腐剂。另外,悬浮液可以包含助悬剂,如例如乙氧基化异硬脂醇、聚氧乙烯山梨醇和脱水山梨醇酯、微晶纤维素、偏氢氧化铝(aluminum metahydroxide)、膨润土、琼脂-琼脂和黄芪胶、以及其混合物。
在一些实施方案中,用于BRAF抑制剂组合物的局部、经皮、表皮或皮肤施用的制剂包括散剂、喷雾、软膏、糊剂、乳霜、洗液、凝胶、溶液、贴剂、敷料和吸入剂。活性组分可以在无菌条件下与药学上可接受的载体、以及与可需要的任何防腐剂、缓冲液或推进剂混合。此类软膏、糊剂、乳霜和凝胶除了BRAF抑制剂组合物之外可以包含赋形剂,诸如动物和植物脂肪、油、蜡、石蜡、淀粉、黄芪胶、纤维素衍生物、聚乙二醇、硅酮、膨润土、硅酸、滑石和氧化锌或其混合物。散剂和喷雾除了BRAF抑制剂组合物之外可以包含赋形剂,诸如乳糖、滑石、硅酸、氢氧化铝、硅酸钙和聚酰胺粉末、或这些物质的混合物。喷雾可以另外含有通常的推进剂,诸如氯氟烃和挥发性的未被取代的烃,诸如丁烷和丙烷。
在某些方面,BRAF抑制剂或其药物组合物可以通过雾化吸入被施用。这通过制备含有BRAF抑制剂的水性气雾剂、脂质体制品或固体颗粒或粉末来实现。可以使用非水性(例如,氟碳化合物推进剂)悬浮液。也可以使用声波喷雾器。水性气雾剂通过将剂的水性溶液或悬浮液与常规的药学上可接受的载体和稳定剂配制在一起制成。载体和稳定剂随着特定化合物的需要而不同,但通常包括非离子型表面活性剂(吐温、普朗尼克或聚乙二醇)、无害的蛋白质如血清白蛋白、脱水山梨醇酯、油酸、卵磷脂、氨基酸(诸如甘氨酸)、缓冲液、盐、糖或糖醇。通常从等渗溶液制备气雾剂。
经皮贴剂或伤口敷料还可以用于将BRAF抑制剂或其药物组合物递送到伤口部位。在上文详细描述了可以使用的伤口敷料的实例。此类制剂可以通过将剂溶解或分散在适当的介质中制成。吸收促进剂还可以用于增加拟肽穿透皮肤的通量。此类通量的速率可通过提供速率控制膜或将拟肽分散在聚合物基质或凝胶中来控制。
在一些实施方案中,在治疗伤口的方法中使用的BRAF抑制剂或其药物组合物是伤口敷料的部分。在一些方面,这意味着,BRAF抑制剂或其药物组合物被用于涂覆或浸渍如上文描述的伤口敷料的全部或一部分。可以根据该实施方案使用的伤口敷料包括,藻酸盐敷料、抗微生物敷料、绷带、生物合成的敷料、生物敷料、胶原敷料、复合敷料、压缩敷料、接触层敷料、泡沫敷料、纱布敷料、水胶体敷料、水凝胶敷料、皮肤密封剂或液体皮肤敷料、专用吸收性敷料、透明薄膜式敷料或伤口填充物。
如本文使用的术语“有效量”指产生期望的效果的BRAF抑制剂的量。例如,细胞群体可以与有效量的BRAF抑制剂接触以研究其体外效果(例如,细胞培养物)或以产生期望的离体或体外治疗效果。有效量的BRAF抑制剂可以用于在受试者中产生治疗效果,诸如治疗靶状况、缓解与状况相关的症状或产生期望的生理作用。例如,BRAF抑制剂的有效量可以是刺激伤口愈合的量。在此类情况中,BRAF抑制剂的有效量是“治疗有效量”、“治疗有效浓度”或“治疗有效剂量”。精确的有效量或治疗有效量是在给定的受试者或细胞群体中在治疗功效方面将产生最有效结果的BRAF抑制剂的量。该量将取决于多种因素而不同,所述因素包括但不限于BRAF抑制剂的特征(包括活性、药代动力学、药效动力学和生物利用度)、受试者的生理状况(包括年龄、性别、伤口类型和状态、全身性状况、对给定剂量的反应和药物的类型)或细胞的生理状况、制剂中的药学上可接受的一种或更多种载体的性质、和施用途径。另外,取决于BRAF抑制剂是单独施用还是与化合物、药物、疗法或其他治疗方法或方式组合施用,有效量或治疗有效量可以不同。临床和药理学领域的技术人员通过常规实验将能够确定有效量或治疗有效量,也就是通过监测细胞或受试者对施用的BRAF抑制剂的反应并且相应地调整剂量将能够确定有效量或治疗有效量。对于另外的指导,参见Remington:The Science and Practice of Pharmacy,21st Edition,Univ.of Sciences in Philadelphia(USIP),Lippincott Williams&Wilkins,Philadelphia,PA,2005,其在此通过引用被并入,如同在本文充分陈述。
伤口的治疗“(treating)”或“治疗(treatment)”可以指使用任何剂或敷料以帮助治愈、保护、修复或恢复急性或慢性受伤的、损伤的或患病的组织的结构和功能;预防状况,减慢状况的发作或发展的速率,预防或降低发生继发于伤口的状况的风险,杀死存在于伤口部位的抗微生物感染,预防或延迟与伤口相关的疼痛和其他症状的发展,减少或终止与伤口相关的疼痛和其他症状,产生伤口的完全或部分消退,或其一些组合。
在一些实施方案中,如以上描述的BRAF抑制剂或其药物组合物可以与一种或更多种另外的治疗剂组合或联合施用或递送。BRAF抑制剂与治疗剂可一起叠加地或协同地作用。如本文使用的“组合”、“与……组合”或“与……联合”意指在治疗同一受试者的同一伤口的过程中,以任何顺序并且以任何次数的应用,使用两种或更多种剂、敷料、药物、治疗方案、治疗方式或其组合。这包括同时施用及以间隔多达若干天的时间上间隔的顺序的施用。两种或更多种剂、敷料、药物、治疗方案、治疗方式或其组合可以是单一应用或施用的部分,或可被分开应用或施用。例如,BRAF抑制剂可以作为药物组合物或制剂的成分被施用。该组合物或制剂可以包括作为单一局部用组合物被应用的一种或更多种另外的治疗剂,或可选地,该组合物可与含有一种或更多种另外的治疗剂的第二治疗组合物或制剂一起应用于伤口。当应用组合物或制剂后,可在局部用组合物上应用伤口敷料。在另一个实例中,BRAF抑制剂可单独地或作为药物组合物的部分被用于浸渍伤口敷料。组合治疗还可以包括多于一次施用剂、药物、治疗方案或治疗方式中的任何一种或更多种。此外,两种或更多种剂、敷料、药物、治疗方案、治疗方式或其组合的施用可通过同一或不同的施用途径进行。
可以与BRAF抑制剂和其药物组合物组合或联合施用或递送的合适的治疗剂可包括但不限于伤口治疗剂诸如生长因子(例如,重组血小板来源的生长因子(PDGF;/贝卡普勒明凝胶))、基于鱼皮的MariGen Omega3组织再生技术、糖、抗酸药、维生素A、维生素D、抗微生物剂和防腐剂(例如,醋酸、酸化亚硝酸盐、acticoat 7、aquacel-Ag、抗微生物肽、杆菌肽、BCTP纳米乳剂、卡地姆碘、碘、西曲溴铵、氯己定、精油、flammacerium、FPQC、夫西地酸、庆大霉素、葡糖酸盐、六氯酚、蜂蜜、碘化合物、碘酊、脂质体碘、醋酸磺胺米隆、甲硝唑、莫匹罗星、莫匹罗星钙、硫酸新霉素、新孢霉素、硝基糠腙、制霉菌素、噬菌体疗法、木瓜、益生素、多粘菌素B、聚维酮碘、瑞他帕林、次氯酸钠、过氧化氢、银、silvercel、银羊膜、硝酸银、银敷料、银泡沫、磺胺嘧啶银、磺胺醋酰Na+和超氧水);和止痛剂诸如发红剂(例如,水杨酸盐、烟酸盐、辣椒素、辣椒提取物)、NSAID(例如,布洛芬、双氯芬酸、联苯乙酸、酮洛芬、吡罗昔康、萘普生、氟比洛芬)、氢化可的松、苯扎氯铵、苄达明、多磺酸粘多糖、水杨酰胺、苯酚、冷却喷雾、炉甘石和局部麻醉剂(例如,利多卡因、利诺卡因、丙胺卡因、苯佐卡因、普莫卡因、地布卡因)。
以下实施例旨在说明本发明的多种实施方案。如此,讨论的特定实施方案不被解释为对本发明范围的限制。对于本领域技术人员将是明显的是可以做出多个等同物、变化和修改而不偏离发明的范围,并且应理解,此类等同的实施方案将被本文包括。例如,尽管下面的实施例针对的是用维罗非尼治疗进行的实验,本领域技术人员将理解,其他BRAF抑制剂可被用于代替维罗非尼以产生类似的结果。此外,本公开内容中引用的所有参考文献在此通过引用以其整体被并入,如同在本文充分陈述。
实施例
BRAF抑制剂对于治疗患有BRAFV600E突变的转移性黑素瘤的患者是高度有活性的,其主要副作用是一系列的皮肤增殖变化,从过度角化到浸润性鳞状细胞癌。这些副作用的致病基础是由MAPK通路的特殊激活介导的,其中BRAF抑制剂增加了为BRAF野生型的细胞中的MAPK通路信号传导。在下面的研究中利用了该现象以通过诱导增加的皮肤细胞增殖来加速皮肤伤口愈合。在刮伤测定中,BRAF抑制剂维罗非尼加速了人类角化细胞的增殖和迁移,这是由增加的ERK磷酸化和细胞周期进程介导的。在伤口愈合小鼠模型中,局部应用的维罗非尼通过特殊MAPK激活改善了愈合的伤口的牵张强度,如通过基因表达谱分析评价的。因此,局部用BRAF抑制剂可在加速皮肤伤口的愈合方面具有应用。
实施例1:BRAF抑制剂增强角化细胞的再生长以覆盖体外刮伤部位
使在96孔板中培养的人类成人上皮角化细胞(HEKa)经历刮伤测定,其中增殖的角化细胞应该再生长并且覆盖刮伤。将具有或不具有BRAF抑制剂维罗非尼的重复培养物放置在具有自动显微镜分析仪的培养箱中,并且随着时间的推移记录了原始刮伤中有核细胞的数目。维罗非尼的存在诱导了覆盖原始刮伤方面的统计学上显著的改善,这在研究开始后的6、8和12小时非常明显(图2A和图3A)。使用在每个孔的中部具有播种机闭锁装置(seeder stopper)的96孔板,在维罗非尼的存在下培养的HEKa的增殖优势也是明显的;用维罗非尼处理的增殖的角化细胞在24小时后覆盖孔的中部,而对照处理的孔在中部仍没有细胞(图2B)。通过将曲美替尼(一种MEK抑制剂)添加到用维罗非尼处理的培养物中抑制了增强的迁移(图2B;“TRAME”)。此外,三维软琼脂集落测定了暴露于维罗非尼后增殖的HEKa集落,而BRAFV600E突变的黑素瘤系M249具有集落的减少(图2C和图3B)。HEKa集落不但数目增加,而且其平均斑点尺寸也显著地增加(通过t-检验的p=0.007,图2D)。添加曲美替尼减小了由维罗非尼诱导的HEKa集落的数目和尺寸(图2E)。使用这些培养物,通过蛋白印迹(图2F-2G)和定量磷酸化流式细胞术(图2H和图4A-4B)分析了特殊MAPK激活和细胞增殖。通过这两种测定,维罗非尼在BRAFV600E突变的人类黑素瘤细胞系M249中诱导了预期降低的pERK和细胞周期停滞,而在HEKa细胞中则存在pERK和细胞周期进程的特殊增加(通过t-检验的p=0.0225)。
实施例2:BRAF抑制剂由于上皮细胞的特殊增殖增强皮肤伤口的愈合
在C3H小鼠中的受控制的伤口愈合测定中,诱导了2.5cm的背部皮肤伤口并且用媒介物对照(DMSO/生理盐水)或在媒介物中的2mM的维罗非尼的悬浮液(通过粉碎该剂的临床级丸剂获得)填充。在第0天用手术方法剪出皮肤伤口,并且追踪小鼠直到第14天(图5A-5B)。在这段时间,每隔一天分别向测试组中的24只小鼠或对照组中的24只小鼠局部应用维罗非尼悬浮液或媒介物对照,每只小鼠共七个剂量。在第14天,小鼠被安乐处死并且取下含有伤口的皮肤并且安装在20mm条状物中,每个条状物中一个横断面(horizontal)伤口样品。使用拉力计分析伤口牵张强度(WTS),所述拉力计拉伸条状物并且记录以克力(gf)计的WTS。在三次独立的重复实验中,用维罗非尼治疗的小鼠相比于生理盐水对照在WTS方面具有统计学上显著的改善(52.6%、32.9%和42.8%,通过t-检验的p<0.0001;图5C,实验#1-3)。在单独的皮肤伤口愈合测定中,通过用维罗非尼治疗的WTS方面的37%的改善(对比媒介物对照通过t-检验的p=0.01)通过添加1mg/kg的曲美替尼被部分地逆转(图5B;“TRAME”、“VEM+TRAME”)。对于这些伤口,相比于媒介物对照,WTS降低至29%(通过t-检验的p<0.0001;图5C,实验#4)。
伤口和其周围的区域由两名病理学家通过H&E染色在组织学上进行分析,并且在治疗后第1天、第2天和第6天测量在愈合的伤口两侧的表皮增生的程度(图6A和6B)。在切割后第1天,在维罗非尼的存在下伤口邻近的表皮炎症更广泛,强烈和快速的再上皮化在第2天起始。到第6天,在维罗非尼治疗的组中表面完整性被重建,而在用媒介物、曲美替尼或组合治疗的小鼠中未观察到真皮修复性纤维化的迹象。在曲美替尼或维罗非尼和曲美替尼治疗的小鼠中未观察到愈合或再上皮化的征象,并且伤口溃烂,尤其是仅用曲美替尼治疗的小鼠(图6A)。在第1天和第2天,来自维罗非尼组的皮肤倾向展示比其他治疗组覆盖更大距离的表皮增生(通过单因素ANOVA,分别地,p=0.0132和p=0.0338),而到第6天,维罗非尼组具有较少的表皮增生,与较快的伤口消退相一致(通过单因素ANOVA的p=0.0012;图4B)。到第6天,79%的对照伤口显示再上皮化,而100%的维罗非尼治疗的伤口完全再上皮化。在单独的曲美替尼中和维罗非尼与曲美替尼组合的组中未观察到再上皮化。
实施例3:BRAF抑制剂增强MAPK和伤口愈合通路输出
通过RNASeq分析从用维罗非尼或媒介物治疗的小鼠获得的皮肤样品的MAPK和伤口愈合通路输出中的变化。将MAPK的基因输出与公布的数据或与公布的皮肤伤口愈合基因特征比较,所述公布的数据关于通过使用BRAF抑制剂阻断突变的BRAFV600E下游的致癌MAPK信号传导被差异调节的转录本。如在图7中通过基因表达热图显示的,到第2天(“D2”),在维罗非尼治疗后的BRAF特征中存在略微增加,但在伤口愈合特征中几乎无变化。到第6天(“D6”),在维罗非尼治疗的样品中两种特征相比于其各自的对照被显著富集。在维罗非尼治疗的伤口中观察到BRAF和伤口愈合特征的更明显的降低,与较快愈合相一致。特征的基因集合变异分析(GSVA)富集得分显示相同的趋势。
总体地,在上文实施例1-3中描述的研究表明,通过BRAF抑制剂的特殊MAPK激活现象可以被利用以增强皮肤伤口愈合。这可以具有加速其中恶性肿瘤前期或恶性肿瘤不是临床问题的皮肤伤口诸如擦伤、手术切口和糖尿病性皮肤溃疡的愈合的用途。
参考文献
下面列出的参考文献、专利和公布的专利申请,及以上说明书中引用的所有参考文献在此通过引用以其整体被并入,如同在本文充分陈述。
V.R.Belum,A.Fischer,J.N.Choi,M.E.Lacouture,Dermatological adverse events from BRAF inhibitors:a growing problem.Current oncology reports 15,249(2013年6月).
B.Comin-Anduix等,Modulation of cell signaling networks after CTLA4 blockade in patients with metastatic melanoma.PLoS One 5:e12711(2010).
H.Escuin-Ordinas等,COX-2inhibition prevents the appearance of cutaneous squamous cell carcinomas accelerated by BRAF inhibitors.Mol Oncol,(2014年3月).
K.T.Flaherty等,Combined BRAF and MEK inhibition in melanoma with BRAF V600mutations.The New England journal of medicine 367,1694(2012年11月).
R.Gorodetsky,W.H.McBride,H.R.Withers,Assay of radiation effects in mouse skin as expressed in wound healing.Radiation research 116,135(1988).
R.Gorodetsky,The use of fibrin based matrices and fibrin microbeads(FMB)for cell based tissue regeneration.Expert Opin Biol Ther 8,1831(2008年12月).
C.A.Hall-Jackson等,Paradoxical activation of Raf by a novel Raf inhibitor.Chem Biol 6,559(1999年8月).
S.Hanzelmann,R.Castelo,J.Guinney,GSVA:gene set variation analysis for microarray and RNA-seq data.BMC Bioinformatics 14,7(2013).
G.Hatzivassiliou等,RAF inhibitors prime wild-type RAF to activate the MAPK pathway and enhance growth.Nature 464,431(2010年3月18日).
S.J.Heidorn等,Kinase-dead BRAF and oncogenic RAS cooperate to drive tumor progression through CRAF.Cell 140,209(2010年1月22日).
M.Holderfield等,RAF inhibitors activate the MAPK pathway by relieving inhibitory autophosphorylation.Cancer Cell 23,594(2013年5月13日).
E.W.Joseph等,The RAF inhibitor PLX4032inhibits ERK signaling and tumor cell proliferation in a V600E BRAF-selective manner.Proceedings of the National Academy of Sciences of the United States of America 107,14903(2010年8月17日).
D.Kim等,TopHat2:accurate alignment of transcriptomes in the presence of insertions,deletions and gene fusions.Genome Biol 14,R36(2013).
J.Larkin等,Combined Vemurafenib and Cobimetinib in BRAF-Mutated Melanoma.New England Journal of Medicine(in press),(2014).
G.V.Long等,Combined BRAF and MEK Inhibition Versus BRAF Inhibition Alone in Melanoma.New England Journal of Medicine(in press),(2014).
R.Nazarian等,Melanomas acquire resistance to B-RAF(V600E)inhibition by RTK or N-RAS upregulation.Nature 468,973(2010年12月16日).
P.A.Oberholzer等,RAS Mutations Are Associated With the Development of Cutaneous Squamous Cell Tumors in Patients Treated With RAF Inhibitors.Journal of clinical oncology:official journal of the American Society of Clinical Oncology 30,316(2012年1月20日).
P.I.Poulikakos,C.Zhang,G.Bollag,K.M.Shokat,N.Rosen,RAF inhibitors transactivate RAF dimers and ERK signalling in cells with wild-type BRAF.Nature 464,427(2010年3月18日).
F.Su等,RAS mutations in cutaneous squamous-cell carcinomas in patients treated with BRAF inhibitors.The New England journal of medicine 366,207(2012年1月19日).
J.Zavadil等,Genetic programs of epithelial cell plasticity directed by transforming growth factor-beta.Proc Natl Acad Sci U S A 98,6686(2001年6月5日).
- 还没有人留言评论。精彩留言会获得点赞!