一种利用关节镜冲洗液制备间充质干细胞制剂的方法与流程
本发明涉及间充质干细胞,尤指一种利用关节镜冲洗液制备间充质干细胞制剂的方法。
背景技术:
随着细胞再生医学的发展,干细胞治疗取得了革命性突破,是现代医学最受关注、发展最快的领域之一,为各种传统方法无法治愈的疾病提供了新的治愈希望。但无论细胞移植还是组织工程均缺少来源丰富、采集方便、活性稳定的种子细胞。选择合适的种子细胞成为干细胞治疗的首要问题。关节镜手术冲洗液中含有大量从关节腔内冲洗出来的来自于软骨、滑液、滑膜、关节囊的间充质干细胞(Mesenchymal Stem Cell,MSC),通过采集术中冲洗液,从中提取、培养、扩增得到MSC,并建立细胞库,被认为是目前最为方便快捷、行之有效的获取MSC的方法,而且所获MSC能高效被利用作为细胞治疗或软骨组织工程的种子细胞。MSC制备成为临床级别适用性干细胞制剂后,具有广阔的市场应用前景。
技术实现要素:
针对现有技术的缺点和市场的需要,本发明的目的在于提供一种利用关节镜冲洗液制备间充质干细胞制剂的方法。解决关节软骨损伤和退行性疾病在组织工程和细胞移植治疗中存在缺乏采集方便、来源丰富、活性稳定、特异性强等的种子细胞来源的难题,从常规废弃的关节镜冲洗液中分离、提取、扩增出MSC,为关节软骨损伤及退变的再生修复治疗提供可靠的种子细胞。
本发明解决其技术问题所采用的技术方案是:提供一种利用关节镜冲洗液制备间充质干细胞制剂的方法,包括如下步骤:
一、收集关节镜术中冲洗液:关节镜手术过程中用无菌收集瓶对冲洗液进行收集,保存备用;
二、提取扩增干细胞:将收集的关节镜冲洗液在超净工作台分装、离心分离,弃上层清液,在所得沉淀物中加入含2%重量份的血清替代物的DMEM培养基后重新悬浮,接种到培养瓶中,45-50h后第一次换液,之后每隔3天换液一次,持续12~16天,获得贴壁细胞,待细胞克隆相互接触时进行传代;细胞传代后得到纯化与扩增,取第6代细胞进行后续步骤;
三、干细胞特性鉴定:使用CCK-8试剂检测干细胞增殖能力;利用诱导液进行干细胞成脂、成骨和成软骨诱导,用染色法鉴定干细胞多向分化能力;通过分析干细胞表面标志物CD34-、CD45-、CD73+、CD90+和CD105+,鉴定间充质干细胞特异性抗原,CD34-、CD45-表达小于1%为阴性,而CD73+、CD90+和CD105+表达都超过95%为阳性;
四、制备干细胞制剂:所得干细胞在无血清培养基及其储存添加物中按1×106个/ml~1×108个/ml的浓度分装保存于细胞库中;
五、干细胞制剂的质控:根据我国2015年8月21日出台的《干细胞制剂质量控制及临床前研究指导原则(试行)》,进行包括干细胞存活率及生长活性、纯度和均一性、无菌试验和支原体检测、细胞内外源致病因子的检测、内毒素检测、培养基及其他添加成分残余量的检测,均合格的为成品。
本发明的有益效果是:从常规废弃的关节镜冲洗液中分离、提取、扩增出MSC,与其它来源的MSC相比,具有采集方便、来源丰富、活性稳定、特异性强等优势,将成为软骨再生修复新型优质的种子细胞并能为临床及科研提供大量的干细胞资源。制备出临床级别的干细胞制剂并建立干细胞库,为干细胞治疗提供种子细胞来源,其产业化和市场化前景非常广阔。
附图说明
图1是本发明关节镜冲洗液来源干细胞的分离培养中干细胞在第1天光镜下的形态。
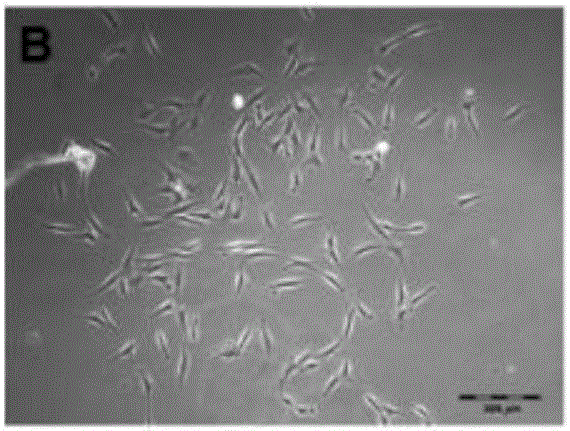
图2是本发明关节镜冲洗液来源干细胞的分离培养中干细胞在第3天光镜下的形态。
图3是本发明关节镜冲洗液来源干细胞的分离培养中干细胞在第7天光镜下的形态。
图4是干细胞集落形成后染色状态图。
图5为CCK-8检测的干细胞增殖能力图。
图6是关节镜冲洗液来源干细胞的成脂定向诱导分化图。
图7是关节镜冲洗液来源干细胞的成骨定向诱导分化图。
图8是关节镜冲洗液来源干细胞的成软骨定向诱导分化图。
图9是关节镜冲洗液来源干细胞表面标志物流式鉴定图。
具体实施方式
实施例:本发明一种利用关节镜冲洗液制备间充质干细胞制剂的方法,包括如下步骤:
一、收集关节镜术中冲洗液:关节镜手术过程中用无菌收集瓶对冲洗液进行收集,保存备用;
二、提取扩增干细胞:将收集的关节镜冲洗液在超净工作台分装(1000ml/瓶)离心,速度1200rpm持续15min,弃上清液,所得沉淀加入含2%血清替代物的DMEM培养基后重新悬浮,接种到T25培养瓶中,48h后第一次换液,之后每隔3天换液一次,持续12~16天,获得贴壁细胞,待细胞克隆相互接触时进行传代;细胞传代后得到纯化与扩增,使用第6代细胞进行后续干细胞鉴定和制剂制备;
三、干细胞特性鉴定:使用CCK-8试剂检测干细胞增殖能力;利用诱导液进行干细胞成脂、成骨和成软骨诱导,用染色法鉴定干细胞多向分化能力;通过流式细胞仪分析干细胞表面标志物(CD34-、CD45-、CD73+、CD90+和CD105+),鉴定间充质干细胞特异性抗原;
四、制定干细胞制剂的制备工艺标准:制定干细胞的采集、分离、纯化、扩增和传代,干细胞(系)的建立、向功能性细胞定向分化,培养基、辅料和包材的选择标准及使用,细胞冻存、复苏、分装和标记,以及残余物去除等干细胞制剂制备工艺标准操作流程及每一过程的标准操作程序(SOP);
五、制备关节镜冲洗液来源干细胞制剂:所得干细胞在无血清培养基及其储存添加物中按1×107个/ml的浓度分装保存于细胞库中,并分成主细胞库和工作细胞库,自体细胞回输可排除免疫原性反应的发生;
六、干细胞制剂的质控:根据我国2015年8月21日出台的《干细胞制剂质量控制及临床前研究指导原则(试行)》,并参考国内外有关细胞基质和干细胞制剂的质量控制指导原则,进行全面的细胞质量、安全性和有效性的检验,包括干细胞存活率及生长活性、纯度和均一性、无菌试验和支原体检测、细胞内外源致病因子的检测、内毒素检测、培养基及其他添加成分残余量的检测等,制定放行检验标准;
七、关节镜冲洗液来源干细胞制剂的临床试验:制备的关节镜冲洗液来源干细胞制剂在门诊自体回输注射进入患者关节腔进行损伤组织的再生修复。
- 还没有人留言评论。精彩留言会获得点赞!