一种亲水小分子脑靶向二级递送载药体及其制备方法与流程
本发明属于脑靶向载体技术领域,具体涉及一种亲水小分子脑靶向二级递送载药体及其制备方法。
背景技术:
中枢神经系统疾病是造成健康生命损失最高的疾病,而治疗其疾病最大的困难就是药物难以通过血脑屏障。虽然多数药物的分子量小于500Da,但实际上只有少于2%的小分子药物可以通过血脑屏障。大多数亲水小分子药物很难通过血脑屏障,因为小分子亲水药物本身极性强,组织渗透性差,肾脏滤过率高,体内分布不理想;如与血浆蛋白结合,可进一步降低血脑屏障通透率和自身药物活性。为了达到理想的药效,往往需要提高药物剂量,导致毒性反应增强。
以γ-羟丁酸钠作为亲水小分子中枢神经药物代表,γ-羟丁酸钠为白色微细结晶,易溶于水,水溶液稳定,系GABA的中间代谢产物,可模拟GABA产生似生理性睡眠,因而临床上作为镇静类麻醉药物。与其他麻醉药不同,γ-羟丁酸钠不影响脑血流量,不增加颅内压,对缺血器官有保护作用;对循环无抑制作用,注射后脉搏有力,血压不降低,心排量无变化或稍增加,可增加心肌对缺氧的耐受力,扩张外周血管,毛细血管充盈良好;对呼吸抑制作用小,不抑制呼吸中枢对CO2变化的反应,临床常规剂量使潮气量稍有增加,呼吸频率稍减慢,每分钟通气量不变或略增加;能抑制咽喉反射,使下颌松弛,辅助表面麻醉后可施行保留呼吸的气管内插管、异物取出;在体内进行氨基转换,进入三羧酸循环,降解成水和CO2经肾和肺排出,并产生能量,对肝、肾无毒性作用,安全范围大,即使黄疸患者也可选用。然而,γ-羟丁酸钠由于脂溶性差,血脑屏障通透率低,为达到充分镇静,全麻诱导静注量极大,为疏水镇静药丙泊酚的30-40倍,依托咪酯的200-300倍,从而使苏醒时间延长,导致该药在临床麻醉领域已经基本被淘汰。但作为睡眠辅助的口服长效药物,该药的镇静效果却不足以维持一夜,需要夜间加服药第二次药物,如一次服用量过大,会导致中毒反应。
为此新型γ-羟丁酸钠制剂的研究方兴未艾,国外相关发明专利大多于近3年授权,主要用于治疗发作性睡病患者的日间嗜睡和减少猝倒发作次数。其改良策略包括三种类型:1.基于配伍的基础改造:(1)将γ-羟丁酸与羧酸转运体抑制剂(如丙戊酸钠、双氯芬酸、布洛芬)复合使用,以减少γ-羟丁酸使用量(US9486426B2)。(2)制备γ-羟丁酸的钠、钾、镁、钙盐的混合物减少单纯钠盐对高血压、心肾疾病、中风的风险(US9132107B2)。(3)通过添加药用辅料以提高γ-羟丁酸及盐的稳定性、抗菌性等(WO2014096984,US8952062B2)。2.基于交联的结构改造:制备γ-羟丁酸氘化类似物,或与生物相容性分子(如碳水化合物、氨基酸、磷脂、脂肪酸、烷基等)发生酯化、酰化、成环、聚合等反应,制成γ-羟丁酸前药,以延长药物作用时间(US8778301B2、US9309182B2、CN103370289B)。3.基于载体的改造:(1)制备pH值触发药物,使药物在十二指肠、结肠等不同部位特异性快速释放,以延长药物作用时间(US8598191B2)。(2)制备高剂量水溶性和吸湿性药物的控释剂,延长药物作用时间(CN102917697B)。(3)制备高浓度γ-羟丁酸钠片剂,可达到与口服水剂类似的生物等效性(US8771735B2)。以上改良策略主要着重于提高γ-羟丁酸的稳定性,增强药效、延长其药物作用时间,无法实现起效快、血脑屏障通透率高,药物使用量少、毒副作用小、可控性好等性能,主要适应于患者夜间口服给药改善睡眠,并不适于静脉全麻诱导和维持及器官缺血保护,主要原因是药物血脑屏障通透效率低且无脑靶向功能。
技术实现要素:
本发明的目的在于提供一种亲水小分子脑靶向二级递送载药体及其制备方法,该二级递送载药体利用血脑屏障高脑磷脂特异性,采用脑磷脂氢键触发释放磷脂酰药物前体,磷脂酰药物再利用其良好的疏水性和局部浓度梯度透过血脑屏障,实现了药物从外周循环靶向到血脑屏障释放的第一级递送;随后,磷脂酰药物再利用其良好的疏水性能在疏水脑实质内渗透,在磷脂酶D的作用下水解释放小分子药物,实现了药物从血脑屏障到脑实质的第二次递送。
本发明是通过以下技术方案来实现:
本发明公开的一种亲水小分子脑靶向二级递送载药体,由一级递送载药外壳和包覆于其内部的二级递送载药内芯构成;其中,一级递送载药外壳用于将亲水小分子从外周血液循环靶向释放至血脑屏障;二级递送载药内芯用于将亲水小分子从血脑屏障释放至脑实质。
所述二级递送载药内芯是利用磷脂酶D碱基转移反应将亲水性小分子与卵磷脂反应生成的磷脂酰药物前体;或者采用其他反应方式使亲水小分子与脑磷脂等磷脂形式交联。
所述一级递送载药外壳是利用改性直链淀粉包裹磷脂酰药物前体,生成螺旋复合物,该螺旋复合物内侧疏水,外侧亲水。
所述亲水小分子为能够作用于中枢神经系统的亲水小分子药物。
所述亲水小分子药物包括镇静药物、抗癫痫药物、抗肿瘤药物、抗菌药物、脑血管药物及解热镇痛药物等中枢用药。
所述亲水小分子药物包括镇静药物γ-羟丁酸钠、抗癫痫药物丙戊酸钠、抗肿瘤药物环磷酰胺、抗菌药物阿莫西林、脑血管药物盐酸法舒地尔、解热镇痛药物双氯芬酸钠等中枢用药。
本发明还公开了一种亲水小分子脑靶向二级递送载药体的制备方法,包括以下步骤:
1)磷脂酰药物前体的制备
将亲水小分子溶解于水相,卵磷脂溶解于油相,将水油两相混合后加入磷脂酶D催化反应合成磷脂酰药物前体;
2)酯化直链淀粉螺旋载体的制备
将直链淀粉溶于DMSO溶液中,添加酸酐和催化剂,反应生成酯化直链淀粉,用无水乙醇析出酯化直链淀粉,抽滤洗涤并烘干,研磨成粉备用;
3)亲水小分子脑靶向二级递送载药体的制备
将酯化直链淀粉溶于PBS溶液中,添加磷脂酰药物前体,充分搅拌使酯化直链淀粉负载磷脂酰药物前体,用硅胶柱柱层析法分离出未包裹的磷脂酰药物前体,制得亲水小分子脑靶向二级递送载药体。
所述催化剂为1-甲基咪唑。
所述亲水小分子为镇静药物、抗癫痫药物、抗肿瘤药物、抗菌药物、脑血管药物及解热镇痛药物等中枢用药。
所述亲水小分子药物包括镇静药物γ-羟丁酸钠、抗癫痫药物丙戊酸钠、抗肿瘤药物环磷酰胺、抗菌药物阿莫西林、脑血管药物盐酸法舒地尔、解热镇痛药物双氯芬酸钠。
与现有技术相比,本发明具有以下有益的技术效果:
针对血脑屏障和脑实质不同的组织特征,本发明公开的亲水小分子脑靶向二级递送载药体,由一级递送载药外壳和包覆于其内部的二级递送载药内芯构成。突破以往添加靶头的受体介导内吞方式,以简洁有效的二级递送方式,将亲水小分子药物递送到脑实质。首先,利用血脑屏障高脑磷脂特异性,采用脑磷脂氢键触发释放磷脂酰药物前体,实现了亲水小分子药物从外周循环靶向到血脑屏障释放的第一级递送;随后,磷脂酰药物再利用其良好的疏水性能在疏水脑实质内渗透,在磷脂酶D的作用下水解释放亲水小分子药物,实现了亲水小分子药物从血脑屏障到脑实质的第二次递送。本发明二级递送载药体与其他亲水小分子药物制剂相比具有显著功能优势:
1、亲水小分子药物包裹在载体螺旋结构当中,避免了亲水小分子药物与血浆蛋白结合,减少了肾脏清除率,提高了有效血药浓度,减少了药物使用量和毒性反应。
2、利用血脑屏障触发、局部高浓度疏水性磷脂酰前体血脑屏障和脑组织渗透、磷脂酶D高效水解三种关键技术,提高了脑靶向功能和血脑屏障通透率,减少了药物使用量和毒性反应。
3、磷脂和淀粉均属于天然材料,代谢产物安全无毒,具有良好的生物相容性和代谢性能。
附图说明
图1.亲水小分子脑靶向二级递送载药体示意图;
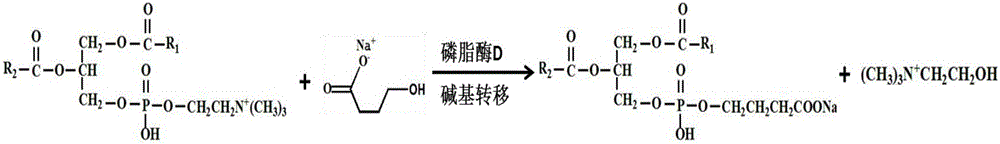
图2.磷脂酰γ-羟基丁酸钠的合成路线;
图3.磷脂酰γ-羟基丁酸钠、卵磷脂红外光谱;
图4.丙酸酯直链淀粉、PHSCP、HSBH2D的红外光谱图;
图5.单次少量注射γ-羟基丁酸钠、PHSCP、HSBH2D的镇静苏醒实验:a表示诱导时间、维持时间、苏醒时间(与游离γ-羟基丁酸钠和PHSCP比较,*P<0.05);b代表BIS值诱导期变化;
图6.HSBH2D被脑磷脂双分子层触发释放PHSCP图(a)分子模拟,(b)释放曲线;
图7.采用Cy5NHS标记亲水小分子脑靶向二级递送载药体的近红外小动物成像结果;
图8.磷脂酶D水解释放化学式;
图9.气相色谱法检测γ-羟基丁酸钠的释放曲线。
具体实施方式
下面结合具体的实施例对本发明做进一步的详细说明,所述是对本发明的解释而不是限定。
亲水小分子药物载体的设计难点在于亲水环境不漏药,静脉注射快速渗透到达脑实质。参见图1,采用具有良好生物相容性和生物降解性的淀粉和卵磷脂作为原料。利用磷脂酶D碱基转移特异性将亲水小分子酯化成为磷脂酰药物前体,并用酯化直链淀粉纳米螺旋载体负载磷脂酰药物前体,制备成亲水小分子脑靶向二级递送载药体。由于酯化直链淀粉螺旋载体外部羟基具有亲水性,亲水小分子脑靶向二级递送载药体可以均匀分散于亲水溶液及血液系统;相对于亲水小分子,磷脂酰结构分子量大、疏水性强,使磷脂酰药物前体疏水性好,可以稳定负载于螺旋载体内部疏水结构,从而使亲水小分子脑靶向二级递送载药体在亲水环境可以稳定负载亲水小分子药物不漏药。
本发明中,PHSCP(Phosphatidyl Hydrophilic Small molecule Central nervous system Prodrug,PHSCP)表示磷脂酰亲水小分子中枢神经系统药物前体,简称磷脂酰药物前体;HSBH2D(Hydrophilic Small molecule drug brain targeting helix two stages drug delivery system)表示亲水小分子药物脑靶向纳米螺旋二级递送载药体系,简称亲水小分子脑靶向二级递送载药体。
实施例1
本实验设计:亲水小分子γ-羟丁酸钠脑靶向纳米螺旋二级递送载药体系,利用磷脂酶D碱基转移特异性将亲水小分子酯化成磷脂酰γ-羟丁酸钠,再用酯化直链淀粉纳米螺旋载体负载磷脂酰药物前体。
其体内释放策略为:静脉注射后,螺旋载体被血脑屏障脑磷脂触发释放磷脂酰γ-羟丁酸钠,磷脂酰γ-羟丁酸钠利用良好的疏水性和局部浓度梯度快速高效通过血脑屏障,实现载体第一级递送;磷脂酰γ-羟丁酸钠利用良好的疏水性可以在疏水脑组织内渗透移动,被广泛存在于各功能脑区(在海马、下丘脑、皮质、中脑、纹状体等脑区内存在大量的磷脂酶D)的磷脂酶D水解释放亲水小分子活性药物,实现载体第二级递送。
通过载体的二级递送最终提高γ-羟丁酸钠血脑屏障和脑组织渗透率,使脑组织内快速达到有效血药浓度,降低肾脏滤过率,减少药物用量,减少剂量相关毒性反应。
1、具体实验步骤包括:
1)磷脂酰γ-羟基丁酸钠的制备
参见图2,利用磷脂酶D的碱基转移特性,将γ-羟基丁酸钠羟基与卵磷脂的磷脂酰基团发生碱基转移酯化反应,生成磷脂酰γ-羟基丁酸钠。
将γ-羟基丁酸钠溶解于水相,卵磷脂溶解于油相(γ-羟基丁酸与卵磷脂钠质量比10-100:1),将水油两相在三角瓶中混合(油水体积比1-4:1),加入磷脂酶D催化反应合成磷脂酰γ-羟基丁酸(磷脂酶D与卵磷脂比例为1U:0.1-1g),PH4-7,温度20-37℃,采用薄层层析法取样动态检测反应过程。
对合成得到的磷脂酰γ-羟基丁酸钠进行结构分析,将0.25g磷脂酰γ-羟基丁酸钠和0.25g卵磷脂分别与0.1g光谱分析级别KBr混合后研磨,并压成KBr红外光谱样品片,采用傅里叶红外光谱分析仪检测化学键变化。
结果如图3所示,磷脂酰γ-羟基丁酸钠与卵磷脂有很多相似的特征峰,如1734cm-1的C=O特征峰,1242cm-1与1072cm-1的P-O特征峰。而磷脂酰γ-羟基丁酸钠不含有卵磷脂1172cm-1的N-C特征峰,含有1578cm-1的来自γ-羟基丁酸钠的-COOH特征峰,因此说明我课题组已经成功合成了纯度较高的磷脂酰γ-羟基丁酸钠。
2)酯化直链淀粉螺旋载体的制备
将1g直链淀粉溶于40-60mlDMSO溶液中,添加0.3-0.5酸酐(乙酸酐、丙酸肝、丁酸酐)和0.2ml催化剂1-甲基咪唑,反应生成酯化直链淀粉,用无水乙醇析出酯化直链淀粉,抽滤洗涤并烘干,研磨成粉备用;
3)亲水小分子脑靶向二级递送载药体的制备
将50-100mg酯化直链淀粉溶于5-10mLPBS溶液中,添加10-30mg磷脂酰药物前体,充分搅拌使酯化直链淀粉负载磷脂酰药物前体,用硅胶柱柱层析法分离出未包裹的磷脂酰药物前体,制得亲水小分子脑靶向二级递送载药体。
2、对制得的亲水小分子脑靶向二级递送载药体进行结构分析:
将0.25gγ-羟基丁酸钠脑靶向二级递送载药体、磷脂酰γ-羟基丁酸钠、酯化直链淀粉分别与0.1g光谱分析级别KBr混合后研磨,并压成KBr红外光谱样品片,采用傅里叶红外光谱分析仪检测化学键变化。γ-羟基丁酸钠脑靶向纳米螺旋二级递送载药体系的红外光谱图参见图4,HSBH2D含有PHSCP的特征峰,如1734cm-1的C=O特征峰、1242cm-1和1072cm-1的P-O特征峰、1578cm-1来自γ-羟基丁酸钠的-COOH特征峰;HSBH2D含有丙酸酯直链淀粉的特征峰,如2800cm-1的-OH特征峰,说明本发明已经成功合成了纯度较高的γ-羟基丁酸钠脑靶向纳米螺旋二级递送载药体系HSBH2D。
实施例2
γ-羟基丁酸钠脑靶向二级递送载药体系药学性质分析
1、HSBH2D可以实现家兔快速镇静苏醒
将18只雄性家兔随机分为3组,分别从家兔耳缘静脉单次推注50mg/kgγ-羟基丁酸钠当量(相当于诱导量的1/4)的游离γ-羟基丁酸钠、PHSCP、HSBH2D三种剂型,用BIS监测家兔镇静情况,以BIS值≤85定义镇静,以BIS≥90定义清醒,比较诱导(BIS值从清醒值降到85所用时间)、维持(BIS值维持在85的时间)、苏醒时间(BIS值从85到90所用时间)。参见图5,a表示诱导时间、维持时间、苏醒时间(与游离γ-羟基丁酸钠和PHSCP比较,*P<0.05);b代表BIS值诱导期变化。可以看出,与游离γ-羟基丁酸钠和PHSCP比较,HSBH2D可显著缩短诱导、维持、苏醒时间(*P<0.05),同时提供有效麻醉维持深度,使得麻醉可控性增强。
2、HSBH2D被脑磷脂双分子层触发释放PHSCP
参见图6,如图6中a所示,采用在GROMOS 53A6力场下,HSBH2D放入10nm×10nm×12nm脑磷脂脂质双分子层模型,平衡200ns后HSBH2D被脑磷脂触发释放。在被动血脑屏障模型中,十二烷配制的2%猪脑极性脂溶液(Avanti Polar Lipid,Inc.,USA)常作为简易的血脑屏障,该猪脑极性脂包括33%脑磷脂和其他磷脂。将5μL 2%猪脑极性脂溶液平铺在普通96孔板底部,再滴加150μL 25μg/mL的HSBH2D,同时制作多孔,分别在5、10、15、20、25、30min时间点取上清液,HPLC测PHSCP含量,绘制释放曲线。如图6中b所示,HSBH2DB可被血脑屏障快速触发释放PHSCP。
3、近红外小动物成像实验:
采用脑磷脂与水溶性菁染料琥珀酰亚胺酯Cy5NHS反应生成Cy5NHS标记的磷脂酰药物前体,负载于丙酸酯直链淀粉,形成Cy5NHS标记的亲水小分子脑靶向二级递送载药体,通过裸鼠尾静脉注射0.1mL 50μg/mL Cy3NHS,以等量游离Cy5NHS为对照。
复合X-射线定位和近红外荧光显影技术(IVIS luminaⅢ,Caliper,USA),动态观察荧光标记在裸鼠体内的分布。如图7所示,注射10min后,采用软件扣除对照游离Cy5NHS小鼠的荧光,Cy5NHS标记的亲水小分子脑靶向二级递送载药体小鼠可以明显看到脑部的强荧光显影,说明本发明的亲水小分子脑靶向二级递送载药体可以实现脑靶向给药。
4、气相色谱法检测γ-羟基丁酸钠的释放曲线:
参见图8,亲水小分子脑靶向二级递送系统之磷脂酶D水解释放化学式。说明:磷脂酶D可以有效水解磷脂酰γ-羟基丁酸钠,将γ-羟基丁酸钠游离出来。
以100mg磷脂酰γ-羟基丁酸钠为底物,溶解在20ml正己烷与水(V/V=15:5)的二相溶液,并用磁力搅拌器以200r/min持续搅拌,加入1U色褐链霉菌源磷脂酶D,调整反应温度为37℃10,水相ph值为7.35。每10min取1ml浑浊反应液,离心后取水相样品,用气相色谱仪检测γ-羟基丁酸钠浓度,计算释放比例。Sigma的磷脂酶D反应效率很高,20min即可将90%的底物水解,与说明书所述酶效率基本一致。参见图9,说明磷脂酶D可以高效水解磷脂酰γ-羟基丁酸钠。
- 还没有人留言评论。精彩留言会获得点赞!