MANF蛋白的应用的制作方法
本发明属于生物技术及医药领域,具体涉及一种manf蛋白在制备治疗干燥综合征药物中的应用。
背景技术:
干燥综合征(sjogren,ssyndrome,ss)是一种自身免疫性疾病,主要累及唾液腺与泪腺,表现为口干、眼干;也可累及皮肤等其他器官出现多系统改变;受累器官可见大量淋巴细胞浸润,血清中可检出多种自身抗体,常伴有高免疫球蛋白血症。根据发病原因可将干燥综合征分为原发性和继发性两种:原发性干燥综合征是不合并有其它结缔组织病的;而继发性干燥综合征是指在已有肯定诊断的结缔组织病如系统性红斑狼疮、类风湿关节炎、系统性硬化病等基础上出现的干燥综合征。
原发性干燥综合症(primarysjogrensyndrome,pss)是以口干燥症状、干燥性角膜结膜炎及皮肤干燥为主要特征的慢性炎性疾病。主要累及唾液腺与泪腺,受累器官可见大量淋巴细胞浸润,血清中可检测到多种自身抗体。本病人群患病率为0.29%~0.77%,中老年女性高发,发病年龄多在40~50岁之间,男:女比约为1:9~1:20。
ss的病因尚未明确,多数学者认为与遗传因素、病毒感染、自身抗原等因素有关。t、b淋巴细胞和树突细胞等免疫细胞参与了ss的病理过程,涎腺和其他受累器官中有大量的淋巴细胞浸润、聚集成灶,其中活化的th占优势,th17与treg平衡紊乱;b淋巴细胞功能高度亢进,高球蛋白血症,多种自身抗体大量产生。
目前临床上ss尚没有理想的特异性治疗药物,主要治疗模式为主观症状的对症治疗和替代治疗:如使用匹罗卡品、人工泪液或唾液等以减轻患者眼干、口干,必要时加用羟基氯喹(hcqs)。伴有系统受累的ss的常规治疗则采用糖皮质激素和免疫抑制剂。这些药物在治疗疾病的同时,也给患者带来严重的不良反应,如hcqs不良反应较多,主要为视野缺失、黄斑变性、肝脏及心脏毒性;免疫抑制剂甚至有诱发肿瘤的危险。
manf(mesencephalicastrocyte-derivedneurotrophicfactor,manf)蛋白是一个分泌蛋白,其由星形胶质细胞源性神经营养因子基因编码得到,该星形胶质细胞源性神经营养因子基因是通过微阵列(microarray)技术从30000个基因中筛选出的对内质网应激最敏感的基因,现有技术中采用manf蛋白使得er(内质网)应激可上调其表达和分泌,在内质网应激中起保护作用。目前未有manf蛋白应用于干燥综合征方面的研究报道。
技术实现要素:
针对现有技术的不足,本发明提供一种manf蛋白在制备治疗干燥综合征药物中的应用,用解决背景技术中的问题。
本发明解决技术问题采用如下技术方案:
本发明提供了一种manf蛋白在制备治疗干燥综合征药物中的应用。
进一步的,所述干燥综合征包括原发性干燥综合征或继发性干燥综合征中的一种。
进一步的,所述manf蛋白由星形胶质细胞源性神经营养因子基因编码得到。
本发明还提供了编码manf蛋白的基因在制备治疗干燥综合征药物中的应用。
进一步的,所述干燥综合征包括原发性干燥综合征或继发性干燥综合征中的一种。
本发明还提供了含有manf蛋白编码基因的生物材料在制备治疗干燥综合征药物中的应用。
进一步的,所述生物材料包括表达载体或宿主细胞。
进一步的,所述干燥综合征包括原发性干燥综合征或继发性干燥综合征中的一种。
与现有技术相比,本发明具有如下的有益效果:
本发明创造性的提供了manf蛋白在制备治疗干燥综合征药物中的应用,进而治疗包括原发性干燥综合征或继发性干燥综合征在内的自身免疫性疾病,同时本发明通过对小鼠成功建立诱导型干燥综合征模型,并持续研究跟踪得到了manf对建立的小鼠诱导型干燥综合征模型有较好的治疗作用,能够改善ss小鼠一般状况,缓解ss小鼠唾液量的减少,有效改善ss小鼠颌下腺病理学变化,降低特异性自身抗体抗ssa、ssb水平。
关于本发明相对于现有技术,其他突出的实质性特点和显著的进步在实施例部分进一步详细介绍。
附图说明
通过阅读参照以下附图对非限制性实施例所作的详细描述,本发明的其它特征、目的和优点将会变得更明显:
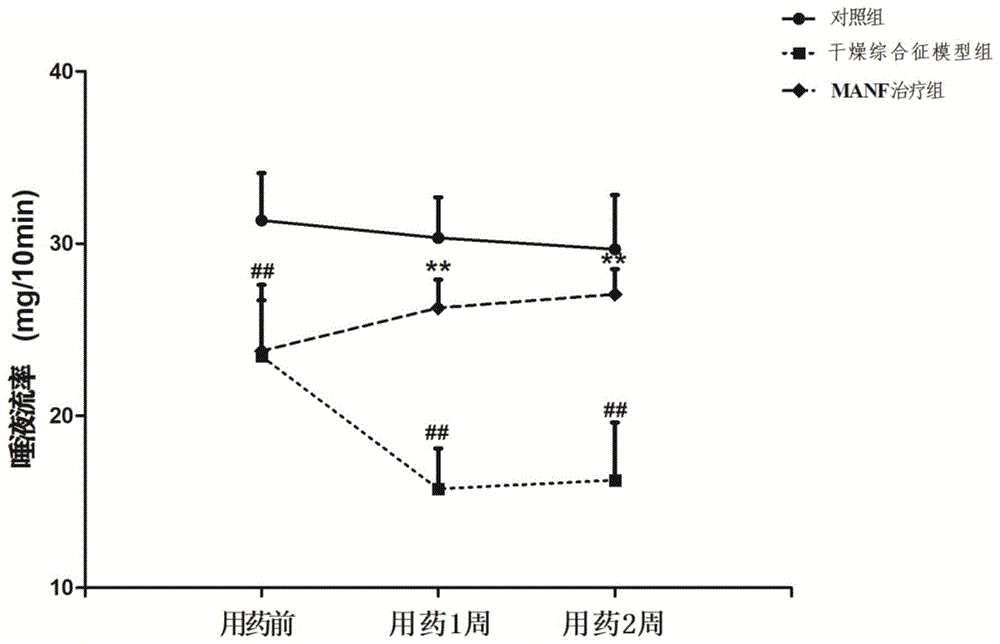
图1为实施例1的对照组、干燥综合征模型组、manf治疗组的小鼠唾液流率的对比图;
图2为实施例1的对照组小鼠颌下腺病理在he×100下的观察结果图;
图3为实施例1的干燥综合征模型组小鼠颌下腺病理在he×100下的观察结果图;
图4为实施例1的manf治疗组小鼠颌下腺病理在he×100下的观察结果图;
图5为实施例1的的对照组、干燥综合征模型组、manf治疗组的小鼠病理的评分量化结果示意图。
图6为实施例1的的对照组、干燥综合征模型组、manf治疗组的小鼠特异性抗ssa、ssb抗体含量对比示意图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
本实施例提供了一种manf蛋白在制备治疗干燥综合征药物中的应用,其中本实施例中的干燥综合征包括原发性干燥综合征或继发性干燥综合征中的一种,本实施中manf蛋白由星形胶质细胞源性神经营养因子基因编码得到。
为了验证本发明的效果,本实施例中采用的材料包括动物、药物和试剂以及仪器,其中:
动物为c57bl/6小鼠,雌性,体质量18g±2g,购自安徽医科大学。饲养于安徽省实验动物中心spf级实验室,温度23±1℃恒温,湿度50%~60%,自由进食进水。动物购进后,进行一周的适应性饲养后,开始实验。
药物和试剂包括:
(1)重组人manf蛋白,购自美国creativebiomart公司,溶于生理盐水,腹腔注射;
(2)戊巴比妥钠:25g/瓶,购于安徽医科大学设备管理处,取2.4g溶于100ml双蒸水制成溶液(2.4%)供小鼠腹腔注射用;
(3)毛果芸香碱(pilocarpine):购于sigma公司白色粉末,称取10mg溶于10ml双蒸水中配制成1mg/ml,使用时稀释成所需浓度(0.025mg/ml);
(4)elisa试剂盒:抗ssa抗体试剂盒(no.5710)与抗ssb抗体试剂盒(no.5810),购于alphadiagnostic公司。
主要仪器包括
分析天平:赛多利斯科学仪器(北京)有限公司
multiskango全波长酶标仪:美国thermo公司
-80℃超低温冰箱:三洋公司;
rm2135石蜡切片机:德国徕卡公司;
脱水机:亚光公司;
bmⅱ型病理组织包埋机:安徽电子科学研究所
本实施例中先进行动物模型的建立及分组,包括:
抗原的制备
在无菌操作台上取c57bl/6小鼠颌下腺,提取颌下腺蛋白,bca法蛋白定量为4.5-5mg/ml。加完全弗式佐剂使抗原终浓度为2.5mg/ml。
分组及抗原的注射
spf级30只雌性c57bl/6小鼠,6w,16-18g,随机分为3组:正常对照组,模型组,manf治疗组。除正常对照组外,第0、7天,各组小鼠背部酒精消毒后背部皮内多点注射抗原,每只小鼠共注射0.1ml抗原。第14天,用不完全弗氏佐剂将颌下腺抗原调整为2.5mg/ml,注射抗原方式同前。
给药
manf治疗组第7w起开始,0.7mg/kg重组人manf蛋白腹腔注射,每周3次,连续给药2周,正常对照组及模型组给予同等剂量溶媒。第9w处死小鼠。
本实施例的指标检测包括:
全身情况观察,具体为:
观察小鼠全身皮肤有无搔抓、破损现象,口唇情况等。
唾液量检测,具体为:
用药前,给药1周,给药2周分别测量各组小鼠的唾液量,共收集10分钟唾液量。测量前小鼠腹腔注射2.4%的戊巴比妥钠(100ul/20g),以呼吸平稳,眼角膜反射消失,四肢肌群松弛为麻醉标准。完全麻醉后注射0.025mg/ml毛果芸香碱溶液(1.2mg/㎏),5分钟后开始收集唾液,共收集10分钟唾液量(将事先称好的无菌小棉球塞入小鼠舌下,10分钟后取出称重)。
检测颌下腺组织病理学检查颌下腺组织病理,具体为:
处死小鼠,取颌下腺10%福尔马林固定,he染色光镜下观察,采用chisholm和mason提出的唇腺活检评判标准分级,0级,无淋巴细胞浸润。ⅰ级,淋巴细胞轻度散在浸润。ⅱ级,淋巴细胞中度浸润,但末形成灶性。ⅲ级,每4mm2有一个或以上但少于两个淋巴细胞浸润灶。ⅳ级,每4mm2有两个及以上的淋巴细胞浸润灶(注:一个淋巴细胞浸润灶是指有50个或更多的淋巴细胞)。
运用elisa法测定各组小鼠血清中抗ssa和抗ssb抗体水平,具体为:
直接采用elisa试剂盒进行检测。
本实施例的结果追踪包括:
全身情况观察结果,具体为:
从免疫第3w起,模型组小鼠先后出现舔舌,抓挠口唇等现象,而对照组并无明显的此现象,manf治疗后情况有所改善;
各组小鼠不同时间唾液量的变化,请参照图1,具体为:
与正常对照组相比,用药前模型组唾液量逐渐减少,差异具有显著性。而与模型组相比,manf用药1周,用药2周小鼠唾液量均有升高,其中##p<0.01vs对照组,**p<0.01vs干燥综合征模型组均具有统计学意义上的统计学差异。
各组颌下腺病理观察结果及分级,请参照图2-5,具体为:
模型组小鼠颌下腺均表现出不同程度的淋巴细胞浸润,浸润细胞多分布在血管及导管周围,浸润程度严重的主要表现为淋巴细胞浸润灶的增加及浸润灶面积的增大;从图4中manf治疗组可显著改善淋巴细胞的浸润。参照图5即为三组小鼠按照评判标准分级标准得到的病理的评分量化结果,其中##p<0.01vs对照组,*p<0.05vs干燥综合征模型,具有统计学意义上的统计学差异。
运用elisa法测定血清中抗ssa和抗ssb抗体水平结果,请参照图5,具体为:
与正常对照组相比,模型组小鼠外周血清抗ssa、ssb抗体水平明显升高,;与模型组相比,cp-25高剂量组(70mg/kg)小鼠血清中抗ssa、ssb抗体水平显著降低,其中#p<0.05,##p<0.01vs对照组,*p<0.05,**p<0.01vs干燥综合征模型组均具有统计学意义上的统计学差异。
通过以上结果的分析可以明显得到:
本实施例的c57bl/6小鼠诱导型干燥综合征模型构建成功。通过与正常对照组的比较,c57bl/6小鼠诱导型干燥综合征模型唾液量的显著减少、颌下腺病理学的改变及特异性抗体抗ssa、ssb水平的明显升高均提示c57bl/6小鼠诱导型干燥综合征模型构建成功;
manf蛋白可改善ss小鼠一般状况,缓解ss小鼠唾液量的减少,改善ss小鼠颌下腺病理学变化,降低特异性自身抗体抗ssa、ssb水平,manf蛋白对c57bl/6小鼠诱导型干燥综合征模型有明显的治疗作用。
在此基础上,本发明还提供了编码manf蛋白的基因在制备治疗干燥综合征药物中的应用,以及含有manf蛋白编码基因的生物材料在制备治疗干燥综合征药物中的应用。其中,生物材料包括表达载体或宿主细胞。
对于本领域技术人员而言,虽然,上文中已经用一般性说明、具体实施方式及试验,对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。
此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
序列表
<110>安徽医科大学
<120>manf蛋白的应用
<130>2020
<160>1
<170>siposequencelisting1.0
<210>1
<211>158
<212>prt
<213>人工合成(artificialsequence)
<400>1
leuargproglyaspcysgluvalcysilesertyrleuglyargphe
151015
tyrglnaspleulysaspargaspvalthrpheserproalathrile
202530
gluasngluleuilelysphecysargglualaargglylysgluasn
354045
argleucystyrtyrileglyalathraspaspalaalathrlysile
505560
ileasngluvalserlysproleualahishisileprovalglulys
65707580
ilecysglulysleulyslyslysaspserglnilecysgluleulys
859095
tyrasplysglnileaspleuserthrvalaspleulyslysleuarg
100105110
vallysgluleulyslysileleuaspasptrpglygluthrcyslys
115120125
glycysalaglulysserasptyrilearglysileasngluleumet
130135140
prolystyralaprolysalaalaseralaargthraspleu
145150155
- 还没有人留言评论。精彩留言会获得点赞!