一种硫化锡材料的制备方法及应用与流程
本发明涉及材料制备技术、污染物监测与光催化降解技术,具体是一种形貌可控的硫化锡(SnS)材料的制备方法及应用。
背景技术:
光催化材料具有光分解水制氢和光降解有机污染物两大功能,因此在解决能源和环境问题方面有着重要的应用前景。随着社会经济的飞速发展,来自工农业生产中产生的各种毒害有机污染物严重威胁着环境和人类的健康。因此,寻求一种新型高效的环境治理技术具有重要的意义。光催化技术因其节能、高效、污染物降解彻底、无二次污染等特点,因而成为未来高新技术的新希望。南京大学邹志刚教授认为,发展可见光响应光催化材料是实现高效太阳能转换的最重要途径之一。在此背景下, 人们对开发可见光响应型光催化材料表现出了浓厚的兴趣。
1976年和1977年,Carey和Frank等人分别利用TiO2悬浮液,在紫外辐射下成功降解多氯联苯和氰化物,开启了光催化降解水中污染物的新纪元。虽然TiO2对绝大多数光化学反应具有很高的催化活性,拥有优异的化学及光化学稳定性。但因其较大的能带宽度值(Eg≈3.2ev,Eg = 1240/λ),只对紫外光有吸收(紫外光只占太阳光的5%),光利用率低,兼具有e-和h+的复合速度快、量子效率低等缺点,在一定程度上限制了其工业化应用。硫化锡由于具有较窄的能带宽度,原料无毒、丰富,能对可见光响应,化学及热稳定性好的特点而备受关注,现已成为光催化剂材料研究的热点之一。SnS是能带宽度为1.0~2.3eV的半导体材料,由于近红外吸收及独特的结构,在太阳能电池、探测器、锂离子电池、超级电容器上也有应用。SnS中Sn含量的不同,可能使得SnS是p型或是n型半导体,这一特点更扩大了其在光催化领域的应用范围。
2013年,Biacchi等人合成了形貌可控的伪四方SnS纳米晶体:纳米立方体、球形多面体、纳米片。合成方法的不同,导致合成的SnS纳米材料的形貌不一,因此对降解底物MB的降解催化效果也不同。结果表明,纳米立方体对MB的降解速率是球形多面体的两倍,并且二者对MB的降解速率均高于纳米片。对于纳米立方体,011平面对MB的降解催化活性比010、001平面的更高。同年,Patra等人采用不同的溶剂在5s反应时间内合成了SnS纳米立方体和纳米四面体,并比较这两种形貌的SnS降解MB的光催化性能。结果表明,两种形貌的SnS均对MB有降解作用,但SnS四面体的130面比SnS立方体的101、040面的催化效果更好,分析原因可能是因为表面能的影响,从而影响降解过程载流子的迁移。本文采用溶剂热法合成了形貌可控的SnS材料,并研究了其光催化降解MO、Rh B、MB等有机污染物的催化性能。而关于这种方法制备的SnS光催化材料用于光催化降解有机废水方面的研究还未见报道。已报道的关于硫化锡材料的制备方法中,有离子液体援助法,声波降解法等,溶剂热法相对其而言,具有反应条件温和、方法简单、成本较低等优点。
技术实现要素:
本发明的目的在于合成形貌和晶粒大小可控的SnS材料,解决目前SnS在光催化等方面研究的不足和缺陷,锡是一种重要的有色金属,通过深加工提升材料的附加值,对国家经济建设具有显著的意义;目前工业生产中应用到的探测器材料、电池电极材料等,可通过形貌和晶粒大小可控的纯SnS改性得到。
本发明一种形貌可控的硫化锡(SnS)材料的制备方法具体步骤如下:
(1)将SnCl2·2H2O、硫源、表面活性剂分别溶解于溶剂中,超声至完全溶解;
(2)将步骤(1)中的SnCl2·2H2O溶液、硫源溶液、表面活性剂溶液依次滴加入到反应釜中,磁力搅拌10~20min后,将水热反应釜温度设置在80~200℃,反应3~24h,其中S2-与Sn2+的摩尔比为1~4︰1,表面活性剂与SnCl2·2H2O的质量比为0.5~3;
(3)将步骤(2)中获得沉淀取出后用去离子水和乙醇分别洗涤3~5次,将获得的产物在40~50℃下干燥7-12h,即得形貌可控的SnS材料。
所述硫源为Na2S•9H2O、硫代乙酰胺、硫代乙醇酸、硫脲、硫代硫酸钠、硫化胺中的一种。
所述表面活性剂为十六烷基三甲基溴化铵、聚乙烯吡咯烷酮、十二烷基苯磺酸钠中的一种。
所述溶剂为乙二醇、乙二胺、乙醇、蒸馏水中的一种。
本发明另一目的是提供上述硫化锡材料的新用途,即在作为光催化材料中的应用。
用X-射线衍射(XRD)检测产品,可以证明该产物为纯的SnS。用能谱分析(EDS)检测产品,可以证明该产物的Sn2+和S2-的摩尔比接近于1。用扫描电镜(SEM)及透射电镜(TEM)检测产品,可以证明该产物为形貌和晶粒大小可控的SnS。
与现有的技术相比,本发明具有如下优点:
(1)本发明提出了一种简单有效的SnS材料控制合成思路,其特点是反应条件温和、方法简单、成本较低;
(2)本发明提出的形貌可控的SnS的简单有效制备方法;
(3)本发明所采用的原料环境友好、工艺简单、易于工业化生产;
(4)本发明合成的产品,较其他光催化剂具有较高的光催化活性,作为光催化材料具有较好的工业应用前景。
附图说明
图1是实施例3所制备的SnS X-射线衍射(XRD)图;
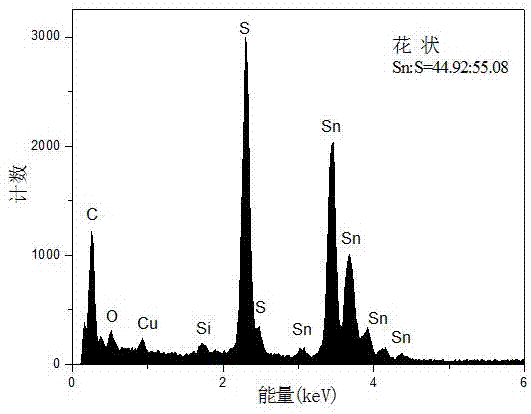
图2是实施例3所制备的SnS能谱(EDS)图;
图3是实施例1所制备的SnS扫描电镜(SEM)图(A图)及透射电镜(TEM)图(B图);
图4是实施例2所制备的SnS扫描电镜(SEM)图(A图)及透射电镜(TEM)图(B图);
图5是实施例3所制备的SnS扫描电镜(SEM)图(A图)及透射电镜(TEM)图(B图);
图6是实施例4所制备的SnS扫描电镜(SEM)图(A图)及透射电镜(TEM)图(B图);
图7是实施例5所制备的SnS扫描电镜(SEM)图(A图)及透射电镜(TEM)图(B图);
图8是实施例6的光催化降解Rh B的C/C0-时间图;
图9是实施例6的光催化降解Rh B、MO、MB、MG的C/C0-时间图。
具体实施方式
下面通过附图和实施例对本发明作进一步详细说明,但本发明的保护范围不局限于所述内容。
实施例1:
(1)首先将8mmol SnCl2·2H2O和16mmol Na2S•9H2O分别溶解于40mL和20mL溶剂中,分别超声至溶解,其次将0.9026g聚乙烯吡咯烷酮加入到20mL溶剂中,超声至溶解;
(2)将上述SnCl2·2H2O溶液、Na2S•9H2O溶液、聚乙烯吡咯烷酮溶液依次滴加入到水热反应釜(150mL)中,并加入20 mL溶剂,磁力搅拌20min后,将水热反应釜温度设置在160℃下进行反应,反应时间24h;
(3)将步骤(2)中获得沉淀取出后用去离子水和乙醇分别洗涤3次,直至滤液澄清;将获得的产物在50℃下干燥12h,即得形貌可控的SnS 纳米棒,纳米棒的平均直径为25~100 nm,长度大约为1 μm,如图3所示。
实施例2:
(1)首先将8mmol SnCl2·2H2O和8mmol硫脲分别溶解于40mL和20mL溶剂中,分别超声至溶解;其次将0.9026g聚乙烯吡咯烷酮加入到20mL溶剂中,超声至溶解;
(2)将上述溶液依次滴加入到水热反应釜(150mL)中,并加入20 mL溶剂,在磁力搅拌15min后,将水热反应釜温度设置在120℃下进行反应,反应时间17h;
(3)将步骤(2)中获得沉淀取出后用去离子水和乙醇分别洗涤4次,直至滤液澄清,将获得的产物在45℃下干燥12h,即得形貌可控的杆状SnS,杆状SnS的平均直径大约为1 μm,长度大约为4.5~5 μm,如图4所示;图8显示,纳米棒的粒径较小,其相对杆状SnS的催化活性较好。
实施例3:
(1)首先将3mmol SnCl2·2H2O和12mmol硫代乙酰胺TAA分别溶解于40mL和20mL溶剂中,分别超声至溶解;其次将0.6770g十六烷基三甲基溴化铵加入到20mL溶剂中,超声至溶解;
(2)将上述溶液依次滴加入到水热反应釜(150mL)中,并加入20 mL溶剂,在磁力搅拌10min后,将水热反应釜温度设置在120℃下进行反应,反应时间24h;
(3)将步骤(2)中获得沉淀取出后用去离子水和乙醇分别洗涤5次,直至滤液澄;将获得的产物在40℃下干燥12h,即得形貌可控的花状SnS,其平均直径大约为600 nm,如图1、2、5所示,从图中可看出制备得到的SnS材料与标准卡片一致,其晶格参数为:a=11.19 Å, b=3.98 Å, c=4.33 Å (JCPDS card No.75-2115),并且Sn2+和S2-的摩尔比为44.92:55.08,接近于1,证明其为p型半导体,花状SnS的平均直径大约为600 nm。
实施例4:
(1)首先将2mmol SnCl2·2H2O和6mmol硫代乙酰胺(TAA)分别溶解于40mL和20mL溶剂中,分别超声至溶解,其次将0.6770g聚乙烯吡咯烷酮加入到20mL溶剂中,超声至溶解;
(2)将上述溶液依次滴加入到水热反应釜(150mL)中,并加入20 mL溶剂,在磁力搅拌20min后,将水热反应釜温度设置在150℃下进行反应,反应时间24h;
(3)将步骤(2)中获得沉淀取出后用去离子水和乙醇分别洗涤3次,直至滤液澄清;将获得的产物在45℃下干燥10h,即得形貌可控的花状SnS,其平均直径大约为1.2~1.5 μm,如图6所示。
实施例5:
(1)首先将1mmol SnCl2·2H2O和1mmol TAA分别溶解于40mL和20mL溶剂中,分别超声至溶解,其次将0.6770g十二烷基苯磺酸钠加入到20mL溶剂中,超声至溶解;
(2)将上述溶液依次滴加入到水热反应釜(150mL)中,并加入20 mL溶剂,在磁力搅拌20min后,将水热反应釜温度设置在160℃下进行反应,反应时间10h;
(3)将步骤(2)中获得沉淀取出后用去离子水和乙醇分别洗涤5次,直至滤液澄清,将获得的产物在50℃下干燥12h,即得形貌可控的树枝状SnS,如图7所示。
实施例6:
污染物的降解是在可见光照射水溶液中进行的,光源为500 W Xe灯。取实施例1-5制备得到的硫化锡材料各20mg,分别倒入Rh B浓度为1×10-5mol/L的水溶液中(50mL);同时取实施例3中的4份硫化锡材料各10mg,分别倒入浓度均为3mg/L的MB、MG、Rh B和MO的50mL溶液中。反应前,材料样品在避光条件下搅拌1h,以达到吸附-脱附平衡。光照开始后,每隔60min取反应液样品4mL,并用滤膜去除催化剂,滤液通过紫外可见分光光度计在200-700nm范围内测定吸光度。Rh B的特征吸收波长为553nm,MB的特征吸收波长为665nm,MO的特征吸收波长为463nm,MG的特征吸收波长为618nm。降解率=((C0-C))/C0) × 100,C0是初始浓度,C是每隔一段时间取样的浓度。C/C0-时间图如图8,9所示。
从图8可以看出,光催化降解Rh B的催化活性为花状>树枝状>棒状,并且粒径相对较小对催化活性更有利。对于实施例3制备得到的花状SnS,在反应时间为60min时间内,就已经全部降解,比已报道的用其他方法制备得到的SnS光催化活性要高出许多,例如:Hu等人采用一步裂解法制备得到了SnS光催化材料,用1g/L SnS降解1×10-5mol/L Rh B,在暗反应60min内,只有50%Rh B被吸附,而在随后的光照条件下,基本没什么降解发生。
从图9可以看出,实施例3制备得到的10mg SnS催化剂用于降解浓度分别为3mg/L MO,3mg/L Rh B,3mg/L MG 和 3mg/L MB的底物,得到在120min时间照射内各拟一级反应速率常数分别为:MB :k=3.2 × 10-2 min-1;MG : k=2.9 × 10-2 min-1;Rh B : k=2.4× 10-2min-1;MO : k=2.2× 10-2 min-1,相比其他可见光光催化剂有明显的提高。例如:Chen等人采用溶胶-凝胶水热法制备得到的80mg Bi4Ti3O12,光催化降解6ppm Rh B的拟一级反应常数为0.0211min-1;Li等人合成得到的50mg Cu2O,光催化降解10mg/L的MO,7小时后降解率才达到80%左右;Chen等人通过煅烧含Zn前驱体得到了ZnO纳米片,将15mg ZnO纳米片光催化剂用于降解5×10-5mol/L MO,拟一级反应速率常数为0.81h-1;Yuan等人合成了3D花状SnS2-MgFe2O4/rGO光催化材料,用于降解MB,其拟一级反应速率常数为0.0085min-1。
以上列举的仅是本发明的具体实施例。显然本发明不限于以上实施例,还可以有许多变化。在纳米材料和介孔材料等的形貌控制领域的普通技术人员能从本发明公开的内容直接导出或联想到的所有变化,如表面活性剂可以是聚乙二醇、季铵化合物、硬脂酸等。硫源还可以是硫代硫酸钠、硫化胺等。溶剂还可以是甲醇等。均应认为是本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!