一种基于磷酸钙-PEG的质粒转染的方法与流程
本发明属于生物技术领域,具体地说,本发明涉及一种基于磷酸钙-PEG的质粒转染的方法。
背景技术:
磷酸钙法转染法是实验室广泛使用一种转染哺乳动物细胞的方法。DNA与磷酸钙形成复合物,粘附到细胞表面,通过细胞内吞作用将DNA摄入细胞内。它具有方便,廉价,细胞毒性小等优点,同时也存在明显局限性。磷酸钙转染法操作时受到多种因素的影响,使得转染效率非常不稳定,不同的实验室选择用磷酸钙转染法时通常需要花很大精力优化转染体系,费时费力。
聚乙二醇(polyethylene glycol,PEG)在医药化工领域广泛使用一种辅料,在实验中常用于做细胞融合,原生质体转染。4%-6%的PEG溶液能促进微粒之间的聚合,增强微粒的稳定性。
技术实现要素:
本发明的目的在于提供一种基于磷酸钙-PEG的质粒转染的方法。本发明人意外地发现,使用PEG能够增强DNA-磷酸钙复合物形成的稳定性,提高磷酸钙转染法的转染效率。
本发明的第一方面提供了一种基于磷酸钙-PEG的质粒转染方法,所述方法包括步骤:
(1)配制PEG-DNA溶液
在1ml 2%-6%(w/v)的PEG溶液中加入5-15μg质粒DNA(待转染质粒),混匀制得PEG-DNA溶液;
(2)PEG-DNA氯化钙溶液配制
1ml PEG-DNA溶液中加入40-80μl 2M CaCl2溶液,配制成PEG-DNA氯化钙溶液。
(3)PEG‐磷酸钙转染复合物配制
在离心管中加入1ml 2×HBS溶液,逐滴加入所述PEG-DNA氯化钙溶液,配制成PEG-磷酸钙转染复合物;
(4)细胞转染
将转染复合物加入细胞培养物中,转染复合物与培养基体积为1:5-15,进行细胞转染。
优选的,步骤(1)中,PEG溶液的浓度(w/v)为3%-4%。
优选的,步骤(1)中,加入10μg质粒DNA。
优选的,步骤(2)中,加入60μl 2M CaCl2溶液。
优选的,步骤(3)中,HBS溶液和PEG-DNA氯化钙溶液的体积比为1-3:3-1。
优选的,步骤(4)中,转染复合物与培养基比率为1:10。
本发明的基于磷酸钙-PEG的质粒转染方法,具有极高的转染效率,而且转染稳定性良好。
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
附图说明
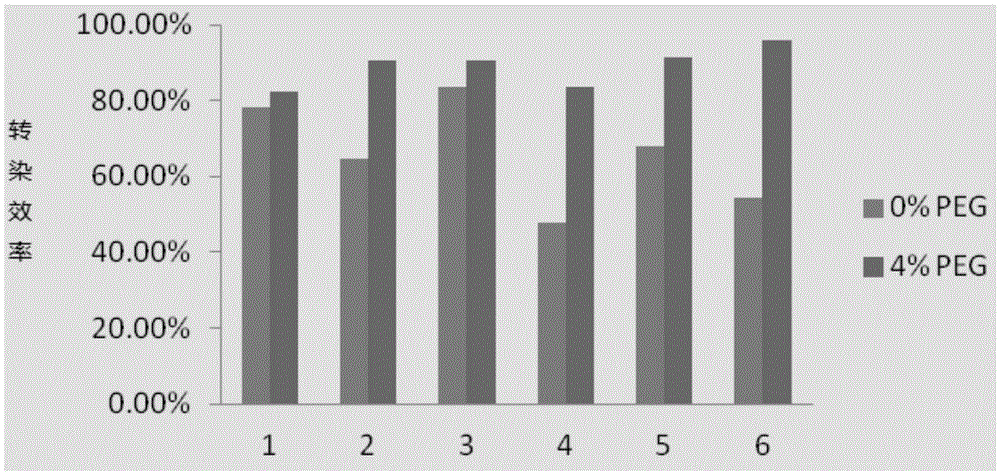
图1显示了PEG浓度对转染效率的影响,n=5。
图2显示了PEG-磷酸钙不同批次实验转染稳定性。
图3显示了PEG-磷酸钙转染复合物室温放置不同时间后的转染效率。
图4显示了不同培养器皿对PEG-磷酸钙转染复合物的转染效率的影响。
图5显示了PEG-磷酸钙转染不同质粒DNA的转染效率。
具体实施方式
下面结合具体实施例,进一步陈述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明详细条件的实验方法,通常按照常规条件如美国Sambrook.J等著《分子克隆实验室指南》(黄培堂等译,北京:科学出版社,2002年)中所述的条件,或按照制造厂商所建 议的条件。除非另外说明,否则百分比和份数按重量计算。以下实施例中所用的实验材料和试剂如无特别说明均可从市售渠道获得。
实施例1
1.主要实验材料
2M CaCl2溶液:称取23.96g无水氯化钙,加入80ml超纯水溶解,冷却到室温,定容至100ml,0.22μm滤膜过滤后,4℃保存备用。
2×HBS溶液:称取NaCl 16.3g,KCl 0.74g,Na2HPO40.214g,Glucose 2.4g,HEPES 10g,加入900ml超纯水溶解,调整pH值至7.05,定容至1000ml,0.22μm滤膜过滤后,4℃保存备用。
12%PEG溶液:称取12g PEG4000,加入80ml超纯水溶解,定容至100ml,0.22μm滤膜过滤后,4℃保存备用。
转染用质粒DNA:pEGFP‐N1(4.7kb),pcDNA3.1‐EGFP(6.1kb),pLVX‐ZsGreen1‐C1(8.7kb),均可购自上海麒盟生物科技有限公司。
转染细胞系:293T细胞,可购自上海麒盟生物科技有限公司。
2.PEG‐磷酸钙转染复合物配制
2.1 PEG-DNA溶液配制
将12%PEG溶液用无菌水稀释至所需浓度,1ml PEG溶液中加入10μg质粒DNA,混匀。
不同浓度PEG溶液配制见表1
表1不同浓度PEG配制
2.2 PEG‐DNA氯化钙溶液配制
1ml PEG-DNA溶液加入60μl 2M CaCl2溶液,配制成PEG-DNA氯化钙溶液。
2.3 PEG‐磷酸钙转染复合物配制
在15ml离心管中加入1ml 2×HBS溶液,离心管置于涡旋振荡器上,用1ml移液器逐滴加入PEG‐DNA氯化钙溶液,配制成PEG‐磷酸钙转染复合物。
2.4转染细胞
将转染复合物加入细胞培养物中,转染复合物与培养基比率为1:10。混匀后放入培养箱继续培养。不同培养板(瓶)中加入的转染复合物参考表2。
表2不同培养皿(瓶)加入转染复合物参考值
3.检测转染效率
转染24后用流式细胞术检测转染效率。
4.实验结果
4.1不同浓度PEG对转染效率的影响
PEG浓度的从1%增加到4%转染效率有显著提升,转染效率提高了20%以上,PEG浓度从4%增加到6%对转染效率基本没有影响。
4.2 PEG-磷酸钙转染复合物转染稳定性检测
4.2.1不同批次配制试剂稳定性检测
在不同时间配制2M CaCl2溶液和2×HBS溶液,12%PEG溶液,在不同时间内做转染,检测PEG-磷酸钙转染的稳定性。磷酸钙转染法在不同批次实验中转染率在40%~90%,转染稳定性不好。在含有4%PEG的PEG-磷酸钙转染复合物转染稳定性有明显提升,转染效率在6重复实验中都没有低于80%。
4.2.2转染复合物时间稳定性
转染复合物配制完成后,在室温条件下放置不同时间,检测转染复合物的时间稳定性。实验结果显示PEG-磷酸钙转染复合物能在室温放置1h,对转染效率没有影响。
4.3不同培养器皿的影响
实验检测PEG-磷酸钙转染复合物在不同细胞培养器皿中对转染效率的影响,结果显示,对于常用几种型号的培养器皿,PEG-磷酸钙转染复合物的转染效率没有显著差异。
4.4不同质粒对转染的影响
实验检测几种不同大小质粒DNA使用PEG-磷酸钙转染方法,结果显示,质粒DNA的大小对于PEG-磷酸钙转染复合物的转染效率没有影响。
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
-
 0访客 来自[江苏省常州市电信] 2019年03月06日 14:40质粒转染除了磷酸钙法转染法,还可以使用DeofectEU Transfection Reagent,采用生物可降解材料,细胞毒性低;培养基可含或不含血清,可以用PBS或无血清培养基稀释质粒;结果重复性好,转染过程不需换液;适用范围广,可用于多种真核细胞。
0访客 来自[江苏省常州市电信] 2019年03月06日 14:40质粒转染除了磷酸钙法转染法,还可以使用DeofectEU Transfection Reagent,采用生物可降解材料,细胞毒性低;培养基可含或不含血清,可以用PBS或无血清培养基稀释质粒;结果重复性好,转染过程不需换液;适用范围广,可用于多种真核细胞。