肿瘤标志物的组合检测方法及其应用与流程
本发明涉及基因检测,尤其涉及将基因肿瘤标识物与蛋白质肿瘤标志物相结合用于疾病的体外辅助诊断的肿瘤标志物的组合检测方法及其应用。
背景技术:
癌症是全球主要的死亡原因之一:2004年,全球癌症死亡人数达740万(约占所有死亡人数的13%),全球癌症死亡人数将继续增加,2030年,死亡人数预计将达1200万。全世界2005年至2015年期间有8400万人左右死于癌症,每年导致癌症总死亡率的主要癌症种类为:肺癌(130万)、胃癌(80.3万)、结肠癌(63.9万)、肝癌(61万)和乳癌(51.9万)。2015年美国共有170万新发癌症病例。2015年预估中国每年新发癌症病例约为429.16万例,死亡281.42万例,占新发病例65.6%。2015年预估中国每年新发癌症病例的主要癌症种类为肺癌(73.33万)、胃癌(67.91万)、食管癌(47.79万)、肝癌(46.61万)、结直肠癌(37.63万)和乳癌(27.24万)。2015年预估中国每年导致癌症总死亡率的主要癌症种类为:肺癌(61.02万)、胃癌(49.80万)、肝癌(42.2万)、食管癌(37.5万)、结直肠癌(19.1万)、胰腺癌(7.94万)、和乳癌(7.07万死亡)。
肿瘤是一种全身性疾病,几乎可以发生在身体的所有部位,肿瘤包括恶性肿瘤和良性肿瘤,恶性肿瘤中大多数是癌症。目前危害人类的主要肿瘤有肺癌、胃癌、肝癌、结直肠癌、乳腺癌和食道癌,其他常见的肿瘤有子宫颈癌、前列腺癌、膀胱癌、胰腺癌、甲状腺癌、淋巴瘤,子宫体癌、卵巢癌和脑瘤等。全世界最常见的癌症种类(按全球死亡人数排序)为:男性:肺癌、胃癌、肝癌、结肠直肠癌、食道癌和前列腺癌。女性:乳癌、肺癌、胃癌、结肠直肠癌和子宫颈癌。中国的排序略有不同,2015年中国男性五种最常见肿瘤依次肺癌、胃癌、食管癌、肝癌和结直肠癌,这五种癌占所有癌症病例的2/3。女性最常见肿瘤依次乳腺癌、肺癌、胃癌、结直肠癌和食管癌,占所有癌症病例的60%。2015年中国主要癌症的总死亡人数排序为肺癌(21.68%)、胃癌(17.7%)、肝癌(15.0%)、食道癌(13.33%)、结肠直肠癌(6.79%)、胰腺癌(2.82))和乳腺癌(2.51%)。
人类经过和肿瘤的艰苦和漫长博弈,认识到对iii-iv期的晚期肿瘤来说,即使经过各种复杂的手术治疗、化学治疗、放射治疗、免疫治疗、基因治疗、靶向治疗等,5年存活率只有5-15%;而对i-ii期的早期肿瘤,5年存活率可达80-90%,癌前病变或称0期癌或原位癌的治疗效果更好。所以,近年来业界的共识是要早期发现和早期干预肿瘤,这才是解决肿瘤的根本措施。临床研究发现,多数癌症从病灶开始形成,到患者出现临床症状的过程平均需要数年时间,这为发现早期癌症、提高早期癌症的确诊率提供了一个有效的窗口期。因此,充分利用这个窗口期,研发灵敏、准确、无创、方便的早期癌症的检测和检查技术,提高早期癌症的发现率,是改善癌症治疗效果、降低癌症死亡率的重要途径。
遗憾的是在肿瘤早期检查或癌前病变的检查中,由于没有明显的受检者的主诉、临床症状和体征,难以针对性的选择相应的临床辅助检查如x-线透视、ct、mri、超声波、或腔镜检查。这些传统方法由于检测技术的限制,对早期癌症的灵敏性和特异性低,例如低剂量螺旋ct检测肺癌的假阳性率高,提高了过度治疗的风险,并且操作复杂、侵入性强(如:肠镜、胃镜等)。检测成本高(如:ct、mri需要昂贵的设备和专业培训的技术人员)是用于肿瘤早期检查的明显障碍,而且仅对单一癌症进行检测,不适用于多种癌症的早期检查。在众多的检测方法中,人们很难选择出有针对性的检测方法来早期的检测某出某一种肿瘤,同时能排除其他肿瘤的可能性。由于受检者都是没有症状的大量的正常(无病)人群,对受检者来说,肿瘤检测要采样方便,样品需求量少,对受检者没有痛苦和伤害,价格适当,容易被受检者接受。对施行肿瘤检测的机构来说,检测方法要简单快速,对检测设备、场地和人员的没有过分要求,容易实现。这就需要一种从检测技术上具有特异、广谱、灵敏和能从血液中检测早期癌症的方法,从普及施行上简易、方便和减少受检者负担的检测方法。
传统的蛋白质肿瘤标志物已经广为使用,但对多种肿瘤精准的早期检测尚不尽人意。甲胎蛋白(α-fetoprotein,αfp或afp)是一个特异性较强的蛋白质肿瘤标志物,可以在大约80%的肝癌患者血清中升高,而且随着病情恶化它在血清中的含量会急剧增加,一直认为是诊断原发性肝癌的特异性肿瘤标志物,具有确立诊断、早期诊断、鉴别诊断的作用。但该检测只能检测原发性肝癌,对其他癌症则检测效果有限,单独使用特异性较强的肿瘤标志物,如甲胎蛋白检测,就会漏掉上述其他的癌症。
为了不漏掉其他肿瘤,可以采用广谱性肿瘤标志物来检测早期肿瘤。癌胚抗原(carcino-embryonicantigen,cea)是一个广谱性肿瘤标志物,除原发性结肠癌、乳腺癌和肺癌以外,胰腺癌、胆管癌、胃癌、食管癌、粘液腺癌和泌尿系统的肿瘤阳性率也升高,它能向人们反映出多种肿瘤的存在,对结直肠癌、乳腺癌和肺癌的疗效判断、病情发展、监测和预后估计是一个较好的肿瘤标志物,但业界公认的是其特异性不强,灵敏度不高,对肿瘤早期诊断作用不明显。
为了兼顾广谱性、特异性、灵敏性和能从血液中检测早期癌症这些技术要求,相比甲胎蛋白和癌胚抗原这些传统的蛋白质肿瘤标志物来说,检测核酸肿瘤标志物被公认为符合上述技术要求。尤其能从血液中检测到肿瘤释放出的dna,起到液体活检(liquidbiopsy)的作用。常用的核酸检测技术有固相芯片、液相芯片、实时定量pcr(polymerasechainreaction)、数字pcr、sangerdna测序和高通量dna测序(“next-generation”sequencing)等。上述这些核酸检测方法中,以高通量dna测序最符合兼顾广谱性、特异性、灵敏性和能从血液中检测早期癌症这些技术要求,高通量测序技术是对传统测序一次革命性的改变,一次对几十万到几百万条dna分子进行序列测定,使得对一个肿瘤的转录组和基因组进行细致全貌的分析成为可能。但高通量dna测序对检测设备、场地和人员的有很高的要求,不容易实现,不符合对检测方法的简易和方便的要求。目前高通量dna测序价格偏贵,对受检者形成负担,不一定适合没有症状的大量的正常(无病)受检者。
实时定量pcr除兼顾广谱性、特异性、灵敏性和能从血液中检测早期癌症这些技术要求外,还在施行肿瘤检测的机构中有广泛普及,价格合适,不会对受检者形成负担,适合没有症状的大量的正常(无病)受检者。除了合适的技术平台外,能兼顾广谱性、特异性、灵敏性和能从血液中检测早期癌症这些技术要求核酸肿瘤标志物更为重要。
技术实现要素:
基于上述背景技术,本发明的目的在于提供一种通过综合分析基因甲基化谱(methylome)和蛋白质肿瘤标志物数据,用于疾病的体外辅助诊断的肿瘤标志物的组合检测方法。
本发明提供了一种肿瘤标志物的组合检测方法,所述方法包括:
1)提供来自检查对象的样本,优选地,所述检查对象为人;
2)对步骤1)所述的样本进行检测,所述检测为测定septin9基因是否存在甲基化以及测定蛋白质肿瘤标志物是否存在;
其中,所述样本选自细胞系、组织学切片、组织活检/石蜡包埋的组织、体液、粪便、结肠流出物、尿、血浆、血清、全血、分离的血细胞;从血液中分离的细胞、体液、痰液、咽拭子,或其组合;优选地选自结肠流出物、尿、血浆、血清、全血、分离的血细胞、从血液中分离的细胞中的一种或多种;
所述蛋白质肿瘤标志物选自脑癌、胃癌、肝癌、食管癌、宫颈癌、甲状腺癌、淋巴癌、膀胱癌、白血病、肾癌、胰腺癌、结直肠癌、肺癌、乳腺癌、卵巢癌、前列腺癌或子宫癌的蛋白质肿瘤标志物中的一种或多种。
在根据本发明的一个实施方案中,步骤2)中所述septin9基因甲基化的测定是通过实时定量pcr实现的。
在根据本发明的一个实施方案中,所述实时定量pcr的上游引物序列为seqidno:1;下游引物序列为seqidno:2;阻断剂序列为seqidno:3;探针序列为seqidno:4和seqidno:5;优选地,所述实时定量pcr以actb为内对照基因;更优选地,所述actb的上游引物序列为seqidno:6;下游引物序列为seqidno:7;探针序列为seqidno:8;进一步优选地,所述实时定量pcr的反应程序为:阶段1:一个循环94℃,20分钟;阶段2:45个循环,62℃,5秒,55.5℃,35秒,93℃,30秒;阶段3:40℃,5秒。
在根据本发明的一个实施方案中,步骤2)中所述蛋白质肿瘤标志物的测定方法选自液态芯片、固态芯片、酶联免疫、放射免疫、化学发光免疫、质谱、高效液相层析、western印记和序列分析中的一种或多种。
在根据本发明的一个实施方案中,所述蛋白质肿瘤标志物选自癌胚抗原(carcino-embryonicantigencea)、大便中血红蛋白、mg7、idh1、ca199、甲胎蛋白(afp)、ca125、ca72-4、ca242、ca50、cyfra21-1、psa、fpsa/tpsa、nse、scc、progrp、pg、pgi/pgii、tpa、tps、ca153、β-hcg、sf、h3k4me1、h3k4me3、h4k8ac、auto-abp53中的一种或多种。
在根据本发明的一个实施方案中,所述蛋白质肿瘤标志物选自癌胚抗原(carcino-embryonicantigencea)、大便中血红蛋白、ca724、甲胎蛋白、ca242、ca199、cyfra21-1、ca153、ca125、psa和β-hcg中的一种或多种。
在根据本发明的一个实施方案中,所述蛋白质肿瘤标志物为癌胚抗原、大便中血红蛋白、ca724、甲胎蛋白、ca242和ca199。
在根据本发明的一个实施方案中,所述蛋白质肿瘤标志物为癌胚抗原、大便中血红蛋白、ca724、甲胎蛋白、ca242、ca199、cyfra21-1、ca153、ca125、psa和β-hcg。
在根据本发明的一个实施方案中,所述方法还包括测定辅助核酸肿瘤标志物,所述辅助核酸肿瘤标志物选自kras、braf、egfr、rnf180、shox2、ptger4、foxl2、gng4、c1orf70、c9orf50、ctsf、cyp1b1、rnf135、hoxd8、cyba、sim1、c7orf51、arrdc2、gabrg3、rnls、pax2、proc、pitpnm3、hoxxd10、lyplal1、hsa-mir-122、hsa-let-7b中的一种或多种;所述辅助核酸肿瘤标志物的测定方法包括pcr、实时定量pcr、数字pcr、液态芯片、固态芯片、原位杂交、普通测序和高通量测序中的一种或多种。
本发明还提供了一种用于上述检测方法的试剂盒,所述试剂盒包含用于通过实时定量pcr测定septin9基因甲基化的所需要引物、探针和试剂,以及测定蛋白质肿瘤标志物的方法所需要的试剂。
在根据本发明的一个实施方案中,所述蛋白质肿瘤标志物选自癌胚抗原、大便中血红蛋白、ca724、甲胎蛋白、ca242、ca199、cyfra21-1、ca153、ca125、psa和β-hcg中的一种或多种。
在根据本发明的一个实施方案中,所述测定蛋白质肿瘤标志物的方法选自液态芯片、固态芯片、酶联免疫、放射免疫、化学发光免疫、质谱、高效液相层析、western印记和序列分析中的一种或多种。
一方面,本发明具有以下有益效果:
本发明将不同的肿瘤标志物形成组合检测,用以提高肿瘤早期检测的灵敏性。将血浆中septin9基因甲基化检测和大便中血红蛋白检测组合,或和血清中cea的检测组合,检测结直肠癌的灵敏性可以分别提高17%或11%,检测早期结直肠癌的灵敏性提高20%。将血浆中septin9基因甲基化检测和血浆中rnf180基因甲基化检测组合,检测胃癌的灵敏性可以提高18%,检测早期胃癌的灵敏性提高10%。
另一个方面,本发明提供了一种综合性分析判读方法和应用。由于本发明是对早期肿瘤进行检测,受检者大多是是无症状人群,采集和参考受检者的临床信息,包括问卷,主诉、症状、体征、年龄、性别、体重、抽烟历史,家族史,传染病史,糖尿病史等可以对组合性检测结果提供导向性线索,提供给综合性分析判读方法和应用。
在分析检测结果时,要根据本发明中对多种肿瘤的组合性检测的结果,参考受检者的临床信息和其他临床辅助检验结果,对肿瘤检测结果进行综合性分析和判读。这些就构成了本发明的对多种肿瘤精准的组合性检测和综合性分析判读方法和应用。
本发明提供了一种简易、方便和减少受检者负担的对多种肿瘤精准的组合性检测和综合性分析判读方法,应用于对多种肿瘤的临床检测、高危人群筛查和普通人群的普查。其中所述组合性检测包括对受检者进行septin9基因甲基化的测定、进行多种肿瘤标志物的测定、和进行使用医疗器械及设备对受检者的检查。其中所述综合性分析判读方法包括综合受检者的临床问卷、家族史、临床主诉、临床症状、临床体征、septin9基因甲基化的测定结果、多种肿瘤标志物的测定结果、和使用医疗器械及设备对受检者的检查结果进行综合分析。通过本发明的方法,可以实现一次采取受检者样品,通过组合性检测和综合性分析判读方法,对受检者进行多种肿瘤精准的测定。
本发明提出的用实时定量pcr检测septin9基因甲基化除兼顾广谱性、灵敏性和能从血液中检测早期癌症这些特征外,septin9基因甲基化对结直肠癌具备一定的特异性。许多肿瘤都有septin9基因甲基化,是一个相对广谱的肿瘤标志物,septin9基因甲基化发生在各种癌症的早期阶段,可以用实时定量pcr从血液中检测到早期癌症。目前已经从许多癌症患者的血浆中测到septin9基因甲基化,包括结直肠癌、胃癌、肺癌、肝癌、贲门癌、胰腺癌和食道癌,为了鉴别是那些癌症导致septin9基因甲基化,可以加上一些具有一定特异性的蛋白质肿瘤标志物,如癌胚抗原(结直肠癌),大便中血红蛋白(结直肠癌),ca724(胃癌),cyfra21-1(肺癌),和甲胎蛋白的(肝癌)来鉴别肿瘤的来源。这些蛋白质肿瘤标志物检测可以用免疫的方法来测定,如酶联免疫吸附(enzyme-linkedimmunosorbentassayelisa)的方法,该方法相对简易和费用低廉,在施行肿瘤检测的机构中有广泛普及,对受检者的负担也很低。因此,用实时定量pcr从血液中检测septin9基因甲基化,加上一些具有一定特异性的蛋白质肿瘤标志物的免疫学方法检测,就形成了本发明中对多种肿瘤的组合性检测。
在本发明的基础上还可以进一步采集和参考受检者的临床信息,包括问卷,主诉、症状、体征、年龄、性别、体重、抽烟历史,家族史,传染病史,糖尿病史等,或者采集和参考其他临床辅助检验结果,如影像学和腔镜的检查结果以进一步判断癌症产生的风险。在分析检测结果时,要根据本发明中对多种肿瘤的组合性检测的结果,参考受检者的临床信息和其他临床辅助检验结果,对肿瘤检测结果进行综合性分析和判读。这些就构成了本发明的对多种肿瘤精准的组合性检测和综合性分析判读方法和应用。
附图说明
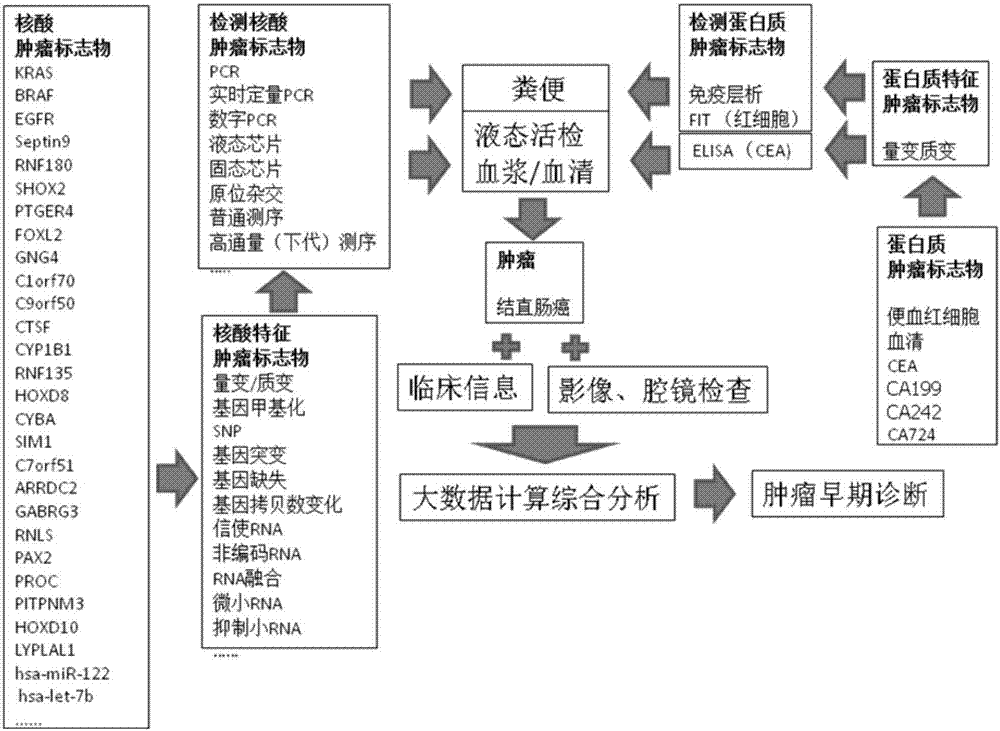
图1为对多种肿瘤精准的组合性检测和综合性分析判读方法和应用的框架图。
图2为本发明在结直肠癌联检时对多种肿瘤标志物的精准组合性检测和综合性分析判读方法和应用。
图3为多种肿瘤的septin9基因甲基化和蛋白质肿瘤标志物的阳性率和特异性。
具体实施方式
下面结合实施例进一步说明本发明,应当理解,实施例仅用于进一步说明和阐释本发明,并非用于限制本发明。
除非特别指明,本发明所使用的试剂和材料均可通过商业途径获得。
除非另有说明,本申请的实施将采用常规的分子生物学(包括重组技术)、微生物学、细胞生物学、生物化学和基因学技术,其均在本领域常规技术手段的范围内。在文献中对此类技术进行了详细说明如molecularcloning:alaboratorymanual,第二版(sambrook等,1989);oligonucleotidesynthesis(m.j.gait,1984版);animalcellculture(r.i.freshney,1987版);methodsinenzymology丛书(美国学术出版社有限公司);currentprotocolsinmolecularbiology(f.m.ausubel等,1987版,和定期更新);pcr:thepolymerasechainreaction(mullis等,1994版)。本申请中使用的引物、探针和试剂盒可以采用本领域公知的标准技术制备。
除非另有定义,本申请所使用的技术和科学术语与本发明所属领域的普通技术人员的通常理解具有相同的含义。singleton等,dictionaryofmicrobiologyandmolecularbiology,第二版,j.wiley&sons(newyork,n.y.1994),和march,advancedorganicchemistryreactions,mechanismsandstructure,第四版,johnwiley&sons(newyork,n.y.1992),针对本申请中使用的多个术语为本领域技术人员提供了一般性的指导。
定义
本申请的“癌症”表示并包括任何恶性肿瘤(malignancy)、或恶性细胞分裂或恶性肿瘤(malignanttumour),或具有不受控制的或不适当的细胞增殖的任何疾病状态,并且包括但不限于特征为不受控制的或不适当的细胞增殖的任何疾病。
本申请的“肺癌(lungcancer)”,是一种肺部的恶性肿瘤,特征为肺部组织中的细胞不受控制地生长。肺癌主要分为小细胞肺癌(small-celllungcarcinoma,sclc)和非小细胞肺癌(non-small-celllungcarcinoma,nsclc)。
本申请的“肺癌细胞”表示具有肺癌特征的细胞,并且包括癌症前期细胞。
本申请的“癌症前期”表示处于转化为癌细胞的早期阶段或倾向于转化为癌细胞的细胞。这样的细胞可以表现出一种或多种具有癌细胞特征的表型性状。
本申请中的“核酸”、“核酸序列”等等指的是聚核苷酸,可以是gdna、cdna或rna,也可以是单链或双链的。术语也包括肽核酸(pna),或任何化学的dna类或rna类物质。“cdna”指的是从天然生成的mrna复制的dna。“gdna”指的是基因组dna。也可以使这些物质的组合(即部分是gdna和部分是cdna的重组核酸)。
本申请的“dna甲基化”是指甲基添加到胞嘧啶(c)的5位,这通常(但不必须)是在cpg(胞嘧啶之后为鸟嘌呤)二核苷酸的情况下。本文所用的“增加的甲基化程度”或“显著的甲基化程度”是指dna序列中至少存在一个甲基化的c核苷酸,其中正常对照样品(例如从非癌细胞或组织样品提取的dna样品或对dna残基的甲基化进行处理的dna样品)中的对应c是非甲基化的,在某些实施方案中,至少2、3、4、5、6、7、8、9、10或更多个c可以是甲基化的,其中对照dna样品中的这些位置的c是非甲基化的。
在实施方案中,多种不同的方法可用于检测dna甲基化改变。检测dna甲基化的方法包括,例如,利用southern或聚合酶链反应(pcr)分析的甲基化敏感的限制性内切核酸酶(msre)测定、甲基化特异性或甲基化敏感的pcr(ms-pcr)、甲基化敏感的单核苷酸引物延伸(ms-snupe)、高分辨率熔解(hrm)分析、重亚硫酸盐测序、焦磷酸测序、甲基化特异性单链构象分析(ms-ssca)、组合重亚硫酸盐限制分析(cobra)、甲基化特异性变性梯度凝胶电泳(ms-dgge)、甲基化特异性熔解曲线分析(ms-mca)、甲基化特异性变性高效液相色谱(ms-dhplc)、甲基化特异性微阵列(mso)。这些测定可以是pcr分析、利用荧光标记的定量分析或southern印记分析。
本申请的“甲基化测定”指确定dna序列内一个或多个cpg二核苷酸序列的甲基化状态的任何测定。
本申请的“生物样品”或“样品”包括诸如活检和尸检样品的组织切片、和为了组织学目的而获取的冷冻切片、或任何这些样品的处理后形式。生物样品包括血液和血液组分或产物(例如血清、血浆、血小板、红细胞等),痰液或唾液,淋巴和舌组织,诸如原代培养物、外植体和转化的细胞的培养的细胞,粪便,尿液,胃活检组织等。生物样品通常获自真核生物,所述真核生物可以是哺乳动物,可以是灵长类并且可以是人类个体。
本申请的“检测”表示观察生物样品中的标志物或标志物改变(例如标志物甲基化状态的改变或核酸或蛋白序列的表达水平)的任何过程,无论实际上是否检测到标志物或标志物改变。换言之,探测样品的标志物或标志物改变的行为是“检测”,即使标志物被测定为不存在或低于灵敏度水平。检测可以是定量、半定量或非定量观察,并且可以基于与一个或多个对照样品的比较。应当理解,检测本文公开的肺癌包括检测癌症前期细胞,所述癌症前期细胞开始发展为肺癌细胞或将要发展为肺癌细胞,或具有增加的发展为肺癌细胞的倾向。检测肺癌还可以包括检测可能的死亡概率或疾病条件的可能的预后。
本申请的“聚合酶链反应”或“pcr”表示这样的技术:变性、与引物的退火和与dna聚合酶的延伸的循环被用于将靶dna序列的拷贝数扩增至约106倍或更多。用于扩增核酸的聚合酶链反应过程可参见美国专利第4,683,195号和第4,683,202号。
本申请的“灵敏度”表示从一定癌症样本中检测出癌症的比例,其计算公式为:灵敏度=(检测到的癌症/所有的癌症),而“特异性”表示一定正常人样本中检测出正常的比例,其计算公式为特异性=(未检测到的阴性/总的阴性)。
可以使用多种不同方法检测核酸分子。核酸检测方法包括,例如,pcr和核酸杂交(例如,southern印迹、northern印迹或原位杂交)。具体而言,能够扩增靶核酸的寡核苷酸(例如,寡核苷酸引物)可以用于pcr反应。pcr方法通常包括以下步骤:获得样品、从所述样品分离核酸(例如,dna、rna或两者)和使所述核酸与一种或多种寡核苷酸引物接触,所述引物在能使模板核酸扩增发生的条件下特异性地与模板核酸杂交。在模板核酸的存在下,产生扩增产物。核酸扩增和扩增产物检测的条件是本领域技术人员已知的。已开发出多种对于基础pcr技术的改进,包括但不限于,锚定pcr、racepcr、rt-pcr和连接酶链式反应(lcr)。扩增反应中的引物对必须与模板核酸的相对链退火,并且应该彼此保持合适的距离,使得聚合酶能有效地跨过区域进行聚合并使得可以例如使用电泳来容易地检测扩增产物。例如,可以使用诸如oligo(molecularbiologyinsightsinc.,cascade,colo.)的计算机程序来设计寡核苷酸引物,以助于设计具有相似熔解温度的引物。通常,寡核苷酸引物长度为10-30或40或50个核苷酸(例如,长度为10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50个核苷酸),但是寡核苷酸引物可以更长或更短,只要使用合适的扩增条件。
本申请的“sept9基因”位于染色体17q25.3,septin家族是一组高度保守的gtp结合蛋白,广泛存在于人类细胞。他们在细胞分裂过程中提供结构支撑。在人类,总共有13个septin基因,相应编码15个多肽。所有septin可以形成异聚复合物,并参与高级结构的组成,例如丝状结构,戒指状结构和笼状结构的形成。这些独特的结构是控制细胞过程所必需的。它在肌动蛋白动力学,血管生成,细胞运动,细胞增殖,细胞形状,细胞质分裂,微管调节,囊泡靶向与胞吐作用方面均有重要的生理作用。
本申请的“癌胚抗原(cea)”是结直肠癌组织产生的一种糖蛋白,作为抗原可引起患者的免疫反应。此种抗原称为癌胚抗原(carcino-embryonicantigen,cea),可广泛存在于内胚叶起源的消化系统癌,也存在于正常胚胎的消化管组织中,在正常人血清中也可有微量存在。癌胚抗原是一个广谱性肿瘤标志物,它能向人们反映出多种肿瘤的存在,对结直肠癌、乳腺癌和肺癌的疗效判断、病情发展、监测和预后估计是一个较好的肿瘤标志物,但其特异性不强,灵敏度不高,对肿瘤早期诊断作用不明显。
本申请的“ca19-9”是一种粘蛋白型的糖类蛋白肿瘤标志物,为细胞膜上的糖脂质,分子量大于1000kd,是迄今报道的对胰腺癌敏感性最高的标志物。在血清中它以唾液粘蛋白形式存在,分布于正常胎儿胰腺、胆囊、肝、肠和正常成年人胰腺、胆管上皮等处,是存在于血液循环的胃肠道肿瘤相关抗原。
本申请的“ca242”是一种唾液酸化的糖类抗原,能被结肠癌细胞株经杂交瘤技术得到的一系列单克隆抗体之一ca242所识别,它是一种存在于多器官恶性肿瘤中呈粘蛋白类型的糖蛋白叫canag,即不能与lewisa型抗原反应,也不能与唾液酸化的半乳糖苷反应。免疫化学研究已表明它不同于其他已知的肿瘤相关粘蛋白如:ca199、ca50、ca125、ca153等,健康人和良性疾病血清中含量较低。ca242是近年来应用于临床较新的一种肿瘤标志物,胰腺癌和结肠癌较好的肿瘤标志物。
本申请的“ca72-4”是一种由cc49和b72.3两株单抗识别的粘蛋白样的高分子量糖蛋白,分子量为220-400kd,正常人血清中含量<6u/ml,异常升高在各种消化道肿瘤、卵巢癌均可产生。对于胃癌的检测特异性较高,以>6u/ml为临界值。良性胃病仅<1%者升高,而胃癌升高者比例可达42.6%,如与ca19-9同时检测,阳性率可达56%。
本申请的“甲胎蛋白(afp)”是一种糖蛋白,正常情况下,这种蛋白主要来自胚胎的肝细胞,胎儿出生后约两周甲胎蛋白从血液中消失,因此正常人血清中甲胎蛋白的含量尚不到20微克/升。
本申请的“铁蛋白(sf)”为机体内一种贮存铁的可溶组织蛋白,正常人血清中含有少量铁蛋白,但不同的检测法有不同的正常值,一般正常均值男性约80-130ug/l(80-130ng/ml),女性约35-55ug/l(35-55ng/ml),血清铁水平在妊娠期及急性贫血时降低,急慢性肝脏损害和肝癌时升高,国内报道肝癌患者阳性率高达90%。
本申请的“前列腺特异抗原(prostatespecificantigen,psa)”是由前列腺腺泡和导管的上皮细胞分泌的一种单链糖蛋白,在功能上属于类激肽释放酶的一种丝氨酸蛋白酶,参与精液的液化过程,是临床常规用于前列腺良性与恶性疾病诊断与鉴别诊断及前列腺癌患者术后随访的重要指标。
本申请的“β2微球蛋白(β2-microglobulin,β2-m)”表达在大多数有核细胞表面。临床上多用于诊断淋巴增殖性疾病,如白血病、淋巴瘤及多发性骨髓瘤。其水平与肿瘤细胞数量、生长速率、预后及疾病活动性有关。此外,根据此水平还可用于骨髓瘤患者分期。血清β2-mg可以在肾功能衰竭、炎症及多种疾病中均可增高。故应排除由于某些炎症性疾病或肾小球滤过功能减低所致的血清β2-mg增高。
本申请的“癌抗原50,ca50”又被称为糖链抗原50,是一种以唾液酸酯和唾液酸糖蛋白为主的糖蛋白,也是一种肿瘤抗原。癌抗原50是一种非特异性的广谱肿瘤标志物,与癌抗原19-9有一定的交叉抗原性,主要用于胰腺癌、结肠/直肠癌、胃癌的辅助诊断,其中胰腺癌病人增高最明显。例如,增高见于胰腺癌(阳性率可达87%)、结肠/直肠癌、胃癌、肺癌、肝癌、卵巢癌、乳腺癌等恶性肿瘤;溃疡性结肠炎、肝硬化、黑色素瘤、淋巴瘤、自身免疫性疾病等也增高。
本申请的“组织多肽抗原,tpa”是存在于胎盘和大部分肿瘤组织细胞膜和细胞质中的一种单链多肽。在恶性肿瘤患者血清中的检出率可高达70%以上,但它的增高与肿瘤发生部位和组织类型无相关性。然而在观察疗效上则有较高的敏感性。恶性肿瘤患者血清tpa水平可显著升高。经治疗好转后,tpa水平降低;若tpa再次增高,提示有肿瘤复发。tpa与cea同时检测可有利于恶性与非恶性乳腺病的鉴别诊断。80%的卵巢癌患者血中tpa升高。此外,肺癌、急性肝炎、胰腺炎、肺炎等tpa水平也可增高。
本申请的“组织多肽特异抗原,tps”是肿瘤细胞分泌的一种多肽抗原,是tpa在血中的特异部分。tps在卵巢癌患者血清中普遍可出现升高现象,其他如肺癌、乳腺癌患者也可出现其血清水平升高;tps与其它标志物一起作为诊断、跟踪肿瘤及病情变化的辅助指标。
本申请的“ca15-3”是乳腺癌的最重要的特异性标志物。30%-50%的乳腺癌患者的ca15-3明显升高,其含量的变化与治疗效果密切相关,是乳腺癌患者诊断和监测术后复发、观察疗效的最佳指标。ca15-3的动态测定有助于ii期和iii期乳腺癌病人治疗后复发的早期发现;当ca15-3大于100u/ml时,可认为有转移性病变。
本申请的“ca125”是1983年由bast等从上皮性卵巢癌抗原检测出可被单克隆抗体oc125结合的一种糖蛋白,来源于胚胎发育期体腔上皮,在正常卵巢组织中不存在,因此最常见于上皮性卵巢肿瘤(浆液性肿瘤)患者的血清中,其诊断的敏感性较高,但特异性较差。黏液性卵巢肿瘤中不存在。80%的卵巢上皮性肿瘤患者血清ca125升高,但近半数的早期病例并不升高,故不单独用于卵巢上皮性癌的早期诊断。90%患者血清ca125与病程进展有关,故多用于病情检测和疗效评估。95%的健康成年妇女ca125的水平≤40u/ml,若升高至正常值的2倍以上应引起重视。另外ca125也可见于结核性腹膜炎患者的血清检查中,且ca125水平呈数十倍升高,在卵巢癌术前应明确排除结核性腹膜炎、盆腔炎可能。
本申请的“人绒毛膜促性腺激素,β-hcg”是由胎盘的滋养层细胞分泌的一种糖蛋白,它是由α和β二聚体的糖蛋白组成。β-hcg升高还有下列几种可能:正常怀孕、双胞胎,葡萄胎、或某些疾病或肿瘤。如在内分泌疾病中,如脑垂体疾病、甲状腺功能亢进、妇科疾病如卵巢囊肿、子宫癌等hcg也可增高。发现恶性肿瘤如默契胎瘤、胰腺癌、胃癌、肝癌、乳腺癌、肺癌等血中hcg也可升高因此在肿瘤科,将hcg看作是癌标志物之一。
本申请的“cyfra21-1”是细胞角蛋白19的可溶性片段,目前主要用做肿瘤标志物,对肺癌的诊断有较大意义。细胞角蛋白(cytokeratins)是形成上皮细胞的结构蛋白之一中间丝的亚单位。根据其分子量和双向电泳中等电点的不同,可以分为20种不同类型。它们被分为两个亚群:ⅰ类(酸性蛋白),ⅱ类(碱性蛋白)。细胞角蛋白是由ⅰ类和ⅱ类角蛋白组成的异聚合体。细胞角蛋白19(cyk-19)是一分子量约40,000da的ⅰ类角蛋白(酸性蛋白),是角蛋白家族中最小的成员。cyk-19广泛分布在正常组织表面,如层状或鳞状上皮中。在恶性上皮细胞中,激活的蛋白酶加速了细胞的降解,使得大量细胞角蛋白片段释放入血,其可溶性片段可与两株单克隆抗体ks19.1和bm19.21特异性结合,故称为cyfra21-1。cyfra21-1分子量约30,000da。在恶性肺癌组织中,cyfra21-1含量丰富,尤其是在肺鳞癌中有高表达。
本申请的“神经元特异性烯醇化酶(neuron-specificenolase,nse)”是参与糖酵解途径的烯醇化酶中的一种,存在于神经组织和神经内分泌组织中。nse在脑组织细胞的活性最高,外周神经和神经分泌组织的活性水平居中,最低值见于非神经组织、血清和脊髓液。它被发现在与神经内分泌组织起源有关的肿瘤中,特别是sclc中有过量的nse表达,导致血清中nse明显升高。
本申请的“鳞癌抗原scc”是子宫颈鳞癌的首选肿瘤标志物。它的cutoff值一般在2.5μg/l,scc参与正常和恶变时的蛋白分解调控,子宫颈鳞癌时明显升高。但因目前尚未发现100%特异性和100%灵敏度的肿瘤标志物,肿瘤与肿瘤标志物之间不是一一对应关系,它们只是相关性。因此,并不能单纯仅从该指标升高就确诊是子宫颈鳞癌。需要紧密结合临床及其他检查手段综合判断。另外,部分肺癌、胃癌、卵巢癌患者该指标也会升高。
本申请的“胃蛋白酶原(pgi/ii)是由胃部分泌的参与消化的胃蛋白酶的前体,通常约1%的pg可通过胃黏膜进入血液循环,可分为pgi和pgii两种亚型,血清胃蛋白酶原可以较为准确地显示胃黏膜的状态和功能。pg是浅表性胃炎、糜烂性胃炎、胃溃疡、十二指肠溃疡、萎缩性胃炎、胃癌等胃部疾病的初筛选指标和治疗的监控指标。在常规体检中每个人做胃镜是不现实的,可通过非侵入性血清pg检测将浅表性胃炎、糜烂性胃炎、胃溃疡、十二指肠溃疡、胃癌等胃病高危人群检查出来,再进行胃镜检查是一个切实可行的方案。研究发现,在常规体检中大约有15%左右的人的血清pg水平异常,而进一步进行胃镜检查,其中90%以上的患者有不同程度的浅表性胃炎、糜烂性胃炎、胃溃疡、十二指肠溃疡、萎缩性胃炎、胃癌等胃部疾病。pgi及pgi/pgii比值明显降低的高危人群的胃癌发生率一般比正常人群高数十倍。
概述
本发明提供了一种简易、方便和减少受检者负担的对多种肿瘤精准的组合性检测和综合性分析判读方法,应用于对多种肿瘤的临床检测、高危人群筛查和普通人群的普查。其中所述组合性检测包括对受检者进行septin9基因甲基化的测定、进行多种肿瘤标志物的测定、和进行使用医疗器械及设备对受检者的检查。其中所述综合性分析判读方法包括综合受检者的临床问卷、家族史、临床主诉、临床症状、临床体征、septin9基因甲基化的测定结果、多种肿瘤标志物的测定结果、和使用医疗器械及设备对受检者的检查结果进行综合分析。通过本发明的方法,可以实现一次采取受检者样品,通过组合性检测和综合性分析判读方法,对受检者进行多种肿瘤精准的测定。
septin9基因甲基化的检测是检测血浆中的游离dna,检测使用10mledta真空采血管(紫帽)采集患者静脉血,全血样本量至少为10ml×1管或者5ml×2管,离心装有血样的采血管12分钟,离心力1350±150rcf。从离心机中取出采血管,用一个干净的15cm一次性移液管把血浆转移到聚丙烯材质、圆锥底的15ml离心管中。
离心血浆12分钟,离心力1350±150rcf。用新的一次性移液管或者血清移液管将3.5ml血浆移入标记好的圆锥底的离心管中。将3.5ml血浆样本、阳性对照品、阴性对照品分别转移到事先标记好的15ml离心管中;依次加入3.5ml裂解吸附液。盖紧离心管盖,涡旋混匀。离心管室温(15-30℃)中放置10±1分钟。
依次将下列试剂添加到15ml离心管中:90μl磁珠(新鲜悬浮);2.5ml无水乙醇(分子生物学级别,纯度≥99.5%)。盖紧离心管盖,颠倒混匀5-6次。把离心管置于轮状旋转混匀器上,室温中速(大约10-20rpm)旋转45±5分钟,旋转角度大约35~45°。
将15ml离心管放置于dynamagtm-15磁性试管架上吸附5-10分钟。小心倒掉上清(注意不要倒掉磁珠,倒掉上清时保持15ml离心管放置于dynamagtm-15磁性试管架上)。加入1.5ml洗液a,涡旋混匀确保磁珠彻底重悬。用一次性移液管将磁珠悬浮液移至标记好的2.0ml离心管中。再次用移液管吸取残留磁珠悬浮液,将其转移至2.0ml离心管中。
将2.0ml离心管放置于dynamagtm-2磁性试管架上吸附2-6分钟。用一次性移液管尽量除去液体,注意不要吸取磁珠。短暂离心2.0ml离心管。放置2.0ml离心管在dynamagtm-2磁性试管架上重新吸附2-6分钟,用10-100μl移液器尽量除去残余液体。
将离心管移至无磁性试管架上。涡旋混匀洗脱液,加入100μl洗脱液至各个离心管中,盖紧离心管,涡旋混匀,重悬磁珠。将离心管放置于恒温振荡器中,转速设为1000±100rpm,温度设为80℃,震荡10±1分钟。短暂离心离心管。将离心管置于dynamagtm-2磁性试管架上2-6分钟。将全部洗脱液移至新的2.0ml离心管中(约100μldna洗脱液)。
在含有dna洗脱液的2.0ml离心管中一次加入150μl亚硫酸盐溶液,25μl保护液。盖紧离心管后,涡旋混匀离心管中的反应液。短暂离心离心管。将离心管置于恒温振荡器中,80℃恒温孵育45±5分钟,不要振荡。45±5分钟后,立即将离心管取出。
短暂离心上述反应后的2.0ml离心管。在离心管中依次加入:1000μl洗液a;20μl磁珠(新鲜悬浮)。涡旋混匀。将离心管置于23℃的恒温振荡器中,调整转速为1000±100rpm,孵育45±5分钟。短暂离心离心管,将离心管置于dynamagtm-2磁性试管架2–6分钟。用一次性移液管尽量去除液体。
第一次洗涤:将离心管从磁力架上取下,加入800μl洗液a。涡旋混匀重悬磁珠,短暂离心离心管。将离心管置于dynamagtm-2磁性试管架2–6分钟。用一次性移液管尽量去除液体。
第二次洗涤:将离心管从磁力架上取下,加入800μl洗液b。涡旋混匀重悬磁珠。短暂离心离心管。将离心管置于dynamagtm-2磁性试管架2–6分钟。用一次性移液管尽量去除液体。
第三次洗涤:将离心管从磁力架上取下,加入400μl洗液b。涡旋混匀重悬磁珠。短暂离心离心管。将离心管置于dynamagtm-2磁性试管架2–6分钟。用一次性移液管尽量去除液体。短暂离心离心管。将离心管置于dynamagtm-2磁性试管架2–6分钟,用10-100ul移液器尽量除去残余液体。短暂离心离心管。将离心管置于dynamagtm-2磁性试管架2–6分钟,用10-100ul移液器尽量除去残余液体。
干燥和洗脱:打开离心管管盖。将离心管置于恒温振荡器中,23±2℃静置10分钟待沉淀干燥,不要震荡。将离心管移至无磁性试管架上,加入60μl洗脱液。盖好离心管,涡旋混匀重悬磁珠。将离心管放入恒温振荡器中,23±2℃,1000±100rpm孵育10分钟。短暂离心离心管。将离心管置于dynamagtm-2磁性架2–6分钟。用10-100μl移液器将洗脱液(约60μl)转移至96孔板中,并使用粘性薄膜和封膜器密封96孔板。
pcr设置:每个pcr反应需要32μlpcr反应液和1.6μl聚合酶。按比例将相应体积的pcr反应液和聚合酶加入到2.0ml的离心管中。涡旋混匀pcr预反应液,短暂离心离心管,将管壁液滴离下来。将30μlpcr预反应液加至选定好96孔板孔中。加入30μl的bisdna至pcr板对应的孔中。用
pcr反应:pcr过程使用appliedbiosystems7500pcr仪,该仪器sdsv2.0.5软件和sdsv1.4软件已经通过验证。pcr预反应液中不包含rox或其它染料。因此,passivereference设置必须为“none”,septin9选取fam荧光通道,actb选取joe通道,反应程序为:阶段1,一个循环94℃,20分钟;阶段2,45个循环,62℃,5秒,55.5℃,35秒,93℃,30秒;阶段3,40℃,5秒。
分析条件设置:(1)sdsv2.0.5版本,设置基线10-22个循环,设置septin9阈值30000,actb阈值14000。用对照品验证pcr反应的有效性:阳性对照septin9的ct值≤41.1,actb的ct值≤29.8;阴性对照septin9的ct值无,actb的ct值≤37.2;任何一个条件不符合,则本次实验结果“无效”。(2)sdsv1.4版本软件设置:设置基线10-22个循环,设置septin9阈值100000,actb阈值60000。用对照品验证pcr反应的有效性:阳性对照septin9的ct值≤41.1,actb的ct值≤29.8;阴性对照septin9的ct值无,actb的ct值≤37.2;任何一个条件不符合,则本次实验结果“无效”。
样本pcr反应结果的解释:单个样本结果解释:如果actb的ct值≤32.1,septin9的ct值≤41,定义该样本为阳性;如果actb的ct值≤32.1,septin9的ct值>41,定义该样本为阴性;如果actb的ct值>32.1,定义该pcr反应“无效”。
septin9检测所使用的引物、探针及blocker为寡核苷酸,其中引物、探针和阻断剂(blocker,一段非扩增的单体可以防止探针退火后的延伸)的序列为:上游引物,seqidno:1gtagtagttagtttagtatttatttt;下游引物,seqidno:2cccaccaaccatcatat;阻断剂,seqidno:3catcatatcaaaccccacaatcaacacacaac;探针1,seqidno:4gttcgaaatgattttatttagttgc;探针2,seqidno:5cgttgatcgcggggttc。引物、探针、blocker的位置位于septin9基因v2转录产物的1λ外显子的cpg岛处,blocker覆盖5个cpg甲基化位点,探针1覆盖3个cpg甲基化位点,探针2覆盖1个cpg甲基化位点。
actb引物、探针信息:actb的的引物、探针设计选择持家基因actb的保守序列区域。序列信息为:上游引物,seqidno:6gtgatggaggaggtttagtaagtt;下游引物,seqidno:7ccaataaaacctactcctcccttaa;探针,seqidno:8accaccacccaacacacaataacaaacaca。
蛋白质肿瘤标志物检测是采用医院检验科的化学发光法常规试剂和蛋白质芯片法常规试剂。本发明使用的具有代表性的用化学发光法来检测蛋白质肿瘤标志物是深圳市新产业生物医学工程股份有限公司的仪器和试剂系统,可以检测afp、cea、psa、f-psa、ca125、ca153、ca199、fer、nse、ca50、scc、cyfra211、ca724、ca242、he4、s-100、pg-i、pg-ii、hcg和hgh等。具有代表性的用蛋白质芯片法来检测蛋白质肿瘤标志物是上海数康生物科技有限公司的仪器和试剂系统,可以检测afp、cea、psa、f-psa、ca125、ca153、ca199、fer、nse、ca242、hcg和hgh等
粪便免疫化学检测(fecalimmunochemicaltest,fit)是采用医院检验科的常规试剂。
实施例1组合使用基因甲基化和蛋白质肿瘤标志物
组合使用基因甲基化和蛋白质肿瘤标志物可以增加检测的灵敏性,提高肿瘤早期诊断的成功率。在1031例的septin9基因甲基化试剂盒检测结直肠癌临床试验中,医院检验科用septin9基因甲基化试剂盒检测受检者血浆中的基因甲基化含量,同时用医院检验科的粪便免疫化学检测(fecalimmunochemicaltest,fit)试剂盒检测受检者大便中的血红蛋白,或者用医院检验科的cea检测受检者血液中cea的含量。
如表1所示,当分别检测三项指标时,septin9检测肿瘤的灵敏性为77%,特异性为96%,检测早期肿瘤的灵敏性为68%,都分别比fit(70%,95%,58%)和cea(52%,85%,31%)好,而将septin9的结果和fit结果综合分析,组合检测肿瘤的灵敏性为94%,比组合前septin9单独检测的灵敏性77%提高了17%,特异性下降4%。如果将septin9的结果和cea结果综合分析,组合检测肿瘤的灵敏性为88%,比组合前septin9单独检测的灵敏性77%提高了11%,特异性下降6%。如果将septin9的结果和fit以及cea结果综合分析,组合检测肿瘤的灵敏性为97%提高20%,但特异性也相应下降较多,低于90%(表中未显示),要谨慎选用过多和不适当的组合。
组合使用基因甲基化和蛋白质肿瘤标志物最大优势是可以增加早期肿瘤的检测灵敏性,本发明中septin9检测和fit检测组合,可将早期肿瘤的检测灵敏性提高18%,由septin9单独检测早期肿瘤的灵敏性为68%提高到86%。其主要原因是septin9基因甲基化发生在肿瘤发生的非常早期阶段,甚至是在癌前病变阶段,检测septin9基因甲基化是检测肿瘤的早期变化,这是蛋白质肿瘤标志物所不及的地方,尽管蛋白质肿瘤标志物对早期肿瘤的检测灵敏性也有一定的贡献。肿瘤组织在核酸水平的改变和蛋白质水平的改变是截然不同的两个生物学层面,核酸水平的改变趋于早期和广谱,蛋白质水平的改变趋于中晚期和形成一定的组织特异性。二者的组合能够形成很好的协同效应。
表1
septin9基因甲基化检测方法参考博尔诚公司的《septin9基因甲基化检测试剂盒(pcr荧光探针法)说明书》,septin9基因甲基化检测试剂盒包括两个步骤:
步骤1:使用血浆处理试剂盒提取血浆中的游离dna,然后用亚硫酸盐转化未发生甲基化的胞嘧啶,通过脱氨基反应产生尿嘧啶磺酸盐,发生甲基化的胞嘧啶则不会被亚硫酸盐转化;
步骤2:将亚硫酸盐转化的dna(bisdna)做双重pcr扩增,pcr反应中的阻断剂和探针能区分甲基化和非甲基化序列,甲基化序列优先得到扩增,与甲基化septin9基因序列特异性结合的荧光素探针可以在pcr反应中专一地检测出甲基化序列。内对照actb(β-actin)基因用于评估检测中dna量是否足够。试剂盒中提供了阳性和阴性对照,每一次检测中都需要同时检测阴、阳性对照。
将septin9的结果和fit结果综合分析,灵敏性提高17%,可将早期肿瘤的检测灵敏性提高20%,特异性下降4%。将septin9的结果和cea结果综合分析,灵敏性提高11%,特异性下降6%。如果将septin9的结果和fit以及cea结果综合分析,灵敏性提高20%,达到97%,特异性也相应下降较多,低于90%,要谨慎选用过多和不适当的组合。
septin9的结果和rnf180结果综合分析,灵敏性提高18%,特异性不变。结果提示组合使用不同的基因甲基化肿瘤标志物对提高整体肿瘤的检测灵敏性(18%)与组合基因甲基化和蛋白质肿瘤标志物检测方法(17%)相近。
实施例2组合使用两个基因甲基化肿瘤标志物
组合使用不同的基因甲基化肿瘤标志物可以增加检测的灵敏性,提高肿瘤早期诊断的成功率。在202例的septin9+rnf180基因甲基化试剂盒检测胃癌临床试验中,医院检验科用septin9+rnf180基因甲基化试剂盒检测受检者血浆中的基因甲基化含量。如表2所示,当分别分析两项指标时,septin9和rnf180检测肿瘤的灵敏性分别为43%和48%,都在50%以下,而将septin9的结果和rnf180结果综合分析,组合检测肿瘤的灵敏性为66%,提高了18%,特异性不变。结果提示组合使用不同的基因甲基化肿瘤标志物对提高整体肿瘤的检测灵敏性(18%)和组合基因甲基化和蛋白质肿瘤标志物检测方法(17%)相近。
组合使用不同的基因甲基化肿瘤标志物也具有增加早期肿瘤的检测灵敏性的优势,本发明中septin9和rnf180检测早期肿瘤的灵敏性分别为28%和38%,而septin9检测和rnf180检测组合,可将早期肿瘤的检测灵敏性提高10%,从单独rnf180检测早期肿瘤38%的灵敏性提高到48%。结果提示组合使用不同的基因甲基化肿瘤标志物对提高早期肿瘤的检测灵敏性(10%)和组合基因甲基化和蛋白质肿瘤标志物检测方法(18%)有明显的差距。其可能原因是septin9基因甲基化和rnf180基因甲基化都处在肿瘤发生的相同早期阶段,甚至是在癌前病变阶段,检测septin9基因甲基化和rnf180基因甲基化都是检测肿瘤的早期变化,两者在生物学机理上重复较多,具有叠加效果。而检测septin9基因甲基化和检测蛋白质肿瘤标志物检测的是不同的物质,两者在生物学的机理上差别很大,有着超常的协同效应。而这一现象仅发生在检测早期肿瘤的阶段,如果将各期肿瘤合并在一起,则并不具备协同效应。因为在总体来说组合使用不同的基因甲基化肿瘤标志物检测提高了整体胃癌的检测灵敏性(18%),其协同效应和组合基因甲基化和蛋白质肿瘤标志物检测方法提高整体结直肠癌的检测灵敏性(17%)相近。组合检测septin9基因甲基化和检测蛋白质肿瘤标志物对早期肿瘤诊断的超常的协同效应,尚未见过报道。本发明的组合检测septin9基因甲基化和检测蛋白质肿瘤标志物方法的协同效应不是显而易见的。
表2
实施例3对多种肿瘤精准的组合性检测和综合性分析判读方法和应用-septin9+
根据实施例1和2的发现,本发明设计和开发了对多种肿瘤精准的组合性检测和综合性分析判读方法和应用---septin9+。如图1所示,本发明是组合septin9基因甲基化和蛋白质肿瘤标志物检测方法,septin9基因甲基化的检测方法使用液态活检的途径,用实时定量pcr的方法测定检测受检者血浆中游离的甲基化septin9基因。蛋白质肿瘤标志物检测方法可采取elisa或化学放光免疫的方法测定,也可采用液相蛋白芯片或固相蛋白芯片的方法测定。这些测定方法都可以按产品说明书操作。检测septin9基因甲基化是为了检测早期肿瘤,并且利用其广谱性的特点,对多种肿瘤进行检测,检测多种蛋白质肿瘤标志物是为了对不同的肿瘤进行组织特异性定位。二者的组合测定,可以提高早期肿瘤的检测灵敏性20%,提高各期肿瘤的整体灵敏性17%。
所述的多种肿瘤包括肺癌、胃癌、肝癌、结直肠癌、食管癌、乳腺癌、脑癌、宫颈癌、胰腺癌、甲状腺癌、淋巴癌、膀胱癌、白血病、肾癌、子宫癌、前列腺癌、卵巢癌等。
本发明的另一个方面,提供了一种综合性分析判读方法和应用。由于本发明是对早期肿瘤进行检测,受检者大多是是无症状人群,采集和参考受检者的临床信息,包括问卷,年龄、性别、体重、抽烟历史,家族史,传染病史,糖尿病史等可以对组合性检测结果提供导向性线索,提供给综合性分析判读方法和应用。
本发明还要采集和参考其他临床辅助检验结果,尤其是组合性检测结果提示有问题,需要进一步核实的情况下,要采用其他临床辅助检验。其他临床辅助检验方法包括影像学和腔镜的检查。影像学检测方法包括x线透视,ct,mri和超声波等,腔镜检查包括胃镜、肠镜、腹腔镜、十二指肠镜、支气管镜、胸腔镜、膀胱镜、宫腔镜等。
在分析检测结果时,要根据本发明中对多种肿瘤的组合性检测的结果,参考受检者的临床信息和其他临床辅助检验结果,对肿瘤检测结果进行综合性分析和判读。这些就构成了本发明的对多种肿瘤精准的组合性检测和综合性分析判读方法和应用。
实施例4:消化系统肿瘤联合检查组合
甲基化的septin9基因在结直肠癌患者的血浆中升高的比例最高,根据1031例的临床试验结果,可达77%。在胃癌患者的血浆中升高的比例可达50%。在食道癌、胰腺癌和肝癌的患者的血浆中都有不同程度升高的比例。最关键的是septin9基因甲基化可以检测早期肿瘤。蛋白质肿瘤标志物有一定的组织特异性,和septin9基因甲基化检测有很好的互补性和协同性。根据实施例三的设计和框架,本发明衍生出消化系统肿瘤联合检查组合,详见表3.
结直肠癌的蛋白质肿瘤标志物fit和cea的协同效应已经在实施例1中详述。对胃癌来说,ca724是一个首选的肿瘤标志物,近年来pgi/ii也受到重视,pg是浅表性胃炎、糜烂性胃炎、胃溃疡、十二指肠溃疡、萎缩性胃炎、胃癌等胃部疾病的初筛选指标和治疗的监控指标,加入组合更为有利。afp和cea对肝癌的检测已经在临床应用多年,afp对原发性肝癌有很好的特异性。ca242对食道癌有较好的特异性,配上tpa、tps和cea组合,效果更好。ca199对胰腺癌有有较好的特异性,是迄今报道的对胰腺癌敏感性最高的标志物。ca50在胰腺癌的阳性率可达87%。
一次抽血可以完成用于该组合检测的样品采集,一个septin9的实时定量pcr检测,一个蛋白质液相芯片检测即可完成检测全部蛋白质肿瘤标志物。医学检验机构自动化发光免疫或elisa也可以完成蛋白质肿瘤标志物的检测。
表3
实施例5:十个肿瘤联合检查组合
甲基化的septin9基因在肺癌患者的血浆中升高的比例约有40%以上,乳腺癌、卵巢癌、子宫癌和前列腺癌患者的血浆中也有一定的升高比例。按照实施例三的设计和框架,本发明衍生出十个肿瘤联合检查组合,其中五个主要肿瘤的联合检查组合详见表4,加上表3中五个消化系统的肿瘤,总共是十个肿瘤联合检查组合。
cyfra21-1是细胞角蛋白19的可溶性片段,目前主要用做肿瘤标志物,对肺癌的诊断有较大意义。在恶性肺癌组织中,cyfra21-1含量丰富,尤其是在肺鳞癌中有高表达。ca15-3是乳腺癌的最重要的特异性标志物。30%-50%的乳腺癌患者的ca15-3明显升高,其含量的变化与治疗效果密切相关,是乳腺癌患者诊断和监测术后复发、观察疗效的最佳指标。80%的卵巢上皮性肿瘤患者血清ca125升高,但近半数的早期病例并不升高,故不单独用于卵巢上皮性癌的早期诊断。前列腺特异抗原(prostatespecificantigen),人绒毛膜促性腺激素是由胎盘的滋养层细胞分泌的一种糖蛋白,对子宫癌有很好的特异性,但肺癌是也会升高。psa是由前列腺腺泡和导管的上皮细胞分泌的一种单链糖蛋白,是临床常规用于前列腺良性与恶性疾病诊断与鉴别诊断及前列腺癌患者术后随访的重要指标。
一次抽血可以完成用于该组合检测的样品采集,一个septin9的实时定量pcr检测,一个蛋白质液相芯片检测即可完成检测全部蛋白质肿瘤标志物。医学检验机构自动化发光免疫或elisa也可以完成蛋白质肿瘤标志物的检测。
表4
实施例6:结直肠癌联合检查组合
根据实施例1和2的发现,本发明设计和开发了对结直肠癌精准的组合性检测和综合性分析判读方法和应用---结直肠癌联合检查。如图2所示,本发明是组合基因甲基化、基因突变、微小rna等核酸肿瘤标志物检测和各种与结直肠癌相关的蛋白质肿瘤标志物的检测方法组合在一起构成结直肠癌联检的组合方案,通过检测粪便和血液对结直肠癌进行早期诊断、指导治疗和预后监测。核酸肿瘤标志物检测(septin9基因甲基化)和各种与结直肠癌相关的蛋白质肿瘤标志物的检测(fit、cea)方法组合可以提高早期肿瘤的检测灵敏性20%,提高各期肿瘤的整体灵敏性17%。
在结直肠癌联合检查组合中可以检测多种基因的甲基化、基因突变和微小rna的变化,也可以只检测septin9基因甲基化,加上检测血液中的多种肿瘤标志物如cea、ca199、ca242和ca724等,再加上用fit检测粪便如表5所示。这些测定方法都可以按产品说明书操作。检测septin9基因甲基化是为了检测早期肿瘤,检测多种蛋白质肿瘤标志物是为了增加灵敏性、指导治疗和预后监测等。
表5
实施例7:分析和判读的实施步骤
分析和判读的实施步骤分为三个主要部分,第一部分是数据采集,包括1.采集基因甲基化肿瘤标志物和蛋白质肿瘤标志物检测结果,2.采集受检者的临床信息,包括问卷,主诉、症状、体征、年龄、性别、体重、抽烟历史,家族史,传染病史,糖尿病史;3.采集和其他临床辅助检验结果包括影像学和腔镜的检查。影像学检测方法包括x线透视,ct,mri和超声波等,腔镜检查包括胃镜、肠镜、腹腔镜、十二指肠镜、支气管镜、胸腔镜、膀胱镜、宫腔镜等的结果。
第二部分是分析第一部分采集的三套不同性质和反映受检者不同状态的结果。每一个结果定义为一个因素,因为是多因素分析,在分析过程中对每一个因素分配权重,分配权重的原则是根据对上述三套因素的综合分析。第一套因素是分析基因甲基化肿瘤标志物和蛋白质肿瘤标志物检测结果,1)阳性的分析方法可以是几个肿瘤标志物中任何一个阳性则分析为阳性,或任何两个、三个、或四个等等阳性则分析为阳性。2)早期肿瘤的广谱分析:septin9基因甲基化擅长于检测早期和广谱的癌症,以septin9基因甲基化为高权重因素3)肿瘤组织特异性分析使用蛋白质肿瘤标志物来权衡,如表3和表4中“肿瘤特异性相对好”一列中所列举的蛋白质肿瘤标志物更加具有相对各自一行对应肿瘤的组织特异性,如fit加重结直肠癌权重,afp加重肝癌权重,cyfra21-1加重肺癌权重,psa加重前列腺癌权重等等,这些蛋白质肿瘤标志物可加上对组织特异性的权重。
第二部分还可以包括分析第二套因素,即临床信息,包括问卷,主诉、症状、体征、年龄、性别、体重、抽烟历史,家族史,传染病史,糖尿病史等。主要是提供肿瘤的早期表现和肿瘤的组织特异性。例如,腹部不适、食欲骤减加重胃癌的权重,面色发黄加重肝癌权重,大便型状改变加重结直肠癌权重,吞咽困难加重食管癌的权重,快速体重下降加重胰腺癌权重,抽烟历史加重肺癌权重,家里血缘亲属有人患乳腺癌加重结乳腺癌权重。第二部分还可以包括分析第三套因素,其他临床辅助检验结果包括影像学和腔镜的检查。影像学检测方法包括x线透视,ct,mri和超声波等,腔镜检查包括胃镜、肠镜、腹腔镜、十二指肠镜、支气管镜、胸腔镜、膀胱镜、宫腔镜等的结果。例如,当x线透视发现过胃溃疡,加重胃癌的权重,超声波发现过肝脏中有占位性病变,加重肝癌的权重,ct发现过有肺部结节,加重肺癌的权重,胃镜发现过萎缩性胃炎或肠化生,加重胃癌的权重,肠镜发现过多发性息肉,加重结直肠癌的权重,x线透视发现过乳房结节,加重乳腺癌的权重等等。
第三部分是综合判读,综合上述三套不同性质和反映受检者不同状态的结果或因素,综合各因素的权重来判读受检者是否患有早期肿瘤,各种因素从几种到几十种或上百种。因素少的可用简单分析,因素多的需要用计算机进行数据综合分析判读,或进一步用“大数据”处理方式来进行综合分析判读。多因素综合分析后形成算法公式来进行判读。举例如下,例1,受检者septin9基因甲基化阳性,和蛋白质肿瘤标志物ca724阳性,提示受检者有早期胃癌的可能。例2,受检者septin9基因甲基化阳性,其他蛋白质肿瘤标志物均为阴性,由于septin9基因甲基化多发生在结直肠癌,应首先判断受检者为结直肠癌,但受检者有腹部不适、食欲骤减,更提示受检者有早期胃癌的可能。例3,受检者septin9基因甲基化阴性,蛋白质肿瘤标志物ca724和mg7二者均阳性,并且受检者有过x线胃造影发现过胃溃疡的历史,仍应判断为胃癌;例4,受检者septin9基因甲基化阳性,蛋白质肿瘤标志物cea和cyfra21-1阳性,有直系血缘亲属患结直肠癌。由于有septin9基因甲基化阳性、蛋白质肿瘤标志物cea阳性加上有直系血缘亲属患结直肠癌这些和结直肠癌相关权重大的因素,判断为结直肠癌的可能性大。但是经过进一步的检查,发现受检者还有咳嗽、胸部ct发现有结节这些和肺癌相关权重大的因素,受检者判断为肺癌的可能性更大,因为cyfra21-1阳性是和肺癌的相关权重很大的因素,cea也和肺癌的相关权重较大。所以,通过综合分析各种因素的权重大小,可以有更准确的判断受检者可能是患肺癌。
上述例4涉及到如何赋予各种因素的权重大小这一关键环节,这是一个非常需要疾病和医学知识的整合,并进行综合性逻辑判断的过程,每一个因素的权重不是一成不变的,例如咳嗽这个因素,如果胸部ct没有发现结节,咳嗽的权重在之前的肿瘤判读中就很低,但是当胸部ct发现结节后,咳嗽的权重在肿瘤判读中就非常高,而其他因素的权重,如直系血缘亲属患结直肠癌就变得低了许多,受检者更倾向于判读为肺癌。受检者的病史因素也很重要,对例4来说,病史中的新的因素又会改变其他因素的权重。例如,在回顾受检者的病史中七年前做过结肠镜的记录,并且切除过2.2厘米大小的绒毛状腺瘤,这一新的因素,又会重新改变其他因素的权重,直系血缘亲属患结直肠癌这一因素的权重就变得高了许多,受检者又更倾向于判读为结直肠癌,因为2厘米以上的绒毛状腺瘤癌变的可能性很大,受检者可能是手术七年后绒毛状腺瘤的癌变,septin9基因甲基化阳性,蛋白质肿瘤标志物cea阳性仍然支持结直肠癌的判读。此时,咳嗽这个因素的权重并没有减低,有可能受检者的结直肠癌已经转移到肺部,从而造成咳嗽和肺部ct发现结节。
从以上叙述可以看到各个因素的权重不是一成不变的,受到其他因素的改变而改变。所以,本发明采集三套不同性质和反映受检者不同状态的结果或因素,包括1.核酸检测结果和蛋白质肿瘤标志物的检测结果,2.临床信息包括问卷,主诉、症状、体征、年龄、性别、体重、抽烟历史,家族史,传染病史,糖尿病史等,和3.其他临床辅助检验结果包括影像学和腔镜的检查。影像学检测方法包括x线透视,ct,mri和超声波等,腔镜检查包括胃镜、肠镜、腹腔镜、十二指肠镜、支气管镜、胸腔镜、膀胱镜、宫腔镜等的结果进行综合分析,得到对肿瘤包括早期肿瘤的精准判读。由于本发明采集的因素较多,上述这些综合分析判读可以通过计算机的运算来找到综合因素权重最大的组合来精准判断肿瘤包括早期肿瘤。
以上的七个实施例中,每一个实施例都可以单独的形成实用的产品,应用在多种肿瘤的早期诊断、指导治疗和预后监测等。每一个实施例中可以用简单的组合检查和综合性分析,达到需要用多种和多个目前存在的、复杂昂贵的检测才能达到的目的。对受检者来说,减少到医院抽血和采样本的次数和检测的经济负担,所以本发明提供了一种简易、方便和减少受检者负担的对多种肿瘤精准的组合性检测和综合性分析判读方法。
本发明中的肿瘤标志物在肿瘤检测中的灵敏性和特异性,来源于发明者在临床试验中的测定和积累的数据,也参考了目前已有的数据。实施例中只是举例说明发明人的部分组合性检测,还有一些组合性检测未体现在本说明书中。图3是对部分肿瘤标志物在肿瘤检测中的灵敏性和特异性的的汇总分析,对筛选不同的肿瘤标志物进入不同的组合,提供依据,有经验的人还可以根据本发明做出不同的组合性检测。
实施例中在说明书中提及的所有发表文献和专利申请表明与本发明相关领域内技术人员的水平。所有的发表文献和专利申请通过引用的方式结合到本文中,就如每个发表文献和专利申请被具体地、单个地注明通过引用的方式结合到本文中一样。仅仅对这些发表文献和专利申请的提及不能理解为成人它们相对于本申请是现有技术文献。
尽管本发明已进行了一定程度的描述,明显地,在不脱离本发明的精神和范围的条件下,可进行各个条件的适当变化。可以理解,本发明不限于所述实施方案,而归于权利要求的范围,其包括所述每个因素的等同替换。
- 还没有人留言评论。精彩留言会获得点赞!