一种伊曲康唑晶型化合物及其制备方法与流程
本发明涉及医药领域,具体涉及一种光学异构体2R,4S,2’S-伊曲康唑晶型及其制备方法。
背景技术:
伊曲康唑是目前疗效较好,副作用较小的一种三唑类广谱抗真菌药物,其体外抗菌谱较广,注射剂可达到肺部感染部位,用于治疗肺部曲霉菌感染。其英文名称为Itraconazole,中文化学名:顺-4-[4-[4-[4-[[-2-(2,4-二氯苯基)-2-(1H-1,2,4-三唑-1-基甲基)-1,3-二氧戊环-4-基]甲氧基]苯基]哌嗪-1-基]苯基]-2-[(2’S)-1-甲基丙基]-1,2,4-三唑-3-酮。其化学结构式如下所示:
伊曲康唑有3个手性碳原子,共有8种光学异构体,临床使用的是其结构中二氧戊烷环上4个顺式异构体的混合物,对应为2S,4R,2’R-伊曲康唑(A)、2S,4R,2’S-伊曲康唑(C)、2R,4S,2’R-伊曲康唑(B)及2R,4S,2’S-伊曲康唑(D),其化学结构式如下所示:
研究发现,伊曲康唑各异构体的生物活性及毒副作用存在较大差异,如CN103263417A公开了伊曲康唑异构体组合能够提高对真菌和内皮细胞的选择性,同时也是具有治疗真菌及血管新生相关疾病潜力的候选药物,单一构型的光学纯伊曲康唑还能显著降低肝细胞毒性,可避免伊曲康唑引起的副作用。
文献ChemBiol,2007(2):263-70报道了伊曲康唑具有潜在的抑制血管内皮细胞增生作用,而其他抗真菌药物如氟康唑、酮康唑等却对血管内皮细胞无影响;CN101711156 A公开了一种伊曲康唑单一手性纯异构体预防和治疗血管新生相关疾病的方法,伊曲康唑异构体可以抑制肿瘤新生血管,是抗肿瘤的候选化合物。
消旋的伊曲康唑在临床上的严重不良反应包括胃肠道不适,如厌食、恶心、腹痛和便秘,少见的副作用包括头痛、可逆性氨基转移酶升高、月经紊乱、头晕和过敏反应(如瘙痒、红斑、风团和血管性水肿),尤其是肝毒性,一般一个疗程为半个月,对肝脏的损伤非常明显,严重者会发生肝功能衰竭导致死亡,在治疗过程中通常不被作为一线用药。文献DRUG METABOLISM AND DISPOSITION.2006,34:583-590.报道了伊曲康唑四个顺式异构体的人体内代谢研究结果表明,只有2R,4S,2’R和2R,4S,2’S能够被CYP3A4代谢成羟基伊曲康唑、酮基伊曲康唑和N-脱烷基伊曲康唑,而2S,4R,2’R和2S,4R,2’S不能被代谢,因而具有更高的生物利用度,肝细胞毒性实验测试也表明,伊曲康唑异构体2S,4R,2’S和2R,4S,2’S具有更高的安全性。
专利CN201510350844.3公开了光学异构体2S,4R,2’S-伊曲康唑晶型,因此,制备单一异构体2R,4S,2’S-伊曲康唑的稳定结晶,对于进一步研究该化合物的物理化学性质,研究其药物组合及临床应用,具有十分重要的意义。
技术实现要素:
为解决现有技术存在的上述技术问题,本发明提供了一种新的光学异构体2R,4S,2’S-伊曲康唑晶型,具有很好的稳定性,具有较好的药物活性。
为实现上述目的,本发明采用的技术方案是:
一种伊曲康唑晶型化合物,其特征在于:所述化合物为光学异构体2R,4S,2’S-伊曲康唑晶型化合物,其以2θ±0.2°衍射角表示的X-射线粉末衍射图谱在2.21°、3.37°、4.97°、5.38°、6.74°、8.21°、9.75°、11.07°、12.84°、13.86°、14.28°、15.05°、15.75°、18.27°、20.86°、21.34°、24.72°、25.28°、25.85°、28.34°、28.72°、29.12°和30.55°处显示有特征衍射峰。
作为优选的,所述的伊曲康唑晶型化合物,其特征在于,使用Cu-Kα射线测量得到的X-射线粉末衍射谱图如图1所示。
本发明还公开了所述的伊曲康唑晶型化合物的制备方法,其特征在于包括如下步骤:
a)将2R,4S,2’S-伊曲康唑溶解在40~60℃有机溶剂中,所述的有机溶剂为乙酸丙酯和石油醚的混合溶剂,石油醚和乙酸丙酯的体积比为1:4~6;
b)边搅拌,边降温,降温至10℃~15℃,析出晶体,继续降温至-5℃~0℃,保温搅拌养晶至析晶完全;
c)抽滤,收集晶体,少量乙醇洗涤,真空干燥,得到2R,4S,2’S-伊曲康唑结晶。
作为优选的,步骤a)中,溶质和溶剂的质量体积比为1:10~1:20。
作为优选的,步骤b)中,降温幅度为每分钟1℃~5℃,养晶温度为-5℃~0℃,养晶时间为0.5~10h。
作为优选的,步骤c)中,干燥温度为40℃~60℃。
本发明还公开了上述光学异构体2S,4R,2’S-伊曲康唑晶型在制备用于抗真菌感染和治疗肿瘤药物中的应用。
相对于现有技术,本发明具有以下的有益效果:
1、本发明所述的光学异构体2R,4S,2’S-伊曲康唑晶型晶体单一,纯度更高,稳定性更好,溶解度较高,具有很好的药物活性和较高的生物利用率。
2、本发明的晶型稳定性高,即使在较苛刻的储存条件下,也能够保持稳定,在随后的制剂制备和储存中不会改变。
3、本发明的制备方法简单,成本较低,容易实现规模化、工业化生产。
4、本发明所述的光学异构体2R,4S,2’S-伊曲康唑晶型,以及含有该晶型的药物组合物,不仅可用于抗真菌感染,还是一种有效的mTOR抑制剂,因此还可用于各种肿瘤(如非小细胞肺癌、前列腺癌等)的治疗。
附图说明
下面结合附图对本发明作进一步的说明。
图1是光学异构体2R,4S,2’S-伊曲康唑晶型的X-射线粉末衍射(XRD)谱图。
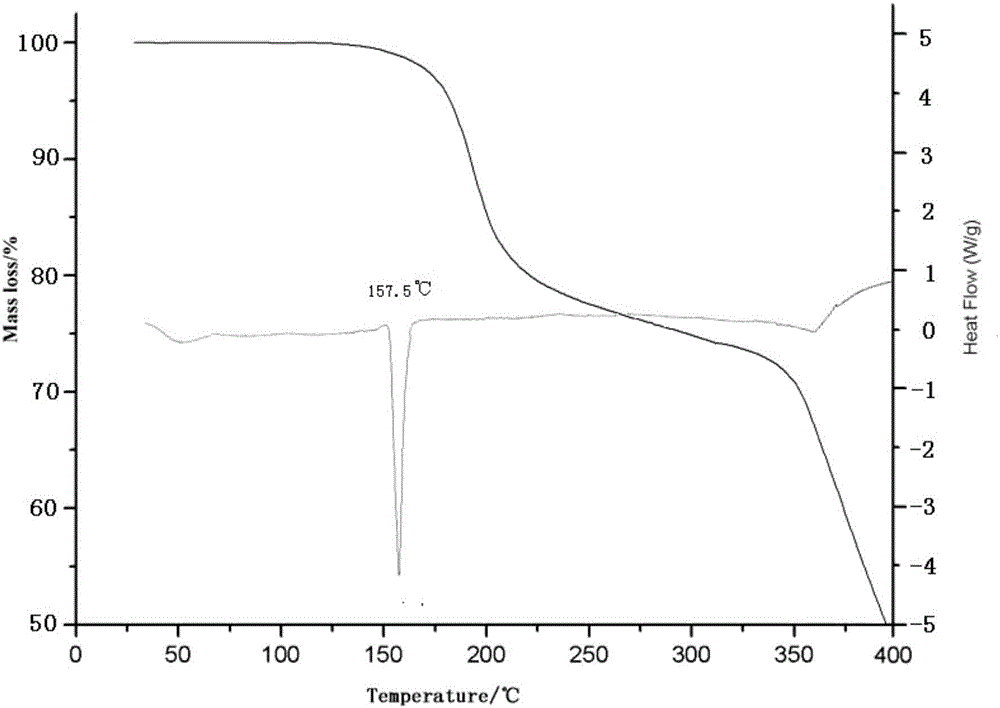
图2是光学异构体2R,4S,2’S-伊曲康唑晶型的TG-DSC图谱。
具体实施方式
为了更好的理解本发明的内容,下面结合具体实施例来做进一步的说明,但具体的实施方式并不是对本发明的内容所做的限制。
实施例1:
取光学异构体2R,4S,2’S-伊曲康唑15g于反应瓶中,加入300ml石油醚和乙酸丙酯的混合溶液(体积比为1:5),加热至40℃,搅拌溶清,边搅拌,边降温至10℃,析出固体,继续降温至0℃搅拌10h。真空抽滤,滤饼于50℃真空干燥6h,得13.5g白色针状固体,收率90.3%。
相关分析试验:
1、X-射线粉末衍射测试:
仪器型号:Bruker D8ADVANCE;光源Cu-Ka 40kV 40mA;石墨单色器;发散狭缝(DS):1°;LynxEye阵列探测器,扫描方式:θ/θ,连续扫描;扫描范围:0°~40°。实验结果:其X-射线粉末衍射谱图如图1所示,所述晶型以2θ±0.2°衍射角表示的X-射线粉末衍射谱图谱在2.21°、3.37°、4.53°、4.97°、5.38°、6.74°、8.21°、9.75°、11.07°、12.84°、13.86°、14.28°、15.05°、15.75°、18.27°、20.86°、21.34°、24.72°、25.28°、25.85°、28.34°、28.72°、29.12°和30.55°处显示出特征衍射峰。与市售伊曲康唑样品和专利CN201510350844.3公开的光学异构体2S,4R,2’S-伊曲康唑晶型的X-射线粉末衍射谱图谱比较,其图谱中衍射峰位置和强度完全不同,故其为一种新的晶型。
2、水分测定:用卡尔-费休氏法测得该物质中水分为0.23%,由水分结果可以看出该物质不含有结晶水,不是水合物,其水分只是吸附水。
3、差热分析和熔点测定:
对本发明制备的2R,4S,2’S-伊曲康唑晶体进行差热和热重分析,结果如附图2所示;结果表明,本品在150℃前没有吸收峰,说明样品中无结晶水或结晶溶剂;本品在157.5℃处有放热峰。本品经熔点测定:157~159℃。由现有技术可知伊曲康唑的熔点为165~169℃,从侧面证明了其为一种不同的晶型。
实施例2:
取光学异构体2R,4S,2’S-伊曲康唑15g于反应瓶中,加入150ml石油醚和乙酸丙酯的混合溶液(体积比为1:4),加热至60℃,搅拌溶清,边搅拌,边降温至15℃,析出固体,继续降温至-5℃搅拌6h。真空抽滤,滤饼于40℃真空干燥10h,得13.3g白色针状固体,收率88.5%。所制得晶体的使用Cu-Kα射线测量得到的X-射线粉末衍射谱图与实施例1相似。
实施例3:
取光学异构体2R,4S,2’S-伊曲康唑15g于反应瓶中,加入225ml石油醚和乙酸丙酯的混合溶液(体积比为1:5),加热至50℃,搅拌溶清,边搅拌,边降温至15℃,析出固体,继续降温至-5℃搅拌4h。真空抽滤,滤饼于60℃真空干燥4h,得13.8g白色针状固体,收率91.8%。所制得的2R,4S,2’S-伊曲康唑晶体使用Cu-Kα射线测量得到的X-射线粉末衍射谱图与实施例1相似。
实施例4:光学异构体2R,4S,2’S-伊曲康唑晶型的光照实验
将实施例3所提供的光学异构体2R,4S,2’S-伊曲康唑晶型均匀分摊至敞口培养皿中,厚度≤5mm,调节光照强度为4500±500Lx,30天后取样检测,并于0天的结果进行比照。结果见表1。
表1 光学异构体2R,4S,2’S-伊曲康唑结晶的光照实验
结果表明:未发生显著变化,在此条件下保持稳定。
实施例5:光学异构体2R,4S,2’S-伊曲康唑晶型的高温实验
将本发明实施例3所提供的光学异构体2R,4S,2’S-伊曲康唑晶型放置于密封铝箔袋中,置于60℃恒温干燥箱中,30天后进行检测,并于0天的结果进行比照。结果见表2。
表2 光学异构体2R,4S,2’S-伊曲康唑结晶高温实验
结果表明:未发生显著变化,在此条件下保持稳定。
实施例6:光学异构体2R,4S,2’S-伊曲康唑晶型的高湿实验
将本发明实施例3所提供的光学异构体2R,4S,2’S-伊曲康唑晶型开口置恒湿密闭容器中,在25℃于相对湿度(90±5)%条件下放置十天,于五、十天取样,按稳定性重点考察项目要求检测,同时准确称量试验前后供试品的重量,以考察供试品的吸湿潮解性能。结果见表3。
表3 光学异构体2R,4S,2’S-伊曲康唑晶型结晶高湿实验
结果表明:未发生显著变化,在此条件下保持稳定,无引湿性。
实施例7:光学异构体2R,4S,2’S-伊曲康唑晶型的加速实验
实验方法:按照《中华人民共和国药典》2010年版二部附录XIX C原料药与药物制剂稳定性试验指导原则中的方法进行。将本发明实施例3所提供的光学异构体2R,4S,2’S-伊曲康唑晶体放置于铝箔袋中,置于40±2℃,相对湿度为75±5%的恒温干燥箱中,1月、2月、3月和6月后分别进行取样检测,以考察其稳定性。结果见表4。
表4 光学异构体2R,4S,2’S-伊曲康唑结晶加速实验
结果表明,经6个月的加速试验,本发明实施例3所提供的2R,4S,2’S-伊曲康唑晶型各项质量指标均符合中国药典2010版标准要求,有关物质含量低,各指标均无明显变化,本品质量稳定性好。
实验例8:25℃下本发明伊曲康唑晶体化合物与现有技术晶型在水中的溶解度对比
试验品:本发明实施例1-3所制备的样品;
对照品1是市售伊曲康唑原料药;
对照品2是参照专利201510350844.3实施例2制备的光学异构体2S,4R,2’S-伊曲康唑晶型。
测定方法:将过量的试验品和对照品置于50ml锥形瓶中,加入30ml蒸馏水,25℃恒温搅拌72小时,取样5ml。样品经0.45μm微孔滤膜过滤,弃去初滤液,取续滤液20μL测定药物含量即为水中溶解度(mg/ml)。结果见表5:
表5 本发明晶型与现有技术晶型在水中的溶解度对比
从表55可以看出,25℃下,本发明所提供的2R,4S,2’S-伊曲康唑晶型在水中的溶解度与现有技术相比,有显著提高。
实施例9:光学异构体2R,4S,2’S-伊曲康唑晶型的药物活性试验
将本发明实施例3所提供的光学异构体2R,4S,2’S-伊曲康唑晶型与伊曲康唑对照品分别与HUVEC细胞和人原代肝细胞进行孵育,得到两种药物对细胞活性的抑制作用,其中试验品为本发明实施例3所制备的样品;对照品1是市售伊曲康唑原料药;对照品2是参照专利201510350844.3实施例2制备的光学异构体2S,4R,2’S-伊曲康唑晶型。结果见表6所示。
表6 光学异构体2R,4S,2’S-伊曲康唑伊曲康唑晶型的药物活性试验
由研究结果可知,本发明实施例3所提供的2R,4S,2’S-伊曲康唑晶型对人脐静脉内皮细胞(HUVEC)的抑制作用优于消旋体伊曲康唑,而对人原代肝细胞的抑制低于消旋体伊曲康唑,说明2R,4S,2’S-伊曲康唑晶体具有较高的抗肿瘤活性和较低的肝毒性。
- 还没有人留言评论。精彩留言会获得点赞!