制备具有改进的仓库储存稳定性的抑制淀粉的方法与流程
本发明涉及一种用于制备具有改进的仓库储存稳定性的抑制淀粉(inhibitedstarch)的方法,涉及使用所述方法制备的抑制淀粉,涉及使用所述抑制淀粉作为食物产品中的成分,并且涉及含有所述抑制淀粉的食物产品。
背景技术:
淀粉是食品工业的重要成分,并且非常常用于大量的食品应用和食品生产过程中。天然的未改性的淀粉,作为“天然淀粉”为本领域技术人员所知,其有时用于这些食品应用和食品生产过程中,但具有若干缺点。
淀粉在食品应用中的主要功能是作为增稠剂以便提供食物产品所要求的粘度、质地和口感。通过在水性悬浮液中加热颗粒淀粉时实现的颗粒淀粉的水合作用逐渐获得该质地和粘度性质。当温度升高到糊化温度以上时颗粒淀粉吸水,即淀粉颗粒水合和溶胀并且其粘度显著增加。在使用天然淀粉的情况下,水合和溶胀的淀粉颗粒不稳定,且因此,如果该温度保持较长时间或增加到更高温度,则粘度将达到其所谓的“峰值粘度”。因此,颗粒形状将被破坏并分解。其粘度将显著降低。除了降低的粘度外,另一个缺点是令人不悦的长而粘着的质地。
作为上述问题的结果,控制或避免这些问题的最重要的参数是高温、剪切力、以及特别是酸性条件。当厨师超出“峰值粘度”时,结果是颗粒结构的分解。相反,希望的是改变淀粉性质使得粘度稳定或甚至随时间而增加,从而避免当在高热、强剪切力和/或酸性条件下处理时粘度降低和颗粒分解。这维持了高度的水合溶胀但完整的水合淀粉颗粒。
所要求的效果通常被称为增加的淀粉稳健性。因此,颗粒淀粉更耐高温、较长的加热时间、强剪切力和酸性条件或这些参数的组合。
为淀粉提供增加的工艺耐受性的最常用的改性方法是使用称为化学交联的技术。化学交联抑制淀粉颗粒,所以当使其在水中加热时其溶胀受到抑制。如果交联水平太低,则结合或不结合强的物理力的连续加热将结束于完全或部分淀粉溶液。化学交联防止了在此类处理下的颗粒分解。通过用双功能试剂代替淀粉来实现化学交联,导致淀粉分子之间的共价键。这可以通过某些批准的方法和化学药品进行,例如三氯氧磷、stmp(三偏磷酸钠)、己二酸-醋酸混合酸酐和表氯醇。不同的批准的化学交联方法在文献中有很好的描述,且常用于淀粉工业中。在实践中,这意味着通过淀粉颗粒的交联,当暴露于温度和高剪切力或高温下、没有或具有低剪切程度时,淀粉颗粒将能够维持其颗粒完整性。交联程度越高,淀粉对抗高温、剪切力和酸性条件或这些参数的组合将越稳健。
在实践中,用于改变淀粉颗粒溶胀性质的这些交联技术可以适应于使用淀粉的应用和过程中,以便由于淀粉本身而获得粘度和质地形式的最佳性质。
在食品工业中,由于在食品成分中趋于“天然的”的趋势,所以非常希望的是用非化学改性的淀粉来代替化学改性的淀粉。淀粉将仍然具有与化学改性的淀粉相同的性质。
淀粉颗粒的非化学抑制可以用干热抑制(也称为碱性干烤)进行,类似于所谓的糊精(britishgums)。在该方法中,将淀粉经受在几乎完全不含水的条件下的高温组合通过添加例如氢氧化钠或苏打达到的碱性ph。温度为120℃-160℃,ph为8-11,反应时间为2-120小时,给出不同的抑制水平。该技术被熟知且披露于文献中(cross-linkingofstarchbyalkaliroasting,journalofappliedpolymersciencevol.11pp1283-1288(1967)[通过碱性干烧的淀粉的交联,应用聚合物科学期刊,第11卷,第1283-1288页(1967)];irvinmartin,nationalstarchandchemicalcorporation[irvinmartin,国家淀粉与化学公司])且披露于几项专利中(us8,268,989b2;ep0721471;ep10382882;us-a-3977897;us4,303,451;日本专利号61-254602;us4,303,452和us-a3490917)。
淀粉的热抑制问题在于副反应淀粉给出不希望的味道和颜色。在高于大约130℃的温度下发生淀粉的变色。为了避免副反应的问题,可以降低温度,但这导致反应时间延长,从而显著增加生产成本。此外,热抑制技术需要高能量成本和高投资成本。
进一步已知的是,通过使淀粉颗粒经过低浓度的漂白剂(即碱性ph下的氧化剂(氧化试剂)连同所谓的不同的含氮化合物的氧化改性剂)处理来实现弱抑制。在一些情况下,提取后剩余的淀粉颗粒中的残留蛋白质可以用作氧化改性剂,但通常需要比现在商业淀粉较不纯的淀粉,具有即淀粉干物质的0.4%以上的蛋白质含量。该抑制技术是已知的并且披露于美国专利号2,317,752和英国专利申请gb2506695中。然而,后两种抑制淀粉的方法只能达到有限的抑制水平。如果添加更高水平的氧化剂,则淀粉将被氧化,导致去聚合,这导致粘度降低并且在烹饪期间更容易破坏颗粒结构。
还已知抑制颗粒淀粉可以通过组合氧化剂和氨基酸甘氨酸来实现。该过程披露于美国专利no.3,463,668中。然而,该方法导致不稳定的临时抑制,从而不能替代食品工业中颗粒淀粉的化学交联。
因此,需要开发一种抑制淀粉至更高水平的方法,即导致具有改进的味道、气味和颜色等性质的抑制淀粉的方法,并且该方法比传统的生产技术更具成本效益并且克服了在前文描述的技术中的缺点。还需要抑制食品淀粉以及从其生产的食物产品,该抑制食品淀粉在仓库中的储存期间是稳定的并且具有改进的感官特性。
技术实现要素:
本发明的目的是满足上述需要并提供所披露的、具有所希望的有利性质的抑制淀粉。该目的通过根据如权利要求1中所定义的本发明的方法来实现。该目的还通过在扩展的储存条件下稳定的抑制淀粉、通过使用其作为食物产品中的成分、以及通过含有所述抑制淀粉的食物产品来实现,如所附的独立权利要求中所定义的。在从属权利要求中披露了具体以及优选的实施例。
本发明的一个方面涉及一种用于制备具有改进的仓库储存稳定性的抑制淀粉的方法,其中该方法包括以下步骤
a)提供包含从含有原材料的淀粉中获得的天然颗粒淀粉的浆液,
b)向该浆液中添加至少一种氨基酸或这些氨基酸中的两种或更多种的组合以及至少一种氧化剂,以便在烹调期间抑制颗粒淀粉的溶胀,
c)向该浆液中添加至少一种有机酸或亚硫酸氢盐,以便消除残留的氧化剂化学药品、异味和不希望的气味,并且
d)向该浆液中添加至少一种抗氧化剂,以便在仓库储存期间稳定已实现的淀粉抑制。
在另一个方面,本发明涉及用根据本发明的方法制备的具有改进的仓库储存稳定性的抑制淀粉。
在又另一个方面,本发明涉及所述抑制淀粉作为食物产品中的成分的用途。
在进一步的方面,本发明是含有所述抑制淀粉的食物产品。
更准确地说,本发明提供了一种用于抑制颗粒淀粉至更高的抑制水平的方法,对于该方法所实现的抑制是稳定的,其中该抑制的颗粒淀粉还具有例如对抗温度升高、剪切力和酸性条件的粘度稳定性等有益的特性。这意味着被抑制的淀粉将具有增加的工艺稳健性,即在某些食品工艺(例如在高于淀粉的天然糊化温度的加工温度下进行的高压均质化)中变得更有抗性。此外,所述抑制颗粒淀粉在几摄氏度下具有增加的糊化温度,其中在这类食品工艺中该抑制颗粒淀粉更能维持其天然结构,即颗粒形状。
伴随本发明的进一步的优点是中和或消除了通常在不用化学交联制成的常规抑制淀粉中表达的令人不悦的异味。又另一个优点是,最初从淀粉原材料(即天然淀粉已经从其中提取的原材料来源)中分离的蛋白质(更准确地说,其中天然存在的氨基酸和其中分子量低于1kda的肽)可以用作参与本发明方法的氨基酸添加物的来源。这意味着抑制可以仅从与提取淀粉相同的原材料进行,或者该抑制可以通过使用合成的氨基酸或来自外来蛋白质来源的氨基酸来制得。
附图说明
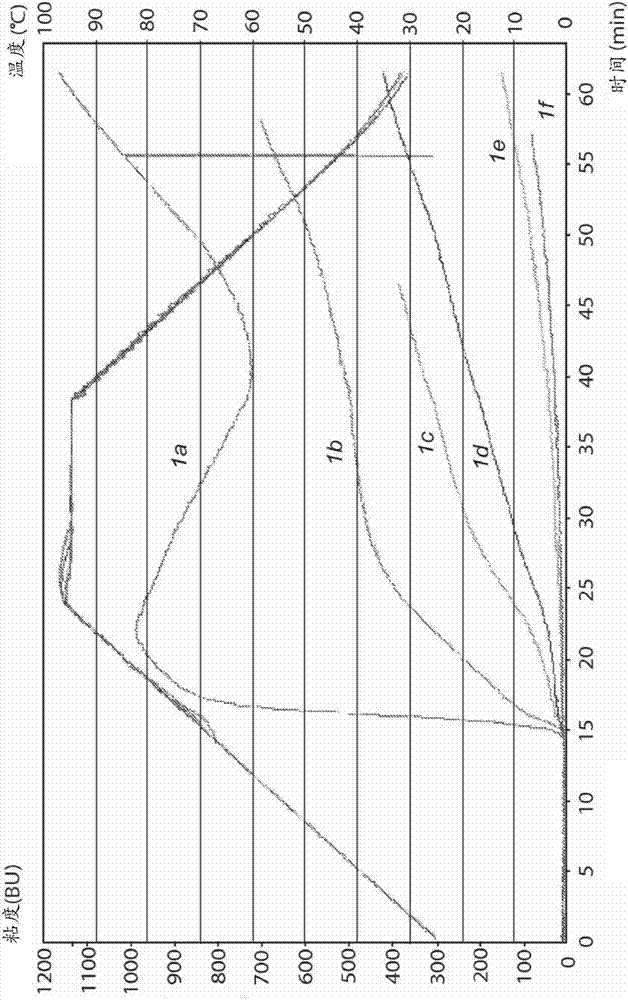
图1示出了根据实例1a)-1f)抑制淀粉在中性ph下的brabender粘度曲线。使用brabenderamyloviscograph型号e。活性氯:0.1%-0.8%w/w的dm淀粉。甘氨酸:33.3%w/w的活性氯。因此,活性氯和甘氨酸之间的比例为3:1。淀粉浓度:5%w/w。350cmg扭转弹簧。在测量中使用蒸馏水制备淀粉浆液。
图2示出了根据实例1a)-1f)抑制淀粉在ph3下的brabender粘度曲线。使用brabenderamyloviscograph型号e。活性氯:0.1%-0.8%w/w的dm淀粉。甘氨酸:33.3%w/w的活性氯。因此,活性氯和甘氨酸之间的比例为3:1。淀粉浓度:5%w/w。350cmg扭转弹簧。在测量中使用蒸馏水制备淀粉浆液。
图3示出了根据实例2a)-2b)抑制淀粉在中性ph下的brabender粘度曲线。使用brabenderamyloviscograph型号e。活性氯:0.4%w/w的dm淀粉。甘氨酸:33.3%w/w的活性氯。因此,活性氯和甘氨酸之间的比例为3:1。将该粘度曲线与不添加甘氨酸但添加相同的活性氯的抑制淀粉产物进行比较。淀粉浓度:5%w/w。350cmg扭转弹簧。在测量中使用蒸馏水制备淀粉浆液。
图4示出了根据实例2a)-2b)抑制淀粉在ph3下的brabender粘度曲线。活性氯:0.4%w/w的dm淀粉。甘氨酸:33.3%w/w的活性氯。因此,活性氯和甘氨酸之间的比例为3:1。将该粘度曲线与不添加甘氨酸但添加相同的活性氯的抑制淀粉产物进行比较。淀粉浓度:5%w/w。350cmg扭转弹簧。在测量中使用蒸馏水制备淀粉浆液。
图5示出了根据实例3抑制淀粉在中性ph下的brabender粘度曲线。活性氯:0.4%w/w的dm淀粉。甘氨酸:33.3%w/w的活性氯。因此,活性氯和甘氨酸之间的比例为3:1。淀粉浓度:5%w/w。350cmg扭转弹簧。在测量中使用蒸馏水制备淀粉浆液。该图示出了抑制水平如何随时间而变化,以及因此储存后抑制作用如何降低。曲线3a)=第1天;曲线3b)=第2天;曲线3c)=第3天。
图6示出了根据实例4抑制淀粉在中性ph下的brabender粘度曲线。活性氯:0.4%w/w的dm淀粉。甘氨酸:33.3%w/w的活性氯。因此,活性氯和甘氨酸之间的比例为3:1。添加9.5克柠檬酸作为抗氧化剂,以便使抑制随时间而稳定。淀粉浓度:5%w/w。350cmg扭转弹簧。在测量中使用蒸馏水制备淀粉浆液。4a=第1天;4d=300天储存时间。
图7示出了根据实例5抑制淀粉在中性ph下的brabender粘度曲线。通过组合苏氨酸和次氯酸钠来实现抑制。在brabender运行中的淀粉固体水平:5%w/w。扭转弹簧:350cmg。在测量中使用蒸馏水制备淀粉浆液。
图8示出了根据实例5抑制淀粉在ph3下的brabender粘度曲线。通过组合苏氨酸和次氯酸钠来实现抑制。在brabender运行中的淀粉固体水平:5%w/w。扭转弹簧:350cmg。在测量中使用蒸馏水制备淀粉浆液。
图9示出了根据实例6抑制淀粉在中性ph下的brabender粘度曲线。通过组合色氨酸和次氯酸钠来实现抑制。在brabender运行中的淀粉固体水平:5%w/w。扭转弹簧:350cmg。在测量中使用蒸馏水制备淀粉浆液。
图10示出了根据实例6抑制淀粉在ph3下的brabender粘度曲线。通过组合色氨酸和次氯酸钠来实现抑制。在brabender运行中的淀粉固体水平:5%w/w。扭转弹簧:350cmg。在测量中使用蒸馏水制备淀粉浆液。
图11示出了根据实例7抑制淀粉在中性ph下的brabender粘度曲线。通过将来源于马铃薯淀粉来源的氨基酸混合物与次氯酸钠组合来实现抑制。在brabender运行中的淀粉固体水平:5%w/w。扭转弹簧:350cmg。在测量中使用蒸馏水制备淀粉浆液。
图12示出了在中性ph和16%dm淀粉下使用brabender粘度曲线评估糊化温度的结果。使用250cmg的扭转弹簧。将根据实例9的抑制淀粉与天然蜡质玉蜀黍(waxymaize)(玉米)淀粉(参比淀粉)以及与具有相似抑制水平的碱性干烤蜡质玉蜀黍(玉米)淀粉进行比较。
图13示出了根据实例8处理的淀粉在中性ph下的brabender粘度曲线。天然马铃薯淀粉用0.8%w/w活性氯处理。淀粉浓度:5%w/w。使用700cmg的扭转弹簧。在测量中使用蒸馏水制备淀粉浆液。
图14示出了根据实例13a-c)处理的淀粉在中性ph下的brabender粘度曲线。通过组合甘氨酸同系物和次氯酸钠来实现抑制。在brabender运行中的淀粉固体水平:5%w/w。扭转弹簧:350cmg。在测量中使用蒸馏水制备淀粉浆液。
具体实施方式及其优选实施例
首先,将定义在本申请文本中出现的一些表达。
在整个申请文本中使用的表达“天然淀粉”旨在表示经提取和纯化的淀粉,即具有dm淀粉的最多0.4%(优选低于该值)的残留蛋白质含量,对于该经提取和纯化的淀粉天然存在的性质尚未经过化学或物理改变。因此,该淀粉仍然处于其天然状态并且具有未改变的性质。术语天然淀粉是本领域技术人员熟知的。
在整个申请文本中使用的表达“氨基酸样化合物”旨在表示一组具有一个或多个氨基-nh2和一个或多个羧基-cooh被或不被任何其他基团取代的有机化合物中的任何一个。这样的“氨基酸样化合物”可以用作本文披露的方法中的氨基酸的补充或替代物。
在整个申请文本中使用的表达“氨基酸同系物”旨在表示氨基被一个或多个基团取代的相同骨架的氨基酸。
在整个申请文本中使用的表达“蛋白质水解产物”旨在表示来自不同来源的纯化的蛋白质浓缩物,其通过酸和高于95℃的高温、和/或通过用蛋白水解酶处理这样的蛋白质已经被水解。水解的结果是将蛋白质组分离成具有不同分子量的肽和游离氨基酸(即由不同数量的氨基酸结构单元组合)和/或分离成单个氨基酸。为了能够将淀粉颗粒渗入其半结晶结构的非晶形部分,肽的大小应在1kda以下。因此,表达“蛋白质水解产物”意指大小在1kda以下的肽和氨基酸单体的未定义混合物,因此可以用作本发明中的含有氨基的反应物部分。
在整个申请文本中使用的表达“氨基酸衍生物”旨在表示被另一个化学基团取代的氨基酸。
在整个申请文本中使用的表达“仓库储存稳定性”旨在表示在仓库和运输中的典型条件下,这样的抑制淀粉维持其抑制水平。
在整个申请文本中使用的表达“计算为活性氯”旨在表示与氧结合成活性氧化剂cio-中的单体形式的氯(摩尔重量为35.5)的量。
在整个申请文本中使用的表达“dm”旨在表示“干物质”(drymatter),其是从真空下蒸发溶液至干燥获得的总固体的量度。dm也可以被称为“通过干燥的总固体”或“干固体”。具有等价含义的替代性表达是“干物质”(drysubstance)和“干重”(dryweight)。
在整个申请文本中使用的表达“含有活性氯(xg/l)”和“dm淀粉的%w/w活性氯”旨在表示结合到活性氧化剂中的cio-中的单体氯量,以克/升计,和来自每克dm淀粉的cio-中的每克cl,以重量百分比计。
在整个申请文本中使用的表达“%w/wdm淀粉”旨在表示以每克dm淀粉中的克数计算的所定义的物质的百分比。
在整个申请文本中使用的表达“蛋白质转化因子”旨在表示用于将分析的%氨基氮(%n)重新计算为蛋白质的转化因子。用于分析蛋白质含量的熟知的方法是所谓的“凯氏定氮法”(kjeldahlmethod),其中测量氨基氮的百分数,并随后通过使用文献中所发现的转化因子重新计算蛋白质的量,这取决于不同蛋白质来源中的平均氮含量。
在本申请文本中的实例中使用的表达“扭转弹簧为250、350或700cmg”旨在表示当评估这样的淀粉糊的粘度曲线时brabenderamylograph扭转弹簧的设置。不同的扭转弹簧由于弹簧的灵敏度而给出不同的反应,因此需要定义使用何种扭转弹簧用于了解粘度反应水平并能够比较不同的brabender曲线。“扭转弹簧cmg”的表达和含义是本领域技术人员熟知的,并且常用于淀粉糊的测量。
在本发明方法中将被抑制的天然淀粉可以从各种各样的原材料中提取,例如马铃薯淀粉、玉蜀黍(玉米)淀粉、木薯淀粉、大麦淀粉、大米淀粉、小麦淀粉、黑麦淀粉、燕麦淀粉、苋菜淀粉、藜麦淀粉、西米淀粉、菜豆淀粉、豌豆淀粉、佛罗里达(floridian)淀粉及其不同品种、蜡质马铃薯淀粉、蜡质玉蜀黍(玉米)淀粉、蜡质木薯淀粉、蜡质大麦淀粉、蜡质大米淀粉、蜡质高粱淀粉、蜡质小麦淀粉、蜡质豌豆淀粉和高直链淀粉等。在淀粉生产过程中,淀粉从原材料中提取、纯化并干燥成粉末,所以称为天然淀粉。来自各种来源的淀粉,例如上文所列出的原材料,可以用于食品应用,无论是处于天然状态下还是用不同技术进一步修饰以给出所希望的性质。
来自不同来源的天然淀粉的生产、天然淀粉的改性方法及其伴随性质是本领域熟知的。
如上所披露,最常用的改性方法之一是化学交联,其旨在使淀粉对抗热、剪切力和酸性条件更有抗性。
在根据本发明的方法的一个实施例中,使用的是蜡质淀粉,即淀粉dm的支链淀粉含量大于90%的富含支链淀粉的淀粉。富含支链淀粉的淀粉被认为是更稳定的,不需要通过化学单基取代以阻止回生(例如乙酰化和羟丙基化)来稳定。众所周知,当提到水合淀粉糊在水中糊化后的的稳定性,所谓的蜡质淀粉比具有较高量的支链淀粉(非蜡质淀粉)的淀粉具有更好的稳定性性质。当提到冻熔稳定性,对于蜡质淀粉来说,稳定性性质也更好。因此,通过将本发明与蜡质淀粉即蜡质玉蜀黍(玉米)、蜡质木薯、蜡质大麦等组合,可以获得具有与化学改性的非蜡质淀粉相当的性质的淀粉产物。从这个角度,可以产生可以与化学改性的稳定的淀粉(即乙酰化和/或羟丙基化淀粉)竞争的淀粉产物。该淀粉的单基取代稳定性与在仓库中的储存期间用本发明获得的稳定性不同。进行淀粉的单基取代稳定化以改善溶液对抗回生的稳定性,而不是使抑制稳定。
在根据本发明的方法中,通过添加氨基酸和氧化剂(氧化试剂)的组合抑制淀粉颗粒来改变天然淀粉或化学改性的稳定化单基取代淀粉的性质。通过提取天然淀粉并将其纯化至残留蛋白质的量低于0.4%w/w的水平来获得抑制淀粉,其中所述淀粉被认为是无蛋白质的淀粉。将天然淀粉进一步与水混合,产生具有5%-45%w/w、更优选20%-35%w/w、甚至更优选25%-30%w/w浓度的淀粉浆液。然后在连续搅拌期间将淀粉浆液加热至5℃-70℃,即低于在周围ph条件下使用的特定淀粉的糊化温度,优选15℃-45℃,更优选25℃-35℃,以避免沉降。用酸或碱调节ph值以获得通常为7-12的值,但是这也可能位于该范围之外,因为不同的氨基酸在处理期间需要不同的ph水平。然而,由于本工艺中使用的活性氯将形成氯气将避免酸性ph,因个人健康风险而不希望出现该酸性ph,并且过高的碱性ph将引起碱性糊化发生。
可以在搅拌期间将至少一种氨基酸或这些氨基酸中的两种或更多种的组合添加到淀粉浆液中。添加的氨基酸的量为0.01%-10%w/wdm淀粉、优选0.05%-3%w/wdm淀粉、更优选0.05%-2.0%w/wdm淀粉。在反应中使用的氨基酸可以从天然来源或合成制备获得,但优选单独使用或以其两种或更多种的任意组合使用的天然存在的氨基酸。在一个有用的实施例中,所述氨基酸来源于相同的淀粉来源,即原材料,将被抑制的淀粉来源于该原材料。在该实施例中,富含蛋白质的片段与淀粉来源分离,并且进一步分级、纯化并水解成富含氨基酸的浓缩物,将其用作抑制反应物。因此,以这种方式,可以获得抑制的淀粉产物而不需要将任何合成来源的氨基酸或从其他原材料中获得的氨基酸添加到反应浆料中,这必须被认为是有益的。在添加用于迁移的氧化剂至淀粉颗粒中之前,将浆液置于搅拌下,例如持续5-15分钟。添加的天然氨基酸的实例是丙氨酸、半胱氨酸、天冬氨酸、谷氨酸、苯丙氨酸、甘氨酸、组氨酸、异亮氨酸、赖氨酸、亮氨酸、甲硫氨酸、天冬酰胺、脯氨酸、谷氨酰胺、精氨酸、丝氨酸、苏氨酸、缬氨酸、色氨酸和酪氨酸、或这些的同系物。同系物的实例是甘氨酸同系物肌氨酸(甲基甘氨酸)、二甲基甘氨酸和甜菜碱(三甲基甘氨酸)。氨基酸样化合物的实例是伞菌氨酸、阿拉诺新、阿司帕坦、天冬氨酰葡糖胺、磺乙谷酰胺、牛磺酸、四唑基甘氨酸、曲辛和胸腺素。上述所列出的氨基酸和氨基酸样化合物的光学异构体的不同形式也尽可能地包括在内使用。
然后将可能是漂白剂的氧化剂在搅拌下添加到淀粉和氨基酸混合物中。氧化剂是活性氯的来源,并且在一个实施例中为次氯酸盐。在特别有用的实施例中,氧化剂是次氯酸钠或另一种类的碱金属或碱土金属次氯酸盐,例如次氯酸钾、次氯酸钙和次氯酸镁。虽然可以使用不同种类的次氯酸盐,但是本发明不限于此类氧化剂。因此,活性氯的其他来源可以单独使用或作为提供活性氯的这样的不同种类的氧化剂的混合物使用。氧化剂的作用尚未完全清楚,但很明显需要氧化剂,并且假定它以某种方式与氨基酸反应,使得其可以与淀粉分子反应并形成交联键。在替代性理论中,假设氧化剂和氨基酸作为催化剂起作用,使得淀粉分子可以直接彼此相互作用以反应并形成交联键。在次氯酸钠作为氧化剂的情况下,氧化剂的添加量以活性氯的添加量计算为0.03%-30%w/w、优选0.1%-10%w/w、更优选0.15%-4%w/w。然后将浆液置于搅拌下,使得可以发生抑制反应。该反应几乎是瞬时的,但由于实际原因,更方便的是使反应进行更长时间以避免活性氯残留在反应容器中。因此,反应时间为1-1200分钟、优选为30-240分钟、更优选为30-180分钟。
本领域技术人员熟知的是,用次氯酸钠处理淀粉将使淀粉氧化,从而导致淀粉分子的分解,其降低了淀粉的分子量,从而降低了其粘度。用次氯酸钠进行氧化反应使淀粉稍微稳定而不会回生。因此,重要的是明确指出,根据本发明的方法,避免了羧基的氧化引入,因此,不会发生造成淀粉结构分解的氧化。当通过氧化试剂(例如次氯酸钠)进行氧化时,在淀粉分子中产生羧基-cooh。这是本领域技术人员熟知的,并且在关于淀粉氧化的文献中可以找到进一步的具体信息。因此,羧基水平的分析可以用作确定淀粉产物是否已被氧化的方法,并且也可以用作定义氧化水平的方法。
羧基含量的分析方法是按照“改性食品淀粉的纯度标准”所述的以及在fao/who文件或再欧盟(eu)法律中找到的官方方法进行的,其中方法采用在环境温和溶液而不是热溶液以及0.01mnaoh溶液而不是0.1mnaoh中进行滴定。
根据国际法律和欧盟法律,可以添加至淀粉中且仍然被认为不被氧化的羧基的最高含量为0.1%w/wdm淀粉。作为这的结果,由此可以确定淀粉产品是否已被氧化试剂处理并且因此是否已被氧化或仅被漂白。已经阐明,根据本发明,当氧化剂与根据本发明方法的氨基酸组合时,在淀粉中不会形成羧基,因为当它自身用氧化剂氧化时,很明显没有发生淀粉分子的氧化,即添加的淀粉dm的羧基低于0.1%。
对于根据实例7c)的产物,形成的羧基的量显示于表1中。因此,用0.91%w/wdmpaac(马铃薯氨基酸浓缩物)和0.73%w/w活性氯处理马铃薯淀粉,将该产物与天然马铃薯淀粉进行比较。使用马铃薯淀粉,必须针对天然淀粉中天然存在的酸性磷酸基团的水平来调节滴度的读数。可以看出,其本身用0.73%w/w活性氯处理的淀粉中羧基的量从0.24%w/w增加到0.38%w/w,即增加0.14%w/w,且因此被定义为氧化淀粉。从而,定义了根据本发明方法已经用0.73%w/w活性氯处理而不添加氨基酸的淀粉被氧化。相反已经根据实例7c)处理的、即具有相同量的活性氯、但与氨基酸paac组合的淀粉,仅具有0.28%w/w的羧基基团,即,以及0.04%w/w的增加的水平。从而,显然通过将活性氯与氨基酸组合,避免了淀粉分子的氧化,并且相反获得对淀粉颗粒的抑制。
表1
对于根据实例1d)的产物,即用0.4%w/w活性氯和0.133%w/w甘氨酸处理的蜡质玉蜀黍(玉米)淀粉,羧基的量显示于表2中。将该淀粉产物与天然蜡质玉蜀黍(玉米)淀粉进行比较,因为必须用天然蜡质玉蜀黍(玉米)淀粉天然存在的水平调节羧基的水平。可以看出,根据实例1f)处理的淀粉中的羧基的量,即0.8%w/w的活性氯的量不增加。因此,该水平与天然蜡质玉蜀黍(玉米)淀粉中的相同,即0.021%w/w。可以看出,根据实例1f)即用0.8%w/w活性氯和0.267%w/w甘氨酸处理的淀粉中的羧基的量,仅从0.021%w/w略微增加到0.026%w/w。因此,羧基的增加仅为淀粉dm的0.005%w/w。从而,显然通过将活性氯与氨基酸组合,避免了淀粉分子的氧化,并且相反获得对淀粉颗粒的抑制。
表2
当抑制反应已经完成时,在洗涤和脱水之前添加有机酸,以便消除使淀粉产物具有令人不悦的游泳池水(即加氯水)的异味或气味的化学残留物,该异味或气味对于已经用次氯酸盐处理的淀粉是常见的。有机酸的种类可以选自通常用于食物产品中的任何一种有机酸,但优选的是具有作为还原剂的能力的酸,如抗坏血酸,其在过去已被用于减少在用次氯酸钠或氯气处理水后在饮用水中氯胺的形成。有机酸的实例是柠檬酸、己二酸、异抗坏血酸、乳酸钠、乳酸钾、乳酸钙、抗坏血酸、磷酸和琥珀酸。有机酸可以单独添加,或以这些有机酸中的两种或更多种的组合添加。在一个实施例中,使用抗坏血酸作为有机酸,因为已经证明其在减少不希望的残留反应物方面特别有效。有机酸的添加量为0.001%-5%w/wdm淀粉、优选0.01%-3%w/wdm淀粉、更优选0.05%-1%w/wdm淀粉。将浆液置于搅拌下,例如持续15-60分钟。
可替代地,可以使用无机酸例如磷酸、硫酸和盐酸,但是发现其效率低得多。
消除味道和气味问题的替代性方法涉及添加亚硫酸氢盐。这是本领域技术人员为了破坏次氯酸根离子或氯气的过量而使用的熟知的方法,使其不再具有任何氧化能力。然而,使用亚硫酸氢盐不是优选的,因为在国际食品法律中视其为有效的过敏原,并且如果淀粉中存在超过10ppm的残留水平,则当用于食物产品中时必须将其标记为过敏原。根据本发明方法迄今为止生产的抑制淀粉是不稳定的且仅是临时的,这意味着当随时间储存时其丧失其抑制作用。当抑制淀粉存在于浆液中时或在淀粉干燥后,在储存期间抑制将分解,并且丧失其调节淀粉颗粒的溶胀的作用,结束于与天然非抑制淀粉相当的淀粉产物。已经发现抑制将相当快速地分解,并且在正常条件下在仓库中仅仅几周的储存时间之后,抑制或多或少完全丧失。根据本发明的方法,以及当使用美国专利号3,463,668中披露的方法时,这同样适用于迄今为止生产的抑制淀粉。然而,本发明已经发现通过添加抗氧化剂可以稳定这样的不稳定的抑制作用。抑制作用如何通过添加抗氧化剂来稳定还不完全清楚,但是实验表明,如果通过添加抗氧化剂淀粉被抑制且不稳定,并且在不与氧气接触的条件下储存,则抑制是稳定的。从而,结论是由于氧化而导致的抑制作用丧失,但是通过添加抗氧化剂,当储存在与空气接触时,抑制作用因此被稳定。抗氧化剂可以选自用于食物产品中的所有可用的抗氧化剂。抗氧化剂的添加量为0.001%-10%w/wdm淀粉、优选0.01%-5%w/wdm淀粉、更优选0.1%-3%w/wdm淀粉。然后将浆液置于搅拌下,例如持续15-60分钟。
抗氧化剂的实例是抗坏血酸、抗坏血酸钠、抗坏血酸钙、异抗坏血酸、异抗坏血酸钠、乳酸钠、乳酸钾、乳酸钙、柠檬酸、柠檬酸一钠、柠檬酸二钠、柠檬酸三钠、柠檬酸一钾、柠檬酸三钾、柠檬酸一钙、柠檬酸二钙、柠檬酸三钙、l-酒石酸、l-酒石酸一钠、l-酒石酸二钠、l-酒石酸一钾、l-酒石酸二钾、l-酒石酸钠钾、磷酸、磷酸一钠、磷酸二钠、磷酸三钠、磷酸一钾、磷酸二钾、磷酸三钾、磷酸一钙、磷酸二钙、磷酸三钙、磷酸一镁、磷酸二镁、苹果酸钠、苹果酸氢钠、苹果酸钾、苹果酸钙、苹果酸氢钙、内消旋酒石酸、l-酒石酸钙、己二酸、己二酸钠、己二酸钾、琥珀酸、柠檬酸三铵。用于稳定淀粉抑制的抗氧化剂可以在抑制反应发生之后单独添加或以其两种或更多种的任何组合添加。
发生抑制反应的温度是非热的,即可以在低于100℃(例如在5℃和70℃之间)的温度下进行。与在淀粉几乎无水分条件下发生抑制的干热抑制过程相反,对于浆液这样的抑制是可能的。然后可以通过使用淀粉生产中使用的任何已知的改性方法来进一步使在浆液中的稳定的抑制淀粉改性,这些改性方法是:例如批准的食品添加剂化学改性和/或物理改性,例如乙酰化、羟丙基化、化学交联、osa改性、酶处理、糊精化、糊化以便使淀粉具有冷水可溶性、和在抑制前预糊化以便使淀粉具有冷水溶胀性、和/或其两种或更多种的组合。此后,可将其作为食品生产中的成分进行回收和添加。可替代地,可以通过进一步的洗涤和干燥从浆液中回收稳定的抑制淀粉,然后可以作为成分添加到食物产品中。
可以使用抑制淀粉的食物产品的实例是不同种类的调味汁、汤类、乳制品(例如发酵的法式奶油和酸奶)、面糊和面包、用于乳制品和/或烘焙产品的水果制剂(例如烘焙稳定的水果制剂)、和基于牛奶的甜点(例如不同的布丁、香草酱、冰淇淋和奶油冻等)。
实例:
下面披露了根据本发明的方法的一些实例。
实例1
实例1a)-f)披露了使用甘氨酸与次氯酸钠组合来抑制天然的颗粒淀粉至不同水平的方法。使用的天然的颗粒淀粉原材料是具有残留蛋白质含量小于0.4%的蜡质玉蜀黍(玉米)淀粉,如凯氏定氮法所分析并用6.25的蛋白质转化因子计算的。
1a)0.1%活性氯
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.29g(0.033%w/w)甘氨酸。在搅拌期间添加9.7g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.1%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
1b)0.2%活性氯
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)甘氨酸。在搅拌期间添加19.3g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.2%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
1c)0.3%活性氯
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.87g(0.1%w/w)甘氨酸。在搅拌期间添加29g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.3%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
1d)0.4%活性氯
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加1.16g(0.133%w/w)甘氨酸。在搅拌期间添加38.7g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.4%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
1e)0.6%活性氯
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加1.74g(0.20%w/w)甘氨酸。在搅拌期间添加57.9g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.6%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
1f)0.8%活性氯
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加2.32g(0.267%w/w)甘氨酸。在搅拌期间添加77.3g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.8%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
实例1a)-1f)中获得的产物用brabenderamyloviscograph型号e、以5%w/w的干固体含量、使用蒸馏水和350cmg的扭转弹簧进行评估。该评估是在中性ph值和在ph3下进行的。
从图1和图2中可以看出,当添加更高水平的活性氯时,达到增加的抑制。因此,抑制水平与活性氯的浓度成比例。还可以看出,在0.6%-0.8%w/w活性氯下连同甘氨酸一起达到的抑制水平比仅通过添加活性氯至处于其天然状态下的相同淀粉可能达到的抑制水平高得多。因此,氨基酸和活性氯的组合产生更高的抑制水平。
实例2
实例2a)和2b)披露了一种用甘氨酸与次氯酸钠组合抑制颗粒淀粉的方法,以及与不添加甘氨酸但添加相同量的活性氯的情况下相同的天然的颗粒淀粉的抑制相比达到的抑制水平。颗粒淀粉原材料是具有残留蛋白质含量小于0.4%的蜡质玉蜀黍(玉米)淀粉,如凯氏定氮法所分析并且用6.25的蛋白质转化因子计算的。
2a)0.4%活性氯+甘氨酸
将869.1g的dm蜡质玉米淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加1.16g(0.133%w/w)甘氨酸。在搅拌期间添加38.7g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.4%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
2b)0.4%活性氯
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600克冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加38.7g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.4%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。该实例实际上是根据美国专利号2,317,752中披露的进行以显示与本发明相比的行为上有何不同。
实例2a)和2b)中获得的产物用brabenderamyloviscograph型号e、以5%w/w的干固体水平、使用蒸馏水和350cmg的扭转弹簧进行评估。在中性ph下(其中结果显示于图3中)和在ph3下(其中结果显示于图4中)进行评估。
图3和图4中的结果说明与仅通过向具有天然存在的残留蛋白质含量的淀粉中添加次氯酸钠实现的抑制相比,通过将氨基酸甘氨酸添加到反应中实现了高得多的抑制水平。这表明与用单独的活性氯达到的抑制相比,通过将氨基酸(在该实例中为甘氨酸)与活性氯组合达到了高得多的抑制水平。
实例3
实例3披露了一种用甘氨酸与次氯酸钠组合抑制颗粒淀粉至不同的抑制水平的方法。实例3进一步说明了根据在美国专利号3,463,668中披露的前述发明的方法中通过组合氨基酸和氧化试剂实现抑制时获得的淀粉颗粒的不稳定的暂时性抑制的问题。
在实例3中使用的天然的颗粒淀粉是具有残留蛋白质含量小于0.4%的蜡质玉蜀黍(玉米)淀粉,如凯氏定氮法所分析并且用6.25的蛋白质转化因子计算的。
3)0.4%活性氯+甘氨酸
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加1.16g(0.133%w/w)甘氨酸。在搅拌期间添加38.7g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.4%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
将实例3中获得的产物在环境条件下储存,并且用brabenderamyloviscograph型号e、在5%dm的淀粉含量下、在不同储存时间后、使用蒸馏水进行评估。使用350cmg的扭转弹簧。在中性ph下进行评估。
来自实例3的结果如图5所示,表明如在美国专利号3,463,668中披露的先前发明中使用的、通过组合氨基酸与氧化试剂获得的抑制是不稳定的,并且在储存期间抑制水平降低。在图5中标示为3a)的曲线表示在第1天的粘度曲线,标示为3b)的曲线表示储存30天,并且标示为3c)的曲线表示储存200天。
实例4
实例4披露了一种用甘氨酸与次氯酸钠组合抑制颗粒淀粉至不同的抑制水平的方法。它进一步说明了如何通过添加稳定所获得的抑制的抗氧化剂来控制在实例3中所示的不稳定的暂时性抑制的问题。在实例4中使用的天然的颗粒淀粉是具有残留蛋白质含量小于0.4%的蜡质玉蜀黍(玉米)淀粉,如凯氏定氮法所分析并且用6.25的蛋白质转化因子计算的。
4)0.4%活性氯+甘氨酸
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加1.16克(0.133%w/w)甘氨酸。在搅拌期间添加38.7克具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.4%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃,在搅拌期间添加9.5g的抗氧化剂柠檬酸。将淀粉浆液置于搅拌下持续30min。将淀粉浆液调节至ph6,并且进一步脱水和干燥至含水量为大约15%的干粉。
将实例4中获得的产品在与周围空气氧气接触的环境条件下储存,并且在不同储存时间后使用蒸馏水以5%的固体含量用brabenderamyloviscograph型号e进行评估。使用350cmg的扭转弹簧。在中性ph下进行评估。
来自实例4的结果如图6所示,表明在实例3中显示为不稳定的、通过氨基酸和氧化试剂之间的组合获得的抑制在通过在抑制反应后添加抗氧化剂(在本实例中为柠檬酸)在储存期间得到稳定。在图6中,标示为“4a-d”的曲线表示在第1-300天的粘度曲线。很明显,在这个延长的储存时间内粘度没有变化。因此,已经证明通过将氨基酸与氧化剂组合获得的不稳定抑制可以在已经发生抑制反应后添加抗氧化剂来稳定。
实例5
实例5披露了一种使用苏氨酸与次氯酸钠组合来抑制天然的颗粒淀粉至不同抑制水平的方法。在该实例中,苏氨酸的添加固定为0.067%w/w,并且次氯酸钠的添加在不同水平下进行,产生在活性氯和苏氨酸之间的不同比例。在实例3中使用的天然的颗粒淀粉是具有残留蛋白质含量小于0.4%的蜡质玉蜀黍(玉米)淀粉,如凯氏定氮法所分析并且用6.25的蛋白质转化因子计算的。
5a)0.067%活性氯+0.067%w/w苏氨酸(比例1:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)苏氨酸。在搅拌期间添加6.48克具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.067%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph6,并且进一步脱水和干燥至含水量为大约15%的干粉。
5b)0.133%活性氯+0.067%w/w苏氨酸(比例2:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)苏氨酸。在搅拌期间添加12.96g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.133%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
5c)0.2%活性氯+0.067%w/w苏氨酸(比例3:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)苏氨酸。在搅拌期间添加19.49g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.2%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
5d)0.268%活性氯+0.067%w/w苏氨酸(比例4:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)苏氨酸。在搅拌期间添加26.12g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.268%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度控制在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
5e)0.335%活性氯+0.067%w/w苏氨酸(比例5:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)苏氨酸。在搅拌期间添加32.65g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.335%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
5f)0.4%活性氯+0.067%w/w苏氨酸(比例6:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)苏氨酸。在搅拌期间添加38.99g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.335%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
实例5a)-5e)中获得的产物用brabenderamyloviscograph型号e、以5%的干固体含量、使用蒸馏水和350cmg的扭转弹簧进行评估。该评估是在中性ph值和在ph3下进行的。
从图7和图8中可以看出,在添加不同水平的活性氯下达到不同的抑制水平。因此,抑制水平取决于活性氯和苏氨酸的比例,并且最佳条件是1:5(苏氨酸:活性氯)的比例。这与氨基酸甘氨酸相比不同,其在1:3(甘氨酸:活性氯)的比例下具有其最佳抑制水平。还可以看出,在0.335%w/w活性氯和0.067%w/w苏氨酸下达到的抑制水平比仅通过添加活性氯至处于其天然状态下的相同淀粉可能达到的抑制水平高得多。因此,氨基酸苏氨酸和活性氯的组合产生更高的抑制水平。实例5说明苏氨酸与活性氯的组合可以用于抑制淀粉至比仅用活性氯可能达到的更高的抑制水平。
实例6
实例6披露了一种使用色氨酸与次氯酸钠组合来抑制天然的颗粒淀粉至不同水平的方法。在该实例中,色氨酸的添加固定为0.067%w/w,并且次氯酸钠的添加在不同水平下进行,产生在活性氯和色氨酸之间的不同比例。天然颗粒淀粉原材料是具有残留蛋白质含量小于0.4%的蜡质玉蜀黍(玉米)淀粉,如凯氏定氮法所分析并且用6.25的蛋白质转化因子计算的。
a)0.067%活性氯+0.067%w/w色氨酸(比例1:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)色氨酸。在搅拌期间添加6.48g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.067%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
6b)0.133%活性氯+0.067%w/w色氨酸(比例2:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)色氨酸。在搅拌期间添加12.96g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.133%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
6c)0.168%活性氯+0.067%w/w色氨酸(比例2.5:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)色氨酸。在搅拌期间添加16.23g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.168%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
6d)0.2%活性氯+0.067%w/w色氨酸(比例3:1)
将869.1g的dm蜡质玉米淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)色氨酸。在搅拌期间添加19.49g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.2%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
6e)0.23%活性氯+0.067%w/w色氨酸(比例3.5:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)色氨酸。在搅拌期间添加22.23g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.23%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
6f)0.268%活性氯+0.067%w/w色氨酸(比例4:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)色氨酸。在搅拌期间添加26.12g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.268%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
实例6a)-6f)中获得的产物用brabenderamyloviscograph型号e、以5%的干固体含量、使用蒸馏水和350cmg的扭转弹簧进行评估。该评估是在中性ph值和在ph3下进行的。
从图9和图10中可以看出,在添加不同水平的活性氯下达到不同的抑制水平。因此,抑制水平取决于活性氯和色氨酸的比例,并且最佳条件是1:2.5(色氨酸:活性氯)的比例。这与氨基酸甘氨酸相比不同,其在1:3(甘氨酸:活性氯)的比例下具有其最佳抑制水平。还可以看出,在0.168%w/w活性氯和0.067%w/w苏氨酸在dm淀粉上获得的抑制水平比仅通过添加活性氯至处于其天然状态下的相同淀粉可能达到的抑制水平高得多。因此,氨基酸色氨酸和活性氯的组合产生更高的抑制水平。总而言之,实例6说明色氨酸与活性氯的组合可以用于抑制淀粉至比仅用活性氯可能达到的更高的抑制水平。
实例7
实例7说明氨基酸或氨基酸的组合可以来源于淀粉原材料来源,并且还可能在不使用合成产生的氨基酸或氨基酸组合的情况下获得改进的抑制水平。
来源于已从其分离淀粉并且富含蛋白质和蛋白质相关化合物(即氨基酸和肽)的马铃薯的果汁在63μm筛上过滤以分离剩余的纤维。随着ph调节至5.1并且温度增加至135℃持续15秒蛋白质凝结。在3000xg下离心3分钟分离并倾析加热凝结的蛋白质。将上清液蒸发浓缩至干物质含量(dm)大于35%。结果,使盐结晶并进一步用倾析分离。
剩余的浓缩溶液具有35%的干物质含量,并且使用0.45μm过滤器通过微量过滤来进行过滤。在本实例中,将过滤的富含氨基酸的溶液(以下称为paac(马铃薯氨基酸浓缩物))用作氨基酸化合物,并且将paac的干物质确定为33.3%w/w。
具有残留蛋白质含量小于0.1%的1000g天然的颗粒马铃薯淀粉dm用凯氏定氮法进行分析,并且用6.25的蛋白质转化因子计算。然后将其与1500g冷自来水混合并平衡至30℃。用氢氧化钠溶液将ph调节至11.0,其后如下所披露的添加不同量的paac。
7a)
在搅拌期间添加2.3gdm(0.23%w/w)paac。在搅拌期间将浆液放置60min,并将ph调节至11.0。在搅拌期间添加20.4g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.18%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约19%的干粉。
7b)
在搅拌期间添加4.55gdm(0.46%w/w)paac。继续搅拌下将浆液放置60min,并将ph调节至11.0。在搅拌期间添加40.8g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.37%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约19%的干粉。
7c)
在搅拌期间添加9.1gdm(0.91%w/w)paac。继续搅拌下将浆液放置60min,并将ph调节至11.0。在搅拌期间添加81.6g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.73%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约19%的干粉。
实例7a)-7c)中获得的产物用brabenderamyloviscograph型号e、以5%的dm淀粉、使用蒸馏水和700cmg的扭转弹簧进行评估。在中性ph下进行评估。如图11所示,在该实例中实现了抑制,并且在更高的paac和活性氯添加量下抑制更强。该实例和结果应与实例8的结果进行比较,其中天然马铃薯淀粉用相同量的活性氯处理但不添加paac。不添加paac的情况下不存在抑制。因此,显然通过添加paac与活性氯的组合来达到抑制。
实例8
实例8说明具有0.01%-0.1%的蛋白质含量的马铃薯淀粉在不添加氨基酸的情况下不能被抑制。
1000g天然的颗粒马铃薯淀粉的dm具有小于0.1%的残留蛋白质含量,如凯氏定氮法所分析并且用6.25的蛋白质转化因子计算的,然后将该天然的颗粒马铃薯淀粉的dm与1500g冷自来水混合并平衡至30℃。用氢氧化钠溶液将ph调节至11.0,其后添加0.8%w/w的活性氯。在实例8中获得的产物用brabenderamyloviscograph型号e、以5%的dm淀粉、使用蒸馏水和700cmg的扭转弹簧进行评估。在中性ph下进行评估。如图13所示,没有淀粉的抑制。因此,其在图13中披露的粘度曲线与天然淀粉的粘度曲线相当。该实例说明通过添加氧化试剂(即活性氯本身)不能实现抑制。因此,根据本发明的方法,其必须结合氨基酸、氨基酸样化合物等的添加。
实例9
实例9披露了使用甘氨酸与次氯酸钠组合来抑制天然的颗粒淀粉的方法。该实例还说明了颗粒淀粉的糊化温度如何因为实现的抑制而改变。天然的颗粒淀粉原材料是具有残留蛋白质含量小于0.4%的蜡质玉蜀黍(玉米)淀粉,如凯氏定氮法所分析并且用6.25的蛋白质转化因子计算的。
9)0.2%活性氯+0.067%甘氨酸(比例3:1)
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)甘氨酸。在搅拌期间添加19.3g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.2%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
在实例9中获得的产物用brabenderamyloviscograph型号e、以16%的dm含量、使用蒸馏水和250cmg的扭转弹簧进行评估。当淀粉糊化时,使用较高浓度以给出即时读数,并且更好地说明了明显增加到更高值的糊化温度的改变。在中性ph下进行评估。将结果与天然蜡质玉蜀黍(玉米)淀粉和具有相似抑制水平的碱性干烤蜡质玉蜀黍(玉米)淀粉进行比较。
结果如图12所示,清楚地说明氨基酸抑制的颗粒淀粉具有更高的糊化温度。根据brabender评估,发现新颖淀粉的糊化温度为67℃,天然蜡质玉蜀黍(玉米)淀粉的糊化温度为64℃,碱性干烤淀粉的糊化温度为60℃。从这些结果可以得出结论该新颖的抑制淀粉与天然淀粉相比具有高3℃的糊化温度,并且与具有相似抑制水平的碱性干烤淀粉相比具有高7℃的糊化温度。因此,使用根据本发明所述的方法,用氨基酸-氧化剂抑制法抑制至相同抑制水平的淀粉具有高得多的糊化温度。
实例10
实例10披露了一种用甘氨酸与次氯酸钠组合抑制颗粒淀粉的方法。它进一步阐明了一种消除使淀粉产物产生令人不悦的游泳池水的异味或气味的残余物的方法。在实例10中使用的天然的颗粒淀粉是具有残留蛋白质含量小于0.4%的蜡质玉蜀黍(玉米)淀粉,如凯氏定氮法所分析并且用6.25的蛋白质转化因子计算的。
10)0.4%活性氯+甘氨酸
将869.1gdm蜡质玉蜀黍(玉米)淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加1.16克(0.133%w/w)甘氨酸。在搅拌期间添加38.7克具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.4%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉浆液脱水至55%dm,并且进一步与890克冷自来水混合。在搅拌期间添加3g抗氧化剂抗坏血酸。将淀粉浆液置于搅拌下持续30分钟。用硫酸将淀粉浆液调节至ph6。在搅拌期间添加10克柠檬酸。将淀粉浆液置于搅拌下30分钟,并且用氢氧化钠进一步调节至ph6。将淀粉产物进一步脱水并干燥至水分含量为大约15%的干粉。在实例11和12中进一步评估了根据实例10的所获得的淀粉产物。
实例11
将根据实例3和10制备的淀粉以5%dm悬浮于蒸馏水中并煮熟。将淀粉糊分配给包括10人的经过培训的评判小组,并且对淀粉糊进行异味和气味测试。所有10人可以在来自实例3的淀粉中感觉到化学异味,但是仅1人从根据实例10制备的淀粉中感觉到化学异味。所有10人都感觉到来自实例3的淀粉的“游泳池”风味,但是没有人能够检测到根据实例10制备的淀粉的任何异味。
实例12
使用以下基本配制品、用根据实例3和10生产的淀粉制备水果制剂:
将淀粉悬浮于水中,并将覆盆子混合于其中。将混合物在搅拌下在火炉上加热至沸腾。当混合物开始煮沸时,添加糖并将其溶解。将水果制剂冷却并给予与在实例11相同的经过培训的评判小组,以进行味道和风味评价。
所有10人拒绝用根据实例3的淀粉制备的制剂,其评论是糟糕的异味和化学风味。鉴于异常气味还评论了气味。对于用来自实例10的淀粉制备的制剂,没有人评论任何化学异味或气味。3人对来自玉蜀黍的味道和掩盖的水果味有所评论,这是可以理解的,因为它是由玉蜀黍淀粉制成的。
虽然已经参考许多实施例描述了本发明,但是本领域技术人员将会理解,在不背离本发明的范围的情况下可以作出各种改变并且能以多种等价物替代其元件。此外,在不背离其本质范围的情况下,可以进行许多修改以使特定情况或材料以适应本发明的教导。因此,意图是本发明不限于作为实施本发明考虑的最佳模式所披露的特定实施例,而是本发明将包括落入所附权利要求书的范围内的所有实施例。
实例13
在实例13中使用以下的甘氨酸的氨基酸同系物;肌氨酸(甲基甘氨酸)、二甲基甘氨酸、甜菜碱(三甲基甘氨酸)。
13a)0.2%活性氯+0.067%w/w肌氨酸(甲基甘氨酸)(比例3:1)
将869.1g的dm蜡质玉米淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。搅拌期间添加0.58g(0.067%w/w)肌氨酸(甲基甘氨酸)。在搅拌期间添加19.49g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.2%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
13b)0.2%活性氯+0.067%w/w二甲基甘氨酸(比例3:1)
将869.1g的dm蜡质玉米淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)二甲基甘氨酸。在搅拌期间添加19.49g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.2%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
13c)0.2%活性氯+0.067%w/w甜菜碱(三甲基甘氨酸)(比例3:1)
将869.1g的dm蜡质玉米淀粉与1600g冷自来水在反应容器中混合。用氢氧化钠溶液将ph调节至9.0。将温度调节至30℃。在搅拌期间添加0.58g(0.067%w/w)甜菜碱(三甲基甘氨酸)。在搅拌期间添加19.49g具有活性氯(107g/l,密度:1.19g/cm3)的次氯酸钠。这相当于添加0.2%w/w的dm淀粉的活性氯。将容器置于搅拌下持续180min,并且将温度保持在30℃。将淀粉用硫酸中和至ph为6,并且进一步脱水和干燥至含水量为大约15%的干粉。
在实例13a)-13c)中获得的产物用brabenderamyloviscograph型号e、以5%的干固体含量、使用蒸馏水和350cmg的扭转弹簧进行评估。在中性ph下进行评估。
在图14中清楚地出现所有的甘氨酸同系物都实现了淀粉的抑制。与二甲基甘氨酸相比,甜菜碱和肌氨酸的抑制更高,但是它们全部都对淀粉颗粒产生了显著的抑制。该实例说明氨基酸的同系物可用于与次氯酸钠组合实现淀粉颗粒的抑制。
- 还没有人留言评论。精彩留言会获得点赞!