1‑(3‑N‑取代‑咔唑基)‑3‑芳基‑3‑二乙酰基次甲基‑丙酮及其制备方法与流程
本发明属于化学合成领域,特别涉及1-(3-n-取代-咔唑基)-3-芳基-3-二乙酰基次甲基-丙酮及其制备方法。
背景技术:
咔唑是一种重要的杂环化合物,咔唑环易形成相对稳定的正离子,已在许多天然植物中广泛发现含咔唑化合物核心结构的药物,其生物活性和药用意义引起了广大化学工作者的研究兴趣。其含有的共轭体系较大和分子内强的电子转移,具有的给电子能力和空穴传输能力较强,及热稳定性和光化学稳定性较高;其衍生物在光电材料、染料、医药、超分子识别、化学传感等领域具有潜在的广泛应用。更为重要的是咔唑类化合物易进行功能团的结构修饰,其3位、6位和9位易引入,导致咔唑衍生品具有许多独特的性能及生物活性,且在紫外光范围有很强的吸收,并带隙在3.2ev左右及发蓝光等特性,其原料容易得到。咔唑是吡咯的两个双键被苯环取代,含有吡咯的化学结构,具有联苯和二苯胺的性质的化合物,对热、碱和冷都稳定。除了咔唑苯环上易发生的亲电取代反应,咔唑的亚氨基可发生的反应有酰化、烷基化和亚硝化等。氮唑类化合物因在医药(抗菌、抗癌、抗阻胺剂、抗氧化、抗炎、神经抑制等)、染料、材料等多领域广阔的应用前景一直备受研究学者的青睐。由此可见,咔唑类化合物的研究成为最有吸引力的研究目标。
查尔酮类化合物是一类广泛存在于多种植物的天然有机化合物,其母体结构为二苯基丙烯酮。自世纪末首次人工合成以来,人们对查尔酮类化合物进行了广泛的研究。其分子中含有柔性较大的,烯酮结构,能与多种受体结合,呈现出如细胞毒性、抗菌等多种生物活性。此外,查尔酮化合物还是合成黄酮类、甜味素等多种天然产物的重要前体,具有优良的反应活性。近年来,关于查尔酮类化合物抗肿瘤活性的研究已有大量报道,查尔其不仅可以抵抗多类致肿瘤物、促肿瘤物,而且可以抑制多种恶性肿瘤细胞的生长。但其水溶性和脂溶性均较差,生物利用率低,限制了其在临床上的应用。因此,有必要对其结构进行改性和修饰,以期得到活性更高、毒性更小、结构新颖的新药。
在有机合成化学中,碳负离子与α,β-不饱和共轭体系(醛、酮、酯、腈和硝基化合物等)进行的共轭加成反应叫做michael(麦克尔)加成反应。它的反应机理是把碳负离子或氮负离子作为亲核试剂,用来进攻c=c键的共轭体系导致其发生1,4共轭加成反应,通常把能够形成亲核性碳负离子的化合物叫做给予体,而把亲电的α,β-不饱和共轭体系称为接受体。在有机合成化学中是一种重要的构成碳碳双键的方法之一。传统的michael加成是以甲醇为溶剂的回流法,反应催化剂效率较低,产物收率低,副产物较多,反应时间长达24h。
技术实现要素:
本发明的目的在于提供一种1-(3-n-取代-咔唑基)-3-芳基-3-二乙酰基次甲基-丙酮及其制备方法,该方法操作简单、反应条件温和,制得的产品具有杀菌、抑菌、除草等功效。
为达到上述目的,本发明采用的技术方案为:
一种1-(3-n-取代-咔唑基)-3-芳基-3-二乙酰基次甲基-丙酮,其结构通式如下:
其中,ar为苯基、卤代苯基、甲基苯基、甲氧基苯基、硝基苯基、羟基苯基、氨基苯基、乙烯基苯基或五元杂环基;
r为甲基、乙基、丙基、丁基、戊基、己基、庚基、辛基、壬基、苯氧亚甲基、对氯苯氧亚甲基、邻氯苯氧亚甲基、2,4-二氯苯氧亚甲基、间氯苯氧亚甲基、对氟苯氧亚甲基、对溴苯氧亚甲基、对碘苯氧亚甲基、对甲氧基苯氧亚甲基、2-硝基苯氧亚甲基、苯氧乙基、α-萘氧亚甲基、β-萘氧亚甲基或β-萘氧乙基。
所述卤代苯基为邻氟苯基、对氟苯基、邻氯苯基、对氯苯基、2,4-二氯苯基、邻溴苯基、间溴苯基或对溴苯基;
所述的甲基苯基为邻甲基苯基、间甲基苯基或对甲基苯基;
所述的甲氧基苯基为间甲氧基苯基或对甲氧基苯基;
所述的硝基苯基为间硝基苯基、3,5-二硝基苯基或对硝基苯基;
所述的羟基苯基为邻羟基苯基或对羟基苯基;
所述的氨基苯基为邻氨基苯基、间氨基苯基或对氨基苯基;
所述的五元杂环基为呋喃基或噻吩基。
所述的1-(3-n-取代-咔唑基)-3-芳基-3-二乙酰基次甲基-丙酮的制备方法,包括以下步骤:
步骤1)将amol1-(3-n-取代-咔唑基)-3-芳基-丙烯酮、bmol碱性催化剂、cmol乙酰丙酮和溶剂无水乙醇加入反应容器中,进行加热回流反应,其中a:b:c=1:(5~6):(5~6);
步骤2)反应完毕后,将反应液冷却至室温,加入0~5℃的冷水,有固体析出,对析出的固体进行水洗、抽滤,滤饼重结晶,然后进行干燥,即得到1-(3-n-取代-咔唑基)-3-芳基-3-二乙酰基次甲基-丙酮。
所述1-(3-n-取代-咔唑基)-3-芳基-丙烯酮的制备方法为:以乙酰基咔唑、芳香醛为原料,以naoh/k2co3为催化剂进行研磨反应,反应完毕后反复水洗、干燥得到粗品,粗品经硅胶柱层析法进行分离提纯,即得到1-(3-n-取代-咔唑基)-3-芳基-丙烯酮。
所述加热回流的反应温度为70~80℃,反应时间为1~2h。
所述加热回流反应过程中用tlc监测反应进程,当1-(3-n-取代-咔唑基)-3-芳基-丙烯酮的原料点消失时表示原料反应完全;其中tlc的展开剂是体积比为1:5的乙酸乙酯与石油醚的混合溶剂。
所述步骤1)中加入dml无水乙醇,a:d=1:(20000~30000)。
所述加热回流反应过程中以60~80rad/min的速度对反应体系进行搅拌。
所述碱性催化剂为粒状的固体naoh。
所述步骤2)中对析出的固体反复进行水洗、抽滤,直到滤液的ph值呈中性,然后用无水乙醇对滤饼进行重结晶,再在20~30℃下干燥20~30h。
相对于现有技术,本发明的有益效果为:
本发明提供的1-(3-n-取代-咔唑基)-3-芳基-3-二乙酰基次甲基-丙酮,是一系列全新的酮类化合物,具有杀菌、抑菌、除草等功效,可用于医药领域和农药领域等领域。
本发明提供的1-(3-n-取代-咔唑基)-3-芳基-3-二乙酰基次甲基-丙酮的制备方法,将1-(3-n-取代-咔唑基)-3-芳基-丙烯酮、碱性催化剂、乙酰丙酮和溶剂无水乙醇加入反应容器中加热回流反应,对反应产物进行后处理即得到目标产物。本发明采用经典的回流法,与传统合成方法相比,本发明的反应现象明显,反应过程简单,操作简单,反应时间短,反应条件温和,水浴下即可进行反应,设备要求低,且该方法的后处理简单,副产物少,产物的产率高。克服了传统合成方法设备要求高,反应时间长等缺点,具有经济、方便、高效、绿色环保的优点。
进一步的,本发明在制备过程中,用tlc监测反应过程,所用的展开剂为体积比为1:5的乙酸乙酯和石油醚,监测准确,利于控制反应进度和结束。同时本发明所用的催化剂为粒状的固体naoh,廉价易得,催化效果良好,使反应更加迅速和完全,且后处理简单。
附图说明
图1为实施例1制得的产物的红外图谱;
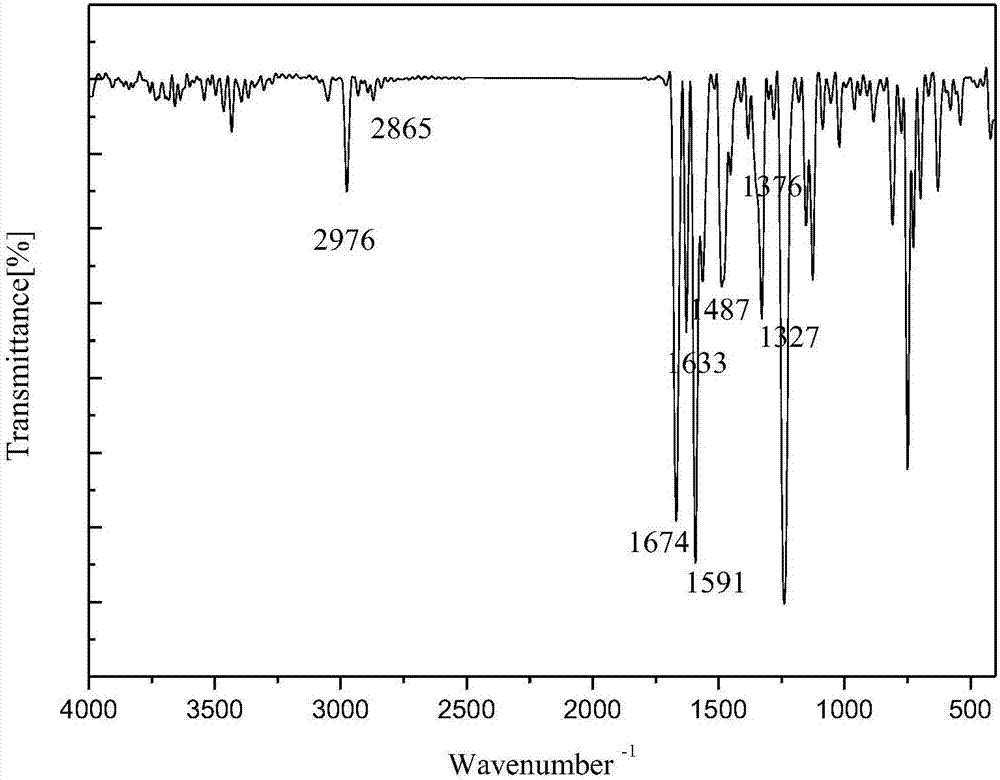
图2为实施例2制得的产物的红外图谱;
图3为实施例1制得的产物的1hnmr图谱;
图4为实施例2制得的产物的1hnmr图谱。
具体实施方式
本发明提供的1-(3-n-取代-咔唑基)-3-芳基-3-二乙酰基次甲基-丙酮的反应方程式如下:
其中ar为芳基,具体为苯基、对氯苯基、对溴苯基、对氟苯基、对甲基苯基、对甲氧基苯基、间硝基苯基、对羟基苯基、邻羟基苯基、乙烯基苯基、邻甲基苯基、间甲基苯基、间甲氧基苯基、2-氟苯基、对氨基苯基、间氨基苯基、邻氨基苯基、邻氯苯基、2,4-二氯苯基、对硝基苯基、3,5-二硝基苯基、邻溴苯基、间溴苯基、呋喃基或噻吩基。
r为甲基、乙基、丙基、丁基、戊基、己基、庚基、辛基、壬基、苯氧亚甲基、对氯苯氧亚甲基、邻氯苯氧亚甲基、2,4-二氯苯氧亚甲基、间氯苯氧亚甲基、对氟苯氧亚甲基、对溴苯氧亚甲基、对碘苯氧亚甲基、对甲氧基苯氧亚甲基、2-硝基苯氧亚甲基、苯氧乙基、α-萘氧亚甲基、β-萘氧亚甲基或β-萘氧乙基。
下面将结合本发明较佳的实施例对本发明做进一步详细说明。
实施例1
在250ml干燥的装有冷凝回流管和搅拌装置的三口瓶中依次加入0.0055mol乙酰丙酮、0.0055mol氢氧化钠(固体、粒状)、以及30ml无水乙醇,于室温下搅拌5min左右,待混合均匀后,将0.001mol的1-(3-n-甲基-咔唑基)-3-对氯苯基-丙烯酮溶解在30ml无水乙醇中,在搅拌器匀速搅拌的条件下用滴管缓慢滴加进三口瓶中,滴加完毕后将水浴缓慢升温至80℃,保持80℃的温度,以70rad/min的速度恒速搅拌并反应100min。反应进程用tlc监测,选用体积比为v(乙酸乙酯):v(石油醚)=1:5的展开剂。反应完全后,停止反应,使反应体系缓慢降到室温,加入20ml3℃冷水,静置,有固体析出,抽滤,滤饼反复水洗至中性后用无水乙醇重结晶,旋转蒸发仪蒸去溶剂,再在25℃真空干燥25h,得到产品1-(3-n-甲基-咔唑基)-3-对氯苯基-3-二乙酰基次甲基-丙酮。
ir(kbr,v/cm-1):2976,1376(-ch3),2899,1487(-ch2),1597,1452(ar-h),1668,1633(c=o),1335(-nr2).
由图1可见,2976、1376cm-1分别为-ch3的伸缩振动吸收峰和弯曲振动峰,2899、1487cm-1为-ch2的伸缩振动吸收峰和弯曲振动峰,1668、1633cm-1为c=o的伸缩振动峰,1335cm-1为n-r2的伸缩振动峰,1597、1452cm-1为苯环的骨架振动吸收特征峰,3060cm-1为芳环中不饱和h的特征吸收峰。
1hnmr:1.45-1.51(t,3h,-ch3),2.01(s,6h,-coch3),2.76-2.78(d,2h,-coch2),4.40-4.44(q,2h,-ch2),3.89-3.92(m,2h,-ch),7.33-7.53(m,8h,-ph),8.12-8.20(m,4h,-ph).如图3所示。
图3中,1.45-1.51ppm处和4.40-4.44ppm处分别为咔唑结构中n上的取代基甲基和亚甲基的质子峰,积分面积比显示为3:4;2.01ppm处的单峰为-coch3的质子峰,积分面积为6个质子,表示此处的两个对称的乙酰基团的质子峰;2.76-2.78ppm处的双重峰是-coch2的质子峰;3.89-3.93ppm处的多重峰积分面积为2个h,表示2个-ch结构的质子峰,7.33-7.53ppm和8.12-8.20ppm处的多重峰表示3个芳环的质子峰,化合物结构中的芳环上总共有12个质子,与谱图分析相符合。
实施例2
在250ml干燥的装有冷凝回流管和搅拌装置的三口瓶中依次加入0.0055mol乙酰丙酮、0.0055mol氢氧化钠(固体、粒状)、以及30ml无水乙醇,于室温下搅拌5min左右,待混合均匀后,将0.001mol的1-(3-n-甲基-咔唑基)-3-苯基-丙烯酮溶解在30ml无水乙醇中,在搅拌器匀速搅拌的条件下用滴管缓慢滴加进三口瓶中,滴加完毕后将水浴缓慢升温至80℃,保持80℃的温度,以70rad/min的速度恒速搅拌并反应100min。反应进程用tlc监测,选用体积比为v(乙酸乙酯):v(石油醚)=1:5的展开剂。反应完全后,停止反应,使反应体系缓慢降到室温,加入20ml3℃冷水,静置,有固体析出,抽滤,滤饼反复水洗至中性后用无水乙醇重结晶,旋转蒸发仪蒸去溶剂,再在25℃真空干燥25h,得到产品1-(3-n-甲基-咔唑基)-3-苯基-3-二乙酰基次甲基-丙酮。
ir(kbr,ν/cm-1):2976,1376(-ch3),2865,1487(-ch2),1591,1446(ar-h),1674,1633(c=o),1327(-nr2).如图2所示。
1hnmr:1.27-1.48(t,3h,-ch3),2.07(s,6h,-ch3),2.76-2.80(d,2h,-coch2),4.42-4.24(m,2h,-ch),7.29-7.46(m,8h,-ph),8.18-8.79(m,4h,-ph).如图4所示。
实施例3
在250ml干燥的装有冷凝回流管和搅拌装置的三口瓶中依次加入0.0055mol乙酰丙酮、0.0055mol氢氧化钠(固体、粒状)、以及30ml无水乙醇,于室温下搅拌5min左右,待混合均匀后,将0.001mol的1-(3-n-甲基-咔唑基)-3-(2-噻吩基)-丙烯酮溶解在30ml无水乙醇中,在搅拌器匀速搅拌的条件下用滴管缓慢滴加进三口瓶中,滴加完毕后将水浴缓慢升温至80℃,保持80℃的温度,以70rad/min的速度恒速搅拌并反应100min。反应进程用tlc监测,选用体积比为v(乙酸乙酯):v(石油醚)=1:5的展开剂。反应完全后,停止反应,使反应体系缓慢降到室温,加入20ml3℃冷水,静置,有固体析出,抽滤,滤饼反复水洗至中性后用无水乙醇重结晶,旋转蒸发仪蒸去溶剂,再在25℃真空干燥25h,得到产品1-(3-n-甲基-咔唑基)-3-(2-噻吩基)-3-二乙酰基次甲基-丙酮。
ir:2976,1376(-ch3),2880,1480(-ch2),1653,1625(c=o),3053,1592,1432(ar-h),1325(nr2).
1hnmr:1.34-1.47(t,3h,-ch3),2.07(s,6h,-coch3),2.85-2.86(d,2h,-coch2),3.44-3.87(m,2h,-ch),3.91-3.98(m,2h,-ch2),6.65-6.67(d,1h,thy-h),6.85-6.88(m,1h,thy-h),7.03-7.04(d,1h,thy-h),7.15-7.19(m,2h,ph-h),7.55-7.78(d,4h,ph-h),7.81(s,1h,ph-h).
实施例4
在250ml干燥的装有冷凝回流管和搅拌装置的三口瓶中依次加入0.0055mol乙酰丙酮、0.0055mol氢氧化钠(固体、粒状)、以及30ml无水乙醇,于室温下搅拌5min左右,待混合均匀后,将0.001mol的1-(3-n-甲基-咔唑基)-3-对硝基苯基-丙烯酮溶解在30ml无水乙醇中,在搅拌器匀速搅拌的条件下用滴管缓慢滴加进三口瓶中,滴加完毕后将水浴缓慢升温至80℃,保持80℃的温度,以70rad/min的速度恒速搅拌并反应100min。反应进程用tlc监测,选用体积比为v(乙酸乙酯):v(石油醚)=1:5的展开剂。反应完全后,停止反应,使反应体系缓慢降到室温,加入20ml3℃冷水,静置,有固体析出,抽滤,滤饼反复水洗至中性后用无水乙醇重结晶,旋转蒸发仪蒸去溶剂,再在25℃真空干燥25h,得到产品1-(3-n-甲基-咔唑基)-3-对硝基苯基-3-二乙酰基次甲基-丙酮。
ir:2934,1353(-ch3),2817,1473(-ch2),1665,1619(c=o),1590,1439(ar-h),1515(-no2),1335(nr2).
1hnmr:1.33-1.37(t,3h,-ch3),2.05(s,6h,-coch3),2.63-2.69(d,2h,-coch2),3.85-3.91(q,2h,-ch2),3.94-4.01(m,2h,-ch),7.42-7.59(m,8h,-ph),7.86-7.99(m,4h,-ph).
实施例5
在250ml干燥的装有冷凝回流管和搅拌装置的三口瓶中依次加入0.0055mol乙酰丙酮、0.0055mol氢氧化钠(固体、粒状)、以及30ml无水乙醇,于室温下搅拌5min左右,待混合均匀后,将0.001mol的1-(3-n-甲基-咔唑基)-3-对氟苯基-丙烯酮溶解在30ml无水乙醇中,在搅拌器匀速搅拌的条件下用滴管缓慢滴加进三口瓶中,滴加完毕后将水浴缓慢升温至80℃,保持80℃的温度,以70rad/min的速度恒速搅拌并反应100min。反应进程用tlc监测,选用体积比为v(乙酸乙酯):v(石油醚)=1:5的展开剂。反应完全后,停止反应,使反应体系缓慢降到室温,加入20ml1℃冷水,静置,有固体析出,抽滤,滤饼反复水洗至中性后用无水乙醇重结晶,旋转蒸发仪蒸去溶剂,再在25℃真空干燥25h,得到产品1-(3-n-甲基-咔唑基)-3-对氟苯基-3-二乙酰基次甲基-丙酮。
ir:2942,1365(-ch3),2847,1436(-ch2),1587,1476(ar),1714,1697(c=o),1331(nr2).
1hnmr:1.25-1.32(t,3h,-ch3),2.07(s,6h,-coch3),2.77-2.81(d,2h,-coch2),3.64-3.73(q,2h,-ch2),3.85-3.97(m,2h,-ch),7.29-7.41(m,8h,-ph),8.03-8.12(m,4h,-ph).
实施例6
在250ml干燥的装有冷凝回流管和搅拌装置的三口瓶中依次加入0.005mol乙酰丙酮、0.005mol氢氧化钠(固体、粒状)、以及20ml无水乙醇,于室温下搅拌5min左右,待混合均匀后,将0.001mol的1-(3-n-乙基-咔唑基)-3-对甲基苯基-丙烯酮溶解在30ml无水乙醇中,在搅拌器匀速搅拌的条件下用滴管缓慢滴加进三口瓶中,滴加完毕后将水浴缓慢升温至70℃,保持70℃的温度,以60rad/min的速度恒速搅拌并反应120min。反应进程用tlc监测,选用体积比为v(乙酸乙酯):v(石油醚)=1:5的展开剂。反应完全后,停止反应,使反应体系缓慢降到室温,加入20ml0℃冷水,静置,有固体析出,抽滤,滤饼反复水洗至中性后用无水乙醇重结晶,旋转蒸发仪蒸去溶剂,再在20℃真空干燥30h,得到产品1-(3-n-乙基-咔唑基)-3-对甲基苯基-3-二乙酰基次甲基-丙酮。
实施例7
在250ml干燥的装有冷凝回流管和搅拌装置的三口瓶中依次加入0.006mol乙酰丙酮、0.006mol氢氧化钠(固体、粒状)、以及25ml无水乙醇,于室温下搅拌5min左右,待混合均匀后,将0.001mol的1-(3-n-丙基-咔唑基)-3-对羟基苯基-丙烯酮溶解在30ml无水乙醇中,在搅拌器匀速搅拌的条件下用滴管缓慢滴加进三口瓶中,滴加完毕后将水浴缓慢升温至75℃,保持75℃的温度,以80rad/min的速度恒速搅拌并反应60min。反应进程用tlc监测,选用体积比为v(乙酸乙酯):v(石油醚)=1:5的展开剂。反应完全后,停止反应,使反应体系缓慢降到室温,加入20ml5℃冷水,静置,有固体析出,抽滤,滤饼反复水洗至中性后用无水乙醇重结晶,旋转蒸发仪蒸去溶剂,再在30℃真空干燥20h,得到产品1-(3-n-丙基-咔唑基)-3-对羟基苯基-3-二乙酰基次甲基-丙酮。
实施例8
在250ml干燥的装有冷凝回流管和搅拌装置的三口瓶中依次加入0.0052mol乙酰丙酮、0.0052mol氢氧化钠(固体、粒状)、以及22ml无水乙醇,于室温下搅拌5min左右,待混合均匀后,将0.001mol的1-(3-n-丁基-咔唑基)-3-对氨基苯基-丙烯酮溶解在30ml无水乙醇中,在搅拌器匀速搅拌的条件下用滴管缓慢滴加进三口瓶中,滴加完毕后将水浴缓慢升温至72℃,保持72℃的温度,以65rad/min的速度恒速搅拌并反应80min。反应进程用tlc监测,选用体积比为v(乙酸乙酯):v(石油醚)=1:5的展开剂。反应完全后,停止反应,使反应体系缓慢降到室温,加入20ml2℃冷水,静置,有固体析出,抽滤,滤饼反复水洗至中性后用无水乙醇重结晶,旋转蒸发仪蒸去溶剂,再在22℃真空干燥28h,得到产品1-(3-n-丁基-咔唑基)-3-对氨基苯基-3-二乙酰基次甲基-丙酮。
实施例9
在250ml干燥的装有冷凝回流管和搅拌装置的三口瓶中依次加入0.0058mol乙酰丙酮、0.0058mol氢氧化钠(固体、粒状)、以及28ml无水乙醇,于室温下搅拌5min左右,待混合均匀后,将0.001mol的1-(3-n-戊基-咔唑基)-3-对甲氧基苯基-丙烯酮溶解在30ml无水乙醇中,在搅拌器匀速搅拌的条件下用滴管缓慢滴加进三口瓶中,滴加完毕后将水浴缓慢升温至78℃,保持78℃的温度,以75rad/min的速度恒速搅拌并反应90min。反应进程用tlc监测,选用体积比为v(乙酸乙酯):v(石油醚)=1:5的展开剂。反应完全后,停止反应,使反应体系缓慢降到室温,加入20ml4℃冷水,静置,有固体析出,抽滤,滤饼反复水洗至中性后用无水乙醇重结晶,旋转蒸发仪蒸去溶剂,再在28℃真空干燥22h,得到产品1-(3-n-戊基-咔唑基)-3-对甲氧基苯基-3-二乙酰基次甲基-丙酮。
除上述实施例外,原料1-(3-n-取代-咔唑基)-3-芳基-丙烯酮还可采用以下物质,其中取代基为己基、庚基、辛基、壬基、苯氧亚甲基、对氯苯氧亚甲基、邻氯苯氧亚甲基、2,4-二氯苯氧亚甲基、间氯苯氧亚甲基、对氟苯氧亚甲基、对溴苯氧亚甲基、对碘苯氧亚甲基、对甲氧基苯氧亚甲基、2-硝基苯氧亚甲基、苯氧乙基、α-萘氧亚甲基、β-萘氧亚甲基或β-萘氧乙基;芳基为间硝基苯基、邻羟基苯基、乙烯基苯基、邻甲基苯基、间甲基苯基、间甲氧基苯基、2-氟苯基、间氨基苯基、邻氨基苯基、邻氯苯基、2,4-二氯苯基、3,5-二硝基苯基、邻溴苯基、对溴苯基、间溴苯基或呋喃基;在此不一一列举。
另外,本发明中的1-(3-n-取代-咔唑基)-3-芳基-丙烯酮可采用以下方法制备:
1)以乙酰基咔唑为原料制备n-取代-咔唑;
2)以n-取代-咔唑为原料制备3-乙酰基-n-取代-咔唑;
3)以3-乙酰基-n-取代-咔唑和芳香醛为原料,以naoh/k2co3为催化剂进行研磨反应,反应完毕后反复水洗、干燥得到粗品,粗品经硅胶柱层析法进行分离提纯,即得到1-(3-n-取代-咔唑基)-3-芳基-丙烯酮。
本发明探索了含新的取代基团的咔唑基michael加成产物以及制备方法,并优化了实验条件,缩短了反应时间,为绿色合成做出了贡献。本发明提供的1-(3-n-取代-咔唑基)-3-芳基-3-二乙酰基次甲基-丙酮,是一系列全新的酮类化合物,具有杀菌、抑菌、除草等功效,可用于医药领域和农药领域等领域。
以上所述,仅是本发明的较佳实施例,并非对本发明作任何限制,凡是根据本发明技术实质对以上实施例所作的任何简单修改、变更以及等效结构变换,均仍属于本发明技术方案的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!