一种利用大孔吸附树脂分离纯化5‑氨基戊酸的方法与流程
本发明属于生物化学领域,具体涉及一种以大孔吸附树脂分离生物转化液中5-氨基戊酸的方法。
背景技术:
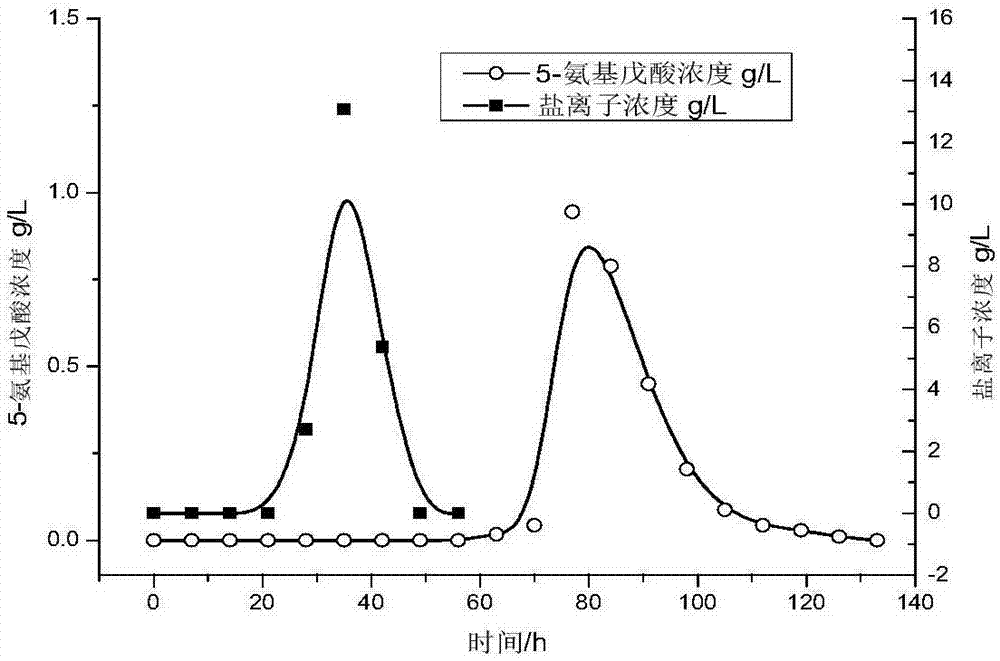
:尼龙是一种非常重要的工程材料,其单体聚酰胺多由石油化学法生产。因此,生物衍生化学品作为环境友好型材料有巨大的潜能去替代化石原料。5-氨基戊酸作为一种生物衍生化学品可用于合成尼龙5的戊内酰胺。除此之外,5-氨基戊酸作为一种c5平台化合物还可用于合成戊二酸、戊二醇、5-戊酸等。目前已报道的5-氨基戊酸的生物合成途径主要有三种:酶催化途径,全细胞催化途径和发酵途径。aliakseiv.pukin,caimeng.boeriu等报道的通过酶催化途径得到的5-氨基戊酸转化液为ph7.8的nh4hco3溶液,转化液中还含有少量的底物赖氨酸和产物5-氨基戊酸;xinwang,peipeicai等报道的利用全细胞催化的方法得到的5-氨基戊酸转化液中含有大约14g/l的磷酸盐缓冲溶液,大约2g/l的硫酸盐,剩余少量的赖氨酸和葡萄糖;sijaepark1,younghoonoh等报道的由发酵法得到的5-氨基戊酸发酵液中含有大约10g/l的磷酸盐,大约16g/l的硫酸盐,少量剩余的葡萄糖和赖氨酸;sijaepark1,younghoonoh等报道利用分离γ-氨基丁酸的方法,通过离子交换树脂分离5-氨基戊酸,其方法要经过絮凝过滤除菌体,大孔吸附树脂脱色,最后通过离子交换树脂分离5-氨基戊酸。其给出的方法较模糊,而且没有给出回收率和纯度等数据。但是,不管由何种途径得到的5-氨基戊酸转化液中都含有大量的盐离子,离子交换树脂会吸附盐离子,这极大地降低离子交换树脂对目标产物的吸附,并影响目标产物的纯度。大孔吸附树脂具有颗粒度均匀,再生容易等特点,因此其在分离方面的应用十分广泛。但是,利用大孔吸附树脂分离5-氨基戊酸的方法至今未见报道。技术实现要素:本发明的目的就在于提供一种以大孔吸附树脂分离生物转化液中5-氨基戊酸的方法,该方法可以从转化液中回收90%纯度达99.9%的5-氨基戊酸,并且适用于分离由任何途径转化得到的5-氨基戊酸转化液,分离操作简单便捷,分离效果显著,树脂再生容易。为了达到上述目的,本发明的技术方案为:一种利用大孔吸附树脂分离纯化5-氨基戊酸的方法,包括如下步骤:1)将5-氨基戊酸转化液通过预处理好的大孔吸附树脂柱进行吸附;2)达到吸附平衡后,用纯水洗脱大孔吸附树脂柱,直到没有物质洗脱下来后,换用盐酸进行洗脱;3)将步骤2)中纯水洗脱液进行减压浓缩后再经乙醇重结晶,得到5-氨基戊酸;将盐酸洗脱液进行减压浓缩得到5-氨基戊酸盐酸盐酸和l-赖氨酸盐酸盐的混合物。步骤1)中所述的5-氨基戊酸转化液来源于酶催化过程、全细胞催化过程或者发酵过程。上述过程得到的5-氨基戊酸转化液经离心,除去99%的菌体及蛋白,留上清溶液,上清液中可以含有缓冲盐和其他少量的金属盐离子,底物l-赖氨酸,产物5-氨基戊酸以及少量的糖和蛋白。由于大孔吸附树脂不吸附盐离子的特性,因此不管由何种途径得到的5-氨基戊酸转化液都可以选择大孔吸附树脂分离回收转化液中的各组分。步骤1)中所述的大孔吸附树脂为非极性树脂或弱极性树脂。步骤1)中大孔吸附树脂的预处理包括以下步骤:用乙醇浸泡24h后,以2bv/h的流速通过树脂柱,至流出的液体不再浑浊为止,相同流速下,用纯水洗至无醇;用1m的盐酸浸泡4-5h,同样流速下冲洗至流出液无色,然后用纯水洗至中性;用1m的naoh浸泡4-5h,同样流速下冲洗至流出液无色,然后用纯水洗至中性。步骤1)中5-氨基戊酸转化液上柱的浓度为10g/l-90g/l,上样流速为0.34bv/h-1.35bv/h,吸附温度为60℃-80℃。步骤2)中纯水洗脱的流速为0.68bv/h-1.35bv/h,洗脱温度与吸附温度相同,盐酸洗脱的浓度为0.5m-2m,流速为0.68bv/h-1.35bv/h,洗脱温度同吸附温度。所述弱极性树脂包括ax-1,ax-13等树脂,非极性树脂包括hd-4,mr-8,mr-5等树脂。优选ax-1树脂。步骤3)中得到的5-氨基戊酸盐酸盐和l-赖氨酸盐酸盐的混合物,可以再次作为底物用于5-氨基戊酸的生产。本发明中纯水和盐酸能够将吸附的5-氨基戊酸和l-赖氨酸完全解析,树脂再生时只要用纯水将树脂柱洗至中性即可,再生方便。大孔吸附树脂柱的再生包括以下步骤:先用1m的盐酸通过树脂柱至流出液不含任何其他组分,相同流速下,用纯水洗至流出液为中性即可。目前市售的5-氨基戊酸的最高浓度为98%,本方法可以使5-氨基戊酸的纯度达到99%以上,更优的纯度可以达到99.9%,分离效果显著,操作简单。有益效果:本发明利用大孔吸附树脂柱对5-氨基戊酸转化液进行分离纯化,可以回收70%-90%的5-氨基戊酸、10%-30%的5-氨基戊酸盐酸盐以及100%的回收赖氨酸盐酸盐,分离的5-氨基戊酸纯度达99%以上,纯水和盐酸已经将吸附的5-氨基戊酸和l-赖氨酸完全解析,树脂再生时只要用纯水将树脂柱洗至中性即可,再生方便。附图说明图1不同树脂对5-氨基戊酸和l-赖氨酸的吸附情况;图260℃下水洗色谱峰;图360℃盐酸洗色谱峰;图480℃水洗色谱峰;图580℃穿透曲线。具体实施方式实施例1树脂的选择1.树脂预处理:将ax-1,ax-13,mr-5,hd-4,mr-8等树脂装柱,乙醇浸泡24h后,以2bv/h的流速通过树脂柱,至流出的液体不再浑浊为止,相同流速下,换用纯水洗至无醇;用1m的盐酸浸泡4-5h,同样流速下冲洗至流出液无色,换用纯水洗至中性;用1m的naoh浸泡4-5h,同样流速下冲洗至流出液无色,换用纯水洗至中性,50℃下烘干待用。2.5-氨基戊酸模拟液的配置:按照5-氨基戊酸转化液中主要组分的浓度配置模拟液:以5-氨基戊酸与l-赖氨酸的质量比大约为25:1的比例称取5-氨基戊酸标准品和l-赖氨酸标准品,溶于磷酸盐缓冲液中,配置成25g/l的5-氨基戊酸和1g/l的l-赖氨酸溶液。3.静态吸附进行树脂的筛选:分别量取预处理过的吸附树脂各1g和配置的5-氨基戊酸模拟液10ml,于100ml的锥形瓶中,室温下150rpm振荡12h。4.数据与分析:分别计算上述树脂对5-氨基戊酸与l-赖氨酸的选择吸附性,数据结果如图1所示。ax-1树脂对l-赖氨酸的分配系数最大,对5-氨基戊酸的分配系数较小,可见ax-1树脂对l-赖氨酸强吸附,对5-氨基戊酸弱吸附,这样就可以将5-氨基戊酸与l-赖氨酸分离开。因为ax-1树脂对5-氨基戊酸弱吸附,因此可以考虑用水做洗脱剂。所以,实验选择ax-1树脂为分离5-氨基戊酸的最优树脂。实施例260℃下ax-1树脂分离5-氨基戊酸1.树脂预处理:将ax-1树脂装柱,乙醇浸泡24h后,以2bv/h的流速通过树脂柱,至流出的液体不再浑浊为止,相同流速下,换用纯水洗至无醇;用1m的盐酸浸泡4-5h,同样流速下冲洗至流出液无色,换用纯水洗至中性;用1m的naoh浸泡4-5h,同样流速下冲洗至流出液无色,换用纯水洗至中性,纯水浸泡并加热到60℃,超声处理30min,60℃装柱,柱子高径比40:1。2.5-氨基戊酸转化液的制备与前处理按照xinwang,peipeicai等报道的全细胞催化的方法生产5-氨基戊酸。转化液于8000rpm下,离心10min,除去转化液中的菌体和蛋白。转化液中的其他成分经测定后见表1。表1:组分含量(g·l-1)5-氨基戊酸25l-赖氨酸1蛋白0.012盐离子21还原糖0.0173.上样与洗脱:取上述得到的5-氨基戊酸转化液10ml,流速0.68bv/h上柱,相同流速下,用60℃沸腾过的纯水先进行洗脱,由自动接液器每隔10min接一管样品,直到检测到流出液中没有任何物质时,相同流速下,换用60℃,0.5m的盐酸进行洗脱,由自动接液器每隔10min接一管样品,直到流出液中不含任何物质停止接样。4.树脂的再生:停止接样后,相同流速下,换用1m的盐酸溶液冲洗柱子2-3h,然后改用60℃沸腾过的纯水冲洗至中性即可。5.实验数据与结果分析:对每一管样品测定其盐离子浓度,5-氨基戊酸浓度,l-赖氨酸浓度,并以时间为横坐标,物质浓度为纵坐标绘制物质的流出色谱峰,计算水对5-氨基戊酸的解析率为80.5%。盐酸对5-氨基戊酸的解析率为18.9%,赖氨酸的解析率为99%。可见,通过水和盐酸的洗脱可以将5-氨基戊酸与l-赖氨酸完全洗脱下来。水洗脱的色谱峰如图2所示,经计算,盐离子与5-氨基戊酸的分离度为1.43。盐酸洗脱的色谱峰如图3所示,可见盐酸可以将5-氨基戊酸与l-赖氨酸同时洗脱下来。6.产品的浓缩:对纯水洗脱部分进行减压蒸馏,得微黄色固体,加入10ml水溶解后,再加入100ml乙醇结晶抽滤,50℃下烘干,得纯度99.9%的5-氨基戊酸0.19g,总收率78%。盐酸洗脱部分经减压浓缩后可以再次作为生产5-氨基戊酸的原料。实施例380℃下ax-1树脂分离5-氨基戊酸1.树脂预处理:将ax-1树脂装柱乙醇浸泡24h后,以2bv/h的流速通过树脂柱,至流出的液体不再浑浊为止,相同流速下,换用纯水洗至无醇;用1m的盐酸浸泡4-5h,同样流速下冲洗至流出液无色,换用纯水洗至中性;用1m的naoh浸泡4-5h,同样流速下冲洗至流出液无色,换用纯水洗至中性,纯水浸泡并加热到80℃,超声处理30min,80℃装柱,柱子高径比40:1。2.5-氨基戊酸转化液的制备与前处理按照aliakseiv.pukin,caimeng.boeriu等报道的酶催化的方法生产5-氨基戊酸。将转化液于8000rpm下,离心10min,除去转化液中的菌体和蛋白。转化液中的其他成分经测定后见表2。表2:组分含量(g·l-1)5-氨基戊酸29l-赖氨酸1蛋白0.012盐离子28还原糖0.0173.上样与洗脱:取上述得到的5-氨基戊酸转化液10ml,其中5-氨基戊酸的浓度为29g/l,l-赖氨酸的浓度大约为1g/l。流速0.68bv/h上柱,相同流速下,用80℃沸腾过的纯水先进行洗脱,由自动接液器每隔10min接一管样品,直到检测到流出液中没有任何物质时,相同流速下,换用80℃,0.5m的盐酸进行洗脱,由自动接液器每隔10min接一管样品,直到流出液中不含任何物质停止接样。4.树脂的再生:停止接样后,相同流速下,换用1m的盐酸溶液冲洗柱子2-3h,然后改用80℃沸腾过的纯水冲洗至中性即可。5.实验数据与结果分析:对每一管样品测定其盐离子浓度,5-氨基戊酸浓度,l-赖氨酸浓度,并以时间为横坐标,物质浓度为纵坐标绘制物质的流出色谱峰,计算水对5-氨基戊酸的解析率为92.1%。盐酸对5-氨基戊酸的解析率为7.1%,赖氨酸的解析率为99.1%,可见,通过水和盐酸的洗脱可以将5-氨基戊酸与l-赖氨酸完全洗脱下来。水洗脱的色谱峰如图4所示,经计算,盐离子与5-氨基戊酸的分离度为0.89。6.产品的浓缩:对纯水洗脱部分进行减压蒸馏,得微黄色固体,加入10ml水溶解后,再加入100ml乙醇结晶抽滤,50℃下烘干,得纯度99.9%的5-氨基戊酸0.24g,总收率83%。盐酸洗脱部分经减压浓缩后可以再次作为生产5-氨基戊酸的原料。ax-1树脂可以很好的分离来自全细胞催化和酶催化的5-氨基戊酸转化液。其中酶催化得到的5-氨基戊酸的解析率较高,这归因于较高的吸附解吸温度。为了提高5-氨基戊酸的解吸率,吸附解吸温度优选为80℃。实施例4ax-1树脂动态分离5-氨基戊酸。1.树脂预处理:将ax-1树脂装柱乙醇浸泡24h后,以2bv/h的流速通过树脂柱,至流出的液体不再浑浊为止,相同流速下,换用纯水洗至无醇;用1m的盐酸浸泡4-5h,同样流速下冲洗至流出液无色,换用纯水洗至中性;用1m的naoh浸泡4-5h,同样流速下冲洗至流出液无色,换用纯水洗至中性,纯水浸泡并加热到80℃,超声处理30min,80℃装柱,柱子高径比40:1。2.上样吸附:取实施例2全细胞催化途径得到的5-氨基戊酸转化液1000ml,其中5-氨基戊酸的浓度为25g/l,l-赖氨酸的浓度大约为1g/l。流速0.68bv/h通过柱子,由自动接液器每隔10min接一管样品,直到检测到流出液中得浓度与原液浓度相同时,停止吸附。3.洗脱:相同流速下,换用80℃纯水,由自动接液器每隔10min接一管样品,直到流出液中不含任何物质时,换用0.5m的盐酸进行洗脱,同样由自动接液器每隔10min接样一次,直到流出液中不含有任何物质时停止接样。4.树脂的再生:停止接样后,相同流速下,换用1m的盐酸溶液冲洗柱子2-3h,然后改用80℃沸腾过的纯水冲洗至中性即可。5.产品的检测与结果分析:在吸附过程中,测量了流出液中吸附质浓度随时间的变化曲线(穿透曲线),如图4所示。由穿透曲线知5-氨基戊酸大约在70min时开始穿透,l-赖氨酸大约在190min开始穿透,这也说明,ax-1树脂对l-赖氨酸的吸附能力大于对5-氨基戊酸的吸附能力,因此,5-氨基戊酸可以被水洗脱而l-赖氨酸需要由盐酸洗脱。经计算ax-1树脂对5-氨基戊酸的最大吸附量为107mg/g,对l-赖氨酸的最大吸附量为13mg/g。80℃纯水对5-氨基戊酸的解析率为91.2%,0.5m的盐酸对5-氨基戊酸的解析率为8.2%,对l-赖氨酸的解析率为99.8%,可见,纯水和0.5m的盐酸已经将吸附的5-氨基戊酸与l-赖氨酸全部洗脱。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1