一种扎那米韦多聚马来酸酐缀合物及合成方法与流程
本发明属于新化合物合成和药物应用领域,涉及一种扎那米韦多聚马来酸酐缀合物的合成。
技术背景
扎那米韦(zanamivir),化学名为4-胍基-2,4-二脱氧-2,3-脱氢-N-乙酰基-D-神经氨酸,是由澳大利亚Biota公司研发的一种抗流感病毒药,1999年在澳大利亚、美国及英国等地上市,商品名Relenza,用于A、B型流感的预防及治疗,也是目前治疗高致病性禽流感(如H5N1亚型病毒导致的禽流感)的有效候选药物之一。扎那米韦是神经氨酸酶抑制剂,通过抑制流感病毒的神经氨酸酶,从而改变流感病毒在感染细胞内的聚集和释放。神经氨酸酶是呼吸道病毒复制的关键酶,能够使唾液酸和细胞表面蛋白之间的化学键断裂,从而使新生成的病毒粒子与已感染细胞分离,进而感染附近正常细胞。抑制神经氨酸酶可以防止病毒向呼吸道其他细胞扩散。扎那米韦可用于治疗和预防流感病毒在呼吸道的扩散,且在症状开始的48h内使用很有效。
糖与蛋白间的高度专一性识别和粘附作用在细胞的生长、分裂、形成、受精、免疫调节、细胞转移和癌细胞转移等识别过程中起着重要作用。然而由于单糖分子与蛋白间的作用较弱,生物体中通过所谓的“多价效应”或“簇糖效应”有效的增强了其亲和能力。基于多价效应人们设计了大量多价糖缀和物,为研究生物体内糖类与蛋白间的相互作用提供了重要途径。自然条件下,流感病毒与细胞表面糖蛋白受体的唾液酸残基之间的识别和结合主要也是利用了多价效应。我们以扎那米韦作为糖基配体,利用多价效应增强其与流感病毒之间的结合能力,以作为强效的流感病毒抑制剂,并且借以研究糖和蛋白之间的多价识别和结合作用。我们选用多聚马来酸酐为高聚物骨架,合成的化合物水溶性好,能够有效的模拟天然的糖和蛋白之间的多价效应。
技术实现要素:
本发明的目的是发明一种扎那米韦多聚马来酸酐缀合物的合成方法,具体是:以N-乙酰基神经氨酸为起始原料,经过十四步化学合成,主要通过扎那米韦单体的合成、7位连接臂的合成,最终以多聚马来酸酐为骨架合成扎那米韦的多聚马来酸酐缀合物。
本发明的目的是通过以下技术方案实现的:
一种扎那米韦多聚马来酸酐缀合物的结构,其特征在于:结构通式如下:
其中,A部分为7位三聚乙二醇连接臂修饰的扎那米韦,通过在扎那米韦7位引入三聚乙二醇作为连接臂,末端经还原后的氨基能够与多聚马来酸酐高聚物通过氨解反应连接,同时不影响扎那米韦与流感病毒表面神经氨酸酶的结合能力;
B部分为多聚马来酸酐高聚物,作为扎那米韦缀合物的骨架,通过在偶联步骤改变A、B的投料比例,可以得到不同聚合度的目标化合物。
一种扎那米韦多聚马来酸酐缀合物的合成方法,以N-乙酰基神经氨酸为起始原料,经过十四步化学合成,主要通过扎那米韦单体的合成、7位连接臂的合成,最终以多聚马来酸酐为骨架合成扎那米韦的多聚马来酸酐缀合物,具体过程如下:
(A)resin,MeOH,90%;(B)Ac2O,Py,80%;(C)TMSOTf,EA,52℃,75%;(D)TMSN3,t-BuOH,92℃,45%;(E)Lindlar catalyst,MeOH,85%;(F)Boc2O,TEA,THF,75℃,87%;(G)MeONa,MeOH,82%;(H)Acetone,Camphorsulfonic acid,70%;(I)4-Nitrobenzoyl chloride,DMAP,Py,80℃,83%;(J)DMAP,NH2CH2CH2OCH2CH2OCH2CH2N3,Py,80%;(K)MeSC(=NBoc)NHBoc,HgCl2,Et3N,46%.(L)0.1M NaOH aq.(M)Lindlar catalyst(N)PMA,TFA/DCM
本发明的优点和积极效果:
1、本发明采用价廉易得的唾液酸和多聚马来酸酐为原料,所发明的反应方法具有低成本,产率高等显著优点。
2、在目标化合物的合成过程中,通过改变扎那米韦与多聚马来酸酐之间的投料比例,可以得到不同缀合度的扎那米韦多聚马来酸酐缀合物。
4、本发明所合成的扎那米韦多聚马来酸酐缀合物能够有效模拟天然糖与蛋白之间的多价结合效应,对于研究生物体内的多价效应和流感病毒与小分子抑制剂之间的多价结合方面具有非常重要的意义。
附图说明
图1为化合物4在氘代三氯甲烷中的核磁氢谱图;
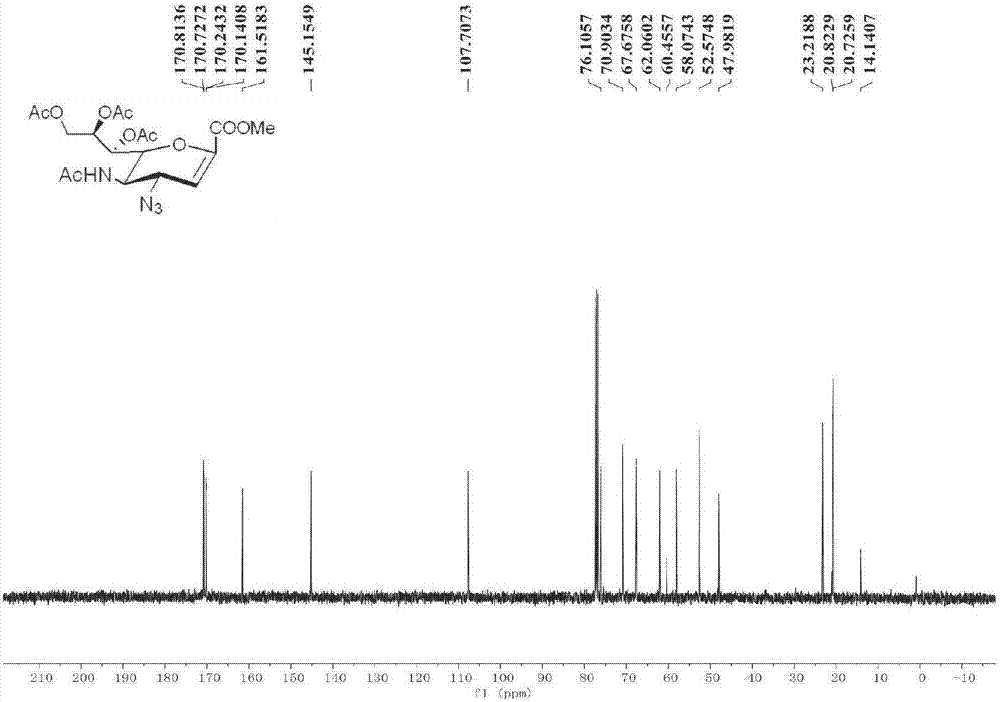
图2为化合物4在氘代三氯甲烷中的核磁碳谱图;
图3为化合物6在氘代三氯甲烷中的核磁氢谱图;
图4为化合物6在氘代三氯甲烷中的核磁碳谱图;
图5为化合物8在氘代甲醇中的核磁氢谱图;
图6为化合物8在氘代甲醇中的核磁碳谱图;
图7为化合物9在氘代三氯甲烷中的核磁氢谱图;
图8为化合物9在氘代三氯甲烷中的核磁碳谱图;
图9为化合物10在氘代三氯甲烷中的核磁氢谱图;
图10为化合物10在氘代三氯甲烷中的核磁碳谱图;
图11为化合物11在氘代三氯甲烷中的核磁氢谱图;
图12为化合物11在氘代三氯甲烷中的核磁碳谱图;
具体的实施方式
为了理解本发明,下面结合实施例对本发明作进一步说明:下述实施例是说明性的,不是限定性的,不能以下述实施例来限定本发明的保护范围。
一种扎那米韦多聚马来酸酐缀合物的结构,其特征在于:结构通式如下:
其中,A部分为7位三聚乙二醇连接臂修饰的扎那米韦,通过在扎那米韦7位引入三聚乙二醇作为连接臂,末端经还原后的氨基能够与多聚马来酸酐高聚物通过氨解反应连接,同时不影响扎那米韦与流感病毒表面神经氨酸酶的结合能力;
B部分为多聚马来酸酐高聚物,作为扎那米韦缀合物的骨架,通过在偶联步骤改变A、B的投料比例,可以得到不同聚合度的目标化合物。
上述扎那米韦多聚马来酸酐缀合物的合成方法,步骤如下:下面通过实施例具体说明目标化合物14的合成路线:
中间体1的合成。
将N乙酰基神经氨酸溶于30mL甲醇,加入阳离子树脂,搅拌12小时后反应液澄清,过滤除去阳离子树脂,浓缩滤液得到白色产品中间体1直接投入下一步反应。
中间体2的合成。
将中间体1溶于吡啶,冰浴下加入乙酸酐,搅拌12个小时,减压浓缩,硅胶柱层析纯化,得到中间体2。收率:80%;
中间体3的合成。
将中间体2溶于乙酸乙酯,加入三氟甲磺酸三甲基硅酯,升温至52℃,反应过夜。
收率:75%。
中间体4的合成。
将中间体3溶于叔丁醇,加入叠氮基三甲基硅烷,升温至92℃。反应8小时。
收率:45%。
中间体5的合成。
将中间体4溶于甲醇,加入林德拉催化剂,将反应瓶放入氢化仪,室温反应12个小时,砂板漏斗过滤,收集滤液旋蒸除去甲醇,得到中间体5。收率:80%。
中间体6的合成。
将中间体5溶于四氢呋喃中,加入二碳酸二叔丁酯,加入三乙胺,75℃回流反应过夜。旋蒸除去四氢呋喃和三乙胺,硅胶柱层析纯化得到中间体6。收率:87%。
中间体7的合成。
将中间体6溶于甲醇,加入甲醇钠,室温反应4个小时。用阳离子树脂中和反应液至近中性,过滤除去阳离子树脂,收集滤液,旋蒸除去甲醇,得到中间体7。收率:82%。
中间体8的合成。
将中间体7溶于丙酮,向反应液中加入对甲基苯磺酸,室温反应12个小时。反应完毕后加入三乙胺调节pH至中性,旋蒸除去丙酮,柱层析纯化得到中间体8。收率:70%;
中间体9的合成。
将中间体9溶于吡啶,加入对硝基苯甲酰氯和4-N,N-二甲氨基吡啶,升温至80℃回流反应16个小时。旋蒸除去吡啶,柱层析纯化得到中间体9。收率:83%。
中间体10的合成。
将2-(2-(2-叠氮乙氧基)乙氧基)乙胺和4-N,N-二甲氨基吡啶溶于吡啶,搅拌30分钟,然后加入中间体9,升温至80℃回流反应12小时。旋蒸除去吡啶,柱层析纯化得到中间体10,收率:80%。
中间体11的合成。
将中间体10溶于二氯甲烷,加入三氟乙酸后搅拌1小时,然后旋蒸除去二氯甲烷和三氟乙酸,所得粗品溶于二氯甲烷,然后加入三乙胺,搅拌30分钟后加入氯化汞和1,3-二(叔-丁氧基羰基)-2-甲基-2-异硫脲,室温搅拌反应12小时。反应液加入稀盐酸,然后用二氯甲烷萃取,浓缩,柱层析纯化得到中间体11。收率:46%。
中间体13的合成。
将中间体11溶于甲醇,再加入等体积的0.1M氢氧化钠水溶液,室温反应1小时后使用阳离子树脂中和PH至7,过滤、旋蒸除去溶剂,得到中间体12。将中间体4溶于甲醇,加入林德拉催化剂,将反应瓶放入氢化仪,室温反应12个小时,砂板漏斗过滤,收集滤液旋蒸除去甲醇,得到中间体13。
目标化合物14的合成。
将中间体13溶于二氯甲烷,加入丙二醇甲醚醋酸酯。反应完毕后在0℃下加入50%的三氟乙酸,搅拌10分钟后将反应瓶转移至室温下反应1小时。旋蒸除去溶剂,所得粗品溶解于蒸馏水,使用Sephadex G-75交联葡聚糖凝胶柱分离纯化,冻干得到目标化合物14。
生物活性评价
神经氨酸酶抑制实验
神经氨酸酶抑制实验是由美国疾病预防控制中心开发的基于荧光的检测方法,用来评价流感病毒对神经氨酸酶抑制剂的敏感性。流感病毒唾液酸水解酶能够水解底物MUNANA,水解产物伞形酮在365nm激发光下发射480nm检测光。NA抑制剂能够与MUNANA竞争性的结合病毒,使水解效率降低,荧光曲线降低,因此通过荧光曲线斜率的变化衡量化合物NA的抑制活性。我们对合成的化合物(ZA-PM)进行活性,使用的病毒毒株为:A/Huairou,Beijing/11069/2014(H3N),A/Chicken/Beijing/AT609/2014(H9N2),A/Puerto Rico/8/1934(H1N1)。具体操作步骤如下:(1)加样:将流感病毒加入384孔板中(15μL/孔),再向孔中分别加入化合物(15μL/孔)。其中只加病毒不加化合物组为阴性对照组,设置三组平行。(2)孵育:将加好样的384孔板放入微孔板离心机中离心,取出后放至恒温振荡孵育器中孵育30分钟。(3)加底物:用移液器吸取30μL配制好的200μM底物MUNANA快速加入到对应的孔中,用微孔板离心机进行离心。(4)荧光信号检测:对上述的384孔酶标板进行荧光强度变化的检测,设置酶
标仪激发光为365nm、发射光为480nm,每2分钟检测一次荧光信号,共检测1.5小时。活性数据如下表所示。
表1-1神经氨酸酶抑制活性
- 还没有人留言评论。精彩留言会获得点赞!