一种核酸检测方法与流程
本发明属于基因技术领域,尤其涉及一种核酸检测方法。
背景技术:
核酸是由核苷酸聚合形成的生物大分子化合物,是生命最基本的物质之一。核酸广泛存在于动植物细胞、微生物体内。根据化学组成的不同,核酸可分为核糖核酸(RNA)及脱氧核糖核酸(DNA)。其中,DNA是储存、复制和传递遗传信息的主要物质基础,而RNA在蛋白质合成过程中起着非常重要的作用。核酸与多种遗传性疾病(如人类镰刀形血细胞贫血症等)相关,肿瘤的发生及病毒的感染等也伴随着核酸的表达。因此,核酸的检测对于疾病的检测、及预后评价等有着非常重要的作用。
目前核酸检测的方法主要是基于核酸的扩增,即通过PCR等技术使检测信号放大,然后通过荧光成像等方法对核酸进行定性定量检测。但是PCR扩增技术在检测过程中可能出现假阴性或假阳性,导致检测的结果不准确。
技术实现要素:
本发明提供一种核酸检测方法,旨在解决现有的PCR扩增技术在检测过程中可能出现假阴性或假阳性,导致检测的结果不准确的问题。
本发明提供一种核酸检测方法,包括:
将核酸捕获序列与待检测的核酸的一端杂交;
将第一核酸序列与所述待检测的核酸的另一端杂交形成直链;
将第二核酸序列与所述直链上的第一核酸序列杂交,其中,第一核酸序列和所述第二核酸序列分别为稀土纳米材料修饰的发卡结构。
本发明提供的一种核酸检测方法,通过将第一核酸序列与第二核酸序列进行杂交,使得稀土纳米材料修饰的发卡结构的核酸序列进行自组装形成三明治结构,大大增加了稀土纳米材料及镧系元素的数量,从而增加了核酸检测的灵敏度,提高检测结果的准确性。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例。
图1是本发明实施例提供的一种核酸检测方法的实现流程示意图;
图2是本发明实施例稀土纳米材料修饰的发卡结构的核酸的制备的流程示意图;
图3是本发明实施例单个稀土胶束组装检测核酸、单个稀土纳米颗粒组装检测核酸及稀土-核酸三明治结构组装检测核酸原理的示意图。
具体实施方式
为使得本发明的发明目的、特征、优点能够更加的明显和易懂,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而非全部实施例。基于本发明中的实施例,本领域技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明提供的一种核酸检测方法,该方法包括:
步骤一、将核酸捕获序列与待检测的核酸的一端杂交;
步骤二、将第一核酸序列与所述待检测的核酸的另一端杂交形成直链;
步骤三、将第二核酸序列与该直链上的第一核酸序列杂交。
其中,第一核酸序列和该第二核酸序列分别为稀土纳米材料修饰的发卡结构。
具体地,以HIV核酸保守序列为检测目标序列时,例如,为GCTAGAGATTTTCCACACTGACTAAAAGGGTCTGAGGG时,核酸捕获序列为biotin-(A)15CCCTCAGACCCTTTTAGT。第一核酸序列为5’-biotin-(A)15CAGTGTGGAAAATCTCTAGCACTTAGGCTAGAGATTTTCC-3’,第二核酸序列为5’-biotin-(A)15GCTAGAG ATTTTCCACACTGGGAAAATCTCTAGCCTAAGT-3’。
需要说明的是,第一核酸序列与第二核酸序列只有在与待检测的核酸形成直链后才可反应,二者单独存在时不反应。第一核酸序列与第二核酸序列中的稀土纳米材料可以通过柠檬酸盐与亲和素修饰末端包含有生物素的发卡结构的核酸链进行反应得到。如图1所示,图1为第一核酸序列(探针1)和第二核酸序列(探针2)的制备流程示意图。
具体地,稀土纳米材料的粒径为1~5nm。优选地,稀土纳米材料为NaEuF4、NaDyF4、NaSmF4和NaTbF4中的至少一种。
进一步地,该方法还包括:
步骤四、将第一核酸序列与在直链上的第二核酸序列杂交。
可选地,在步骤四之后,在步骤四的基础上重复步骤三,再重复步骤四,以此类推。如此,随着反应的进行,第一核酸序列和第二核酸序列不断杂交,形成了具有多个第一核酸序列和第二核酸序列的三明治杂交链。
一、稀土纳米材料修饰的发卡结构的核酸的制备方法包括:
1、稀土纳米材料前驱体制备:将稀土盐溶液、油酸、十八烯按照质量比:5~10:1~2:1~2混合,在140~160℃下反应30~90min,形成透明溶液,冷却至室温;
其中,稀土盐溶液为醋酸铕、氯化铕、醋酸镝、氯化镝、醋酸钐、氯化钐的水溶液,其浓度为0.5~2g/L。
2、稀土纳米材料修饰的发卡结构的核酸的制备:
按照质量比1:1~2:2~3在1得到的前驱体中加入氟化铵和氢氧化钠,室温下搅拌6~18h,并在真空、150~300℃的条件下反应5~30min,得到稀土纳米材料。
将5~10mg的稀土纳米材料分散于2~5mL的氯仿中,并加入3~5mL无水乙醇及1~3mL浓度为0.15~0.2mol/L的柠檬酸钠溶液,室温搅拌8~12h,离心得到柠檬酸盐修饰的稀土米颗粒;
将上述纳米颗粒分散于4mL pH为7.4的磷酸缓冲液中,加入EDC及NHS溶液,室温反应1~3h,加入1mL浓度为1mg/L的亲和素,反应30min后,离心,将得到的物质分散在pH为7.4的磷酸缓冲液中;
在得到的物质所在的磷酸缓冲液中加入0.05mL 10μmol/L生物素修饰的发夹结构第一核酸(探针1)或第二核酸(探针2),反应30~90min,离心分离,稀土纳米材料修饰的发卡结构的核酸得到4℃下保存于pH为7.4的磷酸缓冲液中。
请参阅图2,图2示出了稀土纳米材料修饰的发卡结构的核酸的制备的流程示意图。
二、捕获序列的固定修饰方法:
将2~5mL浓度为1mg/L的亲和素加入到蛋白亲和的96孔板中,室温条件下培育30~60min,利用盐酸缓冲液洗涤2次,加入2~5mL浓度为10μmol/L经生物素修饰的核酸捕获序列,室温条件下反应30~120min,用磷酸缓冲液洗涤2至3遍。
三、待检测的核酸与捕获序列的杂交反应
将待检测的核酸溶液加入到上述修饰的96孔板中,在37℃的条件下反应30~60min,利用磷酸缓冲液洗涤2次。
四、第一核酸序列与第二核酸序列的杂交组装反应
将上述一制备得到的第一核酸序列或第二核酸序列加入已杂交了第二核酸序列或第一核酸序列的直链的溶液中,在37℃下反应2~3h,用磷酸缓冲溶液清洗2次。
五、时间分辨荧光成像
在反应后的96孔板中加入200~400μL增强溶液,反应5min,用荧光显微镜测试其发光强度,并将所得到的荧光强度与标准溶液所测得的荧光强度进行对比,得到待检测的核酸的浓度。
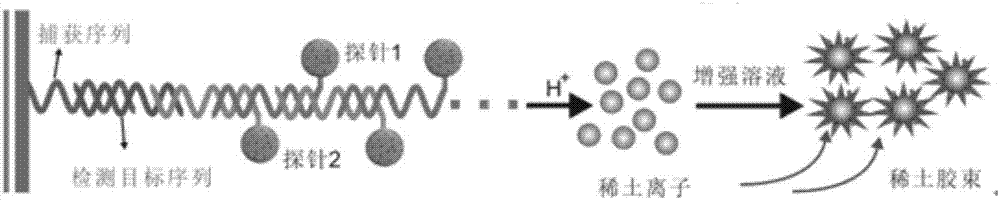
如图3中的a~c所示,分别示出了单个稀土胶束组装检测核酸、单个稀土纳米颗粒组装检测核酸及稀土-核酸三明治结构组装检测核酸原理的示意图。
实施例
(1)稀土纳米材料前驱体制备:5mL醋酸铕溶液(0.2mol/L)与4mL油酸及15mL十八烯溶液混合,在150℃反应1h,形成透明溶液,冷却至室温;
(2)稀土纳米材料制备:在步骤(1)得到的前驱体中加入氟化氨及氢氧化钠溶液,室温下搅拌12h,然后将溶液在真空条件下加热到260℃并反应10min;冷却至室温后,离心分离,最后分散在环己烷溶液中;
(3)稀土纳米材料修饰:将步骤(2)中合成的NaEuF4纳米颗粒分散在5mL氯仿中,并加入3mL无水乙醇及3mL浓度为0.15mol/L柠檬酸钠溶液,室温搅拌约10h,最后高速离心分离得到柠檬酸盐修饰的NaEuF4纳米颗粒,分散在4mL pH 7.4的磷酸缓冲液中;加入EDC及NHS溶液,室温反应3h,然后加入1mL 1mg/L的亲和素,反应30min后,高速离心分离,将NaEuF4纳米颗粒分散在pH 7.4的磷酸缓冲液中;然后加入0.05mL 10μmol/L生物素修饰的发夹结构探针1或探针1并反应30min,离心分离,4度低温保存于pH 7.4的磷酸缓冲液中。
(4)捕获序列的固定修饰:将400μL 1mg/L的亲和素加入到蛋白亲和的96孔板中,室温培育1h,然后用磷酸缓冲液洗涤2遍,加入200μL 10μmol/L生物素修饰的核酸捕获序列,室温反应1h后,用磷酸缓冲液洗涤2遍。
(5)所检测核酸与捕获序列的杂交反应:将所检测的目标核酸序列溶液加入到步骤(4)中修饰的96孔板中,37℃反应30min到60min,再用磷酸缓冲液洗涤2遍。
(6)探针1与探针2的杂交组装反应:加入步骤(3)中合成的200μL NaEuF4纳米颗粒修饰的探针1和探针2,37℃反应3h,然后用磷酸缓冲液洗涤2遍
(7)时间分辨荧光成像:在步骤(6)反应后的96孔板中加入300μL增强溶液,反应约5min后,用荧光显微镜测试其发光强度。所得到的荧光强度与标准溶液所测得的荧光强度进行对比,得到所检测核酸的浓度。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!