三桥环荚孢腔酮类化合物及其制备方法和用途
1.本发明属于天然药物领域,具体涉及三桥环荚孢腔酮类化合物及其制备方 法和用途。
背景技术:
2.神经退行性疾病是一种大脑和脊髓的细胞神经元丧失的疾病状态,随着时 间的推移而恶化,其可分为急性神经退行性疾病和慢性神经退行性疾病,前者 主要包括脑缺血(ci)、脑损伤(bi)等;后者包括老年痴呆、帕金森病(pd)、 亨廷顿氏病(hd)、肌萎缩性侧索硬化(als)、不同类型脊髓小脑共济失 调(sca)以及pick病等。
3.临床上常见的老年痴呆类型包括阿尔茨海默病(alzheimer’s disease,ad)、 血管性痴呆病(vascular dementia,va)、路易体痴呆病(dementia with lewybodies,dlb)以及额颞痴呆(frontotemporal dementia,ftd)等。其中,阿 尔茨海默病患者占老年痴呆患者总数的50~70%,是老年痴呆中最常见的类 型。
4.目前已经上市治疗老年痴呆症的药物主要以乙酰胆碱酯酶抑制剂和n-甲 基-d-天门冬氨酸受体拮抗剂为主,这些药物能在一定程度上改善患者的痴呆 症状,但不能从根本上阻止病情的恶化。实质上,过去20年来神经退行性疾 病领域新药研发几乎全军覆没。礼来、阿斯利康、强生、辉瑞、罗氏等制药巨 头的多个药物均在iii期临床惨遭失败,这为这一领域的新药研发蒙上了厚厚 的阴云。2019年11月03日,我国有一款治疗阿尔茨海默病新药甘露特钠获准 上市,结束了该领域全球17年无新药上市的历史。该药物以来源于海洋的天 然产物提取物为原料制备得到,可以说甘露特钠的成功为我国学者从天然产物 中寻找预防或治疗神经退行性疾病药物的研究思路带来了鼓舞。然而,从世界 范围看,目前仍存在对于疗效好、副作用低、耐受性好的新型预防或治疗神经 退行性疾病药物的持续迫切需求。
5.有鉴于此,本发明人开发了一种用于预防或治疗神经退行性疾病的新型三 桥环荚孢腔酮类化合物及其制备方法和用途。
技术实现要素:
6.本发明的第一个方面提供了一种三桥环荚孢腔酮类化合物或其药学上可 接受的盐,具体结构式如下:
[0007][0008]
其中r1和r2选自h、c
1-c4烷基或oh;
[0009]
或者,r1=ch3或h,r2=ch3或oh;
[0010]
或者,r1=ch3且r2=oh,或r1=h且r2=ch3。
[0011]
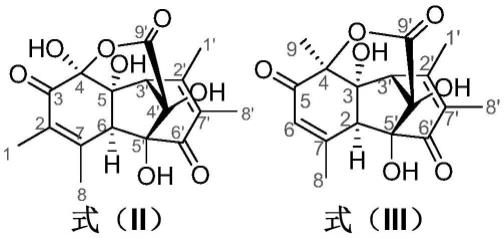
所述三桥环荚孢腔酮类化合物的示例性结构如下所示:
[0012][0013]
本发明的第二个方面提供上述新化合物或其药学上可接受的盐的制备方 法,其方案如下:
[0014]
a.式(i)所示的三桥环荚孢腔酮类化合物的来源微生物培养产生;
[0015]
b.使用有机溶剂提取发酵物,将提取液减压浓缩,得到粗提物;
[0016]
c.使用柱层析色谱方法分离粗提物,经洗脱剂洗脱、后处理得到式(i)所 示的三桥环荚孢腔酮类化合物。
[0017]
其中,所述步骤a中,微生物选自荚孢腔属真菌,保藏号为:cgmcc no. 18810;培养基为大米培养基;培养温度为20-40℃,优选25-30℃,更优选27℃。
[0018]
更为具体地,本发明使用的荚孢腔菌(sporormiella sp.)(菌株编号: 40-1-4-1)从采自中国长白山的地衣尖头石蕊cladonia subulata(l.)wigg.中分 离,经分类学研究鉴定为荚孢腔菌(sporormiella sp.),其its和5.8s rrna 基因序列的genbank登录号为mk942641,并于2019年11月19日保藏于中 国微生物菌种保藏管理委员会普通微生物中心(编号:cgmcc no.18810,地 点:中国北京市朝阳区北辰西路1号院3号中国科学院微生物研究所,100101)。
[0019]
所述步骤b中,有机溶剂选自c
3-10
酯、c
2-10
醚,优选c
4-7
酯、c
4-6
醚,更 优选乙酸乙酯、乙酸丁酯、乙醚、甲基叔丁基醚,最优选乙酸乙酯。
[0020]
所述步骤c中,柱层析色谱选自硅胶柱色谱、ods柱色谱、ods-mplc 柱色谱、hplc色谱或其组合。
[0021]
进一步地,所述步骤c中,粗提物在硅胶柱上环己烷和甲醇洗脱,所得甲 醇部位w经ods柱层析梯度洗脱,洗脱剂为甲醇-水或氯仿-甲醇,得到5个 馏分w1至w5;其中w1经ods-mplc梯度洗脱,洗脱剂为甲醇-水,得到6 个馏分w1-1至w1-6;其中w1-4经hplc分离,洗脱剂为甲醇-水,得到3 个馏分w1-4-1至w1-4-3;其中馏分w1-4-1经hplc分离得到8个馏分 w1-4-1-1至w1-4-1-8;其中馏分w1-4-1-5再经hplc分离获得式(ii)化合 物;其中馏分w1-4-1-4再经hplc分离获得式(iii)化合物。
[0022]
本发明的第三个方面提供上述新化合物或其药学上可接受的盐在制备预 防或治疗神经退行性疾病药物中的应用。
[0023]
所述神经退行性疾病包括但不限于老年痴呆、帕金森病、多发性硬化症、 肌萎缩性侧索硬化和亨廷顿氏病中的一种或几种;其中老年痴呆选自阿尔茨海 默病、血管性痴呆病、路易体痴呆病或额颞痴呆。
[0024]
尽管本发明的化合物可以不经任何配制直接给药,但是本发明在第四个方 面优选提供一种预防和/或治疗神经退行性疾病的药物组合物,其包含上述新化 合物或其药学上可接受的盐,和药学上可接受的辅料,所述药学上可接受的辅 料选自稀释剂、润滑剂、粘合剂、崩解剂、稳定剂或溶剂中的一种或多种。
[0025]
本发明所述稀释剂包括但不限于淀粉、微晶纤维素、蔗糖、糊精、乳糖、 糖粉、葡萄糖等;所述润滑剂包括但不限于硬脂酸镁、硬脂酸、氯化钠、油酸 钠、月桂醇硫酸钠、泊洛沙姆等;所述粘合剂包括但不限于水、乙醇、淀粉浆、 糖浆、羟丙基甲基纤维素、羧甲基纤维素钠、海藻酸钠、聚乙烯吡咯烷酮等; 所述崩解剂包括但不限于淀粉泡腾混合物即碳酸氢钠和枸橼酸、酒石酸、低取 代羟丙基纤维素等;所述稳定剂包括但不限于多糖如金合欢胶、琼脂、藻酸、 纤维素醚和羧甲基甲壳酯等;所述溶剂包括但不限于水、平衡的盐溶液等。
[0026]
可以将所述药物组合物制成各种固体口服制剂、液体口服制剂、注射剂等。 药剂学可接受的口服剂固体制剂有:普通片剂、分散片、肠溶片、颗粒、胶囊、 滴丸、散剂等,口服液体制剂有口服液、乳剂;注射剂有:小水针、输液、冻 干粉针等。上述各种剂型可以根据药物制剂领域的常规工艺制备而成。
[0027]
药物制剂中含有的活性成分(即本发明化合物或其药学上可接受的盐)的 量可以根据患者病情、医生诊断情况等特定地加以应用,所用的化合物或其药 学上可接受的盐的量或浓度可以在一个较宽范围内调节,通常活性化合物或其 药学上可接受的盐的量的范围为药物组合物的1%~90%(重量)。
[0028]
本发明相对于现有技术,具有以下有益效果:本发明所示的三桥环荚孢腔 酮类化合物是一类新骨架聚酮类化合物;通过生物活性测试表明本发明三桥环 荚孢腔酮类化合物能够显著改善老年痴呆果蝇的学习记忆能力,因而可以将其 用于制备预防或治疗神经退行性疾病的药物。
具体实施方式
[0029]
下面将进一步举例说明本发明。需要指出的是,以下说明仅仅是对本发明 要求保护的技术方案的举例说明,并非是对这些技术方案的任何限制。本发明 的保护范围以所附权利要求书记载的内容为准。
[0030]
下列实施例中,质谱仪为美国waters公司生产的waters synapt g2 tof质 谱仪。超导核磁共振仪为bruker av-600和bruker av-400。薄层色谱用硅胶 gf254和柱色谱硅胶(200-300目)均为青岛海洋化工厂产品。反相ods填料 50μm为日本ymc公司产品。中低压液相色谱仪为上海利穗电子科技有限公 司产品。液相分离所使用色谱柱为ymc-pack ods-a色谱柱(10.0
×
250mm, 5μm)。液相色谱用乙腈为色谱纯,水为双重蒸馏水,其他试剂均为分析纯。
[0031]
实施例1:荚孢腔属真菌40-1-4-1大量发酵及其样品前处理方法
[0032]
(1)荚胞腔属真菌40-1-4-1经pda斜面活化后接种于pdb培养基,在 25℃下以200r.min-1
震荡培养3天制备种子液,再按照5%接种量接种200个 装有大米培养基的三角烧瓶中,27℃下,避光静止培养50天,得到发酵物。 所述大米培养基由以下组分组成:大米70g/瓶,纯净水105l/瓶。
[0033]
(2)将发酵物加入乙酸乙酯进行浸泡提取3次,将提取液减压浓缩至干, 得到粗提
物(115.1g)。
[0034]
实施例2:三桥环荚孢腔酮类化合物的制备
[0035]
粗提物上样至硅胶柱,经环己烷和甲醇洗脱,得到环己烷部分c(70.4g) 和甲醇部位(w,38.5g)。甲醇部位经过ods柱层析梯度洗脱(洗脱系统: 甲醇-水30-70、50-50、70-30、100-0,氯仿-甲醇1-1)得到5个馏分w1(19.7 g)、w2(5.1g)、w3(3.3g)、w4(5.7g)、w5(4.2g)。w1经过ods-mplc 梯度洗脱得到6个子馏分w1-1(3.37g)、w1-2(2.64g)、w1-3(0.97g)、 w1-4(9.0g)、w1-5(1.53g)、w1-6(0.5g)[甲醇-水梯度条件:5%-5%(200 min)-6%(100min)
–
10%(100min)
–
20%(100min)
–
50%(100min)-100% (100min)-100%(100min)]。
[0036]
w1-4(9.0g)经hplc制备[18%甲醇-水,100ml/min,制备色谱柱:marchalc
18 6μc
18
色谱柱(6μm,50
×
250mm)]得到馏分w1-4-1(1.4g)、w1-4-2 (775.3mg)、w1-4-3(264.6mg)。其中馏分w1-4-1经hplc分离[8%乙腈
ꢀ‑
水,3ml/min,半制备色谱柱:ymc-pack ods-a 5μc
18
色谱柱(5μm,10
×
250 mm)],得到8个馏分w1-4-1-1至w1-4-1-8;其中馏分w1-4-1-5经hplc制 备[5%乙腈-水,8ml/min,phenomenex kinetex c8色谱柱(5μm,21.2
×
250mm)], 得到化合物(ii),所获化合物纯度为95%。其中馏分w1-4-1-4经hplc制备[10% 甲醇-水,3ml/min,ymc-pack ods-a柱(5μm,10
×
250mm)],得到化合 物(iii),所获化合物纯度为95%。
[0037]
所获得化合物的理化常数如下:
[0038]
化合物式(ii):黄色结晶(meoh);熔点194~199℃;esi-ms(positive): m/z 351[m+h]
+
,m/z 723[2m+na]
+
;hresims(positive)m/z351.1076[m+ h]
+
(计算值:c
17h19
o8,351.1080);uv(meoh)λ
max
(logε)250(4.02)nm; ir(kbr)ν
max
3470,2925,1755,1671,1624,1378,1338,1205,1173,1034cm-1
。1h 和
13
c nmr见表1。
[0039]
化合物式(iii):黄色结晶(meoh);熔点197~203℃;esi-ms(positive): m/z 335[m+h]
+
,m/z 357[m+na]
+
;hresims(positive)m/z335.1124[m+h]
+ (计算值:c
17h19
o7,335.1131);uv(meoh)λ
max
(logε)205(4.00),230(4.08) nm;ir(kbr)ν
max
3418,2921,2900,1758,1677,1626,1380,1211,1170,1037,804 cm-1。1h和
13
c nmr见表2。
[0040]
表1:化合物式(ii)的
13
c nmr(150mhz)及1h nmr(600mhz)数据和归属(dmso-d6为测试溶剂)
[0041][0042]
[0043][0044]
注释:#在核磁中检测不到。
[0045]
表2:化合物式(iii)的
13
c nmr(150mhz)及1h nmr(600mhz)数据和归属(dmso-d6为测试溶剂)
[0046][0047]
[0048]
实施例3:化合物提高老年痴呆果蝇学习记忆活性测试
[0049]
(1)老年痴呆果蝇的培育
[0050]
将w
1118
(isocj1)作为实验的对照组背景果蝇,简称为“2u”。成功转入 致病性aβ
42
蛋白的果蝇为(uas-aβ
42
;简称为“h29.3”)。该品系果蝇通过与 全脑表达gal4启动子果蝇进行杂交,获得携带elav-gal4
c155
(p35)与aβ
42
的果蝇品系。
[0051]
(2)老年痴呆果蝇的给药
[0052]
试验设置健康果蝇无药对照(空白组)、疾病果蝇无药对照(模型组)和 疾病果蝇给药(治疗组)的三种组别。
[0053]
所有测试果蝇的亲本均在恒温24℃,恒湿42%rh的蝇房饲养和繁殖。果 蝇羽化后的第一天将空白组果蝇及模型组果蝇和待给药组果蝇通过二氧化碳 麻醉之后,筛选正确性状的果蝇在含有食物的玻璃管中。在给药阶段,所有测 试果蝇在28℃恒温和42%rh恒湿的保温箱内饲养,以保证果蝇吃药的效率。 每日果蝇喂药4小时,从筛选出果蝇的第2天起一直给药到第8天。
[0054]
所喂药物(阳性对照药:美金刚,化合物(ii))在挑蝇第2天配制并于配 制当天给果蝇喂药。使用100%dmso溶解使药物浓度为10mm。在配制工作 液时,利用4%的蔗糖水溶液将10mm母液稀释至100μm。另外,空白组和 模型组果蝇喂含有1%dmso的蔗糖水溶液。对于每个行为指数(performanceindex,pi),需要有2管果蝇组,每管中含有约100只果蝇。
[0055]
实验在恒温25℃、恒湿70%rh,避光的行为房中进行,具体实验方法可 参见如下文献:tully t,et al.j.comp.physiol.a 1985,157,263-277;tully t,et al. cell 1994,79,35-47;和yin jc,et al.cell 1994,79,49-58。
[0056]
1)在训练阶段,将大约100只果蝇装入安置有铜网交叉电极的训练管, 先后通入辛醇(oct)和甲基环己醇(mch)两种气味各60秒,中间间隔45 秒的新鲜空气。在通入第一种气味(cs+)的同时给予果蝇60v脉冲电击刺激 (us,脉冲时长1.5秒,间隔3.5秒)。通入第二种气味(cs-)时不给予电 击。如此完成一个训练周期。
[0057]
2)在瞬时记忆(学习)能力测试中,将完成一个训练周期的果蝇立即转 移到t-迷宫的选择点,同时从相对的两个方向通入cs+和cs-。经过2min的 选择后两侧的果蝇被分别收集,麻醉或处死后进行计数。pi的计算公式如下: pi=[(cs-)-(cs+)]/[(cs-)+(cs+)]
×
100。
[0058]
分别使用oct和mch作为cs+和cs-进行训练和测试,得到的两个pi 的平均值作为一次实验的pi使用。pi=0表示测试中果蝇对于两种气味的选择 为50:50,即没有形成记忆;pi=100表示测试中果蝇全部逃避伴随电击的气味, 即完美记忆。进行活性测试时,同时进行不给药的同遗传背景健康蝇(p35*2u, 空白组)、不喂药的老年痴呆疾病蝇(p35*h29.3,模型组)、喂测试药(阳性 对照药:美金刚,化合物(ii))的老年痴呆疾病蝇的嗅觉短期记忆缺陷测试, 分别计算其总学习记忆行为指数。将喂测试药的老年痴呆疾病蝇学习记忆行为 指数与不喂药的同遗传背景健康蝇(p35*2u)行为指数、不喂药的老年痴呆疾 病蝇(p35*h29.3)行为指数进行统计学比较,评价测试药物抗老年痴呆的作用。 喂食测试药物的老年痴呆疾病蝇学习记忆行为指数相对越高,则说明测试药物 抗老年痴呆作用越强。采用单因素anova分析进行统计学检验,比较喂食测 试药物的老年痴呆疾病蝇学习记忆行为指数和不喂药(空白组和模型组)的老 年痴呆疾病蝇学习记忆行为指数,p《0.05为具有明
显差异,p《0.01为具有显著 差异,p《0.001为具有极显著差异。使用graphpad prism 8.01对实验结果进行 处理,具体结果见表3。
[0059]
表3:本发明化合物提高老年痴呆果蝇学习记忆活性的结果
[0060][0061]
注释:p35*2u代表健康果蝇;p35*h29.3代表疾病果蝇;美金刚代表阳性对照药治疗组。各 药物治疗组给药浓度为100μm。与p35*2u组比较,
###
p《0.001;与p35*h29.3组比较,
**
p 《0.01;n=6。
[0062]
如上表3中所示,统计学检验的结果表明,模型组与空白组相比其pi值 具有极其显著的差异(p《0.001),表明老年痴呆果蝇模型制备成功,模型组 果蝇的短期学习记忆能力显著变差。阳性对照组以及化合物(ii)组与模型组相 比,其pi值均具有显著性差异(p《0.01),提示给予患病果蝇阳性对照药美 金刚以及实验药物化合物(ii)后,果蝇的短期学习记忆能力得以部分恢复,并 且从表3中可以看出,化合物(ii)改善老年痴呆果蝇学习记忆的能力甚至优于 阳性对照药美金刚。
[0063]
本发明内容仅仅举例说明了要求保护的一些具体实施方案,其中一个或更 多个技术方案中所记载的技术特征可以与任意的一个或多个技术方案相组合, 这些经组合而得到的技术方案也在本技术保护范围内,就像这些经组合而得到 的技术方案已经在本发明公开内容中具体记载一样。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1