一种介孔材料及其修饰方法和用途与流程
本发明涉及一种介孔材料的修饰方法及修饰所得介孔材料的用途,尤其是一种介孔硅材料的修饰方法及修饰后所得介孔硅材料在分离ctdna中的用途。
背景技术:
介孔材料是指孔径介于2-50nm的一类多孔材料。介孔材料具有极高的比表面积、规则有序的孔道结构、狭窄的孔径分布、孔径大小连续可调等特点,使得它在很多微孔沸石分子筛难以完成的大分子的吸附、分离,尤其是催化反应中发挥作用。一般生物大分子如蛋白质、酶、核酸等,当它们的分子质量大约在1~100万之间时尺寸小于10nm,相对分子质量在1000万左右的病毒其尺寸在30nm左右。有序介孔材料的孔径可在2-50nm范围内连续调节和无生理毒性的特点使其非常适用于酶、蛋白质等的固定和分离。
但是,不经过修饰的硅材料对蛋白和核酸的吸附和捕获的能力比较低,主要原因是硅材料表面主要是硅羟基,其在生理环境(ph6-8)下,主要呈负电性,因此对蛋白和核酸等物质的捕获能力比较差。由于硅材料表面的羟基极易发生取代,因此硅材料容易被修饰。通过对硅材料修饰上特定的基团,配合相应的孔径可以实现对蛋白和核酸等的高效捕获。但是,在修饰过程中,需要对整个条件进行控制,以保证修饰效果。但是经过修饰之后,很难实现对硅羟基的完全取代,残留的硅羟基会影响材料对蛋白和核酸的捕获,因此对硅材料表面硅羟基的完全将大大提高材料对蛋白和核酸等的捕获效率。
循环肿瘤dna循环肿瘤dna,即ctdna(circulatingtumordna),是指肿瘤细胞体细胞dna经脱落或者当细胞凋亡后释放进入循环系统,是一种特征性的肿瘤生物标记。通过ctdna检测,能够检出血液中的肿瘤踪迹。对于大部分ctdna,其大小为150bp左右,因此其大小为50nm(直径为2nm,典型的dna双螺旋大约平均一圈为10个bp长34a,即3.4nm,所以1bp=0.34nm,所以通过计算可以得到ctdna的大小)。
然而,对于ctdna在实际应用中存在以下问题:1)ctdna在血液中的半衰期短,只有两个小时左右,同时ctdna在血液中不稳定,因此在检测ctdna时,需要迅速从血液样品中分离出ctdna。2)对于大部分现有技术,绝大多数样品需要两个小时以上进行样品的准备[2].3)ctdna主要来自于血液样品,同时这些样品需要进行一系列复杂操作来分离ctdna,来进行后续的检测。这些复杂的操作需要昂贵的仪器设备和专业摄氏,因此对于一些社区医院和偏远地区,ctdna的检测受到了极大的限制。因此,需要一种迅速而且简单的方法来对ctdna进行分离。
技术实现要素:
本发明的目的在于针对上述现有技术的不足之处而提供一种可控的介孔材料修饰方法及采用所述方法修饰得到的介孔材料;同时,本发明的另一目的在于提供一种采用所述修饰后的介孔材料修饰方法对血液或尿液样品中特定蛋白和ctdna的捕获分离方法。
为实现上述目的,本发明采取的技术方案为:一种介孔材料修饰方法,所述方法包括以下步骤:
(1)将介孔材料烘干;
(2)将介孔材料均匀分散在溶剂中,然后在所述溶剂沸点温度以上油浴至少6小时;
(3)然后加入化合物a,继续油浴至少12小时;
(4)收集步骤(3)中修饰过的介孔材料,用洗脱剂洗脱,然后除去洗脱剂;
其中化合物a的结构式为:
x为甲氧基或乙氧基,y为c18h37、c8h17、ch2或苯基。
本发明所述介孔材料修饰方法,采用所述特定的化合物a在特定的修饰条件下,对介孔材料进行修改,本申请发明人发现,本发明所述方法修饰后所得介孔材料对蛋白和核酸具有较好的捕获能力。
本发明所述介孔材料修饰方法,其中步骤(2)和步骤(3)中的油浴时间分别为至少6小时和至少12小时,本领域技术人员根据实际情况可选择油浴更长的时间。
作为本发明所述介孔材料修饰方法的优选实施方式,所述步骤(2)介孔材料与溶剂的量比为1g/40ml;所述溶剂为苯、甲苯、四氯化碳、二氧乙烷中的至少一种;所述油浴中使用的油为二甲基硅油。将介孔材料按照一定的量比均匀分散在溶剂中,而且选择所述特定的溶剂,采用油浴的方法先油浴一定时间,然后再加入化合物a进行修饰,从而达到本发明所述的修饰效果。作为本发明所述介孔材料修饰方法的更优选实施方式,所述步骤(2)中采用的溶剂为甲苯,所述油浴的温度为至少110℃。所述油浴温度根据选择的溶剂不同会有所不同,一般地,所述油浴温度应大于所选择溶剂的沸点。
作为本发明所述介孔材料修饰方法的优选实施方式,所述步骤(3)中加入的化合物a的量为5×10-4摩尔每100毫克介孔材料。本申请人经过大量研究发现,当步骤(3)中加入的化合物的量为5×10-4摩尔每100毫克介孔材料。时,结合所述特定的修饰条件,加入的化合物a能够对介孔材料起到更好的修饰作用,能够完全将介孔材料上的硅羟基取代,而硅羟基被完全取代后的介孔材料具有对蛋白和核酸类物质更好的捕获分离能力。
作为本发明所述介孔材料修饰方法的优选实施方式,所述化合物a为辛基三甲氧基硅烷。本申请中,所述化合物a的选择不同,即采用不同长度的碳链结构对所述介孔材料进行修改时,所述不同长度的碳链结构会影响材料对蛋白和核酸的捕获能力。本申请发明人经过大量研究发现,当所述化合物a选择辛基三甲氧基硅烷时,所述八个碳的碳链长度修饰所述介孔材料时,即介孔材料上的硅羟基完全被辛烷基取代,修饰后所得介孔材料对蛋白和核酸类物质的捕获分离能力最好。
作为本发明所述介孔材料修饰方法的优选实施方式,所述步骤(1)中,所述介孔材料为介孔硅材料,所述烘干为在8~150℃下烘干6~12小时;所述步骤(4)中采用的洗脱剂为乙醇,除去洗脱剂采用如下方法:在50~100℃下真空4~12小时。本发明所述介孔材料修饰方法中,所述介孔材料为介孔硅材料,所述介孔硅材料可选择mcm-41等。所述步骤(1)中的烘干条件没有严格限定,一般只要能够达到将介孔硅材料烘干的目的即可,一般地,所述烘干是在8~150℃下烘干6~12小时即可达到目的。所述步骤(4)中洗脱的目的主要是将介孔材料中捕获的ctdna洗脱下来,所述洗脱剂优选但不限于选择乙醇,一般采用乙醇洗脱介孔材料三次,即可将介孔材料中捕获的ctdna洗脱下来。所述洗脱剂的除去方法优选但不限于在50~100℃下真空4~12小时,选择不同的洗脱剂,所采用的洗脱剂去除方法会有所不同,本领域技术人员根据所选择的洗脱剂能够合理选择适用的洗脱剂去除方法。
作为本发明所述介孔材料修饰方法的优选实施方式,所述步骤(2)中采用超声处理将介孔材料均匀分散在溶剂中。本发明所述介孔材料修饰方法中,所述步骤(2)中优选但不限于采用超声处理方式将介孔材料均匀分散在溶剂中,所述超声处理优选但不限于:将介孔材料加入到含有超纯水的试管中,将试管置于冰水中(为了防止超声产生的热量会对样品产生影响),然后将超声破碎仪的探头置于试管的底部,超声1~2分钟。
另外,本发明还提供一种对蛋白和核酸捕获效果较好、能够较好应用于ctdna的捕获分离的介孔材料,所述介孔材料采用如上所述方法修饰得到。采用本发明所述方法修饰得到的介孔材料,其中的硅羟基被完全取代,具有对蛋白和核酸类物质更好的捕获分离能力。
最后,本发明还提供了采用如上所述方法修饰得到的介孔材料在分离ctdna中的用途,采用如上所述方法修饰得到的介孔采用在分离ctdna时,具体包括以下步骤:
(a)取血液或尿液为样品,采用大孔材料将样品中的细胞、细胞碎片、大
蛋白及其他生物大分子分离除去;
(b)采用介孔材料对步骤(a)中大孔材料分离后的样品进行捕获筛选,
ctdna大小在介孔材料孔径范围内的被介孔材料捕获分离;
(c)将步骤(b)中介孔材料捕获的ctdna洗脱,然后保存。
本申请中采用本发明所述修饰方法修饰得到的介孔材料用于分离ctdna,由于本发明所述修饰方法修饰得到的介孔材料,其上的硅羟基被完全取代,使得修饰后所得材料对蛋白和核酸类物质具有很好的捕获能力,因此,本发明所述介孔材料可以很好的用于ctdna的捕获分离。
作为本发明所述采用介孔材料分离ctdna的方法的优选实施方式,所述步骤(a)中的大孔材料为大孔硅材料,所述大孔材料的孔径大于50nm。所述步骤(a)中的大孔材料一般选择大孔硅材料,例如大孔泡沫氧化硅材料(mosf)、大孔介孔泡沫氧化硅材料(mcf)等,这些材料的孔径一般大于50nm,例如所述mosf的孔径在1μm左右。
作为本发明所述采用介孔材料分离ctdna的方法的优选实施方式,所述步骤(c)中洗脱ctdna的方法为:将捕获有ctdna的介孔材料离心,去除上清液,然后加入超纯水静置,再离心,上清液即为洗脱的ctdna。
本发明所述介孔材料在分离ctdna时,可以将大孔材料和介孔材料分别包埋于移液枪的枪头中,通过移液枪对样品进行简单的吸放即可获得纯度较高的ctdna样品,操作方式简便。
本发明所得介孔材料用于捕获分离蛋白的过程与捕获分离ctdna的过程类似,只不过所用介孔材料的孔径选择和最后的检测方法(检测的方法:对蛋白用ms(质谱),对核酸用检测荧光的方式)不同。
本发明所述介孔材料的修饰方法,采用所述特定的修饰化合物和特定的修饰条件,能够将介孔材料上的硅羟基完全取代,修饰得到的介孔材料具有对蛋白和核酸类物质更好的捕获分离能力。本发明所述介孔材料,采用所述修饰方法修饰得到,其上的硅羟基被完全取代,能够很好的应用于对蛋白和核酸类物质的捕获分离。本发明所述采用介孔材料分离ctdna的方法,操作简单方便,能够有效解决ctdna已被分解和需要较长预处理时间的瓶颈,为ctdna更广泛的产业化应用奠定了基础。
附图说明
图1为本发明介孔材料的傅氏转换红外线光谱仪检测图。
图2为溶剂选择甲苯时所得介孔材料的傅氏转换红外线光谱仪检测图。
图3为溶剂选择乙腈时所得介孔材料的傅氏转换红外线光谱仪检测图。
图4为将大孔材料和介孔材料分别包埋于移液枪的枪头的示意图。
图5为采用大孔材料处理样品的过程示意图。
图6为采用介孔材料捕获ctdna的过程示意图。
图7为对捕获ctdna后的介孔材料洗脱获得ctdna的过程示意图。
图8为选择不同化合物a修饰所得介孔材料对胰岛素的捕获能力对比图。
图9为选择不同化合物a修饰所得介孔材料对ctdna的捕获能力对比图。
具体实施方式
为更好的说明本发明的目的、技术方案和优点,下面将结合附图和具体实施例对本发明作进一步说明。
实施例1
本发明一种介孔材料修饰方法的一种实施例,本实施例所述介孔材料修饰方法包括如下步骤:
(1)将介孔硅材料置于80℃烘干箱中,烘干12小时;
(2)将烘干后的介孔硅材料采用超声处理均匀分散在苯中,然后在80℃油浴9小时;其中,介孔硅材料与苯的量比为1g/40ml,所述超声处理为:将介孔硅材料加入到含有超纯水的试管中,将试管置于冰水中,然后将超声破碎仪的探头置于试管的底部,超声1~2分钟;所述油浴采用的油为二甲基硅油;
(3)然后加入化合物a,继续油浴12小时;所述化合物a的加入量为5×10-4摩尔每100毫克介孔硅材料;
(4)收集步骤(3)中修饰过的介孔材料,用乙醇洗脱3次,然后在60℃下真空6小时,除去乙醇;
其中化合物a的结构式为:
x为甲氧基,y为c18h37。
实施例2
本发明一种介孔材料修饰方法的一种实施例,本实施例所述介孔材料修饰方法包括如下步骤:
(1)将介孔硅材料置于150℃烘干箱中,烘干6小时;
(2)将烘干后的介孔硅材料采用超声处理均匀分散在二氯乙烷中,然后在84℃油浴7小时;其中,介孔硅材料与二氯乙烷的量比为1g/40ml,所述超声处理为:将介孔硅材料加入到含有超纯水的试管中,将试管置于冰水中,然后将超声破碎仪的探头置于试管的底部,超声1~2分钟;所述油浴采用的油为二甲基硅油;
(3)然后加入化合物a,继续油浴12小时;所述化合物a的加入量为5×10-4摩尔每100毫克介孔硅材料;
(4)收集步骤(3)中修饰过的介孔材料,用乙醇洗脱3次,然后在100℃下真空4小时,除去乙醇;
其中化合物a的结构式为:
x为乙氧基,y为ch2。
实施例3
本发明一种介孔材料修饰方法的一种实施例,本实施例所述介孔材料修饰方法包括如下步骤:
(1)将介孔硅材料置于100℃烘干箱中,烘干12小时;
(2)将烘干后的介孔硅材料采用超声处理均匀分散在甲苯中,然后在110℃油浴6小时;其中,介孔硅材料与甲苯的量比为1g/40ml,所述超声处理为:将介孔硅材料加入到含有超纯水的试管中,将试管置于冰水中,然后将超声破碎仪的探头置于试管的底部,超声1~2分钟;所述油浴采用的油为二甲基硅油;
(3)然后加入辛基三甲氧基硅烷,继续油浴12小时;所述辛基三甲氧基硅烷的加入量为5×10-4摩尔每100毫克介孔硅材料;
(4)收集步骤(3)中修饰过的介孔材料,用乙醇洗脱3次,然后在50℃下真空12小时,除去乙醇。
实施例4
本发明一种介孔材料修饰方法的一种实施例,本实施例所述介孔材料修饰方法包括如下步骤:
(1)将介孔硅材料置于120℃烘干箱中,烘干8小时;
(2)将烘干后的介孔硅材料采用超声处理均匀分散在四氯化碳中,然后在77℃油浴10小时;其中,介孔硅材料与四氯化碳的量比为1g/40ml,所述超声处理为:将介孔硅材料加入到含有超纯水的试管中,将试管置于冰水中,然后将超声破碎仪的探头置于试管的底部,超声1~2分钟;所述油浴采用的油为二甲基硅油;
(3)然后加入化合物a,继续油浴12小时;所述化合物a的加入量为5×10-4摩尔每100毫克介孔硅材料;
(4)收集步骤(3)中修饰过的介孔材料,用乙醇洗脱3次,然后在80℃下真空10小时,除去乙醇;
其中化合物a的结构式为:
x为乙氧基,y为苯基。
实施例5
采用傅氏转换红外线光谱仪检测采用本发明所述修饰方法得到的介孔材料的不同修饰结果
检测方法:
1.打开仪器,首先进行校正,即不加样品时,仪器扫描5次,通过与标准图比对,证明仪器没有问题。
2.将样品粉末置于探头与载物台之间,将样品压实,并将探头置于样品正中间(液体样品,滴在探头上即可,保证检测过程中,液体不干即可)
3.设置扫描分辨率为4cm-1,重复50次。
分别检测本发明所述修饰方法中采用不同的化合物a时,修饰所得介孔材料的修饰情况,结果如附图1所示。
由附图1可知,目标基团已经被修饰到介孔材料上,而且这种结合是通过共价键的方式结合,以此来说明这些修饰基团是被接到介孔材料的表面而不是被吸附到介孔材料的表面。
实施例6
采用不同溶剂对修饰的影响试验
一、采用不同溶剂对修饰基团密度的影响
本发明所述介孔材料的修饰方法中,在其他步骤、试剂选择、试剂用量均相同的情况下,除步骤(2)中介孔材料均匀分散的溶剂选择不同、以及步骤(3)中加入的化合物a的选择及含量不同,从而考察选择选择不同溶剂对修饰后介孔材料的修饰基团密度的影响。试验结果如下表:
上述表格中,碳含量是通过元素分析仪检测的,具体检测方法如下:
根据仪器操作指南进行操作,即:
将仪器预热至指定温度
样品要求均匀分布的微粒样品包裹在锡箔中,称重之后放入自动样品进样器的旋转式进样盘中。每个样品准备三个平行样品,并且用乙酰苯胺作为标准样。同时准备三个空白样品作为对照。
将运行样、标样和待测样品按软件上的样品编号放置在对应的自动进样器空位上。
样品分析结束后,如果标样的结果无误,则认定结果有效进行结果分析。若标样误差较大,则结果无效。
上述表格中,修饰基团的密度是根据碳元素的含量进行计算出来的:
其中,s表示每平方纳米修饰基团的数目,δw%表示元素分析得出的碳元素含量,na是阿伏伽德罗常数,mwc表示碳元素的相对分子质量,nc表示修饰基团上碳原子的个数,sbet是比表面积(m2/g)。
根据文献报导,高温焙烧后,硅材料表面的硅羟基的密度是1.67nm-2。而上述反应是发生在硅羟基与修饰基团之间,因此修饰后的修饰基团的密度应该接近1.67个每平方纳米。
二、采用不同溶剂对介孔材料修饰过程中基团反应的影响
本发明所述介孔材料的修饰方法中,在其他步骤、试剂选择、试剂用量均相同的情况下,除步骤(2)中介孔材料均匀分散的溶剂选择不同,从而考察选择不同溶剂对修饰后介孔材料的影响。
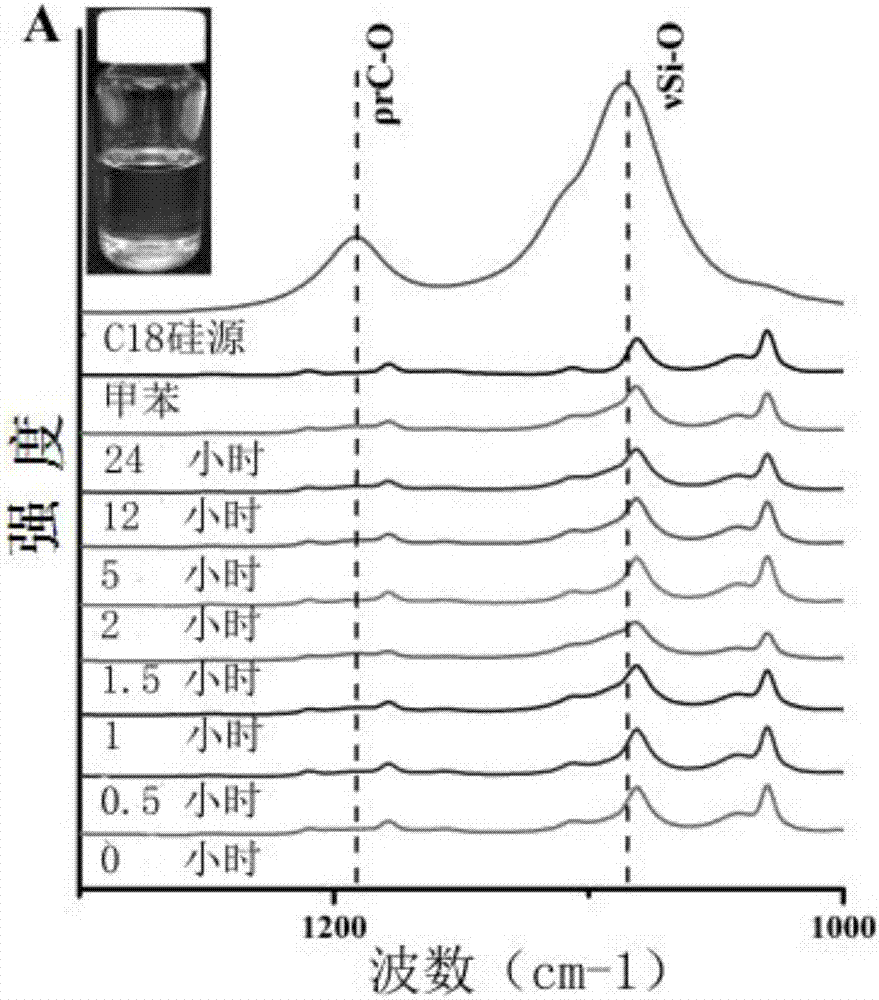
试验方法同实施例5,区别在于实施例5中是在不同时间点取的样品,而本实施例是在相同时间点取的样品。检测不同溶剂对修饰所得介孔材料的影响,结果如附图2和3所示。
附图2和3主要是说明我们对于溶剂的选择会影响修饰的过程。因为在甲苯(图2)中,加入的十八烷基三甲氧基硅烷,硅烷(十八烷基三甲氧基硅烷)之间不会发生反应(1200左右有两个峰),因此在修饰的过程中,硅烷是和硅材料表面的硅羟基基团发生反应,而不是硅烷之间发生反应,然后再跟材料发生反应,这主要是和结论中硅羟基完全被取代相照应(也就是一个硅羟基被一个c18或者c8反应,而不是一个硅羟基和三个或者四个c18或者c8发生反应)。在图3中,十八烷基三甲氧基硅烷加入到乙腈中,1200左右的峰消失了,这说明硅烷发生了反应,在溶液中没有硅烷了。并且图片左上方有颗粒形成,这么这种反应进行了,并且反应很快速。图2和图3证明了,本发明所述介孔材料的修饰方法中,所述溶剂的选择是本申请发明人付出创造性劳动的所得,而不是常规普通选择,并且所述溶剂的选择,直接影响是否能够实现介孔材料中的硅羟基被完全取代。
实施例7
本发明所述介孔材料分离ctdna的一种实施例,本实施例中所用介孔材料的孔径大小为50nm,本实施例所述分离方法包括如下步骤:
(1)将大孔材料和介孔材料分别包埋于移液抢的枪头:即制作两种枪头,一种为含大孔材料的枪头,另一种为含有介孔材料的枪头,如附图4所示;
(2)取血液或尿液为样品,采用大孔材料将样品中的细胞、细胞碎片、大蛋白及其他生物大分子分离除去,如附图5所示;该步骤的主要目的就是去除一些无关的蛋白、核算和细胞碎片等;所述大孔材料一般选择大孔硅材料,例如大孔泡沫氧化硅材料(mosf)、大孔介孔泡沫氧化硅材料(mcf)等,这些材料的孔径一般大于50nm,本实施例中所述大孔材料采用mosf,其孔径在1μm左右;
(3)采用介孔材料对步骤(2)中大孔材料分离后的样品进行捕获筛选,ctdna大小在介孔材料孔径范围内的被介孔材料捕获分离,如附图6所示;此步骤中,ctdna被介孔材料筛选,从而暂时性的保存在介孔材料的介孔中;
(4)将步骤(3)中介孔材料捕获的ctdna洗脱,然后保存,如附图7所示;所述洗脱方法为:将捕获有ctdna的介孔材料离心,去除上清液,然后加入超纯水静置,再离心,上清液即为洗脱的ctdna。
本实施例可以简单而快速的对ctdna进行分离,时间长度大约在十分钟左右。同时这种方法简单易行,不需要专业的仪器设施和受过培训的专业人员对样品进行处理。此外,这种方法快速获得ctdna,从而实现了对ctdna的实时捕获。
实施例8
选择不同化合物a进行修饰所得介孔材料对蛋白捕获能力的影响试验
本实施例主要考察化合物a的选择不同时,对修饰所得介孔材料捕获蛋白能力的影响。所述修饰方法中,除化合物a的选择不同外,其余条件等均相同。
试验方法:
1、样品用标准溶剂(50%h2o,50%乙腈)溶解或稀释;
2、将配好的样品或标准品吸入进样器(针),将进样针放置于进样泵中;
3、将进样针直接与离子源连接;
4、设置进样泵的流速为120微升/小时。
在人尿样本中,加入胰岛素,来监测本发明所述修饰方法中采用不同的化合物a时,修饰所得介孔材料对胰岛素捕获能力的区别。本实施例中,除所用介孔材料的孔径与实施例7不同外,本实施例所述介孔材料捕获分离胰岛素的方法与实施例7中捕获分离ctdna的方法相同;本实施例中所用介孔材料的孔径大小为6nm,因为胰岛素的大小为5nm。试验结果如附图8所示。
由附图8可知,c8修饰的介孔材料对于胰岛素的捕获能力最强。当然,捕获胰岛素的过程与捕获ctdna的过程类似,由此也可证明,c8修饰的介孔材料对于ctdna的捕获能力也最强。而且本申请发明人通过实施例8发现,本申请所得介孔材料对胰岛素的捕获能力与现有技术常用方法相比,提高了一千倍。
实施例9
选择不同化合物a进行修饰所得介孔材料对ctdna捕获能力的影响试验
本实施例主要考察化合物a的选择不同时,对修饰所得介孔材料捕获ctdna能力的影响。所述修饰方法中,除化合物a的选择不同外,其余条件等均相同。
本实施例中,通过pcr的方法获得长度为187bp的dna(作为ctdna的模型),分别采用四种不同修饰的材料按照实施例7中所述的方法捕获ctdna,然后pcr扩增这个片段。本实施例中选择不同化合物a进行修饰所得介孔材料捕获ctdna的结果见附图9所示。
由附图9可看出,c1、c8、c18修饰可以捕获ctdna,未经过修饰的材料对dna没有捕获效果。
最后所应当说明的是,参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
- 还没有人留言评论。精彩留言会获得点赞!