冷冻法制备生物活性物质/水溶性药物微胶囊的方法及其应用与流程
本发明涉及生物为纳米空心材料制备、药物输送、生物传感器技术领域,尤其涉及一种冷冻法制备生物活性物质/水溶性药物微胶囊的方法及其应用。
背景技术:
由于我国制剂研究长期滞后,传统制剂和低水平重复的制剂较多,缓释、控释制剂较少,因此我国应加大缓释、控释技术的开发力度,力争在几年内将使用品种中的传统制剂改造成缓释控释制剂加强靶向制剂研究,增加高效药物制剂新品种加强复方缓释、控释制剂、液体缓释、控释制剂的研究开发步伐。
微胶囊技术是指把分散的固体物质、液滴或气体完全包封在一层致密膜中形成微胶囊的方法。通常致密膜是由天然或合成高分子材料,可降解材料制成,含固体的微胶囊形状一般与固体相同,含液体或气体的微胶囊的形状一般为球形。最近几年随着高分子微胶囊技术的进步,微胶囊已经被应用于高尖端的技术领域,如医疗、医药、生物化学和电子信息等领域。
为了治疗各种疾病,人们常需服用各种药物,药物是对生理功能有影响的化学物质。但有些药物在服用时会存在一些缺点,因此可将药物微胶囊化克服这些缺点。微胶囊膜具有改变物质外观及性质,以及延长和控制膜内物质的释放,提高储存稳定性,将不可混溶成分隔离等作用。微胶囊根据其囊材的不同分为不透微胶囊和半透微胶囊,不透微胶囊的囊材相对比较厚,为芯材提供适合的内部环境,并将芯材和外部环境隔离开来,防止其同外部环境的物质发生反应,当需要释放的时候,用加压、加温或辐射等方法破坏囊材。半透微胶囊在使用的时候不需要破坏囊材,芯材或外部环境中的小分子物质能够自由的通过囊材,并快速达到平衡,因而可以达到缓释和控制释放的功能。对于半透微胶囊,微胶囊的表面结构、膜厚度、多孔性和芯材分布等物理性质是决定芯材缓释性能的主要因素。其主要特点是增加药物的稳定性避免首过效应延缓释放,减少毒副作用改变药物及物材的性状掩盖不良异味与刺激性。
自微胶囊制备技术问世以来,其制备的新方法、新技术就一直是许多工作者的主要研究方向之一。目前,主要形成了化学法、物理法和物理化学法三大类制备方法。然而,绝大多数微胶囊制备法由于反应条件的限制都需要经过较高温度(>37℃)进行处理,如喷雾干燥法、高分子界面聚合法等。过高的温度会破坏生物活性物质的活性或者药物的药效,不利于生物功能性材料的制备。生物活性材料的特点在于低温条件下不会破坏其生物活性功能,有利于生物活性功能的保存和运输,因此在低温环境下进行生物活性物质微胶囊固化符合生产力发展的要求。
技术实现要素:
本发明所要解决的技术问题是提供一种冷冻法制备生物活性物质/水溶性药物微胶囊的方法及其应用,以克服上述现有技术中的不足。
本发明解决上述技术问题的技术方案如下:一种冷冻法制备生物活性物质/水溶性药物微胶囊的方法,具体包括如下步骤:
s100、将水溶性生物活性物质/水溶性药物溶于溶解剂中,冷藏保存,得到生物活性/水溶性药物水溶液;
s200、将有机溶剂、生物相容性表面活性剂、生物活性/水溶性药物水溶液进行搅拌混合,形成稳定的微乳体系;
s300、将微乳液盛装到密闭容器中,并在剧烈搅拌作用下冷冻保存;
s400、向冷冻好的乳液中边搅拌边反应的加入无机阳离子脂类材料;
s500、反应结束后取出样品,并将样品冷冻干燥,得到生物活性/水溶性药物微胶囊。
在上述技术方案的基础上,本发明还可以做如下改进。
进一步,所述步骤s100中,制备生物活性/水溶性药物水溶液具体包括以下步骤:
s110、将水溶性生物活性物质/水溶性药物进行生物前处理,生物前处理过程包括灭菌、除杂、除氧、提纯、冷冻;
s120、在无菌条件下,将处理后的水溶性生物活性物质/水溶性药物溶于0℃至4℃的溶解剂中,配成相应的生物活性/水溶性药物水溶液;
s130、将配好的生物活性/水溶性药物水溶液放置于4℃以下的环境中冷藏保存。
进一步,所述步骤s200中,将有机溶剂、生物相容性表面活性剂、生物活性/水溶性药物水溶液进行搅拌混合时,须在0℃至4℃的环境中进行。
采用上述进一步的有益效果为:1、0℃以上保证水的流动性和溶解性,2、4℃以下是许多药物和生物材料长期贮存保持活性的温度,如疫苗、抗癌药一类的需要在4℃以下冷藏保存,高于4℃会破坏其活性。
进一步,所述有机溶剂为无毒低凝固点不溶于水的有机溶剂,包括环己烷、正己烷、液体石蜡、乙酸乙酯、二氯甲烷。
进一步,微乳体系内溶解剂的质量为有机溶剂质量的1%至60%,生物相容性表面活性剂的质量为溶解剂质量的1%至30%,生物活性物质/水溶性药物的质量为溶解剂的质量的1%至30%。
采用上述进一步的有益效果为:保证有机溶剂含量大于溶解剂含量,形成稳定的油包水体系。
进一步,所述步骤s300中,搅拌的速度为200r/min至1500r/min。
采用上述进一步的有益效果为:保证分散性以及油包水体系中,水滴粒径小于2微米,从而在冷冻法体系中形成的小冰滴粒径小于2微米。
进一步,微乳液在进行冷冻时,需按1℃/min至5℃/min的降温速率在0℃至-80℃的温度下,冷冻2h至148h。
进一步,所述生物相容性表面活性剂包括辛胺、span-80、十六烷基三甲基溴化铵、十二烷基苯磺酸钠、十二烷基硫酸钠、a-烯烃磺酸盐、烷基磺酸盐、a-磺基单羧酸及其衍生物、脂肪酸磺烷基酷、脂肪酸磺烷基酰胺、琥珀酸双酷磺酸盐、硫酸酯盐、明胶、烷基甘油醚磺酸盐、蔗糖酯和磷酸酯盐中的一种或几种的组合。
进一步,所述水溶性生物活性物质/水溶性药物包括但不限于:葡萄糖氧化酶、纳豆激酶、间充质干细胞、口蹄疫dna疫苗、甲基乙二醛、甘草酸、单甲氧基聚乙二醇一聚丙交酷乙交酷、针剂乙型肝炎疫苗、β-半乳糖苷酶基因dna疫苗、人肝癌细胞株、veroe6细胞、琉甲丙脯酸、碱性蛋白酶、牛血清白蛋白、磷酸地塞米松、分泌抗体cd137和抗体ox40的杂交瘤细胞、甲氧萘丙酸、氢化棕榈油、乳杆酸、蒜氨酸、1-吡啶-4-(3-胺基)嘧啶哌嗪、4-(3-氯-4-甲氧基苯胺基)-6-碘喹唑啉、卡托普利、细胞、生物酶、卡介苗、灭活sars疫苗、罗非鱼链球菌疫苗、致病性大肠杆菌疫苗、虾青素等水溶性酶、细菌、药物、病毒等生物活性、药物物质。
进一步,生物活性/水溶性药物微胶囊粒径大小为10nm至1000nm,微胶囊壁厚为1nm至100nm。
本发明的有益效果是:
1)利用水滴低温发生相态转变凝结成冰的特点,结合了软硬模板剂的优点,具有纳米空心材料形貌、大小、反应可控,模板剂容易去除;
2)采用水相作为模板剂,有利于保护分散活性组分;
3)反应条件温和,有利于工艺放大;
4)反应无需加热,保护生物材料的活性,反映在冰水滴表面进行,保护内部的生物材料;
5)整个工艺具有操作简单,绿色环保,药物包裹性好,生物活性组分稳定,成本较低。
所制得的生物活性物质/水溶性药物微胶囊作为生物传感器或缓释药物输送系统上的应用。
附图说明
图1空心二氧化钛包裹虾青素的tem图。
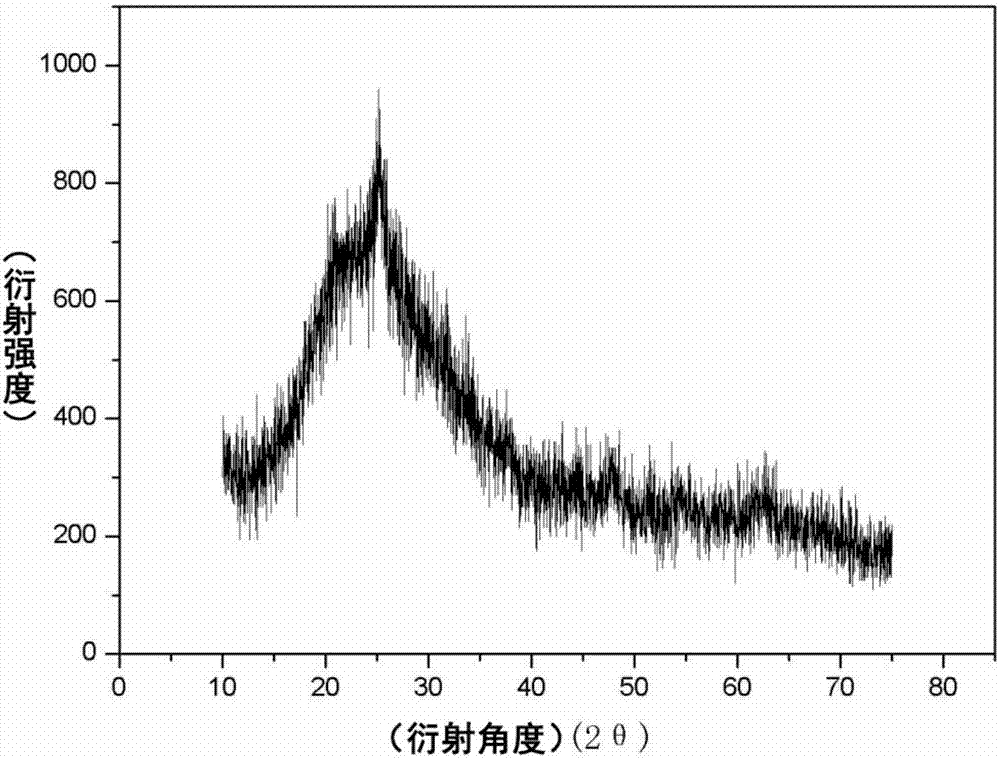
图2空心二氧化钛包裹牛血清白蛋白的xrd图。
图3空心二氧化硅包裹乙肝疫苗的tem图。
图4空心二氧化硅包裹卡托普利xrd图谱。
图5空心二氧化钛包裹葡萄糖氧化酶的ir图。
具体实施方式
以下结合附图对本发明的原理和特征进行描述,所举实例只用于解释本发明,并非用于限定本发明的范围。
本发明是利用模板剂在合成过程中发生相态变化的特点,结合了软模板法、硬模板法的优点,设计出了冷冻法制备生物活性物质/水溶性药物微胶囊的方法。该方法可以用于生物酶固化、细胞固化、病毒固化、药物输送等领域,用于制备生物活性酶微胶囊、dna疫苗微胶囊、病毒微胶囊、细胞微胶囊、水溶性药物微胶囊等生物活性物质微胶囊,可以用于制造酶传感器、水溶性药物给药系统、癌细胞传感器、病毒传感器、疫苗传感器等生物系统的制造。
实施例一:
冷冻法制备充质干细胞生物微胶囊的方法,具体包括如下步骤:
s100、制备细胞悬液:配置细胞培养皿内细胞密度为6×106个/ml,在每皿加入细胞消化液10ml,消化5min至10min,加入dmem培养基20ml终止消化,收集于离心管中,用细胞存活率及计数分析仪计数后,在2000rpm/min的速度下离心3min,去上层液体得到纯化细胞,再加入无菌生理盐水稀释至所需浓度,制得细胞悬液,将0.1ml充质干细胞悬液在4℃条件下溶于5ml蒸馏水中;
s200、将2ml辛胺、50ml正己烷溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱内,以3℃/min降温至-40℃,在温度-40℃下,冷冻搅拌12小时,搅拌速度为800r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯,继续冷冻搅拌反应48h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得二氧化硅包裹充质干细胞生物微胶囊。
实施例二:
冷冻法制备抗癌药1-吡啶-4-(3-胺基)嘧啶哌嗪微胶囊的方法,具体包括如下步骤:
s100、将0.1g水溶性抗癌药1-吡啶-4-(3-胺基)嘧啶哌嗪(ma2bc)在4℃条件下溶于5ml的蒸馏水中;
s200、将2mlspan80、50ml乙酸乙酯溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以4℃/min降温至-40℃,并在温度-40℃下,冷冻搅拌12小时,搅拌速度为1200r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量钛酸四丁脂酯,继续冷冻搅拌反应105h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得二氧化钛包裹1-吡啶-4-(3-胺基)嘧啶哌嗪微胶囊。
如图4所示,实施例三:
冷冻法制备卡托普利药物微胶囊的方法,具体包括如下步骤:
s100、将卡托普利原料药在4℃条件下溶于去离子水,配成一定浓度的原料液;
s200、将2mlspan80、50ml液体石蜡溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以2℃/min降温至-20℃,在温度-20℃下,冷冻搅拌12小时,搅拌速度为1150r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量铝酸酯,继续冷冻搅拌反应120h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化铝包裹的卡托普利药物微胶囊。
图4为空心二氧化硅包裹卡托普利xrd图谱,该图所表达的含义为:峰型为无定形二氧化硅包裹卡托普利的特征峰。
实施例四:
冷冻法制备靶向抗癌药4-(3-氯-4-甲氧基苯胺基)-6-碘喹唑啉微胶囊的方法,具体包括如下步骤:
s100、将0.1g4-(3-氯-4-甲氧基苯胺基)-6-碘喹唑啉原料药在4℃条件下溶于去离子水,配成一定浓度的原料液;
s200、将2mlspan80、50ml液体石蜡溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以1℃/min降温至-20℃,并在温度-20℃下,冷冻搅拌12小时,搅拌速度为950r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯,继续冷冻搅拌反应86h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅包裹的4-(3-氯-4-甲氧基苯胺基)-6-碘喹唑啉药物微胶囊。
如图3所示,实施例五:
冷冻法制备乙肝疫苗微胶囊的方法,具体包括如下步骤:
s100、将0.1g针剂乙型肝炎疫苗(简称乙肝疫苗)在4℃条件下溶于去离子水,进行无菌处理后配成一定浓度的原料液;
s200、将2mlspan80、50ml正戊烷溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将微乳液装在密闭容器中放入冷浴锅或者冰箱,以2℃/min降温至-20℃,在温度-20℃下,冷冻搅拌12小时,搅拌速度为1000r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯加入到冷冻好的乳液中,继续冷冻搅拌反应64h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅包裹的乙肝疫苗药物微胶囊。
图3为空心二氧化硅包裹乙肝疫苗的tem图,该图所表达的含义为:二氧化硅空心球粒径为30-100nm,乙肝疫苗被包裹在二氧化硅空心球内部,壁厚为3-5nm。
实施例六:
冷冻法制备灭活sars疫苗药物微胶囊的方法,具体包括如下步骤:
s100、无菌操作下取0.1ml纯化的灭活sars-cov溶液在4℃条件下溶于去离子水,配成一定浓度的原料液;
s200、将2mlspan80、50ml正戊烷溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以3℃/min降温至-40℃,在温度-40℃下,冷冻搅拌12小时,搅拌速度为1050r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯,加入到冷冻好的乳液中,继续冷冻搅拌反应52h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅包裹的灭活sars疫苗药物微胶囊。
如图1所示,实施例七:
冷冻法制备虾青素微胶囊的方法,具体包括如下步骤:
s100、无菌避光操作下取0.1g虾青素在4℃条件下溶于去离子水,配成一定浓度的原料液;
s200、将2ml乳化剂(蔗糖酯)、50ml乙酸乙酯溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以2℃/min降温至-40℃,并在温度-40℃下,冷冻搅拌12小时,搅拌速度为850r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯,,继续冷冻搅拌反应48h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅包裹的虾青素微胶囊。
图1为空心二氧化钛包裹虾青素的tem图,该图所表达的含义为:二氧化钛空心球粒径为300-600纳米,青虾素被包裹在二氧化钛空心球内部,壁厚为100-200nm。
实施例八:
冷冻法制备卡介苗生物微胶囊的方法,具体包括如下步骤:
s100、在4℃无菌条件下将卡介苗冷冻干粉剂0.1g溶于5%碳酸氢钠溶液内,配成一定浓度的原料液;
s200、将2ml乳化剂(蔗糖酯)、50ml乙酸乙酯溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以5℃/min降温至-40℃在温度-40℃下,冷冻搅拌12小时,搅拌速度为350r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯,继续冷冻搅拌反应72h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅包裹的虾青素微胶囊。
如图5所示,实施例九:
冷冻法制备葡萄糖氧化酶微胶囊的方法,具体包括如下步骤:
s100、无菌操作下将葡萄糖氧化酶0.1g溶于去离子水中,配成一定浓度的原料液;
s200、将2ml辛胺、50ml正戊烷溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以5℃/min降温至-40℃,在温度-40℃下,冷冻搅拌12小时,搅拌速度为1200r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯,继续冷冻搅拌反应106h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅固化的葡萄糖氧化酶微胶囊。
图5为空心二氧化钛包裹葡萄糖氧化酶的ir图,该图所表达的含义为:ir图谱为葡萄糖氧化酶的特征峰和二氧化钛的特征峰。
实施例十:
冷冻法制备纳豆激酶微胶囊的方法,具体包括如下步骤:
s100、无菌操作下将经过深层液体发酵第二天产生的发酵液以5000rpm、15min离心分离,得到上清液,再将得到的上清液进行抽滤,可得到滤液溶于去离子水中,配成一定浓度的纳豆激酶发酵原料液;
s200、将2g明胶、50ml二氯甲烷溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以5℃/min降温至-40℃在温度-40℃下,冷冻搅拌12小时,搅拌速度为450r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯,继续冷冻搅拌反应110h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅固化的纳豆激酶微胶囊。
如图2所示,实施例十一:
冷冻法制备牛血清蛋白微胶囊的方法,具体包括如下步骤:
s100、无菌操作下将牛血清蛋白溶液溶于去离子水中,配成一定浓度的牛血清蛋白原料液;
s200、将2g明胶、50ml液体石蜡溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以5℃/min降温至-20℃在温度-40℃下,冷冻搅拌12小时,搅拌速度为450r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯加入到冷冻好的乳液中,继续冷冻搅拌反应144h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅固化的牛血清蛋白微胶囊。
图2为空心二氧化钛包裹牛血清白蛋白的xrd图,该图所表达的含义为:峰型为无定形二氧化钛包裹牛血清白蛋白的特征峰。
实施例十二:
冷冻法制备β-半乳糖苷酶基因dna疫苗微胶囊的方法,具体包括如下步骤:
s100、无菌操作下将β-半乳糖苷酶基因dna疫苗溶液溶于去离子水中,配成一定浓度的β-半乳糖苷酶基因dna疫苗原料液;
s200、将2g明胶、50ml正己烷溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以5℃/min降温至-40℃在温度-40℃下,冷冻搅拌12小时,搅拌速度为550r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯,继续冷冻搅拌反应72h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅固化的β-半乳糖苷酶基因dna疫苗微胶囊。
实施例十三:
冷冻法制备罗非鱼链球菌微胶囊的方法,具体包括如下步骤:
s100、罗非鱼无乳链球菌sip原核表达工程菌sip-pet32a(+)菌株接种于lb液体培养基中,37℃振荡培养至od600为0.5至0.6,加入诱导剂itpg,25℃诱导表达6h,4000r/min,离心15min,收集菌体,超声波破碎菌液,收集sip蛋白并纯化备用,并将sip蛋白溶于去离子水中,配成一定浓度的sip蛋白原料液;
s200、将2gspan80、50ml正己烷溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以5℃/min降温至-30℃在温度-30℃下,冷冻搅拌12小时,搅拌速度为700r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯,继续冷冻搅拌反应72h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅固化的罗非鱼链球菌微胶囊。
实施例十四:
冷冻法制备致病性大肠杆菌微胶囊疫苗的方法,具体包括如下步骤:
s100、将大肠杆菌全菌体疫苗溶于去离子水配成合适的浓度;
s200、将2g明胶、50ml正己烷溶入到步骤s100中的溶液内,搅拌均匀,形成w/o微乳液;
s300、将w/o微乳液装在密闭容器中放入冷浴锅或者冰箱,以5℃/min降温至-40℃在温度-40℃下,冷冻搅拌12小时,搅拌速度为800r/min;
s400、向步骤s300中冷冻好的乳液内加入一定量正硅酸乙酯,继续冷冻搅拌反应72h;
s500、反应结束后取出样品,乙醇洗涤离心,然后将样品冷冻干燥,得氧化硅固化的致病性大肠杆菌微胶囊疫苗。
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
- 还没有人留言评论。精彩留言会获得点赞!