测试装置和测试装置的使用方法与流程
本发明涉及测试装置和使用测试装置的方法。在具体实施例中,该测试装置是作为与体液监控器一起使用从而确定个体的液体样本中的分析物的浓度的电化学测试条。
背景技术:
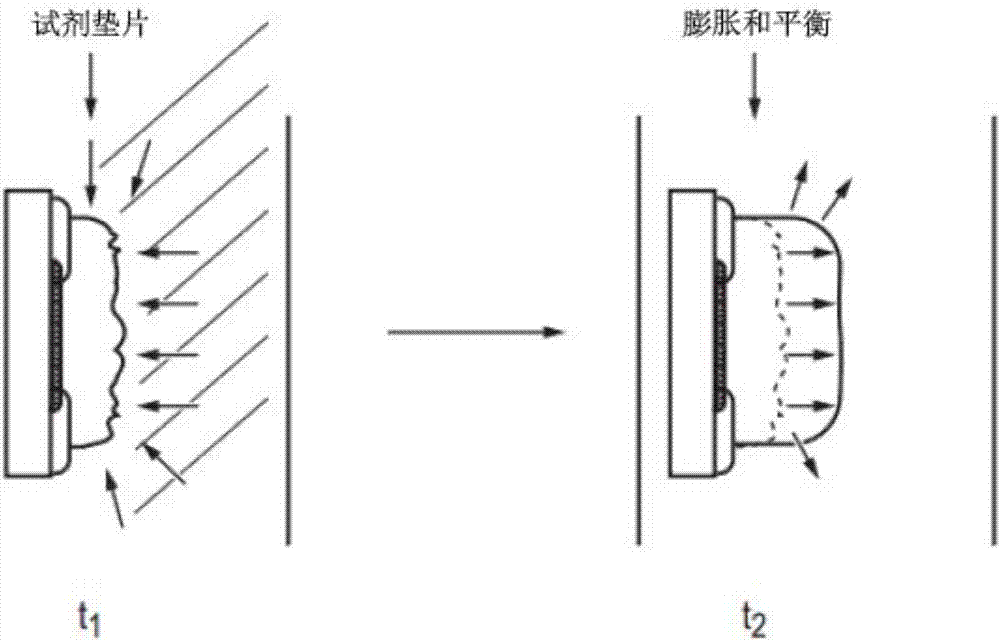
:在诊断装置领域,如用在医疗器械行业中,尤其用于分析血液或其他体液样本的诊断装置,在用户监控存在于例如他们的血液中的某些化学品、物质或分析物的水平等生物特征。例如,特别是糖尿病患者,必须定期监控在他们的血液中的血糖浓度,以便预料高血糖症或低血糖症的病发,并且根据需要采取预防措施。这样的诊断装置的存在极大地减少了对医疗系统的压力,因为患者能够在他们自己的家里注射胰岛素,而不必在医务人员在场的情况下才这么做。一般来说,患者将使用穿刺装置来执行手指针刺,从手指或替代部位提取小的血滴。接着,通常是条的电化学测试装置插入诊断仪中,并且将样本应用到测试条上。通过毛细管作用,样本流经装置的测量室,并且与涂有传感化学物的一个或多个电极或类似的导电元件接触,该传感化学物用于与血液样本中的特定分析物或其他特定化学物(例如,葡萄糖)反应。反应强度取决于在血液样本中的分析物的浓度。诊断仪可能检测由试剂与分析物的反应产生的电流,接着向用户显示结果。一般而言,这样的电化学测试装置具有工作电极和对/参考电极,并且可能具有一个以上的工作电极。ep2056107公开了一种具有测量相同的分析物的两个工作电极的测试条。这使得分析物能够被测量两次,从而对两次测量值进行比较,以致每个测量值均可用作另一测量值的检查。这使得在两个测量值存在明显差异的情况下,能够检测到条的填充不足或制造缺陷。us2007/0131549公开了这一种具有两个工作电极的测试条,其中一个工作电极使用葡萄糖氧化酶测量葡萄糖,另一个工作电极使用葡萄糖脱氢酶测量葡萄糖。这两个电极在整个线性范围内对葡萄糖做出响应。如果样本具有较低的氧分压,基于葡萄糖氧化酶的电极将给出较高的响应,而基于葡萄糖脱氢酶的电极将给出准确的结果。在这些情况下,来自基于葡萄糖脱氢酶的电极的读数是优选的。如果样本包含将给出错误的高葡萄糖读数的麦芽糖或乳糖,那么基于葡萄糖脱氢酶的电极将给出更高的响应,而基于葡萄糖氧化酶的电极将给出准确的结果。在这些情况下,来自基于葡萄糖氧化酶的电极的读数是优选的。在这个背景下,仍然存在改进电化学测试条等测试装置,并且改进使用测量装置的方法的需要,使得从中可以得到更加准确的测量值。特别地,当测量装置同流体样本起反应时,需要更准确地测量由测量装置产生的电流,从而更准确地确定在样本中的分析物的量。技术实现要素:在第一方面,本发明提供一种用于测量流体样本中分析物的量的测试装置,其包括基片。在所述基片上具有第一分析物试剂,所述第一分析物试剂配制为与分析物反应以产生指示分析物在样本中的存在或量的信号。所述第一分析物试剂具有第一基于时间的响应特性。在所述基底上还具有第二分析物试剂,所述第二分析物试剂配制为与分析物反应以产生指示分析物在样本中的存在或量的信号。所述第二分析物试剂具有第二基于时间的响应特性。例如,当所述第一和第二分析物试剂与所述样本接触时,它们可能有不同的溶剂化,从而产生具有不同电流-时间特性的分析物依赖信号。相对快溶剂化的试剂关于消除制造变化的影响更精确,但是对系统样本误差更敏感。在待测试的样本为血液的情况下,系统样本误差可能是红细胞比容。在另一方面,相对慢溶剂化的试剂关于制造变化的影响较不精确,但是对系统样本误差较不敏感。例如,快溶剂化的试剂将在约10%的总测试时间(例如,测量在电极处的电流的一段时间)内平衡,然而,慢溶剂化的试剂将在约大于20%的总测试时间内不会完全平衡。总的测试时间可能通常达到5-15s,但是也可能使用其他测试时间。随着试剂垫片在不同物理阶段的过程中的进展,同时产生化学反应的潜在信号的进行,可以通过获取在测量过程中的一个或多个时间点的信号读数——例如电流读数,并且优选地通过获取测量中的多个时间点的读数,建立每个电极基于时间的响应特性。为了本发明的目的,可能简单地获取一个或多个基于时间的读数以构成基于时间的响应特性。可选择地,可能获取内插的一系列的多个基于时间的读数以构成基于时间的响应特性。还可选择地,可能获取回归至任意合适平衡的来自多个基于时间的读数的合适的参数拟合。可选择地,可能通过对多个基于时间的读数的回归获得非参数拟合,并且采用该非参数拟合来构造基于时间的响应特性。此外,可能采用上述列举的替代选择的任意数学变换(例如,加、乘、差、积分、微分、对数或指数)来构造基于时间的响应特性。因为在两电极处生成化学和电化学反应的潜在信号以及过程能够被很好地理解,并且可能在表面上是相似的,而传感器垫片进行的不同物理阶段受到与样本的复杂的相互作用,因此已经被发现,采用合适的配方,观察到的两个分析物试剂的基于时间的响应信号特性之间的相对差值可以用于说明和校正系统误差,同时通过合适的算法将精确度最大化。在一个实施例中,各分析物试剂合成物被设计为具有不同的扩散、溶剂化和/或溶解行为特性,以便它们可以产生带有不同基于时间的响应特性的信号。通常,试剂垫片首先将经历“溶剂化”阶段,在这个阶段,主导过程将涉及来自样本溶液的溶剂(例如,水或血浆)渗透到试剂垫片中,潜在的化学反应主要被限制在该主导过程中。随后,试剂垫片可能膨胀,并且可能到达溶解阶段,其中,主导过程变为来自试剂垫片的溶质材料扩散到主体样本层中(这里溶解定义为垫片溶质组分渗透进入主体样本中)。同时在垫片和主体区域中将发生反应,同时溶解正在不断进行。最后,可能到达平衡阶段,其中,已经很大程度上产生完全溶解,垫片和主体区域已经变得稳定,并且可能基本一致。潜在的化学反应将继续,但是将很大程度上不受试剂垫片和主体样本层之间的组分的物理交换的影响,这将已经达到稳定的平衡,响应信号随后被潜在的活性反应组分的扩散限制反应动力学单独控制。为清楚起见,上面将这三个阶段描述为独立的连续步骤,然而,在现实中,它们可能在一定程度上重叠,在它们之间出现具有各自要素和特性的过渡阶段。此外,试剂垫片的不同子组分可能以不同的速率通过这些阶段而进展,使得试剂垫片的行为总体上变成它的单独的子组分的行为的综合结构。因此,本领域技术人员可以意识到改变试剂垫片中的子组分的配方是设计和控制任意给定试剂垫片的通过这些阶段的基于时间的进度的合适手段。此外,对于在给定的测试的特定维持时间内的给定个体试剂垫片配方和合成物,其中一个阶段可能在整个测试过程中在一定程度上占主导地位,使得其他阶段看起来不存在。可选择地,对于在给定的测试的特定维持时间内的任意个体试剂垫片配方和合成物,其中一个阶段可能在一定程度上被最小化,使得该阶段看起来不存在。在快溶剂化系统的情况下,上述平衡阶段可能在尽可能少的10~25%的总测试时间,例如0.5~2.5秒,开始占主导地位,并且溶剂化阶段可能看起来实际上不存在。在此情况下,基于时间的响应特性的最有用部分将是超过约2-3秒的部分,优选地,超过约3-5秒,最优选地,超过约5秒,由于响应信号将受到在这个区域中的潜在的活性反应组分的扩散限制反应动力学的控制,并且在传感器制造过程中产生的不一致将被最大程度地平衡。在采用的算法中,在2-3秒之前,优选地,在3-4秒之前,最优选地在5秒之前,可能仍然包含一些有用的信息,因为即使在这样的配方中的这些时间点存在有限的和噪声的样本校正信息,但是当与来自更慢溶剂化系统的更强校正信号在算法上组合时,可能仍然导致有益校正和交叉验证。然而,当导出最终测量值时,相对于来自超过越2-3秒,优选地超过约3-5秒,最优选地超过约5秒的基于时间的响应特性,来自这个区域的基于时间的相应特性通常将占更低的权重。在较慢溶剂化系统的情况下,上述溶剂化和溶解阶段可能在至少约20%的总测试时间,例如大于1.5-3秒或在其附近,占主导地位,直到至少约40%的总测试时间,例如,3-5秒或在其附近,更优选地在5秒之后,甚至超过总测试时间的持续时间,达到完全平衡阶段。在此情况下,基于时间的响应特性的第一个最有用部分将是超过约0.5-1秒的部分,优选地在1秒和5秒之间,这将使得能够使用精度和样本误差(例如)红细胞比容相关信息之间的最佳权衡获得测量结果,因为,响应信号将受垫片组分和样本组分之间变化的相互作用的影响,并且由(在溶剂化过程中)最小暴露于干扰样品组分而导致的基于时间的响应变化,和由(在溶解过程中)逐步增加地暴露于干扰样品组分而导致的最大差异变化将在基于时间的响应特性的这部分中最为丰富。来自慢溶剂化系统中的基于时间的响应特性的第二个最有用部分将是最靠近测试的结束的部分,优选地超过约5秒,更优选地约7秒到10秒。在这一点,溶解将最靠近在对电极组合物的测试中可以达到的平衡点,并且它将处于该制剂的最精确位置处,但是它对从暴露至相同的分析物的相邻快溶剂化电极系统观察到的行为的相对相似性也将被最大化。因而,可以创建以下算法,其中,通过组合将测量信号最大化,同时通过使用对由在相同测试条中的多个电极上的相同样本同时产生的合适的基于时间的响应特性的加权组合的差异比较将误差信号最小化,其已经精心设计和/或配制为产生来自相同样本的不同的基于时间的响应特性。可以影响基于时间的响应的其他响应特性包括试剂垫片高度、试剂垫片微观结构、样本进入测试室的传送时间、垫片孔隙率、流在测试过程中的流体的体力学特性、潜溶作用、ph作用和缓冲程度、试剂垫片的表面能、试剂垫片的除气、试剂垫片的相对面积、试剂垫片的厚度变化、在酶垫片中的酶抑制剂、试剂垫片中的电化学添加剂、以及试剂垫片中的电化学催化剂和/或抑制剂。可能影响响应的电流-时间特性的任何其他基于时间的响应特性也被考虑在本公开的范围内。测试装置可能是电化学测试测量装置,其包括两个工作电极,其中一个工作电极包括第一分析物试剂,另一个工作电极包括第二分析物试剂。各试剂可能在电极上以层的形式形成,这些试剂设计和配制为具有明显不同的扩散、溶剂化和/或溶解响应特性。测试装置可能包括两个工作电极的电化学测试测量装置。这两个电极中的第一电极可能包括第一分析物试剂。这两个电极中的第二电极可能同时包括第一分析物试剂和第二分析物试剂。各试剂可能在电极上以层的形式形成。例如,第一分析物试剂可能被用作同时应用于第一和第二电极的层。第二分析物试剂可能被用作应用于第二电极的第二层。此外,测试装置可能包括反电极。第一工作电极可能包括第一分析物试剂,其具有相对快的溶解、溶剂化和/或与样本的扩散交换和平衡。这样的试剂将快速产生基本上独立于在测试条的制造过程中出现的缺陷和偏差,并因而显示出降低的不同测试条之间的结果的不一致性的读数。电极对将电化学测试测量装置中和之间的精度误差最小化起作用。然而,这种电极的响应难免很容易受到来自保护分析物的样本的溶剂化、溶解和溶解性能中的系统差异和变化造成的误差。在样本为血液的情况下,将产生这样的误差的系统样本差异的非限制性实施例包括在红细胞体积(红细胞比容)中的个体测试对象中和之间的变化。第二工作电极可能包括第二分析物试剂,其相比于第一分析物试剂具有与样本更进步的平衡。因此,这种试剂对制造变化和其中的不准确伴随物更加敏感。然而,它在试剂内维持更大程度的扩散限制,而主体样本组分渗透进入试剂以及试剂组分扩散进入主体更平缓。因此,这个电极至少在开始的时候对主体样本的扩散特性导致的系统差异(例如,在样本为血液的情况下的红细胞压积造成的差异)很不敏感。第一和第二分析物试剂可能包括酶和介质。当分析物是葡萄糖时,分析物可能是葡萄糖氧化酶或葡萄糖脱氢酶,介质可能是亚铁氰化钾(iii)。用于葡萄糖和其他分析物的检测的其他合适的酶和介质对于本领域技术人员是已知的。例如,介质可能选自:四氮六甲圜ru(iii)氯盐及其衍生物、二茂铁介质(包括水溶性高分子二茂铁介质和水溶性二茂铁盐)、吩噻嗪介质、和醌介质,如四硫富瓦烯、二亚胺、硫堇金属氧酸盐、多金属酞菁、吡咯并喹啉醌、芴酮、和醌型氧化还原染料,如吲达胺、吩嗪和吩噁嗪。在一些实施例中,第一和/或第二试剂可能包括酶和介质中的其中一种。例如,在一些实施例中,第一试剂可能同时包括酶和介质,第二试剂可能包括介质但是不包括酶。除了这些组分以外,试剂可能包括成膜组分和非成膜组分。通过调节这些组分的相对比例,各分析物试剂可以被调节以在选定的时间内提供表明分析物的存在或量的信号。非成膜组分相对于成膜组分的高比例可以提供快速溶解以便在相对较短的一段时间后产生信号的试剂。相反地,成膜组分相对于非成膜组分的高比例可以提供更慢溶剂以便在相对较长的一段时间后产生信号的试剂。产生在不同的时间段内溶解的溶剂在技术人员的能力范围内。在其他条件相同的情况下,相比于低密度(或比重)的等效组分,高密度(或比重)的成膜组分将需要以更高水平出现,以实现在溶解性能上的相同效果。类似地,在其他条件相同的情况下,相比于低密度(或比重)的等效非成膜组分,高密度或比重的非成膜组分需要以更高水平出现以实现在溶解性能上的相同效果。此外,在其他条件相同的情况下,相比于具有更快溶解的自然倾向的成膜组分,具有缓慢溶解的自然倾向的成膜组分以较低水平并入,以实现在溶解性能上的相同效果。反之,在其他条件相同的情况下,相比于具有更快溶解的自然倾向的非成膜组分,具有缓慢溶解的自然倾向的非成膜组分以较高水平并入,以实现在溶解性能上的相同效果。然而,在成膜剂和非成膜剂都快速溶解,并且成膜组分的比重为约1和非成膜组分的比重为约1.8的情况下,在干燥状态下,快速溶解试剂配方通常包括成膜组分与非成膜组分的比率小于1:1.1,更优选地小于1:2,并且最优选地约1:3或更小。在干燥状态下,缓慢溶剂试剂配方通常包括成膜组分与非成膜组分的比率为1:1或更大,更优选地约3:2或更大。成膜组分包括当从溶液中浇铸到表面上然后被干燥时,具有形成层的倾向的任意材料,该层效地将固体/空气界面处的表面积最小化以便相应地将此处的自由表面能最小化,产生平整和均匀薄膜层的趋势。一个这样的材料的例子是羟乙基纤维素(hec),但是很明显的是存在可以作为合适替代品工作的其他亲水成膜聚合物,如聚乙烯醇(pva)、聚乙烯氧(peo)、支链淀粉、羧甲基纤维素(cmc)、丙烯酸、水溶性聚酯和多元醇、右旋糖酐、黄原胶等类似材料。优选地,成膜组分具有以下性质:水溶性、在所需浓度的黏性(关于覆层性能)、与分析物试剂的其他组分的兼容性。可以利用聚合物的更高分子量/粘度梯度在较低水平维持类似湿试剂行为,同时降低存在的成膜组分相对于其他组分的总量。相反地,可以利用处于较高水平的较低粘度/分子量类似物来维持分析物试剂的覆层浓度,同时增加成膜组分与其他组分的比率。因此,调整成膜组分相对于其他组分的水平同时维持类似可印染性行为的策略对于本领域技术人员是显而易见的,通过该策略,分析物试剂的溶剂化性能可能被控制在所需限制内。类似的,可能使用具有更大或更小可溶性的不同聚合物来影响分析物试剂的溶剂化性能。非成膜组分包括破坏膜形成的结晶材料。结晶形成的过程,例如,从热力学角度来看可以在产生的固体空气界面超过表面能最小化而占主导地位,这样晶体生成的区域在膜表面中延伸,并且伸出膜表面,增大固体/空气界面的表面积以远远超过其最小值,并且这样的结晶区域和相邻区域(包含其他组分)之间的组分差异性可以通过类似组分的热力学推动协会自发地提出。快速溶剂化结晶材料的例子包括无机盐,如磷酸钾、氯化钠、氯化钾、硝酸盐、铵盐、有机材料(如蔗糖)、柠檬酸盐、乙磺酸盐(如pipes、hepes,mes)等其他快速溶剂化结晶材料。电化学介质还可充当非成膜组分。还可能采用干扰试剂层的相对成膜-非成膜倾向的另一种方法,例如,结合彼此存在有限的兼容性的聚合物组合,或者在干燥和膜形成过程中干扰试剂层子组分的兼容性的非挥发性溶剂(例如,辛醇)。第一和第二分析物试剂可能包括表面活性剂。通常它们应用于使分析物试剂到基片的应用变得容易。表面活性剂及其使用的水平的选择还可以影响膜的可湿性和样本组分到其上的渗透性。使用不同的表面活性剂和/或表面活性剂组合来加快或减缓样本渗透进试剂中将被认为是可行的策略,分析物试剂溶剂化性能还可能受其影响。本领域技术人员可以选择合适的表面活性剂。表面活性剂的例子包括:tergitolnp-9、tritontmx100;borchigoltmla200、1375、la6;brijtm35、pluronictmp103;tergitoltmnp-7。本发明的基片可能包括基底材料层,其可能是,例如,聚合物(pet)或板或涂覆纸。基底材料层可能具有,通过例如丝网印刷导电炭-石墨层,或者使用au、pd、pt或本领域技术人员已知的其他合适电极导体的金属层沉积方法,沉积在其上的图案化的导电电极层。如上所述,分析物可能是葡萄糖。可选择地,它可能选自:胆固醇、酮、乳酸、游离脂肪酸、酒精(乙醇)和甘油。样本可能是血液。采用血液的特定问题是可以有的红细胞比容对其中的分析物的水平的测量的影响。红细胞压积可以在影响分析物的性能的样本到与分析物试剂的接触之间变化。第一和第二分析物试剂的存在旨在减轻红细胞比容对分析物的检测和测量的影响。可选择地,样本可能是尿、组织液、血浆、血清、唾液或脊髓液。在第二方面,本本发明提供了一种用于测量流体样本中分析物的量的测试装置的制造方法。该方法包括将第一分析物试剂和第二分析物试剂应用至基片。第一分析物试剂具有第一基于时间的响应特性,并且配制为与分析物反应以产生指示分析物在样本中的存在或量的信号。第二分析物试剂具有第二基于时间的响应特性,并且配制为与分析物反应以产生指示分析物在样本中的存在或量的信号。在第三方面,本发明提供了一种使用测量装置的方法,该测量装置包括两个工作电极,其中一个工作电极包括第一分析物试剂,另一个工作电极包括第二分析物试剂。该方法包括将第一和第二工作电极相对于反/参考电极极化。例如,在第一(工作)电极和反/参考电极之间,并且在第二(工作)电极和反/参考电极之间,施加电势差。该方法还包括向测试装置提供流体样本;测量在第一工作电极处的一个或多个第一电流;测量在第二工作电极处的一个或多个第二电流;以及使用一个或多个第一和第二电流来确定校正的电流测量值。该方法可能还包括根据校正的电流测量值,确定在流体样本中的分析物的量。通过将在第一工作电极处产生的一组电流和在第二工作电极处产生的一组电流一起使用,可以确定更具代表性的总体电流测量值,并且其可能被用于更精确地确定分析物在样本中的量。在第一时间段期间可能测量一个或多个第一电流。在第二时间段和第三时间段期间可能测量一个或多个第二电流。在一些实施例中,第一时间段可能与第二和/或第三时间段重叠。可能在包括完整的第一、第二和第三时间段的测试时间段期间测量一个或多个第一和第二电流。当第一分析物试剂和分析物之间的反应处于基本稳定状态时,可能开始第一时间段。当第一分析物基本完全解离或溶解在液体样本中时,可能开始第一时间段。第一时间段可能被选择为足够长,使得第一分析物试剂的精确度已经被最大化,并且间隔时间可能使平均值不易受随机噪声的影响。理想地,在分析物试剂已经完全解离之后的任意时间均是合适的。分析物试剂溶解、解离和平衡得越快,第一时间可能开始的时间越早。在第一时间段结束的时候,分析物的溶剂应当基本上完成。当第二分析物试剂与分析物之间的反应处于基本非稳定状态时,可能开始第二时间段。当第二分析物试剂开始解离或溶解在流体样本中时,可能开始第二时间段。第二时间段可能选择为将可获得的红细胞比容信息最大化,从而将原始的红细胞比容影响最小化,同时尽量避免不精确度高得足以混淆获得的有用信息的区域。非常早的时间点往往是充满噪声的,并且通常受其他系统参数(例如,填充速度)的影响。因此,相比相对快的溶解化学反应(如在第一分析物试剂中),通过使用较慢的溶解化学反应,可以用相当的精度获得来自溶解过程的“早期”阶段的信息。因此,当第二分析物试剂已经足够溶剂化以给出分析物-敏感响应但是由于溶剂化仍然处于相对较早的阶段因此基体干扰被最小化时,可能开始第二时间段。如果第二时间段开始得太早,那么校正效果可能迷失在噪声中,因为测量的反应还没有建立足够的动力。在另一方面,如果第二时间段开始得太晚,那么系统可能已经过于平衡,校正信息可能与第三时间段期间获取的电流测量值相混淆,可能丢失红细胞比容校正信息。如果第二分析物试剂具有足够慢的溶解速率,那么即使第一时间段的开始表现出更大程度的溶解,也可能在第一时间段已经开始之后开始第二时间段,因为第一时间段涉及到相对快地溶解分析物试剂,在第一时间段中通常更快地发生溶解。当流体样本中的第二分析物试剂的溶解或解离处于基本稳定的状态时,可能开始第三时间段。当流体样本中的第二分析物试剂的溶解或解离没有完成时,可能开始第三时间段。当第二分析物试剂的溶解不完全但是系统平衡,并且存在明显的红细胞比容敏感度时,可能开始第三时间段。一个目标是选择将在第二时间段期间测量到的电流和在第三时间段期间测量到的电流之间的信号差异最大化,同时还避免在相对早的时间点处变化系数太高的区域的第二和第三时间段。可能根据经验对第一、第二和第三时间段进行优化,但是最佳值通常深受第一和第二被分析试剂的相对溶解速率的影响和控制。相对于进行测定的时间,在血细胞比例和精确度之间存在权衡。换句话说,要尽快执行测定的期望应当与所需的精确度平衡。总之,当第一被分析试剂完全溶解因而系统平衡时,可能开始第一时间段。当第二分析物试剂开始溶解并且系统还没有平衡,但同时可以获得足够的信号和精确度时,可能开始第二时间段。当第二分析物试剂的溶解平衡,但是不必完成时,可能开始第三时间段。可能合适地选择每个时间段的持续时间以实现所需的平均和平滑。使用一个或多个第一和第二电流来确定校正的电流测量值可能包括:通过求一个或多个第一电流的平均值确定第一电流平均值;通过求在第二时间段上测量到的一个或多个第二电流之和与在第三时间段上测量到的一个或多个第二电流之和的差值,确定第二电流平均值;以及求第一电流平均值和第二电流平均值之和的平均值。多个测量装置中的每个测量装置可能都执行上述步骤,从而获得一组第二电流平均值。可能根据对这组第二电流平均值的线性回归分析,调整每个第二电流平均值。通过将第一和第二分析物试剂暴露于相同的样本,可能产生具有改进的测量准确度的系统。可能使用一个或多个算法来利用蓄意设想出的基于时间的响应特性在第一和第二分析物试剂之间的差异,以产生优越的分析物测量系统。例如,可能有效地使用第二分析物试剂的响应在算法上校正第一电极的响应(反之亦然),从而将可以从组合的系统中派生而来的精确度和准确度最大化。可选择地,信号之间的差异可以用于产生预测的误差项,通过该预测的误差项可以做出测量校正。例如,第一分析物试剂可以用于预测来自第二分析物的预期响应(反之亦然),并且根据来自第一分析物试剂的实际响应,来自第二分析物试剂的预测响应的第二分析物试剂的试剂响应的偏差的一些测量可以用作误差预测项。接着,根据误差项的大小和观察到的信号响应,预测的误差项可以用于根据系统的预期行为产生校正的响应。可选择地,可以调整在第一分析物试剂处的校正的水平,使得在系统误差被预测为小的区域(信任区域)中,可以将使用第一(精确的)分析物试剂的校正的水平最小化,从而增强系统误差被预测为小的地方的精确度,而不牺牲系统误差被预测为大的区域的准确度。在另一方面,在系统误差被预测为大的地方(即,非信任区域),可以在牺牲测量精确度以有利于在系统误差占比超过与主体样本快速平衡的传感器积累的精确度得益的区域的临床准确性的程度上将校正最大化。在一个实施例中,可能实施以下步骤:-在一个或多个给定时刻(t1)处测量来自第二分析物试剂的响应读数。-使用响应读数预测在一个或多个给定时刻(t2)处来自第一分析物试剂的预期结果。-在一个或多个不同的时刻(t2)为第一分析物试剂的分析物结果测量精确的实际读数。-使用预测的第一分析物试剂响应相对于实际的第一分析物试剂响应的差值来估计主体样本扩散行为与一些正常值的差异产生的偏差。-根据预期的主体样本扩散行为与正常值的偏差,校正第一被分析试剂响应,该正常值基于在经受样本扩散行为的改变时传感器的已知行为。-可选地,根据观察到的来自第一分析物试剂和/或第二分析物试剂的响应进行加权处理,使得校正的响应为:e1(校正的)=wfun×e1(实际的)+(1-wfun)×e1(预测的)其中,e1是第一分析物试剂,e2是第二分析物试剂,wfun是e1和/或e2响应的函数。-通过实际分析物浓度历史导出的回归,使用e1corrected导出校准的响应值。在替代例子中,在不同时间点来自两个(或两个以上)分析物试剂的信号可以被组合,生成组合信号的算法允许得到分析物测量值的最大似然估计(mle),其优于从任何一个分析物试剂单独得到的估计值。示例mle算法可以通过利用主成分分析和逐步线性回归等方法的回归分析获得,以下将做更详细的解释。附图说明现在将参照以下说明书附图说明本发明的具体实施例:图1为根据本发明的实施例的电化学测试条的工作部分的横截面示意图;图2为根据本发明的实施例的电化学测试条的工作部分在与样本接触前后的横截面示意图;图3为在测量的过程中在试剂垫片的内部和外部发生的并且邻近工作的电极表面的扩散过程的示意模型;图4展示了在测量的不同阶段发生的继发事件;图5a展示了将从相对较薄的试剂垫片合成物观察到的基于时间的特性响应的形状,该试剂垫片合成物还经历快速溶剂化和近似完全的溶解;图5b展示了在试剂层经历渐进溶剂化和非完全溶解的情况下将观察到的基于时间的响应的形状变化,其中,试剂垫片厚度是变化;图5c展示了扩散性变化对基于时间的响应的影响;图5d展示了在不同试剂和样本条件下,可能由系统的复杂动力学导致的多种基于时间的特性响应,其中,在测试中,溶解、溶剂化、扩散和分隔性能随时间改变;图6a展示了在具有相同试剂配方的相同电极暴露于不同浓度的分析物以产生响应时观察到的基于时间的特性响应的例子,通过合适的算法,响应的大小可以易于影响试剂浓度的测量值;图6b展示了在具有相同试剂配方的相同电极暴露于具有相同分析物浓度但是样本的红细胞比容已经变化的多个样本以产生信号响应时观察到的基于时间的响应的例子,由于改变的红细胞比容对基于时间的特性响应的混杂作用,信号响应的大小通常容易受到系统误差的影响;图7展示了于本发明的测试条一起使用的基于pca(主成分分析)的测量算法所涉及的流程步骤;图8展示了用于根据在从本发明的实施例导出的并且与该实施例一起使用的算法中使用的测试时刻的结果产生主成分得分的系数矩阵;图9展示了用于根据在从本发明的另一个实施例导出的并且于该实施例一起使用的算法中使用的测试时刻的结果产生主成分得分的系数矩阵;图10a展示了根据本发明的实施例生成的随测试的样本的红细胞比容水平和参考葡萄糖浓度绘制的校准的测量结果的三维图;图10b为图10a的旋转示意图,其展示了根据本发明的实施例的葡萄糖测量性能;图10c为图10a的旋转示意图,其展示了根据本发明的实施例的测量值对红细胞比容变化不敏感;图10d展示了在不同的红细胞比容和葡萄糖组合下660个单独的测试条的不同葡萄糖水平的红细胞比容的偏差图,这些组合的百分比在每个测试水平处实现在参考值的15%内的准确度。具体实施方式本发明寻求提供一种识别、验证或认证电化学装置的改进方法。虽然以下描述了本发明的各种实施例,但是本发明不限于这些实施例,并且这些实施例的变化可能也落入本发明的范围,本发明的范围只受所附的权利要求的限制。参照图1.根据本发明的电化学测试的工作部分由多个功能层构建,包括基底材料层100,该基底材料层100可能是,例如,聚合物(pet)或板或涂覆纸。在这个层上有通过例如丝网印刷导电炭-石墨层,或者使用au、pd、pt或本领域技术人员已知的其他合适电极导体的金属层沉积方法沉积的图案化的导电电极层200。如图所示,可能包括涂覆在导电层200上方的介质层300,通过该介质层300,导电层200的电化学活性区域可以被更准确地定义。试剂层400设置在导电电极层200的上方,覆盖可选择的介质层300。可能存在其他试剂层。一个或多个试剂可能应用于测试装置的每个电极。例如,包括第一试剂的第一试剂层可能应用于测试装置的第一工作电极和测试装置的第二工作电极。包括第二试剂的第二试剂层可能应用于测试装置的第一和第二工作电极的其中一个工作电极,从而确保第一和第二试剂同时提供给其中一个工作电极。本领域技术人员将认识到,根据最优地建立所需特性的需要,每个单独的功能层如果有需要可能可选择地由多个单独的层和/或以多个阶段或流程步骤建立,所需特性包括:(1)所需的层厚度;(2)导电性;(3)物理完整性;(4)层的均匀性;(5)孔隙率;(6)表面积;(7)表面能,或这些特性通过各种功能层的任何所需分级。因此组装的工作电极部分位于样本空间——例如,样本毛细管容积500内,形成完整的工作电化学测量测试条的组成部分。它设置为使得紧邻试剂层的样本容积500在使用时被样本流体填充满。在样本容积500中的样本流体将与试剂层400交换组分,试剂层的组分溶解和扩散进入样本主体,样本流体的元素渗透试剂层400,来自这二者的组分最终能够在导电层200的表面处电化学地反应。图2概念地展示了在时刻t1随着流体样本被引入到样本空间500中,试剂垫片400发生了什么。来自样本的溶剂和溶质渗透试剂垫片。其中的组分溶解并扩散。这在试剂垫片上产生溶胀效应。它还影响了它的扩散性。随着试剂垫片膨胀,组分扩散进入主体中,在制造过程中产生的不一致性随着进展到时刻t2而达到平衡。为了理解随着时间推移垫片性质的这些改变的意义,具有反映电极响应实际上是如何导出并且哪种试剂垫片性质对该响应产生关键影响的模型是很有用的。在图3中仅示意性地展示了这样的模型。工作电极响应来自扩散受控过程,在这个过程中,由主体样本内的分析物的反应得到的还原的(或者,在替代情况下,氧化的)物质向它们电化学氧化(或者,在替代情况下,还原)所处的导电层200扩散,从而从系统移除。从主体向导电层200的物质流通量最终控制在工作电极出测量到的响应信号。由于导电层200实际上是这些还原(或者,在替代情况下,氧化)物质的无限反应位点,在边界处的还原(或者,在替代情况下,氧化)物质的浓度名义上维持在零。因此,根据费克(fick)定律,在这个界面和主体层之间不断产生浓度梯度(dc/dx),主体层沿着这个浓度梯度具有净流量的氧化物质。从图1可以很明显得知,系统实际上由作为主体样本的两个单独的流量区域和试剂垫片层组成。这两个区域将具有不同性质。与产生电极信号的扩散通量有关的关键性质为:1.区域和电极片之间的距离(x),其控制浓度梯度(dc/dx),沿着该浓度梯度,扩散通量可以在任意时间点被驱动;2.扩散率(d)——分子可以穿过特定层内的线性距离的相对速度,其调节沿着给定的浓度梯度观察到的相对通量;3.分区(p)——区域可以充当膜从而排除具有任何给定物理性质(例如,物理尺寸、溶剂化体积/分子量、电荷/极性)的物质的渗透的相对程度。这些性质在整个测量过程中的不同时刻具有的在两个单独的区域(主体和试剂垫片)内的相对值将从根本上影响由其导出的响应信号。通常预期的是,如果其他所有条件不变,那么在垫片中的扩散率将低于在主体中的扩散率,因为一些垫片组分将作为扩散物质要穿过的障碍,垫片距离(x)是小的并且有限的,而主体边界是相对较大的并且可能是半无限的,垫片可能选择性地对来自样本内部的一些物质进行分区,而主体层将不会对来自样本内部的物质进行分区,但是它可能作为从试剂垫片扩散出来的一些物质的选择性分区。这种简单的具有已经描述过的静态参数的两个区域模型,对电极的实际的基于时间的特性响应行为的预测提出了复杂的分析挑战,但是可以并且已经建立计算模型,该计算模型能够对这个系统展示出的响应行为的做出有用的并且很有说服力的预测。特别值得注意的是,这样的计算模型非常有助于增进理解产生的信号响应如何与系统的物理性质发生关系并且受这些物理性质的影响,从而能够做出有用的预测,同时影响工作电极的物理设计和将响应信号转化为结果的算法的选择,如本文所述,该结果由于已经同时对由制造变化引起的误差和由样本成分自身中固有差异引起的系统误差进行校正,因此具有改进的准确性。同时,这样的计算模型已经用于定性地验证本文所述的影响和作用,从而证明采取的方法的内在效用,应当注意的是,实际系统比这两个区域模型更复杂,随着试剂垫片越来越多地与主体样本反应(反之亦然),在上述模型中描述的驱动信号响应的关键性质实际上在测量的整个过程中容易改变它们自身。图4示意性展示可随着时间的推进,试剂垫片和主体样本之间预期的一连串相互作用。试剂层首先从致密层溶剂化,从而变成膨胀的和溶剂化的扩散层,此后经历几乎完全分散进样本主体并且与样本主体平衡的完全溶解。在这些阶段的进展中的差异导致在不同条件下的预测的基于时间的特性响应的改变。通过电极设计和试剂组分配方控制这些转变的速度和程度使得产生的基于时间的特性响应能够可选择地用于测量和校正的目的。在试剂垫片溶剂化的初始阶段(t1),试剂垫片很大程度上停留在完整状态。它的扩散率将是相对较低的。它的分区在某些情况下是很高的,因为垫片和主体之间的组分差异性将处于它们的最大值,所以孔隙率、溶解力等性质中的差异将被夸大。因此,在反应的这个阶段的干扰物质的渗透可能被限制,如果样本是血液,那么从垫片层对细胞组分——例如,红细胞的排除将被最大化。因此,在处理的这个阶段,原始信号对例如,不同血液样本红细胞比容值的敏感度将处于最小值。在这个时刻系统将很少有机会实现平衡,因此由制造过程中的变化导致的试剂垫片中的任何变化和物理缺陷的影响将被类似地夸大。在这个时刻试剂垫片的有效厚度将低到适中,并且是最反复无常的。在垫片层内或附近将大量地产生流量。随着时间的推进(t2)以及在垫片和主体之间发生更多的物质交换,试剂垫片将膨胀。首先,它的扩散率将增大,并且它的厚度也将增大。它的分区能力将降低。然而,将稍微有机会平衡试剂垫片内由制造工艺产生的缺陷和不一致性,并且将观察到传感器之间的信号一致性和精确度的提高。随着反应物消耗在电极附近,浓度梯度dc/dx变得更浅,并且通过试剂垫片和主体层性质的平衡支配流量。随着时间的进一步推进,试剂垫片可能达到几乎完全分解的阶段。在这个时刻,垫片已经与主体样本有效地平衡。它在任何有意义的意义下都不再充当分区层。传感器有效地由邻近电极(x→0)的单个主体层组成,该主体层的扩散性几乎完全受主体样本性质的控制,试剂垫片性质的影响变得可以忽略。在这个时刻,试剂垫片内的制造变化对响应的影响将已经被最小化,斌全国将可以观察到传感器之间的最佳信号一致性和精确度。然而,在这个阶段,由于例如,影响得出响应信号的扩散过程的干扰物质的存在或者细胞组成的存在,在样本自身出现的系统差异所导致的不准确将被相应地最大化。通过理解这些过程,如何最好地设计传感器(传感器如何和何时应当在这些阶段转化,以及在对应于这些阶段的不同时间点处哪些测量值和校正信息变成在响应信号内可获得的)和如何最好地利用信息的权衡变得很明显。具体地,配制和设计(在分析物测试测定时间内)快速平衡并且向着t3的完全分解阶段快速移动的传感器垫片将最大限度地提高精确度,并且降低由制造变化造成的不精确误差。然而,这样的系统将容易过度受到包含分析物的主体样本的扩散和溶解性质的变化造成的样本之间的系统不准确性的影响。例如,在样本为血液的情况下,红细胞压积的变化将造成差异。相反地,配置和设计(在分析物测试测定时间内)缓慢通过阶段t1和t2的传感器在某些时间点,将减少包含分析物的主体样本的扩散和溶解性质的变化(例如,在样本为血液的情况下,红细胞压积的变化将造成差异)造成的影响,同时在相同的时间,潜在地将在这些不同时间点可获得的信息最大化,通过这些信息,可以在算法上校正该影响。然而,这样的配方将遭受由试剂垫片的制造变化引起的不精确性的增加,没有足够的机会平衡这些不精确性。在图5a-5d中展示了来自具有不同垫片厚度和影响扩散率和平衡时间的组分的系统的期望信号响应的例子。本发明的装置运用上面的理解。提供的装置具有根据上述转变故意配置为在不同极端工作的第一和第二分析物试剂,将可以用于提取测量值的完全可用的信息的数量和质量同时最大化。通过合适的算法,可以得到更准确的测量值,该测量值受到包含分析物的主体样本的扩散和溶解性质的变化(例如,在样本为血液的情况下,红细胞压积的变化将造成差异)造成的误差的影响的程度更轻,同时受到没有足够的机会被平衡的由试剂垫片的制造变化引起的不精确误差的影响的程度更轻。在下面非限制的示例例子中将对本发明进行进一步描述。然而,应当注意到,红细胞的相对排出(即,红细胞比容)的变化造成的信号差异被看作差别的电极和算法如何可以用于导出可能用于校正不准确性的洞察力和信息的明显例子,同时对于本领域技术人员也很明显的是,其他干扰效果(例如,直接电化学干扰物质)也将受差别的分区的影响,分区效果取决于试剂垫片是如何配置以及它们是如何设计以随时间反应,因此,本发明还容易使其适用于其他额外的误差校正策略。实施例1具有快速的溶解、和与主体样本的扩散交换和平衡的用于分析物测量工作电极的酶墨水配方配制如下,并且被指定为“inka”。制备调节至ph7.4的100ml的0.1mol/l的磷酸钾缓冲水溶液。添加和溶解3g的250mbr级羟乙基纤维素(ashlandchemicalsltd),形成粘稠浆料。添加以下组分:1.5g的煅制氧化硅(hdkk40级,来自wackergmbh)0.5g的tergitolnp/9表面活性剂(sigma)(密度=1.055g/ml)表面张力=32(dynes/cm,1%活性剂,25℃)德拉夫斯浸润=0.06(德雷夫斯20秒浸润,wt%在25℃)21s在0.05wt%在25℃)2.0g的葡萄糖脱氢酶fadh酶(sekisuidiagnostics)15.0g的亚铁氰化钾(iii)(fisherscientific)这些组分被混合为均匀糊状物。通过将导电碳墨水丝网印刷到基片上形成设定的图案,并且采用介质层可选择地涂覆在其上方以暴露出设定的工作电极区域、反电极区域和电接触,制造电化学测试条。在实施例1所述的层压步骤之前,两层的上述inka被丝网印刷和干结于测试条的工作电极区域和反电极区域中的一个上。在采用inka涂覆电极区域之后,通过在条上层压合适的分隔层和亲水顶层在电极区域上形成设定的样本空间容积,使得样本填充开口和空气逸出开口与样本空间处于有效的流体接触。随后,对于本领域技术人员而言变得明显的是,相对于以下inkb和inkc,inka具有以下关键性质。●非挥发性组分对溶剂(水)的相对较低的比例,导致在干燥后形成相对较薄的层,因而其在使用后可以快速分解;●与聚合物成膜剂和粘合剂相比,快速溶解高度可溶性无机物(亚铁氰化钾(iii))相对较高的比例。这在使用时将驱动快速溶剂化和与主体样本的快速平衡,以及试剂层相对快速的分解。●相对于促进在墨水干燥后的膜内的纯亚铁氰化钾(iii)的区域的晶体生长的其他组分,高溶性无机成分亚铁氰化钾(iii)的高负载,导致膜的不均匀性,并且在试剂垫片层内产生相对大的异常快速溶解和快速扩散区域。这种结晶作用还在干燥的层中产生非常高的表面积,这将进一步促进试剂垫片层在使用后的快速溶解。●相对于成膜材料和聚合物(hec和表面活性剂),相对较高水平的非成膜剂(不可溶硅和可溶亚铁氰化钾(iii))在试剂垫片内产生更多孔、开放的膜结构,(与连续平的、致密的膜完全不同)其有助于驱动由其和类似组分构成的试剂垫片的快速溶解和相对高的扩散率。总之,上述配方和性质选择的最终的结果是一种快速溶解的、高扩散率的试剂垫片,其有很少或有限的对主体样本的子组分进行差异分区的倾向。对于本领域技术人员而言将明显的是,在上述具体的配方a中,亚铁氰化钾(iii)承担电化学介质的作用,使得电子在氧化还原反应中在分析物和电极之间往复移动。对于本领域技术人员而言还将明显的是,相对于其他成分,特别是成膜剂,处于高比例的亚铁氰化钾(iii)产生相对较大的快速溶剂化的结晶区域,该结晶区域破坏了连续的膜的形成,并且帮助在使用中形成的试剂层的快速溶剂化和最终分解。这两个功能可能被认为是单独的设计元素,其在这个具体实施例中的单个材料选择中容易不谋而合的发生。可以设想替代的成分组合,其中,电化学介质的预期作用和对连续的膜形成的破坏的预期作用可能通过单独组分的组合实现,而不是通过假设同时具有两种功能的单一材料实现。所有这样的组合都通过扩展并入本文。实施例2具有更渐进的溶解、和与主体样本的扩散交换和平衡的用于分析物测量工作电极的酶墨水配方配制如下,并且被指定为“inkb”。制备调节至ph7.4的100ml的0.1mol/l的磷酸钾缓冲水溶液。添加和溶解15g的250lr级羟乙基纤维素(ashlandchemicalsltd),轻微搅拌超过2个小时形成粘稠浆料。添加以下组分:1.5g的煅制氧化硅(hdkk40级,来自wackergmbh)0.5g的tergitolnp/9表面活性剂(sigma)2.0g的葡萄糖脱氢酶fadh酶(sekisuidiagnostics)15.0g的亚铁氰化钾(iii)(fisherscientific)这些组分被混合为均匀糊状物。上述两层的上述inkb被丝网印刷和干结于实施例1所述的测试条的其中一个工作电极区域上。实施例3具有愈发渐进的溶解、和与主体样本的扩散交换和平衡的用于分析物测量工作电极的酶墨水配方配制如下,并且被指定为“inkc”。制备调节至ph7.4的100ml的0.1mol/l的磷酸钾缓冲水溶液。添加和溶解20g的250lr级羟乙基纤维素(ashlandchemicalsltd),轻微搅拌超过2个小时形成粘稠浆料。添加以下组分:1.5g的煅制氧化硅(hdkk40级,来自wackergmbh)0.5g的tergitolnp/9表面活性剂(sigma)2.0g的葡萄糖脱氢酶fadh酶(sekisuidiagnostics)5.0g的亚铁氰化钾(iii)(fisherscientific)这些组分被混合为均匀糊状物。上述两层的上述inkc被丝网印刷和干结于实施例1所述的测试条的其中一个工作电极区域上。对于本领域技术人员而言明显的是,相对于上述inka,inkc具有以下关键性质。●非挥发性组分对溶剂(水)相对较高的比例,导致在干燥后形成相对较厚的层,因而其在使用后可以缓慢分解;●与聚合物成膜剂、粘合剂和表面活性剂相比,快速溶解高度可溶性无机物(亚铁氰化钾(iii))相对较低的比例。这在使用时将驱动更慢的溶剂化和与主体样本的更慢的平衡,以及试剂层在使用时分解的倾向性更低。●相对于抑制在墨水干燥后的膜内的纯亚铁氰化钾(iii)的区域的晶体生长的其他组分,高溶性无机成分亚铁氰化钾(iii)的相对较低负载,导致在试剂垫片层内的大的异常快速溶解和快速扩散区域的相对缺乏。这种结晶的相对缺乏还在干燥的层中产生具有较低表面积的更均匀的膜,这将促进试剂垫片层在使用后的缓慢溶解。●相对于成膜聚合物(hec),相对较低水平的非成膜膜剂(不可溶硅和可溶亚铁氰化钾(iii))在试剂垫片内产生更致密、封闭的膜结构,其有助于限制由其和类似组分构成的试剂垫片的溶解和扩散,并且增加了其中的一些样本子组分的选择分区的倾斜。总之,上述配方和性质选择的最终的结果是一种逐步溶解的、较低扩散率的试剂垫片,其至少在最初阶段有将主体样本的子组分进行差异分区到试剂垫片中的一些最初倾向。实施例4使用实施例1中所述的过程制备测试条,包括inka的试剂层涂覆在其中一个工作电极和反电极上,inkb涂覆在额外的相邻的工作电极上。实施例5使用在实施例1中所述的过程制备测试条,包括inka的试剂层涂覆在其中一个工作电极和反电极上,inkb涂覆在额外的相邻的工作电极上。实施例6根据在实施例2中所述的过程,只使用inka制备用于测量全血中的葡萄糖的一次性使用的电化学测试条。接着,使用全血的多个样本测试这些测试条,全血包含在大约50mg/dl和~550mg/dl之间变化的不同浓度的beta-d-葡萄糖分析物,其包含有三个额外的中间水平,红细胞压积(红细胞比容)在20%v/v和60%v/v之间变化,其包含有额外的三个中间红细胞比容水平。在引入样本之前,在条上的工作电极和反电极之间设定300mv的外加电压,在大约10秒的时间内测量产生的电流。在图6a和6b中展示了产生的电流信号响应概括所选择的实施例。图6a展示了在具有相同试剂配方的多个几乎相同的电极暴露与具有不同浓度的分析物的类似样本,以产生响应时,观察到的基于时间的响应特性的例子,通过合适的算法该响应的大小可以很容易地用于影响分析物浓度的测量值。在这点上,请参阅iso15197,其以引用的方式并入本文。很明显的是,传感器响应信号不仅受到感兴趣的分析物的浓度的影响,还受到系统误差和包含分析物的主体样本容积的扩散和溶解性质的变化的影响,其中,红细胞压积或“血细胞”仅是一个例子。实施例7使用实施例1所述的过程制备一次性使用的测试条,包括来自实施例2的墨水a的试剂层涂覆在其中一个工作电极(工作电极1——以下简称为“we1”)和反电极上,来自实施例4的墨水b涂覆在额外的相邻的工作电极(工作电极2,以下简称为“we2”)上。接着,在与上述实施例6中所述的样式等价的样式中测试这些电极,但是这两个电极相对于反电极被同样地极化,并且通过每一个电极测量产生的电流响应。组合的电极输出的测量算法在另一个实施例中,根据来自两个电极的两个信号响应的组合,采用新的算法来做出增强的测量值。通过利用有意设计的不同分析物试剂的不同的基于时间的响应特性,在最终测量的响应中可能实现增强的精确度和红细胞比容不敏感性之间的平衡,这对于单独地采用任一电极系统是不可能的,或者如果不存在不同的基于时间的响应特性,这也是不可能的。在本实施例中,第一和第二电极相对于反/参考电极被极化。在第一时间段内[tk;tk+n],测量第一工作电极处的一个或多个第一电流iwe1,在第二和第三时间段内[ta;tb]和[tc;td],测量第二工作电极处的一个或多个第二电流iwe2。一个或多个第一和第二电流被用来根据以下算法确定校正的电流测量值。在时刻k和时刻k+n之间的第一工作电极上的第一电流的平均值根据下式确定:在ta和tb之间的第二工作电极上的第二电流之和q1根据下式确定:在tc和td之间的第二工作电极上的第二电流之和q2根据下式确定:qδ根据下式确定:0δ=01-q2根据(qδ),第一工作电极上的预测电流根据下式确定:i1(predicted)=β0+β1qδ在第一工作电极处的实际电流的偏差根据下式确定:iδ=i1(actual)-i1(predicted)检查偏差来看看它是否低于更低的阈值:|iδ|<la如果偏差在更大的阈值之上,那么可能报告该误差:|iδ|>ha→报告误差否则:la<=|iδ|<=ha校正电流是实际电流和预测电流的平均值:导出的红细胞比容预测是基于偏差和预测电流:hpredicted=β2+β3i1(predicted)+β4iδ导出的红细胞比容偏差根据下式确定:hδ=42-hpredicted从红细胞比容偏差导出校正的电流:采用以下加权函数:i1(actual)<inominali1(actual)>=inominalwf=1在本实施例中使用以下系数:系数说明值k以秒为单位的时间5.50n以秒为单位的时间2.00a以秒为单位的时间2.50b以秒为单位的时间4.00c以秒为单位的时间5.50d以秒为单位的时间7.70β0电流扩展项0.3027μampsβ1电流扩展项8.72e-8ampsla低校正电流阈值0.0800μampsha高校正电流中断2e-6ampsβ2血细胞扩展项25.07β3血细胞扩展项1.485e7β4血细胞扩展项3.578e7hb血细胞补偿项1.5inominal用于加权的标称电流1e-6amps按照下式,icorr被转变为样本浓度的估计值:c=p1icorr+p2p1和p2是可以通过使用合适方法(例如,线性最小二乘回归)的数据回归根据经验容易地导出,并且预测地应用于测量目的的后续等效测试情况的校准系数。在本实施例中,p1是192,p2是-27。还将明显的是,以上得出的算法系数值是特定的电极设计和采用的外加电压的函数,并且还可能通过使用合适方法(例如,线性最小二乘回归)的数据回归根据经验得出。通过线性回归根据经验最容易确定系数β0和β1。当系统设计和配方是固定的时候,对于任意一组时间点,处于标称的红细胞比容的qδ和i1actual之间的关系也(在理论上)变成固定的(不考虑噪声/误差)。因此,测试在标称的、固定的红细胞比容处具有不同葡萄糖浓度的条,并且为这些条测量i1actual和qδ将说明它们关联所用到的系数。随后β0和β1可以用于导出i1pred的值。在红细胞比容是标称值的时候,i1pred应当近似i1actual。在红细胞比容从标称值偏离的情况下,iδ是非零的并且背离已经通过差异化设计揭露的红细胞比容信息。本领域技术人员已知的是,存在可能揭露qδ/i1actual关系的其他手段(例如,数据挖掘、启发估计等)。然而,由于对于任意给定设计,关系有效地变得固定,因此可能采用任何合适的回归或发现手段。下表量化了在本实施例中观察到的不精确,将仅从墨水a电极产生的测量响应、从仅墨水b电极产生的测量响应、以及从这两个电极的算法组合产生的测量响应进行比较,当计算为在这个水平读取的参考测量值的百分比时,表示为从多个重复测量值产生的标准偏差。在五个红细胞比容水平中的每一个红细胞比容水平上的精确测量与包含所有单独的红细胞比容水平的总体标准偏差一起显示。表格还为三种情况中的每种情况显示了由样本红细胞比容的改变造成的系统误差,表示为在测量到的响应中的百分比变化,其直接归因与红细胞比容中的每百分之一改变,负值表明红细胞比容增加的下降响应,正值表明红细胞比容增加的上升响应。从这个表可以容易看出,相比单独使用的基于墨水a的测量值,这个组合的系统显示出降低的红细胞比容敏感度,并且相比单独使用的基于墨水b的测量值,这个组合的系统具有提高的精确度。实施例8使用实施例1所述的过程制备一次性使用的测试条,包括来自实施例2的墨水a的试剂层涂覆在其中一个工作电极(工作电极1——以下简称为“we1”)和反电极上,来自实施例7的墨水c涂覆在额外的相邻的工作电极(工作电极2,以下简称为“we2”)上。实施例7中所述的类型的算法,根据来自两个电极的两个信号响应的组合(特别是利用每个墨水的不同的基于时间的响应特性)增强测量值,被用于产生这里所述的测量响应。在这种情况下,使用上述等式,并且利用以下算法系数:系数说明值k以秒为单位的时间5.50n以秒为单位的时间2.00a以秒为单位的时间2.0b以秒为单位的时间3.5c以秒为单位的时间5.50d以秒为单位的时间7.70β0电流扩展项0.64μampsβ1电流扩展项9.98e-8ampsla低校正电流阈值0.120μampsha高校正电流中断2e-6ampsβ2红细胞比容扩展项20.1β3红细胞比容扩展项1.7e7β4红细胞比容扩展项3.2e7hb红细胞比容扩补偿语1.8inominal用于加权的标称电流1e-6ampsp1系数项(斜率)259p2系数项(截断)-60.7下表量化了根据对仅从墨水a电极(we1)产生的测量响应、从仅墨水c电极(we2)产生的测量响应、以及从这两个电极的算法组合产生的测量响应进行比较观察到的不精确,并且量化了归因于在每种情况下的样本红细胞比容的变化的系统误差,如上面的实施例6所述。实施例9使用实施例1所述的过程制备一次性使用的测试条,包括来自实施例2的墨水a的试剂层涂覆在其中一个工作电极(工作电极1——以下简称为“we1”)和反电极上,来自实施例4的墨水c涂覆在额外的相邻的工作电极(工作电极2,以下简称为“we2”)上。算法开发流程在另一个实施例中,使用了另一个算法,其利用在多个时间点同时来自两个电极的组合响应。在图7中示意地展示了可以得到和使用这样的算法的大致流程。在这个具体实施例中,在1秒、2秒、3秒、4秒、5秒、6秒、7秒和8秒处对inkc(we2)进行以安培为单位的测量,在1秒、2秒、3秒、4秒、5秒、6秒、7秒和8秒处对inka(we1)进行以安培为单位的测量,以为每个测量产生总共16个信号输入。这些输入按照这里所列的顺序呈现,并且编号为1到16。这个算法利用主成分分析(pca)的方法使所有这些16个输入之间的变化正交化,并且使用该变化产生具有增强的预测能力的模型。在这种情况下,首先通过从每个响应中减去标称平均值和标称标准偏差,将原始输入转化为“z-分数”:使用的值为根据所有分析物浓度和红细胞比容范围预期的所有读数的平均值和标志偏差,由此可以为每个时间点和每个电极获得测量值。接着,使用通过回归计算推导出的系数矩阵的矩阵乘法,将产生的16个输入转化为它们的主成分分数。在图8中展示了在这个实施例中用于z-分数转化的标称平均值和标称标准偏差的实际值,以及在这种情况下用于将16个原始输入转化为它们的主成分的系数矩阵。由将z分数与上述系数矩阵的矩阵乘法产生的16个主成分中的每一个主成分被分配相应的名称x1、x2、x3……x6,得到的并且用于预测最终响应的模型项,以及它们的系数值如下所示(x1是与模型项x1关联的系数,x1:x2是用于x1和x2之间的相互作用的系数,即它们的乘积的系数):当这个算法应用于来自所述测试条的测量数据时,在图x展示了产生的结果,其中,样本具有5个红细胞比容(从20%变化至60%)和5个血糖水平(在50和500mg/dl之间变化)。参照下表可以容易地看出这个组合的系统与单独使用基于inka和inkc的测试相比表现出更低的红细胞比容敏感度,并且当与单独使用基于inkc的测试相比,具有更高的精确度。实施例10使用实施例1所述的过程制备一次性使用的测试条,包括来自实施例2的墨水a的试剂层涂覆在其中一个工作电极(工作电极1——以下简称为“we1”)和反电极上,来自实施例4的墨水c涂覆在额外的相邻的工作电极(工作电极2,以下简称为“we2”)上。在这种情况下,使用不同的电化学测试过程,先施加+300mv的电压8秒,然后施加-300mv的电压2秒以驱动反向的电化学反应一段时间,给出额外的、放大的电流信号,以下展示了其中一个实施例。通过如上所述的计算回归开放了与实施例9所述的算法类型类似的pca算法。在这种情况下,使用来自2个电极的21个时间点的输入,如下表所示:使用以下参数计算z-分数:在图9中展示了用于驱动主成分的变换矩阵。每个pca项均被输入到模型中,x1表示pca1,x2表示pca2,等等。用于产生最终葡萄糖结果的模型系数如下所示:当这个算法被应用于测试条输出信号以预测分析物响应时,从葡萄糖浓度和红细胞比容水平已经被控制在以下所示参考范围的血液样本,可以得到图10a-10d所示的结果。从下表可以看出这种电极设计和算法组合可以产生对红细胞比容改变的干扰效果不敏感的精确测量值。通过适当的改变,上述实施例的任意特征可以与其他实施例的特征相结合。此外,虽然已经结合优选的实施例对本发明进行描述。但是可以理解的是本发明不限于这些实施例,本领域技术人员可以对这些实施例进行变更、修改和变化,而不背离被发明的范围。例如,虽然已经主要在验证的带有计量器的电化学装置的情况下对本发明进行了说明,但是本发明还可以用在其他领域,例如,健康与健身、食物、饮料、生物安全应用、环境样本监测等。本文所述的实施例同样可能用在动物的/兽医的药物和健康(包括狗和马)背景下。此外,虽然已经说明了本发明与电化学测试条一起使用,但是它可能延伸至其他电化学装置,如主动从用户获取流体样本(如组织液)并对样本进行电化学反应的可穿戴装置。这样的例子为患有糖尿病的用户用于控制葡萄糖浓度(和胰岛素剂量)的连续的(或半连续的)葡萄糖监测装置。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1