一种麦芽糖化过程中亚油酸代谢物的分析方法与流程
本发明涉及一种分析方法,具体涉及一种麦芽糖化过程中亚油酸代谢物的分析方法,尤其是亚油酸代谢物中的反-2-壬烯醛前驱体的分析方法。
背景技术:
啤酒是饮料市场最普遍的产品之一,其口感和风味的稳定性是制造商控制的重要质量因素。然而,啤酒从发酵结束后就开始老化。通常来说,老化源于啤酒发酵结束后,并随着原料性质、存储条件的变化而变化。羰基化合物通常是老化的指示剂,特别是低臭味阈值的醛类物质。这些醛类物质是由氨基酸、醇类和脂肪酸氧化得来的。反-2-壬烯醛的臭味阈值只有0.1ppb,因此被广泛认为是一种重要的老化指示物。
目前,啤酒中的反-2-壬烯醛的生成机制大致分为两种,一种认为其可以通过非氧化机制释放出来,另一种认为其是通过氧化机制转化而来,例如麦芽中的不饱和脂肪酸先经脂肪氧化酶(LOX,不饱和脂肪酸转化为反-2-壬烯醛的关键酶)的作用转化为9-氢过氧化物与13-氢过氧化物,然后再分别转化为反-2-壬烯醛和己醛等。但不论上述哪种机制,目前仅能够利用不稳定存在的反-2-壬烯醛的前驱体,例如氢过氧化物等来研究反-2-壬烯醛的生成机制。由于其前驱体的不稳定存在性,导致并不能全面有效地研究反-2-壬烯醛的生成机制。因此,如何提供一种全面有效地研究反-2-壬烯醛的生成机制的方法,这对于控制啤酒老化,提高啤酒的可饮性具有重要意义。
技术实现要素:
本发明的目的在于提供一种麦芽糖化过程中亚油酸代谢物的分析方法,能够全面有效地研究反-2-壬烯醛的生成机制,有利于控制啤酒老化,提高啤酒的可饮性。
本发明提供了一种麦芽糖化过程中亚油酸代谢物的分析方法,包括如下步骤:
将13C标记的亚油酸加入到麦芽粉中,按照协定麦汁法对其进行糖化;
移取糖化过程中不同反应时间段的发酵液,离心,将离心后得到的上清液分别真空冷冻干燥,得到多个中间体粉末;
向多个中间体粉末中分别加入盐酸羟胺吡啶溶液,待热烘0.75-1小时后,再分别加入衍生化试剂,再热烘1.5-2.5小时,取出后自然冷却至室温,得到多个标记干燥粉末;
以标准亚油酸替代13C标记的亚油酸,重复上述步骤,得到与所述多个标记干燥粉末相对应的多个标准干燥粉末;
利用气相色谱-质谱联用仪对所述多个标记干燥粉末和与其相对应的多个标准干燥粉末分别进行定性检测,通过比对数据库,分析得到不同的亚油酸代谢物。
作为可选方案,将50-120μL 99%纯度的13C标记的亚油酸加入到10g已粉碎过筛的麦芽粉中,加入20mL蒸馏水,于46-47℃下按照协定麦汁法,对其进行糖化。
作为优选方案,糖化过程中不同反应时间段分为糖化过程的早期、中期、末期反应时间段,其中,所述早期为反应开始0分钟时,所述中期为反应开始0-15分钟时,所述末期为反应开始15-30分钟时。
作为可选方案,移取糖化后的不同反应时间段的发酵液50-100ml,10000-14000rpm离心8-12分钟,将离心后得到的上清液真空冷冻干燥,得到多个中间体粉末,分别密封保存。
作为优选方案,向多个中间体粉末中分别加入20-30mg/mL盐酸羟胺吡啶溶液100μL,65℃-75℃热烘0.75-1小时后,再分别加入55-70μL衍生化试剂,再65℃-75℃热烘1.5-2.5小时,取出后自然冷却至室温。
作为可选方案,所述衍生化试剂选自N,O-双三甲基硅基三氟乙酰胺、N,O-双三甲基硅基乙酰胺、N-甲基叔丁基二甲基硅基三氟乙酰胺或N-甲基三甲基硅基三氟乙酰胺中的至少一种。
作为优选方案,所述气相色谱-质谱联用仪配备DB-5MS毛细管柱(0.25mm×30m×0.25μm);气相条件为:进样口温度250℃,进样体积1μL;升温程序:初始温度100℃,保持2min,3℃/min升温至184℃,0.5℃/min升温至192℃,保持2min,1℃/min升温至280℃;载气:99.999%氦气,流速1.0mL/min;质谱条件为:接口温度:250℃;离子源温度:200℃;扫描模式,Scan,扫描范围40~600amu。
作为优选方案,所述亚油酸代谢物包括蓖麻油酸、9-十八碳烯酸-12-羟基-甲酯[R-(Z)]、顺-9-十六碳烯醛和1-正癸醇的一种或多种。
本发明提供了一种麦芽糖化过程中亚油酸代谢物的分析方法,相比于现有方法而言,本申请所提供的方法主要是利用所提取到的生成反-2-壬烯醛的稳定存在的前驱体来分析反-2-壬烯醛的生成机制。由于这些前驱体相比于氢过氧化物是更稳定存在的,因此能够更客观、有效地全面认识反-2-壬烯醛的生成途径,从而可有针对性的改善啤酒自身抗氧化力的主要工艺措施,有利于控制啤酒老化,以提高啤酒风味稳定性及可饮性。
附图说明
图1为本发明实施例所提供的早期反应阶段的气相色谱图;
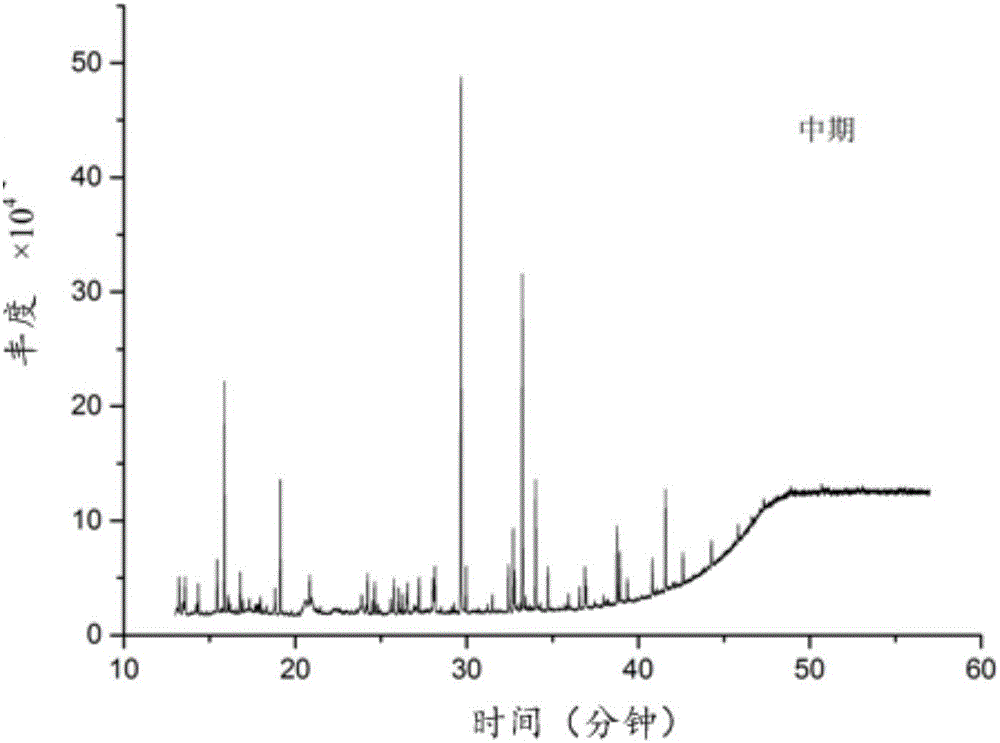
图2为本发明实施例所提供的中期反应阶段的气相色谱图;
图3为本发明实施例所提供的末期反应阶段的气相色谱图;
图4为本发明实施例所提供的典型中间产物-蓖麻油酸的加标(A)和标准(B)质谱图;
图5为本发明实施例所提供的典型中间产物-9-十八碳烯酸-12-羟基-甲酯[R-(Z)]的加标(A)和标准(B)质谱图;
图6为本发明实施例所提供的典型中间产物-1-正癸醇的加标(A)和标准(B)质谱图;
图7为本发明实施例所提供的典型中间产物-顺-9-十六碳烯醛的加标(A)和标准(B)质谱图。
具体实施方式
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明实施例的一方面提供了一种麦芽糖化过程中亚油酸代谢物的分析方法,包括如下步骤:
S1:将13C标记的亚油酸加入到麦芽粉中,按照协定麦汁法对其进行糖化。
在本步骤中,可按照常规的协定麦汁法对加入亚油酸的麦芽粉进行糖化,不同之处在于,在麦芽粉中加入的亚油酸为13C标记的亚油酸,利用同位素标记的亚油酸作对比,这样可与后续未加同位素做标记的亚油酸进行分析对比。
S2:移取糖化过程中不同反应时间段的发酵液,离心,将离心后得到的上清液分别真空冷冻干燥,得到多个中间体粉末。
本步骤主要是为了获得可用于后续处理分析的中间体粉末,在本步骤中,提取了不同反应时间段的糖化过程中发酵液以进行平行性分析,从而有利于明确获知哪个反应时间段的提取液中包含对于影响反-2-壬烯醛生成更为重要的前驱体。
S3:向多个中间体粉末中分别加入盐酸羟胺吡啶溶液,待热烘0.75-1小时后,再分别加入衍生化试剂,再热烘1.5-2.5小时,取出后自然冷却至室温,得到多个标记干燥粉末。
在本步骤中,对上述得到的中间体粉末进行进一步处理,主要是通过加入盐酸羟胺吡啶溶液和衍生化试剂,其中,加入盐酸羟胺吡啶溶液是为了生成气态化的反应物,而加入衍生化试剂则是为了将气态化的反应物转化为其衍生物,从而有利于后续进行气质检测。
S4:以标准亚油酸替代13C标记的亚油酸,重复上述步骤,得到与所述多个标记干燥粉末相对应的多个标准干燥粉末。
在本步骤中,平行制备得到在与上述加标物的反应时间段相对应的反应时间段内由提取得到的发酵液处理得到的多个标准干燥粉末,所制备得到的多个标准干燥粉末与上述的多个标记干燥粉末相对应,以利于后续对比分析。
S5:利用气相色谱-质谱联用仪对所述多个标记干燥粉末和与其相对应的多个标准干燥粉末分别进行定性检测,通过比对数据库,分析得到不同的亚油酸代谢物。
在本步骤中,利用气质联用仪对上述粉末进行定性检测,具体的,将原始分析图谱经过滤噪、归一化、基线校准和峰匹配处理后,获得保留时间、峰面积等分析数据,结合NIST和Wiley数据库,对分析图谱中各代谢物进行结构解析,并通过与未加标记的标准质谱图作比较,根据其独特的质荷比值找到与之相关的代谢物,从而确定反-2-壬烯醛的前驱体。
在一可选实施例中,将50-120μL 99%纯度的13C标记的亚油酸加入到10g已粉碎过筛的麦芽粉中,加入20mL蒸馏水,于46-47℃下按照协定麦汁法,对其进行糖化。在本实施例中,对糖化步骤进行了限定,其中所加入的同位素标记的亚油酸为高纯度同位素标记的亚油酸,这样有利于避免杂质的干扰以及分析的准确性,该步骤中所使用的协定麦汁法为常规方法,根据上述所明确的各组分的加入量,本领域技术人员可按照比例进行相应的调整,且不论使用哪种方法,只要最终结果与本实施例的相同就均视为落在本申请的保护范围内。
在一优选实施例中,所述糖化过程在20℃-70℃的温度范围内进行,优选40℃-45℃。在本实施例中,需要将糖化过程的温度控制在麦芽脂肪氧化酶的合理活性温度下,例如可以为20℃、30℃、40℃、50℃、60℃、70℃等,在一优选实施例中,糖化过程可以控制在麦芽脂肪氧化酶的最佳活性温度下,例如可以为40℃、41℃、42℃、43℃、44℃、45℃等,这样可使糖化反应进行的更加充分,有助于所获得的发酵液为反应充分最佳的发酵液,可以理解的是,本领域技术人员可根据实际反应条件在上述范围内确定适宜的糖化温度。
在一优选实施例中,糖化过程中不同反应时间段分为糖化过程的早期、中期、末期反应时间段,其中,所述早期为反应开始0分钟时,所述中期为反应开始0-15分钟时,所述末期为反应开始15-30分钟时。在本实施例中,对糖化过程中的不同反应时间段进行了限定,具体的,可根据整个反应周期、以及不同反应阶段中反应物转化为反-2-壬烯醛的程度确定时间段的划分,例如可划分为反应开始没有任何物质转化为反-2-壬烯醛的阶段、反应进行了一段时间已有部分物质转化为反-2-壬烯醛的阶段、反应后期可转化为反-2-壬烯醛的物质已全部转化为反-2-壬烯醛的阶段,根据上述阶段,可将时间段划分为0分钟、0-15分钟、15-30分钟。可以理解的是,在不同的反应条件、外界因素影响下,反应程度会有所不同,在这种情况下,本领域技术人员可根据上述划分依据优化时间段的划分,以清楚明确哪个阶段所得到的化合物对后续反-2-壬烯醛的转化更具影响性。
在一可选实施例中,移取糖化后的不同反应时间段的发酵液50-100ml,10000-14000rpm离心8-12分钟,将离心后得到的上清液真空冷冻干燥,得到多个中间体粉末,分别密封保存。在本实施例中,主要是对发酵液的处理,具体为获得上清液并将上清液冷冻干燥保存,以用于后续的进一步处理中。可以理解的是,本实施例并不局限于上述所列举的具体参数,本领域技术人员可依据实际反应情况进行调整,例如对于发酵液的体积还可以为60、70、80、90ml、离心的转速还可以为11000、12000、13000rpm,离心时间还可以为9、10、11分钟等,只要能够获得有利于后续分析的干燥粉末即可。
在一优选实施例中,向多个中间体粉末中分别加入20-30mg/mL盐酸羟胺吡啶溶液100μL,65℃-75℃热烘0.75-1小时后,再分别加入55-70μL衍生化试剂,再65℃-75℃热烘1.5-2.5小时,取出后自然冷却至室温。在本实施例中,说明了加入盐酸羟胺吡啶溶液和衍生化试剂的具体体积以及相应的具体步骤,其中,在加入相应的试剂后均需加热烘干一段合理的时间,确保反应的更加充分,以有利于获得进行后续质谱分析的样品。可以理解的是,本实施例中的盐酸羟胺吡啶溶液的浓度还可以为22、24、26、28mg/mL,衍生化试剂的加入体积还可以为60、65μL等,本领域技术人员可根据实际反应情况进行调整。在一可选实施例中,所述衍生化试剂选自N,O-双三甲基硅基三氟乙酰胺、N,O-双三甲基硅基乙酰胺、N-甲基叔丁基二甲基硅基三氟乙酰胺或N-甲基三甲基硅基三氟乙酰胺中的至少一种。可以理解的是,本实施例并不局限于上述所列举的衍生化试剂,还可以是本领域所常用的其他类似衍生化试剂。
在一优选实施例中,所述气相色谱-质谱联用仪配备DB-5MS毛细管柱(0.25mm×30m×0.25μm);气相条件为:进样口温度250℃,进样体积1μL;升温程序:初始温度100℃,保持2min,3℃/min升温至184℃,0.5℃/min升温至192℃,保持2min,1℃/min升温至280℃;载气:99.999%氦气,流速1.0mL/min;质谱条件为:接口温度:250℃;离子源温度:200℃;扫描模式,Scan,扫描范围40~600amu。本实施例具体说明了气相条件和质谱条件,所选用的条件参数均为分析化合物的优化参数,所使用的气相色谱的型号为7890A,质谱型号为5975C。
在一优选实施例中,所述亚油酸代谢物包括蓖麻油酸、9-十八碳烯酸-12-羟基-甲酯[R-(Z)]、顺-9-十六碳烯醛和1-正癸醇的一种或多种。在本实施例中,一共分析得到了4个稳定存在的转化为反-2-壬烯醛的前驱体,其中,1-正癸醇、顺-9-十六碳烯醛是由中期干燥粉末样品中分析得到的,蓖麻油酸、9-十八碳烯酸-12-羟基-甲酯[R-(Z)]是由末期干燥粉末样品中分析得到的。由于早期反应还未发生,因此没有检测得到反-2-壬烯醛的前驱体。需要说明的是,本实施例主要是从化合物的结构及其在整个过程中的量变化幅度两方面来分析得到反-2-壬烯醛的前驱体。
经本实施例方法测得,上述四个化合物为亚油酸发展代谢到反-2-壬烯醛的重要前驱体,其中,以顺-9-十六碳烯醛最为重要,蓖麻油酸、9-十八碳烯酸-12-羟基-甲酯[R-(Z)]和1-正癸醇为次重要前驱体。由于反-2-壬烯醛是一种重要的老化指示物,因此,后续可进一步监测上述四个化合物与反-2-壬烯醛在老化程度上的关联性,如果其前驱体也具备上述性能,这样结合反-2-壬烯醛的现有评判就可更有利于有针对性的改善啤酒自身抗氧化力的主要工艺措施,有利于控制啤酒老化,以提高啤酒风味稳定性及可饮性。
为了更清楚详细地介绍本发明实施例所提供的麦芽糖化过程中亚油酸代谢物的分析方法,现将结合具体实施例进行详细说明。
实施例1
将50μL 99%纯度的13C标记的亚油酸加入到10g麦芽粉中,加入20mL蒸馏水,于47℃下按照协定麦汁法对其进行糖化;在40℃下,分别移取糖化过程中早期0分钟、中期0-15分钟、末期15-30分钟的发酵液50ml,12000rpm离心8分钟,将离心后得到的上清液分别真空冷冻干燥,依次得到中间体粉末1、2、3;向中间体粉末1、2、3中分别加入25mg/mL盐酸羟胺吡啶溶液100μL,65℃热烘0.75小时后,再分别加入衍生化试剂60μL,再65℃热烘1.5小时,取出后自然冷却至室温,依次得到标记干燥粉末1、2、3;以标准亚油酸替代13C标记的亚油酸,重复上述步骤,得到与标记干燥粉末1、2、3相对应的标准干燥粉末1’、2’、3’;利用气相色谱-质谱联用仪对标记干燥粉末1、2、3和标准干燥粉末1’、2’、3’分别进行定性检测,分别得到标准图谱和如图1-3所示的标记图谱,通过比对数据库,分析得到不同的亚油酸代谢物,如图4-7所示,具体如表1-表2所示:
表1标记图谱中所分析得到的化合物相关信息
表2标准图谱中所分析得到的化合物相关信息
结合表1和表2可知,通过将标记图谱和标准图谱比对,结合保留时间并比对数据库,我们分析得到了四种不同的亚油酸代谢物,这四种代谢物为转化为反-2-壬烯醛的前驱体,分别为蓖麻油酸、9-十八碳烯酸-12-羟基-甲酯[R-(Z)]、顺-9-十六碳烯醛和1-正癸醇。由此,我们更加客观、全面地认识了生成反-2-壬烯醛的生成途径,可以理解的是,本发明的主旨在于提供一种这样客观的分析方法来分析反-2-壬烯醛的生成途径,经由这种方法分析得到的化合物均可认为是对反-2-壬烯醛的生成产生影响的化合物,本发明基于目前实验条件、图谱分析程度仅检测出了以上四种,但这并不表示仅有这四个化合物才能够影响反-2-壬烯醛的生成,以上四种可被理解为是较为重要的,但本发明并不排除保护利用本发明所提供的方法所分析得到的其它可能的化合物。
- 还没有人留言评论。精彩留言会获得点赞!