一种氧化还原缓冲熔盐体系的腐蚀测试方法与流程
本发明涉及一种氧化还原缓冲熔盐体系的腐蚀测试方法。
背景技术
熔盐作为一种传蓄热介质具有工作温度高、范围宽、压力低、比热容高等特点,受到核能、太阳能等新能源领域的日益重视。熔盐工质对合金材料的腐蚀控制是所有相关应用必须面对的问题。特别是工作在500-700℃下的氟盐或氯盐,其腐蚀行为如果控制不当,将对热工系统的安全运行带来严重威胁。在高温下,除了熔盐本身物理化学特性对金属材料造成的本征腐蚀驱动外,由于熔盐介质的强离子导电性,为电化学腐蚀的发生提供了非常合适的外部条件。另外,熔盐中的氧化性杂质是公认引起熔盐腐蚀重要驱动力之一。
熔盐腐蚀控制的方法通常首先考虑尽量降低熔盐中腐蚀性杂质,并保持在干燥、惰性气氛覆盖的环境中工作。即便如此,仍然不能保证环境中的氧化性物质不进入熔盐系统内部。例如,空气中无所不在的氧气和水气。另外,有些熔盐系统内容会生成氧化性物质,如熔盐堆系统中核燃料裂变即会产生少量氧化性产物进入熔盐冷却剂,从而逐步提高熔盐的腐蚀性。因此,除了做好熔盐净化以及提供干燥惰性气氛,还需对熔盐体系作进一步的腐蚀控制措施。
对于相对封闭的熔盐热工系统,采用插入活泼金属棒以牺牲阳极的方式或类似的加直流电阴极保护方法进行熔盐腐蚀防护在工程上比较难以实现。而以金属离子氧化还原缓冲离子对来控制熔盐的电位,从而达到减缓腐蚀的目的在工程上则更容易实现。该技术的主要原理是氧化还原缓冲离子对的存在,可有效缓冲少量氧化性杂质对熔盐电位的改变,从而达到腐蚀控制的目的。例如,在美国橡树岭实验室的熔盐堆实验(msre,1964-1969)中,通过u4+/u3+这一氧化还原缓冲离子对将一回路燃料熔盐(lif-bef2-zrf4-uf4)的电位控制在一定范围,从而有效控制了氧化性裂变产物对合金材料的腐蚀作用。
缓冲离子对的选择可以根据实际工况选择廉价易得的材料,从而降低使用成本。例如,有学者建议采用eu3+/eu2+、ce4+/ce3+等稀土离子对作为缓冲离子对控制腐蚀的,但也可以采用更为廉价cr3+/cr2+、zr4+/zr2+、fe3+/fe2+作为某些工况下的缓冲离子对来控制熔盐的腐蚀。使用缓冲离子对进行腐蚀控制的另一个关键因素是确定合适的熔盐电位控制范围,也即缓冲离子离子对的浓度比范围。因为根据能斯特公式,熔盐电位由缓冲离子对浓度比决定,因此需要事先确定不同电位下(或者说不同浓度比例下)熔盐对金属材料的腐蚀速率,从而为工程实施确定合适的熔盐电位控制范围。
由于熔盐电位随时间变化会有一定的波动,传统挂片法不适宜评价某一熔盐电位下熔盐对金属的腐蚀速率。塔菲尔(tafel)极化曲线外推法(以下简称tafel外推法)是一种经典的电化学腐蚀测试方法,可以在短时间内(一般不超过半小时)完成特定工况下的腐蚀评价,非常适合上述工况不太稳定体系的腐蚀评价。然而,实际工作中发现,经典的tafel外推法适合用于阳极极化电流只包含金属腐蚀溶解电流时的情况,但不适合用于含有氧化还原缓冲离子对的熔盐体系腐蚀评价。因此,研发一种适用于测试含有氧化还原缓冲离子对的熔盐体系腐蚀的方法是本领域亟待解决的问题。
技术实现要素:
本发明所解决的技术问题在于克服现有的塔菲尔(tafel)极化曲线外推法不适合含有氧化还原缓冲离子对的熔盐体系腐蚀评价的缺陷,提供了一种氧化还原缓冲熔盐体系的腐蚀测试方法。本发明的测试方法适用于含有氧化还原缓冲离子对的熔盐体系的腐蚀测试,该方法简单快捷,可以在较短时间内获得系列熔盐腐蚀控制工程中需要的数据。
本发明通过以下技术方案解决上述技术问题。
本发明提供了一种氧化还原缓冲熔盐体系的腐蚀测试方法,其包括下述步骤:
(1)分别检测氧化还原缓冲熔盐体系的待测金属的工作电极和惰性金属的工作电极,以获得两组阳极极化电流曲线;
(2)对获得的两组所述阳极极化电流曲线的数据进行数学处理:将所述待测金属的工作电极的极化电流ia减去所述惰性金属的工作电极的极化电流ia,惰,以得到与腐蚀相关的阳极极化电流ia,corr;
(3)以lgia,corr为纵坐标,以极化电位δe为横坐标作图,对获得的曲线进行线性拟合,根据拟合结果计算得到所述待测金属在所述氧化还原缓冲熔盐体系中的腐蚀电流值icorr;
其中,所述氧化还原缓冲熔盐体系包括氟盐和/或氯盐,还包括选自下述氧化还原离子对中的一种:eu3+/eu2+、ce4+/ce3+、cr3+/cr2+、zr4+/zr2+、fe3+/fe2+和u4+/u3+;
所述待测金属的工作电极和所述惰性金属的工作电极的形状、大小和工作面积完全相同。
本发明中,所述氟盐较佳地为碱金属氟盐和/或碱土金属氟盐,例如所述氟盐可为lif、kf、naf和bef2盐中的两种或多种。
本发明中,较佳地,所述氟盐为lif、kf和naf的混合物。
其中,较佳地,所述lif、kf和naf的混合物中所述lif、所述kf和所述naf的摩尔比为(45-47):(10-12):(41-43),更佳地,所述lif的摩尔百分比为46.5%,所述kf的摩尔百分比为11.5%,和所述naf的摩尔百分比为42%。
本发明中,较佳地,所述氟盐为lif和bef2的混合物。
其中,较佳地,所述lif和bef2的混合物中所述lif和所述bef2的摩尔比为(65-68):(32-35),更佳地,所述lif的摩尔百分比为67%,所述bef2的摩尔百分比为33%。
本发明中,所述氯盐较佳地为碱金属氯盐和/或碱土金属氯盐,例如所述氯盐可为nacl、kcl、mgcl2和cacl2中的两种或多种。
本发明中,所述熔盐体系中的所述氧化还原离子对中每种离子的质量浓度可为本领域常规,较佳地为100-1000ppm,更佳地为400-800ppm,进一步更佳地为600ppm。
本发明中,用于检测所述金属工作电极和所述惰性金属工作电极的装置可为本领域常规,例如三电极电化学测试系统,较佳地采用瑞士万通autolab302n型电化学工作站,其自带nova2.1软件。
本发明中,较佳地,所述待测金属为金属铬、铁、镍及其合金材料,例如316l不锈钢、304不锈钢、hastelloyc276合金等。
本发明中,较佳地,所述待测金属以金属丝的形式使用;其中,所述金属丝的直径较佳地为1-2mm。
本发明中,所述惰性金属为本领域常规使用的惰性金属,较佳地,所述惰性金属为银;较佳地,所述银以银丝的形式使用;其中,所述银丝的直径较佳地为1-2mm。
本发明中,所述检测的过程中的扫描速率可为本领域常规,较佳地为0.5-1mv/s。
本发明中,所述检测的过程中的温度可为本领域常规,较佳地为550-750℃,更佳地为600-650℃。
本发明中,本领域技术人员知晓,当所述待测金属的工作电极和所述惰性金属的工作电极的形状、大小和工作面积完全相同时,由氧化还原离子对在两者上因相互转变产生的非腐蚀阳极极化电流相等,因此,所述熔盐体系的与腐蚀相关的极化电流应为所述待测金属的工作电极在强极化区上获得的极化电流减去所述惰性金属的工作电极上同一极化区获得的极化电流。
本发明中,本领域技术人员知晓,可选用butler-volmer电极动力学方程来表达阳极极化电流与极化电位之间的函数关系。以316l不锈钢作为所述待测金属为例,对其在flinak-crf3/crf2熔盐体系中的腐蚀情况进行检测,进行所述数学处理的具体推导过程如下:
316l不锈钢作为腐蚀电极在flinak-crf3/crf2熔盐体系存在以下两种电化学反应:
对316l不锈钢腐蚀电极进行阳极极化时,阳极极化电流可表达为:
ia=i1,a+i2,a(3)
同理,在阴极极化时,阴极极化电流可表达为:
ic=i2,c+i1,c(4)
上式中下标1对应反应(1),下标2对应反应(2),a对应阳极反应,c对应阴极反应。
根据butler-volmer电极动力学方程(以下简称b-v方程),ia和ic电流表达式可展开为:
其中,
α为传质系数,β=1-α,e1,e为反应(1)的平衡电位,e2,e为反应(2)的平衡电位。
对阳极极化电流ia表达式变换一下形式:
进一步分解为:
在腐蚀电化学中,腐蚀电流icorr定义为在腐蚀电位ecorr下,金属被氧化腐蚀溶解而产生的电流。在本案例中,腐蚀电流则对应316l不锈钢中金属铬被氧化生成cr2+的电流,根据butler-volmer电极动力学方程(b-v方程)icorr的表达式为:
将icorr代入上式可得:
在惰性金属工作电极上进行阳极极化时,反应式(1)所示的阳极反应不存在,阳极极化电流主要由反应式(2)的阳极反应贡献,即
式中e2,e是cr3+/cr2+的平衡电位,
用在316l不锈钢的工作电极上测得强极化区阳极电流ia减去惰性金属的工作电极上测得的阳极电流ia,惰,得到氧化还原缓冲熔盐体系与腐蚀相关的阳极极化电流ia,corr:
两边取对数:
在阳极强极化区,以lgia,corr对极化电位δe作图,并进行线性拟合,可以获得lgicorr,进而计算得到腐蚀电流icorr。
本发明中,本领域技术人员知晓,所述极化电位δe通常为测试得到的电位e与腐蚀电位ecorr的差值,即δe=e-ecorr。
本发明中,本领域技术人员知晓,所述线性拟合的区域通常为阳极或阴极极化电流曲线上的强极化区,较佳地为阳极极化电流曲线上的强极化区,例如所述极化电位δe为0.13-0.15v的区域。
本发明中,本领域技术人员知晓,所述线性拟合的相关指数通常用r表示,数值r2越接近1表明解释变量x和预测变量y之间的线性相关性越强,本发明中,较佳地,所述线性拟合后得到的r2值大于0.92,更佳地为0.99以上。
在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
本发明所用试剂和原料均市售可得。
本发明的积极进步效果在于:
本发明的方法适用于含有氧化还原缓冲离子对的熔盐体系的腐蚀测试,该方法简单快捷,可以在较短时间内获得熔盐腐蚀控制工程中需要的系列数据。
附图说明
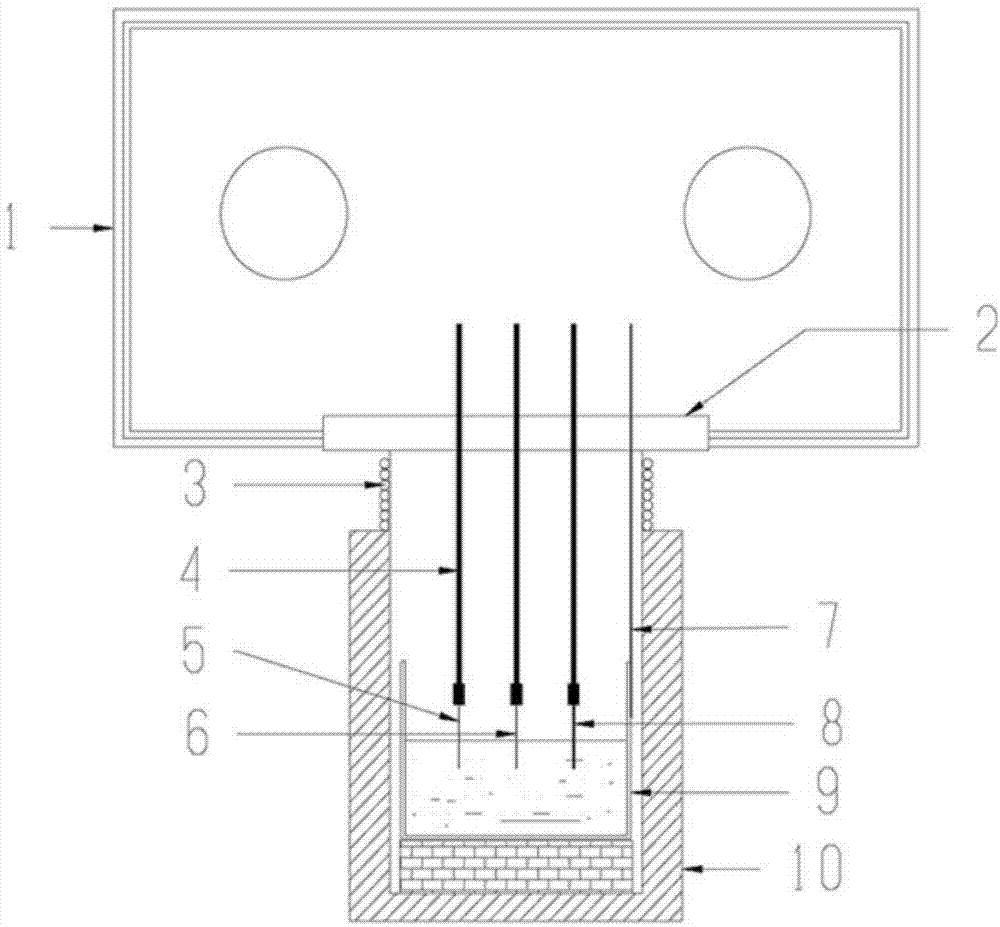
图1为本发明实施例1-9使用的腐蚀测试装置结构示意图。
图2为经典tafel极化曲线外推法理论示意图。
图3为熔盐体系只含有crf3体系时用经典的tafel方法得到的腐蚀测试曲线。
图4为本发明实施例1-9的腐蚀测试方法原理示意图。
图5为本发明实施例1的腐蚀测试曲线。
图6为本发明实施例2的腐蚀测试曲线。
图7为本发明实施例3的腐蚀测试曲线。
图1中的附图标记说明如下:
手套箱1
炉盖2
水冷套3
电极导杆4
待测金属工作电极5
辅助工作电极6
热电偶7
参比电极8
玻璃碳坩埚9
井式炉10
具体实施方式
下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。
本领域技术人员知晓,电化学法测量腐蚀速率是实验室和现场常用的一种间接测试方法。测量时首先对腐蚀电极进行“极化”,根据获得的极化曲线利用电化学理论推算出腐蚀电流icorr或腐蚀速率,其理论是依据wagner和trand的混合电位理论和叠加原理推导出的腐蚀体系的动力学方程式。利用该方程式在极化曲线的强极化区,外加电流与电极极化呈tafel关系,即在半对数坐标上是直线,该直线也就是局部阳、阴极极化曲线(即阳极或阴极强极化区,也是拟合时选择的区域,如图2中“tafel曲线强极化区;线性拟合区间”所示的区域。),两直线相交于自腐蚀电位点,从tafel直线与自腐蚀电位水平线的的交点可求出腐蚀金属电极的自腐蚀电流icorr。
以下实施例中,除了所含添加物的不同,其它工况假定完全一致,如温度、被腐蚀合金种类、形状、大小等。尽管与以下理论推导没有关系,还是进一步设定工作温度为600℃,被腐蚀合金为316l不锈钢。其它温度或合金材料不影响推导过程,但是本领域技术人员知晓,考虑到添加物的溶解度,实际工况是具有一定的温度下限的。
以下实施例1-9使用的腐蚀测试装置如图1所示,腐蚀测试的熔盐电解池置于与手套箱1连接的井式炉10中,井式炉10与手套箱1的连接处设有炉盖2,贯穿炉盖2设有若干电极导杆4和热电偶7,井式炉10的炉盖2下方设有水冷套3。井式炉10的炉管与外界保持密封,与自净化惰性气氛手套箱1的箱体相通,炉管内气氛与手套箱1一致。手套箱1为带有自净化功能的惰性气氛手套箱,箱内气氛中的水和氧气之和控制在10ppm以下。腐蚀测试三电极体系中待测金属工作电极5为待测金属样品或比对的惰性金属对电极。待测金属样品与惰性金属工作电极尺寸、形状、大小需保持一致,以下实施例和对比例采用直径1±0.05mm金属丝为待测金属工作电极5,测试时浸入熔盐深度须保持相同,以获得相等的工作面积。熔盐存在于玻璃碳坩埚9中。辅助工作电极6可采用石墨、玻璃碳、惰性金属等材料,面积远大于工作电极。参比电极8采用自制nif2/ni参比电极,制作方法为:采用壁厚1mm的热压氮化硼管为参比电极管,内充10%nif2熔盐溶液,熔盐组成与腐蚀测试体系的熔盐一致,然后通过纯镍丝插入管内与nif2溶液组成参比电极8。本文所采用的电化学测量装置为瑞士万通autolab302n型电化学工作站,及其自带的nova2.1软件。
本领域技术人员知晓,进行极化曲线测试时,先从开路电压往正向扫描0.15v,扫描速度为0.5mv/s,获得阳极极化曲线,阴极极化曲线则从开路电位往负向扫描获得。经典tafel外推法可以从分别从阳极极化和阴极极化获得腐蚀电流,而本发明的方法则只能从阳极极化曲线获得腐蚀电流。
经典tafel外推法的具体方法如下:
在flinak-crf3体系,经典tafel外推法可以直接用于测试其对316l不锈钢的腐蚀速率。如图2所示,在进行阳极极化曲线测试时,316l不锈钢电极上主要发生式(1)所示的电化学反应。该反应对应316l不锈钢铬元素的溶解腐蚀。阴极极化则对应(2)式的电化学反应。以lgi对极化电位e作图,在tafel阳极极化区或阴极极化区进行线性拟合(见图2中文字描述部分),所得截距即为lgicorr。由此可以测得316l不锈钢在flinak-crf3体系的腐蚀速率icorr。根据电化学理论的具体推导如下:
316l不锈钢作为腐蚀电极在flinak-crf3熔盐体系存在以下两种电化学反应:
对316l不锈钢腐蚀电极进行阳极极化时,阳极极化电流可表达为:
ia=i1,a-i2,c
考虑到我们只对强极化区的数据进行处理,在强极化区i2,c可忽略不计,所以我们对推导过程做进一步简化处理:
ia=i1,a
同理,在阴极极化时,阴极极化电流可表达为:
ic=i2,c
(下标1对应反应(1),下标2对应反应(2),a对应阳极反应,c对应阴极反应)
阳极和阴极上电化学反应的动力学方程都可以用b-v方程(butler-volmer电极动力学方程)表示,即:
式中,
当腐蚀金属电极处于自腐蚀电位时,此时测得的外电流为零,腐蚀金属电极上的电位就是它的腐蚀电位ecorr,此时:
i1,a=icorr=i2,c
则:
变换形式:
转化为:
即:
后期数据处理,在强极化区,对阳极电流表达式两边取对数:
具体地,测试316l不锈钢在含有600ppmcrf3的flinak熔盐中的腐蚀速率。测试温度为600℃,待测316l不锈钢金属丝直径1mm,浸入熔盐中3cm。以待测金属丝为工作电极,以0.5mv/s的扫描速度,分别从开路电位向正向和负向扫描0.15v,获得阳极和阴极极化曲线,如图3所示。由于熔盐体系只含有crf3体系,用经典的tafel方法,即可分别从阳极极化曲线或阴极极化曲线上得到腐蚀速率。在极化曲线强极化区进行线性拟合,拟合后得到两条直线,其直线方程分别为:y=5.633x-3.767(r2=0.988,其中r是线性拟合的相关指数,r2越接近1,表明解释变量x和预测变量y之间的线性相关性越强),和y=-1.834x-3.688(r2=0.924)。所得直线与纵轴交汇点即为lgicorr。从阳极极化曲线中得到的腐蚀电流密度为171μa/cm2,从阴极极化曲线中得到的腐蚀电流密度为205μa/cm2。
以下实施例1-9中的腐蚀测试方法根据电化学理论的具体推导如下:
316l不锈钢作为腐蚀电极在flinak-crf3/crf2熔盐体系存在以下两种电化学反应:
对316l不锈钢腐蚀电极进行阳极极化时,阳极极化电流可表达为:
ia=i1,a+i2,a
同理,在阴极极化时,阴极极化电流可表达为:
ic=i2,c+i1,c
上式中下标1对应反应(1),下标2对应反应(2),a对应阳极反应,c对应阴极反应。
根据butler-volmer电极动力学方程(以下简称b-v方程),ia和ic电流表达式可展开为:
其中,
α为传质系数,β=1-α。
对阳极极化电流ia表达式变换一下形式:
进一步分解为:
在腐蚀电化学中,腐蚀电流icorr定义为在腐蚀电位ecorr下,金属被氧化腐蚀溶解而产生的电流。在本案例中,腐蚀电流则对应316l不锈钢中金属铬被氧化生成cr2+的电流,根据b-v方程icorr的表达式为:
将icorr代入上式可得:
由此,可以获得氧化还原缓冲熔盐flinak-crf3/crf2体系中316l不锈钢电极在阳极极化时极化电流与极化电位的关系表达式。式中虽然含有icorr这一常数,却不能通过类似经典tafel外推法的数学处理方式,通过上式获得lgicorr的数值,因此经典tafel外推法不能适用于氧化还原缓冲熔盐体系的电化学腐蚀测试。造成这一现象的主要原因是阳极极化电流ia含有i2,a这一项,即阳极极化电流中除了金属铬的腐蚀溶解电流,还有一部分cr2+氧化为cr3+所产生的电流。
在惰性金属工作电极上进行阳极极化时,反应式(1)所示的阳极反应不存在,阳极极化电流主要由反应式(2)的阳极反应贡献,即
式中e2,e是cr3+/cr2+的平衡电位,
用在316l不锈钢的工作电极上测得强极化区阳极电流ia减去惰性金属的工作电极上测得的阳极电流ia,惰,得到氧化还原缓冲熔盐体系与腐蚀相关的阳极极化电流ia,corr:
两边取对数:
在阳极强极化区,以lgia,corr对极化电位△e作图,并进行线性拟合,可以获得lgicorr,进而计算得到腐蚀电流icorr。图4为以下实施例1-9的腐蚀测试方法原理示意图。
316l不锈钢的工作电极与惰性金属的工作电极的形状、大小以及工作面积完全相同时,两者产生的阳极极化电流i2,a相等,具体论述如下:
根据分析,惰性电极阴极极化时,极化电流则由反应(1)、(2)对应的阴极反应产生,与316l不锈钢工作电极上的阴极极化电流表达式一致,即
ic,惰=i2,c+i1,c
实测数据表明,相同尺寸惰性电极与316l不锈钢电极上获得的阴极极化电流基本一致。由此说明,316l不锈钢的工作电极与惰性金属的工作电极的形状、大小以及工作面积完全相同时,两者产生的阳极极化电流i2,a相等。
实施例1
测试316l不锈钢(316lss)在含有1000ppmcrf3及600ppmcrf2的flinak熔盐中的腐蚀速率。测试温度为600℃,待测316l不锈钢金属丝直径1mm,浸入熔盐中3cm。比对惰性金属电极为直径1mm银丝,浸入熔盐中3cm。分别以待测金属丝和银丝为工作电极,以0.5mv/s的扫描速度,从开路电位向正向和负向扫描0.15v,获得两组阳极和阴极极化曲线,如图5所示。由于熔盐体系含有crf2/crf3缓冲离子对,经典的tafel外推法不适用,需采用本发明方法进行测试。即,在阳极强极化区(δe约为0.13~0.15v),将316l不锈钢电极上获得的极化电流减去同一极化电位下在银电极上获得的极化电流值,得到的电流取对数后再与δe作图,得到新的lgi~δe曲线。根据前文理论推导,对该新获得的lgi~δe曲线进行线性拟合,获得的直线的方程为:y=8.163x-4.123(r2=0.999),该直线与纵轴的交汇点即对应相应的lgicorr。本例中,从新获得的lgi~δe曲线中得到的腐蚀电流密度为75μa/cm2。重复测定5次的平均值为76μa/cm2,相对标准偏差rsd为2.5%。
实施例2
测试304不锈钢(304ss)在含有1000ppmcrf3及800ppmcrf2的flinak熔盐中的腐蚀速率。测试温度为600℃,待测304不锈钢金属丝直径1mm,浸入熔盐中3cm。比对惰性金属电极为直径1mm银丝,浸入熔盐中3cm。分别以待测金属丝和银丝为工作电极,以0.5mv/s的扫描速度,从开路电位向正向和负向扫描0.15v,获得两组阳极和阴极极化曲线,如图6所示。采用类似实施例1的处理方法,得到新的lgi~δe曲线,对该曲线进行线性拟合,获得的直线的方程为:y=11.69x-4.165(r2=0.999),从与纵轴截距计算得到的304不锈钢在该氧化还原缓冲熔盐体系中的腐蚀电流密度为68μa/cm2。重复测定5次的平均值为67μa/cm2,相对标准偏差rsd为2.3%。
实施例3
测试hastelloyc276合金在含有1000ppmcrf3及800ppmcrf2的flinak熔盐中的腐蚀速率。测试温度为600℃,待测hastelloyc276金属丝直径1mm,浸入熔盐中3cm。比对惰性金属电极为直径1mm银丝,浸入熔盐中3cm。分别以待测金属丝和银丝为工作电极,以0.5mv/s的扫描速度,从开路电位向正向和负向扫描0.15v,获得两组阳极和阴极极化曲线,如图7所示。采用类似实施例1的处理方法,得到新的lgi~δe曲线,对该曲线进行线性拟合,获得的直线的方程为:y=3.142x-4.515,从与纵轴截距计算得到的hastelloyc276合金在该氧化还原缓冲熔盐体系中的腐蚀电流密度为31μa/cm2。重复测定5次的平均值为30μa/cm2,相对标准偏差rsd为5.2%。
实施例4
测试铁在含有1000ppmfef3及800ppmfef2的flinak熔盐中的腐蚀速率。测试温度为600℃,待测铁金属丝直径1mm,浸入熔盐中3cm。比对惰性金属电极为直径1mm银丝,浸入熔盐中3cm。分别以待测金属丝和银丝为工作电极,以0.5mv/s的扫描速度,从开路电位向正向和负向扫描0.15v,获得两组阳极和阴极极化曲线。采用类似实施例1的处理方法,得到新的lgi~δe曲线,对该曲线进行线性拟合,从与纵轴截距计算得到的金属铁在该氧化还原缓冲熔盐体系中的腐蚀电流密度为165μa/cm2。重复测定5次的平均值为167μa/cm2,相对标准偏差rsd为1.1%。
实施例5
测试铁在含有1000ppmfef3及800ppmfef2的flibe熔盐(lif-bef2,67-33mol%)中的腐蚀速率。测试温度为600℃,待测铁金属丝直径1mm,浸入熔盐中3cm。比对惰性金属电极为直径1mm银丝,浸入熔盐中3cm。分别以待测金属丝和银丝为工作电极,以0.5mv/s的扫描速度,从开路电位向正向和负向扫描0.15v,获得两组阳极和阴极极化曲线。采用类似实施例1的处理方法,得到新的lgi~δe曲线,对该曲线进行线性拟合,从与纵轴截距计算得到的金属铁在该氧化还原缓冲熔盐体系中的腐蚀电流密度为123μa/cm2。重复测定5次的平均值为121μa/cm2,相对标准偏差rsd为2.4%。
实施例6
测试316l不锈钢在含有1000ppmuf4及400ppmuf3的flibe熔盐中的腐蚀速率。测试温度为600℃,待测316l不锈钢金属丝直径1mm,浸入熔盐中3cm。比对惰性金属电极为直径1mm银丝,浸入熔盐中3cm。分别以待测金属丝和银丝为工作电极,以0.5mv/s的扫描速度,从开路电位向正向和负向扫描0.15v,获得两组阳极和阴极极化曲线。采用类似实施例1的处理方法,得到新的lgi~δe曲线,对该曲线进行线性拟合,从与纵轴截距计算得到的316l不锈钢在该氧化还原缓冲熔盐体系中的腐蚀电流密度为63μa/cm2。重复测定5次的平均值为65μa/cm2,相对标准偏差rsd为2.8%。
实施例7
测试316l不锈钢在含有1000ppmzrf4及600ppmzrf2的flibe熔盐中的腐蚀速率。测试温度为600℃,待测316l不锈钢金属丝直径1mm,浸入熔盐中3cm。比对惰性金属电极为直径1mm银丝,浸入熔盐中3cm。分别以待测金属丝和银丝为工作电极,以0.5mv/s的扫描速度,从开路电位向正向和负向扫描0.15v,获得两组阳极和阴极极化曲线。采用类似实施例1的处理方法,得到新的lgi~δe曲线,对该曲线进行线性拟合,从与纵轴截距计算得到的316l不锈钢在该氧化还原缓冲熔盐体系中的腐蚀电流密度为79μa/cm2。重复测定5次的平均值为79μa/cm2,相对标准偏差rsd为2.4%。
实施例8
测试316l不锈钢在含有800ppmeuf3及800ppmeuf2的flinak熔盐中的腐蚀速率。测试温度为650℃,待测316l不锈钢金属丝直径1mm,浸入熔盐中3cm。比对惰性金属电极为直径1mm银丝,浸入熔盐中3cm。分别以待测金属丝和银丝为工作电极,以0.5mv/s的扫描速度,从开路电位向正向和负向扫描0.15v,获得两组阳极和阴极极化曲线。采用类似实施例1的处理方法,得到新的lgi~δe曲线,对该曲线进行线性拟合,从与纵轴截距计算得到的316l不锈钢在该氧化还原缓冲熔盐体系中的腐蚀电流密度为97μa/cm2。重复测定5次的平均值为99μa/cm2,相对标准偏差rsd为2.7%。
实施例9
测试hastelloyc276合金在含有100ppmcef4及1000ppmcef3的flinak熔盐中的腐蚀速率。测试温度为650℃,待测hastelloyc276合金金属丝直径1mm,浸入熔盐中3cm。比对惰性金属电极为直径1mm银丝,浸入熔盐中3cm。分别以待测金属丝和银丝为工作电极,以0.5mv/s的扫描速度,从开路电位向正向和负向扫描0.15v,获得两组阳极和阴极极化曲线。采用类似实施例1的处理方法,得到新的lgi~δe曲线,对该曲线进行线性拟合,从与纵轴截距计算得到的hastelloyc276合金在该氧化还原缓冲熔盐体系中的腐蚀电流密度为253μa/cm2。重复测定5次的平均值为257μa/cm2,相对标准偏差rsd为2.1%。
虽然以上描述了本发明的具体实施方式,但是本领域的技术人员应当理解,这仅是举例说明,本发明的保护范围是由所附权利要求书限定的。本领域的技术人员在不背离本发明的原理和实质的前提下,可以对这些实施方式做出多种变更或修改,但这些变更和修改均落入本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!