昭和草萃取物用于治疗乳癌的用途的制作方法
本公开涉及昭和草(crassocephalumrabens)萃取物的用途,特别地,涉及昭和草萃取物用于治疗乳癌的用途。
背景技术:
三阴性乳癌(triplenegativebreastcancer,tnbc)为一种侵袭性乳癌亚型,其特征为可当标靶的雌激素(er)、孕酮(pr)及人类表皮生长因子(her2)受体的缺乏或较低表达(sledgegw,mamounasep,hortobagyign等人,(2014)past,present,andfuturechallengesinbreastcancertreatment.jclinoncol32(19):1979-1986)。于手术之后,一般利用具有细胞毒性的化学疗法来预防肿瘤患者的肿瘤生长及转移(zeichnersb,terawakih及goginenik(2016)areviewofsystemictreatmentinmetastatictriplenegativebreastcancer.breastcancer(auckl)10:25-36)。当今市面上最常给予的tnbc化学治疗药物之一为多柔比星(doxorubicin)(
技术实现要素:
本公开提供昭和草用于治疗乳癌的用途。
本公开提供一种在需要治疗的个体中治疗乳癌及/或治疗乳癌转移的方法,其包含给予该个体有效量的昭和草萃取物及视情况医药上可接受的载剂或赋形剂。
本公开提供昭和草萃取物用于制备治疗乳癌及/或治疗乳癌转移药物的用途。
本公开提供一种治疗乳癌及/或治疗乳癌转移的医药组合物,其包含有效量的昭和草萃取物及视情况医药上可接受的载剂或赋形剂。
本公开提供昭和草萃取物,其用于治疗乳癌及/或治疗乳癌转移。
本公开提供一种在需要治疗的个体中治疗乳癌及/或治疗乳癌转移的方法,其包含给予该个体有效量的如式i所示的化合物:1,2-二-o-α-亚麻酰基-3-o-β-吡喃半乳糖基-sn-甘油、1(2)-o-α-亚麻酰基-2(1)-o-α-亚油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:2)、1(2)-o-α-亚麻酰基-2(1)-o-α-棕榈酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/16:0)、1(2)-o-α-亚麻酰基-2(1)-o-α-油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:1)、1,2-二-o-α-亚麻酰基-3-o-(6-o-α-吡喃半乳糖β-吡喃半乳糖)-sn-甘油、或其医药上可接受的衍生物及视情况医药上可接受的载剂或赋形剂;
其中r1及r2独立为c(o)ra,其中ra为具有0至3个双键的c15-17烷基,及r3为单半乳糖基或二半乳糖基。
本公开提供如式i所示的化合物:1,2-二-o-α-亚麻酰基-3-o-β-吡喃半乳糖基-sn-甘油、1(2)-o-α-亚麻酰基-2(1)-o-α-亚油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:2)、1(2)-o-α-亚麻酰基-2(1)-o-α-棕榈酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/16:0)、1(2)-o-α-亚麻酰基-2(1)-o-α-油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:1)、1,2-二-o-α-亚麻酰基-3-o-(6-o-α-吡喃半乳糖β-吡喃半乳糖)-sn-甘油、或其医药上可接受的衍生物用于制备治疗乳癌及/或治疗乳癌转移药物的用途。
本公开提供一种治疗乳癌及/或治疗乳癌转移的医药组合物,其包含有效量的如式i所示的化合物:1,2-二-o-α-亚麻酰基-3-o-β-吡喃半乳糖基-sn-甘油、1(2)-o-α-亚麻酰基-2(1)-o-α-亚油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:2)、1(2)-o-α-亚麻酰基-2(1)-o-α-棕榈酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/16:0)、1(2)-o-α-亚麻酰基-2(1)-o-α-油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:1)、1,2-二-o-α-亚麻酰基-3-o-(6-o-α-吡喃半乳糖β-吡喃半乳糖)-sn-甘油、或其医药上可接受的衍生物及视情况医药上可接受的载剂或赋形剂。
本公开提供如式i所示的化合物:1,2-二-o-α-亚麻酰基-3-o-β-吡喃半乳糖基-sn-甘油、1(2)-o-α-亚麻酰基-2(1)-o-α-亚油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:2)、1(2)-o-α-亚麻酰基-2(1)-o-α-棕榈酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/16:0)、1(2)-o-α-亚麻酰基-2(1)-o-α-油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:1)、1,2-二-o-α-亚麻酰基-3-o-(6-o-α-吡喃半乳糖β-吡喃半乳糖)-sn-甘油、或其医药上可接受的衍生物,其用于治疗乳癌及/或治疗乳癌转移。
以下部分详细描述了本发明。本发明的其他特征、目的和优点描述于发明具体实施方式和权利要求中。
附图说明
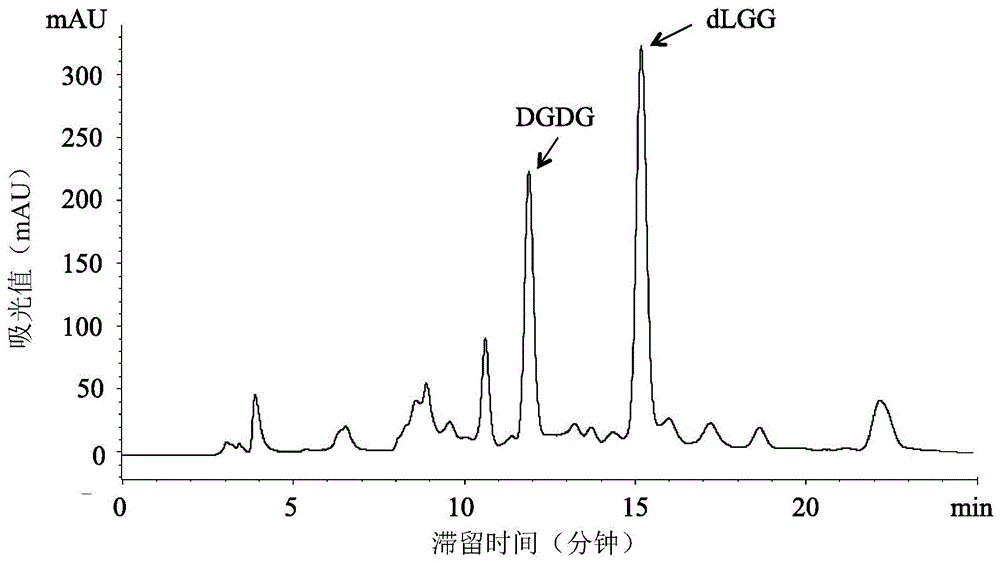
图1显示来自昭和草的cr-api萃取物的hplc特征曲线,其在210nm吸光度下测定。生物活性化合物1,2-二-o-α-亚油酰基-3-o-(6-o-α-吡喃半乳糖基-β-吡喃半乳糖基)-sn-甘油(dgdg)及1,2-二-o-α-亚油酰基-3-o-β-吡喃半乳糖基-sn-甘油(dlgg)的滞留时间(rt)经检测分别为约12及15分钟。
图2显示4t1原位乳癌模型的实验设计及治疗方案,该乳癌模型用于评估来源于昭和草的dlgg及富含dlgg的萃取物(cr-api)的作用。多柔比星用作阳性对照组。每3天监测药物及化合物/萃取物对肿瘤尺寸的作用。所有测试动物在第30天安乐死。
图3显示在体外试验中dlgg处理显著降低tnbc细胞的存活率。细胞(3×103个细胞/孔)用指定浓度的dlgg(μm)或cr-api(μg/ml)处理24小时。细胞存活率利用mtt分析测定。所呈现的资料代表3次独立实验,每次实验5次技术重复。
图4a至图4b表明cr-api及dlgg疗法延长肿瘤植入动物的存活期且维持肿瘤植入动物的正常体重。带有肿瘤的小鼠用以下治疗:pbs(肿瘤对照)、dox5(5mg/kg/每3天;i.v.)、dlgg5(每天5mg/kg;o.p.)、dlgg25(每天25mg/kg;o.p.)、cr-api200(每天200mg/kg;o.p.)、cr-api400(每天400mg/kg;o.p.)及dox5+dlgg5组合疗法。图4a是存活曲线,其表明cr-api及dlgg治疗组的死亡率低于肿瘤对照组及dox治疗组。图4b表明dlgg5组合疗法使dox诱导的体重损失减少。单独cr-api或dlgg治疗组经观测无显著的体重损失。数据呈现以平均值±sem,n=8。
图5a至图5c表明cr-api及dlgg抑制小鼠的4t1肿瘤生长具有剂量依赖性。图5a表明癌细胞植入之后每3天量测所有治疗组的肿瘤体积。在观测期(30天)结束时,观测到dox5(p<0.0001)、dox5+dlgg5(p=0.0015)及dlgg25(p=0.0015)治疗小鼠之后的肿瘤体积相较于肿瘤对照组显著减小。图5b表明第30天,收集肿瘤且记录重量。dox5、dox5+dlgg5、cr-api400、dlgg5及dlgg25治疗组的肿瘤重量显著低于肿瘤对照组。图5c显示所有不同治疗组的代表性肿瘤。此外还显示以肿瘤对照组的肿瘤重量为100%的其他处理组所减少肿瘤重量的%(比例条:5mm)。
图6a及图6b表明,cr-api及dlgg疗法减少肿瘤细胞增殖,同时诱导细胞凋亡。图示经以下抗体分别染色且用核指示剂苏木精共染色(浅蓝色)的肿瘤组织的代表性ihc影像:(图6a)ki67(浅棕色)(一种细胞增殖标记蛋白质),及(图6b)裂解半胱天冬酶3(一种细胞凋亡标记蛋白质)(比例条:50μm)。
图7a及图7b表明cr-api及dlgg治疗小鼠减少tnbc对远程肺器官的转移。图7a显示所有治疗组的肺组织的代表性h&e影像。该影像显示转移性肿瘤结节在肿瘤对照组、dlgg5及cr-api200组中可见,但在dlgg25、cr-api400、dox5及dox5+dlgg5组中检测不到。图7b为ihc影像分析显示测试动物的肺中出现ki67高表现的转移性tnbc肿瘤结节(比例条:50μm)。
图8a及图8b表明cr-api及dlgg治疗小鼠减少tnbc对远程肝器官的转移。肝组织中的ki67过度表现细胞的代表性h&e影像(图8a)及ihc分析(图8b)表明肿瘤对照组的肝中存在转移性肿瘤结节,而在化合物或萃取物治疗组中则减少许多。影像中的红色箭头突出显示代表性的ki67过度表现肿瘤结节(比例条:50μm)。
图9a及图9b表明cr-api及dlgg治疗缓解肿瘤或多柔比星(dox)诱导的肺脏及肝脏发炎。经促发炎性cox-2免疫染色的所有组的肝(图9a)及肺(图9b)组织的代表性ihc影像表明dlgg或cr-api治疗减少肿瘤或dox诱导tnbc转移器官部位的发炎(比例条:50μm)。
图10表明cr-api及dlgg治疗负调节肿瘤组织中的癌转移相关信号传导。西方墨点分析结果表明,cr-api或dlgg治疗减弱src/fak信号联级且影响癌细胞的膜重塑及脂质代谢相关蛋白质的表现量。
具体实施方式
本公开提供一种在需要治疗的个体中治疗乳癌及/或治疗乳癌转移的方法,其包含给予该个体有效量的昭和草萃取物及视情况医药上可接受的载剂或赋形剂。
本公开提供昭和草萃取物用于制备治疗乳癌及/或治疗乳癌转移药物的用途。
本公开提供一种治疗乳癌及/或治疗乳癌转移的医药组合物,其包含有效量的昭和草萃取物及视情况医药上可接受的载剂或赋形剂。
本公开提供昭和草萃取物,其用于治疗乳癌及/或治疗乳癌转移。
本公开提供一种在需要治疗的个体中治疗乳癌及/或治疗乳癌转移的方法,其包含给予该个体有效量的如式i所示的化合物:1,2-二-o-α-亚麻酰基-3-o-β-吡喃半乳糖基-sn-甘油、1(2)-o-α-亚麻酰基-2(1)-o-α-亚油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:2)、1(2)-o-α-亚麻酰基-2(1)-o-α-棕榈酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/16:0)、1(2)-o-α-亚麻酰基-2(1)-o-α-油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:1)、1,2-二-o-α-亚麻酰基-3-o-(6-o-α-吡喃半乳糖β-吡喃半乳糖)-sn-甘油、或其医药上可接受的衍生物及视情况医药上可接受的载剂或赋形剂;
其中r1及r2独立为c(o)ra,其中ra为具有0至3个双键的c15-17烷基,及r3为单半乳糖基或二半乳糖基。
本公开提供如式i所示的化合物:1,2-二-o-α-亚麻酰基-3-o-β-吡喃半乳糖基-sn-甘油、1(2)-o-α-亚麻酰基-2(1)-o-α-亚油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:2)、1(2)-o-α-亚麻酰基-2(1)-o-α-棕榈酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/16:0)、1(2)-o-α-亚麻酰基-2(1)-o-α-油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:1)、1,2-二-o-α-亚麻酰基-3-o-(6-o-α-吡喃半乳糖β-吡喃半乳糖)-sn-甘油、或其医药上可接受的衍生物用于制备治疗乳癌及/或治疗乳癌转移药物的用途。
本公开提供一种治疗乳癌及/或治疗乳癌转移的医药组合物,其包含有效量的如式i所示的化合物:1,2-二-o-α-亚麻酰基-3-o-β-吡喃半乳糖基-sn-甘油、1(2)-o-α-亚麻酰基-2(1)-o-α-亚油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:2)、1(2)-o-α-亚麻酰基-2(1)-o-α-棕榈酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/16:0)、1(2)-o-α-亚麻酰基-2(1)-o-α-油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:1)、1,2-二-o-α-亚麻酰基-3-o-(6-o-α-吡喃半乳糖β-吡喃半乳糖)-sn-甘油、或其医药上可接受的衍生物及视情况医药上可接受的载剂或赋形剂。
本公开提供如式i所示的化合物:1,2-二-o-α-亚麻酰基-3-o-β-吡喃半乳糖基-sn-甘油、1(2)-o-α-亚麻酰基-2(1)-o-α-亚油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:2)、1(2)-o-α-亚麻酰基-2(1)-o-α-棕榈酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/16:0)、1(2)-o-α-亚麻酰基-2(1)-o-α-油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:1)、1,2-二-o-α-亚麻酰基-3-o-(6-o-α-吡喃半乳糖β-吡喃半乳糖)-sn-甘油、或其医药上可接受的衍生物,其用于治疗乳癌及/或治疗乳癌转移。
经由参考以下详细说明的本公开各种具体实施例、实例以及化学图和表及其相关描述,可以更容易地理解本发明。应理解,除非在权利要求中另外特别指出,否则本发明不限于特定的制备方法、载体或制剂,或将本公开的萃取物调剂为用于局部、口服或肠胃外的产品或组合物的特定模式,因本发明所属技术领域技术人员很清楚,前述项目当然可以变化。还应理解,本文使用的术语仅用于描述特定具体实施例的目的,而非用以限制。
除非另外指出,否则如本发明所用的以下术语应解释为具有以下含义:
如本文所用的术语“医药学上可接受的衍生物”表示自本发明化合物改质而来,但性质及功效与本公开化合物相同或更好的化合物。医药学上可接受的衍生物优选为本公开化合物的医药学上可接受的盐、溶剂合物、水合物或前药。
本公开的化合物还可以溶剂合物及水合物形式存在。因此,这种化合物可与例如水合水或一个、许多或任何分率的母液溶剂分子一起结晶。这种化合物的溶剂合物及水合物包括在本发明的范围内。
范围在本文中通常表述为“约”一个特定值及/或至“约”另一个特定值。当表述此类范围时,态样为包括一个特定值及/或至另一个特定值的范围。类似地,当值通过使用字“约”表述为近似值时,应了解特定值可形成另一态样。另外应了解,每一范围的各端点均有显著性,一端点与另一端点既有相关性,也彼此独立。
“视情况”或“视情况地”意谓随后所述的事件或状况可能发生或可能不发生,且该描述包括该事件或状况发生的情况及其未发生的情况。举例而言,“视情况包含药剂”意谓该药剂可能存在或可能不存在。
必须指出,除非上下文另外清楚规定,否则如本说明书及随附权利要求中所用的单数形式“一”及“该”包括复数个所指标的物。因此,除非上下文另外需要,否则单数术语应包括复数且复数术语应包括单数。
如本文所用的术语“个体”表示任何动物,优选为哺乳动物,且更优选为人类。个体的实例包括人类、非人类灵长类动物、啮齿动物、天竺鼠、兔、绵羊、猪、山羊、母牛、马、狗及猫。
术语如本文所提供的化合物的“有效量”意谓该萃取物的量足以提供对所需功能的所需调节。如下文所指出,确实的需要量将在个体之间有变化,此视个体的疾病病况、身体状况、年龄、性别、物种及体重、组合物的特性及配方等而定。给药方案可经调整以诱导最佳治疗反应。举例而言,可每日投予若干分次剂量,或可依治疗情形的紧急程度按比例减少剂量。因此,很难指定确实的“有效量”。然而,本发明领域技术人员使用常规实验即可确定适当的有效量。
如本文所用的术语“治疗”表示逆转、减轻或改善此术语所适用的病症或病状、或该病症或病状之一或多种症状,或抑制其进展。
如本文所用的术语“载剂”或“赋形剂”是指自身并不为治疗剂,而是用作用于将治疗剂传递至个体的载剂及/或稀释剂及/或佐剂或媒剂,或添加至调配物中以改善调配物的处理或储存性质或允许或有助于组合物的剂量单位形成适于投予的剂量单位的任何物质。适合的载剂或赋形剂为一般熟习制造医药调配物或食品的通常知识的技术人员所熟知。载剂或赋形剂可包括(举例而言但不限于)缓冲剂、稀释剂、崩解剂、黏合剂、黏着剂、湿润剂、聚合物、润滑剂、滑动剂、为遮蔽或抵消不良味道或气味而添加的物质、调味剂、染料、芳香剂及为改善组合物的外观而添加的物质。可接受的载剂或赋形剂包括柠檬酸盐缓冲剂、磷酸盐缓冲剂、乙酸盐缓冲剂、碳酸氢盐缓冲剂、硬脂酸、硬脂酸镁、氧化镁、磷酸及硫酸的钠盐及钙盐、碳酸镁、滑石、明胶、阿拉伯胶、海藻酸钠、果胶、糊精、甘露糖醇、山梨糖醇、乳糖、蔗糖、淀粉、明胶、纤维素物质(诸如烷酸的纤维素酯及纤维素烷基酯)、低熔点蜡、可可脂、氨基酸、尿素、醇类、抗坏血酸、磷脂、蛋白质(例如血清白蛋白)、乙二胺四乙酸(edta)、二甲亚砜(dmso)、氯化钠或其他盐、脂质体、甘露糖醇、山梨糖醇、甘油或粉末、聚合物(诸如聚乙烯吡咯啶酮、聚乙烯醇及聚乙二醇)、及其他医药学上可接受的物质。载剂不应破坏治疗剂的药理学活性,且在以足以传递治疗量的药剂的剂量投予时应无毒性。
植物化合物调节癌症和免疫细胞代谢中的关键过程,是开发更有效化学治疗剂的丰富资源。其可单独使用或与现有药物组合使用,以增强其有效性或使其副作用最小化。
根据本发明的昭和草(crassocephalumrabens)也可知为c.rabenss.moore、c.rubenss.moore、c.crepidioidess.moore及crassocephalumcrepidioides。如本文中所使用,昭和草植物可为整个植株或其一或多个部位,包含但不限于种子、花、叶、枝干及根。在本发明的一个具体实施例中,该昭和草植物为整个植株。在本发明的另一个具体实施例中,该昭和草植物为种子、花、叶或其任意组合。在本发明的一个优选具体实施例中,该昭和草植物经干燥及粉碎。
根据本发明的昭和草萃取物优选为醇萃取物。优选地,其中该醇为c1至c4醇。本文中所称“c1至c4醇”是指直链或支链、具有取代或不具有取代、一元或多元、饱和或不饱和的醇,优选为不具有取代、一元及饱和醇。在本发明的一个优选具体实施例中,该c1至c4醇为甲醇、乙醇、正丙醇(n-propanol)、异丙醇(isopropanol)、正丁醇、异丁醇(iso-butanol)、仲丁醇(sec-butanol)、叔丁醇(tert-butanol)。尤其优选地,该c1至c4醇为甲醇或乙醇。该c1至c4醇可单独使用或混合多种使用。
于本公开的一个优选具体实施例中,该昭和草萃取物为该醇萃取物的乙酸乙酯亚组份。于本公开的一个更优选的具体实施例中,进一步的纯化如高效液相层析可用于从该醇萃取物或其乙酸乙酯亚组份中分离活性化合物。
在本公开的一个优选具体实施例中,该昭和草萃取物由下述方法所制备,该方法包含将昭和草植物与醇混合以形成第一溶液的方法;从第一溶液中除去醇以获得第二溶液;于该第二溶液中加入乙酸乙酯,并形成有机部分和无机部分(或水部分);将该有机部分分成多个组份;及收集含有半乳糖脂化合物的组份。例如,该有机部分可以在硅胶管柱上以含有二氯甲烷和甲醇的溶液分离,得到含有半乳糖脂化合物的组份。
包含于根据本发明的该昭和草萃取物中的半乳糖脂化合物包括但不限于1,2-二-o-α-亚麻酰基-3-o-β-吡喃半乳糖基-sn-甘油(1,2-di-o-α-linolenoyl-3-o-β-galactopyranosyl-sn-glycerol,dlgg)、1(2)-o-α-亚麻酰基-2(1)-o-α-亚油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:2)[1(2)-o-α-linolenoyl-2(1)-o-α-linoleoyl3-o-β-galactopyranosyl-sn-glycerol(18:3/18:2)]、1(2)-o-α-亚麻酰基-2(1)-o-α-棕榈酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/16:0)[1(2)-o-α-linolenoyl-2(1)-o-α-palmitoyl3-o-β-galactopyranosyl-sn-glycerol(18:3/16:0)]、1(2)-o-α-亚麻酰基-2(1)-o-α-油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:1)[1(2)-o-α-linolenoyl-2(1)-o-α-oleoyl3-o-β-galactopyranosyl-sn-glycerol(18:3/18:1)]及1,2-二-o-α-亚麻酰基-3-o-(6-o-α-吡喃半乳糖β-吡喃半乳糖)-sn-甘油[1,2-di-o-α-linolenoyl-3-o-(6-o-α-galactopyranosyl-β-galactopyranosyl)-sn-glycerol,dgdg]。
该萃取物可包含如式i所示的半乳糖脂化合物:
其中r1及r2独立为c(o)ra,其中ra为具有0至3个双键的c15-17烷基,及r3为单半乳糖基(monogalactosyl)或二半乳糖基(digalactosyl)。于本发明的一个具体实施例中,该单半乳糖机二半乳糖基甘油选自1,2-二-o-α-亚麻酰基-3-o-β-吡喃半乳糖基-sn-甘油、1(2)-o-α-亚麻酰基-2(1)-o-α-亚油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:2)、1(2)-o-α-亚麻酰基-2(1)-o-α-棕榈酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/16:0)、1(2)-o-α-亚麻酰基-2(1)-o-α-油酰基3-o-β-吡喃半乳糖基-sn-甘油(18:3/18:1)及1,2-二-o-α-亚麻酰基-3-o-(6-o-α-吡喃半乳糖β-吡喃半乳糖)-sn-甘油。优选地,该化合物为dlgg。
根据本公开的化合物可通过任何已知方法进一步转化为医药上可接受的衍生物,例如药学上可接受的盐、溶剂合物或前药。
该昭和草萃取物优选包含于萃取组合物中。
根据本发明的该萃取组合物优选为医药组合物、食品组合物或化妆品组合物。
本发明的医药组合物可通过本发明领域中已知的任何方法局部或全身投予,包括但不限于通过肌肉内、皮内、静脉内、皮下、腹膜内、鼻内、经口、黏膜或外部途径投予。适当的投药途径、调配方法及投药时程可由本发明领域技术人员来决定。在本发明中,医药组合物可根据相应投药途径以多种方式调配,诸如液体溶液、悬浮液、乳液、糖浆、锭剂、丸剂、胶囊、持续释放调配物、散剂、颗粒、安瓿、注射液、输注液、套组、软膏、洗剂、擦剂、乳膏或其组合。视情况,其可经灭菌或与任何医药学上可接受的载剂或赋形剂混合,其中有许多医药学上可接受的载剂或赋形剂已为技术人员所知。
本发明所说的外部途径也可称为局部投药,包含但不限于以吹气或吸入投药。局部投药的各类制剂实例包含软膏、乳液、乳霜、凝胶、发泡体,以经皮贴片输送的制剂,吸入或吹气用的粉末、喷雾剂、气溶胶、胶囊或药匣,或滴剂(例如眼睛用或鼻子用滴剂),供雾化用溶液/悬浮液、栓剂、阴道药栓、驻留灌肠剂及咀嚼剂或可吸入的锭剂或药片或脂质或为胶囊制剂。
软膏、乳霜及凝胶可例如配合水性或油性基质,且添加适用增稠剂及/或胶凝剂及/或溶剂调配。该基质因此可包含例如水及/或油,如液态链烷或植物油,如花生油或蓖麻油,或溶剂如聚乙二醇。可依据基质性质使用的增稠剂及胶凝剂包含软质链烷、硬脂酸铝、鲸酰硬脂基醇、聚乙二醇、毛脂肪、蜜蜡、羧基聚亚甲基及纤维素衍生物,及/或单硬脂酸甘油酯,及/或非离子性乳化剂。
乳液可配合水性或油性基质调配,且通常还含有一或多种乳化剂、安定剂、分散剂、悬浮剂或增稠剂。
外涂用粉末可配合任何适用的粉末状基质形成,例如滑石、乳糖或淀粉。滴剂可配合水性或非水性基质调配,且还包括一或多种分散剂、溶解剂、悬浮剂或保存剂。
喷雾组合物可例如调配成水溶液或悬浮液,或调配成自预加压袋输送的气溶胶,如剂量吸入器,且配合使用适用的液化推进剂。适用于吸入用的气溶胶组合物可为悬浮液或溶液,该气溶胶组合物可视情况含有额外的熟知的调配佐药,如接口活性剂例如油酸或卵磷脂及共溶剂例如乙醇。
局部用制剂可通过每天对欲作用的区域施用一或多次投药;且在皮肤区域上优选使用覆盖贴片。可通过黏着剂储存系统持续或延长输送。
根据本发明的化妆品组合物可为水相调配物,其本质上包括水;其还可包含水及与水互溶溶剂的混合物(在25℃为大于50重量%的水互溶力),例如含1至5个碳原子的低碳单醇,如乙醇或异丙醇,含2至8个碳原子的二醇,如丙二醇、乙二醇、1,3-丁二醇、或二丙二醇,c3-c4酮与c2-c4醛,及甘油。该水相调配物优选为水性凝胶或水凝胶调配物的形式。水凝胶调配物包含增稠剂以将液态溶液增稠。增稠剂的实例包括但不限于碳合物、纤维素为主材料、胶、海藻素、瓜尔胶、果胶、鹿角菜苷、明胶、矿物性或经改质矿物性增稠剂、聚乙二醇与多醇、聚丙烯酰胺、及其他的聚合增稠剂。优选为使用对组合物赋与安定性及最适流动特性的增稠剂。
根据本发明的化妆品组合物可为乳液或乳霜调配物的形式。其可含乳化界面活性剂,这些界面活性剂可选自阴离子及非离子界面活性剂。对于界面活性剂的性质及功能(乳化),可参考文件"encyclopediaofchemicaltechnology,kirk-othmer",第22卷,第333-432页,第3版,1979,wiley,对于阴离子及非离子界面活性剂,特别是该参考数据的第347-377页。
优选地,用于本发明组合物的界面活性剂选自:非离子界面活性剂:脂肪酸,脂肪醇,聚乙氧化或聚乙二醇化脂肪醇,如聚乙氧化硬脂醇或鲸蜡基硬脂醇,蔗糖的脂肪酸酯,烷基葡萄糖酯,特别是c1-c6烷基葡萄糖的聚氧伸乙基化脂肪酸酯,及其混合物;阴离子界面活性剂:经胺、氨水或碱盐降低的c16-c30脂肪酸,及其混合物。优选为使用可得到水包油或水包蜡乳液的界面活性剂。
根据本发明的化妆品组合物可进一步包含有效量的生理上可接受抗氧化剂,其选自丁基化对甲酚、丁基化氢醌一甲醚与生育酚。
本发明的组合物可进一步包含天然或改质氨基酸、天然或改质固醇化合物、天然或改质胶蛋白、丝蛋白或大豆蛋白。
本发明的组合物优选为调配成局部应用于角蛋白材料,如皮肤、毛发、睫毛、或指甲。其可为正常用于此型应用的任何表现形式,特别是水性或油性溶液、水包油或油包水乳液、聚硅氧乳液、微乳液或纳米乳液、水性或油性凝胶或液体、浆状或固态水合产物的形式。
本发明通常可为流体且可具有白色或有色乳霜、软膏、乳汁、洗剂、浆液、浆料、慕斯、或凝胶的外观。其可视需要以气溶胶、贴片或粉末的形式局部地应用于皮肤上。其也可为固态形式,例如棒形式。其可作为皮肤用保养产品及/或化妆产品使用。或者,其可调配成洗发精或润丝精。
在已知方式中,本发明的组合物还可含化妆品常用的添加剂及佐剂,如亲水性或亲脂性胶化剂、防腐剂、抗氧化剂、溶剂、香料、填料、颜料、臭味吸收剂、与染料。
根据本发明的食品组合物中,该萃取组合物可在食品制造过程中,添加于常用的食品组合物中(也即可食用的食品或饮品或其前驱物)。几乎所有的食品组合物均可添加根据本发明的该萃取组合物。可添加根据本发明的该萃取组合物的食品组合物包含,但不限于糖果、烘焙食品、冰淇淋、乳制品、甜品及风味小点、小吃、肉类替代产品、快餐食品、汤类、面食、面条、罐头食品、冷冻食品、干制食品、冷藏食品、油脂、婴儿食品、软食物、或面包涂酱或其混合物。
如本文所用,术语“转移”是指癌症从初始或主要部位扩散到一个体内的不同或次要部位。癌细胞可从其最初形成之处扩散到身体的另一部分。在转移中,癌细胞脱离原始(原发)肿瘤,穿过血液或淋巴系统,并在身体的其他器官或组织中形成新的肿瘤。优选地,该昭和草萃取物或包含于该昭和草萃取物中的半乳糖脂化合物有效于治疗乳癌转移至肺或肝。于本公开的一个具体实施例中,经昭和草萃取物或纯半乳糖脂化合物处理后,降低了转移部位(肺和肝)中细胞增殖标记物的表达水平,并呈剂量依赖模式。在本公开的另一个具体实施例中,经昭和草萃取物或纯半乳糖脂化合物处理后,也降低了肝和肺组织中肿瘤转移诱导的发炎。
优选地,昭和草萃取物或包含于昭和草萃取物中的半乳糖脂化合物可有效降低与癌转移相关蛋白质的表达水平,其选自src、fak、rac1、cav-1、cyp2c19和cox-2。于本公开的一个具体实施例中,西方墨点法的结果显示经昭和草萃取物或纯半乳糖脂化合物处理后,降低了对肿瘤微环境感知(src及fak)、膜重组(rac1及cav-1)及生物活性脂质代谢(cyp2c19及cox-2)有关的重要蛋白质的表达。
根据本公开的乳癌为自乳房组织发展的癌症。该乳癌包含乳癌细胞。乳癌细胞的示例包括但不限于er+乳癌细胞、her2+乳癌细胞及er-、pr-与her2-乳癌细胞。
优选地,昭和草萃取物或包含于昭和草萃取物中的半乳糖脂化合物可有效抑制乳癌细胞的增殖。于本公开的一个具体实施例中,与肿瘤控制组相比,经昭和草萃取物或纯半乳醣脂化合物处理后,显著减小了肿瘤体积。再者,于本公开的一个具体实施例中,经昭和草萃取物或纯半乳糖脂化合物处理后,降低了于肿瘤组织中增殖标记物的表达水平,并呈剂量依赖模式。
优选地,昭和草萃取物或包含于昭和草萃取物中的半乳糖脂化合物可有效促进乳癌细胞的细胞凋亡。于本公开的一个具体实施例中,与肿瘤控制组相比,经昭和草萃取物或纯半乳糖脂化合物处理后,增加了于组织中肿瘤细胞凋亡标记物的表达水平。
优选地,昭和草萃取物或包含于昭和草萃取物中的半乳糖脂化合物可有效抑制肿瘤诱导的发炎或转移诱导的发炎。
优选地,昭和草萃取物或包含于昭和草萃取物中的半乳糖脂化合物可有效增加该个体的存活率。于本公开的一个具体实施例中,与抗肿瘤药多柔比星(doxorubicin,dox)处理组及肿瘤控制组(赋形剂处理)相比,昭和草萃取物或纯半乳醣脂化合物增加了肿瘤接种动物的存活率。
于本公开的一个优选具体实施例中,该处理与其他抗癌药剂合并。根据本发明的抗肿瘤药剂示例包括但不限于多柔比星;紫杉烷类(taxanes)或蒽环类抗生素(anthracyclines),例如多西他赛(docetaxel)及环磷酰胺(cyclophosphamide);表柔比星(epirubicin);贝伐单抗(bevacizumab);吉西他滨(gemcitabine);5-氟尿嘧啶(5-fluorouracil);卡培他滨(capecitabine);环磷酰胺;卡铂(carboplatin);顺铂(cisplatin);奥沙利铂(oxaliplatin)或长春碱(vinblastine);优选为多柔比星。
优选地,昭和草萃取物或包含于昭和草萃取物中的半乳糖脂化合物可有效降低该抗癌药剂的副作用。该副作用的示例包括但不限于体重减轻、免疫反应受损、恶病质、疲劳、心肌病和cox-2过度表达。于本公开的一些具体实施例中,低剂量半乳糖脂化合物联合治疗可减弱dox诱导的体重减轻,而单独使用昭和草萃取物或半乳糖脂化合物治疗的组则未观察到明显的体重减轻。此外,远程器官中,因抗癌药剂处理所诱导的cox-2过度表达也因dox和半乳糖脂化合物组合治疗而减弱。
以下实例的提供仅用于说明的目的,并不意图限制本发明的范围。
昭和草萃取
新鲜完整的crassocephalumrabenss.moore(asteraceae)(也称为c.crepidioidess.moore)植物用70%乙醇萃取一周且重复两次。粗萃取物使用配有snap滤筒kp-c18-hs的biotage-flash纯化系统进一步分级分离,且用乙醇水溶液(76%-100%,w/w)溶离。收集cv9至cv12之间的萃取液(cv:滤筒体积)以产生cr-api萃取物。在配有二极管数组检测器(uv/dad)的agilent1100系列hplc系统中,以phenomenexlunac18(2)柱(5μm,250×4.6mm)对cr-api的代谢物进行特征分析。溶离条件使用移动相为等梯度98%甲醇溶离,流量为1ml/min。波长设置在190-400nm范围内且获取210nm代表性层析图。cr-api的代表性柱层析图显示于图1中,其中指数及生物活性化合物dlgg于约15分钟呈现。
dlgg的分离
cr-api萃取物进一步使用制备型rp-hplc(cosmosil,5c18-ar-ii柱,250×20mm)纯化,以收集纯dlgg。dlgg滞留时间为约37分钟(98%甲醇,5ml/min,210nm),且dlgg的纯度(>98%)及结构通过分析型rp-hplc(phenomenexluna5μmc18(2)柱,250×4.6mm)及nmr光谱法[通过brukeravii500nmr仪器测得(数据未展示)]检查。
实例:用于治疗乳癌及/或治疗乳癌转移的昭和草萃取物及半乳糖脂化合物
材料及方法
试剂及抗体
3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四唑鎓溴化物(mtt)及二甲亚砜(dmso)购自sigma-aldrich。用于sds-page的分子量标记物通过使用染色前的蛋白质标记物(bioman,中国台湾台北)估算。使用针对肌动蛋白(millipore)、ki-67、裂解半胱天冬酶-3、src、磷酸基-(419及547)src(abcam)、cav-1(thermoscientific)及cox-2、fak、磷酸基-fak、cyp2c19、rac1(santacruz)的初级抗体。所有其他化学品及溶剂为试剂级或高效液相层析级。
细胞株及培养条件
永生化正常人类乳腺上皮细胞(mcf10a)及乳癌细胞株,包括her2+(skbr3)、er+(mcf7)、三阴性(mda-mb-231)及鼠类tnbc细胞株4t1,获自atcc(usa)。接收原始储备液之后,扩增细胞且在低继代下冷冻。将细胞解冻且在15次继代内使用。细胞在制造商推荐的培养基中、在37℃、增湿的5%co2培育箱中培养,该培养基补充有10%fbs、100个单位/ml青霉素及100mg/ml链霉素。
动物
balb/cbyjnar1雌性小鼠(4周龄)由中国台湾某实验室动物中心(中国台湾台北)供应,且让其任意取用标准实验室膳食及蒸馏水,并保持22±2℃、依12小时亮/暗循环。此研究根据机构准则执行且由中国台湾某机构批准。
细胞存活率分析
将细胞(3×103个细胞/槽)接种于96孔盘中隔夜且处理24小时。通过基于mtt比色分析测定细胞生长。经单独媒剂(0.5%dmso)处理的细胞存活率定义为100%存活率。化合物处理之后的细胞存活率使用下式计算:活细胞数目(%)=[od570(经处理的细胞)/od570(媒剂对照物)]×100。
cr-api及dlgg针对tnbc的活体内作用
来自昭和草的dlgg或富含dlgg的cr-api溶离分针对tnbc的治疗效果使用原位肿瘤模型评估。简言之,小鼠在异氟醚麻醉下,将4t1(鼠类tnbc)细胞(5x106个细胞/100μlpbs及50μl基质胶/小鼠)皮下注射至第四乳腺脂肪垫中。每天监测肿瘤生长及体重。肿瘤在植入后第7天生长至约150mm3尺寸之后,将测试小鼠随机分为不同组(每组8只小鼠)且进行三周化合物治疗方案(图2)。测试小鼠相应地如下分组:假处理对照组(pbso.p.);肿瘤对照组(pbso.p.);每3天以5mg/kg静脉内投与多柔比星(dox5);分别进行的低剂量及高剂量dlgg治疗,每天5及25mg/kg,o.p.(dlgg5及dlgg25);多柔比星及低剂量dlgg组合疗法(dox5+dlgg5);及分别进行的低剂量及高剂量cr-api治疗,每天200及400mg/kg,o.p.(cr-api200及cr-api400)。多柔比星治疗剂量及频率基于动物研究中常用的浓度范围内的最大可耐受剂量,其由内部毒性实验确定(baol,haquea,jacksonk等人,(2011)increasedexpressionofp-glycoproteinisassociatedwithdoxorubicinchemoresistanceinthemetastatic4t1breastcancermodel.theamericanjournalofpathology.2011;178(2):838-852)。通过一周三次监测肿瘤尺寸及体重来评估药物/化合物/萃取物的作用。肿瘤植入后第30天,通过颈椎脱位术进行安乐死。立即收集肿瘤、器官组织(肺、肝、肾脏、脾)及血清且加以分配以用于西方墨点法(立即使用液态氮急骤冷冻且在-80℃下储存)或用于石蜡固定(立即浸没于10%福尔马林溶液中维持至少一周)。石蜡包埋的组织在室温下储存。此动物研究的详细实验设计示于图2中。
组织学及免疫组织化学
将肿瘤及器官组织固定于10%缓冲福尔马林中且包埋于石蜡中。将石蜡包埋的样品切片(6μm)且进行苏木精及曙红(h&e)或免疫组织化学(ihc)染色。使石蜡包埋的组织切片热固着且使用二甲苯脱蜡且在一系列分级乙醇中复水,最后用蒸馏水洗涤。使用柠檬酸盐修复缓冲液及decloakingchamber(biocaremedical)进行抗原修复。使用axiovision软件(carlzeissmicroimaging,inc.)捕捉影像。
西方墨点法
将来自各小鼠的肿瘤组织的总蛋白质(0.1g)在混合球磨机(mm301,retsch,haan,germany)中均质化2分钟,通过添加0.4mlripa溶解缓冲液来萃取且在4℃下以15,000×g离心30分钟。收集上清液,且通过使用dc蛋白质分析套组(bio-rad)来测定样品总蛋白质浓度。通过10%梯度sds-page解析蛋白质且使用增强型化学发光试剂(ecl,amersham)及针对指定蛋白质的抗体进行免疫墨点分析。
资料分析
来源于动物实验的所有资料的定量均以平均值±sem表示。在不能同时完全提供的情况下,提供代表所有治疗组的3-5只小鼠。
结果及讨论
dlgg抑制各种乳癌细胞增殖
首先使用人源mcf10a(正常乳腺上皮细胞)、mcf7(er+乳癌细胞)、skbr3(her2+乳癌细胞)、mda-mb-231(er-、pr-及her2-tnbc细胞)及鼠源4t1tnbc细胞评估cr-api或dlgg的抗增殖作用(图3)。cr-api在mda-mb-231细胞株中的ic50在65μg/ml下达到。对于人源与鼠源tnbc细胞而言,dlgg的ic50为55μm,而其他人源乳癌细胞在测试浓度范围(5-100μm)内均未达到ic50。有趣的是,24小时dlgg治疗之后,未观测到mcf10a的细胞存活率发生显著变化。该结果突出显示了cr-api及dlgg抑制tnbc细胞增殖的功效,而对正常乳腺上皮细胞不具有毒性效应。
在tnbc小鼠模型中,cr-api或dlgg治疗展示的存活率优于dox治疗
探究富含dlgg的cr-api溶离分及纯dlgg化合物对小鼠乳腺4t1原位肿瘤生长及同种移植小鼠中的转移的功效。商业上使用的化学治疗药物多柔比星用作阳性对照物。还使用dlgg及多柔比星进行组合疗法(dox5+dlgg5),以评估dlgg减少多柔比星诱导的副作用的潜力。低(dlgg5)及高(dlgg25)剂量的dlgg及低(cr-api200)及高(cr-api400)剂量的cr-api经口治疗用于评估化合物/萃取物对肿瘤植入动物的剂量依赖性作用。结果表明,在30天治疗期结束时,所有cr-api及dlgg及dox5+dlgg5治疗组中的存活动物百分比显著地高于肿瘤对照组及dox5治疗组(图4a)。dlgg5、dlgg25、cr-api400及dox5+dlgg5疗法获得100%存活率。该结果表明,富含dlgg溶离分或dlgg纯化合物治疗不诱导任何不当的毒性且对肿瘤植入小鼠的总体福祉具有正面影响。其也表明dlgg组合疗法可以在tnbc中缓解多柔比星诱导的体重损失或副作用。
与低剂量dlgg组合疗法缓解多柔比星诱导测试动物体重的损失
在持续治疗期间,每3天记录所有测试动物的体重(图4b)。第30天,观测到相较于所有治疗组,仅dox5治疗组展示显著的体重损失(测试动物初始体重的10%)。此现象在dox5+dlgg5治疗组中减少(p=0.0014),表明dlgg缓解了与多柔比星治疗相关的体重损失。单独cr-api或dlgg治疗组经观测无显著的体重损失。
dlgg及cr-api减小tnbc肿瘤块具剂量依赖性
在整个实验期期间监测所有组的肿瘤负荷(图5a)。所测肿瘤体积在肿瘤对照组与dox5(p<0.0001)、dox5+dlgg5(p=0.0015)或dlgg25(p=0.0015)治疗小鼠之间具有较高的统计差异。还测量所有治疗组的肿瘤重量且与终点时的肿瘤对照组肿瘤重量进行比较(图5b及5c)。相较于肿瘤对照组,dlgg疗法使肿瘤体积显著地且剂量依赖性地减小18%(dlgg5)及47%(dlgg25)(p<0.05)。观测到经dox5及dox5+dlgg5治疗的测试动物的肿瘤重量分别减少60%及62%(p<0.05)。观测到cr-api200及cr-api400疗法分别使肿瘤重量减少12%(p=0.1526)及24%(p=0.0528)。综合而言,该结果表明dlgg以剂量依赖型方式缓解tnbc肿瘤生长。
在肿瘤组织中,cr-api及dlgg疗法减少ki-67表达且增加半胱天冬酶-3表达
为了展现cr-api或dlgg疗法对tnbc肿瘤组织的作用,进行ihc染色。使用ki67(一种细胞增殖标记物)来见证本发明的萃取物是否对肿瘤细胞增殖具有直接作用(图6a)。观测到ki-67过度表达于肿瘤对照组中,其表示快速生长及增殖的细胞。不论使用cr-api或dlgg的剂量,均减少此现象。dox5及dox5+dlgg5治疗动物也存在类似的效果。该结果表明dlgg抑制肿瘤细胞增殖且可能会有效地阻滞tnbc的肿瘤生长。
使用裂解半胱天冬酶-3(一种细胞凋亡标记物)的表达量测试化合物疗法对肿瘤组织细胞的细胞凋亡的作用(图6b)。相较于媒剂对照组,所有治疗组均展示裂解半胱天冬酶-3的表达增加。值得注意的是,dox5、cr-api400及dlgg25治疗组中,半胱天冬酶-3表达高于低剂量疗法及dox5+dlgg5组合疗法。该结果表明,cr-api或dlgg疗法诱导tnbc肿瘤发生细胞凋亡,类似于多柔比星疗法的细胞凋亡效应。该结果为cr-api或dlgg作为肿瘤生长抑制剂的重要指标。
cr-api及dlgg治疗抑制肿瘤远程转移至肺及肝脏
在肿瘤对照组中,可检测到自发的肿瘤肺及肝脏转移。因此对两种器官中的ki-67使用h&e及ihc染色,以确定高增殖或转移癌细胞在肿瘤对照小鼠及化合物治疗小鼠的这种远程脏器转移位点的存在。如图7及8中所见,相较于肿瘤对照组,经dox5、dox5+dlgg5、dlgg5与dlgg25、或cr-api200与cr-api400治疗的小鼠的肺及肝组织中的肿瘤转移结节较少。该结果表明,dlgg或cr-api治疗抑制tnbc肿瘤转移且类似于多柔比星的作用。
cr-api及dlgg疗法抑制肿瘤或多柔比星诱导的肺脏及肝脏发炎
肿瘤组织及肝及肺器官中的促炎性cox-2表现总体增加表示发炎加强,此可能加剧肿瘤生长及转移或作为其他潜在副作用的指标(minnja,guptagp,siegelpm等人,(2005)genesthatmediatebreastcancermetastasistolung.nature436(7050):518-524;chiangac及massaguej.(2014)molecularbasisofmetastasis.nengljmed359(26):2814-2823)。比较测试动物的肝(图9a)及肺(图9b)组织中的cox-2蛋白质表达量。dlgg或cr-api治疗组的动物器官中的cox-2表达依药物剂量依赖性的方式减少,并类似于假处理对照组的表达量。另一方面,并观测到dox5治疗法进一步诱导该器官中的cox-2表达。有趣的是,在dox5+dlgg5组合治疗组中,cox-2表达减少且类似于单独dlgg5或cr-api200疗法的表达量。该结果表明dlgg或cr-api疗法抑制可能容易发生tnbc转移的器官发炎。另外,该结果表明,dlgg疗法减少与多柔比星疗法相关的全身/多器官发炎。
cr-api及dlgg减少tnbc肿瘤中的转移相关蛋白质的表达
使用西方墨点分析来探究支持dlgg或富含dlgg的萃取物如何减少肿瘤组织的tnbc转移的可能机制(图10)。分析发炎标记物cox-2及肿瘤中的生物活性脂质代谢标记物cyp2c19(panigrahyd,kaipainena,greeneer,huangs.(2015)cytochromep450-derivedeicosanoids:theneglectedpathwayincancer.cancermetastasisreviews29(4):723-735)。对于所有dlgg及cr-api治疗组而言,观测到使这两种蛋白质表达量减少具有剂量依赖性作用。相较于单独dox5治疗组,组合疗法dox5+dlgg5也使该蛋白质的含量减少。该结果表明,dlgg可以抑制肿瘤组织中的受cyp2c19或cox-2催化衍生的代谢物而影响促炎性肿瘤概貌,该代谢物导致其抗增殖及抗转移效应。另外,还检查膜重塑及微环境感测蛋白质的表达量。在dlgg、cr-api、dox5及dox5+dlgg5高剂量治疗中,cav-1及rac1(细胞迁移及囊泡形成中的两种重要作用因子)(diazj,mendozap,silvap,questaf,torresva.(2014)anovelcaveolin-1/p85α/rab5/tiam1/rac1signalingaxisintumorcellmigrationandinvasion.communintegrbiol7(5):e972850)表达量显著减少。另外,相较于肿瘤对照组,在dox5+dlgg5组中,所有dlgg及cr-api疗法均使src(p-src419)活化受到显著抑制;在dox5治疗组中检测到的效应少得多或根本检测不到效应。高剂量的dlgg、cr-api、dox5及dox5+dlgg5疗法使fak磷酸化受到显著抑制。综合而言,该结果表示dlgg及cr-api通过抑制促炎性肿瘤微环境、膜重塑及肿瘤微环境感测来缓解肿瘤转移。
虽然已经参考本公开的具体实施例描述和说明了本公开,但是这些描述和说明非为限制性。本发明所属技术领域技术人员应该理解,在不脱离由权利要求限定的本公开的真实精神和范围情况下,可以进行各种改变并且可以替换等同物。附图可能不一定按比例绘制。由于制造工艺和限度,本公开中的技艺再现与实际装置之间可能存在区别。可能存在未具体示出的本公开的其他实施例。说明书和附图应被视为说明性的而非限制性的。可以进行修改以使特定情况、材料、物质组成、方法或过程适应本公开的目的、精神和范围。所有这些修改都在权利要求的范围内。尽管已经参考以特定顺序执行的特定操作描述了本文公开的方法,但是应当理解,可以组合、细分或重新排序这些操作以形成等效方法而不悖离本发明的教导。因此,除非在此具体指出,否则操作的顺序和分组不成为本公开的限制。
- 还没有人留言评论。精彩留言会获得点赞!