包含高山蒿提取物的组合物的制作方法
本发明涉及包含高山蒿提取物的组合物。
背景技术:
:应激(Stress),被称作所有现代疾病的原因,是指:当某种程度或更高程度的刺激(不管刺激的种类是什么)以有害的方式作用于身体、对身体构成威胁时,作为对该威胁的应答的非特异性一般适应综合征(Selye,H.:Thestressoflife,Toronto,LongnansGreenandCo.,pp.1-50,1958)。应激的原因主要包括(1)身体因素:过度劳累,睡眠不足,创伤,中毒等;(2)外部因素:自然环境,文化情况,家庭或工作场所的人际关系等;和(3)内部因素:人格,生活中的心理冲突,婴儿或儿童经历的精神创伤等当应激持续很长时间时,它可能引起身体疾病,例如心脏病,胃溃疡和高血压或心理失调,例如失眠,神经症和抑郁症。此外,它可能引起其他疾病,因为身体的生理活性和免疫活性降低,并且身体的体内平衡受到不利影响。在充满冲突和竞争的现代社会中,大多数人在身体/精神上受到更多的压力,因为他们必须适应结构或功能上复杂变化的社会。由应激引起的免疫活性的降低可能导致皮肤稳态的破坏,这继而可削弱保护皮肤免受有害外部因素的皮肤保湿和屏障功能。技术实现要素:技术问题本发明在于提供一种具有维持皮肤稳态的优异效果的组合物。技术方案在一个方面,本发明提供一种用于维持皮肤稳态的组合物,其包含作为活性成分的属于蒿属的高山蒿(Artemisiaumbelliformis)提取物。有益效果本发明的用于保持皮肤稳态的组合物包含作为活性成分的高山蒿(Artemisiaumbelliformis)提取物,其表现出降低NK1R(神经激肽1受体)和EDN1(内皮素1)基因的表达的效果,且减少EDN1量及针对P物质的抗应激效应的效果。因此,由于这些效果,本发明的组合物可有利于维持皮肤稳态和抗应激效应,从而可广泛用于外用于皮肤、药物组合物和化妆品组合物的剂型,因为是安全的,且对细胞没有负面影响。附图说明图1显示了分析根据本发明的一方面的高山蒿提取物对NK1R和EDN1基因的表达的影响的结果。图2显示了分析根据本发明的一方面的高山蒿提取物对EDN1量的影响的结果。具体实施方式2014年4月4日提交的韩国专利申请号10-2014-0040526的全部内容并入本发明中。此外,本申请主张韩国专利申请号10-2014-0040526的优先权,其全部内容通过引用并入本文。在下文中,将详细描述本发明的具体实施例,使得本发明本领域技术人员可以容易地实施本发明。在本发明的一个方面,已知神经肽P物质与情绪障碍、焦虑、压力、疼痛、呕吐等的调节相关。因此,如果能够控制由P物质诱导的因子,则其可以防止由免疫活性中的应激诱导的降低所引起的皮肤稳态的下降。在本发明的一个方面,P物质可以具有以下氨基酸序列和以下化学式。P物质的氨基酸序列:ArgProLysProGlnGlnPhePheGlyLeuMet(RPKPQQFFGLM)。【化学式】已知,P物质的浓度增加导致其受体NK1R(神经激肽1受体,也称为P物质受体(SPR)或速激肽受体1(TACR1))及其蛋白质的表达增加。NK1R的信号传导刺激ECE1(内皮素转化酶1),从而增加活化的EDN1(内皮素1)基因及其蛋白的表达。因为物质P增加NK1R和EDN1基因的表达,所以能够抑制两种基因表达的物质预期抑制物质P的活性,并且通过抑制生理性压力引起的效应。此外,由于NK1R信号传导,细胞中活化的EDN1的增加可能导致黑素细胞产生的黑色素增加。因此,可预期当EDN1的表达被抑制时,可以维持皮肤平衡,因为可以抑制和抑制细胞中的黑色素生成,并且可以治疗、改善或预防由诸如色素沉着的黑色素生成引起的皮肤疾病。在一方面,本发明可涉及包含作为活性成分的高山蒿(Artemisiaumbelliformis)提取物的组合物。具体地,在本发明的一个方面,所述组合物可以是用于维持皮肤稳态的组合物。根据本发明的一个方面的组合物可以是药物、食品或化妆品组合物。具体地,在本发明的一个方面,根据本发明的组合物可以是用于极端施用于皮肤的组合物。在本发明的一个方面,术语“皮肤稳态”可以表示皮肤的环境或生理条件,例如pH,温度,血流量,水含量等被连续地保持为正常状态。一方面,本发明可以涉及维持皮肤稳态的方法,其包括向需要维持皮肤稳态的受试者施用高山蒿提取物。具体地,可以通过本发明中描述的施用方法来实现施用。在一方面,本发明可以涉及高山蒿提取物用于维持皮肤稳态的用途。在一方面,本发明可涉及用于维持皮肤稳态的高山蒿提取物。在一方面,本发明可涉及用于抗应激的组合物或用于减少应激物的组合物,其包含作为活性成分的高山蒿提取物。具体地,在本发明的一个方面,应激物可以是物质P.在一个方面,本发明可以涉及用于对抗应激或减少应激物的方法,其包括向需要抗应激或减轻应激物的受试者给药高山蒿提取物。具体地,可以通过本发明中描述的给药方进行给药。在一方面,本发明可以涉及高山蒿提取物在抗应激或减轻应激物中的用途。在一个方面,本发明可以涉及用于抗应激或减轻应激物中的高山蒿提取物。在一个方面,本发明可涉及用于增强皮肤免疫功能、皮肤保湿功能或皮肤屏障功能的组合物,其包含作为活性成分的高山蒿提取物。在一个方面,本发明可以涉及用于增强皮肤免疫功能、皮肤保湿功能或皮肤屏障功能的方法,其包括向需要增强皮肤免疫功能、皮肤保湿功能或皮肤屏障功能的受试者给药高山蒿提取物。具体地,可以通过本发明中描述的给药方进行给药。在一方面,本发明可涉及高山蒿提取物在增强皮肤免疫功能、皮肤保湿功能或皮肤屏障功能的用途。在一方面,本发明可涉及应用于增强皮肤免疫功能、皮肤保湿功能或皮肤屏障功能中的高山蒿提取物。在一方面,本发明可以涉及用于抑制神经肽物质P的活性的组合物,其包含作为活性成分的高山蒿提取物。在一个方面,本发明可以涉及抑制神经肽物质P的活性的方法,其包括向需要抑制神经肽物质P的活性的受试者给药高山蒿提取物。具体地,可以通过本发明中描述的给药方法进行给药。在一方面,本发明可涉及高山蒿提取物用于抑制神经肽物质P的活性的用途。在一方面,本发明可涉及应用于抑制神经肽P物质的活性中的高山蒿提取物。在一个方面,本发明可涉及用于抑制NK1R(神经激肽1受体,也称为P物质受体(SPR)或速激肽受体1(TACR1))(ACCESSION:NM_001058)基因或EDN1(内皮素1)(ACCESSION:NM_001168319)基因或用于减少EDN1的量,其包含作为活性成分的高山蒿提取物。在一个方面,本
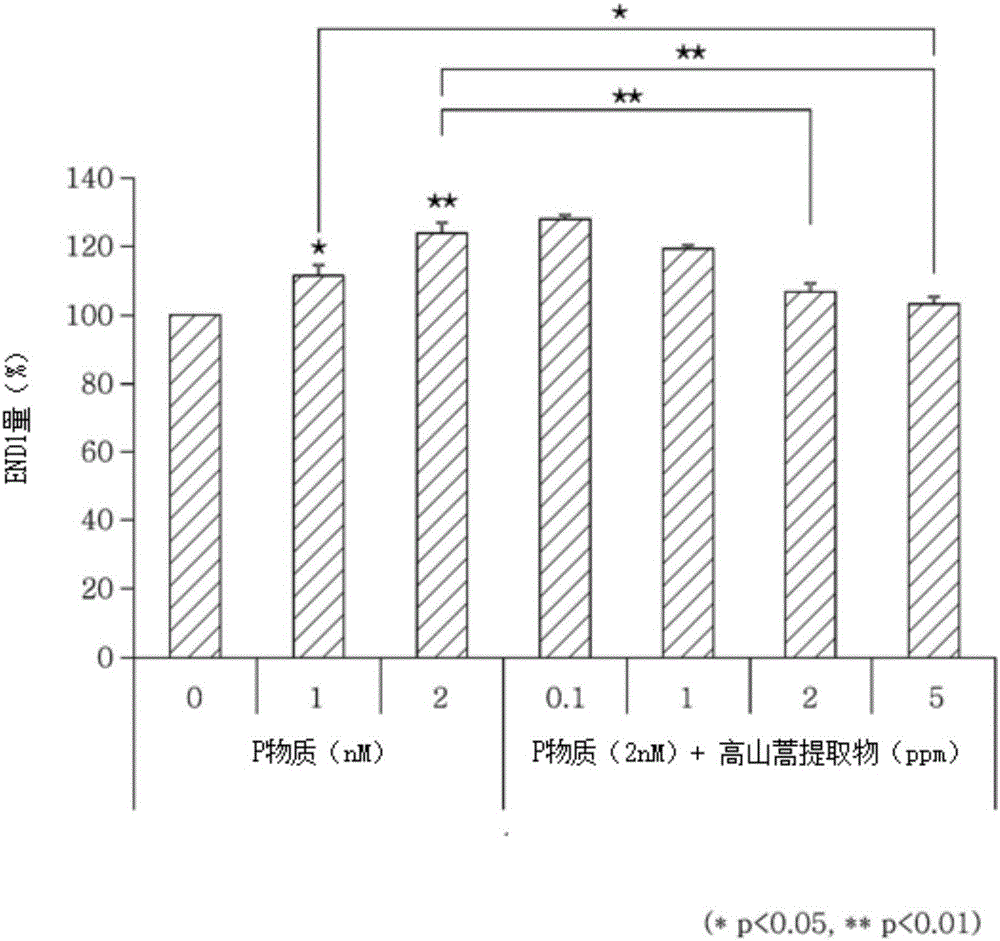
发明内容可以涉及用于抑制NK1R基因或EDN1(内皮素1)基因的表达或减少EDN1的量的方法,其包括向有需要抑制NK1R基因或EDN1基因的抑制或减少EDN1的量的受试者给药高山蒿提取物。具体地,可以通过本发明中所描述的给药方法来进行给药。在一方面,本发明可以涉及高山蒿提取物在抑制NK1R基因或EDN1(内皮素1)基因的表达或减少EDN1的量的用途。在一方面,本发明可涉及在抑制NK1R基因或EDN1(内皮素1)基因的表达或减少EDN1的量中使用的高山蒿提取物。在本发明的一个方面,包含其的组合物中的高山蒿提取物的浓度可以为基于组合物总体积的0.1-10ppm,但不限于此。具体地,在本发明的一个方面中,包含所述提取物的组合物中的高山蒿提取物的浓度基于组合物的总体积可以为0.01ppm或以上、0.1ppm或以上、0.5ppm或以上、0.6ppm或以上、0.7ppm或以上、0.8ppm或以上、0.9ppm或以上、1.0ppm或以上、1.3ppm或以上、1.5ppm或以上、1.7ppm或以上、2.0ppm或以上、2.3ppm或以上、2.5ppm或以上、2.7ppm或以上、3.0ppm或以上、3.5ppm或以上、4.0ppm或以上、4.1ppm或以上、4.2ppm或以上、4.3ppm或以上、4.4ppm或以上、4.5ppm或以上、4.6ppm或以上、4.7ppm或以上、4.8ppm或以上、4.9ppm或以上、5ppm或以上、5.2ppm或以上、5.4ppm或以上、5.6ppm或以上、5.8ppm或以上、6.0ppm或以上、6.5ppm或以上、7.0ppm或以上、7.5ppm或以上、8.0ppm或以上、9.0ppm或以上、10.0ppm或以上、11.0ppm或以上、12.0ppm或以上、50ppm或以上、100ppm或以上、500ppm或更高或1000ppm或以上、但不限于此,并且可以为2000ppm或以下、1000ppm或以下、500ppm或以下、100ppm或以下、50ppm或以下、40ppm或以下、30ppm或以下、20ppm或以下、15.0ppm或以下、10.0ppm或以下、8.0ppm或以下、6.0ppm或以下、5.8ppm或以下、5.6ppm或以下、5.4ppm或以下、5.2ppm或以下、5.0ppm或以下、或以下、4.6ppm或以下、4.4ppm或以下、4.2ppm或以下、4.0ppm或以下、3.7ppm或以下、3.5ppm或以下、3.3ppm或以下、3.0ppm或以下、2.8ppm或以下、或以下、2.4ppm或以下、2.2ppm或以下、2.0ppm或以下、1.8ppm或以下、1.6ppm或以下、1.4ppm或以下、1.2ppm或以下、1.0ppm或以下、0.8ppm或以下、或以下、0.3ppm或更低或0.1ppm或以下。在本发明的一个方面,所述高山蒿可以是选自植物高山蒿的叶、花、茎和根中的一种或多种。在本发明的一个方面,所述高山蒿提取物可以通过包括以下步骤的方法制备:(1)用水、有机溶剂或其组合提取高山蒿的步骤。在本发明的一个方面,所述方法可以在步骤(1)之前进一步包括对高山蒿进行加工的步骤。具体地,所述加工可以是干燥和粉碎高山蒿。然而,不限于此,可包括用于促进提取的任何处理。具体地,干燥可以是日光干燥、热空气干燥、蒸发干燥、喷雾干燥或冷冻干燥,更具体为热空气干燥。另一方面,在本发明的一方面,可以直接提取生的高山蒿,而不进行任何处理。在本发明的一个方面,所述方法可以进一步包括在萃取之后通过蒸馏除去溶剂的步骤。具体地,所述蒸馏可以是真空蒸馏。在本发明的一个方面,所述方法可以进一步包括在蒸馏后向所得浓缩物中加入一种或多种甘油和防腐剂的步骤。在本发明的一个方面,所述方法可以进一步包括在除去溶剂之后或在添加甘油和防腐剂中的一种或多种之后进行过滤的步骤。在本发明的一个方面,所述高山蒿(Artemisiaumbelliformis)提取物可以是选自水、有机溶剂及其混合物中的一种或多种的提取物。具体地,在本发明的一个方面中,有机溶剂可以是选自C1-C6低级醇、丁二醇和丙二醇中的一种或多种溶剂。更具体地,所述低级醇可以是乙醇。用于本发明的黑素细胞可以是PCT/KR2012/007815或韩国专利申请10-2011-0099728(角质形成细胞适应性黑素细胞,KaMC)中公开的黑素细胞。本发明中使用的黑素细胞可以是根据所述参考文献中公开的方法和程序获得的那些,并且还可以根据所述参考文献中公开的方法进行培养。黑色素细胞在布达佩斯条约下于2011年9月14日保藏于韩国生物科学和生物技术研究所的韩国典型菌种保藏中心(KCTC),保藏号为KCTC12015BP。在本发明中,“皮肤”是指覆盖生物体表面的器官。它由表皮,真皮和皮下脂肪层组成,并且以最广泛的概念使用,不仅包括覆盖身体的面部或整个外部部分的组织,而且包括头皮和头发。在本发明中,也称为白皮蠹或GenepiBlanco的“高山蒿(Artemisiaumbelliformis)”是指菊科(Asteraceae)蒿属的草本。高山蒿用于生产Genepi酒,且其叶子用于茶或调味品的制备。在本发明中,“提取物”是指从天然产物提取的物质,不管提取方法,提取溶剂,提取的组分或提取物的类型,其以广义概念使用,包括任何物质,其通过加工或处理从天然产物提取的物质而获得。具体地,加工或处理可以是发酵或酶处理提取物。因此,在本发明中,提取物以广义概念使用,包括发酵产物,浓缩物和干燥产物。具体地,在本发明中,提取物可以是发酵产物。在本发明中,“高山蒿提取物”包括通过提取高山蒿而获得的任何物质,不论其提取方法、提取溶剂、提取的组分或提取物的类型。它包括通过包括用热、酸、碱、酶等处理的提取方法来获得的物质,并且以广泛的概念使用,包括可以从高山蒿中通过加工或处理所提取的物质而获得的任何物质。具体地,加工或处理可以是发酵或酶处理高山蒿的提取物。因此,本发明的高山蒿提取物可以是发酵产物。在本发明的一个方面,“高山蒿(Artemisiaumbelliformis)”可以是提取物,活高山蒿、活高山蒿的粉碎产物,活高山蒿的干燥产物、活高山蒿的干燥粉碎产物或高山蒿的发酵产物,但不限于此。并且,本发明中使用的高山蒿不限于如何获得。它可以是栽培的或商购的。此外,可以使用其面积部分或根部分的全部或部分。更具体地,可以使用选自植物高山蒿的叶、茎、根和花的一种或多种。本发明的高山蒿不一定干燥,并且可以是任何形式,只要可以充分提取高山蒿的活性成分即可。在本发明的一个方面,水包括蒸馏水或纯化水,并且有机溶剂包括选自如C1-C5低级醇的醇、丙酮、醚、乙酸乙酯、乙醚,乙基甲基酮和氯仿中的一种或多种,但不限于此。在本发明的一方面,所述高山蒿提取物可以包含高山蒿的C1-C6醇提取物。具体地,所述醇可以是甲醇或乙醇。在本发明的一个方面,所述高山蒿(Artemisiaumbelliformis)提取物可以根据包括通过用水、有机溶剂或其混合物提取高山蒿(Artemisiaumbelliformis)的步骤的方法获得。在本发明的一个方面,所述高山蒿(Artemisiaumbelliformis)提取物可以是选自水、有机溶剂及其组合的溶剂的粗提取物。有机溶剂可以是C1-C6醇。具体地,C1-C6醇可以是甲醇或乙醇。在本发明的一个方面,当用溶剂提取高山蒿时,所加入的溶剂的量可以是高山蒿量的5-15倍。具体地,可以以高山蒿(艾蒿)的10倍的量加入所述溶剂,但不限于此。在本发明的一个方面,提取可以通过热水提取、乙醇提取、加热提取、冷提取、回流提取、回流冷凝提取、超声波提取等来进行。本领域技术人员已知的任何提取方法可无限制地使用。具体地,可以通过热水提取或乙醇提取进行提取。在本发明的一个方面,提取可以在室温下进行。然而,为了更有效的提取,其可以在升高的温度下进行。具体地,提取可以在约40-100℃,更具体地在约80℃进行,但不限于此。提取可进行约2-14小时,具体为约8-14小时,更具体为约11-13小时,最具体为12小时。然而,提取时间不限于此,并且可以根据诸如提取溶剂、提取温度等条件而变化。提取可以进行多于一次,以获得更大量的活性成分。提取可以连续进行1-5次,更具体地3次,并且所得提取物可以组合用于进一步使用。在本发明的一个方面,所述高山蒿(Artemisiaumbelliformis)提取物可以包含如上所述的高山蒿(Artemisiaumbelliformis)的粗提取物,并且还可以包含具有低极性的有机溶剂的可溶性馏分,其通过用有机溶剂进一步提取粗提取物而获得。在本发明的一个方面,有机溶剂可以是己烷、二氯甲烷、乙酸乙酯、正丁醇等,但不限于此。提取物或提取物的可溶性馏分可以直接使用,过滤然后浓缩来使用,或者在浓缩和干燥后使用。在本发明的一方面,干燥可以是蒸发干燥,喷雾干燥或冷冻干燥。具体地,冷冻干燥可以在-50至-70℃进行3-4天。根据本发明的一方面的化妆品组合物的剂型没有特别限制,但可以根据目的适当地选择。例如,可以将组合物制备成选自以下剂型中的一种或多种剂型:化妆水、柔肤水、爽肤水、收敛水、乳液、保湿乳液、滋养乳液、按摩霜、滋补霜、保湿霜、护手霜、粉底、精华液、滋养精华、面膜、香皂、清洁泡沫、清洁洗剂、清洁霜、身体乳液和身体清洁剂,但不限于此。当根据本发明的化妆品组合物被制备成糊剂、霜剂或凝胶时,可将动物纤维、植物纤维、蜡、石蜡、淀粉、黄芪胶、纤维素衍生物、聚乙二醇、硅酮、膨润土、滑石、氧化锌等用作载体组分。当根据本发明的化妆品组合物被制备成粉末或喷雾剂时,可将乳糖、滑石、二氧化硅、氢氧化铝、硅酸钙或聚酰胺粉末用作载体组分。特别地,当被制成喷雾剂时,其可以进一步包含推进剂,例如氯氟烃、丙烷/丁烷或二甲醚。当根据本发明的化妆品组合物被制成溶液或乳液时,可将溶剂、增溶剂或乳化剂用作载体组分。例如,可以使用水、乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苄酯、丙二醇、1,3-丁二醇油、甘油脂肪酸酯、或聚乙二醇或脱水山梨醇的脂肪酸酯。当根据本发明的化妆品组合物被制成悬浮液时,作为载体成分可以使用如水、乙醇或丙二醇的稀释剂、如乙氧基化异硬脂醇、聚氧乙烯山梨醇酯和聚氧乙烯脱水山梨醇酯的悬浮剂、微晶纤维素、偏氢氧化铝、膨润土、琼脂,黄蓍胶等。当根据本发明的化妆品组合物被制成含表面活性剂的清洁剂时,可将脂肪醇硫酸盐、脂肪醇醚硫酸盐、磺基琥珀酸单酯、羟乙基磺酸盐、咪唑啉衍生物、甲基牛磺酸盐、肌氨酸盐、脂肪酸酰胺醚硫酸盐、烷基酰胺基甜菜碱、脂肪醇、脂肪酸甘油酯、脂肪酸二乙醇酰胺、植物油、羊毛脂衍生物、乙氧基化甘油脂肪酸酯等用作载体成分。除了高山蒿(Artemisiaumbelliformis)提取物之外,根据本发明的化妆品组合物还可以包含功能性添加剂和常用于化妆品组合物中的成分。功能性添加剂可以包括选自水溶性维生素、油溶性维生素、多肽、多糖、鞘脂和海藻提取物的物质。如有需要,本发明的化妆品组合物除了包含功能性添加剂之外还可以包含常用于化妆品组合物中的成分。进一步所包含的成分的例子可以包括油、脂肪、湿润剂、润肤剂、表面活性剂、有机或无机颜料、有机粉末、UV吸收剂、防腐剂、灭菌剂、抗氧化剂、植物提取物、pH调节剂、醇、着色剂、香料、血液循环促进剂、清凉剂、止汗剂、纯净水等。本发明还涉及皮肤外用组合物,其包含作为活性成分的高山蒿(Artemisiaumbelliformis)提取物。皮肤外用组合物是指可以从皮肤外部施用的任何类型的组合物,且其中可以包括各种类型的化妆品。根据本发明的药物组合物可以是各种口服或肠胃外剂型的形式。当将所述组合物制成剂型时,使用常用的稀释剂或赋形剂,例如填充剂、增量剂、粘合剂、润湿剂、崩解剂、表面活性剂等。用于口服给药的固体剂型包括片剂、丸剂、粉剂、颗粒剂、软或硬胶囊等,并且这些固体剂型可以通过与至少一种赋形剂如淀粉、碳酸钙、蔗糖、乳糖、明胶等混合制备。除了简单赋形剂之外,还可以使用润滑剂如硬脂酸镁、滑石等。用于口服给药的液体剂型的例子包含悬浮液、内部使用的液体、乳剂、糖浆等。除了通常使用的简单稀释剂如水和液体石蜡之外,还可以包含各种赋形剂,例如保湿剂、甜味剂、芳香剂、防腐剂等。用于肠胃外给药的剂型包括灭菌水溶液、非水溶液、悬浮液、乳液、冻干产品和栓剂。非水溶液或悬浮液可以包含丙二醇、聚乙二醇、植物油如橄榄油、可注射的酯如油酸乙酯等。作为栓剂的基质,可以使用witepsol、聚乙二醇、吐温61、可可脂、月桂油、甘油明胶等。本发明的组合物可以包含所述活性成分的药学上可接受的盐,并且可以单独使用或与另一种药学活性化合物组合使用。所述盐没有特别限制,只要其是药学上可接受的盐即可。例如,可以使用盐酸、硫酸、硝酸、磷酸、氢氟酸、氢溴酸、甲酸、乙酸、酒石酸、乳酸、柠檬酸、富马酸、马来酸、琥珀酸、甲磺酸、苯磺酸、甲苯磺酸、萘磺酸等的盐。本发明的组合物可以根据所期望的目的进行胃肠外或口服给药。每日给药剂量可以为0.1-500mg/kg/体重,特别是1-100mg/kg/体重,每天给药一次或几次。特定患者的给药剂量可以根据患者的体重、年龄、性别和健康状况、饮食、给药时间、给药方法、排泄率、疾病的严重程度等而有所改变。根据常用方法,本发明的药物组合物可以配制成任何药学上合适的形式,可包括:口服剂型,例如粉末、颗粒剂、片剂、软或硬胶囊、悬浮剂、乳剂、糖浆、气溶胶等;皮肤外用剂型,例如软膏、霜剂等;栓剂、注射剂、注射用无菌溶液等。具体地,本发明的药物组合物可以被制成施用于皮肤外部的注射剂或剂型。本发明的组合物可以经由包括胃肠外途径和口服途径等各种途径给包括大鼠、小鼠、牛、人等的哺乳动物进行给药。可以预期所有类型的给药。例如,其可以口服给药、经皮给药、直肠给药、静脉内给药、肌内给药、皮下给药、宫内给药或脑室内给药。根据本发明的组合物可以通过本领域技术人员容易选择的多种途径进行给药。特别地,根据本发明的药物组合物可作为皮肤外用剂型施用于皮肤上。在本发明的一个方面,所述食品组合物可以是保健功能性食品组合物。根据本发明的食品组合物的剂型没有特别限制。例如,其可以配制成片剂、颗粒剂、粉末、液体如饮料、焦糖、凝胶、棒剂等。每种剂型的食品组合物除了包含活性成分外,还包含本领域中通常使用的成分,这些成分的可以由本领域的技术人员毫无困难地进行选择。在这种情况下,可以实现协同效应。在根据本发明的食品组合物中,在本领域技术人员的水平内可以确定活性成分的给药剂量。例如,每日剂量可以是0.1-5000mg/kg/天,更具体为50-500mg/kg/天。然而,不限于此,施用剂量可以根据各种因素而变化,例如受试者的年龄和健康状况,并发症的存在等。例如,根据本发明的食品组合物可以是各种食品,例如口香糖、焦糖、糖果、冰棒、糖果等、饮料如软饮料、矿泉水、酒精饮料、或包含维生素、矿物质等的健康功能性食品。此外,根据本发明的食品组合物可以包含各种营养素、维生素、矿物质(电解质)、包含合成和天然香料的风味剂、着色剂、增量剂(干酪,巧克力等)、果胶酸及其盐、藻酸及其盐、有机酸、保护性胶体增稠剂、pH调节剂、稳定剂、防腐剂,甘油、醇、碳酸饮料中使用的碳酸化剂等。此外,本发明的功能性食品组合物可包含用于制备天然果汁、果汁饮料和蔬菜饮料的果肉。这些成分可以单独使用或组合使用。这些添加剂的含量不是很重要。通常,将本发明的组合物按100重量份计,它们的含量在约0-20重量份的范围内。在下文中,将通过实施例和试验实施例详细描述本发明。然而,以下实施例和测试实施例仅用于说明目的,本发明的范围不受实施例和测试实施例的限制。[实施例1]高山蒿(Artemisiaumbelliformis)提取物的制备收割高山蒿的花,用热空气干燥并粉碎成粉末。所得粉末用乙醇/水溶液提取,然后通过真空蒸馏除去乙醇。在向所得浓缩物中加入甘油和防腐剂后,通过过滤获得高山蒿。从DSMNutritionalProductsLtd.(4002Basel,Switzerland)购买根据上述方法制备的高山蒿提取物(ArtemisaAO),用于以下试验实施例。[测试实施例1]基因表达测定(1)细胞培养在37℃的5%CO2培养箱中,在6孔板中的人黑素细胞生长补充剂(HMGS;GibcoBRL,NY,USA)的M-254培养基(GibcoBRL,NY,USA)内,培养被保藏在韩国典型菌种保藏中心中的黑素细胞(KCTC)(KCTC12015BP),每隔一天更换培养基,直到细胞占据板面积的95%(95%融合)。(2)提取物的处理当6孔板上的黑素细胞密度达到约80%(80%融合)时,将它们与2nM的应激诱导P物质(BachemFechemikalien,Bubendorf,Switzerland)或不同浓度(0,0.1,1,2和5ppm)的实施例1的高山蒿提取物一起孵化共5天。未用P物质或实施例1的高山蒿提取物处理的细胞用作对照组。(3)RNA的提取和定量在从6孔板上培养的黑素细胞中去除培养基后,用冷的磷酸盐缓冲盐水(PBS)洗涤细胞2次并完全去除剩余的水。待向细胞中加入1mLTRIzol试剂(Invitrogen,CA,USA)并收集所有细胞后,将细胞与200μL氯仿充分混合并在室温下保持5分钟。然后,在4℃和12,000rpm下离心15分钟后,将透明上清液转移至新管中,与相同体积的异丙醇(Sigma-Aldrich,St.Louis,USA)充分混合,并在室温下保持10分钟。在4℃和12,000rpm下再次离心10分钟后,弃去上清。向剩余的颗粒中加入1mL的100%EtOH(Sigma-Aldrich,St.Louis,USA)并轻微洗涤后,在4℃和12,000rpm下离心5分钟。在再次加入1mL的70%EtOH并洗涤后,在4℃和12,000rpm下离心5分钟,将所述颗粒干燥直至它们变得透明。通过向经干燥的颗粒中加入50μL三重蒸馏水来完成RNA提取。使用SynergyII(Biotek,USA)对1μL的RNA进行定量。(4)RNA的提取和定量对于cDNA的合成,将1μg的经定量的RNA放入0.2-mL试管中并利用RevertAidFirstStrandcDNA合成试剂盒(ThermoScientific,USA),通过使用C-1000热循环PCR仪(Bio-Rad,USA)根据逆转录-聚合酶链反应(RT-PCR)合成cDNA。(5)实时PCR的基因表达测定使用蒸馏水将合成的cDNA稀释至1/20。待向9μL稀释的cDNA中加入10μL的TaqmanGeneExpressionMasterMix(LifeTechnologies,USA)和1μL的NK1R(ACCESSION:NM_001058)和EDN1(ACCESSION:NM_001168319)基因的Assays-on-DemandTM(LifeTechnologies,USA)后,通过使用7500FastReal-TimePCR(LifeTechnologies,USA)与作为对照组的甘油醛3-磷酸脱氢酶(GAPDH,ACCESSION:NM001256799)进行比较来相对定量分析所述基因的表达。也就是说,将NK1R和EDN1基因的表达水平与GAPDH的表达水平进行比较。其结果示于图1。如图1所示,可以看出当用2nMP物质处理并将对照组的表达设为1时,NK1R和EDN1基因的表达分别增加到4.2和3.6。当用2nMP物质处理细胞,然后加入5ppm本发明的一个方面的高山蒿提取物时,NK1R和EDN1基因的表达分别降低至2.5和1.6。从该结果,证实了根据本发明的一个方面的高山蒿提取物有效减少由P物质诱导的生物现象。这表明,根据本发明的一个方面的高山蒿提取物具有恢复已由应激破坏的皮肤稳态的效果和抗应激效应的效果。特别地,考虑到NK1R基因是表达P物质的受体蛋白质的基因,预期该基因表达的降低将导致身体对P物质的摄取减少,并防止由应激物如P物质引起的皮肤稳态的破坏。[测试实施例2]内皮素1的定量(1)细胞的回收和蛋白质的定量将在6孔板上培养的黑素细胞(KaMC)加入到400μL的Accutase溶液(Millipore,CA,USA)中。搅拌1分钟后,通过加入600μL的M-254培养基来回收共1mL的含细胞的培养基。然后,在12,000rpm下离心15分钟后,弃去上清,并向剩余的颗粒中加入20μL的MCL裂解缓冲液(Sigma-Aldrich,St.Louis,USA)。待充分混合并再次在12,000rpm下离心15分钟后,分离上清和细胞碎片。将1μL经分离的上清加入到96孔板中后,加入蒸馏水至终体积为25μL。然后,使用BCA蛋白测定试剂盒(ThermoScientific,IL,USA)在562nm下测定蛋白质的量。其结果展示于表1中。【表1】(2)内皮素1ELISA测定回收用测试实施例1中(2)的提取物所处理的细胞培养基,通过使用人总内皮素ELISA试剂盒(MyBioSource,USA)在450nm测量所述培养基所含的内皮素1(EDN1)的量。图2显示了根据式1计算蛋白质在总蛋白中的比例的结果。【式1】内皮素含量(%)=(吸光度/总蛋白含量)×100如图2所示,当用2nM的P物质处理所述细胞并将对照组的量作为100%时,内皮素1的含量增加到124%P。当用2nM的P物质处理所述细胞,然后加入5ppm根据本发明的一个方面的高山蒿提取物时,内皮素1的含量与对照组相比降低至103%。该结果表明,根据本发明的一个方面的高山蒿提取物具有减少内皮素1的量的显著效果。由P物质诱导的内皮素1的量的减少表明,根据本发明的一方面的高山蒿提取物通过抑制由应激物引起的生理效应来提供维持皮肤稳态的显著效果及抗应激效应。以下,将描述根据本发明的一方面的组合物的剂型实施例。然而,也可以制成其他剂型,因此本发明的范围不限于这些剂型实施例。【剂型实施例1】软胶囊根据常用方法,混合8mg实施例1的高山蒿提取物、9mg维生素E、9mg维生素C、2mg棕榈油、8mg氢化植物油、4mg黄蜂蜡和9mg卵磷脂,然后通过每个胶囊填充400mg混合物来制备软胶囊。与此同时,用66重量份明胶、24重量份甘油和10重量份山梨醇制备软胶囊片,然后被所述混合物所填充,来制备包含400mg的本发明的组合物的软胶囊。【剂型实施例2】片剂将8mg实施例1的高山蒿提取物、9mg维生素E、9mg维生素C、200mg低聚半乳糖、60mg乳糖和140mg麦芽糖进行混合并使用流化床烘干机。然后,在加入6mg糖酯后,根据常用方法将混合物制备成包含500mg组合物的片剂。【剂型实施例3】饮剂将8mg实施例1的高山蒿提取物、9mg维生素E、9mg维生素C、10g葡萄糖、0.6g柠檬酸和25g寡糖糖浆进行混合,并加入300mL纯净水。将200mL混合物装入瓶中。然后,通过在130℃下灭菌4-5秒来制备饮剂。【剂型实施例4】颗粒剂将8mg实施例1的高山蒿提取物、9mg维生素E、9mg维生素C、250mg无水结晶葡萄糖和550mg淀粉进行混合并使用流化床制粒机造粒。将所得颗粒填充在袋中。【剂型实施例5】注射剂根据常用方法,用表2所述的组合物制备注射剂。【表2】成分含量实施例1的高山蒿(Artemisiaumbelliformis)提取物10-50mg灭菌注射用蒸馏水适量pH调节剂适量【剂型实施例6】保健功能性食品根据常用方法,用表3所述的组合物制备保健功能性食品。【表3】成分含量实施例1的高山蒿(Artemisiaumbelliformis)提取物20mg维生素A乙酸酯70μg维生素E1.0mg维生素B10.13mg维生素B20.15mg维生素B60.5mg维生素B120.2μg维生素C10mg生物素10μg烟酰胺1.7mg叶酸50μg泛酸钙0.5mg硫酸亚铁1.75mg氧化锌0.82mg碳酸镁25.3mg磷酸二氢钾15mg磷酸一氢钙55mg柠檬酸钾90mg碳酸钙100mg氯化镁24.8mg虽然上面描述了适用于保健功能性食品的维生素和矿物质混合物的具体组合物,但是这些组合可以根据需要进行调整。【剂型实施例7】健康饮料根据常用方法,用表4中所述的组合物制备健康饮料。【表4】成分含量实施例1的高山蒿(Artemisiaumbelliformis)提取物1000mg柠檬酸1000mg寡糖100g牛磺酸1g纯净水余量根据常用的保健饮料制备方法,将上述成分混合并在搅拌的同时在85℃下加热约1小时。将所得溶液过滤并灭菌。【剂型实施例8】柔肤水(化妆水)根据常用方法,用表5中所述的组合物制备柔肤水。【表5】成分含量(wt%)实施例1的高山蒿(Artemisiaumbelliformis)提取物0.2甘油3.0丁二醇2.0丙二醇2.0羧基乙烯基聚合物0.1PEG-12壬基苯基醚0.2聚山梨醇酯800.4乙醇10.0三乙醇胺0.1防腐剂、颜料和香料适量纯净水余量【剂型实施例9】滋养乳液(乳液)根据常用方法,用表6中所述的组合物制备滋养乳液。【表6】成分含量(wt%)实施例1的高山蒿(Artemisiaumbelliformis)提取物1.0甘油3.0丁二醇3.0丙二醇3.0羧基乙烯基聚合物0.1蜂蜡4.0聚山梨醇酯601.5辛酸/癸酸甘油三酯5.0角鲨烷5.0脱水山梨醇倍半油酸酯1.5液体石蜡0.5十六烷醇1.0三乙醇胺0.2防腐剂、颜料和香料适量纯净水余量【剂型实施例10】滋养霜根据常用方法,用表7中所述的组合物制备滋养霜。【表7】成分含量(wt%)实施例1的高山蒿(Artemisiaumbelliformis)提取物2.0甘油3.0丁二醇3.0液体石蜡7.0β-葡聚糖7.0卡波姆0.1辛酸/癸酸甘油三酯3.0角鲨烷5.0十六烷基葡糖苷1.5硬脂酸脱水山梨醇酯0.4聚山梨醇酯601.2三乙醇胺0.1防腐剂、颜料和香料适量纯净水余量【剂型实施例11】按摩霜根据常用方法,用表8中所述的组合物制备按摩霜。【表8】成分含量(wt%)实施例1的高山蒿(Artemisiaumbelliformis)提取物2.0甘油8.0丁二醇4.0液体石蜡45.0β-葡聚糖7.0卡波姆0.1辛酸/癸酸甘油三酯3.0蜂蜡4.0十六烷基葡糖苷1.5脱水山梨醇倍半油酸酯0.9凡士林3.0石蜡1.5防腐剂、颜料和香料适量纯净水余量【剂型实施例12】面膜根据常用方法,用表9中所述的组合物制备面膜。【表9】成分含量(wt%)实施例1的高山蒿(Artemisiaumbelliformis)提取物0.2甘油4.0聚乙烯醇15.0透明质酸提取物5.0β-葡聚糖7.0尿囊素0.1壬基苯基醚0.4聚山梨醇酯601.2乙醇6.0防腐剂、颜料和香料适量纯净水余量尽管已经示出和描述了示例性实施例,但是本领域技术人员将理解,在不脱离由所附权利要求限定的本发明的精神和范围的情况下,可以对其进行形式和细节上的各种改变。因此,应当理解的是,本发明的实质范围由所附权利要求及其等同物限定。【保藏编号】保藏机构:韩国生物科学和生物技术研究所保藏编号:KCTC12015BP保藏日期:2011年9月14。【保藏证明】当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1