一种中药组合物的含量测定方法与流程
本发明涉及到一种中药组合物的含量测定方法,属于药品的质量控制方法领域。
背景技术:
中药是中医防病治病的最重要物质手段。我国自“九五”以来开展实施的中药现代化是推动中药产业发展的重大举措。而中药的质量控制和评价是中药现代化的关键问题之一,也是中药研究的难点和热点。中药质量控制的目的是保证中药的有效性和安全性。中药质量控制就是监测中药的药效物质、有毒物质及其变化规律,是依据一系列质量标准对中药生产过程中的每一个环节进行质量检测与控制。而中药质量评价的技术、方法和策略的研究是制订科学、合理、先进的质量标准的基础。液相色谱具有很高的分离度,可把复杂的化学成分进行分离而形成高低不同的峰组成一张色谱图,这些色谱峰的高度和峰面积分别代表了各种不同化学成分和其含量,其含量的大小可以有效的反应产品质量及其稳定性。目前含量测定方法中以单一成分为主,很少有一种方法同时测定多个有效成分的含量测定方法。
本发明要求保护一种中药组合物的含量测定方法,该中药组合物由以下药材组成:连翘、金银花、板蓝根、苦杏仁、薄荷脑、鱼腥草、大黄、广藿香、绵马贯众、红景天、麻黄、甘草、石膏,该含量测定方法,同时测定了新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷和甘草酸七个成分的含量,可以有效的节约能源,降低分析成本,而现有技术中并没有公开该技术内容。
技术实现要素:
本发明提供一种中药组合物的含量测定方法。该方法可以同时测定所述中药组合物中多种有效成分。
该中药组合物由如下重量份的原料药制成:连翘200-300、麻黄60-100、大黄40-60、鱼腥草200-300、金银花200-300、板蓝根200-300、广藿香60-100、绵马贯众200-300、红景天60-100、薄荷脑5-9、苦杏仁60-100、甘草60-100、石膏200-300,含量测定方法如下:
供试品溶液制备:取所述中药组合物0.5g研细,精密称定,置具塞锥形瓶中,加乙醇或甲醇25ml,超声或者回流提取30分钟,过滤,得滤液,蒸干,残渣用乙醇或甲醇溶解并定容至25ml,即得;
对照品溶液的制备:取新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷、甘草酸铵对照品适量,精密称定,加50%甲醇制成每1ml含34.4µg新绿原酸、76.7µg绿原酸、34.2µg隐绿原酸、56.2µg异连翘酯苷a、14.9µg4,5-二-o-咖啡酰奎宁酸、11.2µg槲皮苷和42.8µg甘草酸铵的混合溶液,即得,其中,甘草酸重量=甘草酸铵重量/1.0207;
色谱条件:以甲醇-乙腈-0.1%磷酸溶液为流动相,洗脱比例如下表:
检测波长分别为327nm和250nm;250nm下检测槲皮苷和甘草酸,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸;色谱柱为c18色谱柱;
测定法:分别精密吸取对照品溶液与供试品溶液各2µl,注入液相色谱仪,测定,记录色谱图,即得。
本发明所述的中药组合物优选的重量份原料药为:连翘200、金银花300、板蓝根200、大黄40、广藿香60、绵马贯众300、红景天100、薄荷脑9、麻黄60、苦杏仁100、鱼腥草200、甘草100、石膏200。
本发明所述的中药组合物优选的重量份原料药为:连翘300、金银花200、板蓝根300、大黄60、广藿香100、绵马贯众200、红景天60、薄荷脑5、麻黄100、苦杏仁60、鱼腥草300、甘草60、石膏300。
本发明所述的中药组合物优选的重量份原料药为:连翘278、金银花294、板蓝根285、大黄55、广藿香95、绵马贯众290、红景天87、薄荷脑8.5、麻黄88、苦杏仁80、鱼腥草284、甘草95、石膏277。
本发明所述的中药组合物优选的重量份原料药为:连翘255、金银花255、板蓝根255、大黄51、广藿香85、绵马贯255、红景天85、薄荷脑7.5、麻黄85、苦杏仁85、鱼腥草255、甘草85、石膏255。
本发明所述的中药组合物制剂的制备方法为:
(1)按照原料药重量比例称取中药材,净选,酌情碎断;
(2)广藿香碎断,加10倍量水提取挥发油,提油时间8小时,收集挥发油,备用;提取液过滤后,残渣弃去,滤液备用;
(3)连翘、麻黄、鱼腥草、大黄,用12倍量70%的乙醇提取3次,每次2.5小时,提取液合并过滤,回收乙醇,滤液备用;
(4)金银花、石膏、板蓝根、绵马贯众、甘草、红景天,加12倍量水煎煮至沸,加入苦杏仁,煎煮2次,每次1小时,提取液合并过滤,所得滤液与步骤(2)广藿香提油后的滤液合并,浓缩成在60℃时测定相对密度为1.10-1.15的清膏,加入乙醇,调节至醇浓度为70%,冷藏放置,过滤,回收乙醇至无醇味,得清膏备用;
(5)将步骤(4)所得清膏与步骤(3)所得醇提液合并,浓缩至在60℃时测定相对密度为1.15-1.20的清膏,干燥,得干膏粉,备用;
(6)将步骤(5)所得干膏粉加入适当药学上可接受的辅料制粒;
(7)将薄荷脑、步骤(2)所得挥发油加入乙醇溶解,喷入步骤(6)所得颗粒,密闭,混匀,压片或者装胶囊、或者装袋。
本发明所述的含量测定方法优选为:
供试品溶液制备:取所述中药组合物0.5g研细,精密称定,置具塞锥形瓶中,加50%乙醇25ml,超声提取,功率500w,频率40khz,提取30分钟,过滤,得滤液,将滤纸连同残渣一起加入具塞锥形瓶中,再加50%乙醇25ml,超声处理30分钟,过滤,用50%乙醇洗涤药渣4次,每次5ml,合并两次滤液及洗涤液,蒸干,残渣用50%甲醇溶解并定容至25ml,即得;
对照品溶液的制备:取新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷、甘草酸铵对照品适量,精密称定,加50%甲醇制成每1ml含34.4µg新绿原酸、76.7µg绿原酸、34.2µg隐绿原酸、56.2µg异连翘酯苷a、14.9µg4,5-二-o-咖啡酰奎宁酸、11.2µg槲皮苷和42.8µg甘草酸铵的混合溶液,即得,其中,甘草酸重量=甘草酸铵重量/1.0207;
色谱条件:以甲醇-乙腈-0.1%磷酸溶液为流动相,洗脱比例如下表:
检测波长分别为327nm和250nm;250nm下检测槲皮苷和甘草酸,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸;色谱柱:acquityuplc®hsst3(1.8µm,2.1×100mm);柱温为35℃;
测定法:分别精密吸取对照品溶液与供试品溶液各2µl,注入液相色谱仪,测定,记录色谱图,即得。
本发明所述的含量测定方法还优选为:
供试品溶液制备:取所述中药组合物0.5g研细,精密称定,置具塞锥形瓶中,加50%甲醇25ml,超声提取,功率500w,频率40khz,提取30分钟,过滤,得滤液,将滤纸连同残渣一起加入具塞锥形瓶中,再加50%甲醇25ml,超声处理30分钟,过滤,用50%甲醇洗涤药渣4次,每次5ml,合并两次滤液及洗涤液,蒸干,残渣用50%甲醇溶解并定容至25ml,即得;
对照品溶液的制备:取新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷、甘草酸铵对照品适量,精密称定,加50%甲醇制成每1ml含34.4µg新绿原酸、76.7µg绿原酸、34.2µg隐绿原酸、56.2µg异连翘酯苷a、14.9µg4,5-二-o-咖啡酰奎宁酸、11.2µg槲皮苷和42.8µg甘草酸铵的混合溶液,即得,其中,甘草酸重量=甘草酸铵重量/1.0207;
色谱条件:以甲醇-乙腈-0.1%磷酸溶液为流动相,洗脱比例如下表:
检测波长分别为327nm和250nm;250nm下检测槲皮苷和甘草酸,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸;色谱柱为acquityuplc®cshtmc18;
测定法:分别精密吸取对照品溶液与供试品溶液各2µl,注入液相色谱仪,测定,记录色谱图,即得。
本发明所述的含量测定方法还优选为:
供试品溶液制备:取所述中药组合物0.5g研细,精密称定,置具塞锥形瓶中,加甲醇25ml,回流提取,功率500w,频率40khz,提取30分钟,过滤,得滤液,将滤纸连同残渣一起加入具塞锥形瓶中,再加甲醇25ml,超声处理30分钟,过滤,用甲醇洗涤药渣4次,每次5ml,合并两次滤液及洗涤液,蒸干,残渣用50%甲醇溶解并定容至25ml,即得;
对照品溶液的制备:取新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷、甘草酸铵对照品适量,精密称定,加50%甲醇制成每1ml含34.4µg新绿原酸、76.7µg绿原酸、34.2µg隐绿原酸、56.2µg异连翘酯苷a、14.9µg4,5-二-o-咖啡酰奎宁酸、11.2µg槲皮苷和42.8µg甘草酸铵的混合溶液,即得,其中,甘草酸重量=甘草酸铵重量/1.0207;
色谱条件:以甲醇-乙腈-0.1%磷酸溶液为流动相,洗脱比例如下表:
检测波长分别为327nm和250nm;250nm下检测槲皮苷和甘草酸,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸;色谱柱为acquityuplc®behc18;
测定法:分别精密吸取对照品溶液与供试品溶液各2µl,注入液相色谱仪,测定,记录色谱图,即得。
本发明所述含量测定方法还优选为:
供试品溶液制备:取所述中药组合物0.5g研细,精密称定,置具塞锥形瓶中,加乙醇25ml,超声提取,功率500w,频率40khz,提取30分钟,过滤,得滤液,将滤纸连同残渣一起加入具塞锥形瓶中,再加乙醇25ml,超声处理30分钟,过滤,用乙醇洗涤药渣4次,每次5ml,合并两次滤液及洗涤液,蒸干,残渣用50%甲醇溶解并定容至25ml,即得;
对照品溶液的制备:取新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷、甘草酸铵对照品适量,精密称定,加50%甲醇制成每1ml含34.4µg新绿原酸、76.7µg绿原酸、34.2µg隐绿原酸、56.2µg异连翘酯苷a、14.9µg4,5-二-o-咖啡酰奎宁酸、11.2µg槲皮苷和42.8µg甘草酸铵的混合溶液,即得,其中,甘草酸重量=甘草酸铵重量/1.0207;
色谱条件:以甲醇-乙腈-0.1%磷酸溶液为流动相,洗脱比例如下表:
检测波长分别为327nm和250nm;250nm下检测槲皮苷和甘草酸,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸;色谱柱为acquityuplc®behc18;
测定法:分别精密吸取对照品溶液与供试品溶液各2µl,注入液相色谱仪,测定,记录色谱图,即得。
用实施例1制备的样品,对本发明含量测定方法,从多个方面评价该方法的可行性,评价方法如下:
1.仪器、试剂与试药
1.1仪器
美国watersacquityuplch-class超高效液相色谱仪(tuv检测器,empower3.0色谱工作站),循环式多用真空泵(郑州长城科工贸有限公司),kq250db型超声波清洗器(昆山市超声仪器有限公司),瑞士mettlertoledoal204型电子分析天平,瑞士mettlertoledoab135-s型电子分析天平,上海精科ja2603b电子天平。
1.2试剂
乙醇(分析纯,天津市光复科技发展有限公司),磷酸(分析纯,天津市光复科技发展有限公司),乙腈(色谱纯,美国fisher公司),甲醇(色谱纯,美国fisher公司),新绿原酸(成都普瑞法科技开发有限公司,批号:13112712,纯度≥98%),绿原酸(中国食品药品检定研究院,批号:110753-201314,纯度,96.6%)、隐绿原酸(上海源叶生物科技有限公司,批号:zf0226ba14,纯度≥98%)、异连翘酯苷a(上海源叶生物科技有限公司,批号:ya0817hb14,纯度≥98%)、4,5-二-o-咖啡酰奎宁酸(中国食品药品检定研究院,批号:111894-201102,纯度,94.1%)、槲皮苷(hwianalytikgmbhpharmasolutions,批号:hwi01112,纯度,91.7%)、甘草酸铵(councilofeurope-edqm,批号:1.1,纯度≥98%)。
1.3试药:本发明中药组合物
2.色谱条件
2.1检测波长的选择
根据待测成分的对照品溶液的uv光谱图,选择327nm、250nm处的最大吸收峰作为检测波长,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸,250nm下检测槲皮苷和甘草酸,以尽量减少其它成分的干扰。
2.2流动相的选择
考察了不同比例的乙腈-甲醇-0.1%磷酸流动相系统,结果表明,按下表梯度洗脱所得色谱峰分离度好,基线平稳,待测色谱峰周围没有明显杂质干扰。
梯度洗脱表
2.3色谱条件的确定
以甲醇-乙腈-0.1%磷酸溶液为流动相,按上表进行梯度洗脱。检测波长分别为327nm和250nm;250nm下检测槲皮苷和甘草酸,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸;色谱柱:acquityuplc®hsst3(1.8µm,2.1×100mm);柱温为35℃。
3.1提取溶剂的考察
取本发明中药组合物适量,研细,取8份,每份0.5g,精密称定,置具塞锥形瓶中,每两份分别加入25ml甲醇、乙醇、50%甲醇和50%乙醇,超声处理(功率500w,频率40khz)30分钟,过滤,得滤液,将滤纸连同残渣一起加入具塞锥形瓶中,再分别加入25ml甲醇、乙醇、50%甲醇和50%乙醇,超声处理30分钟,过滤,用各提取溶剂洗涤药渣4次,每次5ml,合并洗涤液及两次滤液,蒸干,残渣用50%甲醇溶解并定容至25ml,作为供试品溶液。
分别吸取供试品溶液2µl,注入液相色谱仪,测定供试品中待测成分的峰面积,结果见表1。
表1不同提取溶剂考察的实验结果
实验结果表明:用50%乙醇作为提取溶剂时,待测成分的提取率最高。
3.2提取方法的考察
取本发明中药组合物适量,研细,取4份,每份0.5g,精密称定,置具塞锥形瓶中,分别加入50%乙醇25ml,每2份分别采用回流提取2小时和超声处理30分钟(2次)两种不同的提取方法提取,将提取液过滤,用50%乙醇洗涤药渣4次,每次5ml,将洗涤液与滤液合并,蒸干,残渣用50%甲醇溶解并定容至25ml,作为供试品溶液。分别精密吸取供试品溶液各2µl,注入液相色谱仪,测定供试品溶液中待测成分的峰面积,结果见表2。
实验结果表明,回流提取比超声提取峰面积略高,均可作为本发明中药组合物的提取方式。
3.3提取次数的考察
分别考察超声提取1次、2次和3次,比较不同提取次数的提取效果,考察结果见下表:
实验结果表明提取3次时,待测成分提取效率最高,但是提取3次时,提取效率仅比提取2次提高了1~2%,表明提取2次和提取3次所得结果差别不大。
3.4供试品溶液制备方法的确定
取本发明中药组合物适量,研细,取0.5g,精密称定,置具塞锥形瓶中,加50%乙醇25ml,超声处理(功率500w,频率40khz)30分钟,过滤,得滤液,将滤纸连同残渣一起加入具塞锥形瓶中,再加50%乙醇25ml,超声处理30分钟,过滤,用50%乙醇洗涤药渣4次,每次5ml,合并两次滤液及洗涤液,蒸干,残渣用50%甲醇溶解并定容至25ml,即得。
对照品溶液的制备
取新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷、甘草酸铵对照品适量,精密称定,加50%甲醇制成每1ml含34.4µg新绿原酸、76.7µg绿原酸、34.2µg隐绿原酸、56.2µg异连翘酯苷a、14.9µg4,5-二-o-咖啡酰奎宁酸、11.2µg槲皮苷和42.8µg甘草酸铵的混合溶液,即得(甘草酸重量=甘草酸铵重量/1.0207)。
线性关系考察
分别精密称取15.56mg新绿原酸与15.66mg隐绿原酸置于10ml容量瓶中,用50%甲醇溶解并稀释至刻度作为对照品母液1;分别精密称取15.35mg绿原酸与11.24mg异连翘酯苷a置于10ml容量瓶中,用50%甲醇溶解并稀释至刻度作为对照品母液2;分别精密称取15.88mg4,5-二-o-咖啡酰奎宁酸与12.24mg槲皮苷对照品置于10ml的容量瓶中用50%甲醇溶解并稀释至刻度作为对照品母液3,分别精密称取10.69mg甘草酸铵对照品置于10ml的容量瓶中用50%甲醇溶解并稀释至刻度作为对照品母液4,再分别从对照品母液1、2、3、4中精密吸取1ml、3ml、1ml、2ml置于10ml容量瓶中,用50%甲醇定容至刻度作为对照品的储备液,再分别从储备液中精密吸取0.1、0.2、0.5、1、2、4ml置于10ml的容量瓶中,用50%的甲醇定容至刻度,得到不同质量浓度的系列对照品溶液。
分别精密吸取含新绿原酸1.56µg/ml、3.12µg/ml、7.78µg/ml、15.56µg/ml、31.12µg/ml和62.24µg/ml,含绿原酸4.45µg/ml、8.90µg/ml、22.24µg/ml、44.48µg/ml、88.97µg/ml和177.94µg/ml,含隐绿原酸1.57µg/ml、3.13µg/ml、7.83µg/ml、15.66µg/ml、31.32µg/ml、62.64µg/ml,含异连翘酯苷a3.37µg/ml、6.74µg/ml、16.86µg/ml、33.72µg/ml、67.44µg/ml、134.88µg/ml,含4,5-二-o-咖啡酰奎宁酸1.49µg/ml、2.99µg/ml、7.47µg/ml、14.94µg/ml、29.89µg/ml、59.77µg/ml,含槲皮苷1.12µg/ml、2.24µg/ml、5.61µg/ml、11.22µg/ml、22.45µg/ml、44.90µg/ml,含甘草酸2.09µg/ml、4.19µg/ml、10.47µg/ml、20.95µg/ml、41.89µg/ml、83.79µg/ml的系列对照品溶液各2µl,分别注入超高效液相色谱仪,按拟定的色谱条件测定,以对照品质量浓度为横坐标,峰面积为纵坐标,绘制标准曲线,得新绿原酸回归方程:y=20628x-1699.7(r²=0.9999),结果表明新绿原酸在1.56µg/ml~62.24µg/ml范围内线性良好;绿原酸回归方程:y=19778x+8305.9(r²=0.9999),结果表明绿原酸在4.45µg/ml~177.94µg/ml范围内线性良好;隐绿原酸回归方程:y=14319x-933.94(r²=0.9999),结果表明隐绿原酸在1.57µg/ml~62.64µg/ml范围内线性良好;异连翘酯苷a回归方程:y=7951.8x-2304.5(r²=0.9999),结果表明异连翘酯苷a在3.37µg/ml~134.88µg/ml范围内线性良好;4,5-二-o-咖啡酰奎宁酸回归方程为:y=20148x-2422.8(r²=0.9999),结果表明4,5-二-o-咖啡酰奎宁酸在1.49µg/ml~59.77µg/ml范围内线性良好;槲皮苷回归方程:y=13288x-3121.6(r²=0.9999),结果表明槲皮苷在1.12µg/ml~44.90µg/ml范围内线性良好;甘草酸回归方程为:y=2731.3x+810.9(r²=0.9999),结果表明甘草酸在2.09µg/ml~83.79µg/ml范围内线性良好。实验结果见表4。
5.检测限和定量限的确定
将待测成分的混合对照品溶液稀释成一系列浓度的溶液,进行uplc检测,记录信号强度与噪音强度的比值,将信号强度和噪音强度之比等于3时的浓度作为检测限,将信号强度和噪音强度之比等于10时的浓度作为定量限。最终确定新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、槲皮苷、4,5-二-o-咖啡酰奎宁酸、甘草酸的检测限分别为0.051µg/ml、0.049µg/ml、0.052µg/ml、0.111µg/ml、0.037µg/ml、0.049µg/ml和2.095µg/ml;定量限分别为0.156µg/ml、0.147µg/ml、0.157µg/ml、0.337µg/ml、0.112µg/ml、0.149µg/ml和6.200µg/ml。
精密度考察
取对照品溶液(浓度为:新绿原酸31.12µg/ml;绿原酸88.97µg/ml;隐绿原酸31.32µg/ml;异连翘酯苷a67.44µg/ml;4,5-二-o-咖啡酰奎宁酸29.89µg/ml;槲皮苷22.45µg/ml;甘草酸41.89µg/ml)连续进样6次,记录峰面积,计算各色谱峰峰面积的相对标准偏差(rsd)来考察仪器精密度,结果见表8。
待测成分峰面积的rsd均小于2%,表明仪器精密度良好。
重复性考察
取同一批本发明中药组合物适量,分别按“供试品溶液的制备”中取样量的80%、100%、120%取样,每个取样量各制备3份,依法测定。根据每一份所含待测成分的含量,计算rsd,结果见表9。
由测定结果可知,待测成分含量的rsd均小于3%,表明该方法重复性良好。
稳定性考察
精密吸取供试品溶液,分别于室温放置0、2、4、6、8和12小时时进样一次,分别记录待测成分的峰面积,并计算峰面积的rsd,对稳定性进行考察,测定结果见表10。
由测定结果可知,待测成分的峰面积的rsd均在3%以内,表明供试品溶液12h内稳定。
加样回收率考察
按取样量0.5g的二分之一,即0.25g,称取本品,精密称定,平行9份,分为3组,分别加入低、中、高3种质量浓度的待测成分对照品溶液,按“供试品溶液制备方法”制备待测溶液,依法测定,对回收率试验进行考察。结果见表11。
从表11测定结果可知,新绿原酸的平均加样回收率为99.44%,rsd为2.71%,符合要求。
从表12测定结果可知,绿原酸的平均加样回收率为99.82%,rsd为2.67%,符合要求。
从表13测定结果可知,隐绿原酸的平均加样回收率为97.61%,rsd为1.64%,符合要求。
从表14测定结果可知,异连翘酯苷a的平均加样回收率为97.17%,rsd为1.63%,符合要求。
从表15测定结果可知,槲皮苷的平均加样回收率为99.19%,rsd为2.89%,符合要求。
从表16测定结果可知,4,5-二-o-咖啡酰奎宁酸的平均加样回收率为100.46%,rsd为1.92%,符合要求。
从表17测定结果可知,甘草酸的平均加样回收率为100.32%,rsd为0.97%,符合要求。
系统耐用性试验
10.1流速变化对多成分含量测定的影响
取供试品溶液,固定其他色谱条件,分别在流速为0.25ml/min、0.3ml/min和0.35ml/min进行测定,并按各个成分的对照品做对照,分别计算待测成分的含量,比较流速变化对测定结果的影响,结果见表18。
由上述结果可知,流速变化后,隐绿原酸,槲皮苷和甘草酸的rsd大于3%,表明流速的微小变化,对样品中这3个成分的影响较大。
10.2波长变化对待测成分的含量测定的影响
取供试品溶液,固定其他色谱条件,分别在波长322、245nm,327、250nm和332、255nm进行测定,并以各个待测成分对照品做对照,分别计算待测成分的含量,比较波长变化对测定结果的影响。结果见表19。
由上述结果可知,波长变化后,隐绿原酸,槲皮苷和4,5-二-o咖啡酰奎宁酸含量测定结果的rsd值大于3%,表明波长的微小变化,对样品中这3个成分含量测定结果影响较大。
10.3柱温变化对待测成分的含量测定的影响
取供试品溶液,固定其他色谱条件,分别在柱温30℃、35℃和40℃进行测定,并以各个待测成分的对照品做对照,分别计算待测成分的含量,比较柱温变化对测定结果的影响。
由上述结果可知,柱温变化后,隐绿原酸,4,5-二-o咖啡酰奎宁酸,甘草酸含量测定结果的rsd值均大于3%,表明柱温的微小变化,对样品中这3个成分的含量测定结果影响较大。
10.4不同色谱柱对待测成分的含量测定的影响
取供试品溶液,固定其他色谱条件,分别用acquityuplc®cshtmc18(1.7µm,2.1×100mm)、acquityuplc®behc18(1.7µm,2.1×100mm)、acquityuplc®behshieldrp18(1.7µm,2.1×100mm)和acquityuplc®hsst3(1.8µm,2.1×100mm)等四种不同的色谱柱进行测试,比较不同色谱柱对待测成分峰形以及分离度的影响。结果表明均可用于本发明中药组合物四种成分的含量测定,使用hsst3柱时,待测成分峰形以及分离度最好。
中间精密度
按照已确定的含量测定方法,分别由不同的分析人员在不同的时间、分别用两台不同的uplc仪器测定同一批次本发明中药组合物待测成分的含量,每次试验平行操作3份供试品,对中间精密度进行考察。结果见表21-25。
由上述试验结果可知,由不同人员在不同时间、不同仪器测定同一批次本发明中药组合物待测成分含量的rsd值均小于5%,表明该方法中间精密度良好。
三批本发明中药组合物七种成分含量测定
用所制定的含量测定方法,对3批本发明中药组合物待测成分的含量进行了测定,结果见表26。
本发明建立了本发明中药组合物的四种药材中七种成分的含量测定方法,通过方法学研究结果表明,本方法测定连翘、金银花、鱼腥草和甘草四种药材中的有效成分具有良好的准确度、精密度、稳定性和重复性,可以有效的控制该中药组合物的质量及安全。
附图说明
图1:327nm下对照品色谱图,其中1为新绿原酸,2为绿原酸,3为隐绿原酸,4为异连翘酯苷a,5为4,5-二-o-咖啡酰奎宁酸
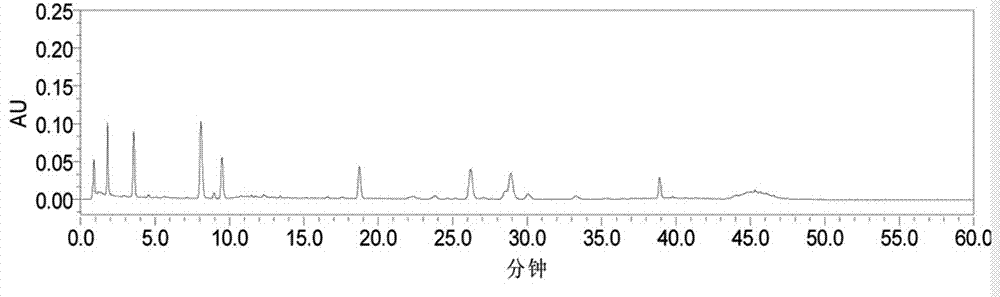
图2:供试品溶液在327nm下色谱图
图3:250nm下对照品色谱图,其中6为槲皮苷,7为甘草酸
图4:供试品溶液在250nm下色谱图
图5:实施例1色谱图谱:a图为327nm下对照品色谱图,其中1为新绿原酸,2为绿原酸,3为隐绿原酸,4为异连翘酯苷a,5为4,5-二-o-咖啡酰奎宁酸;b图为327nm下供试品色谱图;c图为250nm下对照品色谱图,其中6为槲皮苷,7为甘草酸;d图为250nm下供试品色谱图。
图6:实施例2色谱图谱:a图为327nm下对照品色谱图,其中1为新绿原酸,2为绿原酸,3为隐绿原酸,4为异连翘酯苷a,5为4,5-二-o-咖啡酰奎宁酸;b图为327nm下供试品色谱图;c图为250nm下对照品色谱图,其中6为槲皮苷,7为甘草酸;d图为250nm下供试品色谱图。
图7:实施例3色谱图谱:a图为327nm下对照品色谱图,其中1为新绿原酸,2为绿原酸,3为隐绿原酸,4为异连翘酯苷a,5为4,5-二-o-咖啡酰奎宁酸;b图为327nm下供试品色谱图;c图为250nm下对照品色谱图,其中6为槲皮苷,7为甘草酸;d图为250nm下供试品色谱图。
图8:实施例4色谱图谱:a图为327nm下对照品色谱图,其中1为新绿原酸,2为绿原酸,3为隐绿原酸,4为异连翘酯苷a,5为4,5-二-o-咖啡酰奎宁酸;b图为327nm下供试品色谱图;c图为250nm下对照品色谱图,其中6为槲皮苷,7为甘草酸;d图为250nm下供试品色谱图。
具体实施方式
实施例1
按比例称取:连翘200g、金银花300g、板蓝根200g、大黄40g、广藿香60g、绵马贯众300g、红景天100g、薄荷脑9g、麻黄60g、苦杏仁100g、鱼腥草200g、甘草100g、石膏200g,按照以下工艺提取:
(1)按照原料药重量比例称取中药材,净选,酌情碎断;
(2)广藿香碎断,加10倍量水提取挥发油,提油时间8小时,收集挥发油,备用;提取液过滤后,残渣弃去,滤液备用;
(3)连翘、麻黄、鱼腥草、大黄,用12倍量70%的乙醇提取3次,每次2.5小时,提取液合并过滤,回收乙醇,滤液备用;
(4)金银花、石膏、板蓝根、绵马贯众、甘草、红景天,加12倍量水煎煮至沸,加入苦杏仁,煎煮2次,每次1小时,提取液合并过滤,所得滤液与步骤(2)广藿香提油后的滤液合并,浓缩成在60℃时测定相对密度为1.10-1.15的清膏,加入乙醇,调节至醇浓度为70%,冷藏放置,过滤,回收乙醇至无醇味,得清膏备用;
(5)将步骤(4)所得清膏与步骤(3)所得醇提液合并,浓缩至在60℃时测定相对密度为1.15-1.20的清膏,干燥,得干膏粉,备用;
(6)将步骤(5)所得干膏粉加入适当药学上可接受的辅料制粒;
(7)将薄荷脑、步骤(2)所得挥发油加入乙醇溶解,喷入步骤(6)所得颗粒,装胶囊,即得。
含量测定方法:
供试品溶液制备:取所述中药组合物0.5g研细,精密称定,置具塞锥形瓶中,加50%乙醇25ml,超声提取,功率500w,频率40khz,提取30分钟,过滤,得滤液,将滤纸连同残渣一起加入具塞锥形瓶中,再加50%乙醇25ml,超声处理30分钟,过滤,用50%乙醇洗涤药渣4次,每次5ml,合并两次滤液及洗涤液,蒸干,残渣用50%甲醇溶解并定容至25ml,即得;
对照品溶液的制备:取新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷、甘草酸铵对照品适量,精密称定,加50%甲醇制成每1ml含34.4µg新绿原酸、76.7µg绿原酸、34.2µg隐绿原酸、56.2µg异连翘酯苷a、14.9µg4,5-二-o-咖啡酰奎宁酸、11.2µg槲皮苷和42.8µg甘草酸铵的混合溶液,即得,其中,甘草酸重量=甘草酸铵重量/1.0207;
色谱条件:以甲醇-乙腈-0.1%磷酸溶液为流动相,洗脱比例如下表:
检测波长分别为327nm和250nm;250nm下检测槲皮苷和甘草酸,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸;色谱柱:acquityuplc®hsst3(1.8µm,2.1×100mm);柱温为35℃;
测定法:分别精密吸取对照品溶液与供试品溶液各2µl,注入液相色谱仪,测定,记录色谱图,即得。
结论:结果令人满意,可以用于控制该中药组合物的质量。
实施例2
按比例称取:连翘300g、金银花200g、板蓝根300g、大黄60g、广藿香100g、绵马贯众200g、红景天60g、薄荷脑5g、麻黄100g、苦杏仁60g、鱼腥草300g、甘草60g、石膏300g,按照以下工艺提取:
(1)按照原料药重量比例称取中药材,净选,酌情碎断;
(2)广藿香碎断,加10倍量水提取挥发油,提油时间8小时,收集挥发油,备用;提取液过滤后,残渣弃去,滤液备用;
(3)连翘、麻黄、鱼腥草、大黄,用12倍量70%的乙醇提取3次,每次2.5小时,提取液合并过滤,回收乙醇,滤液备用;
(4)金银花、石膏、板蓝根、绵马贯众、甘草、红景天,加12倍量水煎煮至沸,加入苦杏仁,煎煮2次,每次1小时,提取液合并过滤,所得滤液与步骤(2)广藿香提油后的滤液合并,浓缩成在60℃时测定相对密度为1.10-1.15的清膏,加入乙醇,调节至醇浓度为70%,冷藏放置,过滤,回收乙醇至无醇味,得清膏备用;
(5)将步骤(4)所得清膏与步骤(3)所得醇提液合并,浓缩至在60℃时测定相对密度为1.15-1.20的清膏,干燥,得干膏粉,备用;
(6)将步骤(5)所得干膏粉加入适当药学上可接受的辅料制粒;
(7)将薄荷脑、步骤(2)所得挥发油加入乙醇溶解,喷入步骤(6)所得颗粒,压片,即得。
含量测定方法:
供试品溶液制备:取所述中药组合物0.5g研细,精密称定,置具塞锥形瓶中,加50%甲醇25ml,超声提取,功率500w,频率40khz,提取30分钟,过滤,得滤液,将滤纸连同残渣一起加入具塞锥形瓶中,再加50%甲醇25ml,超声处理30分钟,过滤,用50%甲醇洗涤药渣4次,每次5ml,合并两次滤液及洗涤液,蒸干,残渣用50%甲醇溶解并定容至25ml,即得;
对照品溶液的制备:取新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷、甘草酸铵对照品适量,精密称定,加50%甲醇制成每1ml含34.4µg新绿原酸、76.7µg绿原酸、34.2µg隐绿原酸、56.2µg异连翘酯苷a、14.9µg4,5-二-o-咖啡酰奎宁酸、11.2µg槲皮苷和42.8µg甘草酸铵的混合溶液,即得,其中,甘草酸重量=甘草酸铵重量/1.0207;
色谱条件:以甲醇-乙腈-0.1%磷酸溶液为流动相,洗脱比例如下表:
检测波长分别为327nm和250nm;250nm下检测槲皮苷和甘草酸,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸;色谱柱为acquityuplc®cshtmc18;
测定法:分别精密吸取对照品溶液与供试品溶液各2µl,注入液相色谱仪,测定,记录色谱图,即得。
结论:结果令人满意可以用于控制该中药组合物的质量。
实施例3
原料药配方为:连翘278g、金银花294g、板蓝根285g、大黄55g、广藿香95g、绵马贯众290g、红景天87g、薄荷脑8.5g、麻黄88g、苦杏仁80g、鱼腥草284g、甘草95g、石膏277g,按照以下工艺提取:
(1)按照原料药重量比例称取中药材,净选,酌情碎断;
(2)广藿香碎断,加10倍量水提取挥发油,提油时间8小时,收集挥发油,备用;提取液过滤后,残渣弃去,滤液备用;
(3)连翘、麻黄、鱼腥草、大黄,用12倍量70%的乙醇提取3次,每次2.5小时,提取液合并过滤,回收乙醇,滤液备用;
(4)金银花、石膏、板蓝根、绵马贯众、甘草、红景天,加12倍量水煎煮至沸,加入苦杏仁,煎煮2次,每次1小时,提取液合并过滤,所得滤液与步骤(2)广藿香提油后的滤液合并,浓缩成在60℃时测定相对密度为1.10-1.15的清膏,加入乙醇,调节至醇浓度为70%,冷藏放置,过滤,回收乙醇至无醇味,得清膏备用;
(5)将步骤(4)所得清膏与步骤(3)所得醇提液合并,浓缩至在60℃时测定相对密度为1.15-1.20的清膏,干燥,得干膏粉,备用;
(6)将步骤(5)所得干膏粉加入适当药学上可接受的辅料制粒;
(7)将薄荷脑、步骤(2)所得挥发油加入乙醇溶解,喷入步骤(6)所得颗粒,装袋,即得。
含量测定方法:
供试品溶液制备:取所述中药组合物0.5g研细,精密称定,置具塞锥形瓶中,加甲醇25ml,回流提取,功率500w,频率40khz,提取30分钟,过滤,得滤液,将滤纸连同残渣一起加入具塞锥形瓶中,再加甲醇25ml,超声处理30分钟,过滤,用甲醇洗涤药渣4次,每次5ml,合并两次滤液及洗涤液,蒸干,残渣用50%甲醇溶解并定容至25ml,即得;
对照品溶液的制备:取新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷、甘草酸铵对照品适量,精密称定,加50%甲醇制成每1ml含34.4µg新绿原酸、76.7µg绿原酸、34.2µg隐绿原酸、56.2µg异连翘酯苷a、14.9µg4,5-二-o-咖啡酰奎宁酸、11.2µg槲皮苷和42.8µg甘草酸铵的混合溶液,即得,其中,甘草酸重量=甘草酸铵重量/1.0207;
色谱条件:以甲醇-乙腈-0.1%磷酸溶液为流动相,洗脱比例如下表:
检测波长分别为327nm和250nm;250nm下检测槲皮苷和甘草酸,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸;色谱柱为acquityuplc®behc18;
测定法:分别精密吸取对照品溶液与供试品溶液各2µl,注入液相色谱仪,测定,记录色谱图,即得。
结果:结果令人满意可以用于控制该中药组合物的质量。
实施例4
原料药配方为:按比例称取:连翘200g、金银花300g、板蓝根200g、大黄60g、广藿香60g、绵马贯众300g、红景天60g、薄荷脑9g、麻黄60g、苦杏仁100g、鱼腥草200g、甘草100g、石膏200g,按照以下工艺提取:
(1)按照原料药重量比例称取中药材,净选,酌情碎断;
(2)广藿香碎断,加10倍量水提取挥发油,提油时间8小时,收集挥发油,备用;提取液过滤后,残渣弃去,滤液备用;
(3)连翘、麻黄、鱼腥草、大黄,用12倍量70%的乙醇提取3次,每次2.5小时,提取液合并过滤,回收乙醇,滤液备用;
(4)金银花、石膏、板蓝根、绵马贯众、甘草、红景天,加12倍量水煎煮至沸,加入苦杏仁,煎煮2次,每次1小时,提取液合并过滤,所得滤液与步骤(2)广藿香提油后的滤液合并,浓缩成在60℃时测定相对密度为1.10-1.15的清膏,加入乙醇,调节至醇浓度为70%,冷藏放置,过滤,回收乙醇至无醇味,得清膏备用;
(5)将步骤(4)所得清膏与步骤(3)所得醇提液合并,浓缩至在60℃时测定相对密度为1.15-1.20的清膏,干燥,得干膏粉,备用;
(6)将步骤(5)所得干膏粉加入适当药学上可接受的辅料制粒;
(7)将薄荷脑、步骤(2)所得挥发油加入乙醇溶解,喷入步骤(6)所得颗粒,装胶囊,即得。
含量测定方法:
供试品溶液制备:取所述中药组合物0.5g研细,精密称定,置具塞锥形瓶中,加乙醇25ml,超声提取,功率500w,频率40khz,提取30分钟,过滤,得滤液,将滤纸连同残渣一起加入具塞锥形瓶中,再加乙醇25ml,超声处理30分钟,过滤,用乙醇洗涤药渣4次,每次5ml,合并两次滤液及洗涤液,蒸干,残渣用50%甲醇溶解并定容至25ml,即得;
对照品溶液的制备:取新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a、4,5-二-o-咖啡酰奎宁酸、槲皮苷、甘草酸铵对照品适量,精密称定,加50%甲醇制成每1ml含34.4µg新绿原酸、76.7µg绿原酸、34.2µg隐绿原酸、56.2µg异连翘酯苷a、14.9µg4,5-二-o-咖啡酰奎宁酸、11.2µg槲皮苷和42.8µg甘草酸铵的混合溶液,即得,其中,甘草酸重量=甘草酸铵重量/1.0207;
色谱条件:以甲醇-乙腈-0.1%磷酸溶液为流动相,洗脱比例如下表:
检测波长分别为327nm和250nm;250nm下检测槲皮苷和甘草酸,327nm下检测新绿原酸、绿原酸、隐绿原酸、异连翘酯苷a和4,5-二-o-咖啡酰奎宁酸;色谱柱为acquityuplc®behshieldrp18;
测定法:分别精密吸取对照品溶液与供试品溶液各2µl,注入液相色谱仪,测定,记录色谱图,即得。
结论:结果令人满意可以用于控制该中药组合物的质量。
- 还没有人留言评论。精彩留言会获得点赞!