一种聚苯胺-金-氧化酶纳米颗粒的制备方法及其应用与流程
本发明属于癌细胞治疗剂制备领域,特别涉及一种聚苯胺-金-氧化酶纳米颗粒的制备方法及其应用。
背景技术:
近年来恶性肿瘤呈逐渐高发的态势,成为影响人类健康的重要杀手。目前,临床中采用的传统癌症诊断和治疗手段存在突出的问题,面临着日益严峻的挑战。发展毒副作用小且具有良好癌症治疗效果的方法具有迫切的临床需求和重大的现实意义。纳米技术的发展为恶性肿瘤的有效治疗提供了新的巨大契机。特别的,联合饥饿—光热协同治疗被视为癌症治疗的新策略。葡萄糖作为一种营养物质,在肿瘤生长起着至关重要的作用。肿瘤的增殖主要依赖糖酵解,使肿瘤细胞对葡萄糖的浓度变化更加敏感。饥饿治疗利用葡萄糖氧化酶的催化糖酵解过程可以调节肿瘤微环境,一方面gox迅速消耗肿瘤细胞内的葡萄糖和氧气,产生饥饿和缺氧环境;另一方面,所产生的h2o2不仅显著增强氧化应激,而且还可以转化为羟基自由基杀死癌细胞。利用此特点,gox可以与其它治疗模式相结合实现多模态治疗。
光热治疗是近年来新兴的一种癌症治疗手段,光热纳米材料由于其治疗时间短,治疗效果明显,对人体副作用小而备受关注,其利用具备近红外光(700-950nm)吸收性能的光热转化剂所产生的热量来致死癌细胞。近红外光极少被生物组织吸收,具有良好的组织穿透性和高度的特异性,因而对正常组织和细胞几乎不会产生伤害和副作用。相反,在酸性肿瘤微环境中,光热效应被激活。因此,近红外照射可以通过局部热疗有效杀死癌细胞。目前,使用的光热剂大致分为有机和无机材料。常用的无机材料,如金属和碳纳米材料等,一般不可生物降解,具有潜在的长期毒性,这极大地限制其进一步的临床应用。相比之下,聚多巴胺和聚苯胺等有机材料,因具有良好的生物相容性、优良的光学稳定性和较高的热转换效率,受到广泛的研究和关注。
在众多基于有机材料的光热转化剂中,聚苯胺pani是目前已知的第一种对ph响应的有机光热转化材料,显示出依赖ph的光热转化性能。在碱性环境下,pani表现为基态(eb态);但在酸性条件下,当有h+掺杂时pani会由基态转化为激发态(es)态,此时光热效应被激活,可实现更显著的光热转化效果。聚多巴胺pda是一类有机大分子,可在碱性环境中通过简便的自聚合方法而形成,尺寸可调,具有较好的稳定性和生物相容性。pda有较好的吸附作用,可形成具有强亲和力的表面,是一类简便高效的表面修饰材料。
受肿瘤细胞对葡萄糖等营养物质具有高度依赖性的启发,引入葡萄糖氧化酶gox加速肿瘤部位糖酵解,原位产生大量的葡萄糖酸和h2o2,为pani转态提供良好的酸性环境,同时引起葡萄糖消耗,进而能实现饥饿治疗。于此同时,pani-pda负载的金纳米颗粒具有类过氧化氢酶活性,通过分解肿瘤内过量的h2o2产生氧气,克服肿瘤缺氧,增强肿瘤饥饿治疗。在gox产生葡萄糖酸的酸性环境下,pani完成转态,形成动态循环,实现饥饿-光热联合治疗。本专利采用聚乙烯吡咯烷酮为稳定剂,过硫酸铵为氧化剂制备聚苯胺纳米颗粒,在进行聚多巴胺pda修饰后,负载金纳米颗粒au和葡萄糖氧化酶gox,最后研究该复合纳米颗粒的体外性能。
检索国内外有关聚苯胺纳米颗粒用于癌症治疗方面的文献和专利结果发现:在本发明完成之前,还没有发现基于聚苯胺-金-氧化酶纳米颗粒的制备及其在肿瘤治疗方面的研究报道。
技术实现要素:
本发明所要解决的技术问题是提供一种聚苯胺-金-氧化酶纳米颗粒的制备方法,该方法制备过程温和,简单易行,所得产物具有良好的粒径均一性,表现出显著的催化产氧和催化产酸的能力,在肿瘤治疗领域具有一定的应用前景。
本发明以聚乙烯吡咯烷酮为稳定剂制备聚苯胺纳米颗粒,随后利用聚多巴胺对金纳米颗粒和葡萄糖氧化酶进行负载。本发明涉及了两个基本原理:
(1)利用聚乙烯吡咯烷酮的吡咯烷酮基团与聚苯胺链的氢键的相互作用,可对聚苯胺纳米颗粒提供稳定作用。
(2)利用聚多巴胺表面活性位点,实现对金纳米颗粒和葡萄糖氧化酶的有效负载。
一种载金聚苯胺纳米颗粒的制备方法,其特征在于,包括如下步骤:
(1)称取苯胺单体,将聚乙烯吡咯烷酮水溶液加入其中,冰浴搅拌5-10min后,加入氧化剂过硫酸铵水溶液,使苯胺单体聚合,搅拌反应1.5h,离心纯化后得到聚乙烯吡咯烷酮稳定的聚苯胺纳米颗粒pani;其中,苯胺与聚乙烯吡咯烷酮/过硫酸铵的质量比为1:0.78:2.3;
(2)以tris缓冲液为溶剂,配制上述pani溶液,室温搅拌10min后加入多巴胺单体水溶液,搅拌反应1h,离心纯化,得到多巴胺修饰的聚苯胺纳米颗粒pani-pda;其中,pani和pda的质量比为1:0.05;
(3)取上述pani-pda溶液,加入氯金酸,室温搅拌15-20min后,加入硼氢化钠水溶液搅拌反应2h,离心纯化后得到聚苯胺-金纳米颗粒pani-pda-au;其中,氯金酸和pani-pda的质量比为0.2:1;硼氢化钠和氯金酸的摩尔比为3:1;
(4)配制上述pani-pda-au的tris缓冲液,加入葡萄糖氧化酶gox水溶液,摇匀后震荡24h,离心纯化后得到聚苯胺-金-氧化酶纳米颗粒pani-pda-au-gox。
进一步,所述步骤(1)中聚乙烯吡咯烷酮的mw=13000,加入蒸馏水和过硫酸铵后反应体系中聚乙烯吡咯烷酮的最终浓度为5.4mg/ml。
进一步,所述步骤(1)中过硫酸铵的浓度为120mg/ml。
进一步,所述步骤(2)中多巴胺水溶液的浓度为5mg/ml。
进一步,所述步骤(3)中氯金酸的浓度为5mg/ml。
进一步,所述步骤(4)中tris缓冲液ph为8.5,所用浓度为50mm。
进一步,根据上述方法制备得到聚苯胺-金-氧化酶纳米颗粒pani-pda-au-gox。
进一步,聚苯胺-金-氧化酶纳米颗粒pani-pda-au-gox,具有显著的催化产氧和催化产酸的能力,在肿瘤治疗领域具有一定的应用前景。
有益效果
(1)本发明的制备过程温和,操作简单易行。
(2)本发明方法制备的聚苯胺-金-氧化酶纳米颗粒表现出显著的催化产氧和催化产酸的能力,在肿瘤治疗领域具有一定的应用前景。
附图说明
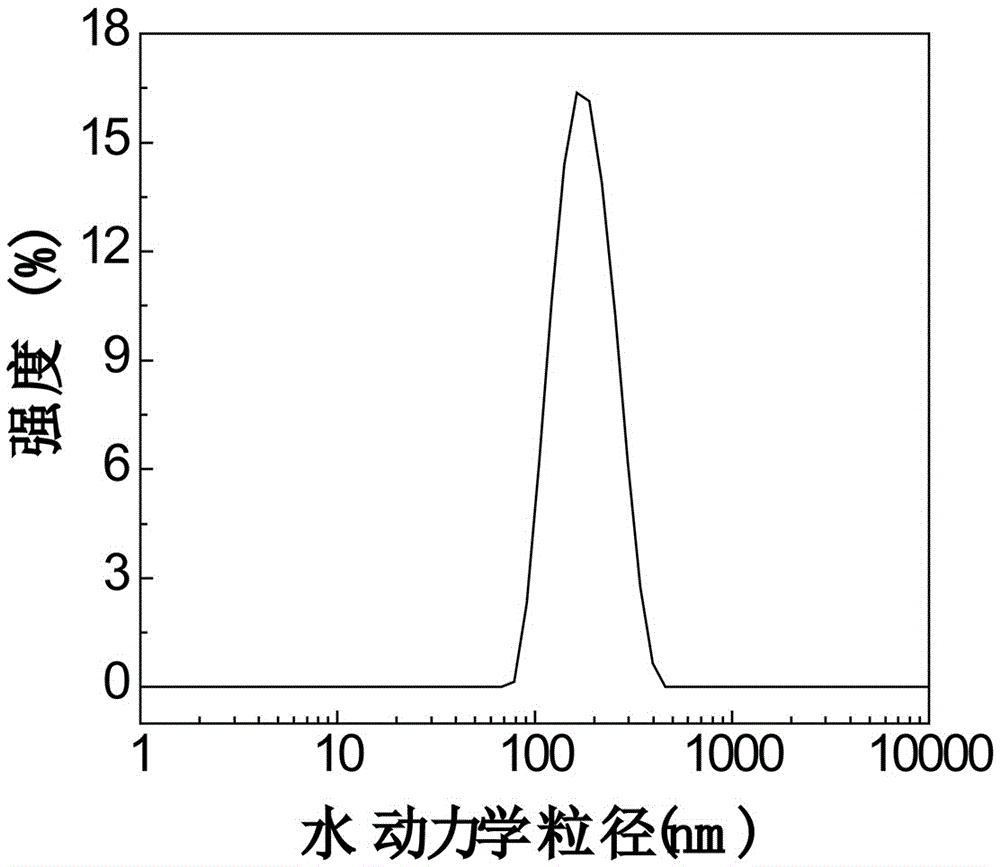
图1为实施例1中聚苯胺pani纳米颗粒的水动力学粒径。
图2为实施例2中pani-pda-au纳米颗粒的透射电镜照片。
图3为实施例3中pani-pda-au-gox纳米颗粒的水动力学粒径。
图4为实施例4中pani-pda-au纳米颗粒催化产氧结果。
图5为实施例5中pani-pda-au-gox纳米颗粒催化产酸结果。
具体实施方式
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
实施例1
配制聚苯胺水溶液,称取苯胺单体100mg,加入13ml聚乙烯吡咯烷酮水溶液(6mg/ml)。冰浴搅拌5-10min后,加入1.916ml过硫酸铵水溶液(120mg/ml)。搅拌反应1.5h,离心纯化后得到聚乙烯吡咯烷酮稳定的聚苯胺纳米颗粒pani。
激光粒度仪(dls)测试结果显示了所得复合纳米颗粒的水动力学尺寸及均一程度。参照说明书附图1。pani纳米颗粒的平均尺寸为149.2±25.2nm,单分散度为0.136±0.032。
实施例2
配制pani-pda水溶液,取8.75ml浓度为50mm的tris缓冲液加入上述所得的pani水溶液中(1.75mg/ml,20ml),室温搅拌10min,待其充分混匀后加入0.35ml多巴胺单体水溶液(5mg/ml)。搅拌反应1h,离心纯化后得到聚多巴胺修饰的聚苯胺纳米颗粒pani-pda。
取制备好的pani-pda纳米颗粒水溶液(1.25mg/ml,4ml),加入200μl氯金酸(5mg/ml),补加蒸馏水至总体积9.424ml。室温下磁力搅拌15-20min,加入576μl硼氢化钠水溶液(0.5mg/ml)搅拌反应2h,对所得溶液离心纯化3次,得到pani-pda-au纳米颗粒水溶液,保存于4℃备用。
使用透射电镜图谱表征纳米颗粒的形貌。参照说明书附图2,金纳米颗粒均匀地分散于pani-pda纳米颗粒上,实现了成功负载。
实施例3
取已制备的pani-pda-au纳米颗粒4ml(2mg/ml),按照pani-pda-au:gox=2:1的质量比加入gox的水溶液4ml(1mg/ml),随后加入3.2ml浓度为50mm的tris缓冲液,并补加蒸馏水定容至10ml。放置于振荡器上反应24h,对产物进行离心纯化(10000rpm,10min)。收集沉淀,即得到聚苯胺-金-氧化酶纳米颗粒pani-pda-au-gox。
激光粒度仪(dls)测试结果显示了所得纳米颗粒的水动力学尺寸及均一程度。参照说明书附图3。pani-pda-au-gox纳米颗粒的平均尺寸为186.7±8.1nm,单分散度为0.140±0.060。
实施例4
取2mg实施例2制备的pani-pda-au纳米颗粒,配制不同浓度的水溶液,与h2o2混合(h2o2终浓度为100mm),密封在37℃水浴中进行搅拌,之后用溶氧仪记录其氧气浓度变化。反应过程中,每0.5min记录一次溶氧值,总共记录20min。
产氧测试结果显示了所得pani-pda-au纳米颗粒的类过氧化氢酶活性。参照说明书附图4。含量变化曲线显示,与纯水相比,100ppm的纳米颗粒可催化过氧化氢产生氧气。这些数据显示所得产品具有良好的催化产氧功能。
实施例5
取实施例3制备的pani-pda-au-gox纳米颗粒(0.75mg/ml)0.25、0.5、1mg,分别与10ml的葡萄糖溶液(800ppm)混合,敞口搅拌。在反应过程中,通过ph计实时监测pani-pda-au-gox纳米颗粒与葡萄糖混合后ph值的变化。
ph变化实验显示所负载的葡萄糖氧化酶的催化性能。参照说明书附图5。实验结果显示,各组样品均显示明显的ph下降曲线。这些结果表明,该产品在肿瘤部位有望催化葡萄糖降解,达到较好的饥饿治疗效果。
- 还没有人留言评论。精彩留言会获得点赞!