一种具有一维链状结构的8‑羟基喹啉锌配合物及其制备方法与流程
本发明属于金属配合物领域,具体涉及一种具有一维链状结构的8-羟基喹啉锌配合物及其制备方法。
背景技术:
有机电致发光器件(OLED)具有视角宽、功耗低、响应速度快、工艺简单、能实现全色显示等优点,因此在平板显示和固体光源领域具有广阔的应用前景。自1987年美国的C.W.Tang首次报道采用三(8-羟基喹啉)铝(Alq3)制作有机电致发光器件以来,众多的新型有机电致发光材料(OELM,Organic Electroluminescence Materials)被成功合成来满足改善OLED器件性能的要求。
发光材料是器件中最终承担发光功能的物质,因此发光材料的发光效率、发光寿命和发光色度等性质都将对OLED的性能产生直接影响。作为OLED中的发光材料应该具备如下条件:1)具有高效率的固态荧光,无明显的浓度猝灭现象;2)具有良好的化学稳定性和热稳定性,不与电极和载流子传输材料发生反应;3)容易形成致密的非晶态薄膜并且不易结晶;4)具有适当的发光波长;5)具有良好的导电特性及一定的载流子传输能力。
8-羟基喹啉金属配合物具有良好的热稳定性、高荧光性以及其很好的电子传输功能,故成为应用到OLED中最可靠的电子传输和发射的材料之一。然而,该类金属配合物的溶解性和成膜性均较差,制备难度大,限制了该类配合物作为一种发光材料在发光器件制备领域中的规模化应用。
技术实现要素:
有鉴于此,本发明提供了一种具有一维链状结构的8-羟基喹啉锌配合物及其制备方法,本发明所提供的8-羟基喹啉锌配合物具有较高的发光强度、良好的热稳定性,以及良好的溶解性。
本发明的具体技术方案如下:
本发明提供了一种具有一维链状结构的8-羟基喹啉锌配合物,具有如式Ⅰ所示的结构:
本发明还提供了一种上述具有一维链状结构的8-羟基喹啉锌配合物的制备方法,包括:
a)将2-甲基-8-羟基喹啉和2,4-二氯苯甲醛在反应溶剂中进行反应,得到反应中间体;
b)将步骤a)得到的反应中间体依次与吡啶、水反应,得到配体;
c)将步骤b)得到的配体和锌盐在反应溶剂中进行反应,得到所述8-羟基喹啉锌配合物。
优选的,步骤a)中所述反应溶剂为乙酸酐。
优选的,步骤a)所述反应的条件为:在惰性气体的保护下进行加热回流;
所述惰性气体包括氮气、氩气或氦气;
所述加热回流的温度为140~145℃,时间为18~20h。
优选的,步骤b)在加入吡啶后先加热搅拌,然后再加入水进行回流加热。
更优选的,所述加热搅拌的温度为132~135℃,时间为20~30min;
所述回流加热的温度为132~135℃,时间为3~5h。
优选的,步骤c)中所述锌盐包括:高氯酸锌、硝酸锌和氯化锌中的一种或多种;
所述配体和锌盐的摩尔比为(3~5):(8~12)。
优选的,步骤c)所述反应溶剂为N,N-二甲基甲酰胺和甲醇的混合溶液;
所述配体和N,N-二甲基甲酰胺的比例为1mmol:(100~150)mL;
所述N,N-二甲基甲酰胺和甲醇的混合体积比为(1~4):(0.5~2)。
优选的,步骤c)中所述反应的温度为60~80℃,时间为24h。
本发明提供了一种具有一维链状结构的8-羟基喹啉锌配合物,其化学结构如式(I)所示,具有独特的一维链状结构,并表现出良好的热稳定性、溶解性和高发光强度,可作为一种性能好、成本较低、空间结构明确的新型可溶性发光小分子;本发明通过在8-羟基喹啉基团中引入氯原子,提高了配合物的溶解性和成膜性,可采用湿法加工制作相关发光器件,避免使用复杂的制备工艺和制作设备,制备成本低廉,原料来源广泛,可实现大规模的生产,具有广阔的商业化前景。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图获得其他的附图。
图1为实施例1中得到的8-羟基喹啉锌配合物的核磁共振氢谱;
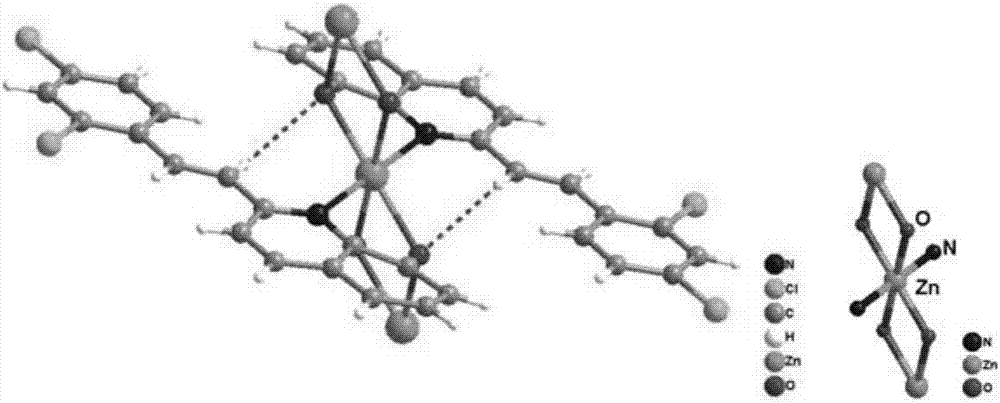
图2为实施例1中得到的8-羟基喹啉锌配合物的晶体结构图;
图3为实施例1中得到的8-羟基喹啉锌配合物的一维链状结构图;
图4为实施例1中得到的8-羟基喹啉锌配合物的PXRD图;
图5为实施例1中配体和锌盐配位的紫外滴定光谱图;
图6为实施例1中锌配合物和配体的荧光滴定光谱图;
图7为实施例1中得到的8-羟基喹啉锌配合物与配体的荧光光谱图;
图8为实施例1中得到的锌配合物的荧光寿命曲线和拟合曲线图;
图9为实施例1中得到的8-羟基喹啉锌配合物的热重分析图(TGA)。
具体实施方式
本发明提供了一种具有一维链状结构的8-羟基喹啉锌配合物,具有如式Ⅰ所示的结构:
在本发明中,所述8-羟基喹啉锌配合物晶体属于中心对称的单斜晶系,其空间群是C2/c,为一维空间聚合结构,其结构单元包含一个六配位的Zn(Ⅱ)原子核两个配体。
本发明还提供了一种上述8-羟基喹啉锌配合物的制备方法,包括:
a)将2-甲基-8-羟基喹啉和2,4-二氯苯甲醛在反应溶剂中进行反应,得到反应中间体,该反应中间体的化学名称为(E)-2-[2,4-二氯-苯基乙烯基]-8-乙酰氧基喹啉;
其中,步骤a)中涉及的反应方程式如下:
b)将步骤a)得到的反应中间体依次与吡啶、水反应,得到配体,该配体的化学名称为(E)-2-[2,4-二氯-苯基乙烯基]-8-羟基喹啉;
其中,步骤b)中涉及的反应方程式如下:
c)将步骤b)得到的配体和锌盐在反应溶剂中进行反应,得到所述8-羟基喹啉锌配合物,其分子式为Zn(C17H11Cl2NO)2;
其中,步骤c)中涉及的反应方程式如下:
在本发明中,步骤a)中所采用的反应溶剂优选为乙酸酐;
所述反应的条件为:在惰性气体的保护下进行加热回流。
进一步的,所述加热回流的温度为140~145℃,时间为18~20h;
所述惰性气体优选为氮气、氩气或氦气,更优选为氮气;
2-甲基-8-羟基喹啉和2,4-二氯苯甲醛的摩尔比优选为(1~1.5):1。
在本发明中,步骤b)中在加入吡啶后先加热搅拌,然后再加入水进行回流加热。
进一步的,所述加热搅拌的温度为132~135℃,时间为20~30min;
所述回流加热的温度为132~135℃,时间为3~5h。
在本发明中,步骤c)中所述锌盐优选为高氯酸锌、硝酸锌和氯化锌中的一种或多种,更优选为高氯酸锌;所述反应溶剂优选为N,N-二甲基甲酰胺和甲醇的混合溶液。
进一步的,所述配体和锌盐的摩尔比优选为(3~5):(8~12),更优选为4:10;
所述配体和N,N-二甲基甲酰胺的比例优选为1mmol:(100~150)mL,更优选为1mmol:125mL;
所述N,N-二甲基甲酰胺和甲醇的混合体积比优选为(1~4):(0.5~2),更优选为2:1;
所述反应的温度为60~80℃,时间为24h。
下面将结合本发明具体实施例对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例只是本发明一部分实施例,而不是全部的实施例。本领域技术人员应当理解,对本发明的具体实施例进行修改或者对部分技术特征进行同等替换,而不脱离本发明技术方案的精神,均应涵盖在本发明保护的范围中。
实施例1
(1)中间体的制备
A、称取2-甲基-8-羟基喹啉1.75g和2,4-二氯苯甲醛1.74g于100mL的圆底烧瓶中,加入10mL的乙酸酐溶解,得到混合液;
B、将步骤A得到的混合液在氮气的保护下进行磁力搅拌、145℃加热回流20h,随着反应的进行,反应溶液的颜色逐渐加深,由一开始的浅黄色转为褐色,反应溶液呈不透明浑浊状态,反应过程中还伴随少量固体析出;
C、反应溶液冷却至室温后把反应溶液倒入至100mL的冰水中,析出黄色固体,滤液用二氯甲烷萃取三次,合并三次萃取所得的有机相;用蒸馏水洗去有机相中的乙酸,然后用无水硫酸钠干燥,再减压浓缩有机相得到粗产品;
D、用石油醚/乙酸乙酯作为洗脱剂进行硅胶柱层析分离出3.46g中间体,产率为88%。
(2)配体的制备
将1g的中间体溶于装有10mL吡啶的100mL圆底烧瓶中,133℃加热搅拌30min后加入5mL水,加入水的同时,溶液迅速变成深色浑浊状态;继续加热回流反应4小时后,得到油状的粘稠物,停止反应。冷却后析出大量的粗产品固体,用石油醚/乙酸乙酯作为洗脱剂分离得到黄色粉末状配体,产率93.6%。
(3)8-羟基喹啉锌配合物的制备
将上述配体(0.004mmol)溶于DMF(0.5mL)中,再加入MeOH(0.25mL),最后加入Zn(ClO4)2(0.01mmol)的DMF溶液,密封在10mL的玻璃瓶中,80℃加热24h,冷却收集得到红色条状晶体,用MeOH洗涤,在30℃下干燥,得到产物,产率86%。其中,DMF和MeOH的体积比为2:1。
(4)8-羟基喹啉锌配合物的结构鉴定
采用核磁共振扫描了配合物的氢信号并对其氢信号进行了指认,结果如图1所示;采用傅里叶变换红外光谱仪测定产物的红外光谱数据,其特征波数(cm-1)为3050,2930,2830,1620,1550,1500,1030,1280。
采用德国布鲁克X单晶衍射仪测定该配合物产物的晶体结构,测定温度为298K,采用经石墨单色器单色化的Mo-Kα射线照射,采用扫描方式收集衍射数据,用SAINT程序进行数据还原整合得到晶体结构图,结果如图2~3所示,单晶X-射线衍射数据表明本发明配合物晶体属于单斜晶系,空间群为C2/c,为一维空间聚合结构,其结构单元包含一个六配位的Zn(Ⅱ)和两个配体。中心的Zn(II)原子接受来自两个不同配体的N和O,同时通过其他配体的苯酚氧原子将相邻中心金属Zn链接成一维无限延伸的空间结构。其中,Zn···Zn距离是围绕在Zn原子周围的Zn-N为Zn-O为和配合物3分子内存在较弱的C-H···O氢键作用(羟基O原子乙烯基上的C-H基团),∠C-H···O=128.9°,这些氢键在聚合物的Zn结构单元中发挥了重要作用。
采用PXRD对所述配合物进行测定,如图4所示,配合物的PXRD测试线和模拟曲线能较好的吻合,说明8-羟基喹啉类锌配合物为单一的纯相。
图5为配体与锌盐配位的紫外滴定光谱图,模拟了配体(L)与金属锌配位的过程,随着锌盐溶液的滴入反应逐步进行,吸收峰出现了明显变化。配体的两个主要吸收峰集中在300~400nm,298nm处的紫外吸收峰为喹啉环的信号峰,347nm左右的紫外吸收是由于电荷转移引起的。在图5中,随着锌盐的加入锌离子比例的增大,配体在347nm处的肩峰随着锌盐的加入逐渐下降,且出现了最大吸收波长发生明显的红移现象,配体在304nm处的吸收峰红移至319nm,在448nm处出现新的配合物吸收峰。从吸收峰红移的可能原因是:配合物中配体之间或者配体内部之间电荷的转移,使得苯氧环上的HOMO轨道与吡啶环上的LUMO轨道间发生π→π*电子跃迁。由图5可知,随着锌离子的不断滴入,锌离子与配体的摩尔比时刻发生变化,摩尔比大于1:2时,不再吸收曲线变化,说明配体与锌离子之间已经反应完全。
为了进一步检测配体与配合物的发光特性,我们追踪了配体和锌盐在甲醇溶液(10-4mol/L)中的荧光滴定过程。如图6所示,配体在340nm的激发光激发下,其液体荧光发射波峰为464nm(蓝色);配合物在340nm(橙黄色)的激发光激发下,其液体荧光发射波峰为608nm。从图6中可以看到配体和锌配位以后,化合物的荧光波长发生了明显的红移,我们认为原因有二:第一,金属配位后金属与配体间的π轨道反向耦合增加了主轨道电子的流动性,金属离子与配体间形成离子键;第二,配位后金属元素加入到环中使了六元环的键长增加,通过抑制苯环电子的流动和增加刚性来形成一个非辐射轨道以降低体系能量,并最终导致π~π*轨道能量的降低。
配体和配合物在室温条件下的荧光性质如图7所示,锌配合物在626nm发射峰处有很强的光致发光,激发波长是360nm,发射较强的红色光。与自由配体L1-L3相比(λem=457nm),其最带大发射波长发生了红移。这源自于配合物的配体内或者配体之间的电荷转移。
图8为配合物的荧光寿命曲线和拟合曲线图,对测试数据进行拟合,通过计算得本实施例的8-羟基喹啉锌配合物单核晶体的荧光寿命为2.90ns。
进一步对8-羟基喹啉类锌配合物单核晶体进行热重分析。测定条件为:升温速率为10℃/min,测量温度范围为20~1000℃,如图9所示,8-羟基喹啉锌配合物单核晶体在第一阶段的失重温度范围在364℃~422℃,其质量分数降低了14.97%。说明该配合物能在较高的温度下相对稳定,为真空蒸镀工艺制作器件提供了必要的条件。
综上所述,具有一维链状结构的可溶性8-羟基喹啉锌配合物晶体在DMSO中具有较好稳定性和溶解度,可有可湿法加工的性质;并且具有相对较高的发光强度和热稳定性,适合用于制备相应发光器件。
显然,本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!