CDHR3作为肿瘤诊断标志物的应用的制作方法
本发明涉及生物医药领域,具体涉及cdhr3作为肿瘤诊断标志物的应用,更具体的涉及cdhr3作为骨肉瘤诊断标志物、cdhr3激动剂在骨肉瘤治疗中的应用。
背景技术:
:cdhr3基因定位于染色体的7q22.3区域,是一种包含六个外钙黏蛋白结构域的跨膜蛋白,其可介导同源性细胞的黏附,参与细胞分化、细胞间相互作用等过程。研究表明其在极早期哮喘形成中起重要作用的基因,但还没有报道表明其与骨肉瘤相关。骨肉瘤是一种起源于骨间叶细胞的原发性恶性骨肿瘤,发病年龄多为8-25岁,社会危害性极大,其血行转移发生早且发生率高,进展迅速,80%的患者在确诊时己有微小转移灶。随着化学治疗、手术技术、骨重建等治疗方法的发展,5年总体生存率得到较大提高。但是,近年来骨肉瘤的治疗遇到瓶颈,尤其是在骨肉瘤早期转移上,即骨肉瘤的早期诊断成为临床亟待解决的问题。肿瘤标志物的研究使得骨肉瘤的早期诊断成为可能。肿瘤标志物的存在或量变可以提示肿瘤的性质,借以了解肿瘤的组织发生、细胞分化、细胞功能,以帮助肿瘤的诊断、分类、预后判断以及治疗指导。不过由于骨肉瘤发病率低,约为0.3/万,导致样本收集困难,没有被深入研究,目前骨肉瘤的分子标志物并不多。本发明对骨肉瘤病例样本进行高通量测序,结合生物信息学分析和分子生物学实验,挑选出与骨肉瘤密切相关的基因cdhr3,cdhr3有望成为骨肉瘤诊断标志物,为其临床诊断提供参考,为骨肉瘤患者带来希望。技术实现要素:本发明的目的在于提供一种骨肉瘤诊断制剂,该制剂检测cdhr3基因和/或cdhr3蛋白的表达。本发明的目的在于提供检测cdhr3基因或蛋白的制剂在制备骨肉瘤诊断试剂中的应用。进一步,骨肉瘤患病组中cdhr3基因或蛋白的表达水平与正常对照组织或者癌旁组织相比,表达水平低。进一步,检测cdhr3基因或蛋白在生物学样品中的表达水平是通过检测cdhr3部分或全部mrna和/或检测编码cdhr3蛋白的部分或全部氨基酸序列进行。优选的,生物学样品为来源于患者的生物样品,包括细胞、组织等,可以是血液或者尿液等,优选为外周血。进一步,骨肉瘤诊断制剂采用荧光定量pcr试剂盒、基因芯片方法、测序方法检测骨肉瘤生物学样品中cdhr3基因的表达。优选的,所述的荧光定量pcr试剂盒中含有一对特异性扩增cdhr3基因的引物;所述的基因芯片中包括与cdhr3基因的核酸序列杂交的探针。更优选的,荧光定量pcr试剂盒内含有特异性检测cdhr3基因的上游引物和下游引物,上游引物序列为seqidno.1,下游引物序列为seqidno.2。荧光定量pcr法是通过荧光染料或荧光标记的特异性的探针,对pcr产物进行标记跟踪,实时在线监控反应过程,结合相应的软件可以对产物进行分析,计算待测样品模板的初始浓度。基因芯片又称为dna微阵列(dnamicroarray),可分为三种主要类型:1)固定在聚合物基片(尼龙膜,硝酸纤维膜等)表面上的核酸探针或cdna片段,通常用同位素标记的靶基因与其杂交,通过放射显影技术进行检测。2)用点样法固定在玻璃板上的dna探针阵列,通过与荧光标记的靶基因杂交进行检测。3)在玻璃等硬质表面上直接合成的寡核苷酸探针阵列,与荧光标记的靶基因杂交进行检测。进一步,骨肉瘤诊断制剂采用免疫方法检测生物学样品中cdhr3蛋白的表达。优选的,免疫方法为elisa检测和/或胶体金检测。进一步,检测cdhr3蛋白的elisa法为使用elisa检测试剂盒。所述试剂盒中的抗体可采用市售的cdhr3单克隆抗体或多克隆抗体。进一步,elisa检测试剂盒包括:包被cdhr3抗体的固相载体,酶标抗体,酶的底物,蛋白标准品,阴性对照品,稀释液,洗涤液,酶反应终止液等。进一步,胶体金检测采用胶体金免疫层析技术或胶体金渗滤法。进一步,所述的胶体金检测试剂盒硝酸纤维素膜上的检测区(t)喷点有抗cdhr3抗体、质控区(c)喷点有免疫球蛋白igg。酶联免疫吸附实验(elisa)即将已知的抗原或抗体吸附在固相载体表面,使酶标记的抗原抗体反应在固相表面进行的技术。elisa检测试剂盒根据检测目的和操作步骤可分为间接法、双抗夹心法、竞争法、双位点一步法、捕获法测igm抗体、应用亲和素和生物素的elisa。elisa检测试剂盒中生色底物可选择辣根过氧化物酶(hrp)或者碱性磷酸酶(ap)。免疫胶体金检测技术:(1)免疫胶体金光镜染色法细胞悬液涂片或组织切片,可用胶体金标记的抗体进行染色,也可在胶体金标记的基础上,以银显影液增强标记,使被还原的银原子沉积于已标记的金颗粒表面,可明显增强胶体金标记的敏感性。(2)免疫胶体金电镜染色法可用胶体金标记的抗体或抗抗体与负染病毒样本或组织超薄切片结合,然后进行负染。可用于病毒形态的观察和病毒检测。(3)斑点免疫金渗滤法应用微孔滤膜作载体,先将抗原或抗体点于膜上,封闭后加待检样本,洗涤后用胶体金标记的抗体检测相应的抗原或抗体。(4)胶体金免疫层析法将特异性的抗原或抗体以条带状固定在膜上,胶体金标记试剂(抗体或单克隆抗体)吸附在结合垫上,当待检样本加到试纸条一端的样本垫上后,通过毛细作用向前移动,溶解结合垫上的胶体金标记试剂后相互反应,当移动至固定的抗原或抗体的区域时,待检物与金标试剂的结合物又与之发生特异性结合而被截留,聚集在检测带上,可通过肉眼观察到显色结果。本发明的目的在于提供一种治疗骨肉瘤的制剂,所述制剂中含有促进cdhr3基因的转录或表达的试剂或化合物。进一步的,所述的cdhr3基因和/或基因的表达产物在骨肉瘤组织中低表达。本领域人员熟知促进基因及其表达产物的表达通常可以采用下述方法中的一种和/或几种:激活基因的启动子、激活基因表达的蛋白或因子、导入促进基因转录或表达的载体。优选的,治疗骨肉瘤的制剂中含有促进cdhr3基因的转录或表达的载体和/或激活cdhr3基因的启动子和/或激活cdhr3基因表达的蛋白或因子。本发明的目的在于提供上述治疗骨肉瘤的制剂在制备骨肉瘤治疗药物或试剂中的应用。本发明的药剂学上可接受的载体为在制剂时通常利用的载体,该载体包含乳糖(lactose)、右旋糖(dextrose)、蔗糖(sucrose)、山梨醇(sorbitol)、甘露醇(mannitol)、淀粉、阿拉伯橡胶、磷酸钙、藻酸盐(alginate)、凝胶(gelatin)、硅酸钙、微晶纤维素、聚乙烯吡咯烷酮(polyvinylpyrrolidone)、纤维素(cellulose)、水、糖浆、甲基纤维素(methylcellulose)、羟基苯甲酸甲酯(methylhydroxybenzoate)、丙基羟基苯甲酸丙酯(propylhydroxybenzoate)、滑石、硬脂酸镁(stearicacidmagnesium)及矿物油(mineraloil)等,但并非局限于此。本发明的药剂学可接受的载体除了上述成分以外还可以包含润滑剂、湿润剂、甜味剂、香味剂、乳化剂、悬浮剂、防腐剂等。药剂学上许可的适合的载体和制剂详细记载于雷明登氏药学全书。本发明的药剂学组合物能通过口服或非口服进行给药,作为非口服给药时,能通过静脉内注射,鼻腔内注射,局部注射,脑室内注射,脊髓腔注射,皮下注射,腹腔注射,经皮给药等方式进行给药。本发明的药剂学组合物的适合的给药剂量根据制剂化方法、给药方式、患者的年龄、体重、性别、病态、食物、给药时间、给药途径、排泄速度及反应灵敏性之类的因素而可以进行多种处方,通常,熟练的医生能够容易地决定及处方对所希望的治疗或预防有效的给药剂量。本发明的药剂学组合物根据本发明所属
技术领域:
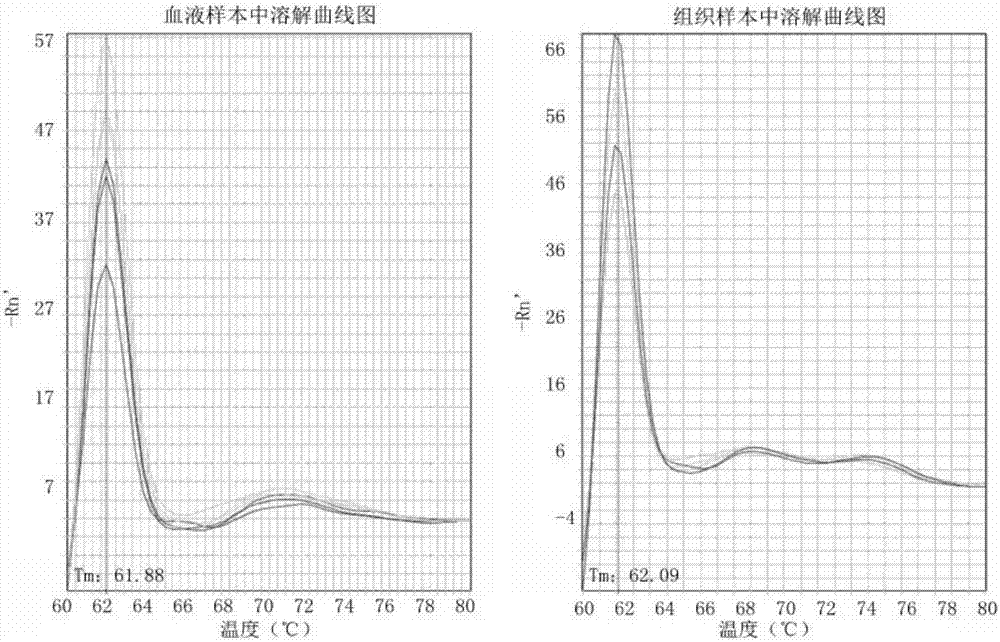
的普通技术人员可以容易实施的方法,利用药剂学上能接受的载体和/或赋形剂来进行制剂化,从而能够以单位用量形态制备或者内装在多容量容器内来制备。此时,剂型是油性或者水性介质中的溶液、悬浮液或乳化液形态,或者也可以是浸膏剂、粉末剂、颗粒剂、片剂或者胶囊剂形态,还可以包括分散剂或者稳定剂。本发明的目的在于提供一种检测骨肉瘤的基因检测试剂盒,所述试剂盒检测基因cdhr3,采用特异的上游引物和下游引物,上游引物序列为seqidno.1,下游引物序列为seqidno.2。进一步,该pcr试剂盒适合于目前存在市场上的所有类型荧光定量基因扩增仪,灵敏度高,定量快速准确、稳定性好,具有良好的应用前景。进一步,上述荧光定量pcr试剂盒组分包括:特异性引物、内参引物、荧光定量pcr反应液。所述内参为gapdh。所述的试剂盒还包含rna抽提试剂。本发明目的是提供了一种骨肉瘤蛋白检测试剂盒,所述的检测试剂盒检测cdhr3蛋白。进一步的,所述的试剂盒还包括其他检测试剂。本发明目的是提供了一种检测骨肉瘤的基因芯片,所述的基因芯片包括与cdhr3基因的核酸序列杂交的探针。附图说明图1是rt-pcr扩增曲线图图2是rt-pcr溶解曲线图图3是在组织样本中cdhr3相对表达量图图4是在血液样本中cdhr3相对表达量图具体实施方式下面结合具体实施例,进一步阐述本发明,仅用于解释本发明,而不能理解为对本发明的限制。本领域的普通技术人员可以理解:在不脱离本发明的原理和宗旨的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由权利要求及其等同物限定。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照厂商所建议的条件实施检测。实施例1高通量测序及分析分别收集10例骨肉瘤病例样本及5例正常对照组织,其中10例骨肉瘤病例样本中5例原发样本、5例转移样本。进行rna提取,rna提取后琼脂糖凝胶电泳,从电泳结果可以初步判定提取的rna样品质量合格与否,是否可以用于进一步的转录组分析。进而通过nanodrop1000分光光度计检测rna样品的提取情况,rna-seq测序的样品要求:od260/od280为1.8-2.2。测序平台为illumina公司的hiseq2500高通量测序平台,进行高通量转录组深度测序,测序后我们运用fast-qc软件对测序数据的质量进行整体评估,包括碱基的质量值分布,质量值的位置分布,gc含量,pcrduplication含量,kmer的frequency等。在差异基因表达分析时,根据得到的fpkm值,采用国际公认算法ebseq进行差异筛选。其中,筛选时,log2fc>1或<-1,fdr<0.05。为了更好的理解差异表达基因的功能,我们对差异表达基因进行了geneonlogy和信号通路分析,并对差异表达基因进行功能注释和蛋白质互相作用网络分析,鉴于以上数据分析的结果,结合文献我们筛选了在骨肉瘤组下调表达明显基因cdhr3。实施例2骨肉瘤组及正常组cdhr3基因表达情况一材料和方法1、材料收集17例骨肉瘤组织样本、28例骨肉瘤血液样本,6例正常骨组织对照、20例正常血液样本对照,对其进行分组及编号。组织提取:患者初次手术时,在无菌操作下术中提取组织样本,每块切成黄豆大小,取出后迅速放入冻存管中,并尽快置于液氮中。血液提取:患者确认后及时采集病例的外周血标本3-5毫升,迅速放入edta抗凝管中,尽快置于-80℃冰箱。2、方法2.1骨肉瘤及正常对照总rna的提取采用reagent(invitrogen,货号15596-018)进行样本rna提取,实验操作按产品说明书进行。提取后,用nanodrop2000紫外分光光度计测量rna纯度及浓度,冻存于-70℃。rna质量判定标准:rna样本的od260/od280值为1.7-2.2之间;总rna电泳图谱有清晰的28s、18s条带;70℃水浴保温1小时后的电泳图谱与水浴保温前的图谱无明显差异。2.2逆转录合成cdna采用primescripttmrtreagentkitwithgdnaeraser(perfectrealtime)(货号:rr047b)进行cdna反转录,首先去除基因组dna反应,在试管中加入5×gdnaeraserbuffer2.0ul,gdnaeraser1.0ul,totalrna1ug,加rnasefreeh20使总体积至10ul,水浴锅中加热2min,再将primescriptrtenzymemixi1.0ul,rtprimermix1.0ul,5×primescriptbuffer2(forrealtime)4.0ul,rnasefreedh204.0ul,混合后加入上述试管中一起混合共20ul,水浴锅中37℃加热15min,85℃加热5sec,合成的cdna需要长期保存时,请于-20℃或更低温度保存。2.3real-timepcr2.3.1仪器及分析方法用abi7300型荧光定量pcr仪,采用法进行数据的相对定量分析。2.3.2引物设计采用在线引物设计软件,引物设计后由invitrogen公司合成。具体引物序列如下:表1操作过程如下:(一)反应体系:表2试剂使用量2×superrealpremixplus10μl上游引物(10um)0.6μl下游引物(10um)0.6μl50×roxreferencedye△2μldna模板2ul灭菌蒸馏水4.8ul扩增程序为:95°15min,(95℃10sec,55℃30sec,72℃32sec)×40个循环,95℃15sec,60℃60sec,95℃15sec)。(二)引物筛选将各样本cdna混合后,以此为模板进行3倍梯度稀释,稀释后样品各取2μl作模板,分别用目的基因引物和内参基因引物进行扩增(见表3),同时在60-95℃进行融解曲线分析,根据扩增效率高和溶解曲线单峰原则进行引物筛选。表3(三)样品realtimepcr检测将各样品cdna3倍稀释后取2μl作模板,分别用目的基因引物和内参基因引物进行扩增。同时在60-95℃进行溶解曲线分析。二实验结果实时定量pcr扩增曲线拐点清楚,扩增曲线整体平行性好,表明各反应管的扩增效率相近,极限平而无上扬现在,曲线指数期斜率较大,说明扩增效率较高(见图1);样本扩增产物溶解曲线都是单峰,说明扩增产物只有一条,为特异性扩增(见图2);根据qrt-pcr的相对定量公式:2-δδct,比较cdhr3基因在骨肉瘤组织和正常组织、骨肉瘤血液样本和正常对照血液样本中的表达水平。结果显示:qrt-pcr扩增结果稳定,在组织样本中,cdhr3在骨肉瘤组的表达水平是正常对照组的0.15倍(具体见图3),在血液样本中,cdhr3在骨肉瘤组的表达水平是正常对照组的0.53倍(具体见图4),以上结果验证了高通量转录组表达数据的整合分析cdhr3在骨肉瘤组中低表达的结果。本发明采用高通量测序筛选出骨肉瘤相关基因cdhr3,结合分子生物学实验证实了cdhr3是骨肉瘤诊治标志物。sequencelisting<110>北京泱深生物信息技术有限公司<120>cdhr3作为肿瘤诊断标志物的应用<160>4<170>patentinversion3.3<210>1<211>22<212>dna<213>人工序列<400>1gcagaaggtctacacctctaca22<210>2<211>22<212>dna<213>人工序列<400>2ggaatgtttcggcttgtgtctt22<210>3<211>21<212>dna<213>人工序列<400>3ggagcgagatccctccaaaat21<210>4<211>23<212>dna<213>人工序列<400>4ggctgttgtcatacttctcatgg23当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 普适型用于同时检测多种肿瘤标志物的微流控芯片装置的制造方法
- 男性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 女性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 一种检测口腔癌的标志物及其试剂盒的制造方法与工艺
- microRNA 标志物组及其在制备检测胃癌淋巴结转移试剂盒中的应用的制造方法与工艺
- 基于弹性蛋白酶荧光底物检测乳腺癌肿瘤标志物CA153的酶联免疫试剂盒制备方法与制造工艺
- 检测和评价力量训练效果的miRNA标志物或其组合及其应用的制造方法与工艺
- 一种最优超平面的构建方法、动态优化系统和构建装置与制造工艺
- 癌症标志物及癌症的判定方法与制造工艺
- 检测尿液中单羟酚类代谢物的试剂盒及其制备方法与制造工艺