一种八氢二吡咯并喹啉类化合物的制备方法与流程
本发明涉及化学合成
技术领域:
,特别涉及一种八氢二吡咯并喹啉类化合物的制备方法。
背景技术:
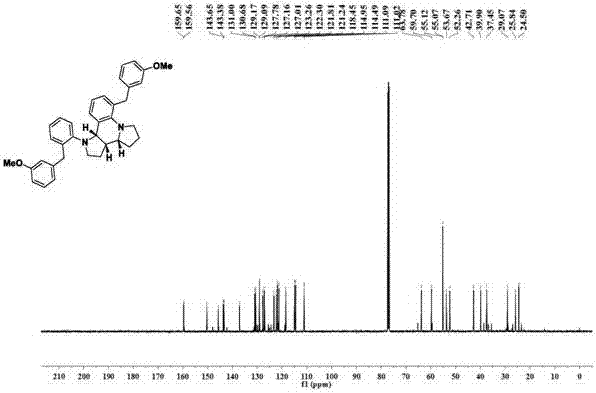
:八氢二吡咯并喹啉骨架是天然产物incargranineb和seneciobipyrrolidine基本骨架的非对映体。目前,生产类似骨架化合物的方法如:所使用的催化剂为:该方法使用手性磷酸和银催化剂成本高,有污染。技术实现要素:针对现有技术中存在的问题,本发明的目的在于提供一种苯基-2-吡咯烷基苄醇类化合物在酸性条件下生成八氢二吡咯并喹啉化合物的方法。具体反应式如下:其中,r1,r2,r3均为h、ch3或och3。苯基-2-吡咯烷基苄醇类化合物以pa(联萘酚磷酸)为催化剂,以甲苯为溶剂,在60℃的条件下,反应24小时,制得八氢二吡咯并喹啉化合物;其中苯基-2-吡咯烷基苄醇类化合物与pa的摩尔比为10:2;溶剂甲苯的用量为:每mmol苯基-2-吡咯烷基苄醇类化合物添加10ml。联萘酚磷酸:反应原理:本发明以苯基-2-吡咯烷基苄醇类化合物在酸性条件下脱水生成碳正离子,四氢吡咯邻位碳上的氢以氢负离子的形式迁移到碳正离子,原位上生成亚胺正离子,其中的一部分亚胺正离子通过质子转移转变为烯胺,烯胺分子与含有亚胺正离子的分子发生分子间的[4+2]环加成反应得到八氢二吡咯并喹啉化合物。本发明实现了通过氢迁移策略构建了八氢二吡咯并喹啉化合物,不需要金属催化剂,绿色环保,成本低廉。附图说明:图1为本发明实施例2产物的核磁共振1h谱;图2为本发明实施例2产物的核磁共振13c谱;图3为本发明实施例3产物的核磁共振1h谱;图4为本发明实施例3产物的核磁共振13c谱;图5为本发明实施例4产物的核磁共振1h谱;图6为本发明实施例4产物的核磁共振13c谱。具体实施方式实施例1以3-甲氧基苯基-2-吡咯烷基-1-基苯基甲醇为例,来制备反应过程如表1所示,将0.2mmol与催化剂(20mol%)混合后加入到2ml的溶剂中,在60℃的条件下反应,反应时间如表中所示,来检查最终产物的产率,结果如表1所示。表1:反应条件及结果催化剂(20mol%)溶剂t/℃time/hyield/%b1csadce6072202tfohdce6072423tfadce60725842,4-二硝基苯甲酸dce6072525padce6048796pachcl36024867patoluene6024968padmf6048619pah2o60246510pathf60246911padcm60247312padioxane60486513paetoh60246714pach3cn604852表1中的17中,dce先进行干燥,干燥的方法为:在每升dce中加入cah25g,于130℃下蒸馏;b:柱色谱分离产率。实施例2原料:3-甲氧基苯基-2-吡咯烷基-1-基苯基甲醇反应条件:甲苯,60℃,pa(20%)产物:化学式:c36h38n2o2精确分子量:530.2933分子量:530.7120结构式:产率:96%,dr5:1.1hnmr(500mhz,cdcl3)δ7.15(dt,j=14.9,7.7hz,4h),7.04–6.96(m,2h),6.79–6.62(m,9h),6.50(t,j=7.5hz,1h),4.80(d,j=8.4hz,1h),4.06(s,2h),3.94–3.81(m,3h),3.74(d,j=12.0hz,6h),3.65(dd,j=10.2,5.4hz,2h),3.53(dd,j=16.1,7.9hz,1h),3.42(td,j=8.5,4.0hz,1h),3.20(td,j=8.7,2.7hz,1h),2.89(dd,j=15.8,8.4hz,1h),2.73(td,j=10.6,2.9hz,1h),2.07–2.00(m,1h),1.98–1.74(m,6h);13cnmr(125mhz,cdcl3)δ159.65,159.56,150.33,145.68,143.65,143.38,137.12,131.00,130.68,129.17,129.09,127.94,127.78,127.16,127.01,123.26,122.30,121.81,121.24,118.45,114.95,114.49,111.09,111.02,63.78,59.70,55.12,55.07,53.67,52.26,42.71,39.90,37.45,29.07,25.84,24.50;hrms(esi):calcdforc36h38n2o2[m+h]+:531.3012,found:531.3014.实施例3原料:4-甲氧基苯基-2-吡咯烷基-1-基苯基甲醇反应条件:甲苯,60℃,pa(20%)产物:化学式:c36h38n2o2精确分子量:530.2933分子量:530.7120结构式:产率:92%,dr5:1.1hnmr(500mhz,cdcl3)δ7.20–7.15(m,1h),7.12(d,j=7.2hz,1h),7.01(dd,j=9.0,5.2hz,4h),6.99(dd,j=5.3,2.0hz,2h),6.80–6.78(m,1h),6.78–6.73(m,4h),6.65(dd,j=9.1,3.7hz,1h),6.49(t,j=7.5hz,1h),4.79(d,j=8.5hz,1h),4.02(d,j=5.2hz,2h),3.88(dd,j=10.6,7.7hz,1h),3.80–3.76(m,1h),3.74(d,j=6.0hz,6h),3.72(d,j=5.3hz,1h),3.65–3.60(m,1h),3.52(dd,j=16.3,7.8hz,1h),3.42(td,j=8.6,4.1hz,1h),3.23–3.18(m,1h),2.89(dt,j=8.7,6.9hz,1h),2.72(qd,j=8.3,3.2hz,1h),2.06–1.98(m,1h),1.96–1.73(m,6h);13cnmr(125mhz,cdcl3)δ157.73,157.71,150.23,145.76,137.81,133.98,133.85,130.94,130.62,130.23,129.65,127.72,127.69,127.07,123.27,122.27,118.44,113.72,113.67,63.75,59.84,55.27,55.26,53.75,52.25,42.82,39.06,36.55,29.07,25.86,24.57;hrms(esi):calcdforc36h38n2o2[m+h]+:531.3012,found:531.3011.实施例4原料:3,5-二甲基苯基-2-吡咯烷基-1-基苯基甲醇反应条件:甲苯,60℃,pa(20%)产物:化学式:c38h42n2精确分子量:526.3348分子量:526.7680结构式:产率:90%,dr5:1.1hnmr(500mhz,cdcl3)δ7.33–7.29(m,1h),7.24(d,j=7.6hz,1h),7.18–7.07(m,3h),6.93(d,j=6.2hz,2h),6.91(d,j=6.0hz,3h),6.88(s,2h),6.82–6.80(m,1h),6.64(t,j=7.5hz,1h),4.96(d,j=8.4hz,1h),4.19(dd,j=26.1,9.8hz,2h),4.04(d,j=15.5hz,1h),3.90(d,j=15.5hz,1h),3.80–3.75(m,1h),3.67(dd,j=16.1,8.1hz,1h),3.58(td,j=8.6,4.3hz,1h),3.34(td,j=8.5,3.4hz,1h),3.07–3.00(m,1h),2.88(ddd,j=18.3,8.4,3.1hz,1h),2.37(d,j=0.6hz,12h),2.35(s,1h),2.29(s,1h),2.21–2.13(m,1h),2.10–1.95(m,5h),1.95–1.88(m,1h);13cnmr(125mhz,cdcl3)δ150.21,141.85,141.61,137.73,137.59,137.58,131.07,130.75,127.73,127.44,127.35,127.33,127.03,126.69,123.24,122.28,118.44,63.73,59.92,53.53,52.30,42.81,39.80,37.36,29.16,25.80,24.59,21.41,21.41,21.39,21.32;hrms(esi):calcdforc38h42n2[m+h]+:527.3426,found:527.3429.以上所述,仅是本发明的较佳实施例而已,并非是对本发明作其它形式的限制,任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更或改型为等同变化的等效实施例。但是凡是未脱离本发明技术方案内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与改型,仍属于本发明技术方案的保护范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1