一种粉末型细胞培养基的锤式生产方法与流程
本发明涉及一种粉末型细胞培养基的锤式生产方法,属于生物
技术领域:
。
背景技术:
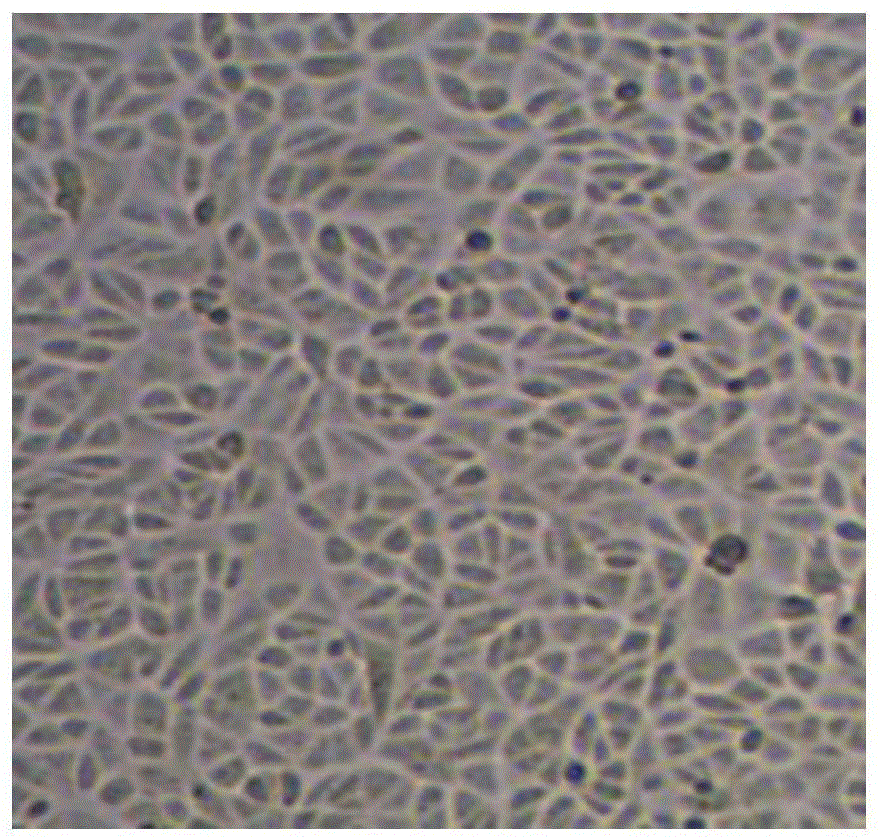
:合成细胞培养基是一种人工配制的适合细胞生长营养要求的混合物质,一般为从体液、血清消化液等天然成分配制而成的培养基,以及应用化学原料配制而成的合成培养基或综合培养基。从培养基的物理性质而论,可以分成加入凝固剂的固体培养基、液体培养基和粉末培养基。国内大部分的企业都是采用传统的球磨方式。球磨虽然结构简单,但钢珠的清洗及搬运费时费力,效率低下,工作噪音大,占地面积大,增加了生产成本和生产时间。另外,球磨工艺采用的是批次生产,造成单批产能有限,批与批之间的批间差较大,产品的稳定性不好。国内疫苗、抗体产业不断发展,规模越来越大,细胞培养基的需求量也越来越大。现有球磨粉碎工艺中,通过传统的不锈钢球在密闭空间内的撞击,使颗粒状原料转变为粉末状原料,同时在球磨过程中产生的热量无法及时有效的传递出去,导致原料发生质变或结块,最终球磨结束后的粉末状原料粒度无法完全保障,如果继续采用球磨方式会很大程度降低培养基的年产能。技术实现要素:为解决上述问题,本发明的目的是提供一种安全、快速、便捷的培养基生产工艺,可完全保证原料粉碎过程中的温度控制及粉碎后粒度大小,不会出现变质或结块。本发明的第一个目的是提供一种粉末型细胞培养基的锤式生产方法,包括如下步骤:(1)分别称量无机盐组分、氨基酸组分、维生素组分、碳氮源组分及微量元素;(2)将步骤(1)称量好的原料预混合5~60min;(3)将步骤(2)混合好的物料,加入锤式粉碎机中,转速2000~14000r/min粉碎20~50min,在粉碎过程中,物料温度控制为5~50℃;(4)将步骤(3)粉碎后的原料终混合20~60min,得到粉末型细胞培养基。进一步地,在步骤(2)中,所述的预混合在三维混合机中进行。进一步地,在步骤(2)中,所述的预混合时间优选为10~40min。进一步地,在步骤(3)中,所述的粉碎优选为在转速3000~13000r/min粉碎30~40min,在粉碎过程中,物料温度控制为10~40℃。进一步地,在步骤(4)中,所述的终混合在三维混合机中进行。进一步地,在步骤(4)中,所述的终混合的时间为30~40min。进一步地,所述的无机盐组分为氯化钠、氯化钾、氯化钙、硫酸镁、四水硝酸钙、无水磷酸二氢钠、无水磷酸氢二钠、六水氯化镁、无水磷酸二氢钾中的一种或一种以上组合。进一步地,所述的氨基酸组分为丙氨酸、精氨酸、谷氨酸、苯丙氨酸、胱氨酸、半胱氨酸、亮氨酸、异亮氨酸、谷氨酰胺、缬氨酸、丝氨酸、色氨酸、赖氨酸、组氨酸、羟脯氨酸、甲硫氨酸、天门冬氨酸、门冬酰胺、苏氨酸、脯氨酸、酪氨酸中的一种或一种以上组合。进一步地,所述的维生素组分为维生素b1、维生素b2、维生素b6、维生素b12、维生素h、叶酸、肌醇、d-泛酸钙、烟酰胺、谷胱甘肽、氯化胆碱、盐酸吡哆醛、亚油酸、维生素c、对氨基苯甲酸中的一种或一种以上组合。进一步地,所述的碳氮源组分为无水葡萄糖、丙酮酸盐、植物水解蛋白中的一种或一种以上组合。进一步地,本发明还包括对粉末型细胞培养基进行包装的步骤。进一步地,将粉末型细胞培养基使用桶或袋进行包装,桶装优选无菌塑料桶进行包装,袋装优选无菌尼龙袋和铝箔袋进行双层包装。本发明的有益效果是:本发明通过以上技术方案,不仅能够生产出稳定均一的细胞培养基,并且其占地面积小,能不间断连续生产,产量大,批间差小及产品性质稳定,能够节约生产成本和生产时间,节约投资资金。附图说明图1为细胞培养72小时照片。具体实施方式下面结合具体实施例对本发明作进一步说明,以使本领域的技术人员可以更好地理解本发明并能予以实施,但所举实施例不作为对本发明的限定。实施例1:dmem/f12培养基生产(1)原料分种类称量,其分种类称量时各组分含量为:表1无机盐组分无机盐mg/l氯化钙116.6硫酸铜0.0013九水合硝酸铁0.05七水合硫酸亚铁0.417氯化钾311.8六水氯化镁28.64无水硫酸镁48.84氯化钠6999.5无水磷酸二氢钠54.35无水磷酸氢二钠71.02七水合硫酸锌0.432表2氨基酸组分氨基酸mg/ll-盐酸精氨酸147.5l-胱氨酸盐酸盐31.29l-谷氨酰胺365甘氨酸18.75l-盐酸组氨酸31.48l-异亮氨酸54.47l-亮氨酸59.05l-盐酸赖氨酸91.25l-甲硫氨酸17.24l-苯丙氨酸35.48l-丝氨酸26.25l-苏氨酸53.45l-丙氨酸4.45l-门冬酰胺7.5l-门冬氨酸6.65l-盐酸半胱氨酸17.56l-谷氨酸7.35l-脯氨酸17.25l-色氨酸9.02l-酪氨酸38.4l-缬氨酸52.85表3维生素组分维生素mg/l亚油酸0.042硫辛酸0.105d-生物素0.0035泛酸钙2.24氯化胆碱8.98叶酸2.65肌醇12.6烟酰胺2.02盐酸吡哆醛2维生素b60.031维生素b20.219维生素b12.17维生素b120.68表4碳氮源组分与微量元素组分mg/l无水葡萄糖3151次黄嘌呤2苯酚红8.11,4-丁二胺二盐酸盐0.081丙酮酸钠55胸苷0.365(2)对称量好的原料进行预混合将称量好的各组原料按顺序加入三维运动混合机中。加料完成后,开启混合机,混合30分钟,使其在锤式粉碎前形成相对均一的物料。(3)将预混好的原料进行粉碎将预混好的相对均一的物料匀速加入锤式粉碎机中,转速调整至10000r/min,同时锤式粉碎机应开启冷水冷却系统,使物料温度控制在10℃-40℃,整个粉碎过程持续30分钟。粉碎结束后,关闭冷水冷却系统。(4)将粉碎好的半成品进行终混将粉碎好的半成品再加入三维运动混合机中。加料完成后,开启混合机,混合40分钟,以确保成品的均一性。(5)将终混的成品进行包装对终混好的成品进行包装,采用无菌塑料桶或内层无菌尼龙袋、外层无菌铝箔袋的方法进行包装,即得终产品。性能测试:依据国家化工行业标准《哺乳类动物细胞培养基》hg/t3935-2007进行检测:(1)澄清度按照中华人民共和国药典2015年版二部附录ixb澄清度检查法,分别检测新制的实施例和市售球磨dmem/f12干粉培养基和在室温、相对湿度50%的环境下储存30天后的实施例和市售球磨dmem/f12干粉培养基与蒸馏水混合后形成的培养基液体。对于干粉培养基,取配制1升的用量,置于1000ml烧杯中,加水1000ml,搅拌至溶解。测试结果如下表5所示:表5培养基澄清度从表5的结果可以看出,本发明的干粉培养基无论是新制还是存储一段时间后,都能达到与市售的干粉培养基相同水平的澄清度。(2)ph值按照中华人民共和国药典2015年版二部附录vihph值测定法,用ph计分别检测新制的实施例和市售球磨dmem/f12干粉培养基和在室温、相对湿度50%的环境下储存30天后的实施例和市售球磨dmem/f12干粉培养基。对于干粉培养基,取配制1升的用量,置于1000ml烧杯中,加水1000ml,搅拌至溶解。测试结果如下表6所示:表6培养基ph从表6的结果可以看出,本发明的干粉培养基无论是新制还是存储一段时间后,都能达到与市售的干粉培养基相同水平。(3)干燥失量按照中华人民共和国药典2015年版二部附录viiil干燥失重测定法,分别检测制的实施例和市售球磨dmem/f12干粉培养基和在室温、相对湿度50%的环境下储存30天后的实施例和市售球磨dmem/f12干粉培养基。测试结果如下表7所示:表7培养基干燥失重从表7的结果可以看出,本发明的干粉培养基无论是新制还是存储一段时间后,都能达到与市售的干粉培养基相同水平。(4)渗透压按照中华人民共和国药典2015年版二部附录ixg渗透压摩尔浓度测定法,分别检测新制的实施例和市售球磨dmem/f12干粉培养基和在室温、相对湿度50%的环境下储存30天后的实施例和市售球磨dmem/f12干粉培养基。对于干粉培养基,取配制1升的用量,置于1000ml烧杯中,加水1000ml,搅拌至溶解。测试结果如下表所示:表8培养基渗透压从表8的结果可以看出,本发明的干粉培养基无论是新制还是存储一段时间后,都能达到与市售的干粉培养基相同水平。(5)细菌内毒素按照中华人民共和国药典2015年版附录xie细菌内毒素检查法中的凝胶法,分别检测新制的实施例和市售球磨dmem/f12干粉培养基和在室温、相对湿度50%的环境下储存30天后的实施例和市售球磨dmem/f12干粉培养基。对于干粉培养基,取配制1升的用量,置于1000ml烧杯中,加水1000ml,搅拌至溶解。取0.1ml培养基(液体)加入细菌内毒素检查用水(美国acc)3.9ml,混匀即得试验溶液。测试结果如下表所示:表9培养基细菌内毒素从表9的结果可以看出,本发明的干粉培养基无论是新制还是存储一段时间后,都能达到与市售的干粉培养基相同水平。符合本行业标准对内毒素水平的要求(<10eu/ml)。(6)微生物限度按中华人民共和国药典2015年版附录xij微生物限度检查法进行,检查项目为细菌数、霉菌数,检查法为平皿法。称取干粉培养基样品10g,加入ph7.0无菌氯化钠-蛋白胨缓冲液摇匀至充分溶解,混合即得试验溶液。测试结果如下表所示:表10培养基微生物限度从表10的结果可以看出,本发明的干粉培养基无论是新制还是存储一段时间后,都能达到与市售的干粉培养基相同水平。符合本行业标准对微生物限度的要求(<200cfu/g的细菌)。(7)细胞生长实验将实施例和市售球磨dmem/f12干粉培养基分别取1l量,溶于900ml超纯水中,向所得混合物中加入100ml小牛血清混合,然后用超纯水定容至1000ml。使用0.20μm的滤菌膜过滤灭菌,即得培养液。在无菌条件下,用灭菌移液器将10ml上述两种培养液转移到t25细胞培养瓶中,接种vero细胞悬液,接种密度为5×104细胞/cm2。然后在(37±1)℃温度条件及(5±0.1)%二氧化碳体积分数条件下进行贴壁培养,培养72h,观察细胞形态,并计数。培养结果见表11,细胞培养72小时的照片见图1。由图1可以看出,被培养的细胞密度大,细胞轮廓清晰。表11培养72h细胞个数(8)粉末颗粒度将实施例和市售球磨dmem/f12干粉培养基分别取100g量,相对湿度40%的环境下使用150目筛网进行过筛,测量过筛率,结果见表12。表12培养基过筛率从以上结果可以看出,本发明所制的培养基与市售球磨干粉培养基的性质并无差异,某些指标甚至优于市售球磨干粉培养基。以上所述实施例仅是为充分说明本发明而所举的较佳的实施例,本发明的保护范围不限于此。本
技术领域:
的技术人员在本发明基础上所作的等同替代或变换,均在本发明的保护范围之内。本发明的保护范围以权利要求书为准。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1