一类氟硼近红外荧光染料及在非质子性溶剂中微量乙醇的检测上的应用的制作方法
本发明涉及有机合成及分析检测领域,具体的涉及bf2-2-(芳乙烯基)-8-(2-苯并咪唑)喹啉类化合物的合成及其它们的分析检测的用途,尤其是应用于非质子性溶剂中乙醇含量的检测。
背景技术:
乙醇是基本的有机化工原料,可用来制取乙醛、乙醚、乙酸乙酯、乙胺等化工原料,也是制取染料、涂料、洗涤剂等产品的原料。同时,乙醇在我们的生活中不可或缺。因此,常常需要对非质子性溶剂中的乙醇含量进行测定。
目前已经有许多分析方法、技术用于测定有机溶剂中乙醇的含量,例如经典的重铬酸钾氧化比色法、滴定法、密度瓶法、基于液相色谱法、气相色谱法的色谱法,基于红外光谱法、紫外-可见光谱法和荧光法的光谱法等。其中基于荧光法的光谱法因其具有方便、快速、高灵敏度和选择性等特点,在乙醇含量测定方面也引许多研究者的兴趣。比率型的荧光探针是在两个不同波长下测定荧光强度(或吸光度),并以其比值作为测定信号,因此其可以通过内置的校正消除环境因素、光源稳定性、探针浓度等因素的干扰,从而使检测结果不受光源强度。仪器灵敏度、探针浓度、环境因素的影响,克服了传统荧光探针所存在的缺点,故比率型荧光探针分子可以得到更精确的检测结果,进而提高检测方法的灵敏度和更宽的动态响应范围,受到了越来越多的关注。此外,基于比色基的荧光检测能实现乙醇含量的原位检测和实时监控,在医药、化工、食品、材料等领域有良好的应用前景。
技术实现要素:
本发明的目的是提供一类用于探测非质子有机溶剂中乙醇含量的荧光探针及其制备方法与应用。
本发明所提供的荧光探针,是以对乙醇含量敏感的氟硼络合物作为荧光探针,该荧光探针由三部分组成,其中a部分为缺电子的苯并咪唑喹啉氟硼配位单元,d部分为供电子的(取代)芳(杂)环单元,a和d通过双键(π)单元相连,形成推拉电子d-π-a体系:
其中a单元中r1~r9为h-或f-,cl-、cf3-取代;d单元为给电子基(取代)五元芳杂环或六元芳香环。
其中d单元包括五元芳杂环包括呋喃、吡咯、噻吩,六元环为(r-取代的)苯系芳香环、(取代)五元、六元稠杂环。
其中(取代)五元、六元稠包括9-取代咔唑、3-(7-取代)香豆素、2-吲哚环及3-吲哚环。
其中d单元取代基r包括烷基(甲基、乙基、异丙基、叔丁基,优选甲基和叔丁基)、羟基、烷氧基(甲氧基、乙氧基、苯氧基、优选甲氧基)、氨基及取代氨基(包括n,n-二甲基、n,n-二乙基、n,n-二苯基、哌啶基、哌嗪基、吗啉基、四氢吡咯基)等。
所述氟硼络合物进一步优选为以下具体化合物:
本发明一种比率型荧光探针分子的应用方法的优点在于:
本发明提供的比率型氟硼荧光探针分子检测乙醇含量的方法依赖的化学反应机制,亲核性乙醇分子进攻探针分子中缺电子硼中心,分解配合物,得到配体。配体及配合物均是推拉电子的d-π-a体系。与配体相比,硼与苯并咪唑喹啉络合后,氟硼的吸电子作用也明显增加了整个分子的偶极作用,增加了供电子基团在分子内的电子转移,从而使其荧光发射光谱红移,荧光发射光谱颜色发生明显改变;同时苯并咪唑及喹啉环的自由旋转受到限制,减少了非辐射的能量损失,从而荧光强度增强,可以自然光及紫外灯下裸眼识别乙醇分子。
本发明提供的比率型氟硼荧光探针分子,乙醇分子存在时,其荧光荧光发射峰减弱,出现配体的吸收峰和荧光发射峰且随着乙醇含量的增加逐渐增强。通过检测两个不同波长下荧光发射强度,并分别以其比值作为测定信号,实现了比色和荧光双通道的乙醇含量的定量检测,可有效地避免因仪器本身、环境以及探针浓度等外界因素造成的干扰。
本发明提供的比率型氟硼荧光探针分子的制备是苯并咪唑喹啉提供活泼的甲基与取代醛,通过knoevenagel反应后进一步与三氟化硼乙醚溶液反应得到的d-π-a结构的喹啉及苯并咪唑中的n形成四配位的六元环硼化合物。配体和探针分子合成均具有合成工艺简单、收率高、纯度高、成本低廉、操作简便优点。
本发明提供的比率型氟硼荧光探针分子检测非质子性溶剂中的乙醇含量,包括烷烃(链烃、环烃等)、芳香烃(苯、甲苯等)、卤代烃(二氯甲烷、三氯甲烷、1,2-二氯乙烷等)、醚类溶剂(乙醚、四氢呋喃、二氧六环等)、酮类(丙酮、戊酮等)、腈类(乙腈)、n,n-二甲基甲酰胺、二甲亚砜等,适用范围广泛。
相对于传统的非质子性有机溶剂中乙醇的测定方法,本法在实用中具有以下突出的优点:(1)合成方法简单,易于生产,成本低廉;(2)对乙醇响应快、灵敏度高、结果准确;(3)检测方式多样,即可荧光吸光光度法;也可裸眼定性,又可比率定量;即可在自然光下,又可在紫外灯下观察;(4)操作简单,感应体系可在待测液中直接形成,无需样品前处理过程,十分利于原位检测和在线实时监控使用;(5)适用范围广,既可应用于不同非质子性有机溶剂中乙醇的测定,又可应用于不同含乙醇量范围的待测体系。
附图说明
图1为实施例6所制备的配体及荧光探针的结构。
图2为实施例6所制备的荧光探针在不同溶剂中紫外吸收图。
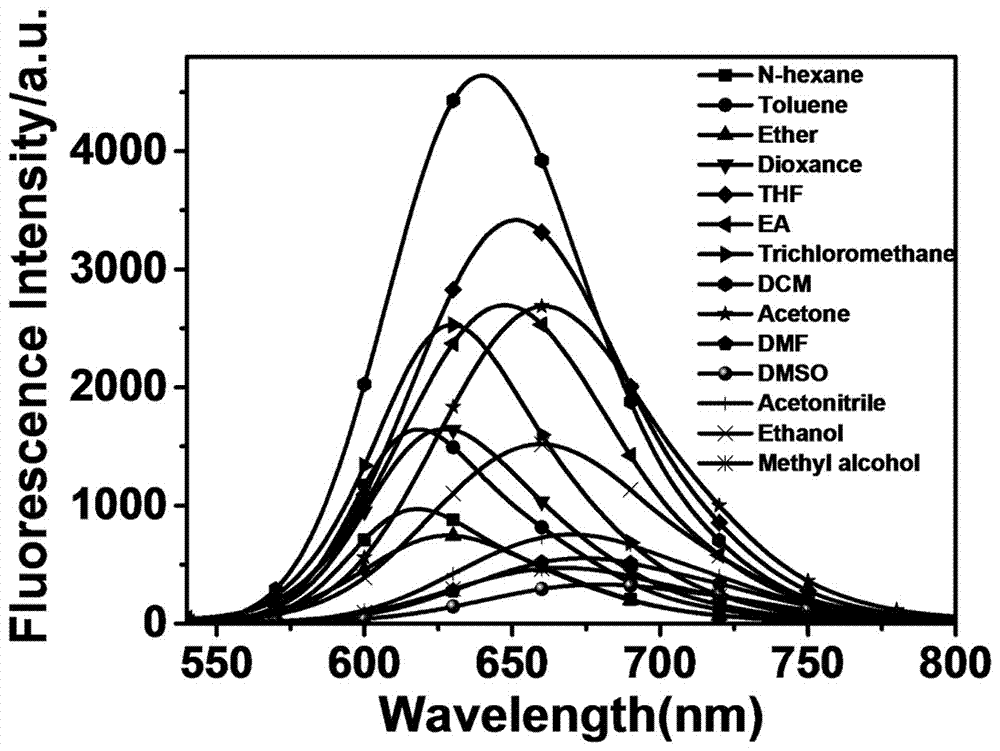
图3为实施例6所制备的荧光探针在不同溶剂中荧光发射图。
图4为实施例6所制备的荧光探针检测乙腈中乙醇含量的荧光发射光谱。
图5为实施例6所制备的荧光探针检测乙腈中乙醇含量的荧光发射比(f570/f667)随乙醇含量变化线性关系图。
具体实施方式
实施例1配体1和荧光探针1的合成
(1)配体1的合成
向50ml两口瓶中依次加入0.51g2-甲基-8苯并咪唑基喹啉(1.9mmol),含0.31g苯甲醛(2.9mmol),10ml甲醇,0.57ml哌啶(4.8mmol),0.33ml冰乙酸(4.8mmol),回流8h,冷却,有黄色固体析出,抽滤得固体,用甲醇洗涤滤饼3次,得黄色固体0.58g,产率:78.4%,熔点179.3~179.5℃。1hnmr(400mhz,cdcl3)δ13.73(s,1h),9.12(dd,j=7.4,1.1hz,1h),8.25(d,j=8.6hz,1h),7.89(dd,j=11.0,7.5hz,2h),7.78–7.63(m,6h),7.52–7.45(m,3h),7.42(t,j=7.3hz,1h),7.35–7.30(m,2h);ms,m/z(%):347.7(m+,100)。
(2)荧光探针1的合成
向50ml两口瓶中依次加入0.35g配体1(1.0mmol),10ml氯仿,1.47ml三乙胺,氮气保护下,在0℃下缓慢滴加1.10ml三氟化硼乙醚,回流6h,有大量固体析出,抽滤,用氯仿洗涤滤饼3次,得固体0.25g,产率:63.3%。
1hnmr(400mhz,cdcl3)δ9.26(d,j=7.6hz,1h),8.65–8.54(m,2h),8.24(d,j=8.6hz,1h),8.00(d,j=7.4hz,1h),7.94(d,j=6.3hz,1h),7.91–7.83(m,2h),7.78(d,j=7.2hz,2h),7.69(d,j=16.3hz,1h),7.51(d,j=7.3hz,3h),7.35(dd,j=5.5,2.8hz,2h);ms,m/z(%):395.2(m+,100)。
实施例2配体3和荧光探针3的合成
(1)配体3的合成
向50ml两口瓶中依次加入0.51g2-甲基-8苯并咪唑基喹啉(1.9mmol),含0.39g苯甲醛(2.9mmol),10ml甲醇,0.57ml哌啶(4.8mmol),0.33ml冰乙酸(4.8mmol),回流8h,冷却,有黄色固体析出,抽滤得固体,用甲醇洗涤滤饼3次,得黄色固体0.48g,产率:65.7%,熔点187.2~187.6℃。1hnmr(400mhz,cdcl3)δ13.80(s,1h),9.10(dd,j=7.5,1.4hz,1h),8.20(d,j=8.6hz,1h),7.88(d,j=12.9hz,1h),7.86–7.79(m,1h),7.76–7.55(m,6h),7.39–7.29(m,3h),7.05–6.97(m,2h);ms,m/z(%):377.6(m+,100)。
(2)荧光探针3的合成
向50ml两口瓶中依次加入0.38g配体3(1.0mmol),10ml氯仿,1.47ml三乙胺,氮气保护下,在0℃下缓慢滴加1.10ml三氟化硼乙醚,回流6h,有大量固体析出,抽滤,用氯仿洗涤滤饼3次,得固体0.19g,产率:42.2%。
1hnmr(400mhz,cdcl3)δ9.26–9.11(m,1h),8.65–8.37(m,2h),8.19(d,j=9.0hz,1h),7.93(d,j=7.9hz,2h),7.90–7.77(m,2h),7.69(dd,j=25.9,12.4hz,3h),7.43–7.30(m,2h),7.01(d,j=8.7hz,2h),3.90(s,3h);13cnmr(100mhz,dmso)δ161.6,160.2,158.1,157.3,148.8,144.2,144.2,137.8,136.1,135.1,131.6,131.1,130.1,129.1,128.6,127.2,126.4,125.8,123.9,119.4,115.0,114.3,55.2;ms,m/z(%):426.1(m+,100)。
实施例3配体5和荧光探针5的合成
(1)配体5的合成
向50ml两口瓶中依次加入0.51g2-甲基-8苯并咪唑基喹啉(1.9mmol),含0.43g苯甲醛(2.9mmol),10ml甲醇,0.57ml哌啶(4.8mmol),0.33ml冰乙酸(4.8mmol),回流8h,冷却,有黄色固体析出,抽滤得固体,用甲醇洗涤滤饼3次,得黄色固体0.68g,产率:87.1%。1hnmr(400mhz,cdcl3)δ13.93(br,1h),9.07(dd,j=7.5,1.5hz,1h),8.14(d,j=8.7hz,1h),7.91–7.88(m,1h),7.81(dd,j=8.0,1.4hz,1h),7.68–7.58(m,6h),7.33–7.31(m,2h),7.22(s,1h),6.78(d,j=8.8hz,2h),3.06(s,6h);ms,m/z(%):390.1(m+,100)。
(2)荧光探针5的合成
向50ml两口瓶中依次加入0.39g配体5(1.0mmol),10ml氯仿,1.47ml三乙胺,氮气保护下,在0℃下缓慢滴加1.10ml三氟化硼乙醚,回流6h,有大量固体析出,抽滤,用氯仿洗涤滤饼3次,得固体0.34g,产率:77.1%。
1hnmr(400mhz,cdcl3):δ9.15(s,1h),8.45–8.38(m,2h),8.18(d,1h),7.92–7.89(m,2h),7.87–7.84(m,1h),7.78(t,1h),7.67-7.60(m,3h),7.36–7.30(m,6h),7.20–7.13(m,6h),7.09(d,2h);13cnmr(100mhz,cdcl3)δ152.5,144.6,141.6,137.2,131.6,130.9,130.9,129.6,127.6,123.4,122.8,122.7,120.5,120.5,118.8,114.0,112.0,111.7;ms,m/z(%):438.1(m+,100)。实施例4配体6和荧光探针6的合成
(1)配体6的合成
向50ml两口瓶中依次加入0.51g2-甲基-8苯并咪唑基喹啉(1.9mmol),0.79g(2.9mmol)4-甲酰基三苯胺,10ml正丁醇,0.57ml(4.8mmol)哌啶,0.33ml(4.8mmol)冰乙酸,回流8h,冷却,有黄色固体析出,抽滤得固体,用乙醇洗涤滤饼3次,得黄色固体0.83g,产率82.1%。熔点186.1~187.0℃。1hnmr(cdcl3,400mhz),δ:13.85(s,1h),9.11(d,j=7.4hz,1h),8.21(d,j=8.6hz,1h),7.85(d,j=8.0hz,2h),7.78–7.42(m,6h),7.32(ddd,j=7.6,6.8,4.2hz,7h),7.23–7.04(m,8h)。ms,m/z(%):514.6(m+,100)。
(2)荧光探针6的合成
向50ml两口瓶中依次加入0.52g(1.0mmol)配体6,10ml氯仿,1.35ml三乙胺,氮气保护下,在0℃下缓慢滴加0.98ml三氟化硼乙醚,回流6h,冷却,有固体析出,抽滤,用氯仿洗涤3次,干燥,得红色固体0.24g,产率42.3%。
1hnmr(cdcl3,400mhz),δ:9.11(dd,j=7.5,1.4hz,1h),8.43(t,j=14.0hz,2h),8.17(d,j=9.0hz,1h),7.91(dt,j=5.0,2.5hz,2h),7.85(dd,j=6.3,2.7hz,1h),7.77(t,j=7.7hz,1h),7.63(dd,j=15.8,12.7hz,3h),7.39–7.29(m,6h),7.17(dd,j=17.8,7.5hz,6h),7.09(d,j=8.7hz,2h);13cnmr(cdcl3,100mhz),δ:158.6,150.7,146.5,146.4,143.8,142.6,137.0,136.2,131.2,130.6,130.1,129.6,129.4,127.9,127.8,127.2,125.8,125.2,124.6,123.8,123.6,123.4,122.1,120.9,120.8,120.0,119.9,118.0,114.2。ms,m/z(%):562.5(m+,100)。
实施例5配体7和荧光探针7的合成
(1)配体7的合成
向50ml两口瓶中依次加入0.51g2-甲基-8苯并咪唑基喹啉(1.9mmol),含0.54g苯甲醛(2.9mmol),10ml甲醇,0.57ml哌啶(4.8mmol),0.33ml冰乙酸(4.8mmol),回流8h,冷却,有黄色固体析出,抽滤得固体,用甲醇洗涤滤饼3次,得黄色固体0.39g,产率:47.6%,1hnmr(400mhz,cdcl3)δ13.63(s,1h),9.12(dd,j=7.4,1.5hz,2h),8.57–8.49(m,4h),8.15(d,j=8.8hz,2h),7.92(tdd,j=5.8,3.8,1.9hz,6h),7.84(t,j=7.7hz,2h),7.68–7.48(m,11h),7.41–7.35(m,4h);ms,m/z(%):426.3(m+,100)。
(2)荧光探针7的合成
向50ml两口瓶中依次加入0.43g配体7(1.0mmol),10ml氯仿,1.47ml三乙胺,氮气保护下,在0℃下缓慢滴加1.10ml三氟化硼乙醚,回流6h,有大量固体析出,抽滤,用氯仿洗涤滤饼3次,得固体0.18g,产率:40.1%。
1hnmr(400mhz,cdcl3)δ9.18(dd,j=7.4,1.5hz,2h),8.57–8.49(m,4h),8.15(d,j=8.8hz,2h),7.92(tdd,j=5.8,3.8,1.9hz,6h),7.84(t,j=7.7hz,2h),7.68–7.48(m,11h),7.41–7.35(m,4h);ms,m/z(%):474.1(m+,100)。
实施例6配体18和荧光探针18的合成
(1)配体18的合成
向50ml单口瓶中依次加入0.6021g(2.4mmol)3-醛基-7-二乙基氨基香豆素,0.5103g(1.9mmol)2-甲基-8苯并咪唑基喹啉,10ml正丁醇,搅拌,再加入0.24ml哌啶,0.13ml冰醋酸,加分水器分水,150℃下搅拌。10h后有大量红色沉淀产生,停止反应,冷却,抽滤得红色固体,用乙醇洗涤所得固体。再抽滤得产物,干燥,称重得0.3687g固体,产率41%,熔点250~252℃。1hnmr(400mhz,cdcl3):δ13.78(s,1h),9.06(d,j=7.5hz,1h),8.29–7.99(m,1h),7.97-7.50(m,7h),7.42–7.28(m,3h),6.59(dd,j=8.8,2.3hz,1h),6.47(d,j=2.1hz,1h),3.42(d,j=7.1hz,4h),1.24(t,j=7.1hz,6h)
(2)荧光探针18的合成
取0.1034g(0.205mmol)配体18于两口瓶中,氮气保护下,依次加入2ml氯仿,0.2ml三乙胺,加热回流,未全溶,补加2ml氯仿,继续加热回流,固体全部溶解,呈红色,缓慢加入0.2mlbf3·et2o,有大量白烟生成,溶液变成紫色,继续搅拌回流,3h后tlc跟踪仍有原料点,补加0.2mlbf3·et2o和1ml氯仿,继续搅拌回流,2h后抽滤,得固体0.06102g,产率60%。
1hnmr(400mhz,dmso)δ9.09(d,j=9.0hz,1h),8.99(d,j=7.5hz,1h),8.89(m,3h),8.75(d,j=9.3hz,1h),8.53(d,j=7.8hz,1h),8.32(s,1h),8.12(m,2h),8.00–7.85(m,1h),7.64(d,j=9.1hz,1h),7.61–7.55(m,1h),6.85(d,j=11.3hz,1h),6.68(s,1h),3.19–2.92(m,4h),1.18(t,j=7.3hz,6h).
实施例7测试溶液的配制
(1)标准溶液的配制
称取一定量的荧光探针配制成浓度为10-3mol/l的乙腈溶液
(2)不同含乙醇量非质子性溶液的配制
分别移取10-3mol/l的乙腈溶液于若干25ml容量瓶中并除去乙醇,再加入不同量的乙醇(加入量为0.01,0.02,0.05,0.10,0.20,0.50,1.00,2.00,5.00,10.00,15.00,20.00),然后用待测溶剂定容。
实施例8非质子性溶剂中乙醇含量的检测
荧光发射分光光度法光谱的测定是荧光仪上进行,将待测溶液置于1cm石英比色皿中,激发波长475nm,
分别测定不同乙醇含量下探针的荧光探针分子和配体分子荧光发光强度,计算其比值,以相对发光强度比值-非质子性溶剂中乙醇含量作图,绘制标准曲线,计算得到检测乙醇含量的检测限和线性范围。其中,根据最低检出限公式(lod=3σ/b)计算,在荧光分光光度法荧光探针对非质子性溶剂中乙醇含量的检测的lod为:3.43%。
- 还没有人留言评论。精彩留言会获得点赞!