一种量子点掺杂二氧化硅@硫化铜荧光光热探针的制备方法及其应用与流程
本发明涉及纳米探针技术领域,具体涉及一种量子点掺杂二氧化硅@硫化铜荧光光热探针的制备方法及其应用。
背景技术:
近年来,纳米材料在生物医学领域得到了广泛研究,并取得了大量成果。成像技术在疾病的诊断、监控和研究中处于十分重要的地位。传统的成像方式已被广泛的研究并应用于临床,如超声波成像、核磁共振成像等,但是传统的成像方式都存在各自的缺点。基于纳米材料的荧光成像,被视为一种具有荧光强度高、稳定性好的医学成像方式,这是由于纳米荧光材料的发光机理是基于材料本身的能级结构,不收外界环境的干扰,从而具有良好的发光特性。同时由于纳米材料的能级随其尺寸的变化而变化,因此其发光波长也会随着发生变化。通过调控纳米材料的尺寸可以实现对其发光波长的调控。临床上对于癌症的治疗手段主要包括手术治疗、辐射治疗、化疗、药物治疗等,但是这些手段都存在一定的缺点。纳米材料的光热治疗则具有无痛、非介入性的特点,因此被视为治疗癌症最方便、合理的手段。研究最为普遍的材料是纳米金属材料和纳米半导体材料,如金纳米笼、硫化铜纳米颗粒等。每种材料都有其各自的缺点,例如金纳米材料结构稳定性差、光学性质易受周围环境影响,硫化铜的光热转换效率偏低、生物相容性差等。
技术实现要素:
为了得到一种集荧光示踪、光热治疗于一身的探针,本发明的目的在于提供一种量子点掺杂二氧化硅@硫化铜荧光光热探针的制备方法。
本发明的另一目的在于提供所述方法制备的荧光光热探针。
本发明的还一目的在于提供所述制备方法及其制备的探针在肿瘤治疗中的应用。
为实现上述目的,本发明首先提供一种量子点掺杂二氧化硅@硫化铜荧光光热探针的制备方法,所述方法包括以下步骤:
(1)量子点掺杂的二氧化硅的制备:
a.首先配备氨水溶液:按比例混合乙二醇或乙醇与氨水得氨水溶液,所述乙二醇或乙醇与氨水的体积比是1:0.1-100;
b.将荧光量子点与二氧化硅源滴加入配备好的氨水溶液中,所述荧光量子点与二氧化硅源的摩尔比为1:1-1000,氨水与二氧化硅源的体积比为1:0.1-1000;
d.对步骤b混合溶液进行持续室温搅拌1-4天后离心洗涤,然后用3-氨丙基三甲氧基硅氧烷或氨丙基三乙氧基硅烷进行氨基化室温搅拌修饰24小时,最后进行离心洗涤,得氨基化的量子点掺杂的二氧化硅溶液,所述3-氨丙基三甲氧基硅氧烷或氨丙基三乙氧基硅烷与二氧化硅源的体积比为1:0.01-100;
(2)量子点掺杂的二氧化硅/硫化铜结构的制备:
向步骤(1)得到的氨基化的量子点掺杂的二氧化硅溶液中加入带修饰基团的硫化铜颗粒,混合溶液室温搅拌1-5天,然后对混合溶液进行离心修洗涤,所述量子点掺杂二氧化硅颗粒与修饰基团的硫化铜颗粒的摩尔比为1:1-100;
(3)量子点掺杂二氧化硅@硫化铜荧光光热探针的制备:
量子点掺杂的二氧化硅/硫化铜复合结构表面的修饰基团与多种生物分子进行交联反应,得量子点掺杂二氧化硅@硫化铜荧光光热探针。
为了增大二氧化硅的孔径,优选的,步骤(1)中b与c之间,还包括加入所述扩孔剂的步骤,所述扩孔剂与二氧化硅源的体积比为1:10-1000。加入扩孔剂可得到不同孔径的量子点掺杂的二氧化硅结构。所述扩孔剂包括十六烷基溴化铵、1,3,5-三甲基苯或癸烷等。
在一优选实施方案中,所述方法包括以下步骤:
(1)量子点掺杂的二氧化硅的制备:
a.首先配备氨水溶液:按比例混合乙二醇或乙醇与氨水得氨水溶液,所述乙二醇或乙醇与氨水的体积比是1:0.2;
b.将荧光量子点与二氧化硅源滴加入配备好的氨水溶液中,所述荧光量子点与二氧化硅源的摩尔比为1:5-50,氨水与二氧化硅源的体积比为1:0.1-1;
c.向步骤b混合溶液加入扩孔剂,所述扩孔剂与二氧化硅源的体积比1:1-20;
d.对步骤c混合溶液进行持续室温搅拌1-4天后离心洗涤,然后用3-氨丙基三甲氧基硅氧烷或氨丙基三乙氧基硅烷进行氨基化室温搅拌修饰24小时,最后进行离心洗涤,得氨基化的量子点掺杂的二氧化硅溶液,所述3-氨丙基三甲氧基硅氧烷或氨丙基三乙氧基硅烷与二氧化硅源的体积比为1:10-100;
(2)量子点掺杂的二氧化硅/硫化铜结构的制备:
向步骤(1)得到的氨基化的量子点掺杂的二氧化硅溶液中加入带修饰基团的硫化铜颗粒,混合溶液室温搅拌1-5天,然后对混合溶液进行离心修洗涤,所述量子点掺杂二氧化硅颗粒与修饰基团的硫化铜颗粒的摩尔比为1:20-100;
(3)量子点掺杂二氧化硅@硫化铜荧光光热探针的制备:
量子点掺杂的二氧化硅/硫化铜复合结构表面的修饰基团与多种生物分子进行交联反应,得量子点掺杂二氧化硅@硫化铜荧光光热探针。
本发明通过液相反应方式制备量子点掺杂的二氧化硅球@硫化铜的复合探针。在量子点掺杂二氧化硅结构的制备过程中,加入扩孔剂增大二氧化硅结构的孔径尺寸;在硫化铜制备阶段,通过改变硫源和铜源的比例得到具有不同缺陷电子结构的硫化铜,从而可以改变硫化铜的吸收特性。复合探针可以同时实现对特定癌细胞的荧光标记和光热治疗;利用多孔二氧化硅的多孔结构实现对药物分子的有效负载;量子点被包裹于探针内部,可以提高量子点的荧光强度和降低量子点的生物毒性;硫化铜被链接到二氧化硅表面,可以提高硫化铜的光热效应和其生物相容性。
优选的,所述荧光量子点包括cdtes、cdse、碳点、锰掺杂量子点、agins、agznins中的任何一种或几种。
优选的,所述二氧化硅源可以是正硅酸四乙酯、2-(3,4-环氧环己烷)乙基三甲氧基硅烷、(3-巯丙基)三甲氧基硅烷、(3-巯丙基)三乙氧基硅烷、巯丙基甲基二甲氧基硅烷中的任何一种或几种。
优选的,步骤(2)中所述修饰的硫化铜颗粒包括羧基修饰的硫化铜颗粒、柠檬酸修饰的硫化铜、抗坏血酸修饰的硫化铜、半胱氨酸修饰的硫化铜、硫代乙醇酸修饰的硫化铜、硬脂酸修饰的硫化铜中的任意一种。
优选的,所述生物分子包括抗体、dna片段和生物配体中的任意一种。
在一最优选实施方案中,所述方法包括以下步骤:
(1)量子点掺杂的二氧化硅的制备:
a.首先配备氨水溶液:按比例混合乙二醇与氨水得氨水溶液,所述乙二醇与氨水的体积比是1:0.2;
b.将荧光量子点cdse与(3-巯丙基)三甲氧基硅烷滴加入配备好的氨水溶液中,所述荧光量子点cdse与(3-巯丙基)三甲氧基硅烷的摩尔比为最佳为1:20,氨水与(3-巯丙基)三甲氧基硅烷的体积比为1:0.625;
c.向步骤b混合溶液加入扩孔剂十六烷基溴化铵,所述十六烷基溴化铵与(3-巯丙基)三甲氧基硅烷的体积比1:5;
d.对步骤c混合溶液进行持续室温搅拌1-4天后离心洗涤,然后用3-氨丙基三甲氧基硅氧烷进行氨基化室温搅拌修饰24小时,最后进行离心洗涤,得氨基化的量子点掺杂的二氧化硅溶液,所述3-氨丙基三甲氧基硅氧烷或与二氧化硅源的体积比为1:20;
(2)量子点掺杂的二氧化硅/硫化铜结构的制备:
向步骤(1)得到的氨基化的量子点掺杂的二氧化硅溶液中加入柠檬酸修饰的硫化铜颗粒,混合溶液室温搅拌1-5天,然后对混合溶液进行离心修洗涤,所述量子点掺杂二氧化硅颗粒与柠檬酸修饰的硫化铜颗粒的摩尔比为1:50;
(3)量子点掺杂二氧化硅@硫化铜荧光光热探针的制备:
量子点掺杂的二氧化硅/硫化铜复合结构表面的修饰基团与多种生物分子进行交联反应,得量子点掺杂二氧化硅@硫化铜荧光光热探针。
进一步地,本发明提供了所述方法制备的量子点掺杂二氧化硅@硫化铜荧光光热探针。
更进一步地,本发明提供了所述量子点掺杂二氧化硅@硫化铜荧光光热探针在癌细胞定向追踪,癌细胞的荧光标记和癌细胞光热治疗中的应用。
有益效果
本发明中通过液相反应制备了荧光量子点与硫化铜的复合探针,对于传统的单一功能探针,本发明的量子点掺杂的二氧化硅@硫化铜纳米探针是集荧光示踪、光热治疗于一身的探针,利用二氧化硅包覆作用降低了量子的生物毒性,同时依赖其良好的生物特性提高了硫化铜的生物相容性。
(1)荧光量子点的荧光强度提高、生物毒性降低。
(2)硫化铜的光热治疗效应提高,同时其生物相容性被增强。
(3)二氧化硅壳的多孔结构降低了探针的质量,增强了负载能力。
(4)复合探针同时实现了荧光成像和光热治疗的目的。
附图说明
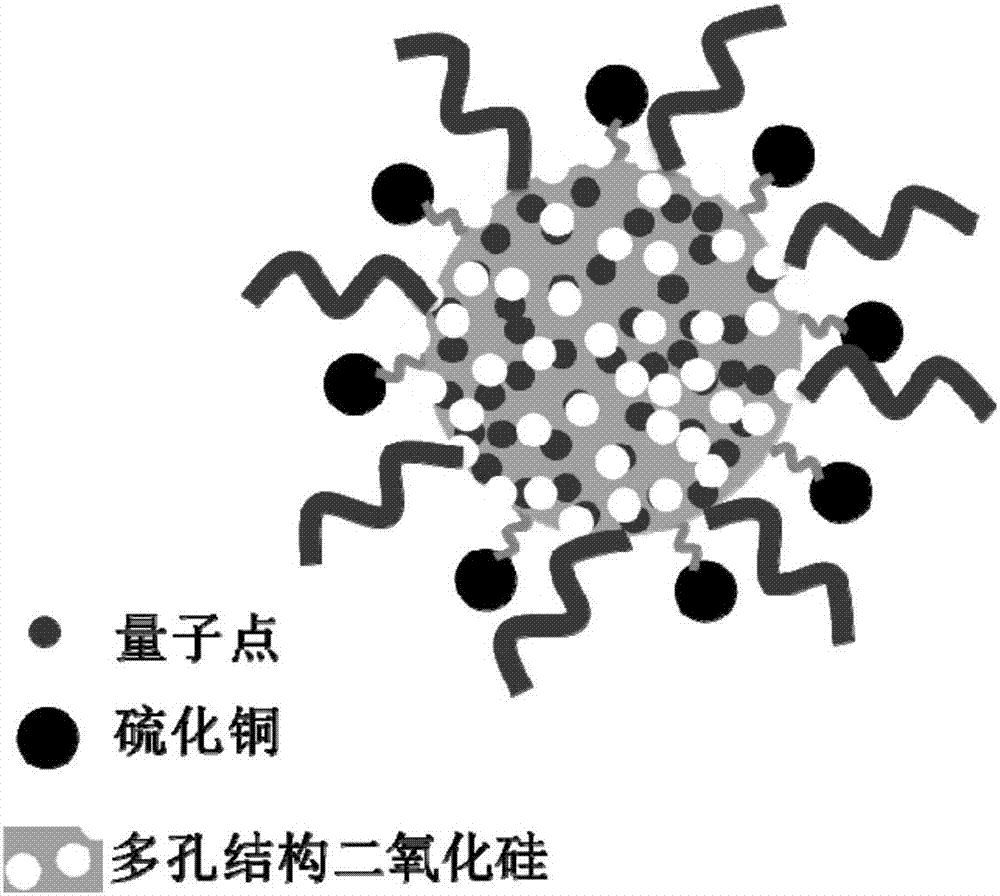
图1量子点掺杂二氧化硅@硫化铜结构示意图;
图2量子点掺杂二氧化硅@硫化铜的透射电镜图片;
图3复合探针与单纯量子点荧光强度对比图(量子点浓度相同);
图4复合探针与单纯量子点毒性对比图(量子点浓度相同);
图5复合探针与硫化铜的升温曲线(808nm激发光功率密度:2w/cm2);
图6复合探针与硫化铜的光热杀灭癌细胞对比图(a图为硫化铜的光热效果,b图示复合探针的光热效果;)
图7是6个实施例得到的复合探针的荧光光谱图;
图8是6个实施例得到的复合探针的升温曲线图。
具体实施方式
以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段。
实施例1:
(1)量子点掺杂的二氧化硅的制备:
首先配备10ml的乙二醇与2ml的浓氨水混合于50ml水中,然后将0.05mmolcdse量子点与0.125ml(1mmol)的(3-巯丙基)三甲氧基硅烷滴加入配备好的氨水溶液中,同时加入25微升的十六烷基溴化铵,此时对混合溶液进行持续室温搅拌1天后离心洗涤,然后用6.25微升的3-氨丙基三甲氧基硅氧烷进行氨基化室温搅拌修饰24小时,最后进行离心洗涤。
(2)量子点掺杂的二氧化硅/硫化铜结构的制备:
向0.005mmol的氨基化的量子点掺杂的二氧化硅溶液中加入0.25mmol的柠檬酸修饰的硫化铜颗粒,此混合溶液室温搅拌1天,然后对混合溶液进行离心修洗涤。
(3)多孔二氧化硅/四氧化三铁复合探针的制备:
利用复合结构表面的氨基基团、羧基基团可以发生交联反应,从而实现对多种生物分子(如抗体、dna片段、生物配体等)的链接。37度环境下,将0.05mmol的抗体分子加入到0.005mmol的复合纳米颗粒中,然后在37度下进行交联4小时,然后进行洗涤离心,最后在外界光场作用下,实现对癌细胞的荧光标记和光热治疗。
本发明制备的量子点掺杂二氧化硅@硫化铜结构示意图如图1所示;图中:中间灰色颗粒代表量子点,外围黑色颗粒隙代表硫化铜,外侧曲线代表表面基团。
量子点掺杂二氧化硅@硫化铜的透射电镜图片如图2所示,中间是量子点掺杂二氧化硅,外面是硫化铜颗粒。
在量子点浓度相同时,复合探针比单纯量子点荧光强度要强很多,对比图如图3所示。同时复合探针要比单纯量子点毒性低很多,对比图如图4所示。
在808nm激发光功率密度:2w/cm2条件下,复合探针与硫化铜的升温曲线如图5所示,结果说明在相同的激光强度和照射时间下,复合探针的升温效果更佳明显。
复合探针与硫化铜的光热杀灭癌细胞整体对比图如图6所示,a图为硫化铜的光热效果,b图示复合探针的光热效果。从图上可以看出复合探针杀灭癌细胞的情况明显好于硫化铜的光热效果。
实施例2:
(1)量子点掺杂的二氧化硅的制备:
首先配备10ml的乙醇与2ml的浓氨水混合于50ml水中,然后将0.02mmolcdse量子点与0.125ml(1mmol)的(3-巯丙基)三甲氧基硅烷滴加入配备好的氨水溶液中,同时加入6微升的十六烷基溴化铵,此时对混合溶液进行持续室温搅拌1天后离心洗涤,然后用6.25微升的3-氨丙基三甲氧基硅氧烷进行氨基化室温搅拌修饰24小时,最后进行离心洗涤。
(2)量子点掺杂的二氧化硅/硫化铜结构的制备:
向0.005mmol的氨基化的量子点掺杂的二氧化硅溶液中加入0.1mmol的柠檬酸修饰的硫化铜颗粒,此混合溶液室温搅拌1天,然后对混合溶液进行离心修洗涤。
(3)多孔二氧化硅/四氧化三铁复合探针的制备:
利用复合结构表面的氨基基团、羧基基团可以发生交联反应,从而实现对多种生物分子(如抗体、dna片段、生物配体等)的链接。37度环境下,将0.05mmol的抗体分子加入到0.005mmol的复合纳米颗粒中,然后在37度下进行交联4小时,然后进行洗涤离心,最后在外界光场作用下,实现对癌细胞的荧光标记和光热治疗。
实施例3:
(1)量子点掺杂的二氧化硅的制备:
首先配备10ml的乙二醇与2ml的浓氨水混合于50ml水中,然后将0.2mmolcdse量子点与0.125ml(1mmol)的(3-巯丙基)三甲氧基硅烷滴加入配备好的氨水溶液中,同时加入125微升的十六烷基溴化铵,此时对混合溶液进行持续室温搅拌1天后离心洗涤,然后用6.25微升的3-氨丙基三甲氧基硅氧烷进行氨基化室温搅拌修饰24小时,最后进行离心洗涤。
(2)量子点掺杂的二氧化硅/硫化铜结构的制备:
向0.005mmol的氨基化的量子点掺杂的二氧化硅溶液中加入0.5mmol的柠檬酸修饰的硫化铜颗粒,此混合溶液室温搅拌1天,然后对混合溶液进行离心修洗涤。
(3)多孔二氧化硅/四氧化三铁复合探针的制备:
利用复合结构表面的氨基基团、羧基基团可以发生交联反应,从而实现对多种生物分子(如抗体、dna片段、生物配体等)的链接。37度环境下,将0.05mmol的抗体分子加入到0.005mmol的复合纳米颗粒中,然后在37度下进行交联4小时,然后进行洗涤离心,最后在外界光场作用下,实现对癌细胞的荧光标记和光热治疗。
实施例4:
(1)量子点掺杂的二氧化硅的制备:
首先配备10ml的乙二醇与2ml的浓氨水混合于50ml水中,然后将0.05mmolcdse量子点与0.125ml(1mmol)的(3-巯丙基)三甲氧基硅烷滴加入配备好的氨水溶液中,同时加入100微升的1,3,5-三甲基苯,此时对混合溶液进行持续室温搅拌1天后离心洗涤,然后用6.25微升的3-氨丙基三甲氧基硅氧烷进行氨基化室温搅拌修饰24小时,最后进行离心洗涤。
(2)量子点掺杂的二氧化硅/硫化铜结构的制备:
向0.005mmol的氨基化的量子点掺杂的二氧化硅溶液中加入0.25mmol的抗坏血酸修饰的硫化铜颗粒,此混合溶液室温搅拌1天,然后对混合溶液进行离心修洗涤。
(3)多孔二氧化硅/四氧化三铁复合探针的制备:
利用复合结构表面的氨基基团、羧基基团可以发生交联反应,从而实现对多种生物分子(如抗体、dna片段、生物配体等)的链接。37度环境下,将0.05mmol的抗体分子加入到0.005mmol的复合纳米颗粒中,然后在37度下进行交联4小时,然后进行洗涤离心,最后在外界光场作用下,实现对癌细胞的荧光标记和光热治疗。
实施例5:
(1)量子点掺杂的二氧化硅的制备:
首先配备10ml的乙二醇与2ml的浓氨水混合于50ml水中,然后将0.05mmolcdse量子点与0.125ml(1mmol)的巯丙基甲基二甲氧基硅烷滴加入配备好的氨水溶液中,同时加入25微升的癸烷,此时对混合溶液进行持续室温搅拌1天后离心洗涤,然后用6.25微升的3-氨丙基三甲氧基硅氧烷进行氨基化室温搅拌修饰24小时,最后进行离心洗涤。
(2)量子点掺杂的二氧化硅/硫化铜结构的制备:
向0.005mmol的氨基化的量子点掺杂的二氧化硅溶液中加入0.25mmol的半胱氨酸修饰的硫化铜颗粒,此混合溶液室温搅拌1天,然后对混合溶液进行离心修洗涤。
(3)多孔二氧化硅/四氧化三铁复合探针的制备:
利用复合结构表面的氨基基团、羧基基团可以发生交联反应,从而实现对多种生物分子(如抗体、dna片段、生物配体等)的链接。37度环境下,将0.05mmol的抗体分子加入到0.005mmol的复合纳米颗粒中,然后在37度下进行交联4小时,然后进行洗涤离心,最后在外界光场作用下,实现对癌细胞的荧光标记和光热治疗。
实施例6:
(1)量子点掺杂的二氧化硅的制备:
首先配备10ml的乙二醇与2ml的浓氨水混合于50ml水中,然后将0.05mmolagins量子点与0.125ml(1mmol)的(3-巯丙基)三甲氧基硅烷滴加入配备好的氨水溶液中,同时加入125微升的1,3,5-三甲基苯,此时对混合溶液进行持续室温搅拌1天后离心洗涤,然后用6.25微升的3-氨丙基三甲氧基硅氧烷进行氨基化室温搅拌修饰24小时,最后进行离心洗涤。
(2)量子点掺杂的二氧化硅/硫化铜结构的制备:
向0.005mmol的氨基化的量子点掺杂的二氧化硅溶液中加入0.25mmol的硬脂酸修饰的硫化铜颗粒,此混合溶液室温搅拌1天,然后对混合溶液进行离心修洗涤。
(3)多孔二氧化硅/四氧化三铁复合探针的制备:
利用复合结构表面的氨基基团、羧基基团可以发生交联反应,从而实现对多种生物分子(如抗体、dna片段、生物配体等)的链接。37度环境下,将0.05mmol的抗体分子加入到0.005mmol的复合纳米颗粒中,然后在37度下进行交联4小时,然后进行洗涤离心,最后在外界光场作用下,实现对癌细胞的荧光标记和光热治疗。
应用例
本发明针对6个实施例的得到的复合探针做了光热杀灭癌细胞的情况分析。癌细胞是人乳腺癌细胞mda-mb-231(商业购买)。
乳腺癌细胞mda-mb-231细胞的杀灭实验:将乳腺癌细胞生长到96孔培养板上,然后在37度下生长24小时,然后用pbs缓冲液对培养基冲洗三次,然后将连接有生物分子(如抗体)的复合纳米颗粒和1.9ml的dmem(dulbecco'smodifiedeaglemedium)加入到培养基中,当培养基在37度下培养4小时后,对培养基用pbs缓冲液进行冲洗三次以除去未连接的复合纳米颗粒。最后进行光热效应研究,所用激光器的波长是808nm,功率是2w/cm2。对于培养基中的癌细胞照射10分钟后,对细胞进行染色(使用双色试剂盒,橙红色代表死细胞,绿色代表活细胞),并在奥里帕斯显微镜下进行观察并拍摄细胞图像。
如图7所示,实施例1中量子点掺杂量是最合适的,量子点浓度低导致荧光弱,太高由于浓度效应也会造成减弱。
如图8所示,实施例1中硫化铜的用量是最合适的,硫化铜用量小导致升温效果不明显,用量太大难以实现完全链接。
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 基于量子点的CA15‑3免疫层析试纸条的制备方法与制造工艺
- 肌红蛋白荧光免疫层析试纸条用活化荧光乳胶微球及应用的制造方法与工艺
- 铁蛋白荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 全程C‑反应蛋白荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 一种微流控芯片上基于荧光量子点磁性富集并分离结核分枝杆菌TB的方法及装置与制造工艺
- 25‑羟基维生素D荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 25‑羟基维生素D3荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 降钙素原荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 一种改变量子点荧光色的方法与制造工艺
- 一种基于荧光免疫层析技术的定量检测计算方法与制造工艺