纳米纤维结构及其合成方法和用途与流程
本申请根据35u.s.c.§119(e)要求于2014年9月29日递交的us临时专利申请号62/056,899的优先权。上述申请通过引用并入本文。
本发明是在政府支持下由国家健康研究院授予的授权号2p20gm103480做出的。政府对本发明具有一定的权利。
发明领域
本发明涉及纳米纤维和纳米纤维结构领域。更具体地,本发明提供了用于增加纳米纤维结构的厚度和/或孔隙率的方法。
背景技术:
在整个说明书中引用了若干出版物和专利文献,以便描述本发明所属领域的技术状态。这些引文的每一篇通过引用并入本文,如同完全阐述一样。
再生医学是包含三个主要元素的多学科主题:细胞、支架(scaffold)和信号分子(khademhosseini等人(2006)proc.natl.acad.sci.,103:2480-2487)。支架起重要作用,因为它们不仅提供用于细胞粘附和增殖的基底,而且还可以递送多种线索以调节用于组织再生的细胞反应(grafahrend等人(2011)nat.mater.,10:67-73)。已经开发了用于制造支架的多种微制造技术(derby,b.(2012)science338:921-926;moutos等人(2007)nat.mater.,6:162-167;wegst等人)nat.mater.,14:23-36)。电纺纳米纤维由于其对细胞外基质(ecm)的结构和ecm胶原纤维的尺寸的生物模拟已显示出作为用于再生医学的支架的巨大希望(xie等人(2008)macromol.rapidcommun.,29:1775-1792;liu等人(2012)adv.healthcaremater.,1:10-25)。传统的静电纺丝通常产生不受控制的和密集堆积的纤维,然而,导致紧凑的二维(2d)纳米纤维垫/膜和阻碍贯穿纳米纤维支架的细胞浸润和生长。因此,传统的2d纳米纤维垫被限制为用于其在再生医学和工程化三维(3d)组织模型中的应用的理想底物(bhardwaj等人(2010)biotechnol.adv.,28:325-347)。
为了克服这个巨大的障碍,已经进行了许多尝试来开发可以增强细胞向内生长的3d电纺纳米纤维支架(blakeney等人(2011)biomaterials,32:1583-1590;lee等人(2011)tissueeng.,parta,17:2695-2702;cai等人(2013)langmuir29:2311-2318;sheikh等人(2014)nanomedicine11:681-691;jeong等人(2014)j.mater.chem.b,2:8116-8122)。不幸的是,大多数方法局限于制造由无规取向的纳米纤维和/或某些材料(例如,具有添加剂)组成的3d纳米纤维支架(jin等人,(2015)angew.chem.,int.ed.,54:7587-7591)。这些方法通常导致不足的厚度和/或受限的几何形状和/或不受控制的孔隙率。此外,获得的先前的3d支架与无序结构和缺乏对于有组织的组织例如腱、神经和肌肉的再生至关重要的纳米形貌线索相关联(liu等人(2012)adv.healthcaremater.,1:10-25;ma等人(2013)nanomedicine8:1459-1481)。或者,其他研究已经致力于使用具有大得多的直径(≈几至几十μm)的电纺纤维,以便增强细胞浸润(fong等(2013)proc.natl.acad.sci.,110:6500-6505;soliman等人(2011)j.biomed.mater.res.,parta,96a:566-574)。这种微纤维缺乏仿生性质和纳米形态线索,导致与使用纳米纤维相比不同的细胞应答。作为显著的实例,与膜和微纤维支架相比,纳米纤维支架可以最小化炎症反应(saino等人(2011)biomacromolecules12:1900-1911)。此外,浸润的细胞仍然主要分布在微纤维支架的表面部分(fong等人(2013)proc.natl.acad.sci.,110:6500-6505)。期望保持特定的纳米形貌线索,例如由用于3d电纺支架的排列的纳米纤维提供的各向异性特性。这样的纳米形貌线索可以用作细胞行为的调节剂(例如,促进细胞骨架重组和人间充质干细胞的细胞和核伸长,引导和增强人皮肤成纤细胞迁移和轴突生长,以及调节腱干细胞分化)用于受欢迎的组织再生(dang等人(2007)adv.mater.,19:2775-2779;patel等人(2007)nanolett.,7:2122-2128;yin等人(2010)biomaterials31:2163-2175)。因此,必须开发简单、可控和有效的方法以生成3d电纺纳米纤维支架,其能够以在细胞接种和增殖后具有高度有序的结构和均匀的细胞分布支持细胞浸润和组织。
技术实现要素:
根据本发明,提供了用于生产具有增加的孔隙率和/或厚度的纳米纤维结构的方法。该方法包括将包含多个纳米纤维的纳米纤维结构(例如,垫)暴露于气泡。气泡可以通过化学反应和/或物理手段产生。在具体实施方案中,气泡作为化学反应(例如硼氢化钠的水解)的产物产生。该方法还可包括在暴露于气泡之前制备包含多个纳米纤维(例如,单轴排列的、无规的、缠结的和/或电纺纤维)的纳米纤维结构。该方法还可以包括在暴露于气泡之后洗涤纳米纤维结构,去除捕获在纳米纤维结构内的气泡,和/或冻干所产生的纳米纤维结构。
根据本发明的另一方面,提供了具有增加的厚度和/或孔隙率的三维纳米纤维结构。
附图说明
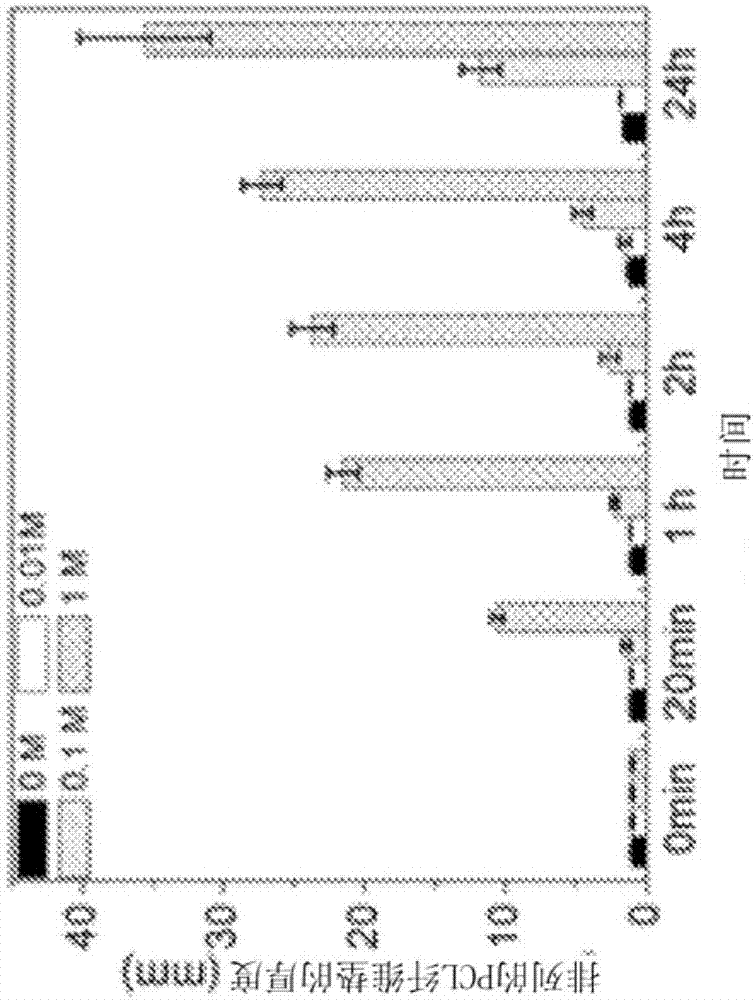
图1a、1b和1c显示了排列的纳米纤维支架的膨胀和表征。图1a:用1mnabh4处理0分钟、20分钟和24小时的排列的pcl纤维垫的照片。插图显示了相应的原理图。图1b:在浸入水、0.01m、0.1m、1mnabh4中20分钟、1小时、2小时、4小时和24小时后测量排列的pcl纤维垫的厚度。图1c:在浸入水、0.01m、0.1m、1mnabh4中20分钟、1小时、2小时、4小时和24小时后估计排列的pcl纤维垫的相应孔隙率。
图2a、2b和2c显示了排列的纳米纤维支架的形态和微观结构。图2a:sem图像显示在1mnabh4溶液中膨胀20分钟和24小时之前和之后的排列的pcl纤维垫的横截面形态。比例尺为20μm。图2b:在膨胀20分钟和24小时后,纳米纤维支架的相邻层之间的间隙距离的分布。图2c:膨胀20分钟和24小时后纳米纤维支架的层厚度的分布。通过imagej软件基于sem图像测量间隙距离和层厚度。
图3a、3b、3c、3d、3e和3f显示了无规纳米纤维支架的膨胀和表征。图3a:显示无规pcl纳米纤维垫在用1m的nabh4水溶液处理前和处理20分钟和24小时后的照片。图3b:sem图像显示pcl纤维垫在用1mnabh4水溶液处理前和处理20分钟和24小时后的横截面形态。图3c:无规纳米纤维垫在用1m的nabh4水溶液处理前和处理不同时间后的厚度。图3d:估计无规纳米纤维垫在用1m的nabh4水溶液处理前和处理不同时间后的孔隙率。比例尺为20μm。图3e:在膨胀20分钟和24小时后,无规纳米纤维支架的相邻层之间的间隙距离的分布。图3f:膨胀20分钟和24小时后无规纳米纤维支架的层厚度的分布。通过imagej软件基于sem图像测量间隙距离和层厚度。
图4a、4b、4c和4d显示了管状纳米纤维支架的膨胀和表征。图4a:显示了在用1mnabh4处理1小时和24小时之前和之后,由外层中的无规纳米纤维和在内层(rla)中纵向排列的纳米纤维制成的管状支架的照片。图4b:显示了在用1mnabh4处理1小时和24小时之前和之后,由外层中的无规纳米纤维和在内层(rca)中周向排列的纳米纤维制成的管状支架的照片。图4c:用1mnabh4溶液处理不同时间后的管状支架(rla)的内径和外径的变化。图4d:用1mnabh4溶液处理不同时间之前和之后的管状支架(rca)的内径和外径的变化。
图5显示了管状纳米纤维支架的形态。sem图像显示在1mnabh4溶液中膨胀24小时之前和之后的管状纳米纤维支架(rla和rca)的横截面形态。管状纳米纤维支架在膨胀后形成层状结构。
图6a和6b显示了在孵育1天(图6a)和7天(图6b)之后接种nih3t3成纤细胞的排列的pcl纳米纤维支架(未膨胀vs.膨胀的)的苏木精-伊红染色。将支架以1mm的厚度切片用于苏木精-伊红染色。细胞分布在传统纳米纤维支架表面。相比之下,细胞分布在整个膨胀的支架。
图7a和7b示出了图6a和6b的高度放大图像。在孵育1天(图7a)和7天(图7b)之后接种nih3t3成纤细胞的排列的pcl纳米纤维支架(未膨胀vs.膨胀的)的苏木精-伊红染色。将支架以1mm的厚度切片用于苏木精-伊红染色。细胞分布在传统纳米纤维支架表面上。相比之下,细胞分布在整个膨胀的支架。
图8a和8b显示气泡形成。光学显微镜图像显示在不存在(图8a)和存在(图8b)电纺纳米纤维支架的情况下在nabh4溶液中的气泡形成。
图9提供了说明纳米纤维支架在nabh4溶液中的膨胀过程的示意图:(i)由毛细作用驱动的nabh4水溶液快速渗透到排列的纳米纤维支架中;(ii)在纳米纤维的表面上或在不完全排列的纳米纤维的交叉处气泡的异相成核;(iii)在持续产生越来越多的氢的情况下成核气泡的生长;(iv)相邻气泡的聚结;和(v)由于气泡的进一步生长和聚结而形成“气泡层”。
图10a和10b显示了纳米纤维支架的形态。显示在膨胀之前(图10a)和之后(图10b)的排列的纳米纤维支架的照片。图10b中的支架交替浸泡在1mnahco3和1mhcl溶液中数轮。
图11提供了纳米纤维膜的两个图像,其中每个图像中右侧的样品在膨胀之前,和每个图像中左侧的样品在液体co2中膨胀之后。
具体实施方式
由于其生物模拟,电纺纳米纤维已经显示出作为用于再生医学的支架的巨大潜力。然而,传统的二维电纺纳米纤维垫抑制了它们的应用,因为其致密的结构和缺乏有效的细胞浸润以及缺乏氧和营养物扩散。这里,提供了一种在第三维中膨胀电纺纳米纤维垫的新方法,特别是使用改进的气体成泡技术。所得纳米纤维支架显示具有可控间隙宽度和微米级的层厚度的层状结构。膨胀纳米纤维支架具有比传统的二维纳米纤维膜显著更高的孔隙率,同时保持纳米形貌线索。间隙宽度和层厚度的分布直接取决于纳米纤维垫在气泡形成溶液内的处理时间。与在传统纳米纤维垫表面上的有限细胞增殖相比,体外试验显示出在膨胀的纳米纤维支架内强健的细胞浸润和增殖。重要的是,在孵育7天后,在整个膨胀和排列的纳米纤维支架中观察到细胞排列。所提出的方法进一步应用于制造由膨胀纳米纤维组成的管状支架。共同地,这种新型的支架在再生医学和建立用于药物筛选和生物学研究的3d体外组织模型的应用中具有重要的前景。
用于增加纳米纤维支架的孔隙率的先前方法主要包括超声波处理、增加纤维直径和选择性去除牺牲纤维(lee等人(2011)tissueeng.parta.,17:2695-702;pham等人(2006)biomacromolecules7:2796-805;baeretal.(2008)biomaterials29:2348-58;kidoaki等人(2005)biomaterials26:37-46;yang等人(2009)tissueeng.a.,15:945-56;zhou等人(2006)polymer47:7497-505;brown等人(2011)adv.mater.,23:5651-7;bkakeney等人(2011)biomaterials32(6):1583-90;zhang等人(2007)adv.mater.,19:3664-7;xie等人(2011)small7:293-7;thandayamoorthy等人(2006)j.appl.polym.sci.,101:3121-4;yan等人(2011)langmuir27:4285-9;xie等人(2012)adv.healthcaremater.,1:674-8;lee等人(2010)tissueeng.c.methods17:651-61)。然而,这些技术仍然与有限的孔隙率、生产中的低效率、复杂的方法、耗时的工艺以及对特别昂贵的设备的需求相关联。本发明的优点包括但不限于:1)孔隙率的范围大于目前可用的技术;2)常规纤维制作后不需要特殊设备;3)适用于大多数聚合物纤维;(4)该技术可以容易地扩展至制造用于再生神经和肠组织和血管的其它医疗装置,以及(5)该方法简单且易于工业化。
气体成泡技术通常包括三个基本步骤:(1)聚合物/气体溶液形成,(2)气泡(孔)成核和(3)气泡(孔)生长和体积膨胀(park等人(1995)polym.eng.sci.,35:432-440)。气泡/成泡方法在材料科学(例如,制造泡沫和中空金属球)、环境管理(例如水处理)、医学(例如医学成像、治疗学和用于气体、药物和基因的载体)和食品工业(例如,食品混合和增强质地)的领域中具有多种应用(rodriguez-rodriguez等人(2015)annu.rev.fluidmech.,47:405-429;lindner等人(2004)nat.rev.drugdiscovery3:527-533;lee等人(2015)softmatter11:2067-2079;sirsi等人(2009)bubblesci.,eng.,technol.,1:3-17)。虽然气体成泡可以用于制造具有高孔隙率的海绵支架用于组织工程中的应用,但是它没有用于膨胀电纺纳米纤维垫(nam等人(2000)j.biomed.mater.res.,53:1-7)。
本发明涉及新的微纤维(直径>1μm)和纳米纤维(直径<1μm)结构(例如垫)以及以后处理方式将微纤维或纳米纤维结构(例如垫)的第三维度扩展以增加结构的孔隙率。尽管本申请通常描述了纳米纤维结构的改性和三维纳米纤维结构的合成,但是本发明还包括微纤维结构的改性和三维微纤维结构的合成。所述方法可以利用化学反应和/或物理手段来产生气泡形成。本发明的纤维可以通过任何方法制造,然后可以放置在其中产生气泡不同时间量的条件下(例如,浸没或浸泡在液体中)。
电纺纳米纤维通常沉积在基底上以形成纳米纤维垫。然而,由于其固有的缺点,纤维垫通常是致密的并且难以实现用于细胞浸润的合适的孔隙率。本发明提供了通过利用气泡(例如,通过在水溶液中的化学反应产生的)来膨胀纳米纤维垫的第三维度的简单方法。例如,可以使用气体生产化学反应;通过在高压和/或低温下在液体中的溶解气体;加压气体(例如,co2)液体;和/或物理手段(例如,激光(例如,脉冲激光)、声诱导或流动诱导),但不限于此,来产生气泡。本发明的方法还可以用于扩大其它类型的纤维材料(即,不限于电纺纳米纤维)的孔隙率。获得的支架可以模拟细胞外基质的结构。所获得的支架也可以具有大的孔隙率,从而允许细胞容易地浸润。通过本发明的方法产生的纳米纤维支架可用于组织再生(例如骨、腱、软骨、皮肤、神经和/或血管)。与细胞组合,可以容易地形成三维组织构建体以修复受损的组织或器官。
盐浸提/气体成泡方法已经用于生产双孔纳米纤维支架(lee等人(2005)biomaterials26:3165-3172)。使用碳酸氢铵作为气体成泡剂。然而,该方法与使用相对高的温度(90℃)用于浸出nh4hco3颗粒和在固化的聚合物基质内产生气态氨和二氧化碳相关。此外,没有提出层状结构和纳米形貌线索的维护。另一项研究仅使用气体成泡技术研究了无规纤维膜(joshi等人(2015)chem.eng.j.,275:79-88)。
本文中,提供了利用改进的气体成泡技术,任选地,然后冷冻干燥用于三维膨胀纳米纤维垫(例如,电纺纳米纤维垫;例如包含聚(ε-己内酯)(pcl,fda批准的、生物相容性和生物可降解的聚合物)的垫)的新方法。证明了该方法可靠地产生具有高度有序架构的3d纳米纤维支架的能力,其理想地用于支持和组织浸润和增殖细胞。
根据本发明,提供了用于生产三维纳米纤维(或微纤维)结构的方法。换句话说,该方法增加纳米纤维(或微纤维)结构(例如,包括多个纳米纤维(或微纤维)(例如,单轴排列、无规、缠结和/或电纺丝))的厚度和/或孔隙率。该方法包括将纳米纤维(或微纤维)结构(例如,垫)暴露于气泡。如本文所解释的,气泡可以通过化学反应或物理操作产生。例如,纳米纤维结构可以浸没或浸入气泡/气体产生化学反应或物理操作中。通常,暴露于气泡的时间越长,纳米纤维结构的厚度和孔隙率增加越大。纳米纤维结构还可在模具(例如,金属、塑料或在气泡存在下不膨胀的其它材料)中膨胀,使得膨胀的纳米纤维结构形成所需形状(例如管)。纳米纤维结构可以在暴露于气泡之前用空气等离子体处理(例如,以增加亲水性)。
在暴露于气泡之后,纳米纤维结构可以在水和/或期望的载体或缓冲液(例如,药学或生物学可接受的载体)中洗涤或漂洗。可以通过对纳米纤维结构施加真空来去除捕获的气泡。例如,膨胀的纳米纤维结构可以浸没或浸入在液体(例如水和/或期望的载体或缓冲液)中,并且可以施加真空以快速除去气泡。在膨胀之后(例如,在漂洗和去除捕获的气体之后),纳米纤维结构可以被冻干和/或冷冻干燥。
本发明的方法还可以包括在暴露于气泡之前合成纳米纤维结构(例如,垫)。在具体实施方案中,使用电纺丝合成纳米纤维结构。在一个具体实施方案中,纳米纤维结构包括单轴排列的纤维、无规纤维和/或缠结纤维。纳米纤维结构可以在膨胀之前切割或成形。
本发明的气泡可以通过本领域已知的任何方法制备。气泡可以例如通过化学反应或通过物理方法产生。在一个具体实施方案中,化学反应或物理操作不损伤或改变或基本上不损坏或改变纳米纤维(例如,纳米纤维在化学反应中是惰性的,而不是化学改性的)。如上所述,纳米纤维结构可以浸没或浸入在包含产生气泡的化学反应的试剂的液体中。产生气泡的化学反应的实例包括但不限于:
nabh4+2h2o=nabo2+4h2
nabh4+4h2o=4h2(g)+h3bo3+naoh
hco3-+h+=co2+h2o
nh4++no2-=n2+2h2o
h2co3=h2o+co2
2h++s2-=h2s
2h2o2=o2+2h2o
3hno2=2no+hno3+h2o
ho2cch2coch2co2h=2co2+ch3coch3
2h2o2=2h2+o2
cac2+h2o=c2h2
zn+2hcl=h2+zncl2
2kmno4+16hcl=2kcl+2mncl2+h2o+5cl2
在一个特别的实施方案中,化学反应是nabh4的水解反应(例如nabh4+2h2o=nabo2+4h2)。在一个具体实施方案中,co2气泡(化学或物理产生(见下文))用于亲水性聚合物。
用于产生本发明的气泡的物理方法的实例包括但不限于:1)在密封室中产生高压(填充气体)/热量,并突然降低压力;2)在高压下将气体溶解在液体/水中,并降低压力以释放气泡;3)使用超临界流体(减压)如超临界co2;4)使用气体液体(然后降低压力)(例如,液体co2、液体丙烷和异丁烷);5)流体流;6)将声能或超声应用于液体/水;7)施加激光(例如,到液体或水);8)沸腾;9)降低压力沸腾(例如,用乙醇);和10)施加辐射(例如,在液体或水上的电离辐射)。纳米纤维结构可以浸没或浸入在产生气泡的物理操作的液体中。
本发明的纳米纤维可以包含任何聚合物。在具体实施方案中,聚合物是生物相容的和/或可生物降解的。聚合物可以是疏水的、亲水的或两亲的。在一个具体实施方案中,聚合物是疏水性的。聚合物可以是例如均聚物、无规共聚物、共混聚合物、共聚物或嵌段共聚物。嵌段共聚物最简单地定义为至少两种不同聚合物片段的共轭物。聚合物可以是例如线性、星状、接枝、支化、基于树枝状的或超支化的(例如至少两个支化点)。本发明的聚合物可具有约2至约10,000、约2至约1000、约2至约500、约2至约250或约2至约100个重复单元或单体。本发明的聚合物可以包含封端末端。
疏水性聚合物的实例包括但不限于:聚乙烯醇(pva)、聚(甲基丙烯酸羟乙酯)、聚(n-异丙基丙烯酰胺)、聚乳酸(pla(或pdla))、聚(丙交酯-共-乙交酯)(plg)、聚(乳酸-共-乙醇酸)(plga)、聚乙交酯或聚乙醇酸(pga)、聚己内酯(pcl)、聚天冬氨酸、聚噁唑啉(例如丁基、丙基、戊基、壬基或苯基聚(2-噁唑啉))、聚氧丙烯、聚谷氨酸、聚富马酸丙二酯(ppf)、聚碳酸三亚甲基酯、聚氰基丙烯酸酯、聚氨酯、聚原酸酯(poe)、聚酐、聚酯、聚环氧丙烷、聚己内酯富马酸酯、聚1,2-环氧丁烷、聚正环氧丁烷、聚乙烯亚胺、聚四氢呋喃、乙基纤维素、聚二吡咯/二卡巴唑、淀粉,聚偏二氟乙烯(pvdf)、聚四氟乙烯(ptfe)、聚二噁烷酮(pdo)、聚醚聚氨酯脲(peuu)、醋酸纤维素、聚丙烯(pp)、聚对苯二甲酸乙二醇酯(pet)、尼龙(例如尼龙6)、聚己内酰胺、pla/pcl、聚(3-羟基丁酸酯-共-3-羟基戊酸酯)(phbv)、pcl/碳酸钙和/或聚(苯乙烯)。
亲水性聚合物的实例包括但不限于:聚乙烯基吡咯烷酮(pvp)、聚乙二醇和聚环氧乙烷(peo)、壳聚糖、胶原、硫酸软骨素、藻酸钠、明胶、弹性蛋白、透明质酸、丝纤蛋白,藻酸钠/peo、丝/peo、丝纤蛋白/壳聚糖、透明质酸/明胶、胶原/壳聚糖、硫酸软骨素/胶原和壳聚糖/peo。两亲性共聚物可包含来自上文列出的那些(例如明胶/pva、pcl/胶原、壳聚糖/pva、明胶/弹性蛋白/plga、pdo/弹性蛋白、phbv/胶原、pla/透明质酸、plga/透明质酸、pcl/透明质酸、pcl/胶原/透明质酸、明胶/硅氧烷、plla/mwnt/透明质酸)的亲水性聚合物(例如片段)和疏水性聚合物(例如片段)。
xie等人提供了特别用于静电纺丝的聚合物的实例(macromol.rapidcommun.(2008)29:1775-1792;通过引用并入本文;参见例如表1)。用于本发明的纤维,特别是用于电纺纳米纤维的化合物或聚合物的实例包括但不限于:天然聚合物(例如壳聚糖、明胶、i型、ii型和/或iii型胶原、弹性蛋白、透明质酸、纤维素、丝纤蛋白、磷脂(卵磷脂)、纤维蛋白原、血红蛋白、纤维小牛胸腺na-dna、病毒m13病毒)、合成聚合物(例如plga、pla、pcl、phbv、pdo、pga、plcl、plla-dla、peuu、乙酸纤维素、peg-b-pla、evoh、pva、peo、pvp)、共混的(例如pla/pcl、明胶/pva、pcl/胶原、藻酸钠/peo、壳聚糖/peo、壳聚糖/pva、明胶/弹性蛋白/plga、丝/peo、丝纤蛋白/壳聚糖、pdo/弹性蛋白、phbv/胶原、透明质酸/明胶、胶原/硫酸软骨素、胶原/壳聚糖)和复合材料(例如pdla/ha、pcl/caco3、pcl/ha、plla/ha、明胶/ha、pcl/胶原/ha、胶原/ha、明胶/硅氧烷、plla/mwnts/ha、plga/ha)。
根据本发明,提供了三维纳米纤维结构。在一个具体实施方案中,通过本发明的方法产生纳米纤维结构。纳米纤维结构可以包含在水或生物学和/或药学上可接受的载体中。纳米纤维结构可以是用于生物医学研究的支架,例如再生医学或组织模型。纳米纤维结构的应用在xie等人中提供(macromol.rapidcommun.(2008)29:1775-1792;通过引用并入本文)。在具体实施方案中,纳米纤维结构包含或包封至少一种试剂(例如治疗剂、生长因子、信号分子、细胞因子、抗生素等)。在具体实施方案中,本发明的纳米纤维(在合成方法或最终产物中),使用表面轭合/包被和/或包封(例如,以调节细胞应答和/或促进组织再生),用至少一种试剂或化合物(例如治疗剂、治疗剂、生长因子、信号分子、细胞因子、抗生素等)标记或修饰。
定义
单数形式“一个(a)”、“一种(an)”和“所述(the)”包括多数的引用,除非上下文中另外有明确说明。
如本文所使用的,术语“电纺丝”是指使用流体动力学和带电表面之间的相互作用从溶液或熔体制造纤维(即电纺丝纤维),特别是微米或纳米尺寸的纤维(例如,通过响应于电场使溶液或熔体流动通过孔)。电纺纳米纤维的形式包括但不限于支化纳米纤维、管、带和分裂纳米纤维、纳米纤维纱、表面涂覆的纳米纤维(例如,具有碳、金属等)、在真空中产生的纳米纤维等。电纺纤维的生产描述于例如gibson等人(1999)alchej.,45:190-195。
“药学上可接受的”表示由联邦或州政府的管理机构批准或在美国药典或其它公认的药典中列出的用于动物,更特别是用于人的。
“载体”是指与本发明的活性剂一起施用的例如稀释剂、佐剂、防腐剂(例如,thimersol、苄醇)、抗氧化剂(例如抗坏血酸、焦亚硫酸钠)、增溶剂(例如聚山梨酯80)、乳化剂、缓冲剂(例如,trishcl、乙酸盐、磷酸盐)、水、水溶液、油、填充物质(例如乳糖、甘露醇)、赋形剂、助剂或载具(vehicle)。合适的药物载体描述在e.w.martin的“remington'spharmaceuticalsciences”(mackpublishingco.,easton,pa);gennaro,a.r.,remington:thescienceandpracticeofpharmacy,(lippincott,williamsandwilkins);liberman等人,eds.,pharmaceuticaldosageforms,marceldecker,newyork,n.y.;andkibbe等人,eds.,handbookofpharmaceuticalexcipients(3rded.),americanpharmaceuticalassociation,washington。
如本文所用,术语“聚合物”表示由两个或更多个重复单元或单体化学连接形成的分子。术语“嵌段共聚物”最简单地是指至少两种不同聚合物片段的共轭物,其中每个聚合物片段包含两个或更多个相同类型的相邻单元。
“疏水性”表示优选非极性环境(例如,疏水性物质或结构部分与水相比更容易溶解在非极性溶剂例如烃中,或被其润湿)。在具体实施方案中,疏水性聚合物可具有在37℃下小于约1重量%的水溶解度。在具体实施方案中,在双蒸水中的1%溶液中具有低于约37℃,特别是低于约34℃的浊点的聚合物可以被认为是疏水的。
如本文所用,术语“亲水性”是指溶于水的能力。在具体实施方案中,在双蒸水中的1%溶液中具有高于约37℃,特别是高于约40℃的浊点的聚合物可以被认为是亲水性的。
如本文所用,术语“两亲性”是指既溶于水又溶于脂质/非极性环境中的能力。通常,两亲化合物包含亲水部分和疏水部分。
提供以下实施例以说明本发明的某些实施方案。它们不打算以任何方式限制本发明。
实施例1
材料和方法
电纺纳米纤维支架的制造
纳米纤维是使用标准静电纺丝装置根据已建立的方案生产的(xie等人(2009)biomaterials30:354-362;xie等人(2013)actabiomater.,9:5698-5707;jiang等人(2015)pharm.res.,32:2851-2862)。将pcl(mw=80kda)以10%(w/v)的浓度溶解在由具有4:1(v/v)比例的二氯甲烷(dcm)和n,n-二甲基甲酰胺(dmf)组成的溶剂混合物中。使用注射泵以0.8ml/小时的流速泵送pcl溶液,同时在喷丝头(22号针)和距离喷丝头20cm的接地收集器之间施加15kv的电势。在分别以2000和100rpm的速度旋转的滚筒上收集1mm厚的排列的和无规的纳米纤维垫。在液氮中切割纳米纤维垫以避免边缘上的变形。通过沉积1mm厚的排列的纳米纤维层,随后沉积50μm厚的无规纳米纤维层来制造管状纳米纤维支架。为了制造由外层中的无规纳米纤维和纵向排列的纳米纤维制成的管状支架,将所获得的纤维垫在两个不同方向(平行和垂直)上手动翻转,并用30%pcldcm溶液密封边缘以形成双层管状纳米纤维支架,其由外层中的无规纳米纤维和内层中的纵向或周向排列的纳米纤维组成。为了在溶液中产生气泡,选择以下化学反应用于“概念验证”:
nabh4+2h2o→nabo2+4h2↑
由于其相对高的氢含量(10.9%)和可控的水解反应,nabh4已经被广泛研究用于h2储存和生成(ye等人(2007)j.powersources164:544-548;liu等人(2009)j.powersources187:527-534)。pcl纳米纤维垫(1cm×1cm×1mm)用于研究膨胀过程的影响。将pcl纳米纤维垫浸入40ml新鲜制备的nabh4溶液中并在21℃下以50rpm摇动不同的时间长度(0分钟、20分钟、1小时、2小时、4小时和24小时)。在0.01m、0.1m和1m下制备nabh4溶液。使用游标卡尺在0分钟、20分钟、1小时、2小时、4小时和24小时测量样品厚度,同时通过数码相机记录样品形态。膨胀后,弃去nabh4溶液,将膨胀的pcl纳米纤维支架轻轻转移到烧杯中,用去离子水漂洗三次。为了除去捕获的气泡,将膨胀的支架浸入水中并暴露于真空(~200pa)3秒。最后,用去离子水将膨胀的纳米纤维支架再漂洗三次。
纳米纤维支架的表征
管状纳米纤维支架由外层中的无规纤维和内层中的排列纤维制成,如上所述。管状支架在1mnabh4溶液中膨胀,类似于平面纳米纤维垫。使用游标卡尺测量管状支架的内径和外径,并在0分钟、20分钟、1小时、2小时、4小时和24小时获取数字照片。sem用于检查在膨胀程序之前和之后管状支架的横截面上的纤维结构。在至少三个独立实验中报道了纳米纤维垫的平均厚度和管状支架的直径。根据纳米纤维支架在膨胀前和膨胀后的体积变化计算纳米纤维支架的孔隙率。使用以下等式计算孔隙率
ε=[(v-v0)/v]100%
其中ε是孔隙率,v=l(长度)×w(宽度)×t(厚度)是pcl纳米纤维支架的体积,v0=((m0)/(ρ0))是堆积pcl材料的计算体积,m0是堆积pcl材料的质量,ρ0是堆积pcl材料的密度。
将pcl纳米纤维垫嵌入去离子水中并在-20℃下在膨胀前和膨胀后冷冻。使用低温恒温器获得冷冻纳米纤维支架的横截面并冷冻干燥。sem(fei,quanta200,oregon)用于表征支架横截面内的纳米纤维形态和结构。为了避免充电,将纳米纤维样品固定在具有双面导电带的金属柱上并在10ma的电流强度下在真空下用铂溅射涂覆4分钟。在30kv的加速电压下获取sem图像。基于sem图像通过imagej软件测量在纳米纤维支架中在使用1mnabh4膨胀20分钟和24小时之前和之后观察到的间隙距离和层厚度。已经分析了至少250个间隙或层。
测量纳米纤维支架膨胀前(1cm×1cm×1mm)和膨胀后(1cm×1cm×1cm)的机械性能。将纳米纤维样品安装在两个钢把手和两个1.5cm直径的玻璃盖玻片之间,以分别测量拉伸和压缩模量。平衡后,拉伸和压缩试验的触发器和速率设置为750μn和5.0×10-3s-1。通过加载单元和数字数据采集系统记录所得力(f)和长度变化(δl)。通过将所得力(f)和长度变化(δl)除以横截面积(a)和初始长度(l0)来计算工程应力(σ=f/a)和工程应变(ε=δl/l0)。杨氏模量由e=σ/ε给出。当最大力达到500mn或样品断裂时,测试停止。平行于纤维排列轴(y轴)和与纤维排列轴正交的方向(z轴)完成膨胀后的排列pcl纳米纤维支架的测试,包括最大应力、极限拉伸应力和极限拉伸应变。在与纤维排列轴正交的方向(z轴)完成膨胀后的无规pcl纳米纤维支架的测试,包括最大应力、极限拉伸应力和极限拉伸应变。每种材料/条件对至少五个独立样品进行机械测试。
体外细胞培养
将膨胀的pcl纳米纤维支架(1cm×5mm×1cm)和未膨胀的纳米纤维垫(1cm×5mm×1mm)在70%乙醇中灭菌过夜,并用pbs冲洗3次。在细胞培养之前,将样品浸入培养基中24小时。然后将未膨胀和膨胀的纳米纤维支架置于24孔板中。将1×106个nih3t3细胞接种在每个纳米纤维样品上并孵育3小时。然后翻转样品,将等量的细胞接种在另一侧,并孵育3小时。然后将样品从24孔板转移到含有25ml完全dmem培养基的锥形试管中。
组织学染色
在细胞接种后1天或7天收获培养物。将pcl纳米纤维垫和膨胀的支架都用pbs漂洗三次,并在室温下在4%多聚甲醛中固定30分钟。将所有样品包埋在冷冻培养基中。使用低温恒温器切割,并且在整个冷冻块中每隔1mm收集20μm厚的切片。将切片在50℃下烘烤过夜。根据制造商的说明应用苏木精和曙红(h&e)染色,以将细胞与纳米纤维支架区分,其中细胞核染成蓝色,细胞质和ecm染成粉红色(fischer等人(2008)coldspringharbprotoc.,pdb.prot4986)。简言之,在将苏木精mayer's溶液施用5分钟之前,使切片在蒸馏水中水合。将载玻片用蒸馏水彻底冲洗。应用足够的蓝色试剂以完全覆盖切片并孵育10-15秒。载玻片用蒸馏水漂洗2次,然后浸在无水乙醇中。然后施加足够的曙红y溶液并孵育2-3分钟。然后使用无水乙醇漂洗载玻片,并用无水乙醇脱水。然后将载玻片安装在合成树脂中。从三个独立实验获得体外实验数据。图像由ventana的coreoau载玻片扫描仪捕获。对每个纳米纤维材料和加工条件评价三个切片。
结果
电纺纳米纤维垫在用nabh4水溶液处理后成功地在第三维上膨胀(图1a)。处理的纳米纤维垫的末端厚度随着在溶液中的时间增加和随着nabh4浓度的增加而增加(图1b)。令人惊讶的是,在用1mnabh4水溶液处理仅仅24小时后,纳米纤维垫的厚度从1mm增加到35.6mm。类似地,排列的pcl纳米纤维支架的孔隙率随着反应时间的增加和nabh4的浓度增加而增加,这与厚度的趋势一致(图1c)。起始纳米纤维垫的基线孔隙率为83.6%,用1mnabh4水溶液处理24小时后,支架孔隙率增加至99.2%。
为了在膨胀后保持纳米纤维支架的完整性,使用冷冻干燥器将支架冷冻干燥。然后沿着两个不同的平面(x-y,y-z)切割纳米纤维支架,并通过扫描电子显微镜(sem)检查以显示支架的详细纤维结构。在膨胀之前,排列的电纺pcl纳米纤维垫由致密填充的原纤维结构构成(图2a)。相比之下,膨胀了20分钟和24小时的纳米纤维支架显示层状结构,具有由排列的纳米纤维赋予的保留的纳米形貌线索(图2a)。注意间隙距离随着反应时间增加而增加(图2b)。相比之下,随着反应时间的增加,层厚度从约15μm减小到5μm(图2c)。也比较了膨胀前后排列的纳米纤维支架的机械性能。由于膨胀纳米纤维材料的层状结构和高孔隙率,沿着平行于和垂直于纤维排列方向的拉伸模量与膨胀前的纳米纤维垫相比较低(表1)。与在膨胀之前的纳米纤维垫相比,沿着x、y和z方向测量的排列的纳米纤维支架的压缩杨氏模量在膨胀后较低(表1)。无规取向的pcl纳米纤维垫显示类似于用nabh4水溶液处理后的排列的纳米纤维垫的结果,除了与排列垫相比,无规垫的膨胀程度略小外(图3)。在膨胀后无规取向的纳米纤维支架中的拉伸模量和杨氏模量类似地降低(表2)。在表1和2中缺少在x和y方向上的极限拉伸应力、极限拉伸应变、最大应力、断裂应力和断裂应变的值,因为所有样品在最大拉伸力(500mn)下沿x和y方向没有断裂。该膨胀导致纳米纤维支架沿z方向的层状结构。由于层状结构,在沿着z方向的拉伸强度测试期间,膨胀后的支架可以容易地在层之间分裂。因此,膨胀后的支架沿z方向的拉伸性能未示于表1和表2。
表1:排列pcl纳米纤维支架膨胀前和膨胀后的机械性能。对纳米纤维支架给出的范围包括所有实验组。
表2:无规pcl纳米纤维支架膨胀前和膨胀后的机械性能。对无规pcl纳米纤维支架给出的范围包括所有实验组。
将本发明的膨胀方法应用于非平面纳米纤维支架,以形成对于再生组织化组织如神经、血管和腱而言理想的管状支架(panseri等人(2008)bmcbiotechnol.,8:39;hashi等人(2007)proc.natl.acad.sci.,104:11915-11920;hogan等人(2011)j.am.acad.orthop.surg.,19:134-142)。已经显示了由无规取向的电纺纳米纤维的外层和纵向排列的电纺纳米纤维的内层组成的双层纳米纤维导管的成功制造(xie等人(2014)acsappl.mater.interfaces6:9472-9480;xie等人(2010)nanoscale2:35-44)。尽管具有独特的多腔设计,但是制造的导管在导管的内腔内不包含支架材料。另外的研究尝试在纳米纤维导管的内腔内递送纵向排列的纳米纤维薄膜,以增强神经再生(clements等人(2009)biomaterials30:3834-3846;mukhatyar等人(2014)ann.biomed.eng.42:1436-1455)。无规和排列的纳米纤维的顺序沉积,随后手工缠绕在管状心轴周围,产生由无规取向的纳米纤维的外层和纵向排列的纳米纤维的内层组成的双层纳米纤维导管(图4a)。观察到用1mnabh4的水溶液处理双层纳米纤维导管以使纳米纤维材料膨胀并填充管的整个内腔(图4a)。对于由无规取向的纳米纤维的外层和周向排列的纳米纤维的内层组成的双层纳米纤维导管观察到类似的结果(图4b)。纳米纤维管的内径和外径也在水性介质中膨胀期间。在用1mnabh4的水溶液处理24小时后,由无规取向的纳米纤维的外层和纵向排列的纳米纤维的内层组成的双层导管的内径接近零,其中膨胀纤维占据了管的整个内腔(图4c)。相比之下,由无规取向的纳米纤维的外层和周向排列的纳米纤维的内层组成的双层纳米纤维管的内径在用1mnabh4溶液处理仅4小时后接近零(图4d)。类似于平面纳米纤维材料,膨胀的管状支架形成层状纳米纤维结构,其在同轴的圆周层中取向,延伸了构建体的长度(图5)。重要的是,管状纳米纤维支架维持纳米纤维的内层中的各向异性性质(图5)。在各种再生医学应用中,维持膨胀后的纤维排列是重要的,其中形貌线索是组织细胞群体和组织再生的关键。具体地,由排列纤维组成的膨胀构建体理想地适于提供在神经修复/再生期间增强和指导细胞迁移和轴突生长所必需的接触导向线索(bellamkonda,rv(2006)biomaterials27:3515-3518;patel等人2007)nanolett.,7:2122-2128)。
为了产生3d组织构建体,支架本身起重要作用,因为它不仅提供了仿生结构,而且提供了与某些线索一起支持细胞粘附和生长的底物,以调节细胞行为(murphy等(2014)nat.mater.13:547-557)。在本研究中,nih3t3成纤维细胞接种到由在膨胀前(1mm厚)和膨胀后(1cm厚)的排列纳米纤维组成的平面电纺支架上,并孵育1天和7天。选择成纤维细胞作为细胞培养的模型细胞,以便在接种和增殖后显示细胞浸润和分布。此外,成纤维细胞与腱和韧带组织再生有关。细胞接种的支架的苏木精-曙红(h&e)染色表明细胞成功浸润和增殖遍及整个的膨胀纳米纤维支架(图6)。相比之下,细胞没有穿透未膨胀的纳米纤维支架并且仅在材料的表面上增殖(图7)。甚至在培养7天后,在未膨胀的纳米纤维支架的表面上仅观察到几个细胞层,并且在支架的主体内没有观察到细胞浸润(图7)。重要的是,细胞形态在膨胀和未膨胀支架之间是一致的,因为细胞沿纤维排列的方向显示长形的形状。这种观察表明膨胀的支架保持由排列的纳米纤维赋予的形貌线索。
本文中已经显示,从nabh4水解反应产生的氢气气泡在第三维中膨胀排列的电纺纳米纤维垫,导致形成分层结构并同时维持所赋予的各向异性线索。在存在和不存在电纺纳米纤维支架的情况下观察到在1mnabh4溶液中的气泡形成(图8)。基于这些观察并且不受理论束缚,膨胀过程据称通过以下步骤发生:(i)由毛细作用驱动的nabh4水溶液快速渗透到排列的纳米纤维支架中;(ii)在纳米纤维的表面上或在不完全排列的纳米纤维的交叉处气泡的异相成核;(iii)在持续产生氢气的情况下成核气泡的生长;(iv)相邻气泡的聚结;和(v)在气泡的进一步生长和聚结后,形成“气泡层”。
在膨胀期间,观察到气泡从纳米纤维基质的表面逸出到溶液中和大气中。预期无规纳米纤维支架的膨胀遵循类似的过程,除了由于增加的纳米纤维缠结,水溶液更慢地渗透到无规取向的纳米纤维支架中可能导致更慢的膨胀率(图3)。类似地,因为缠结的纳米纤维之间的强相互作用,无规取向的纳米纤维支架的最大膨胀与排列的支架的最大膨胀相比可能减小。
虽然几项研究已经调查了制造3d电纺纳米纤维支架的手段,但很少有研究集中于由单轴排列的纳米纤维制成的各向异性支架的制造(blakeney等人(2011)biomaterials32:1583-1590;lee等人(2011)tissueeng.,parta,17:2695-2702;cai等人(2013)langmuir29:2311-2318;sheikh等人(2014)nanomedicine11:681-691;jeong等人(2014)j.mater.chem.b2:8116-8122)。本发明的方法允许使用由nabh4水解产生的气泡在第三维中在单轴排列和无规取向的纳米纤维支架中进行膨胀。虽然本研究使用水溶液来在纳米纤维垫内主要地引发气泡产生,但是可以成功地应用多种气体生产方法以实现相同的效果(例如,溶解的气体、高压气体液体/流体和声感应)(leongdengren等人(2011)acoust.ads.,39:54-63)。pcl纳米纤维垫的膨胀也在将其浸入1mnahco3和1mhcl溶液中交替地进行数轮后实现(图10)。此外,纳米纤维膜也使用由液体co2产生的气泡进行膨胀(图11)。
以前的研究表明单轴排列的纳米纤维可以提供指引和增强细胞迁移、细胞排列、肌管形成、轴突生长和伤口愈合的接触导向(murphy等人(2014)nat.mater.,13:547-557;choi等人(2008)biomaterials29:2899-2906;huang等人(2006)nanolett.,6:537-542;xie等人(2009)acsnano3:1151-1159)。此外,排列的纳米纤维已经被证明提供了用于调节干细胞分化的指导性微环境(yin等人(2010)biomaterials31:2163-2175;xie等人(2009)biomaterials30:354-362;ren等人(2013)actabiomater.,9:7727-7736)。虽然成功了,这些研究限于使用2d纳米纤维垫。
本文中,成功地形成了大规模的3d纳米纤维支架,同时保持由对于有组织的组织如神经、肌肉和腱的再生关键的单轴排列的纳米纤维赋予的纳米形貌线索。利用这种方法,可以顺序地沉积和膨胀不同顺序/排列的纳米纤维材料,以便重现复杂的组织结构和解剖结构,例如胃肠道结构或纤维环(bitar等人(2014)gastroenterology146:1614-1624;nerurkar等人(2009)nat.mater.,8:986-992)。此外,本发明的方法允许通过用各种水凝胶或生物基质填充纤维层之间的空间来形成3d、复合的或混合的支架。纳米纤维也可以使用表面轭合/包被或包封用另外的信号分子标记或修饰,以进一步调节细胞响应并促进组织再生(wegst等(2015)nat.mater.,14:23-36)。这些新颖的特征清楚地区分了本发明的膨胀纳米纤维膜的方法和来自先前报道的所得3d电纺纳米纤维支架。
总之,已经提供了用于在第三维中膨胀电纺纳米纤维垫/膜,同时保留赋予的各向异性特征和线索的可控方法。使用这种方法形成的3d支架支持在整个材料本体中强健的细胞浸润和增殖。本技术可用于合成用于再生医学和用于药物筛选和生物学研究的工程化3d组织模型中的支架和构建体。这种新颖的处理技术还可以应用于用于各种医疗应用的先进纳米纤维支架的制造。
虽然上面已经描述和具体例示了本发明的某些优选实施方案,但是并不意味着本发明限于这样的实施方案。在不脱离如所附权利要求中阐述的本发明的范围和精神的情况下,可以对其进行各种修改。
- 还没有人留言评论。精彩留言会获得点赞!