一种聚乙二醇修饰的钙基纳米药物递送颗粒及其制备方法和应用与流程
本发明涉及生物医药领域,具体涉及一种聚乙二醇修饰的钙基纳米药物递送颗粒及其制备方法和应用。
背景技术:
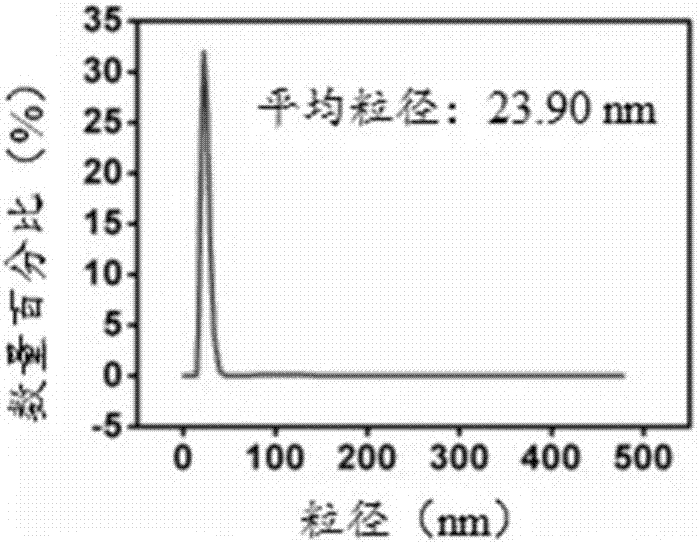
:基因治疗为许多严重的获得性疾病及先天性疾病带来了治愈的希望。但是缺乏安全、高效的和稳定表达的基因投递系统是阻碍基因治疗进入临床的最大障碍。病毒载体是一类常见的基因载体,它利用病毒对宿主细胞的感染将外源基因导入宿主细胞内。一般包括腺病毒载体(av),腺相关病毒载体(aav),逆转录病毒等。虽然病毒载体具有较高的转染效率,但病毒载体装载基因容量有限,而且具有免疫原性存在潜在的生物安全性隐患,所以病毒基因载体的临床应用亦难以推进。近年来,微环dna(minicircledna,mcdna)的出现,成为基因载体中的一大亮点,微环dna是一个环状的表达盒子,是通过dna重组技术,把标准质粒的细菌dna骨架去除后的产物,即微环dna只含有一个基因表达框而没有外在的细菌骨架序列,其优点是能有效延长靶基因在细胞内的表达时间、大量携带功能基因片段且几乎无任何毒性。但是由于裸露的dna在生理环境中会被迅速清除(主要是机体中各种酶的降解),不能有效进入靶细胞核,所以仍需合适的投递系统将微环dna递送至靶向组织或器官。常用的基因投递系统包括硅酸钙,阳离子脂质体,阳离子多聚物(聚乙烯亚胺pei)等。这类投递系统免疫原性较低、基因装载容量大,但是转染效率低,大大限制了其临床应用。因此,研究开发高效,具有良好生物相容性且具有靶向性的基因投递系统是解决基因药物临床应用的关键。钙硅基(cao·sio2-based)生物材料是近三十年兴起的新型生物活性材料,钙元素的引入使它比传统硅基材料具有更好的生物活性、生物相容性和生物可降解性,它能在模拟体液环境下逐渐转变为类骨磷灰石,是一类具有巨大应用前景的无机生物材料,已经在载药、骨修复、牙齿修复等领域有广泛的应用,而硅酸钙作为基因载体却鲜有报道。传统沉淀法制备的硅酸钙颗粒的粒度可控性差,在水溶液中易团聚,分散性不佳。本发明通过微乳液法制备单分散的硅酸钙纳米颗粒,将微环dna包裹在硅酸钙颗粒内部,外部修饰聚乙二醇(peg),利 用聚乙二醇(peg)形成的水化层,保护dna在体内投递过程中不被机体网状内皮系统(res)清除和各种dna酶的降解,从而实现微环dna的靶向投递。技术实现要素:针对现有技术的不足,本发明提供了一种聚乙二醇修饰的钙基纳米药物递送颗粒及其制备方法和应用。第一方面,本发明提供了一种聚乙二醇修饰的钙基纳米药物递送颗粒,所述聚乙二醇修饰的钙基纳米药物递送颗粒的粒径为20~200nm;所述聚乙二醇修饰的钙基纳米药物递送颗粒包括第一目标投递物、包裹有第一目标投递物的钙基颗粒,其中,所述钙基颗粒表面修饰有聚乙二醇,所述第一目标投递物为生物药物、化学药物或包载有核酸片段的第二目标投递物,所述包载有核酸片段的第二目标投递物为包裹、结合或共混有核酸片段的阳离子聚合物、多肽、聚氨基酸或转染试剂。如本发明所述的,“核酸片段”包括天然或人工合成的dna片段、rna片段、mrna、sirna、shrna等。可选地,所述生物药物包括但不限于核酸、多肽、蛋白和疫苗一种或多种;所述化学药物包括但不限于抗肿瘤小分子药、荧光素和淋巴示踪剂一种或多种。优选地,所述聚乙二醇修饰的钙基纳米药物递送颗粒的载药量为0.001~0.85,进一步优选为0.05~0.85。如本发明所述的,所述“载药量”为所述的被包裹药物与所述聚乙二醇修饰的钙基纳米药物递送颗粒的质量比。可选地,在第一目标投递物中,被包裹药物为生物药物或化学药物;在第二目标投递物中,被包裹药物为核酸片段。优选地,所述钙基为生物可降解性钙盐,所述生物可降解性钙盐包括但不限于硅酸钙、磷酸钙、柠檬酸钙或碳酸钙。优选地,所述包裹、结合或共混有核酸片段的阳离子聚合物(如聚乙烯亚胺)、多肽、聚氨基酸或转染试剂中,所述的阳离子聚合物、多肽、聚氨基酸、转染试剂可分别独立地选自表1中所例举的阳离子聚合物、多肽、聚氨基酸、转染试剂:表1表1中的中英文对照如表2所示:表2进一步优选地,所述的包载有核酸片段的第二目标投递物为将阳离子聚合物(如聚乙烯亚胺)、多肽、聚氨基酸或商品化转染试剂与含有核酸片段的溶液按照氮磷比为0.1~100:1的比例(优选按照氮磷比为10~20:1的比例)混合并孵育制得(优选为5~40min)。如本发明所述的,所述“氮磷比”为阳离子聚合物(如聚乙烯亚胺)、多肽、聚氨基酸或商品化转染试剂中氨基的摩尔数与含有核酸片段的溶液中磷酸根的摩尔数之比。进一步优选地,所述包载有核酸片段的第二目标投递物为将聚乙烯亚胺溶液或聚乙烯亚胺衍生物(peicl)与含有核酸片段的溶液按照氮磷比为0.1~100:1的比例混合并孵育5~40min制得,其中,所述聚乙烯亚胺的分子量为600~70000道尔顿;所述聚乙烯亚胺衍生物(peicl)的分子量为1000~70000道尔顿(优选为34000~70000道尔顿),所述聚乙烯亚胺衍生物(peicl)的结构式如式ⅰ所示,其中,x、y、z为非负整数,且x、y和z均不为零;更进一步优选地,所述聚乙烯亚胺的分子量为25000道尔顿。优选地,所述聚乙二醇修饰的钙基纳米药物递送颗粒的粒径为20~40nm。第二方面,本发明提供了一种聚乙二醇修饰的钙基纳米药物递送颗粒的制备方法,包括如下步骤:(1)将第一目标投递物溶液与第一可溶性钙盐溶液混合均匀后加至有机相中,搅拌20~60min制得微乳液a;其中,所述第一目标投递物为生物药物、化学药物或包载有核酸片段的第二目标投递物;所述有机相为将表面活性剂与碳原子数为6~12的烷烃化合物(优选按体积比为25~40:60~75的比例)混合制得,所述的表面活性剂为聚乙二醇壬基苯基醚(igepalco-520)、聚乙二醇辛基苯基醚(tritonx-100)、双(2-乙基己基)琥珀酸酯磺酸钠(aot)和十二烷基硫酸钠(sds)中的一种或多种;所述包载有核酸片段的第二目标投递物为包裹、结合或共混有核酸片段的阳离子聚合物、多肽、聚氨基酸或转染试剂,其中,阳离子聚合物、多肽、聚氨基酸或转染试剂中氨基的摩尔数与所述核酸片段中磷酸基团的摩尔数之比为0.1~100:1;(2)将可溶性盐溶液加至步骤(1)所得的微乳液a中,搅拌2~4h制得微乳液b;其中,所述可溶性盐溶液包括但不限于可溶性硅盐溶液、可溶性磷酸盐溶液、可溶性柠檬酸盐溶液或可溶性碳酸盐溶液,所述可溶性硅盐溶液中的硅元素、可溶性磷酸盐溶液中的磷元素、可溶性柠檬酸盐溶液中的柠檬酸根或可溶性碳酸盐溶液中的碳酸根与步骤(1)所述第一可溶性钙盐溶液中的钙元素的摩尔比为0.01~10:1(优选为0.43~3.5);(3)将磷酸-聚乙二醇水溶液加至步骤(2)所得的微乳液b中,搅拌2~4h,得到微乳液c,其中,所述磷酸-聚乙二醇水溶液中磷酸-聚乙二醇的质量与步骤(1)第一可溶性钙盐溶液中钙元素的物质的量的比为0.001~100:1(优选为0.008~100);(4)去除步骤(3)所得的微乳液c中的有机相,离心、洗涤后,用水和/或乙醇分散即得聚乙二醇修饰的钙基纳米药物递送颗粒;其中,所得聚乙二醇修饰的钙基纳米药物递送颗 粒的粒径为20~200nm;所述聚乙二醇修饰的钙基纳米药物递送颗粒包括第一目标投递物、包裹有第一目标投递物的钙基颗粒,其中,所述钙基颗粒表面修饰有聚乙二醇,所述第一目标投递物为生物药物、化学药物或包载有核酸片段的第二目标投递物,所述包载有核酸片段的第二目标投递物为包裹、结合或共混有核酸片段的阳离子聚合物、多肽、聚氨基酸或转染试剂。在本发明第二方面提供聚乙二醇修饰的钙基纳米药物递送颗粒的制备方法中,所述的第二目标投递物,采用带正电性阳离子聚合物、多肽、聚氨基酸或转染试剂包载核酸片段,形成几十至几百纳米的小颗粒,为后续钙基的生长提供软模板;进一步地,可以通过调节水体系与有机相的体积来调节所制备的钙基纳米粒子的大小。更进一步地,本发明第二方面提供聚乙二醇修饰的钙基纳米药物递送颗粒的制备方法还可以通过调节核酸片段的量、核酸片段与阳离子聚合物的氮磷(n/p)比来调节所制备的钙基纳米粒子的大小。可选地,所述步骤(1)中,所述生物药物包括但不限于核酸、多肽、蛋白和疫苗中的一种或多种;所述化学药物包括但不限于抗肿瘤小分子药、荧光素和淋巴示踪剂中的一种或多种。优选地,所述步骤(1)中,所述核酸包裹、结合或共混有核酸片段的阳离子聚合物(如聚乙烯亚胺)、多肽、聚氨基酸或转染试剂,所述的阳离子聚合物、多肽、聚氨基酸、转染试剂可分别独立地选自表1中所例举的阳离子聚合物、多肽、聚氨基酸、转染试剂。进一步优选地,所述包载有核酸片段的第二目标投递物中,阳离子聚合物(如聚乙烯亚胺)、多肽、聚氨基酸或商品化转染试剂中氨基的摩尔数与含有核酸片段的溶液中磷酸基团的摩尔数之比为10~20:1。可选地,所述的包载有核酸片段的第二目标投递物为将阳离子聚合物(如聚乙烯亚胺)、多肽、聚氨基酸或商品化转染试剂与含有核酸片段的溶液混合并孵育制得(优选为5~40min)。进一步优选地,所述包载有核酸片段的第二目标投递物为将聚乙烯亚胺溶液或聚乙烯亚胺衍生物(peicl)与含有核酸片段的溶液按照氮磷比为0.1~100:1的比例混合并孵育5~40min制得,其中,所述聚乙烯亚胺的分子量为600~70000道尔顿;所述聚乙烯亚胺衍生物(peicl)的分子量为1000~70000道尔顿(优选为34000~70000道尔顿),所述聚乙烯亚胺衍生物(peicl)的结构式如式ⅰ所示,其中,x、y、z为非负整数,且x、y和z均不为零;更进一步优选地,所述聚乙烯亚胺的分子量为25000道尔顿。优选地,所述步骤(1)中,所述第一可溶性钙盐溶液的浓度为1~1000mm。优选地,所述步骤(1)中,所述第一可溶性钙盐溶液包括但不限于氯化钙、硝酸钙和溴化钙中的一种或多种。优选地,所述步骤(1)中,所述有机相为环己烷与聚乙二醇壬基苯基醚按体积比7:3的比例混合制得。优选地,所述步骤(1)中,第一目标投递物溶液与第一可溶性钙盐溶液的总体积与有机相的体积比为0.01~0.05:1,进一步优选为0.01~0.02:1。优选地,所述步骤(2)中,可溶性盐溶液与步骤(1)所得的微乳液a的体积比为0.01~0.1:1,进一步优选为0.02~0.1:1。优选地,所述步骤(2)中,所述可溶性硅盐包括但不限于正硅酸乙酯、硅酸钠和硅酸钾中的一种或多种。优选地,所述步骤(2)中,所述可溶性硅盐溶液中,硅酸根的浓度为1~1000mm。优选地,所述步骤(2)中,所述可溶性磷酸盐包括但不限于磷酸氢二钠、磷酸二氢钠、磷酸钠、磷酸二氢钾和磷酸氨中的一种或多种。优选地,所述步骤(2)中,所述可溶性磷酸盐溶液中,磷酸根的浓度为1~1000mm。优选地,所述步骤(2)中,所述可溶性柠檬酸盐包括但不限于柠檬酸钠、柠檬酸钙和柠檬酸钾中的一种或多种。优选地,所述步骤(2)中,所述可溶性柠檬酸盐溶液中,柠檬酸根的浓度为1~1000mm。优选地,所述步骤(2)中,所述可溶性碳酸盐包括但不限于碳酸钠、碳酸氢钠和碳酸钾中的一种或多种。优选地,所述步骤(2)中,所述可溶性碳酸盐溶液中,碳酸根浓度为1~1000mm。优选地,所述步骤(2)中,所述的将可溶性盐溶液加至步骤(1)所得的微乳液a中,搅拌2~4h制得微乳液b,具体包括:将可溶性盐溶液加至步骤(1)所得的微乳液a中,搅拌2~4h后,再加入第二可溶性钙盐溶液,搅拌15~18h制得微乳液b;其中,所述第二可溶性钙盐溶液中的钙元素与步骤(1)中的第一可溶性钙盐溶液中的钙元素的摩尔比为0.1~10:1(进一步优选为0.45~8:1)。进一步优选地,所述第一可溶性钙盐溶液和第二可溶性钙盐溶液分别独立地选自氯化钙、硝酸钙和溴化钙中的一种或多种。进一步优选地,所述第二可溶性钙盐溶液的浓度为1~1000mm。进一步优选地,所述步骤(2)中,所述将可溶性盐溶液加至步骤(1)所得的微乳液a中,搅拌2~4h制得微乳液b,具体包括:将可溶性盐溶液加入到有机溶液中,搅拌1~2h后加至步骤(1)所得的微乳液a中,搅拌2~4h后,再加入第二可溶性钙盐溶液,搅拌15~18h制得微乳液b;其中,所述有机溶液为将表面活性剂与碳原子数为6~12的烷烃化合物(优选按体积比为25~40:60~75的比例)混合制得,所述的表面活性剂为聚乙二醇壬基苯基醚(igepalco-520)、聚乙二醇辛基苯基醚(tritonx-100)、双(2-乙基己基)琥珀酸酯磺酸钠(aot)和十二烷基硫酸钠(sds)中的一种或多种;所述第二可溶性钙盐溶液中的钙元素与步骤(1)中的第一可溶性钙盐溶液中的钙元素的摩尔比为0.1~10:1(进一步优选为0.45~8:1)。进一步优选地,所述步骤(2)中,所述有机溶液与步骤(1)中的有机相的体积比为1:1。优选地,所述步骤(3)中,磷酸-聚乙二醇水溶液与步骤(2)所得的微乳液b的体积比为0.002~0.03:1。优选地,所述步骤(3)中,所述磷酸-聚乙二醇的分子量为600~12000道尔顿。进一步优选地,所述磷酸-聚乙二醇的分子量为2000道尔顿。优选地,所述步骤(3)中,所述磷酸-聚乙二醇包括但不限于单磷酸聚乙二醇、双磷酸聚乙二醇、马来酰亚胺磷酸聚乙二醇,其中,所述单磷酸聚乙二醇的结构式如式ⅱ所示,n为非负整数,且不为零,所述双磷酸聚乙二醇的结构式如式ⅲ所示,n为非负整数,且不为零,所述马来酰亚胺磷酸聚乙二醇的结构式如式ⅳ所示,n为非负整数,且不为零,进一步优选地,所述磷酸-聚乙二醇为如式ⅱ所示化合物。优选地,所述步骤(3)中,所述磷酸-聚乙二醇水溶液的浓度为1~1000mm。优选地,所述步骤(3)中,所述磷酸-聚乙二醇水溶液中磷酸-聚乙二醇与第一可溶性钙盐溶液中钙元素的摩尔比为0.001~100:1(进一步优选为0.008~100)。可以理解的是,所述步骤(3)中,磷酸-聚乙二醇中的聚乙二醇端可以连接配体,所述配体包括但不限于叶酸、rgd(如本发明所述的“rgd”由精氨酸、甘氨酸和天冬氨酸组成)及其类似物、多肽、半乳糖、转铁蛋白或抗体,则所述步骤(4)中,所述聚乙二醇修饰的钙基纳米药物递送颗粒中的聚乙二醇端可以连接配体,所述配体包括但不限于叶酸、rgd及其类似物、多肽、半乳糖、转铁蛋白或抗体。优选地,所述步骤(4)中,所述聚乙二醇修饰的钙基纳米药物递送颗粒的粒径为20~40nm。优选地,所述步骤(4)中,所述聚乙二醇修饰的钙基纳米药物递送颗粒的载药量为0.001~0.85(进一步优选为0.05~0.85)。可以理解的是,在第一目标投递物中,被包裹药物为生物药物或化学药物;在第二目标投递物中,被包裹药物为核酸片段。优选地,本发明如第一方面所述的聚乙二醇修饰的钙基纳米药物递送颗粒为采用如第二方面所述的聚乙二醇修饰的钙基纳米药物递送颗粒的制备方法制得。第三方面,本发明还提供了一种药物组合物,包括如第一方面所述的聚乙二醇修饰的钙基纳米药物递送颗粒。第四方面,本发明还提供了一种如第一方面所述的聚乙二醇修饰的钙基纳米药物递送颗粒或如第二方面所述的聚乙二醇修饰的钙基纳米药物递送颗粒的制备方法在制备药物中的应用。优选地,如第一方面所述的聚乙二醇修饰的钙基纳米药物递送颗粒或如第二方面所述的聚乙二醇修饰的钙基纳米药物递送颗粒的制备方法在制备靶向投递药物中的应用。本发明的有益效果在于:(1)与其他无机纳米颗粒相比,本发明所提供的聚乙二醇修饰的钙基纳米药物递送颗粒的粒径得到有效的控制,均在200nm以下,而且可以在乙醇或水中形成单分散颗粒,且分散性质稳定,不会团聚;而且钙基颗粒表面有聚乙二醇(peg)链保护,可以避免颗粒过早的被网状内皮系统吞噬,延长体内循环的时间,用于体内转染研究;(2)可以通过调节核酸片段的量、阳离子聚合物与核酸片段的氮磷(n/p)比、水体系的体积与有机相体积等条件调节制备的钙基纳米粒子的大小;(3)可选地,将聚乙二醇(peg)的另一端接上具有不同靶向性的配体,可以使颗粒具有特定的靶向性;(4)本发明提供的聚乙二醇修饰的钙基纳米药物递送颗粒具有制备成本低、毒性低、安全有效的优势。附图说明图1-2是本发明实施例提供的磷酸-peg修饰的硅酸钙-微环dna纳米颗粒的透射电子显微镜(tem)照片(图1)和粒径分布图(图2);图3是本发明实施例提供的磷酸-peg修饰的硅酸钙-微环dna(egfp)纳米颗粒与293t细胞株体外共培养的荧光(a)和白光(b)图片;图4是本发明实施例提供的聚乙二醇(peg)修饰的硅酸钙包裹该黄绿素形成的纳米颗粒的透射电子显微镜(tem)照片(a)和粒径分布图(b);图5是本发明实施例提供的聚乙二醇(peg)修饰的硅酸钙包裹ir820染料形成的纳米颗粒透射电子显微镜(tem)照片(a)和粒径分布图(b)。具体实施方式下面结合附图和实施例对本发明做进一步说明。本发明实施例采用的peicl的结构式如式ⅰ所示,其中,x、y、z为非负整数,且x、y和z均不为零;本发明实施例1-4、6-17采用的磷酸-聚乙二醇为单磷酸聚乙二醇,所述单磷酸聚乙二醇的结构式如式ⅱ所示,其中,n为非负整数,且不为零,实施例1无聚乙二醇(peg)修饰的硅酸钙-微环dna纳米颗粒的制备本发明一实施例提供了一种无聚乙二醇(peg)修饰的硅酸钙-微环dna纳米颗粒的制备方法,包括如下步骤:(1)将10μldna溶液(0.5μg/μl),与10μlpei25k阳离子聚合物溶液(1.3μg/μl)混合均匀,孵育30分钟;然后,加入80μl氯化钙溶液(500mm,ph10.0),用移液枪吹打使之混合均匀后,在搅拌下滴加到5ml有机相(有机相为环己烷与聚乙二醇壬基苯基醚520(igepalco-520)按体积比7/3混合制得)中,搅拌1h形成微乳液a;(2)将正硅酸乙酯(teos)在搅拌下滴加到步骤(1)所得的微乳液a中,搅拌一个小时形成微乳液b;(3)将100μl氯化钙溶液(500mm,ph10.0)在搅拌下滴加到步骤(2)所得的微乳 液b中,搅拌18小时,得到微乳液c;用旋转蒸发仪蒸发除去微乳液c中的环己烷,再在14000g下离心15分钟,用无水乙醇洗三次,在水中分散即得到硅酸钙-微环dna纳米颗粒。1、粒径测定:将本发明实施例所制得的聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒用1ml双蒸水溶解后,超声30s后,采用透射电镜观察颗粒,以及用马尔文动态光散射粒径仪上测定颗粒粒径;测定结果如表1所示。2、载药量的测定:称取1mg步骤(4)所得的硅酸钙-微环dna纳米颗粒,在900℃附近的重量损失,计算得到药物的装载量,所用升温速率为10℃/min,所用气氛为流动空气气氛;载药量=dna的质量/纳米颗粒的总质量。实验结果:(1)本发明实施例所制备的无聚乙二醇(peg)修饰的硅酸钙-微环dna纳米颗粒的平均粒径为20.36nm;(2)本发明实施例所制备的无聚乙二醇(peg)修饰的硅酸钙-微环dna纳米颗粒的载药量为0.102。实施例2聚乙二醇(peg)修饰的硅酸钙-微环dna纳米颗粒的制备本发明一实施例提供了一种聚乙二醇(peg)修饰的硅酸钙-微环dna纳米颗粒的制备方法,包括如下步骤:(1)将10μldna溶液(0.5μg/μl),与10μl聚乙烯亚胺(pei25k)溶液(1.3μg/μl)混合均匀,孵育30分钟;再加入80μl氯化钙溶液(500mm,ph10.0),用移液枪使之混合均匀后,在搅拌下滴加到5ml有机相(有机相为环己烷与聚乙二醇壬基苯基醚520(igepalco-520)按体积比7/3混合制得)中,搅拌一个小时形成微乳液a;(2)将500μl正硅酸乙酯(teos)在搅拌下滴加到步骤(1)所得的微乳液a中,搅拌4小时后,将在搅拌下滴加入10μl氯化钙溶液(500mm,ph10.0),搅拌18小时,得到微乳液b;(3)将15μl磷酸-peg(磷酸-peg的分子量为2000道尔顿)水溶液(100μg/μl)滴加入步骤(2)所得的微乳液b中,搅拌4小时,得到微乳液c;(4)用旋转蒸发仪蒸发除去微乳液c中的环己烷,再在14000g下离心15分钟,用无水乙醇洗三次,高纯水洗两次,在水中分散即得到聚乙二醇(peg)-硅酸钙-微环dna纳 米颗粒。1、粒径测定:将本发明实施例所制得的聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒用1ml双蒸水溶解后,超声30s后,采用透射电镜观察颗粒,以及用马尔文动态光散射粒径仪上测定颗粒粒径。2、转染实验,包括如下步骤:将人肾上皮细胞系细胞(293t)经复苏、培养,转染前以每孔104个细胞分别均匀接种于96孔板,用含10%胎牛血清的dmem培养基培养,细胞达到70%~80%融合后,换取40μl的不含fbs的空白培养基,37℃,5%co2孵育2~6小时,分别依次加入10μl步骤(5)所得的聚乙二醇(peg)修饰的硅酸钙-微环dna纳米颗粒(每孔含0.5μgdna),用移液器轻柔上下吹吸混合均匀,在37℃,5%co2条件下孵育6小时后,用含10%胎牛血清的培养基换液,在37℃,5%co2条件下继续培养,每隔24小时,用倒置荧光显微镜观察细胞内表达的绿色荧光蛋白(gfp)。3、载药量的测定:称取1mg步骤(4)所得的聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒,在900℃附近的重量损失,计算得到药物的装载量,所用升温速率为10℃/min,所用气氛为流动空气气氛;载药量=dna的质量/纳米颗粒的总质量。实验结果:(1)图1-2是本发明实施例所制得的磷酸-peg修饰的硅酸钙-微环dna纳米颗粒透射电子显微镜(tem)照片(图1)和粒径分布图(图2)。如图1所示,本发明实施例所制得的磷酸-peg修饰的硅酸钙-微环dna纳米颗粒的粒径为20~30nm。如图2所示,本发明实施例所制得的磷酸-peg修饰的硅酸钙-微环dna纳米颗粒的平均粒径为23.90nm。(2)图3是本发明实施例提供的磷酸-peg修饰的硅酸钙-微环dna(egfp)纳米颗粒与293t细胞株体外共培养的荧光(a)和白光(b)图片。从图3可以看出,实施例2步骤(5)所得的聚乙二醇(peg)修饰的硅酸钙-微环dna纳米颗粒对293t细胞有一定的转染效果。(3)本发明实施例所制得的磷酸-peg修饰的硅酸钙-微环dna纳米颗粒的载药量为0.275。实施例3-4为了进一步说明本发明的有益效果,重复实施例2的实验步骤,将实施例2中步骤(1)-(4)中各药品的浓度和体积分别替换成如表1实施例3所示的各药品的浓度和体积,得到聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒。为了进一步说明本发明的有益效果,重复实施例2的实验步骤,将实施例2中步骤(1)-(4)中各药品的浓度和体积分别替换成如表3实施例4所示的各药品的浓度和体积,得到聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒。为了进一步说明本发明的有益效果,重复实施例2的步骤,将实施例2中步骤(2)中的正硅酸乙酯(teos)替换成硅酸钠溶液,所述硅酸钠溶液(ph9.0)的浓度为500mm,体积为100ul,得到聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒。按照实施例2的粒径测定方法和载药量测定方法,分别测得实施例3-5所得聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的平均粒径和载药量。实验结果:(1)实施例3-4所得聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的平均粒径分别为20.4、85.6nm。(2)实施例3-4所得聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的载药量分别为0.05、0.85。表3实施例3-4各步骤所用药品的用量注:表3中“\”表示该表格中不需要提供相关信息。实施例5为了进一步说明本发明的有益效果,重复实施例2的步骤,将实施例2中步骤(2)中的正硅酸乙酯(teos)替换成硅酸钠溶液,所述硅酸钠溶液(ph9.0)的浓度为500mm,体积为100ul,将实施例2中步骤(3)中的磷酸-聚乙二醇替换成双磷酸聚乙二醇,得到聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒;其中,所述双磷酸聚乙二醇的结构式如式ⅲ所示,n为非负整数,且不为零,按照实施例2的粒径测定方法和载药量测定方法,测得本实施例所得的聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的平均粒径和载药量。实验结果:(1)本发明实施例所得的聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的平均粒径分别为37.7nm。(2)本发明实施例所得的聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的载药量分别为0.366。实施例6-7氮磷(n/p)比对粒径和载药量的影响为了进一步说明本发明的有益效果,进一步探讨聚乙烯亚胺阳离子聚合物与dna的氮磷(n/p)比对聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒粒径的影响,重复实施例2的实验步骤,将实施例2中步骤(1)中10ulpei25k溶液(1.3μg/ul)替换成5ulpei25k溶液(1.3μg/ul)(如表4中实施例6所示),得到聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒。为了进一步说明本发明的有益效果,进一步探讨聚乙烯亚胺阳离子聚合物与dna的氮磷(n/p)比对聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒粒径的影响,重复实施例2的实验步骤,将实施例2中步骤(1)中10ulpei25k溶液(1.3μg/ul)替换成1ulpei25k溶液(1.3μg/ul)(如表4中实施例7所示),得到聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒,获得所述纳米颗粒的粒径。按照实施例2的粒径测定方法和载药量测定方法,分别测得实施例6和实施例7所得聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的平均粒径和载药量。实验结果:(1)测定结果如表4所示,本发明实施例2、6、7所得聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的平均粒径分别为23.90、110.23、1040.50nm,随着氮磷比(即n/p,所述聚乙烯亚胺的氨基的摩尔数与所述dna的磷酸根的摩尔数的比)的增大,聚乙烯亚胺压缩dna大分子的效果更加明显,pei与dna的混合物为矿化硅酸钙提供软模板作用,因此,形成的聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的平均粒径减小。(2)如表4所示,本发明实施例2、6、7所得聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的载药量分别为0.275、0.305、0.224,这说明所述的氮磷比对载药量影响不大。表4氮磷(n/p)比对粒径和载药量的影响实施例8-9有机相用量对粒径和载药量的影响为了进一步说明本发明的有益效果,进一步探讨有机相用量对聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒粒径的影响,重复实施例2的实验步骤,将实施例2中步骤(1)中5ml有机相替换成2.5ml有机相(如表5中实施例8所示),得到聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒。为了进一步说明本发明的有益效果,进一步探讨有机相用量对聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒粒径的影响,重复实施例2的实验步骤,将实施例2中步骤(1)中5ml 有机相替换成1ml有机相(如表5中实施例9所示),得到聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒。按照实施例2的粒径测定方法和载药量测定方法,分别测得实施例6和实施例7所得聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的平均粒径和载药量。实验结果:(1)如表5所示,实施例2、8、9所得聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的平均粒径分别为23.90、175.11、788.52nm;随着有机相体积减小(水相体积相对增大),反应过程所形成的微乳液中水滴半径增大,产物粒径随着增大。(2)如表5所示,本发明实施例2、8、9所得聚乙二醇(peg)-硅酸钙-微环dna纳米颗粒的载药量相差不大,分别为0.275、0.314;而本发明实施例9中,这是由于有机相的体积过小(即,水相体积过大)导致所制备的产物在收集过程中被包载的药物渗漏,使得载药量减少,为0.102。表5有机相用量对粒径和载药量的影响实施例有机相的体积/ml平均粒径/nm载药量例2523.900.245例82.5175.110.314例91788.520.102实施例10聚乙二醇(peg)修饰的硅酸钙包裹钙黄绿素纳米颗粒的制备本发明一实施例提供了一种聚乙二醇(peg)修饰的硅酸钙包裹钙黄绿素纳米颗粒的制备方法,包括如下步骤:(1)取5μl钙黄绿素溶液(饱和水溶液),与100μl氯化钙溶液(氯化钙浓度为500mm,ph10.0)混合均匀;将上述混合溶液在搅拌下滴加到5ml有机相(有机相为环己烷与聚乙二醇壬基苯基醚520(igepalco-520)按体积比7/3混合制得)中,搅拌1h形成微乳液a;(2)将10μl正硅酸乙酯(teos)步骤(1)所得的微乳液a中,搅拌4小时后,在搅拌下滴加80μl氯化钙溶液(氯化钙浓度为500mm,ph10.0),搅拌18小时,得到微乳液b;(3)将15μl(100μg/μl)磷酸-peg水溶液滴加入微步骤(2)所得的微乳液b中,搅拌4小时得到微乳液c;(4)用旋转蒸发仪蒸发除去微步骤(3)所得的微乳液c中的环己烷,再在14000g 下离心15分钟,用无水乙醇洗三次,高纯水洗两次,再在水中分散即得到聚乙二醇(peg)-硅酸钙-钙黄绿素纳米颗粒。按照实施例2中的粒径和载药量的测定方法测试步骤(4)所得的聚乙二醇(peg)-硅酸钙-钙黄绿素纳米颗粒的粒径和载药量。实验结果:(1)粒径:图4是本发明实施例提供的聚乙二醇(peg)修饰的硅酸钙包裹钙黄绿素形成的纳米颗粒的透射电子显微镜(tem)照片(a)和粒径分布图(b)。如图4(a)所示,本发明实施例所制得的聚乙二醇(peg)修饰的硅酸钙包裹钙黄绿素形成的纳米颗粒的粒径为30~40nm。如图4(b)所示,本发明实施例所制得的聚乙二醇(peg)修饰的硅酸钙包裹钙黄绿素形成的纳米颗粒的平均粒径为34.1nm。(2)载药量:本发明实施例所制得的聚乙二醇(peg)修饰的硅酸钙包裹钙黄绿素形成的纳米颗粒的载药量为0.112。实施例11聚乙二醇(peg)修饰的硅酸钙包裹钙ir820染料纳米颗粒的制备本发明一实施例提供了一种聚乙二醇(peg)修饰的硅酸钙包裹钙ir820染料纳米颗粒的制备方法,包括如下步骤:(1)取5μl(1μg/μl)ir820水溶液,与100μl氯化钙溶液(500mm,ph10.0)混合均匀;将上述混合溶液在搅拌下滴加到5ml有机相(有机相为环己烷与聚乙二醇壬基苯基醚520(igepalco-520)按体积比7/3混合制得)中,搅拌一个小时形成微乳液a;(2)将100μl正硅酸乙酯(teos)步骤(1)所得的微乳液a中,搅拌4小时后,在搅拌下滴加入80μl氯化钙溶液(500mm,ph10.0),搅拌18小时,得到微乳液b;(3)将1μl磷酸-聚乙二醇(peg)水溶液(10μg/μl)滴加入步骤(2)所得的微乳液b中,搅拌4小时,得到微乳液c;(4)用旋转蒸发仪蒸发除去步骤(3)所得的微乳液c中的环己烷,再在14000g下离心至少15分钟,用无水乙醇洗三次,高纯水洗两次,再在水中分散即得到聚乙二醇(peg)-硅酸钙-ir820纳米颗粒。按照实施例2中的粒径和载药量的测定方法测试步骤(4)所得的聚乙二醇(peg)-硅酸钙-钙黄绿素纳米颗粒的粒径和载药量。实验结果:(1)粒径:图5是本发明实施例提供的聚乙二醇(peg)修饰的硅酸钙包裹ir820染料形成的纳米颗粒的透射电子显微镜(tem)照片(a)和粒径分布图(b)。如图5(a)所示,本发明实施例所制得的聚乙二醇(peg)修饰的硅酸钙包裹ir820染料形成的纳米颗粒的粒径为30~40nm。如图5(b)所示,本发明实施例所制得的聚乙二醇(peg)修饰的硅酸钙包裹ir820染料形成的纳米颗粒的平均粒径为31.1nm。(2)载药量:本发明实施例所制得的聚乙二醇(peg)修饰的硅酸钙包裹ir820染料形成的纳米颗粒的载药量为0.144。实施例12-13磷酸-聚乙二醇(peg)修饰的磷酸钙-微环dna-纳米颗粒的制备本发明实施例12提供了一种磷酸-聚乙二醇(peg)修饰的硅酸钙-微环dna-纳米颗粒的制备方法,包括如下步骤:(1)将5μldna溶液(1μg/μl),与5μlpeicl34k阳离子聚合物溶液(3.8μg/μl)混合均匀,孵育30分钟;再加入90μl氯化钙溶液(100mm,ph9.0),用移液枪使之混合均匀后;在搅拌下滴加到5ml有机相(有机相为环己烷与聚乙二醇壬基苯基醚520(igepalco-520)按体积比7/3混合制得)中,搅拌一个小时形成微乳液a;(2)将100μl磷酸氢二钠溶液(100mm,ph9.0)在搅拌下滴加到5ml有机相(有机相为环己烷与聚乙二醇壬基苯基醚520(igepalco-520)按体积比7/3混合制得)中,搅拌一个小时后,在搅拌下滴加到步骤(1)所得的微乳液a中,搅拌4小时后,在搅拌下滴加入20μl氯化钙溶液(100mm,ph9.0),搅拌18小时得到微乳液b;(3)将20μl磷酸-聚乙二醇(1μg/μl)水溶液在搅拌下滴加到步骤(2)所得的微乳液b中,搅拌4小时,得到微乳液c;(4)用旋转蒸发仪蒸发除去微乳液c中的环己烷,再在14000g下离心15分钟,用无水乙醇洗三次,高纯水洗两次,在水中分散即得到聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒,得到的溶液呈淡黄褐色。为了进一步说明本发明的有益效果,重复上述实验步骤(1)-(4),将所述的步骤(1)-(4)中各药品的浓度和体积分别替换成如表6所示的各药品的浓度和体积,得到聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒。表6实施例13各步骤所用药品的用量注:表6中“\”表示该表格中不需要提供相关信息。按照实施例2的粒径和载药量的测定方法测试步骤(4)所得的聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒的粒径和载药量。实验结果:(1)本发明实施例12、13所制得的聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒的平均粒径分别为21.44、35.23nm。(2)本发明实施例所制得的聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒的载药量分别为0.235、0.344。实施例14-15磷酸-聚乙二醇(peg)修饰的柠檬酸钙-dna纳米颗粒的制备实施例14为重复实施例12的实验步骤(1)-(4),将实施例12的实验步骤(2)中的磷酸氢二钠溶液(ph9.0)替换成柠檬酸钠溶液(ph11.5),获得磷酸-聚乙二醇(peg)修饰的柠檬酸钙-dna纳米颗粒。实施例15为重复实施例13的实验步骤,将实施例13中的磷酸氢二钠溶液(ph9.0)替换成柠檬酸钠溶液(ph11.5),获得磷酸-聚乙二醇(peg)修饰的柠檬酸钙-dna纳米颗粒。按照实施例2的粒径和载药量的测定方法测试实施例14和15所得的聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒的粒径和载药量。实验结果:(1)本发明实施例14和15所制得的聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒 的平均粒径分别为30.40、29.25nm。(2)本发明实施例14和15所制得的聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒的载药量分别为0.307、0.115。实施例16-17磷酸(peg)修饰的碳酸钙-dna纳米颗粒实施例16为重复实施例12的实验步骤(1)-(4),将实施例12的实验步骤(2)中的磷酸氢二钠溶液(ph9.0)替换成碳酸钠溶液(ph11.5),获得磷酸-聚乙二醇(peg)修饰的柠檬酸钙-dna纳米颗粒。实施例17为重复实施例13的实验步骤,将实施例13中的磷酸氢二钠溶液(ph9.0)分别替换成碳酸钠溶液(ph11.5),获得磷酸-聚乙二醇(peg)修饰的柠檬酸钙-dna纳米颗粒。按照实施例2的粒径和载药量的测定方法测试实施例16和17所得的聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒的粒径和载药量。实验结果:(1)本发明实施例所制得的聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒的平均粒径分别为30.12、38.55nm。(2)载药量:本发明实施例所制得的聚乙二醇(peg)-磷酸钙-微环dna纳米颗粒的载药量分别为0.785、0.256。以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本
技术领域:
的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1