药物组合物,其治疗方法及用途与流程
技术领域
本发明涉及包含如下文描述的SGLT2抑制剂和胰岛素的药物组合物,其适用于治疗或预防一种或多种选自I型糖尿病、II型糖尿病、葡萄糖耐量降低(impaired glucose tolerance)、空腹血糖异常(impaired fasting blood glucose)和高血糖症的病症。
此外,本发明涉及在有需要的患者中治疗选自以下的疾病或病症的方法:
-治疗糖尿病;
-治疗糖尿病,其中治疗需要使用胰岛素;
-治疗I型糖尿病;
-治疗、预防低血糖症或降低其风险;
-预防选自糖尿病并发症的病症或障碍、减缓该病症或障碍的进展、延迟或治疗该病症或障碍;
-预防代谢障碍、减缓该代谢障碍的进展、延迟或治疗该代谢障碍;
-改善血糖控制和/或降低空腹血糖、餐后血糖和/或糖基化血红蛋白HbA1c;
-预防、减缓、延迟或逆转葡萄糖耐量降低、空腹血糖异常、胰岛素抵抗和/或代谢综合征进展成II型糖尿病;
-降低体重和/或身体脂肪,或预防或减缓体重和/或身体脂肪增加,或促进体重和/或身体脂肪降低;
-预防、减缓、延迟或治疗由异位脂肪异常蓄积引起的疾病或病症;
-保持和/或改善胰岛素敏感性和/或治疗或预防高胰岛素血症和/或胰岛素抵抗;
-预防移植后新发糖尿病(NODAT)和/或移植后代谢综合征(PTMS)、减缓这些病症进展、延迟或治疗这些病症;
-预防、延迟或减少与NODAT和/或PTMS相关的并发症,包括微血管及大血管疾病及事件、移植排斥、感染和死亡;
-治疗高尿酸血症以及与高尿酸血症相关病症;
-治疗或预防肾结石;
-治疗低钠血症;
-预防、延迟或治疗与囊性纤维化相关的糖尿病或减缓其进展;
其特征在于以组合或交替给药SGLT2抑制剂和胰岛素。
此外,本发明涉及SGLT2抑制剂在制备用于如上下文所述的方法的药物中的用途。
此外,本发明涉及胰岛素在制备用于如上下文所述的方法的药物中的用途。
本发明还涉及根据本发明的药物组合物在如上下文所述的方法中的用途。
本发明还涉及根据本发明的药物组合物在制备用于如上下文所述的方法的药物中的用途。
发明背景
I型糖尿病,也称作胰岛素依赖性糖尿病或青少年糖尿病,是一种源自胰腺中生产胰岛素的β细胞的自身免疫性破坏的糖尿病形式。后续胰岛素缺乏导致血糖浓度增加和尿糖排泄增加。经典症状为多尿、多饮、多食及体重减轻。如果不使用胰岛素治疗,I型糖尿病可为致命的。并发症可与低血糖及高血糖两种状态相关。严重低血糖症可导致需要抢救的痉挛或丧失意识。不控制高血糖症以及胰岛素不足可导致可致命的严重酮酸中毒。高血糖症本身也可短期导致疲劳及视觉障碍且也可导致对器官(例如眼、肾及关节)的长期损害。虽然吸入胰岛素及口服制剂正在临床试验测试中,但皮下注射是最常见的胰岛素给药方式。已研发更易于从注射位点吸收的速效胰岛素类似物,因此比皮下注射的人胰岛素更快起效,旨在在餐后提供高水平(bolus level)的所需胰岛素。其它胰岛素类似物-也称作长效胰岛素(例如甘精胰岛素(insulin glargine)、地特胰岛素(insulin detemir))为可用的,其在一段时间(例如8至24小时)内缓慢释放,旨在提供日间基础胰岛素水平。
II型糖尿病为日益流行的疾病,其因高频率的并发症而导致预期寿命缩短。因为糖尿病相关的微血管并发症,II型糖尿病目前为工业世界中成人发作的目盲、肾衰竭及截肢的最常见起因。此外,II型糖尿病的存在与心血管疾病的风险增加2至5倍有关。
在疾病长期持续之后,大多数II型糖尿病患者的口服疗法最终失效,且变成胰岛素依赖性,必须每天注射胰岛素且每天进行多次葡萄糖测量。
英国前瞻性糖尿病研究(United Kingdom Prospective Diabetes Study,UKPDS)证明用二甲双胍、磺酰脲类或胰岛素强化治疗比常规治疗仅产生有限的血糖控制改善(HbA1c差异为约0.9%)。此外,即使在强化治疗组的患者中,血糖控制还随时间显著恶化,这归因于β细胞功能退化所致。尽管该β细胞功能退化,然而重要的是强化血糖治疗在短期(6年)内与微血管益处相关且在长期(15年)内与大血管益处相关。类似现象也已在I型糖尿病患者中证实,例如在糖尿病控制及并发症试验(DCCT)中,在6.5年的研究期间常规治疗组与强化治疗组之间的中位HbA1c(~1.9%)差异导致了显著的微血管并发症相对风险降低,而在DCCT 11年后关注到大血管益处,例如在EDIC(糖尿病干预及并发症流行病学)研究中所报道,一位患者比另一患者的HbA1c相对降低10%与心血管并发症0.80的风险比相关。尽管有这些令人信服的血糖管理长期效应,许多II型糖尿病或I型糖尿病患者依旧未获充分治疗,部分因为长期效应中的限制,已有抗高血糖疗法的耐受性及给药不便。
疗法(例如一线或二线疗法和/或单一疗法或(初始或追加(add-on))组合疗法)中常用的口服抗糖尿病药物包括但不限于二甲双胍、磺酰脲类、噻唑烷二酮类、列奈类(glinides)及α-葡萄糖苷酶抑制剂。
治疗失败的高发生率可能是II型糖尿病或I型糖尿病患者中高比例的与长期高血糖症相关的并发症或慢性损伤(包括微血管及大血管并发症,例如糖尿病肾病、视网膜病变或神经病变,或心血管并发症)的主要原因。
因此,存在对具有与血糖控制相关、与疾病改善特性相关及与降低心血管发病率及死亡率相关的良好功效同时显示改善的安全性状况的方法、药物及药物组合物的未满足的需要。
SGLT2抑制剂代表一类用于治疗或改善II型糖尿病患者的血糖控制所研发的新药物。吡喃葡萄糖基取代的苯衍生物在现有技术中公开为SGLT2抑制剂,例如公开于WO 01/27128、WO 03/099836、WO 2005/092877、WO 2006/034489、WO 2006/064033、WO 2006/117359、WO 2006/117360、WO 2007/025943、WO 2007/028814、WO 2007/031548、WO 2007/093610、WO 2007/128749、WO 2008/049923、WO 2008/055870、WO 2008/055940中。提出吡喃葡萄糖基取代的苯衍生物作为泌尿系统糖排泄诱导剂及作为治疗糖尿病的药物。
在其它机理中,葡萄糖的肾脏过滤及再吸收有助于稳态血浆葡萄糖浓度,且因此可用作抗糖尿病靶点。穿过肾上皮细胞再吸收过滤的葡萄糖将经位于小管的刷状缘膜(brush-border membrane)中的钠依赖性葡萄糖共转运载体(SGLT)沿钠梯度进行。存在至少三种表达模式以及物理化学特性不同的SGLT亚型。SGLT2仅表达于肾脏中,而SGLT1还表现于如肠、结肠、骨骼及心肌的其他组织中。已发现SGLT3为肠间质细胞中的葡萄糖感应器而不具有任何转运功能。其它相关但尚未表征的基因还可能进一步促进肾脏葡萄糖再吸收。在血糖浓度正常的情形下,葡萄糖完全由肾脏中的SGLT再吸收,而肾脏的再吸收能力在葡萄糖浓度大于10mM时饱和,从而导致糖尿(即“糖尿病”)。此阈浓度可能因SGLT2受抑制而降低。在SGLT抑制剂根皮苷(phlorizin)的实验中已显示,抑制SGLT将部分抑制葡萄糖自肾小球滤液再吸收至血液中,从而导致血糖浓度降低且导致糖尿。
发明目的
本发明的目的在于提供预防代谢障碍(尤其是糖尿病及糖尿病并发症)、减缓该代谢障碍的进展、延迟或治疗该代谢障碍的药物组合物和方法。
本发明的另一目的在于提供治疗I型糖尿病患者的药物组合物和方法。
本发明的另一目的在于在有需要的患者(尤其是I型或II型糖尿病患者)中提供改善血糖控制的药物组合物和方法。
本发明的另一目的在于在患者中提供改善血糖控制的药物组合物和方法。
本发明的另一目的在于提供延长给药至患者的胰岛素的疗效持续时间的药物组合物和方法。
本发明的另一目的在于在患者中提供降低胰岛素所需剂量的药物组合物和方法。
本发明的另一目的在于提供预防、减缓或延迟从葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)、胰岛素抵抗和/或代谢综合征进展成II型糖尿病的药物组合物和方法。
本发明的另一目的在于提供预防选自糖尿病并发症(尤其是I型或II型糖尿病)的病症或障碍、减缓该病症或障碍的进展、延迟或治疗该病症或障碍的药物组合物和方法。
本发明的另一目的在于在有需要的患者中提供降低体重或预防或减缓其体重增加的药物组合物和方法。
本发明的另一目的在于提供高效治疗代谢障碍(尤其是糖尿病、葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)和/或高血糖症)的新药物组合物,其具有良好至极好的药理学和/或药代动力学和/或物理化学特性。
由上文所述及下文的实施例,本领域技术人员将显而易见本发明的其它目的。
发明概述
在本发明范围内,现已令人惊奇地发现SGLT2抑制剂和胰岛素的组合比单独使用胰岛素或SGLT2抑制剂治疗产生更多的血糖降低。因此为实现特定水平的基线血糖,通过使用SGLT2抑制剂和胰岛素的组合可减少胰岛素的剂量。此外已令人惊奇地发现在给予胰岛素一段时间期限后,给予SGLT2抑制剂比单独给予胰岛素延长了血糖降低的时间。
因此SGLT2抑制剂和胰岛素的组合可有利地用于预防患者的代谢障碍、减缓该代谢障碍进展、延迟或治疗该代谢障碍,尤其改善患者的血糖控制。此开辟了治疗及预防I型糖尿病、II型糖尿病、糖尿病并发症及相近疾病状态的新的治疗可能。
因此,在第一方面中,本发明提供药物组合物,其包含
(a)SGLT2抑制剂,以及
(b)胰岛素。
根据本发明的另一方面,提供一种在患者中治疗糖尿病的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的另一方面,提供一种在需要使用胰岛素治疗的患者中治疗糖尿病的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的另一方面,提供一种在患者中治疗I型糖尿病的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的另一方面,提供一种在患者中治疗、预防低血糖症或降低其风险的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的另一方面,提供一种在有需要的患者中预防选自以下的病症或障碍、减缓该病症或障碍的进展、延迟或治疗该病症或障碍的方法:糖尿病并发症,例如白内障和微血管及大血管疾病,例如肾病变、视网膜病变、组织缺血、糖尿病足、动脉硬化、心肌梗塞、急性冠状动脉综合征、不稳定型心绞痛、稳定型心绞痛、中风、外周动脉阻塞性疾病、心肌病、心力衰竭、心律失常及血管再狭窄,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。尤其可治疗糖尿病性肾病的一个或多个方面(例如过度灌注、蛋白尿及白蛋白尿)、减缓其进展,或延迟或预防其发作。术语“组织缺血”尤其包括糖尿病性大血管病变、糖尿病性微血管病变、伤口愈合受损及糖尿病性溃疡。术语“微血管及大血管疾病”及“微血管及大血管并发症”在本申请中可互换使用。
根据本发明的另一方面,提供一种在有需要的患者中预防选自以下的代谢障碍、减缓该代谢障碍进展、延迟或治疗该代谢障碍的方法:II型糖尿病、葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)、高血糖症、餐后高血糖症、超重、肥胖症、代谢综合征、妊娠糖尿病和与囊性纤维化相关的糖尿病,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的另一方面,提供一种在有需要的患者中改善血糖控制和/或降低空腹血糖、餐后血糖和/或糖基化血红蛋白HbAlc的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的药物组合物对于与葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)、胰岛素抵抗和/或代谢综合征相关的疾病或病症还可具有有价值的疾病改善特性。
根据本发明的另一方面,提供一种在有需要的患者中预防、减缓、延迟或逆转葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)、胰岛素抵抗和/或代谢综合征进展成II型糖尿病的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
通过使用根据本发明的药物组合物,可在有需要的患者中改善血糖控制,还可治疗与血糖水平增加有关或由该增加引起的那些病症和/或疾病。
通过给药根据本发明的药物组合物且由于SGLT2抑制剂的活性,过量水平的血糖不会转化成不溶的储存形式(如脂肪),而是经患者的尿排泄。在使用SGLT2抑制剂的动物模型中,可见脂肪减少占所观察到的体重降低的大部分,而未观察到身体水份或蛋白质含量的显著变化。因此,结果为体重不增加、少增加或甚至体重降低。
根据本发明的另一方面,提供一种在有需要的患者中降低体重和/或身体脂肪,或预防或减缓体重和/或身体脂肪增加,或促进体重和/或身体脂肪降低的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
通过给药根据本发明的组合或药物组合物,可降低或抑制异位脂肪(尤其肝脏的异位脂肪)的异常蓄积。因此,根据本发明的另一方面,提供一种在有需要的患者中预防、减缓、延迟或治疗由异位脂肪(尤其肝脏的异位脂肪)的异常蓄积引起的疾病或病症的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。由肝脏脂肪异常蓄积引起的疾病或病症尤其选自:普通脂肪肝(general fatty liver)、非酒精性脂肪肝(NAFL)、非酒精性脂肪性肝炎(non-alcoholic steatohepatitis,NASH)、营养过度诱发的脂肪肝、糖尿病性脂肪肝、酒精诱发的脂肪肝或中毒性脂肪肝。
由此,本发明的另一方面提供一种在有需要的患者中保持和/或改善胰岛素敏感性和/或治疗或预防高胰岛素血症和/或胰岛素抵抗的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的另一方面,提供一种在有需要的患者中预防移植后新发糖尿病(NODAT)和/或移植后代谢综合征(PTMS)、减缓这些病症进展、延迟或治疗这些病症的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的另一方面,提供一种在有需要的患者中预防、延迟或减少与NODAT和/或PTMS相关的并发症(包括微血管及大血管疾病及事件、移植排斥、感染和死亡)的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的另一方面,提供一种在有需要的患者中预防、延迟或治疗与囊性纤维化相关的糖尿病,或减缓其进展的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的药物组合物能够促进患者血清总尿酸盐含量的降低。因此,根据本发明的另一方面,提供一种在有需要的患者中治疗高尿酸血症及高尿酸血症相关病症(例如痛风、高血压和肾衰竭)的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
给予药物组合物增加葡萄糖的尿排泄。该渗透排泄及水排出的增加及尿酸盐含量的降低对肾结石的治疗或预防是有益的。因此,在本发明的另一方面,提供一种在有需要的患者中治疗或预防肾结石的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的另一方面,提供一种在有需要的患者中治疗的低钠血症、水潴留(water retention)及水中毒(water intoxication)的方法,该方法的特征在于SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。通过给予根据本发明的药物组合物,有可能通过对肾脏起作用逆转水潴留及与这些疾病及病症相关的电解质不平衡,来逆转低钠血症、水潴留及水中毒。
根据本发明的另一方面,提供SGLT2抑制剂在制备用于在有需要的患者中实现以下目的的药物中的用途:
-治疗糖尿病;
-治疗糖尿病,其中治疗需要使用胰岛素;
-治疗I型糖尿病;
-治疗、预防低血糖症或降低其风险;
-预防选自糖尿病并发症的病症或障碍、减缓该病症或障碍的进展、延迟或治疗该病症或障碍;
-预防选自以下的代谢障碍、减缓该代谢障碍的进展、延迟或治疗该代谢障碍:I型糖尿病、II型糖尿病、葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)、高血糖症、餐后高血糖症、超重、肥胖症、代谢综合征和妊娠糖尿病;或
-改善血糖控制和/或降低空腹血糖、餐后血糖和/或糖基化血红蛋白HbA1c;或
-预防、减缓、延迟或逆转葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)、胰岛素抵抗和/或代谢综合征进展成II型糖尿病;或
-预防选自以下的病症或障碍、减缓该病症或障碍进展、延迟或治疗该病症或障碍:糖尿病并发症,例如白内障和微血管及大血管疾病,例如肾病变、视网膜病变、组织缺血、动脉硬化、心肌梗塞、中风及外周动脉阻塞性疾病;或
-降低体重和/或身体脂肪或者预防或减缓体重和/或身体脂肪增加或者促进体重和/或身体脂肪降低;或
-预防、减缓、延迟或治疗由异位脂肪异常蓄积引起的疾病或病症;或
-保持和/或改善胰岛素敏感性和/或治疗或预防高胰岛素血症和/或胰岛素抵抗;
-预防、延迟或治疗移植后新发糖尿病(NODAT)和/或移植后代谢综合征(PTMS)或减缓其进展;
-预防、延迟或降低与NODAT和/或PTMS相关的并发症,包括微血管及大血管疾病及事件、移植排斥、感染和死亡;
-治疗与囊性纤维化相关的糖尿病;
-治疗高尿酸血症以及与高尿酸血症相关的病症;
-治疗或预防肾结石;
-治疗低钠血症;
其特征在于SGLT2抑制剂与胰岛素例如以组合或交替给予。
根据本发明的另一方面,提供胰岛素在制备用于在有需要的患者中实现以下目的的药物中的用途:
-治疗糖尿病;
-治疗糖尿病,其中治疗需要使用胰岛素;
-治疗I型糖尿病;
-治疗、预防低血糖症或降低其风险;
-预防选自糖尿病并发症的病症或障碍、减缓该病症或障碍的进展、延迟或治疗该病症或障碍;
-预防选自以下的代谢障碍、减缓该代谢障碍的进展、延迟或治疗该代谢障碍:I型糖尿病、II型糖尿病、葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)、高血糖症、餐后高血糖症、超重、肥胖症、代谢综合征和妊娠糖尿病;或
-改善血糖控制和/或降低空腹血糖、餐后血糖和/或糖基化血红蛋白HbA1c;或
-预防、减缓、延迟或逆转葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)、胰岛素抵抗和/或代谢综合征进展成II型糖尿病;或
-预防选自以下的病症或障碍、减缓该病症或障碍进展、延迟或治疗该病症或障碍:糖尿病并发症,例如白内障和微血管及大血管疾病,例如肾病变、视网膜病变、组织缺血、动脉硬化、心肌梗塞、中风及外周动脉阻塞性疾病;或
-降低体重和/或身体脂肪或者预防或减缓体重和/或身体脂肪增加或者促进体重和/或身体脂肪降低;或
-预防、减缓、延迟或治疗由异位脂肪异常蓄积引起的疾病或病症;或
-保持和/或改善胰岛素敏感性和/或治疗或预防高胰岛素血症和/或胰岛素抵抗;
-预防、延迟或治疗移植后新发糖尿病(NODAT)和/或移植后代谢综合征(PTMS)或减缓其进展;
-预防、延迟或降低与NODAT和/或PTMS相关的并发症,包括微血管及大血管疾病及事件、移植排斥、感染和死亡;
-治疗与囊性纤维化相关的糖尿病;
-治疗高尿酸血症以及与高尿酸血症相关的病症;
-治疗或预防肾结石;
-治疗低钠血症;
其特征在于SGLT2抑制剂与胰岛素例如以组合或交替给予。
根据本发明的另一方面,提供根据本发明的药物组合物在制备用于上下文所述的治疗性及预防性方法的药物中的用途。
定义
本发明的药物组合物的术语“活性成份”是指本发明的SGLT2抑制剂和/或长效胰岛素。
人类患者的术语“体重指数”或“BMI”定义为以千克计的体重除以以米计的身高的平方,如此BMI的单位为kg/m2。
术语“超重”定义为个体的BMI大于25kg/m2且小于30kg/m2的病症。术语“超重”及“肥胖症前期”可互换使用。
术语“肥胖症”定义为个体的BMI等于或大于30kg/m2的病症。根据WHO定义,术语肥胖症可如下分类:术语“I级肥胖症”为BMI等于或大于30kg/m2但小于35kg/m2的病症;术语“II级肥胖症”为BMI等于或大于35kg/m2但小于40kg/m2的病症;术语“III级肥胖症”为BMI等于或大于40kg/m2的病症。
术语“内脏肥胖症”定义为测量到男性腰臀比大于或等于1.0且女性腰臀比大于或等于0.8的病症。其定义胰岛素抵抗及前期糖尿病发展的风险。
术语“腹部肥胖症”一般定义为男性腰围>40英寸或102cm和女性腰围>35英寸或94cm的病症。就日本种族(Japanese ethnicity)或日本患者而言,腹部肥胖症可定义为男性腰围≥85cm且女性腰围≥90cm(例如参见日本代谢综合征诊断调查委员会(investig a ting committee for the diagnosis of metabolic syndrome in Japan))。
术语“血糖正常”定义为个体空腹血糖浓度在正常范围,即大于70mg/dL(3.89mmol/L)且小于100mg/dL(5.6mmol/L)的情况。“空腹”一词具有医学术语的一般含义。
术语“高血糖症”定义为个体空腹血糖浓度高于正常范围,即大于100mg/dL(5.6mmol/L)的病症。“空腹”一词具有医学术语的一般含义。
术语“低血糖症”定义为个体血糖浓度低于正常范围,尤其小于70mg/dL(3.89mmol/L)或甚至低于60mg/dl的病症。
术语“餐后高血糖症”定义为个体餐后2小时血糖或血清葡萄糖浓度大于200mg/dL(11.1mmol/L)的病症。
术语“空腹血糖异常”或“IFG”定义为个体空腹血糖浓度或空腹血清葡萄糖浓度在100至125mg/dl(即5.6至6.9mmol/l)范围内,尤其大于110mg/dL且小于126mg/dl(7.00mmol/L)的病症。“正常空腹葡萄糖”个体的空腹葡萄糖浓度小于100mg/dl,即小于5.6mmol/l。
术语“葡萄糖耐量降低”或“IGT”定义为个体餐后2小时血糖或血清葡萄糖浓度大于140mg/dl(7.8mmol/L)且小于200mg/dL(11.11mmol/L)的病症。异常的葡萄糖耐量(即餐后2小时血糖或血清葡萄糖浓度)可以以空腹后摄取75g葡萄糖之后2小时,每分升血浆的葡萄糖毫克数的血糖含量来量度。“正常葡萄糖耐受性”个体的餐后2小时血糖或血清葡萄糖浓度小于140mg/dl(7.8mmol/L)。
术语“高胰岛素血症”定义为具有胰岛素抵抗且血糖正常或血糖不正常个体的空腹或餐后血清或血浆胰岛素浓度高于无胰岛素抵抗且腰臀比<1.0(男性)或<0.8(女性)的正常瘦个体的病症。
术语“胰岛素敏感”、“胰岛素抵抗改善”或“胰岛素抵抗降低”同义且可互换使用。
术语“胰岛素抵抗”定义为其中需要循环胰岛素含量超过对葡萄糖刺激的正常反应以保持正常血糖状态的状态(Ford ES等人,JAMA.(2002)287:356-9)。测定胰岛素抵抗的方法为正常血糖-高胰岛素血症性钳夹试验(euglycaemic-hyperinsulinaemic clamp test)。在组合胰岛素-葡萄糖输注技术范围内测定胰岛素与葡萄糖的比率。若葡萄糖吸收低于所研究背景群体的25%,则认为具有胰岛素抵抗(WHO定义)。比钳夹试验简易得多的是所谓的迷你模型(minimal model),其中在静脉内葡萄糖耐量试验期间,在固定时间间隔下测量血液中的胰岛素及葡萄糖浓度,且由此计算胰岛素抵抗。以此方法不可能区别肝胰岛素抵抗与外周胰岛素抵抗。
此外,可通过评定“胰岛素抵抗的稳态模型评定(HOMA-IR)”得分(胰岛素抵抗的可靠指示)来定量胰岛素抵抗(即具胰岛素抵抗患者对疗法的反应)、胰岛素敏感性及高胰岛素血症(KatsukIA等人,Diabetes Care 2001;24:362-5)。还参考了测定胰岛素敏感性的HOMA指数的方法(Matthews等人,Diabetologia 1985,28:412-19)、测定完整胰岛素原与胰岛素的比率的方法(Forst等人,Diabetes 2003,52(增刊1):A459)及正常血糖钳夹研究。此外,可以胰岛素敏感性的可能替代来监测血浆脂连蛋白(adiponectin)含量。用下式计算稳态评定模型(HOMA)-IR得分对胰岛素抵抗的估算(Galvin P等人,Diabet Med 1992;9:921-8):
HOMA-IR=[空腹血清胰岛素(μU/mL)]×[空腹血糖(mmol/L)/22.5]
通常,在每天临床实践中使用其它参数评定胰岛素抵抗。优选地,使用例如患者的甘油三酯浓度,因为甘油三酯含量的增加与胰岛素抵抗的存在具显著相关性。
具发展IGT或IFG或II型糖尿病倾向的患者为那些具有高胰岛素血症且定义为胰岛素抵抗的血糖正常者。具有胰岛素抵抗的典型患者一般超重或肥胖症,但其并非总是如此。若可检测到胰岛素抵抗,则此为出现前期糖尿病的强力指示。因此,为了保持葡萄糖稳态,该个体可能需要健康个体2-3倍的胰岛素,否则将导致任何临床症状。
研究胰腺β细胞功能的方法与上文关于胰岛素敏感性、高胰岛素血症或胰岛素抵抗的方法类似:可例如通过测定β细胞功能的HOMA指数(Matthews等人,Diabetologia 1985,28:412-19)、完整胰岛素原与胰岛素的比率(Forst等人,Diabetes 2003,52(增刊1):A459)、口服葡萄糖耐量试验或膳食耐量试验后胰岛素/C-肽分泌,或通过使用高血糖症钳夹研究和/或在频繁取样的静脉内葡萄糖耐量试验后建立迷你模型(Stumvoll等人,Eur J Clin Invest 2001,31:380-81)来测量β细胞功能的改善。
术语“前期糖尿病”为个体倾向于发展II型糖尿病的病症。前期糖尿病扩展了葡萄糖耐量降低的定义,使其包括具有空腹血糖在高正常范围(≥100mg/dL)内(J.B.Meigs等人,Diabetes 2003;52:1475-1484)且具有空腹高胰岛素血症(高血浆胰岛素浓度)的个体。美国糖尿病协会(American Diabetes Association)及美国国立糖尿病和消化与肾病研究所(National Institute of Diabetes and Digestive and Kidney Diseases)在共同发布的题为“The Prevention or Delay of Type 2 Diabetes”的状况报告中阐述鉴别前期糖尿病为严重威胁健康的科学及医学基础(Diabetes Care 2002;25:742-749)。
可能具有胰岛素抵抗的个体为具有两种或多种以下特征的个体:1)超重或肥胖症、2)高血压、3)高脂血症、4)一个或多个一级亲属诊断患有IGT或IFG或II型糖尿病。可通过计算HOMA-IR得分确定这些个体的胰岛素抵抗。出于本发明的目的,胰岛素抵抗定义为个体的HOMA-IR得分>4.0或HOMA-IR得分高于实验室进行葡萄糖及胰岛素分析所定义的正常上限的临床病症。
术语“I型糖尿病”定义为受试者在存在对胰腺β细胞或胰岛素的自身免疫的情况下,空腹血糖或血清葡萄糖浓度大于125mg/dL(6.94mmol/L)的病症。若进行葡萄糖耐量试验,在存在对胰腺β细胞或胰岛素的自身免疫的情况下,糖尿病患者的血糖水平将超过空腹时摄取75g葡萄糖后2小时每分升血浆200mg葡萄糖(11.1mmol/l)。在葡萄糖耐量试验中,在空腹10-12小时后向待测患者口服给予75g葡萄糖,且在即将摄取葡萄糖之前及摄取葡萄糖之后1小时及2小时记录血糖水平。观测对胰腺β细胞的自身免疫的存在,可通过检测循环胰岛细胞自身抗体[“1A型糖尿病”],即以下至少一种:GAD65[谷氨酸脱羧酶-65]、ICA[胰岛细胞细胞质]、IA-2[酪氨酸磷酸酶样蛋白IA-2的胞质内区域]、ZnT8[锌-转运体-8]或胰岛素抗体;或在不存在典型的循环自身抗体情况下的其它自身免疫信号[1B型糖尿病],即如通过胰腺活检或成像检测。通常,存在(但不总是)遗传倾向(例如HLA、INS VNTR及PTPN22)。
术语“II型糖尿病”定义为个体空腹血糖或血清葡萄糖浓度大于125mg/dL(6.94mmol/L)的病症。血糖值的测量为常规医学分析中的标准操作。若进行葡萄糖耐量试验,则糖尿病患者的血糖含量将超过空腹时摄取75g葡萄糖后2小时每分升血浆200mg葡萄糖(11.1mmol/l)。在葡萄糖耐量试验中,在空腹10-12小时后向待测患者口服给予75g葡萄糖,且在即将摄取葡萄糖之前及摄取葡萄糖之后1小时及2小时记录血糖含量。在健康个体中,摄取葡萄糖之前的血糖含量将为每分升血浆60mg至110mg,摄取葡萄糖后1小时,将小于200mg/dL,且摄取后2小时,将小于140mg/dL。若摄取后2小时,值为140mg至200mg,则此被视为异常葡萄糖耐量。
术语“晚期II型糖尿病”包括继发性药物失效、具胰岛素疗法适应症且进展成微血管及大血管并发症(例如糖尿病性肾病或冠心病(CHD)的患者。
术语“HbA1c”是指血红蛋白B链非酶促糖基化的产物。本领域技术人员熟知其测定。在监测糖尿病的治疗时,HbA1c值尤其重要。因为HbA1c的产生基本上取决于血糖含量及红细胞的寿命,所以HbA1c在“血糖记忆”意义上反映前4-6周的平均血糖含量。HbA1c值由糖尿病强化治疗始终良好调节(即小于样品的总血红蛋白的6.5%)的糖尿病患者显著更好地受保护而避免糖尿病性微血管病变。例如,二甲双胍本身对糖尿病患者的HbA1c值达到的平均改善为约1.0-1.5%。在所有糖尿病患者中,此HbA1c值降低不足以达到HbA1c<6.5%且优选<6%的所需目标范围。
在本发明范围中,术语“不充分的血糖控制”或“不足的血糖控制”是指患者显示HbA1c值高于6.5%、尤其高于7.0%、甚至更高于7.5%、尤其高于8%的情况。
“代谢综合征”,还称为“X综合征”(在代谢障碍情况下使用),还称为“代谢不良综合征”,其主要特征为胰岛素抵抗的综合征(Laaksonen DE等人,Am J Epidemiol 2002;156:1070-7)。根据ATP III/NCEP指导方针(Executive Summary of the Third Report of the National Cholesterol Education Program(NCEP)Expert Panel on Detection,Evaluation,and Treatment of High Blood Cholesterol in Adults(Adult Treatment Panel III)JAMA:Journal of the American Medical Association(2001)285:2486-2497),当存在三个或多个以下风险因素时,诊断为代谢综合征:
1.腹部肥胖症,其定义为男性腰围>40英寸或102cm,和女性腰围>35英寸或94cm;或就日本种族或日本患者而言,定义为男性腰围≥85cm且女性腰围≥90cm;
2.甘油三酯:≥150mg/dL
3.男性HDL-胆固醇<40mg/dL
4.血压≥130/85mm Hg(SBP≥130或DBP≥85)
5.空腹血糖≥100mg/dL
已验证NCEP定义(Laaksonen DE等人,Am J Epidemiol.(2002)156:1070-7)。还可由医学分析中及例如Thomas L(编):“Labor und Diagnose”,TH-Books Verlagsgesellschaft mbH,Frankfurt/Main,2000中描述的标准方法测定血液中的甘油三酯及HDL胆固醇。
根据常用定义,若收缩压(SBP)超过140mm Hg且舒张压(DBP)超过90mm Hg,则诊断为高血压。若患者患有显性糖尿病(manifest diabetes),则目前推荐收缩压降至低于130mm Hg且舒张压降至低于80mm Hg的程度。
NODAT(移植后新发糖尿病)及PTMS(移植后代谢综合征)的定义密切遵循美国糖尿病协会(American Diabetes Association)关于II型糖尿病诊断标准的定义及国际糖尿病联合会(International Diabetes Federation,IDF)及美国心脏协会/美国国家心脏、肺及血液研究所(American Heart Association/National Heart,Lung,and Blood Institute)关于代谢综合征的定义。NODAT和/或PTMS与微血管及大血管疾病及事件、移植排斥、感染及死亡的风险增加有关。已鉴别多种与NODAT和/或PTMS相关的潜在风险因子的预测因子,包括移植时较高的年龄、男性性别、移植前体重指数、移植前糖尿病及免疫抑制。
术语“妊娠期糖尿病”(怀孕期糖尿病)表示怀孕期间发展且一般在生产后又立即停止的糖尿病形式。由在怀孕第24周至第28周进行的筛选测试诊断妊娠期糖尿病。其一般为简单测试,其中在给予50g葡萄糖溶液之后1小时,测量血糖含量。若此1小时含量高于140mg/dl,则疑患妊娠期糖尿病。可由标准葡萄糖耐量试验(例如使用75g葡萄糖)最终确认。
术语“高尿酸血症”表示高血清总尿酸盐含量的病症。在人类血液中,美国医学会(American Medical Association)认为3.6mg/dL(约214μmol/L)至8.3mg/dL(约494μmol/L)的尿酸浓度为正常。高血清总尿酸盐含量或高尿酸血症通常与多种疾病有关。例如,高血清总尿酸盐含量可在关节中产生一类称为痛风的关节炎。痛风为由血流中的高浓度总尿酸盐含量引起的在关节的关节软骨、腱及周围组织上形成尿酸单钠或尿酸晶体所产生的病症。在这些组织上形成尿酸盐或尿酸激发这些组织的炎症反应。当尿酸或尿酸盐在肾脏中结晶时,尿液中饱和含量的尿酸可导致形成肾结石。此外,高血清总尿酸盐含量通常与所谓的代谢综合征(包括心血管疾病及高血压)相关。
术语“低钠血症”表示缺乏钠或不缺乏钠的水正平衡的病症,当血浆钠降至135mml/L含量以下时,视为低钠血症。低钠血症为可在过度消耗水的个体中独立出现的病症;然而,低钠血症更通常为导致水排泄减少的药物治疗并发症或其它基础医学病症的并发症。低钠血症可导致因过量水潴留而发生的水中毒,当胞外液体的正常张力(tonicity)降至安全限度以下时发生。水中毒为大脑功能的潜在致命干扰。水中毒的典型症状包括恶心、呕吐、头痛及不适。
本发明范围内的术语“SGLT2抑制剂”是指对钠-葡萄糖转运载体2(SGLT2),尤其人类SGLT2显示抑制作用的化合物,尤其指吡喃葡萄糖基衍生物,即具有吡喃葡萄糖基部分的化合物。以IC50量度的对hSGLT2的抑制作用优选低于1000nM,甚至更优选低于100nM,最优选低于50nM。SGLT2抑制剂的IC50值一般大于0.01nM,或甚至等于或大于0.1nM。可由文献中已知的方法测定对hSGLT2的抑制作用,尤其如申请WO 2005/092877或WO 2007/093610(第23/24页)(将其全文引入本文作为参考)中所述的方法。术语“SGLT2抑制剂”还包含任何其药学上可接受的盐、其水合物及溶剂合物,包括各别结晶形式。
本发明范围内的术语“胰岛素”涉及用于患者(尤其人患者)治疗中的胰岛素及胰岛素类似物,其包括普通胰岛素、人胰岛素、胰岛素衍生物、锌胰岛素及胰岛素类似物,包括其具有改良释放性质的制剂,尤其如用于人治疗的那些。本发明范围内的术语“胰岛素”涵盖以下胰岛素类型:
-速效胰岛素,
-短效胰岛素,
-中效胰岛素,
-长效胰岛素,
及其混合物,例如短效或速效胰岛素与长效胰岛素的混合物。本发明范围内的术语“胰岛素”涵盖通过注射、输注(含泵)、吸入、口服、透皮或其它给药途径给予患者的胰岛素。
术语“治疗”包含治疗性处理已出现该病症(尤其显性形式)的患者。治疗性处理可为减轻具体适应症的症状的症状治疗,或逆转或部分逆转适应症的状况或停止或减缓疾病进展的病因处理。因此,本发明组合物及方法可用作例如一段时间的治疗性处理以及长期疗法。
术语“预防性处理”及“预防”可互换使用,且包含处理处于发展上文所述病症的风险中的患者,从而降低该风险。
附图说明
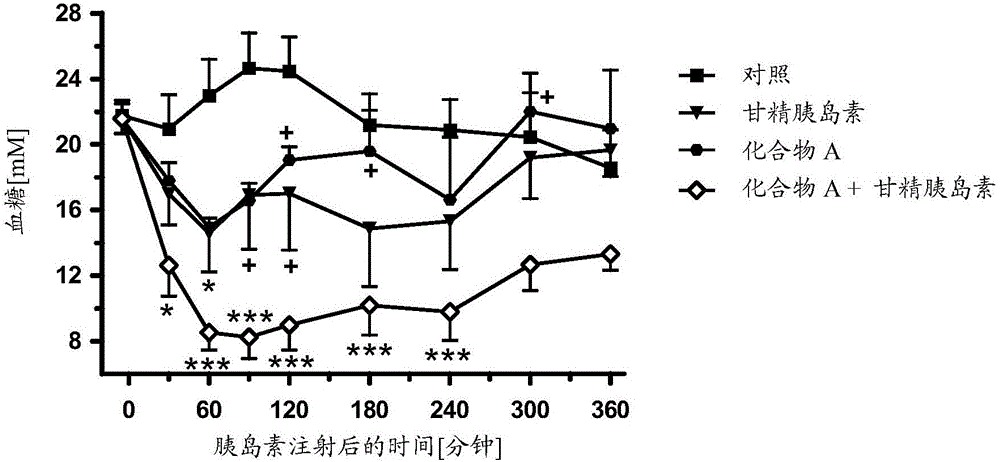
图1显示给药SGLT2抑制剂、甘精胰岛素及其组合后大鼠中的血糖曲线。
图2显示给药低剂量甘精胰岛素、高剂量甘精胰岛素以及SGLT2抑制剂与低剂量甘精胰岛素的组合后大鼠中的血糖曲线。
图3显示给药甘精胰岛素以及120分钟后共同给药SGLT2抑制剂后大鼠中的血糖曲线。
图4显示植入胰岛素释放棒(insulin-releasing sticks)以及单独给予SGLT2抑制剂以及加上植入物后对身体脂肪比例的影响。
发明详述
根据本发明的方面,尤其药物组合物、方法及用途,涉及SGLT2抑制剂和胰岛素。在根据本发明的方法及用途中,任选给予第三种抗糖尿病药,即SGLT2抑制剂和胰岛素组合或不组合第三种抗糖尿病药给予。
SGLT2抑制剂优选选自以下的G1组:达格列净(dapagliflozin)、坎格列净(canagliflozin)、阿格列净(atigliflozin)、艾普格列净(ipragliflozin)、托格列净(tofogliflozin)、瑞格列净(remogliflozin)、舍格列净(sergliflozin)及式(I)的吡喃葡萄糖基取代的苯衍生物
其中R1表示Cl、甲基或氰基,R2表示H、甲基、甲氧基或羟基且R3表示乙基、环丙基、乙炔基、乙氧基、(R)-四氢呋喃-3-基氧基或(S)-四氢呋喃-3-基氧基;或上述一种SGLT2抑制剂的前药。
式(I)化合物及其合成方法公开于例如以下专利申请中:WO 2005/092877、WO 2006/117360、WO 2006/117359、WO 2006/120208、WO 2006/064033、WO 2007/031548、WO 2007/093610、WO 2008/020011、WO 2008/055870。
在上文式(I)的吡喃葡萄糖基取代的苯衍生物中,优选以下的取代基定义。
R1优选表示氯或氰基,尤其氯。
R2优选表示H。
R3优选表示乙基、环丙基、乙炔基、(R)-四氢呋喃-3-基氧基或(S)-四氢呋喃-3-基氧基。R3甚至更优选表示环丙基、乙炔基、(R)-四氢呋喃-3-基氧基或(S)-四氢呋喃-3-基氧基。R3最优选表示乙炔基、(R)-四氢呋喃-3-基氧基或(S)-四氢呋喃-3-基氧基。
优选的式(I)的吡喃葡萄糖基取代的苯衍生物选自化合物(I.1)至(I.11):
根据本发明的一个实施方式,SGLT2抑制剂选自上述式(I)化合物所构成的G1a组。式(I)的吡喃葡萄糖基取代的苯衍生物所构成的G1a组甚至更优选选自化合物(I.6)、(I.7)、(I.8)、(I.9)及(I.11)。G1a组的SGLT2抑制剂的一个优选实例为化合物(I.9)。
根据本发明的另一实施方式,SGLT2抑制剂选自达格列净、坎格列净、阿格列净、艾普格列净及托格列净。
根据本发明,应当理解,上文所列的SGLT2抑制剂(包括式(I)的吡喃葡萄糖基取代的苯衍生物)的定义还包含其水合物、溶剂合物及其多晶型,及其前药。关于优选化合物(I.7),有利的结晶形式公开于国际专利申请WO 2007/028814中,将其全文引入本文作为参考。关于优选化合物(I.8),有利的结晶形式公开于国际专利申请WO 2006/117360中,将其全文引入本文作为参考。关于优选化合物(I.9),有利的结晶形式公开于国际专利申请WO 2006/117359中,将其全文引入本文作为参考。关于优选化合物(I.11),有利的结晶形式公开于国际专利申请WO 2008/049923中,将其全文引入本文作为参考。这些结晶形式具有良好的溶解度特性,其赋予SGLT2抑制剂良好的生物利用度。此外,结晶形式为物理化学稳定的,且因此提供药物组合物良好的存放期稳定性。
如本文所用的术语“达格列净”是指达格列净,包括其水合物及溶剂合物,及其结晶形式。化合物及其合成方法公开于例如WO 03/099836中。优选水合物、溶剂合物及结晶形式公开于例如专利申请WO 2008/116179及WO 2008/002824中。
如本文所用的术语“坎格列净”是指坎格列净,包括其水合物及溶剂合物,及其结晶形式,且具有以下结构:
化合物及其合成方法公开于例如WO 2005/012326及WO 2009/035969中。优选水合物、溶剂合物及结晶形式公开于例如专利申请WO 2008/069327中。
如本文所用的术语“阿格列净”是指阿格列净,包括其水合物及溶剂合物,及其结晶形式,且具有以下结构:
化合物及其合成方法公开于例如WO 2004/007517中。
如本文所用的术语“艾普格列净”是指艾普格列净,包括其水合物及溶剂合物,及其结晶形式,且具有以下结构:
化合物及其合成方法公开于例如WO 2004/080990、WO 2005/012326及WO 2007/114475中。
如本文所用的术语“托格列净”是指托格列净,包括其水合物及溶剂合物,及其结晶形式,且具有以下结构:
化合物及其合成方法公开于例如WO 2007/140191及WO 2008/013280中。
如本文所用的术语“瑞格列净”是指瑞格列净及瑞格列净前药(尤其依碳酸瑞格列净(remogliflozin etabonate)),包括其水合物及溶剂合物,及其结晶形式。其合成方法公开于例如专利申请EP 1213296及EP 1354888中。
如本文所用的术语“舍格列净”是指舍格列净及舍格列净前药(尤其依碳酸舍格列净),包括其水合物及溶剂合物,及其结晶形式。其制备方法公开于例如专利申请EP 1344780及EP 1489089中。
为避免任何疑问,上文引用的与特定SGLT2抑制剂相关的前述各文献的公开内容以其全文引入本文作为参考。
根据本发明的方面,尤其药物组合物、方法及用途,涉及胰岛素,其包括普通胰岛素、人胰岛素、胰岛素衍生物、锌胰岛素(zinc insulin)及胰岛素类似物,包括具有改良释放性质的制剂。尤其如用于人治疗的那些。胰岛素可选自:
-速效胰岛素,
-短效胰岛素,
-中效胰岛素,
-长效胰岛素,
及其混合物。
胰岛素混合物可包括短效或速效胰岛素与长效胰岛素的混合物。例如以Actraphane/Mixtard或Novomix销售的胰岛素混合物。
本发明范围内的术语“胰岛素”涵盖如上下文所述的胰岛素,其通过注射(优选皮下注射)、输注(含泵)、吸入或其它给药途径给予至患者。通过吸入给药的胰岛素例如为Exubera(Pfizer)、AIR(Lilly)及AER(Novo Nordisk)。
速效胰岛素通常在约5至15分钟内开始降低血糖且有效约3至4小时。速效胰岛素的实例为门冬胰岛素(insulin aspart)、赖脯胰岛素(insulin lispro)及谷赖胰岛素(insulin glulisine)。赖脯胰岛素以商品名Humalog及Liprolog销售。门冬胰岛素以商品名NovoLog及NovoRapid销售。谷赖胰岛素以商品名Apidra销售。
短效胰岛素通常在约30分钟内开始降低血糖且有效约5至8小时。一个实例为普通胰岛素或人胰岛素。
中效胰岛素通常在约1至3小时内开始降低血糖且有效约16至24小时。一个实例为NPH胰岛素,也称为Humulin N、Novolin N、Novolin NPH及低精蛋白胰岛素(isophane insulin)。另一实例为慢胰岛素(lente insulin),例如Semilente或Monotard。
长效胰岛素通常在1至6小时内开始降低血糖且有效长达约24小时或甚至长达或超过32小时。长效胰岛素通常提供连续的胰岛素活性水平(长达24至36小时)且通常在约8至12小时、有时更长时间之后以最大强度(平坦作用性质)起作用。长效胰岛素通常在早晨或就寝之前给药。长效胰岛素的实例可包括但不限于作为胰岛素类似物的甘精胰岛素、地特胰岛素或德谷胰岛素(insulin degludec),以及作为配方用于缓慢吸收的常规人胰岛素的特慢胰岛素(ultralente insulin)。长效胰岛素适于提供与饮食胰岛素要求不同的基础胰岛素要求(例如控制高血糖症)。长效胰岛素通常可每天两次或一次、每周三次以上至每周一次(超长效胰岛素)范围内给药。甘精胰岛素例如以商品名Lantus销售。地特胰岛素例如以商品名Levemir销售。
在一个实施方式中,本发明的长效胰岛素是指本领域中已知的任何用于基础胰岛素疗法且具有基础释放性质的胰岛素。基础释放性质是指胰岛素自制剂释放至患者全身循环的动力学、量及速率。在患者平均血浆胰岛素含量对比时间的图中,基础释放性质通常具有最小峰(通常称为“无峰性质”或“平坦性质”),且长期缓慢连续地释放胰岛素。
在另一实施方式中,长效胰岛素为人胰岛素的酰化衍生物。酰化的胰岛素衍生物可为其中亲脂性基团连接至B29位的赖氨酸残基的胰岛素衍生物。市售产品为其包含LysB29(Nε-十四酰基)去(B30)人胰岛素(地特胰岛素)。另一实例为NεB29-(Nα-(ω-羧基十五酰基)-L-γ-谷氨酰基)去(B30)人胰岛素(德谷胰岛素)。
在另一实施方式中,长效胰岛素为包含连接至B链的C末端的带正电荷的氨基酸(例如Arg)的胰岛素。市售产品为(甘精胰岛素),其包含GlyA21、ArgB31、ArgB32人胰岛素。
根据本发明的一个实施方式,胰岛素选自长效胰岛素。
根据另一实施方式,胰岛素选自如下所述的长效胰岛素(L1)至(L7)所构成的G2组:
(L1):甘精胰岛素
甘精胰岛素(由Sanofi-Aventis以销售)已批准及销售用于每天一次皮下给药。甘精胰岛素提供持续24小时的相对恒定的降葡萄糖活性且可在一天中的任何时间给药,只要其在每天的同一时间给药。
(L2):地特胰岛素
地特胰岛素(由Novo Nordisk以销售)已批准及销售用于每天两次或每天一次、优选随晚餐或在就寝时皮下给药。
(L3):德谷胰岛素
德谷胰岛素(NN1250)为中性、可溶性超长效胰岛素,作用持续时间在24小时以上。德谷胰岛素具有极平坦、可预测且平滑的作用性质。其用于每天皮下给药一次或一次以下(例如一周三次)。
(L4):聚乙二醇化(PEGylated)的赖脯胰岛素(insulin lispro)
用高分子量聚(乙二醇)衍生物进行聚乙二醇化的赖脯胰岛素,尤其如WO 2009/152128(其公开内容并入本文中)中所公开,例如式P-[(A)-(B)]的聚乙二醇化的赖脯胰岛素化合物或其药学上可接受的盐,其中A为赖脯胰岛素的A链,B为赖脯胰岛素的B链,且P为分子量在约17.5kDa至约40kDa范围内的PEG,且其中A及B适当交联且P通过氨酯共价键(urethane covalent bond)连接至B的28位的赖氨酸的ε氨基。
(L5):酰胺化的甘精胰岛素
酰胺化的甘精胰岛素,尤其呈GlyA21、ArgB31、ArgB32-NH2人胰岛素(甘精胰岛素酰胺,即甘精胰岛素的B链的C末端被酰胺化)形式,如WO2008/006496或WO 2008/006496(其公开内容并入本文中)中所公开。
(L6):
LysB29(Nε-石胆酰基-γ-Glu)去(B30)人胰岛素或NεB29-ω-羧基十五酰基-γ-氨基-丁酰基去(B30)人胰岛素。
(L7):
酰胺化的胰岛素类似物,如WO 2009/087082(其公开内容并入本文中)中所公开,尤其选自权利要求14的那些,或如WO 2009/087081(其公开内容并入本文中)中所公开,尤其选自权利要求16的那些。
G2组的优选成员为L1、L2和L3,尤其甘精胰岛素。
长效胰岛素类似物通常作为基础抗糖尿病治疗给予I型糖尿病、II型糖尿病或成年发作型隐匿性自身免疫性糖尿病(latent autoimmune diabetes with onset in adults;LADA)患者,以控制不摄入食物时的血糖。如上所述,此类型的胰岛素提供长达36小时的连续的胰岛素活性水平。长效胰岛素在约8至12小时后发挥最大强度。由于其优势,所以认为用这些胰岛素类似物治疗可产生有益作用,例如较少低血糖症、较少体重增加或更佳的代谢控制,从而可能产生较少晚期糖尿病并发症,例如有关眼睛、肾脏或足的问题及心肌梗塞、中风或死亡。
根据本发明,提供治疗患者如上下文所述的疾病及病症的方法,其特征在于将SGLT2抑制剂和胰岛素(例如以组合或交替)给予至患者。所述疾病及病症尤其包括糖尿病、I型糖尿病、II型糖尿病,需要使用胰岛素治疗的疾病、需要使用胰岛素治疗的病症。根据本发明的一个实施方式,该胰岛素是基础胰岛素治疗的一部分。
术语基础胰岛素治疗涉及其中将一种或多种胰岛素给予至患者以使得在患者平均血浆胰岛素含量对比时间的图中,基础释放性质通常具有最小峰(通常称为“无峰性质”或“平坦性质”),且长期缓慢连续地释放胰岛素的治疗。根据一个实施方式,该基础胰岛素治疗包括将长效胰岛素给予至患者。根据另一实施方式,该基础胰岛素治疗包括通过输注,例如通过泵将胰岛素(尤其速效或短效胰岛素,包括人胰岛素)给予至患者以在延长期限(例如超过12或24小时或更长)实现希望的患者平均血浆胰岛素含量。
因此根据本发明的一个实施方式,在患者中提供治疗选自以下的疾病或病症的方法:糖尿病、I型糖尿病、II型糖尿病以及需要使用胰岛素治疗的疾病或病症,该方法的特征在于患者接受基础胰岛素治疗且还将SGLT2抑制剂给予至患者。
根本此实施方式的一个方面,该患者接受基础胰岛素治疗,其中将长效胰岛素给予至患者。例如该长效胰岛素通过注射(例如皮下注射)给药。该SGLT2抑制剂优选口服给予。根据此方面,长效胰岛素与SGLT2抑制剂以组合或交替给予,即在相同或不同时间给予。该长效胰岛素例如以一天一次或两次给予至患者,优选一天一次。该SGLT2抑制剂例如以一天一次或两次给予至患者,优选一天一次。
根据此实施方式的另一方面,该患者接受基础胰岛素治疗,其中通过输注(例如通过泵)将胰岛素给予至患者。根据此方面,胰岛素可为速效或短效胰岛素,例如人胰岛素。该SGLT2抑制剂优选口服给予。根据此方面,胰岛素与SGLT2抑制剂以组合或交替给予,即在相同或不同时间给予。该胰岛素例如通过泵输注每天给予患者数次,其中选择时间与剂量以实现特定范围的血浆胰岛素含量。该SGLT2抑制剂例如以一天一次或两次给予至患者,优选一天一次。
根据本发明的另一实施方式,根据本发明的药物组合物、方法及用途还包含其它抗糖尿病药物。
其它抗糖尿病药物选自以下的G3组:双胍类、噻唑烷二酮类、磺酰脲类、列奈类、α-葡萄糖苷酶抑制剂、GLP-1类似物、DPP-4抑制剂以及amylin类似物,包括上述药物的药学上可接受的盐。下文中描述关于第三种抗糖尿病药物的优选实施方式。
G3组包含双胍类。双胍类的实例为二甲双胍、苯乙双胍(phenformin)及丁福明(buformin)。优选的双胍为二甲双胍。
如本文所用的术语“二甲双胍”是指二甲双胍或其药学上可接受的盐,例如盐酸盐、二甲双胍(2:1)富马酸盐及二甲双胍(2:1)琥珀酸盐、氢溴酸盐、对氯苯氧基乙酸盐或双羟萘酸盐(embonate),及其它已知一元或二元羧酸的二甲双胍盐。本文所用的二甲双胍优选盐酸二甲双胍。
G3组包含噻唑烷二酮类。噻唑烷二酮类(TZD)的实例为吡格列酮(pioglitazone)及罗格列酮(rosiglitazone)。
如本文所用的术语“吡格列酮”是指吡格列酮,包括其对映异构体、其混合物及其外消旋体,或其药学上可接受的盐,例如盐酸盐。
如本文所用的术语“罗格列酮”是指罗格列酮,包括其对映异构体、其混合物及其外消旋体,或其药学上可接受的盐,例如马来酸盐。
G3组包含磺酰脲类。磺酰脲类的实例为格列本脲(glibenclamide)、甲苯磺丁脲(tolbutamide)、格列美脲(glimepiride)、格列吡嗪(glipizide)、格列喹酮(gliquidone)、格列波脲(glibornuride)、格列本脲(glyburide)、格列派特(glisoxepide)及格列齐特(gliclazide)。优选的磺酰脲为甲苯磺丁脲、格列喹酮、格列本脲、格列吡嗪及格列美脲,尤其格列本脲、格列吡嗪及格列美脲。
如本文所用的组“格列本脲”、“格列美脲”、“格列喹酮”、“格列波脲”、“格列齐特”、“格列派特”、“甲苯磺丁脲”及“格列吡嗪”的各术语是指各别活性药物或其药学上可接受的盐。
G3组包含列奈。列奈的实例为那格列奈(nateglinide)、瑞格列奈(repaglinide)及米格列奈(mitiglinide)。
如本文所用的术语“那格列奈”是指那格列奈,包括其对映异构体、其混合物及其外消旋体,或其药学上可接受的盐及酯。
如本文所用的术语“瑞格列奈”是指瑞格列奈,包括其对映异构体、其混合物及其外消旋体,或其药学上可接受的盐及酯。
G3组包含α-葡萄糖苷酶抑制剂。α-葡萄糖苷酶抑制剂的实例为阿卡波糖(acarbose)、伏格列波糖(voglibose)及米格列醇(miglitol)。
如本文所用的组“阿卡波糖”、“伏格列波糖”及“米格列醇”的各术语是指各别活性药物或其药学上可接受的盐。
G3组包含GLP-1类似物的抑制剂。GLP-1类似物的实例为艾塞那肽(exenatide)及利拉鲁肽(liraglutide)。
如本文所用的组“艾塞那肽”及“利拉鲁肽”的各术语是指各别活性药物或其药学上可接受的盐。
G3组包括DPP-4抑制剂。DPP-4抑制剂的实例为利格列汀(linagliptin)、西他列汀(sitagliptin)、维格列汀(vildagliptin)、萨格列汀(saxagliptin)、地那列汀(denagliptin)、阿格列汀(alogliptin)、卡格列汀(carmegliptin)、美格列汀(melogliptin)及度格列汀(dutogliptin),包括其药学上可接受的盐、其水合物及溶剂合物。
G3组包括amylin类似物。amylin类似物的一个实例为普兰林肽(pramlintide),包括其药学上可接受的盐、其水合物及溶剂合物。例如普兰林肽醋酸盐以商品名Symlin销售。
根据一个实施方式,根据本发明的药物组合物、方法及用途涉及SGLT2抑制剂与胰岛素的组合,其优选选自根据表1中条目的子实施方式E1至E36。
表1
在表1中所列的根据本发明的组合中,甚至更优选根据条目E27至E39的组合。
根据另一实施方式,根据本发明的药物组合物、方法及用途涉及SGLT2抑制剂与胰岛素的组合,其还包含其它抗糖尿病药物。优选子实施方式选自表2中的条目F1至F72。
表2
与使用单独的SGLT2抑制剂或胰岛素的单一疗法,例如长效胰岛素(例如甘精胰岛素)的单一疗法相比,根据本发明的SGLT2抑制剂和胰岛素的组合显著改善血糖控制,特别在如下文所述的患者中。此外,与所述胰岛素的单一疗法,例如长效胰岛素(例如甘精胰岛素)的单一疗法相比,根据本发明的SGLT2抑制剂和胰岛素的组合允许减少胰岛素的剂量。伴随胰岛素剂量的减少可预防或减弱与使用所述胰岛素治疗相关的副作用。剂量减少有益于患者,否则他们将潜在遭受使用更高剂量的一种或多种活性成分的治疗副作用(尤其对于胰岛素引起的副作用)。因此,根据本发明的药物组合物和方法显示更小的副作用,因而使得治疗更可耐受并改善患者的治疗顺应性。此外,通过与SGLT2抑制剂组合治疗可延长胰岛素的功效,例如在使用长效胰岛素或短速效胰岛素(包括人胰岛素)的经泵输注基础胰岛素治疗中的胰岛素功效。因此可延长胰岛素两次施用(例如皮下注射或经泵输注)间的时间间隔。例如在根据本发明的使用长效胰岛素以及SGLT2抑制剂的组合疗法中,选择长效胰岛素的剂量、SGLT2抑制剂的剂量、长效胰岛素两次施用间的时间间隔以及长效胰岛素和SGLT2抑制剂施用间的时间间隔,以向患者提供给定时间期限(特别24小时)的良好血糖控制。
当本发明提及需要治疗或预防的患者时,其主要指人的治疗及预防,但药物组合物还可相应用于哺乳动物的兽医学中。在本发明范围内,术语"患者"涵盖成人(年龄为18岁或以上)、青少年(年龄为10至17岁)及儿童(年龄为6-9岁)。
此外,根据本发明的方法和/或用途有利地适用于那些显示一种、两种或多种以下病症的患者:
(a)I型糖尿病;
(b)需要使用胰岛素治疗;
(c)成年发作型隐匿性自身免疫性糖尿病(LADA)。
此外,根据本发明的方法和/或用途有利地适用于那些使用或需要使用胰岛素治疗(例如使用甘精胰岛素或地特胰岛素)的患者,特别是诊断为I型糖尿病且显示一种、两种或多种以下病症(包括发展此类病症的风险)的患者:
(d)夜间和/或清晨低血糖症;
(e)低血糖发作;
(f)高血糖发作;
(g)心脑并发症;
(h)视网膜病变,尤其增殖性视网膜病变;
(i)注射位点反应,例如皮肤或皮下组织紊乱。
如上文所述,通过给予根据本发明的药物组合物,且尤其由于其中SGLT2抑制剂的高SGLT2抑制活性,过量血糖经患者的尿液排出,使得体重可能不增加或甚至体重降低。因此,根据本发明的治疗或预防有利地适于需要该治疗或预防的患者,这些患者经诊断具有一种或多种选自以下的病症:超重及肥胖症,尤其I级肥胖症、II级肥胖症、III级肥胖症、内脏肥胖症及腹部肥胖症。此外,本发明的治疗或预防有利地适于禁忌体重增加的患者。例如由于给予第三种抗糖尿病药物,疗法的任何增加体重的效应可能因此而减弱或甚至消除。
因此,根据本发明的一个优选实施方式,提供一种在有需要的患者中改善血糖控制和/或降低空腹血糖、餐后血糖和/或糖基化血红蛋白HbAlc的方法,该患者经诊断患有葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)、胰岛素抵抗、代谢综合征和/或I型或II型糖尿病,该方法的特征在于如上下文定义的SGLT2抑制剂和胰岛素例如以组合或交替给予至患者。
根据本发明的另一优选实施方式,提供一种作为饮食及运动的辅助手段的改善I型或II型糖尿病患者、尤其成人患者的血糖控制的方法。
可发现通过使用根据本发明的药物组合物,即使在血糖控制不充分的患者中,尤其在尽管经胰岛素治疗,例如尽管经最大推荐或耐受剂量的胰岛素单一治疗但血糖控制仍不充分的患者中,也可达到血糖控制的改善。
此外,根据本发明的药物组合物、方法和用途尤其适于治疗经诊断患有一种或多种以下病症的患者
(a)肥胖症(包括I级、II级和/或III级肥胖症)、内脏肥胖症和/或腹部肥胖症,
(b)甘油三酯血液水平≥150mg/dL,
(c)女性患者HDL-胆固醇血液水平<40mg/dL和男性患者<50mg/dL,
(d)收缩压≥130mm Hg且舒张压≥85mm Hg,
(e)≥100mg/dL。
认为经诊断患有葡萄糖耐量降低(IGT)、空腹血糖异常(IFG)、胰岛素抵抗和/或代谢综合征的患者发展心血管疾病(例如心肌梗塞、冠心病、心脏功能不全、血栓栓塞事件)的风险增加。根据本发明的血糖控制可使得心血管风险降低。
此外,根据本发明的药物组合物、方法及用途尤其适于治疗器官移植后的患者,尤其诊断具有一种或多种以下情况的患者:
(a)年龄较高,尤其高于50岁,
(b)男性;
(c)超重、肥胖症(包括I级、II级和/或III级肥胖症)、内脏肥胖症和/或腹部肥胖症,
(d)移植前糖尿病,
(e)免疫抑制疗法。
此外,根据本发明的药物组合物、方法及用途尤其适于治疗经诊断患有一种或多种以下病症的患者:
(a)低钠血症,尤其慢性低钠血症;
(b)水中毒;
(c)水潴留;
(d)血浆钠浓度低于135mmol/L。
此外,根据本发明的药物组合物、方法及用途尤其适于治疗经诊断患有一种或多种以下病症的患者:
(a)高血清尿酸含量,尤其大于6.0mg/dL(357μmol/L);
(b)痛风关节炎病史,尤其复发性痛风关节炎;
(c)肾结石,尤其复发性肾结石;
(d)形成肾结石的高趋势。
根据本发明的药物组合物,尤其归因于SGLT2抑制剂,显示良好的安全性性质。因此,根据本发明的治疗对于推荐减少胰岛素剂量的患者而言是有利的。
根据本发明的药物组合物尤其适于在I型糖尿病或II型糖尿病中长期治疗或预防上下文所述的疾病和/或病症,尤其适于其长期血糖控制。
如上下文所用的术语“长期”表示对患者的治疗或向患者给药的时间长于12周,优选长于25周,甚至更优选长于1年。
因此,本发明的一个特别优选实施方式提供一种改善(尤其长期改善)I型糖尿病患者的血糖控制的治疗方法(优选口服疗法)。
因此,本发明的一个特别优选实施方式提供一种改善(尤其长期改善)II型糖尿病患者、尤其晚期II型糖尿病患者、尤其还经诊断患有超重、肥胖症(包括I级、II级和/或III级肥胖症)、内脏肥胖症和/或腹部肥胖症的患者的血糖控制的治疗方法(优选口服疗法)。
除非另外说明,根据本发明的组合疗法可涉及一线、二线或三线疗法,或初始或追加疗法或替代疗法。
根据一个实施方式,SGLT2抑制剂和胰岛素以及任选地其它抗糖尿病药物组合给药(即,同时地),例如在一种单一制剂中或在两种单独制剂或剂型中,患者,例如相继地在两种或三种单独制剂或剂型中。因此,一种组合药物(即SGLT2抑制剂或胰岛素)的给药可在另一组合药物的给药之前、同时或之后。在一个实施方式中,对于根据本发明的组合疗法,SGLT2抑制剂和胰岛素在不同制剂或不同剂型中给予。在另一实施方式中,对于根据本发明的组合疗法,SGLT2抑制剂和胰岛素在相同制剂或相同剂型中给予。
因此根据本发明的另一方面,提供了药物组合物或固定剂量复方剂(fixed dose combination),其包含
a)如本文定义的SGLT2抑制剂,以及
b)如本文定义的胰岛素,
以及任选地一种或多种药学上可接受的载体和/或稀释剂。
在本发明的范围内,SGLT2抑制剂优选口服或通过注射给予,优选口服。胰岛素优选通过注射给予,优选皮下注射或通过输注,例如用泵。其它给药形式是可能的且在下文中描述。任选给予的其它抗糖尿病药物优选口服给予。在此种情况中SGLT2抑制剂和其它抗糖尿病药物可共同包含于一个剂型中或在分开剂型中。
因此根据本发明的另一实施方式,提供了特别用于注射或输注给予(例如皮下注射或经泵输注)的系统用药物组合物、递送系统或装置,其包含
a)如本文定义的SGLT2抑制剂,以及任选地,
b)如本文定义的胰岛素,
以及任选地一种或多种药学上可接受的载体和/或稀释剂。
应当理解,欲向患者给予且在根据本发明的治疗或预防中需要使用的根据本发明的SGLT2抑制剂以及胰岛素以及任选地其它抗糖尿病药物的量将随给药途径、需要治疗或预防的病症的性质及严重程度、患者年龄、体重及身体状况、伴随药物而变化,且最终将由住院医生(attendant physician)决定。然而,一般而言,药物组合物或剂型中所包括的根据本发明的SGLT2抑制剂、胰岛素及任选地其它抗糖尿病药物的量足以在其组合和/或交替给予时改善待治疗患者的血糖控制。
为了治疗高尿酸血症或与高尿酸血症相关的病症,药物组合物或剂型中所包含的根据本发明的SGLT2抑制剂的量足以治疗高尿酸血症而不干扰患者的血浆葡萄糖稳态,尤其不诱发低血糖症。
为了治疗或预防肾结石,药物组合物或剂型中所包含的根据本发明的SGLT2抑制剂的量足以治疗或预防肾结石而不干扰患者的血浆葡萄糖稳态,尤其不诱发低血糖症。
为了治疗低钠血症及其相关病症,药物组合物或剂型中所包含的根据本发明的SGLT2抑制剂的量足以治疗低钠血症或相关病症而不干扰患者的血浆葡萄糖稳态,尤其不诱发低血糖症。
下文中描述根据本发明的药物组合物和方法及用途中欲使用的SGLT2抑制剂、胰岛素及任选地其它抗糖尿病药物的量的优选范围。这些范围是指就成人患者(尤其例如体重为约70kg的人)而言每天给予的量且可根据每天给予1或2次及其它给药途径及患者年龄相应加以调整。剂量及量的范围针对分别的活性部分计算。根据本发明的组合疗法中所使用的SGLT2抑制剂、胰岛素和/或任选地其它抗糖尿病药物的剂量宜低于单一疗法或常规疗法中所使用的剂量,从而避免那些药物用作单一疗法时引起的可能的不良副作用。
一般而言,根据本发明的药物组合物、方法及用途中的SGLT2抑制剂的量优选在一般针对使用所述SGLT2抑制剂的单一疗法推荐的量的1/5至1/1范围内。
SGLT2抑制剂的优选剂量范围为每天0.5mg至200mg,甚至更优选每天1至100mg,最优选每天1至50mg。优选口服给药。因此,药物组合物可包含上文所述的量,尤其1至50mg或1至25mg。具体剂量规格(例如每片剂或胶囊)为例如1、2.5、5、7.5、10、12.5、15、20、25或50mg式(I)化合物,尤其化合物(I.9)或达格列净。活性成份的施用可每天进行1次、2次或3次,优选每天1次。
一般而言,根据本发明的药物组合物、方法及用途中的胰岛素的量优选在一般针对使用所述长效胰岛素的单一疗法推荐的量的1/5至1/1范围内。
胰岛素典型通过皮下注射给予,例如在每天两次、每天一次至每周一次注射的范围内。合适的胰岛素剂量及剂型可由本领域技术人员所决定。所有接受胰岛素治疗的患者必须进行血糖监控。将根据对治疗的响应以及所获得的血糖控制而对长效胰岛素的剂量个体化。剂量通常在10至70单位/天的范围内。根据WHO的胰岛素确定每天剂量为40单位。长效胰岛素通常给天给予一次,在早晨或在晚上。可在任意这些时间点给予SGLT-2抑制剂。I型糖尿病患者通常使用包含基础胰岛素(例如长效胰岛素)以及速效胰岛素的每天多次注射方案进行治疗。取决于β细胞功能、年龄、体重、身体活动度及饮食,I型糖尿病中的典型胰岛素每天需求为40至60单位。通常约40-60%的胰岛素每天总需求将以基础胰岛素(例如使用长效胰岛素)给予。
例如,甘精胰岛素(Lantus)为每天皮下给予一次。Lantus可在一天当中的任意时间点给予,但每天是在同一时间。Lantus的剂量基于临床响应个体化。在当前未使用胰岛素治疗的II型糖尿病患者中的Lantus典型起始剂量为10单位,或者0.2U/kg,每天一次,其随后应调节至患者所需。I型糖尿病患者通常将使用包含基础胰岛素以及速效胰岛素的每天多次注射方案进行治疗。取决于β细胞功能、年龄、体重、身体活动度及饮食,I型糖尿病中的典型胰岛素每天需求为40至60单位。通常约40-60%的胰岛素每天总需求将以基础胰岛素给予;当使用Lantus时,在I型糖尿病中的给药原则与在II型糖尿病中的给药原则相同。此外,需要基于临床响应滴定胰岛素剂量。
地特胰岛素(Levemir)为每天皮下给予一次或两次。对于每天使用一次Levemir治疗的患者,优选随同晚餐或在就寝时给药。对于需要每天给药两次的患者,晚间给药可随同晚餐、在就寝时或在早晨给药12小时后。Levemir的剂量基于临床响应个体化。对于口服抗糖尿病药物不能充分控制的初始胰岛素治疗II型糖尿病患者,Levemir的起始剂量应为在晚上每天一次的0.2单位/kg或每天一次或两次10单位,且调节该剂量至实现血糖目标。I型糖尿病患者通常将使用包含基础胰岛素以及速效胰岛素的每天多次注射方案进行治疗。取决于β细胞功能、年龄、体重、身体活动度及饮食,I型糖尿病中的典型胰岛素每天需求为40至60单位。通常约40-60%的胰岛素每天总需求将以基础胰岛素给予;当使用Levemir时,在I型糖尿病中的给药原则与在II型糖尿病中的给药原则相同。此外,需要基于临床响应滴定胰岛素剂量。
此外,长效胰岛素类似物(例如德谷胰岛素以及基础赖脯胰岛素)将发展为U-100的最终制剂且这些胰岛素在I型和II型糖尿病中的给药也将个体化调整。
在SGLT-2抑制剂和胰岛素与其它抗糖尿病药物组合的情况下,其它抗糖尿病药物的剂量优选在使用所述其它抗糖尿病药物的单一疗法推荐的剂量的1/5至1/1范围内。使用低于单一疗法的剂量的其它抗糖尿病药物可避免或最小化当那些药物用作单一疗法时引起的可能毒性及不良副作用。
关于二甲双胍作为优选的其它抗糖尿病药物,二甲双胍的给予剂量通常从每天约500mg至2000mg直至3000mg不等,使用不同给药方案从约100mg至500mg或200mg至850mg(1天1-3次),或1天1次、2次或3次约300mg至1000mg,或缓释二甲双胍,剂量为1天1次或2次约100mg至1000mg或优选500mg至1000mg或1天1次约500mg至2000mg。特别剂量规格可为250、500、625、750、850和1000mg盐酸二甲双胍。
对于年龄为10至16岁的儿童,二甲双胍的推荐起始剂量为每天给予500mg。如果此剂量不能产生足够的结果,则剂量可增至每天2次500mg。进一步增加的增量可从每周500mg至最大日剂量为2000mg,以分份剂量给予(例如2或3个分份剂量)。二甲双胍可与食物一起给予以减少恶心。
关于吡格列酮作为优选的其它抗糖尿病药物,吡格列酮的剂量通常为每天1次约1-10mg、15mg、30mg或45mg。
关于利格列汀作为优选的其它抗糖尿病药物,利格列汀的剂量通常为每天1次约1-10mg,例如每天1、2.5、5或10mg。
在根据本发明的方法及用途中,SGLT2抑制剂和胰岛素以组合或交替给予。术语“组合给予”是指活性成份在同一时间(即同时)或基本上同一时间给予。术语“交替给予”是指首先给予一种或两种活性成份(即SGLT2抑制剂或胰岛素),且一段时间后,给予其它活性成份(即胰岛素或SGLT2抑制剂),即依次给予两种活性成分。首次给予与第二次给予活性成分之间的该段时间可在1分钟至12小时范围内。组合或交替给予可为每天一次、每天两次、每天三次或每天四次,优选每天一次或两次.
呈单独或多个剂型、优选呈试剂盒的药物组合物适用于组合疗法中,以灵活地满足患者的个体化治疗需求。
根据第一实施方式,优选的试剂盒包含
(a)第一容器,其含有包含SGLT2抑制剂及至少一种药学上可接受的载体的剂型,及
(b)第二容器,其含有包含胰岛素及至少一种药学上可接受的载体的剂型。
根据第二实施方式,优选的试剂盒包含
(a)第一容器,其含有包含SGLT2抑制剂及至少一种药学上可接受的载体的剂型,及
(b)第二容器,其含有包含胰岛素及至少一种药学上可接受的载体的剂型,及
(b)第三容器,其含有包含其它抗糖尿病药物(例如二甲双胍、吡格列酮或利格列汀)及至少一种药学上可接受的载体的剂型。
根据第三实施方式,优选的试剂盒包含
(a)第一容器,其含有包含SGLT2抑制剂及其它抗糖尿病药物及至少一种药学上可接受的载体的剂型,及
(b)第二容器,其含有包含胰岛素及至少一种药学上可接受的载体的剂型。
本发明的另一方面为一种制品,其包含根据本发明的呈分别的剂型的药物组合物及标签或药品说明书,该标签或药品说明书包括分别的剂型以组合或交替给予的说明。
根据第一实施方式,制品包含(a)包含根据本发明的SGLT2抑制剂的药物组合物;及(b)标签或药品说明书,其包括药物可例如与包含根据本发明的胰岛素的药物或包含根据本发明的胰岛素及其它抗糖尿病药物的药物以组合或交替给予或与其组合或交替给予的说明。
根据第二实施方式,制品包含(a)包含根据本发明的胰岛素的药物组合物及(b)标签或药品说明书,其包括药物可例如与包含根据本发明SGLT2抑制剂的药物或包含根据本发明的SGLT2抑制剂及其它抗糖尿病药物的药物以组合或交替给予或待与其组合或交替给予的说明。
根据第三实施方式,制品包含(a)包含根据本发明的SGLT2抑制剂及其它抗糖尿病药物的药物组合物及(b)标签或药品说明书,其包括药物可例如与或将与包含根据本发明的胰岛素的药物以组合或交替给予的说明。
根据本发明的药物组合物的所需剂量方便地以每天一次提供或以适当间隔给予的分次剂量(例如每天两次、三次或更多的剂量)提供。
药物组合物可经配方以用于呈液体或固体形式口服、肠胃外(包括皮下)或其它途径给予。优选口服给予SGLT2抑制剂。若适宜,则制剂宜呈不连续的剂量单元,且可由药物领域中熟知的任何方法制备。所有方法均包括以下步骤:将活性成份与一种或多种药学上可接受的载体(如液体载体或细粉状固体载体或两者)混合,且接着在适当时使产品成形为所需制剂。包含SGLT2抑制剂化合物(I.9)的药物组合物的实例公开于WO 2010/092126中。包含SGLT2抑制剂化合物(I.9)和利格列汀的药物组合物的实例公开于WO2010/092124中。
药物组合物可配制为以下形式:溶液、混悬液、乳剂、片剂、颗粒剂、细颗粒剂、散剂、胶囊、小胶囊、软胶囊、丸剂、口服溶液、糖浆、干糖浆、咀嚼片、糖衣片、泡腾片、滴剂、速溶片、口服快速分散片等。SGLT2抑制剂的药物组合物优选为片剂形式。
药物组合物及剂型优选包含一种或多种药学上可接受的载体。优选载体必须为“可接受的”,意思是指与制剂的其它成份相容且对其接受者无害。药学上可接受的载体的实例为本领域技术人员所知。
根据本发明的药物组合物还可配方用于肠胃外给药(例如通过注射,例如快速静脉推注或连续输注),且可呈添加防腐剂的安瓿、预填充注射器、小体积输注或多剂量容器中的单位剂型。组合物可使用例如于油性或水性媒剂中的混悬液、溶液或乳液的形式且可含有例如混悬剂、稳定剂和/或分散剂的配方剂。或者,活性成份可呈通过无菌分离无菌固体或通过自溶液冻干获得的散剂形式,其在使用前以合适的媒剂(例如无菌无热原水)重构。
本发明的胰岛素和/或SGLT2抑制剂的可注射制剂(尤其用于皮下使用)可根据已知制剂技术,例如使用合适的液体载体(其通常包含无菌水)及任选地其它添加剂(例如防腐剂、pH值调节剂、缓冲剂、等渗剂、溶解助剂和/或表面活性剂(tenside)或其类似物)来制备,以获得可注射溶液或悬浮液。此外,可注射制剂可包含其它添加剂,例如延迟药物释放的盐、溶解改良剂或沉淀剂。此外,可注射胰岛素制剂可包含胰岛素稳定剂,例如锌化合物。根据本发明的组合的组分胰岛素优选通过注射(优选皮下)或通过输注(例如使用泵或相当的递送系统)给予。
关于本发明SGLT2抑制剂和/或本发明胰岛素的剂型、制剂及给药的进一步细节,可参考科学文献和/或公开的专利文献、特别是那些本文所引用的文献。
药物组合物(或制剂)可以以多种方式包装。通常地,分配的物件(article fordistribution)包括以恰当形式包含一种或多种药物组合物的一种或多种容器。片剂典型包装在易于处置、分配和保存的合适内包装内,且在保存期间与环境长时间接触时确保组合物的适当稳定性。片剂的内包装可为瓶或泡罩包装。
注射用溶液可以以典型合适的呈现形式获得,例如小瓶、柱或预填充(一次性)笔,可将其进一步包装。
物件还可包括标签或包装说明书,其参考通常包括在治疗产品的商用包装内的说明书,其可包含适应症、用法、用量、给药、禁忌症和/或使用该治疗产品的注意事项等信息。在一个实施方式中,标签或包装说明书指出该组合物可用于上下文所述的任何目的。
与仅包含一种或两种活性成分的药物组合物和方法相比,根据本发明的药物组合物和方法显示治疗及预防上文所述的那些疾病及病症的有利作用。可发现例如关于功效、剂量规格、剂量频率、药效学特性、药代动力学特性、较少不良反应、便利性、顺应性等的额外有利作用。
本领域技术人员已知制备本发明SGLT2抑制剂及其前药的方法。有利地,根据本发明的化合物使用包括上文引用的专利申请文献中所述的合成方法制备。优选制备方法公开于WO2006/120208及WO 2007/031548中。关于优选化合物(I.9),有利的结晶形式公开于国际专利申请WO 2006/117359中,在此将其全文引入本发明。
关于胰岛素,其合成方法为本领域技术人员所知且公开于科学文献和/或公开的专利文献,特别是那些本文所引用的文献中。
活性成分,特别是胰岛素和/或其它抗糖尿病药物,可以以药学上可接受的盐的形式存在。活性成分或其药学上可接受的盐可以以溶剂合物(例如水合物或醇加成物)的形式存在。
可由本领域中已知的动物模型测试本发明范围内的任何上述组合及方法。在下文中,描述适于评估根据本发明的药物组合物和方法的药理学相关特性的体内实验:
在如db/db小鼠、ob/ob小鼠、Zucker Fatty(fa/fa)大鼠或Zucker Diabetic Fatty(ZDF)大鼠的遗传高胰岛素血症性或糖尿病性动物中测试根据本发明的药物组合物和方法。此外,其可在如经链脲霉素(streptozotocin)预处理的HanWistar或Sprague Dawley大鼠的实验诱发糖尿病的动物中进行测试。
可在单次给予单独及组合的SGLT2抑制剂和胰岛素后,在上文所述动物模型中在口服葡萄糖耐量试验中测试根据本发明的组合对血糖控制的作用。在禁食过夜动物中进行口服葡萄糖刺激(glucose challenge)之后,跟踪调查血糖的时程。如峰值葡萄糖浓度降低或葡萄糖AUC降低所测量,与各单一疗法相比,根据本发明的组合显著改善葡萄糖波动。此外,在上文所述动物模型中多次给予单独或组合的SGLT2抑制剂和胰岛素之后,可通过测量血液中的HbAlc值测定对血糖控制的作用。与各单一疗法相比,根据本发明的组合显著降低HbAlc。
可由上文所述动物模型中较低剂量的组合及单一疗法对血糖控制的作用,测试SGLT2抑制剂和胰岛素中的一种或两种的可能的剂量降低。与安慰剂治疗相比,较低剂量的根据本发明的组合显著改善血糖控制,而较低剂量的单一疗法则无效。
可在上文所述动物模型中多次给药后,通过测量胰腺胰岛素含量增加,或通过在胰腺部分免疫组织化学染色后通过形态分析测量增加的β细胞质量,或通过测量经分离胰岛中增加的葡萄糖刺激的胰岛素分泌来确定根据本发明的SGLT2抑制剂和胰岛素的组合对β细胞再生及新生的优异的作用。
药理学实施例
以下实施例显示根据本发明的组合对血糖控制的有益作用。
实施例1a:
以下实施例显示与各自单一疗法相比,SGLT2抑制剂(化合物(I.9))和胰岛素(甘精胰岛素)的组合对血糖控制的有益作用。与使用实验室动物有关的所有实验方案均经过联邦伦理委员会(federal Ethics Committee)审议且经政府部门批准。研究开始两周前,使用腹腔注射60mg/kg的链脲霉素单一剂量预处理大鼠以诱发类似于I型糖尿病的实验性糖尿病。研究期间,在禁食3小时的雄性Sprague-Dawley大鼠(Crl:CD)中测定4小时的血糖,其中该大鼠在研究开始时为8-9周龄。通过尾部取血获得给药前血液样品用于随机分组并在给予胰岛素和/或SGLT2抑制剂30分钟、60分钟、90分钟以及2小时、3小时、4小时后用血糖仪测量血糖。在0分钟时间点向动物(每组n=4-6)注射甘精胰岛素或皮下注射等渗NaCl。同时,所有动物接受口服给予的单独媒剂(0.5%羟乙基纤维素水溶液)或含有SGLT2抑制剂的此媒剂。数据以平均值±S.E.M表示。通过重复测量双向ANOVA(变量分析)后,使用组对比的邦弗朗尼事后检验法(Bonferroni post test)来进行统计比较。认为p值<0.05显示统计学显著差异。结果示于图1a中。术语"化合物A"表示剂量为10mg/kg的SGLT2抑制剂化合物(I.9)。甘精胰岛素的给予剂量为1.5IU/动物。术语"化合物A+甘精胰岛素"表示相同剂量的SGLT2抑制剂化合物(I.9)和甘精胰岛素的组合。相对于对照组的P值由星号表示,单一疗法相对于组合的P值由十字符表示(一个符号,p<0.05;两个符号,p<0.01;三个符号,p<0.001)。给药4小时后,相对于对照,SGLT2抑制剂降低血糖19%而甘精胰岛素降低血糖27%。两种疗法相对于对照均未显示统计学显著差异。组合相对于对照显著降低血糖53%。组合组中的血糖降低与SGLT2单一疗法存在显著差异。
实施例1b:
以下实施例显示与各自单一疗法相比,SGLT2抑制剂(化合物(I.9))和胰岛素(甘精胰岛素)的组合对血糖控制的有益作用。与使用实验室动物有关的所有实验方案均经过联邦伦理委员会审议且经政府部门批准。研究开始两周前,使用腹腔注射60mg/kg的链脲霉素单一剂量预处理大鼠以诱发类似于I型糖尿病的实验性糖尿病。研究期间,在禁食3小时的雄性Sprague-Dawley大鼠(Crl:CD)中测定6小时的血糖,其中该大鼠在研究开始时为8-9周龄。通过尾部取血获得给药前血液样品用于随机分组并在给予胰岛素和/或SGLT2抑制剂30分钟、60分钟、90分钟以及2小时、3小时、4小时、5小时、6小时后用血糖仪测量血糖。在0分钟时间点向动物(每组n=4-6)注射甘精胰岛素或皮下注射等渗NaCl。同时,所有动物接受口服给予的单独媒剂(0.5%羟乙基纤维素水溶液)或含有SGLT2抑制剂的此媒剂。数据以平均值±S.E.M表示。通过重复测量双向ANOVA(变量分析)后,使用组对比的邦弗朗尼事后检验法来进行统计比较。认为p值<0.05显示统计学显著差异。结果示于图1b中。术语"化合物A"表示剂量为10mg/kg的SGLT2抑制剂化合物(I.9)。甘精胰岛素的给予剂量为1.5IU/动物。术语"化合物A+甘精胰岛素"表示相同剂量的SGLT2抑制剂化合物(I.9)和甘精胰岛素的组合。相对于对照组的P值由星号表示,单一疗法相对于组合的P值由十字符表示(一个符号,p<0.05;两个符号,p<0.01;三个符号,p<0.001)。给药6小时后,相对于对照,SGLT2抑制剂降低血糖13%而甘精胰岛素降低血糖22%。两种疗法相对于对照均未显示统计学显著差异。组合相对于对照显著降低血糖49%。组合组中的血糖降低与SGLT2单一疗法存在显著差异。
实施例2a:
以下实施例显示与高剂量胰岛素(甘精胰岛素)相比,SGLT2抑制剂(化合物(I.9))和低剂量胰岛素(甘精胰岛素)的组合对血糖控制的有益作用。与使用实验室动物有关的所有实验方案均经过联邦伦理委员会审议且经政府部门批准。研究开始两周前,使用腹腔注射60mg/kg的链脲霉素单一剂量预处理大鼠以诱发类似于I型糖尿病的实验性糖尿病。研究期间,在禁食3小时的雄性Sprague-Dawley大鼠(Crl:CD)中测定4小时的血糖,其中该大鼠在研究开始时为8-9周龄。通过尾部取血获得给药前血液样品用于随机分组并在单独给予胰岛素或共同给予SGLT2抑制剂30分钟、60分钟、90分钟以及2小时、3小时、4小时后用血糖仪测量血糖。在0分钟时间点向动物(每组n=4-6)注射甘精胰岛素或皮下注射等渗NaCl。同时,所有动物接受口服给予的单独媒剂(0.5%羟乙基纤维素水溶液)或含有SGLT2抑制剂的此媒剂。数据以平均值±S.E.M表示。通过重复测量双向ANOVA(变量分析)后,使用组对比的邦弗朗尼事后检验法来进行统计比较。认为p值<0.05显示统计学显著差异。结果示于图2a中。甘精胰岛素的给予剂量为1.5IU/动物(低剂量)或6IU/动物(高剂量)。术语"化合物A+低剂量甘精胰岛素"表示剂量为10mg/kg的SGLT2抑制剂和剂量为1.5IU/动物的甘精胰岛素的组合。相对于对照组的P值由星号表示,低剂量甘精胰岛素相对于组合或高剂量甘精胰岛素的P值由十字符表示(一个符号,p<0.05;两个符号,p<0.01;三个符号,p<0.001)。给药4小时后,低剂量甘精胰岛素相对于对照降低血糖27%,未显示统计学显著差异。组合降低血糖53%,其在降低血糖47%的高剂量甘精胰岛素的范围内。两种疗法相对于对照均存在显著差异。
实施例2b:
以下实施例显示与高剂量胰岛素(甘精胰岛素)相比,SGLT2抑制剂(化合物(I.9))和低剂量胰岛素(甘精胰岛素)的组合对血糖控制的有益作用。与使用实验室动物有关的所有实验方案均经过联邦伦理委员会审议且经政府部门批准。研究开始两周前,使用腹腔注射60mg/kg的链脲霉素单一剂量预处理大鼠以诱发类似于I型糖尿病的实验性糖尿病。研究期间,在禁食3小时的雄性Sprague-Dawley大鼠(Crl:CD)中测定6小时的血糖,其中该大鼠在研究开始时为8-9周龄。通过尾部取血获得给药前血液样品用于随机分组并在单独给予胰岛素或共同给予SGLT2抑制剂30分钟、60分钟、90分钟以及2小时、3小时、4小时、5小时、6小时后用血糖仪测量血糖。在0分钟时间点向动物(每组n=4-6)注射甘精胰岛素或皮下注射等渗NaCl。同时,所有动物接受口服给予的单独媒剂(0.5%羟乙基纤维素水溶液)或含有SGLT2抑制剂的此媒剂。数据以平均值±S.E.M表示。通过重复测量双向ANOVA(变量分析)后,使用组对比的邦弗朗尼事后检验法来进行统计比较。认为p值<0.05显示统计学显著差异。结果示于图2b中。甘精胰岛素的给予剂量为1.5IU/动物(低剂量)或6IU/动物(高剂量)。术语"化合物A+低剂量甘精胰岛素"表示剂量为10mg/kg的SGLT2抑制剂和剂量为1.5IU/动物的甘精胰岛素的组合。相对于对照组的P值由星号表示,低剂量甘精胰岛素相对于组合或高剂量甘精胰岛素的P值由十字符表示(一个符号,p<0.05;两个符号,p<0.01;三个符号,p<0.001)。给药6小时后,低剂量甘精胰岛素相对于对照降低血糖22%,未显示统计学显著差异。组合降低血糖49%,其在降低血糖44%的高剂量甘精胰岛素的范围内。两种疗法相对于对照均存在显著差异。组合组中降低的血糖相对于高剂量甘精胰岛素组未显示统计学显著差异。
实施例3:
以下实施例显示与单独的胰岛素相比,将SGLT2抑制剂(化合物(I.9))连续加入胰岛素(甘精胰岛素)对血糖控制的有益作用。与使用实验室动物有关的所有实验方案均经过联邦伦理委员会审议且经政府部门批准。研究开始两周前,使用腹腔注射60mg/kg的链脲霉素单一剂量预处理大鼠以诱发类似于I型糖尿病的实验性糖尿病。研究期间,在未禁食的雄性Sprague-Dawley大鼠(Crl:CD)中测定8小时的血糖,其中该大鼠在研究开始时为8-9周龄。通过尾部取血获得给药前血液样品并在给予胰岛素30分钟、60分钟、90分钟以及2小时、3小时、4小时、5小时、6小时、8小时后用血糖仪测量血糖。在0分钟时间点向动物注射甘精胰岛素(n=10)或皮下注射等渗NaCl(n=5)。在120(分钟)时间点根据血糖随机抽样甘精胰岛素处理大鼠并分为2组(每组n=5)。动物接受口服给予的单独媒剂(0.5%羟乙基纤维素水溶液)或含有SGLT2抑制剂的此媒剂。数据以平均值±S.E.M表示。通过重复测量双向ANOVA(变量分析)后,使用组对比的邦弗朗尼事后检验法来进行统计比较。认为p值<0.05显示统计学显著性差异。结果示于图3中。甘精胰岛素的给予剂量为1.5IU/动物。术语"甘精胰岛素/化合物A"表示剂量为1.5IU/动物的甘精胰岛素和剂量为10mg/kg的SGLT2抑制剂的组合。相对于对照组的P值由星号表示,媒介处理组相对于使用SGLT2抑制剂处理的动物的P值由十字符表示(一个符号,p<0.05;两个符号,p<0.01;三个符号,p<0.001)。当与媒介处理大鼠相比时,2至8小时间的血糖显著降低50%。
实施例4:
以下实施例显示于单独的胰岛素(作为胰岛素释放植入物)相比,SGLT2抑制剂(化合物(I.9))与胰岛素(作为胰岛素释放植入物)组合对身体脂肪比例的有益作用。与使用实验室动物有关的所有实验方案均经过联邦伦理委员会审议且经政府部门批准。研究开始两周前,使用腹腔注射60mg/kg的链脲霉素单一剂量预处理大鼠以诱发类似于I型糖尿病的实验性糖尿病。动物每天两次接受口服给予的单独媒剂(0.5%羟乙基纤维素水溶液)或含有SGLT2抑制剂(10mg/kg)的此媒剂。在附加组中,在大鼠颈部皮下植入1或2个胰岛素释放棒。在具有或不具有1个胰岛素植入物的情况下将SGLT2抑制剂给予动物。在第27天使用NMR技术测量身体脂肪。数据以平均值±S.E.M表示。通过单向ANOVA后,使用组对比的邦弗朗尼事后检验法/非配对t-检验法来进行统计比较。认为p值<0.05显示统计学显著性差异。结果示于图4中。术语"化合物A"表示剂量为10mg/kg的SGLT2抑制剂。相对于对照组的P值由星号表示,接受1个植入物的动物相对于1个植入物和SGLT2抑制剂的组合(表示为"化合物A+1个植入物")的P值由十字符表示(一个符号,p<0.05;两个符号,p<0.01;三个符号,p<0.001)。当与对照组相比时,胰岛素释放植入物显著增加身体脂肪比例(1个植入物:+83%;2个植入物:+72%)。当与单独接受1个植入物的大鼠相比时,1个植入物与SGLT2抑制剂(表示为"化合物A+1个植入物")的组合显示出显著更低的身体脂肪。
实施例5:
使用根据本发明的药物组合物治疗I型糖尿病患者,除了产生葡萄糖代谢状况的快速改善外,还可促进长期可维持的良好代谢状况。这可在使用根据本发明的药物组合物长期治疗(例如3个月至1年或甚至1至6年)并与单独使用胰岛素治疗的患者进行对比的患者中观察到。如果与单独使用胰岛素治疗的患者相比,未观测到空腹血糖和/或HbA1c值增加但看到低血糖事件率、葡萄糖波动或胰岛素需求降低,则证明获得了治疗成功。如果与单独使用最优胰岛素治疗的患者相比,显著更小百分率的使用根据本发明的药物组合物治疗的患者经历葡萄糖代谢位点的恶化(例如HbA1c值增加>6.5%或>7%),则进一步证明获得了治疗成功。例如一项具有30名I型糖尿病患者的临床研究(例如利用胰岛素泵或接受包含长效胰岛素的治疗)可探索SGLT2抑制剂(尤其化合物(I.9),例如每天1次10或25mg)作为胰岛素的辅剂对安全和功效的效果。
- 还没有人留言评论。精彩留言会获得点赞!