泛素化途径相关因子在调控调节性T细胞功能中的应用的制作方法
本发明涉及分子生物和生物医药领域。更具体而言,本发明涉及去泛素化途径相关因子在调控调节性T细胞功能中的应用。
背景技术:
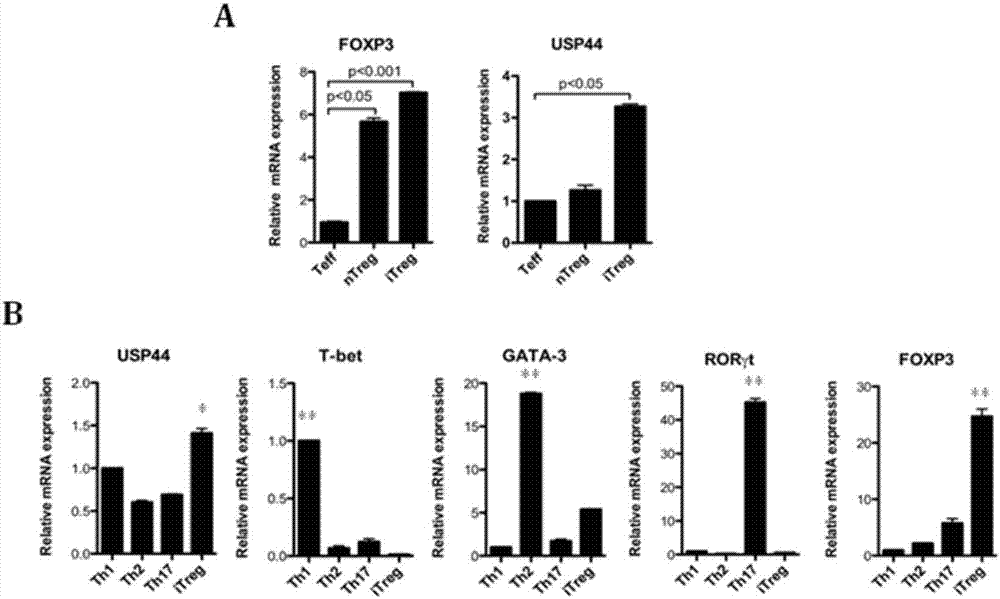
:调节性T细胞(RegulatoryTcells,Tregs)对机体免疫耐受和免疫稳态的维持具有重要作用,防止自身免疫病的发生,抗移植物排斥以及肿瘤免疫中具有重要作用。人叉头蛋白P3(humanforkheadboxP3,Foxp3)是Treg发育和功能维持的重要转录因子,对调控Treg的发育和功能起重要作用。在人体中,FOXP3功能缺失会引起免疫功能紊乱,引起多种内分泌失调,肠道病及X-性连锁综合征IPEX(Immunodysregulation,Polyendocrinopathy,andEnteropathy,X-linked)。在鼠中,FOXP3功能缺失会发展成淋巴组织增生性疾病(Scurfy),表现为严重皮炎、多器官淋巴细胞浸润及自身免疫溶血性贫血,原因为天然型Treg的缺失。将FOXP3基因人工整合到T细胞中表达可以获得Treg的表型。在小鼠中进行骨髓嵌合实验,发现FOXP3基因敲除的骨髓细胞无法发育成Treg,而野生型骨髓细胞则可以。而FOXP3基因3’非编码区的变更导致的FOXP3表达水平的显著下调,会严重削弱Treg的免疫抑制功能,说明FOXP3的表达水平对Treg的功能有直接影响。显示FOXP3是调节Treg细胞发育和功能的重要转录因子。转录因子FOXP3(ForkheadboxP3)不仅能作为CD4+CD25+Treg的标志分子,还是决定CD4+CD25+Treg功能的关键基因。一般情况下,根据发育和分化的位置不同,Treg可以分为两类:一种是在胸腺中经过阳性和阴性筛选发育的亚群为天然型Treg(naturalTreg,nTreg),另一种由外周血中CD4+T细胞在某些特定生理条件下诱导分化获得FOXP3表达和免疫抑制功能而来的,叫做诱导型Treg(inducedTreg,iTreg)。这二者在体内免疫调节中的作用机制是否有差异,目前还不是很清楚。目前的研究显示在自然型调节性T细胞(nTreg)中,FOXP3受多聚泛素化修饰和去泛素化调节,本发明人在梳理前人研究成果中发现,FOXP3的精细调节对iTreg在肿瘤微环境中的功能具有重要作用。但对诱导型调节性T细胞(iTreg)在炎症条件下调节机制的研究还尚不清楚。在体内炎症条件下,FOXP3+Treg功能的紧密调节对疾病的发展至关重要,研究这一调节的分子机制具有重要意义。为今后肿瘤治疗、移植排斥、病毒感染、免疫疾病及炎症反应等的临床治疗提供创新性线索及药物新靶点。本领域技术人员一直致力于开发调节免疫系统活性的技术,用于治疗免疫反应失调所引起的疾病。技术实现要素:本发明的目的在于提供一种泛素化途径相关因子在调控调节性T细胞功能中的应用。本发明的第一方面,提供了去泛素化酶或者去泛素化酶激动剂的用途,用于制备制剂或试剂盒,所述制剂或试剂盒用于:(1)增加FOXP3的稳定性;和/或(2)上调调节性T细胞活性或促进调节性T细胞的分化;和/或(3)上调调节性T细胞细胞因子的表达或活性;和/或(4)治疗和/或预防与调节性T细胞活性过低相关的疾病;和/或(5)促进iTreg的分化。在另一优选例中,所述的调节性T细胞活性过低是指调节性T细胞抑制炎症和免疫反应功能过低。在另一优选例中,所述的与调节性T细胞活性过低相关的疾病选自:自身免疫病,炎症反应、肿瘤和传染性疾病。在另一优选例中,所述自身免疫性疾病选自:多发性硬化症、风湿性关节炎、类风湿关节炎、风湿性心脏病、器官移植中的排异反应、系统性红斑狼疮、克罗恩氏病、溃疡性结肠炎、强直性脊柱炎、自身免疫性脑脊髓炎等自身免疫病,优选溃疡性结肠炎和自身免疫性脑脊髓炎。在另一优选例中,所述炎症反应选自:过敏性炎症、毛囊炎、扁桃体炎、肺炎、肝炎、肾炎、痤疮、哮喘、慢性炎症、慢性前列腺炎、肾小球肾炎、超敏反应、炎性肠道疾病、盆腔炎、再灌注损伤、血管炎或间质性膀胱炎。在另一优选例中,所述肿瘤选自:前列腺癌、乳腺癌、肝癌、胶质瘤、肠癌、子宫颈癌、非小细胞肺癌、肺癌、胰腺癌、胃癌、膀胱癌、皮肤癌、横纹肌癌、舌鳞癌、鼻咽癌、卵巢癌、胎盘绒毛癌、神经胶质瘤、淋巴瘤、白血病、直肠腺癌或黑色素瘤。在另一优选例中,所述传染性疾病选自:鼠疫、霍乱、传染性非典型肺炎、艾滋病、病毒性肝炎、脊髓灰质炎、人感染高致病性禽流感、麻疹、流行性出血热、狂犬病、流行性乙型脑炎、手足口病、登革热、炭疽、细菌性和阿米巴性痢疾、肺结核、伤寒和副伤寒、流行性脑脊髓膜炎、百日咳、白喉、新生儿破伤风、猩红热、布鲁氏菌病、淋病、梅毒、钩端螺旋体病、血吸虫病、疟疾、流行性感冒、流行性腮腺炎、风疹、急性出血性结膜炎、麻风病、流行性和地方性斑疹伤寒、黑热病、包虫病、丝虫病,除霍乱、细菌性和阿米巴性痢疾、伤寒和副伤寒以外的感染性腹泻病、或真菌感染。在另一优选例中,所述去泛素化酶选自下组中的一种或多种:USPs家族(Ubiquitin-specificproteases,USPs)和OUT家族。在另一优选例中,所述去泛素化酶选自下组中的一种或多种:USP44、USP2、USP3、USP4、USP5、USP7、USP10、USP12、USP14、USP17、USP18、USP21、USP22、USP30、USP39、YOD1、CYLD和A20;优选地,所述去泛素化酶为USP44、USP7或其组合。在另一优选例中,所述调节性T细胞选自下组中的一种或多种:nTreg、pTreg、和iTreg。在另一优选例中,所述调节性T细胞细胞因子选自下组中的一种或多种:FOXP3、IL-10、TGF-β和IL-2。在另一优选例中,所述去泛素化酶激动剂选自下组中的一种或多种:去泛素化酶转录促进剂和/或炎性细胞因子,优选地,所述炎性细胞因子为TGF-β。在另一优选例中,所述去泛素化酶转录促进剂是指,促进去泛素化酶进入细胞核的物质(如TGF-β、SMADs家族)。在另一优选例中,所述增加FOXP3的稳定性是通过以下方式实现:对FOXP3进行去泛素化。在另一优选例中,所述去泛素化为催化去除泛素K48偶联的泛素化修饰。在另一优选例中,所述去泛素化作用位点选自:FOXP3的K179、K250、K263、K268。在另一优选例中,所述去泛素化酶源自哺乳动物(选自:人)。在另一优选例中,所述USP44的氨基酸序列如SEQIDNO.:1所示;和/或所述USP7的氨基酸序列如SEQIDNO.:2所示。在另一优选例中,所述的去泛素化酶选自:野生型或突变型的去泛素化酶,也选自:具有与野生型去泛素化酶具有相同功能的去泛素化酶的活性片段或去泛素化酶的衍生物。在另一优选例中,所述去泛素化酶的衍生物选自:经修饰的去泛素化酶分子、氨基酸序列与天然去泛素化酶同源且具有天然去泛素化酶活性的蛋白分子、去泛素化酶的二聚体或多聚体、含有去泛素化酶氨基酸序列的融合蛋白。在另一优选例中,所述经修饰的去泛素化酶是PEG化的去泛素化酶。在另一优选例中,所述“氨基酸序列与天然去泛素化酶同源且具有天然去泛素化酶活性的蛋白分子”是指其氨基酸序列与野生型氨基酸序列相比(如对于USP44而言,与SEQIDNO.:1相比),具有≥85%的同源性,较佳地≥90%的同源性,更佳地≥95%的同源性,最佳地≥98%同源性;并且具有天然去泛素化酶活性的蛋白分子。在另一优选例中,所述与调节性T细胞活性相关的疾病是指与调节性T细胞活性过高或过低相关的疾病或症状。在另一优选例中,所述与调节性T细胞活性相关的疾病选自:肿瘤和传染性疾病。在另一优选例中,所述的制剂选自:药物组合物、保健品组合物、食品组合物、疫苗组合物或实验试剂。本发明的第二方面,提供了去泛素化酶拮抗剂的用途,用于制备制剂或试剂盒,所述制剂或试剂盒用于:(1)降低FOXP3的稳定性;和/或(2)下调调节性T细胞活性或抑制调节性T细胞的分化;和/或(3)下调调节性T细胞细胞因子的表达或活性;和/或(4)治疗和/或预防与调节性T细胞活性过高相关的疾病;和/或(5)上调FOXP3的表达,增强Treg的免疫抑制功能;和/或(6)治疗和/或预防与调节性T细胞活性相关的疾病。在另一优选例中,所述的与调节性T细胞活性过高相关的疾病选自下组:肿瘤和传染性疾病。在另一优选例中,所述肿瘤选自:前列腺癌、乳腺癌、肝癌、胶质瘤、肠癌、子宫颈癌、非小细胞肺癌、肺癌、胰腺癌、胃癌、膀胱癌、皮肤癌、横纹肌癌、舌鳞癌、鼻咽癌、卵巢癌、胎盘绒毛癌、神经胶质瘤、淋巴瘤、白血病、直肠腺癌或黑色素瘤。在另一优选例中,所述传染性疾病选自:鼠疫、霍乱、传染性非典型肺炎、艾滋病、病毒性肝炎、脊髓灰质炎、人感染高致病性禽流感、麻疹、流行性出血热、狂犬病、流行性乙型脑炎、手足口病、登革热、炭疽、细菌性和阿米巴性痢疾、肺结核、伤寒和副伤寒、流行性脑脊髓膜炎、百日咳、白喉、新生儿破伤风、猩红热、布鲁氏菌病、淋病、梅毒、钩端螺旋体病、血吸虫病、疟疾、流行性感冒、流行性腮腺炎、风疹、急性出血性结膜炎、麻风病、流行性和地方性斑疹伤寒、黑热病、包虫病、丝虫病,除霍乱、细菌性和阿米巴性痢疾、伤寒和副伤寒以外的感染性腹泻病、或真菌感染。在另一优选例中,所述去泛素化酶拮抗剂选自:抗体、sh-RNA、miRNA、反义寡核苷酸、化学抑制剂或其组合。在另一优选例中,所述拮抗剂选自:抗USP44抗体、抗USP7抗体、shUSP44(短发夹RNA)、shUSP7(短发夹RNA)、针对USP44或USP7的反义寡核苷酸、USP44或USP7的化学抑制剂。在另一优选例中,所述化学抑制剂为:10-羟基喜树碱(分子式:C20H16N2O5,10-hydroxycamptothecin,10-HCPT)。在另一优选例中,所述调节性T细胞选自:自然调节性T细胞(nTreg)和诱导产生的适应性调节性T细胞(iTreg)。在另一优选例中,所述与调节性T细胞活性相关的疾病选自下组:癌症,病毒感染,自身免疫病,优选癌症。本发明的第三方面,提供了一种用于增加FOXP3的稳定性的组合物,所述组合物选自:去泛素化酶或其衍生物,和/或去泛素化酶激动剂。在另一优选例中,所述去泛素化酶激动剂如上所述。在另一优选例中,所述组合物还含有药学上可接受的载体。在另一优选例中,所述组合物的剂型选自:固态制剂、液态制剂,较佳地为干粉或溶液形式。在另一优选例中,所述的组合物为药物组合物、保健品组合物或疫苗组合物。本发明的第四方面,提供了一种分离的复合物,所述复合物为去泛素化酶和FOXP3相结合所形成的复合物。在另一优选例中,所述复合物为二元复合物。在另一优选例中,所述复合物的分子量≥80KD;优选地所述复合物的分子量≥100KD。在另一优选例中,所述复合物的分子量为100KD-500KD;优选地为100KD-200KD。本发明的第五方面,提供了本发明第四方面所述蛋白复合物的应用,用于筛选药物或化合物,所述药物或化合物促进或抑制去泛素化酶和FOXP3形成所述的复合物。在另一优选例中,当应用所述复合物筛选药物时,所述应用包括步骤:(a)在测试组中,在待测物质存在下,培养调节性T细胞,并且设置无待测物质的对照组;(b)检测测试组中所述复合物的含量H1并与对照组中的复合物含量H0进行比较,其中当H1显著高于H0,则表示所述测试物为去泛素化酶的促进剂;当H1显著低于H0,则表示所述测试物为去泛素化酶的拮抗剂。在另一优选例中,当应用所述复合物筛选药物时,所述应用包括步骤:(a)在测试组中,将待测物质与(a)所述复合物和/或(b)去泛素化酶和FOXP3进行共孵育;并且设置无待测物质的对照组;(b)检测测试组中所述复合物的含量H1并与对照组中的复合物含量H0进行比较,其中当H1显著高于H0,则表示所述测试物为去泛素化酶的促进剂;当H1显著低于H0,则表示所述测试物为去泛素化酶的拮抗剂。本发明的第六方面,提供了一种去泛素化酶拮抗剂的用途,用于制备治疗肿瘤或传染性疾病的药物。在另一优选例中,所述去泛素化酶拮抗剂选自:抗体、sh-RNA、miRNA、反义寡核苷酸、化学抑制剂或其组合。在另一优选例中,所述拮抗剂选自:抗USP44抗体、抗USP7抗体、shUSP44(短发夹RNA)、shUSP7(短发夹RNA)、针对USP44或USP7的反义寡核苷酸、USP44或USP7的化学抑制剂。在另一优选例中,所述化学抑制剂为:10-羟基喜树碱(C20H16N2O5,10-hydroxycamptothecin,10-HCPT)。本发明的第七方面,提供了TGF-β在制备促进去泛素化酶转录的试剂中的用途。在另一优选例中,所述去泛素化酶选自下组中的一种或多种:USPs家族(Ubiquitin-specificproteases,USPs)和OUT家族。在另一优选例中,所述去泛素化酶选自下组中的一种或多种:USP44、USP2、USP3、USP4、USP5、USP7、USP10、USP12、USP14、USP17、USP18、USP21、USP22、USP30、USP39、YOD1、CYLD和A20;优选地,所述去泛素化酶为USP44、USP7或其组合。应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。附图说明图1显示了USP44在iTreg中高表达。其中,图1A用流式细胞技术(FACS)从人外周血细胞(PBMC)中分选出CD4+CD25-Teff细胞,CD4+CD25hiCD127loTreg细胞,CD45RA+CD4+naiveT细胞,在调节性T细胞诱导条件下得到诱导型调节性T细胞(iTreg),抽提RNA进行用特异的引物实时荧光定量PCR(q-RTPCR)或者用特异的抗体蛋白免疫印迹实验(WB),结果显示USP44在iTreg中高表达;图1B用流式细胞技术(FACS)从人外周血细胞(PBMC)中分选出CD45RA+CD4+naiveT细胞,在不同的辅助性T细胞诱导条件下得到不同的辅助性T细胞亚群和诱导型调节性T细胞(iTreg),抽提RNA进行用特异的引物实时荧光定量PCR(q-RTPCR)或者用特异的抗体蛋白免疫印迹实验(WB),结果显示USP44在iTreg中高表达;MS:MassSpectrometry,质谱分析。(*:p<0.05,**:p<0.005)。图2显示了USP44和FOXP3相互作用。其中,图2A在HEK293T细胞中外转表达FLAG标签USP44和MYC标签FOXP3,48h后收集细胞用相应抗体进行双向免疫共沉淀(IP)和蛋白免疫印记(IB)实验(FLAG-USP44表示将FLAG标签和USP44基因连在一起表达的带有FLAG标签的USP44蛋白,MYC-FOXP3a表示将MYC标签和FOXP3a(FOXP3基因不同剪切体中最长的一个)基因连在一起表达的带有MYC标签的FOXP3蛋白,下同)。图2B收集稳定表达HA-FOXP3的JurkatT细胞,用相应抗体进行双向免疫共沉淀和蛋白免疫印记实验(IP-USP44表示用USP44的特异识别抗体在细胞裂解液中对USP44蛋白进行富集,INPUT表示没有经过处理的细胞裂解液的上清,下同)。图2C从人外周血PBMC中分离得到T细胞体外诱导分化的iTreg,用相应抗体进行免疫共沉淀和蛋白免疫印记实验。图2D从人外周血PBMC中分离得到T细胞体外诱导分化成iTreg,用相应抗体进行免疫荧光实验。sAbs:secondaryantibodies,荧光二抗。图3显示了USP44稳定FOXP3蛋白。其中,图3A在HEK293T细胞中外转表达FLAG标签USP44(野生型WT和酶失活突变体C282S,质粒剂量0.5,1,1.5μg)和MYC标签FOXP3,48h后收集细胞用相应抗体进行蛋白免疫印记实验。图3B在HEK293T细胞中外转表达FLAG标签USP44(WT和C282S)和MYC标签FOXP3,分别用蛋白合成抑制剂CHX处理(0,4,8,12h),收集细胞用相应抗体进行蛋白免疫印记实验(WT表示野生型,CA表示USP44的酶活相关位点即氨基酸序列上的第282位的半胱氨酸被突变成了丝氨酸,其蛋白构向和疏水性均发生改变因而酶活降低,下同)。图3C,D从人外周血PBMC中分离得到T细胞体外诱导分化的iTreg,感染带有抗性筛选标记的慢病毒(shCK、shUSP44-1、shUSP44-2),72h后进行筛选,一周后收集细胞裂解,用相应抗体进行蛋白免疫印记实验和FACS分析。图中,shCK为Treg细胞中感染了没有任何靶向性的序列的包装病毒,因此是不会对任何基因的表达有影响的对照,shUSP44-1和shUSP44-2分别为Treg细胞中感染了对USP44基因有特殊靶向性的序列的包装病毒,1和2代表不同的序列,但都对USP44基因具有靶向性,根据同源沉默等原理,这种细胞中USP44基因被特异的敲低。(E)收集图3C中的细胞进行qRT-PCR检测相关基因的表达,此处所示为有代表性的一次独立实验结果。图4显示了USP44影响FOXP3对下游Il2基因的转录抑制。其中图4A在HEK293T细胞中外转包含人Il2基因启动子的荧光素酶报告基因质粒,转染效率内参Renilla,表达FLAG标签USP44(WT和C282S)或USP7或STUB1和MYC标签FOXP3,48h后收集细胞进行荧光素酶活性测定和用相应抗体进行蛋白免疫印记实验。图4B在HEK293T细胞中外转包含人Il2基因启动子的荧光素酶报告基因、Renilla、表达FLAG标签USP44(质粒剂量0.5,1,1.5μg)和MYC标签FOXP3,48h后收集细胞进行荧光素酶活性测定和用相应抗体进行蛋白免疫印记实验。图4C将HEK293T细胞感染带有抗性筛选标记的慢病毒(shCK、shUSP44-1、shUSP44-2),72h后进行筛选,一周后转染包含人Il2基因启动子的荧光素酶报告基因、Renilla和表达FOXP3或空载的质粒,48h后收集细胞裂解,进行荧光素酶活性测定实验,此处所示为有代表性的一次独立实验结果。图5显示USP44去除FOXP3与降解相关的K48偶联的多聚泛素化修饰。其中,图5A在HEK293T细胞中共转染表达USP44(WT)及突变体(C282S),MYC标签FOXP3和His标签的泛素蛋白(ubiquitin)的质粒,44h后加入MG13220μM,4h后收细胞裂解用Ni-NTA磁珠结合His标签进行泛素沉淀,然后用相应抗体检测蛋白表达及FOXP3的泛素化水平(His-ubi表示将6个His标签和泛素基因连在一起表达的带有His标签的泛素蛋白,ubi为泛素蛋白的简称)。图5B将HEK293T细胞感染带有抗性筛选标记的慢病毒(shCK、shUSP44-1、shUSP44-2),72h后进行筛选,一周后转染表达MYC标签FOXP3和His标签的泛素蛋白(ubiquitin)的质粒,44h后加入MG13220μM,4h后收细胞裂解用Ni-NTA磁珠结合His标签进行泛素沉淀,然后用相应抗体检测蛋白表达及FOXP3的泛素化水平。图5C在HEK293T细胞中共转染表达USP44,MYC标签FOXP3和His标签的泛素蛋白(ubiquitin)及其各种突变体的质粒,44h后加入MG13220μM,4h后收细胞裂解用Ni-NTA磁珠结合His标签进行泛素沉淀,然后用相应抗体检测蛋白表达及FOXP3的泛素化水平。图6显示FOXP3蛋白K179/250/263/268是USP44的去泛素化作用位点。其中,图6A将表达FOXP3野生型(WT)及其不同突变体与USP44蛋白的质粒共转染入HEK29T细胞中,48h后收细胞裂解用相应抗体进行蛋白检测。图6B共转染表达FOXP3(WT)及突变体(K179/250/263/268R,即4R),USP44和His标签的泛素蛋白(ubiquitin)的质粒,44h后加入MG13220μM,4h后收细胞裂解用Ni-NTA磁珠结合His标签进行泛素沉淀,然后用相应抗体检测蛋白表达及FOXP3的泛素化水平。图6C共转染表达FOXP3(WT)及突变体(K179/250/263/268R,即4R和所有K突变体20R)和USP44蛋白的质粒,然后用相应抗体检测蛋白表达及FOXP3的泛素化水平(K为赖氨酸的简称)。图7显示TGF-β信号通过上调USP44转录水平促进iTreg分化。其中。图7A将包含USP44基因的启动子序列+17-(-1712)的荧光素酶报告基因载体转染到JurkatT细胞中,36h后用佛波酯(PMA)和离子霉素(Ionomycin)及不同浓度的TGF-β刺激不同时间,收细胞裂解进行荧光素酶活性检测,及相应抗体检测p-SMAD2和SMAD2蛋白水平(P+I为PMA和Inomycin共同处理,用于模拟TCR信号通路刺激,PMA为佛波酯,ionomycin是离子霉素)。图7B,C从PBMC分离的Treg体外扩增,分离T细胞体外诱导分化0,1,2,3,4,5d产生的iTreg,抽提RNA进行qRT-PCR检测相应基因mRNA表达水平,同时通过免疫印记实验用特定抗体检测USP44,USP7,STUB1,Hsp70和FOXP3的蛋白水平,此处所示为有代表性的一次实验结果。图8显示STUB1通过增强USP44多泛素化修饰来降解USP44。其中,图8A将稳定表达USP44蛋白的JurkatT细胞(1×106)先用PMA(50ng/ml)和Ionomycin(1μM)刺激4h,再分别用不同温度刺激不同时间,或用LPS(1μg/ml)刺激不同时间,然后收集细胞裂解用相应抗体进行蛋白免疫印记实验。图8B从人外周血PBMC中分离得到T细胞体外诱导分化的iTreg,加入100U/mlIL-2,分别用(LPS(1μg/ml),IL-6(20ng/ml),IL-1β(10ng/ml))24h,收集细胞裂解,用相应抗体进行蛋白免疫印记实验。图8C在HEK293T细胞中外转表USP44和MYC标签STUB1(0.5,1,1.5μg)的质粒,48h后收集细胞用相应抗体进行蛋白免疫印记实验。图8D在HEK293T细胞中外转表达USP44和MYC标签STUB1(WT,H260Q,K30A)的质粒,48h后收集细胞用相应抗体进行蛋白免疫印记实验。图8E在HEK293T细胞中外转表达FLAG标签USP44和MYC标签STUB1或FOXP3的质粒,48h后收集细胞用相应抗体进行免疫共沉淀和蛋白免疫印记实验。图8F在HEK293T细胞中外转表达USP44和MYC标签STUB1(WT,H260Q,K30A)的质粒,48h后收集细胞用相应抗体进行免疫共沉淀和蛋白免疫印记实验。图8G在HEK293T细胞中共转染表达USP44,STUB1和HA标签的泛素蛋白(ubiquitin)的质粒,44h后加入MG13220μM,4h后收细胞裂解用相应抗体进行免疫共沉淀和蛋白免疫印记实验检测蛋白表达及USP44的泛素化水平。图9显示USP44和USP7协同作用稳定FOXP3。其中,图9A在HEK293T细胞中外转表达MYC标签USP44和FLAG标签USP7的质粒,48h后收集细胞用相应抗体进行双向免疫共沉淀和蛋白免疫印记实验。图9B在HEK293T细胞中外转表达USP44,MYC标签FOXP3和FLAG标签USP7(0.5,1,1.5μg)的质粒,48h后收集细胞用相应抗体进行免疫共沉淀和蛋白免疫印记实验。图9C在HEK293T细胞中共转染表达FLAG标签USP44,USP7,MYC标签FOXP3和His标签的泛素蛋白(ubiquitin)的质粒,44h后加入MG13220μM,4h后收细胞裂解用相应抗体进行免疫共沉淀和蛋白免疫印记实验检测蛋白表达及FOXP3的泛素化水平。图9D在HEK293T细胞中外转带有shCK或shSTUB1的慢病毒包装质粒,1天后,再转入表达USP44和MYC标签USP7的质粒,48h后收集细胞用相应抗体进行蛋白免疫印记实验。图9E在HEK293T细胞中外转表达FLAG标签USP44(WT,C282S)和MYC标签STUB1(WT,H260Q)或USP7(WT,C223S)的质粒,48h后收集细胞用相应抗体进行蛋白免疫印记实验。图10显示USP44基因敲除小鼠中分离的Treg,其FOXP3的表达和Treg的抑制功能明显受到抑制,分离的T细胞在免疫缺陷小鼠体内进行分化iTreg也明显受到了抑制,IFN-γ和IL-17的表达则显著上调。其中,图10A将1×106CD4+T细胞(CD62LhighCD25-)单独或者与野生型Treg或USP44基因敲除小鼠中分离的Treg细胞4×105打入RAG2-/-免疫缺陷小鼠体内制造肠炎模型,在一定时间(如图)记录其体重并做曲线图(N=6),对照组设计如图。图10B,C取图10A中打入细胞8周后的肠炎小鼠模型的远端肠组织进行苏木精-伊红(H/E)染色,并进行组织切片显微镜下白光(100×)分析,并进行疾病评估打分做出柱状图。图10D将与T细胞和野生型Treg和USP44基因敲除小鼠中分离的Treg细胞一同打入免疫缺陷小鼠体内,一定时间后取小鼠的黏膜淋巴结(mLN),外周淋巴结(pLN),脾脏(SPL)进行分离Treg细胞(CD4+/Thy1.1+),用特异抗体进行FACS分析FOXP3的表达,对照组设计如图。图10E将与不同Treg的一同打入免疫缺陷小鼠体内的T细胞,在一定时间取出并用特异抗体(CD4+/Thy1.2+)进行FACS分析IFN-γ和IL-17的表达,对照组设计如图。图11显示USP44和FOXP3在HCV阳性的肝癌病人样本的癌组织中共同高表达。其中,图11A在HCV阳性的肝癌病人样本的癌组织中用USP44抗体进行免疫组化实验,发现USP44特异表达在肿瘤间质中。图11B统计信息显示在17例由HCV感染最终导致肝癌(HCC)的病人的癌组织和癌旁及正常组织中,USP44和FOXP3在其中11例样本的癌组织中共同高表达。图11C免疫组化实验结果显示在17例由HCV感染最终导致肝癌(HCC)的病人的癌组织和癌旁及正常组织中,USP44和FOXP3在其中11例样本的癌组织中共同高表达。图12显示10-羟基喜树碱(10-HCPT)可以特异的抑制USP44对FOXP3蛋白的稳定。在HEK293T细胞中共转染FLAG标签USP44和MYC标签FOXP3,并用不同浓度的10-羟基喜树碱处理,DMSO作为对照,结果显示,10-羟基喜树碱(10-HCPT)可以特异的抑制USP44对FOXP3蛋白的稳定,且呈剂量依赖。具体实施方式本发明人通过广泛而深入的研究,意外的发现,去泛素化酶对于上调FOXP3的稳定性具有显著影响,进而能够上调调节性T细胞活性及其分化并且能够上调调节性T细胞细胞因子的表达,在此基础上完成了本发明。术语去泛素化酶及其制备方法迄今为止已经发现大约100种去泛素化酶,主要功能是通过水解泛素上羧基末端残基,将泛素分子从连接有泛素的蛋白上水解下来。根据其结构和功能特点可分为五个家族:泛素羧基末端水解酶家族(UbiquitinC-terminalhydrolases,UCHs)、泛素特异性水解酶家族(Ubiquitin-specificproteases,USPs)、卵巢肿瘤相关蛋白酶(Ovariantumor,OTU)、Ataxin-3(含Josephin结构域)、MPN(+)/JAMM蛋白酶(JAB1/MPN/Mov34metlloenzymedomainzinc-dependentmetalloproteasefamily)。目前发现去泛素化酶功能包括:①去泛素化酶通过共同翻译的方式激活泛素前蛋白。泛素作为一个前蛋白表达并融合到核糖体蛋白或线性多聚泛素上,同时多聚泛素基因产物也必须去除碳端多余的残基才能活化泛素。②去泛素化可回收被包含巯基酯中间体的小细胞亲核试剂捕获的泛素,从而参与蛋白的泛素化。③去泛素化酶反向去除靶蛋白的泛素化或泛素样修饰。去泛素化酶拮抗蛋白的泛素化,类似于激酶/磷酸酶调节通路中磷酸酶的作用。④去泛素酶负责来自非锚定多聚泛素链上单泛素的再生。去泛素化酶USP44专门去除底物蛋白的单聚或者多聚泛素化并阻止其进入蛋白酶体降解或者影响其发挥功能,从而影响肿瘤发生,细胞凋亡,免疫反应等活动。研究发现USP44可以通过靶作用与细胞周期蛋白CDC20从而抑制细胞分裂,也可以通过去除组蛋白单泛素化来影响干细胞分化。但是,USP44对免疫系统的影响仍然不清楚。而去泛素化酶USP7通过稳定p53影响肿瘤细胞生长。本研究发现USP7可以稳定USP44,并和USP44功能上具有协同作用。因此,深入研究调节性T细胞及转录因子FOXP3、IL-10、IL-2和TGF-β中的生化活性、生理功能及其调控的分子机理,对于治疗性控制人体内调节性T细胞的免疫活性以及基于调节性T细胞的免疫治疗皆至关重要。这为将基础免疫研究转化为临床研究,以及理解人类自身免疫性疾病,肿瘤和传染性疾病提供了新的研究命题与挑战,有望成为新的治疗靶点。本发明所述的去泛素化酶选自:野生型或突变型的去泛素化酶,也选自:具有与野生型去泛素化酶具有相同功能的去泛素化酶的活性片段或去泛素化酶的衍生物。在另一优选例中,所述去泛素化酶的衍生物选自:经修饰的去泛素化酶分子、氨基酸序列与天然去泛素化酶同源且具有天然去泛素化酶活性的蛋白分子、去泛素化酶的二聚体或多聚体、含有去泛素化酶氨基酸序列的融合蛋白。如本发明所用,去泛素化酶“USP44”或“USP7”是指一种蛋白质,该蛋白质(a)具有与(FrankStegmeier,etal.Nature.2007)、(RobertaVisconti,etal.NatCommun.2012)(JorgvanLoosdregt,etal.Immunity.2013)中描述的“USP44”或“USP7”基本相同的氨基酸序列和(b)具有与天然“USP44”或“USP7”相同的生物学活性,且具有基本相同的氨基酸序列。本发明的“USP44”或“USP7”包括,但不限于:人“USP44”或“USP7”、重组人“USP44”或“USP7”、鼠“USP44”或“USP7”和/或重组鼠“USP44”或“USP7”。在本发明的一些实施方式中,USP44的核苷酸序列为:ATGCTAGCAATGGATACGTGCAAACATGTTGGGCAGCTGCAGCTTGCTCAAGACCATTCCAGCCTCAACCCTCAGAAATGGCACTGTGTGGACTGCAACACGACCGAGTCCATTTGGGCTTGCCTTAGCTGCTCCCATGTTGCCTGTGGAAGATATATTGAAGAGCATGCACTCAAGCACTTTCAAGAAAGCAGTCATCCTGTTGCATTGGAGGTGAATGAGATGTACGTTTTTTGTTACCTTTGTGATGATTATGTTCTGAATGATAACACAACTGGAGACCTGAAGTTACTACGACGTACATTAAGTGCCATCAAAAGTCAAAATTATCACTGCACAACTCGTAGTGGGAGGTTTTTACGGTCCATGGGTACAGGTGATGATTCTTATTTCTTACATGACGGTGCCCAATCTCTGCTTCAAAGTGAAGATCAACTGTATACTGCTCTTTGGCACAGGAGAAGGATACTAATGGGTAAAATCTTTCGAACATGGTTTGAACAATCACCCATTGGAAGAAAAAAGCAAGAAGAACCATTTCAGGAAAAAATAGTAGTAAAAAGAGAAGTAAAGAAAAGACGGCAGGAATTGGAGTATCAAGTTAAAGCAGAATTGGAAAGTATGCCTCCAAGAAAGAGTTTACGTTTACAAGGGCTCGCTCAGTCGACCATAATAGAAATAGTTTCTGTTCAGGTGCCAGCACAAACGCCAGCATCACCAGCAAAAGATAAAGTACTCTCTACCTCAGAAAATGAAATATCTCAAAAAGTCAGTGACTCCTCAGTTAAACGAAGGCCAATAGTAACTCCTGGTGTAACAGGATTGAGAAATTTGGGAAATACTTGCTATATGAATTCTGTTCTTCAGGTGTTGAGTCATTTACTTATTTTTCGACAATGTTTTTTAAAGCTTGATCTGAACCAATGGCTGGCTATGACTGCTAGCGAGAAGACAAGATCTTGTAAGCATCCACCAGTCACAGATACAGTAGTATATCAAATGAATGAATGTCAGGAAAAAGATACAGGTTTTGTTTGCTCCAGACAATCAAGTCTGTCATCAGGACTAAGTGGTGGAGCATCAAAAGGTAGAAAGATGGAACTTATTCAGCCAAAGGAGCCAACTTCACAGTACATTTCTCTTTGTCATGAATTGCATACTTTGTTCCAAGTCATGTGGTCTGGAAAGTGGGCGTTGGTCTCACCATTTGCTATGCTACACTCAGTGTGGAGACTCATTCCTGCCTTTCGTGGTTACGCCCAACAAGACGCTCAGGAATTTCTTTGTGAACTTTTAGATAAAATACAACGTGAATTAGAGACAACTGGTACCAGTTTACCAGCTCTTATCCCCACTTCTCAAAGGAAACTCATCAAACAAGTTCTGAATGTTGTAAATAACATTTTTCATGGACAACTTCTTAGTCAGGTTACATGTCTTGCATGTGACAACAAATCAAATACCATAGAACCTTTCTGGGACTTGTCATTGGAGTTTCCAGAAAGGTATCAATGCAGTGGAAAAGATATTGCTTCCCAGCCATGTCTGGTTACTGAAATGTTGGCCAAATTTACAGAAACTGAAGCTTTAGAAGGAAAAATCTACGTATGTGACCAGTGTAACTCAAAGCGTAGAAGGTTTTCCTCCAAACCAGTTGTACTCACAGAAGCCCAGAAACAACTTATGATATGCCACCTACCTCAGGTTCTCAGACTGCACCTCAAACGATTCAGGTGGTCAGGACGTAATAACCGAGAGAAGATTGGTGTTCATGTTGGCTTTGAGGAAATCTTAAACATGGAGCCCTATTGCTGCAGGGAGACCCTGAAATCCCTCAGACCAGAATGCTTTATCTATGACTTGTCCGCGGTGGTGATGCACCATGGGAAAGGATTTGGCTCAGGGCACTACACTGCCTACTGCTATAATTCTGAAGGAGGGTTCTGGGTACACTGCAATGATTCCAAACTAAGCATGTGCACTATGGATGAAGTATGCAAGGCTCAAGCTTATATCTTGTTTTATACCCAACGAGTTACTGAGAATGGACATTCTAAACTTTTGCCTCCAGAGCTCCTGTTGGGGAGCCAACATCCCAATGAAGACGCTGATACCTCGTCTAATGAAATCCTTAGCTGA(SEQIDNO.1)USP44的氨基酸序列为:MLAMDTCKHVGQLQLAQDHSSLNPQKWHCVDCNTTESIWACLSCSHVACGRYIEEHALKHFQESSHPVALEVNEMYVFCYLCDDYVLNDNTTGDLKLLRRTLSAIKSQNYHCTTRSGRFLRSMGTGDDSYFLHDGAQSLLQSEDQLYTALWHRRRILMGKIFRTWFEQSPIGRKKQEEPFQEKIVVKREVKKRRQELEYQVKAELESMPPRKSLRLQGLAQSTIIEIVSVQVPAQTPASPAKDKVLSTSENEISQKVSDSSVKRRPIVTPGVTGLRNLGNTCYMNSVLQVLSHLLIFRQCFLKLDLNQWLAMTASEKTRSCKHPPVTDTVVYQMNECQEKDTGFVCSRQSSLSSGLSGGASKGRKMELIQPKEPTSQYISLCHELHTLFQVMWSGKWALVSPFAMLHSVWRLIPAFRGYAQQDAQEFLCELLDKIQRELETTGTSLPALIPTSQRKLIKQVLNVVNNIFHGQLLSQVTCLACDNKSNTIEPFWDLSLEFPERYQCSGKDIASQPCLVTEMLAKFTETEALEGKIYVCDQCNSKRRRFSSKPVVLTEAQKQLMICHLPQVLRLHLKRFRWSGRNNREKIGVHVGFEEILNMEPYCCRETLKSLRPECFIYDLSAVVMHHGKGFGSGHYTAYCYNSEGGFWVHCNDSKLSMCTMDEVCKAQAYILFYTQRVTENGHSKLLPPELLLGSQHPNEDADTSSNEILS(SEQIDNO.2)在本发明的一些实施方式中,USP7的核苷酸序列为:ATGAACCACCAGCAGCAGCAGCAGCAGCAGAAAGCGGGCGAGCAGCAGTTGAGCGAGCCCGAGGACATGGAGATGGAAGCGGGAGATACAGATGACCCACCAAGAATTACTCAGAACCCTGTGATCAATGGGAATGTGGCCCTGAGTGATGGACACAACACCGCGGAGGAGGACATGGAGGATGACACCAGTTGGCGCTCCGAGGCAACCTTTCAGTTCACTGTGGAGCGCTTCAGCAGACTGAGTGAGTCGGTCCTTAGCCCTCCGTGTTTTGTGCGAAATCTGCCATGGAAGATTATGGTGATGCCACGCTTTTATCCAGACAGACCACACCAAAAAAGCGTAGGATTCTTTCTCCAGTGCAATGCTGAATCTGATTCCACGTCATGGTCTTGCCATGCACAAGCAGTGCTGAAGATAATAAATTACAGAGATGATGAAAAGTCGTTCAGTCGTCGTATTAGTCATTTGTTCTTCCATAAAGAAAATGATTGGGGATTTTCCAATTTTATGGCCTGGAGTGAAGTGACCGATCCTGAGAAAGGATTTATAGATGATGACAAAGTTACCTTTGAAGTCTTTGTACAGGCGGATGCTCCCCATGGAGTTGCGTGGGATTCAAAGAAGCACACAGGCTACGTCGGCTTAAAGAATCAGGGAGCGACTTGTTACATGAACAGCCTGCTACAGACGTTATTTTTCACGAATCAGCTACGAAAGGCTGTGTACATGATGCCAACCGAGGGGGATGATTCGTCTAAAAGCGTCCCTTTAGCATTACAAAGAGTGTTCTATGAATTACAGCATAGTGATAAACCTGTAGGAACAAAAAAGTTAACAAAGTCATTTGGGTGGGAAACTTTAGATAGCTTCATGCAACATGATGTTCAGGAGCTTTGTCGAGTGTTGCTCGATAATGTGGAAAATAAGATGAAAGGCACCTGTGTAGAGGGCACCATACCCAAATTATTCCGCGGCAAAATGGTGTCCTATATCCAGTGTAAAGAAGTAGACTATCGGTCTGATAGAAGAGAAGATTATTATGATATCCAGCTAAGTATCAAAGGAAAGAAAAATATATTTGAATCATTTGTGGATTATGTGGCAGTAGAACAGCTCGATGGGGACAATAAATACGACGCTGGGGAACATGGCTTACAGGAAGCAGAGAAAGGTGTGAAATTCCTAACATTGCCACCAGTGTTACATCTACAACTGATGAGATTTATGTATGACCCTCAGACGGACCAAAATATCAAGATCAATGATAGGTTTGAATTCCCAGAGCAGTTACCACTTGATGAATTTTTGCAAAAAACAGATCCTAAGGACCCTGCAAATTATATTCTTCATGCAGTCCTGGTTCATAGTGGAGATAATCATGGTGGACATTATGTGGTTTATCTAAACCCCAAAGGGGATGGCAAATGGTGTAAATTTGATGACGACGTGGTGTCAAGGTGTACTAAAGAGGAAGCAATTGAGCACAATTATGGGGGTCACGATGACGACCTGTCTGTTCGACACTGCACTAATGCTTACATGTTAGTCTACATCAGGGAATCAAAACTGAGTGAAGTTTTACAGGCGGTCACCGACCATGATATTCCTCAGCAGTTGGTGGAGCGATTACAAGAAGAGAAAAGGATCGAGGCTCAGAAGCGGAAGGAGCGGCAGGAAGCCCATCTCTATATGCAAGTGCAGATAGTCGCAGAGGACCAGTTTTGTGGCCACCAAGGGAATGACATGTACGATGAAGAAAAAGTGAAATACACTGTGTTCAAAGTATTGAAGAACTCCTCGCTTGCTGAGTTTGTTCAGAGCCTCTCTCAGACCATGGGATTTCCACAAGATCAAATTCGATTGTGGCCCATGCAAGCAAGGAGTAATGGAACAAAACGACCAGCAATGTTAGATAATGAAGCCGACGGCAATAAAACAATGATTGAGCTCAGTGATAATGAAAACCCTTGGACAATATTCCTGGAAACAGTTGATCCCGAGCTGGCTGCTAGTGGAGCGACCTTACCCAAGTTTGATAAAGATCATGATGTAATGTTATTTTTGAAGATGTATGATCCCAAAACGCGGAGCTTGAATTACTGTGGGCATATCTACACACCAATATCCTGTAAAATACGTGACTTGCTCCCAGTTATGTGTGACAGAGCAGGATTTATTCAAGATACTAGCCTTATCCTCTATGAGGAAGTTAAACCGAATTTAACAGAGAGAATTCAGGACTATGACGTGTCTCTTGATAAAGCCCTTGATGAACTAATGGATGGTGACATCATAGTATTTCAGAAGGATGACCCTGAAAATGATAACAGTGAATTACCCACCGCAAAGGAGTATTTCCGAGATCTCTACCACCGCGTTGATGTCATTTTCTGTGATAAAACAATCCCTAATGATCCTGGATTTGTGGTTACGTTATCAAATAGAATGAATTATTTTCAGGTTGCAAAGACAGTTGCACAGAGGCTCAACACAGATCCAATGTTGCTGCAGTTTTTCAAGTCTCAAGGTTATAGGGATGGCCCAGGTAATCCTCTTAGACATAATTATGAAGGTACTTTAAGAGATCTTCTACAGTTCTTCAAGCCTAGACAACCTAAGAAACTTTACTATCAGCAGCTTAAGATGAAAATCACAGACTTTGAGAACAGGCGAAGTTTTAAATGTATATGGTTAAACAGCCAATTTAGGGAAGAGGAAATAACACTATATCCAGACAAGCATGGGTGTGTCCGGGACCTGTTAGAAGAATGTAAAAAGGCCGTGGAGCTTGGGGAGAAAGCATCAGGGAAACTTAGGCTGCTAGAAATTGTAAGCTACAAAATCATTGGTGTTCATCAAGAAGATGAACTATTAGAATGTTTATCTCCTGCAACGAGCCGGACGTTTCGAATAGAGGAAATCCCTTTGGACCAGGTGGACATAGACAAAGAGAATGAGATGCTTGTCACAGTGGCGCATTTCCACAAAGAGGTCTTCGGAACGTTCGGAATCCCGTTTTTGCTGAGGATACACCAGGGCGAGCATTTTCGAGAAGTGATGAAGCGAATCCAGAGCCTGCTGGACATCCAGGAGAAGGAGTTTGAGAAGTTTAAATTTGCAATTGTAATGATGGGCCGACACCAGTACATAAATGAAGACGAGTATGAAGTAAATTTGAAAGACTTTGAGCCACAGCCCGGTAATATGTCTCATCCTCGGCCTTGGCTAGGGCTCGACCACTTCAACAAAGCCCCAAAGAGGAGTCGCTACACTTACCTTGAAAAGGCCATTAAAATCCATAACTGA(SEQIDNO.3)USP7氨基酸序列为:MNHQQQQQQQKAGEQQLSEPEDMEMEAGDTDDPPRITQNPVINGNVALSDGHNTAEEDMEDDTSWRSEATFQFTVERFSRLSESVLSPPCFVRNLPWKIMVMPRFYPDRPHQKSVGFFLQCNAESDSTSWSCHAQAVLKIINYRDDEKSFSRRISHLFFHKENDWGFSNFMAWSEVTDPEKGFIDDDKVTFEVFVQADAPHGVAWDSKKHTGYVGLKNQGATCYMNSLLQTLFFTNQLRKAVYMMPTEGDDSSKSVPLALQRVFYELQHSDKPVGTKKLTKSFGWETLDSFMQHDVQELCRVLLDNVENKMKGTCVEGTIPKLFRGKMVSYIQCKEVDYRSDRREDYYDIQLSIKGKKNIFESFVDYVAVEQLDGDNKYDAGEHGLQEAEKGVKFLTLPPVLHLQLMRFMYDPQTDQNIKINDRFEFPEQLPLDEFLQKTDPKDPANYILHAVLVHSGDNHGGHYVVYLNPKGDGKWCKFDDDVVSRCTKEEAIEHNYGGHDDDLSVRHCTNAYMLVYIRESKLSEVLQAVTDHDIPQQLVERLQEEKRIEAQKRKERQEAHLYMQVQIVAEDQFCGHQGNDMYDEEKVKYTVFKVLKNSSLAEFVQSLSQTMGFPQDQIRLWPMQARSNGTKRPAMLDNEADGNKTMIELSDNENPWTIFLETVDPELAASGATLPKFDKDHDVMLFLKMYDPKTRSLNYCGHIYTPISCKIRDLLPVMCDRAGFIQDTSLILYEEVKPNLTERIQDYDVSLDKALDELMDGDIIVFQKDDPENDNSELPTAKEYFRDLYHRVDVIFCDKTIPNDPGFVVTLSNRMNYFQVAKTVAQRLNTDPMLLQFFKSQGYRDGPGNPLRHNYEGTLRDLLQFFKPRQPKKLYYQQLKMKITDFENRRSFKCIWLNSQFREEEITLYPDKHGCVRDLLEECKKAVELGEKASGKLRLLEIVSYKIIGVHQEDELLECLSPATSRTFRIEEIPLDQVDIDKENEMLVTVAHFHKEVFGTFGIPFLLRIHQGEHFREVMKRIQSLLDIQEKEFEKFKFAIVMMGRHQYINEDEYEVNLKDFEPQPGNMSHPRPWLGLDHFNKAPKRSRYTYLEKAIKIHN(SEQIDNO.4)术语“基本相同的氨基酸序列”是指序列相同或由一个或多个氨基酸改变(缺失、增加、取代)引起的不同,但这种改变基本上不降低其生物学活性。任何符合“基本相同”要求的去泛素化酶均包括在本发明内,无论它是糖基化的(即来源于天然的或来源于真核生物表达系统的)或是非糖基化的(即来源于原核生物表达系统或化学合成的)。“去泛素化酶”还包括PEG化的去泛素化酶以及共价修饰的去泛素化酶蛋白质。例如,可用各种活化的分子量为5,000~100,000的聚乙二醇(PEG)修饰以使IL-17高分子化,延长其半衰期。具体操作可参见Greenwaldetal.,Bioorg.Med.Chem.Lett.1994,4,2465;Calicetietal.,ILFarmaco,1993,48,919;ZalipskyandLee,《聚乙二醇化学:生物技术与生物医学应用》,J.M.Harris编,PlenumPress,N.Y.,1992。本发明的去泛素化酶可用基因重组技术克隆表达的。表达的宿主细胞包括原核细胞、酵母细胞或者高等真核生物细胞。除了原核细胞,真核细胞如丝状真菌(filamentousfungi)或酵母菌(yeast)等同样适用于表达或者克隆本发明的白介素-17。用于表达糖基化的本发明的去泛素化酶的宿主细胞来源于多细胞有机体。无脊椎动物细胞的例子包括昆虫细胞如DrosophilaS2和SpodopteraSf9,植物细胞。适用的哺乳动物宿主细胞的例子包括中华仓鼠卵巢细胞(CHO),COS细胞。本领域的普通技术人员应知如何选择合适的宿主细胞。上述宿主细胞经去泛素化酶表达载体或克隆载体转染或者转化后可在传统的营养基(nutrientmedia)中培养,所述营养基经修饰后适于诱导启动子(promoter)、选择性转化体(selectingtransformant)或者扩增去泛素化酶编码基因序列。培养条件如培养基、温度、pH等的选择对本领域的普通技术人员来说则是应知的。如何使细胞培养繁殖力最大化的一般原则、方案以及操作技术可参见MammalianCellBiotechnology:aPracticalApproach,M.Butler,ed.(IRLPress,1991)andSambrooketal.,supra。本发明的去泛素化酶不但可以通过基因重组直接表达,也可以通过与异种多肽形成融和多肽的方式生产,后者可以是一段位于成熟蛋白质或多肽N端的信号序列,也可以是位于成熟蛋白质或多肽N端的具有特异性切割位点的其他多肽片段。去泛素化酶二聚体及其制备方法编码本发明去泛素化酶二聚体或融合蛋白的DNA序列,可以全部人工合成。也可用PCR扩增或合成的方法获得去泛素化酶第一单体和/或去泛素化酶第二单体的编码DNA序列,然后将其拼接在一起,形成编码本发明融合蛋白的DNA序列。为了提高宿主细胞的表达量,可以对去泛素化酶二聚体编码序列进行改造,例如采用宿主细胞偏好的密码子,消除不利于基因转录及翻译的序列。在本发明中,可以采用酵母细胞或哺乳动物细胞偏好的密码子,并采用计算机DNA软件对去泛素化酶二聚体基因进行检测,排除在基因中不利于基因转录及翻译的序列,包括内含子剪切位点,转录终止序列等。在获得了编码本发明新融合蛋白的DNA序列之后,将其连入合适的表达载体,再转入合适的宿主细胞。最后,培养转化后的宿主细胞,通过分离纯化得到本发明的新的融合蛋白。如本文所用,术语“载体”包括质粒、粘粒、表达载体、克隆载体、病毒载体等。在本发明中,可选用本领域已知的各种载体如市售的载体。比如,选用市售的载体,然后将编码本发明新融合蛋白的核苷酸序列可操作地连于表达调控序列,可以形成蛋白表达载体。如本文所用,“可操作地连于”指这样一种状况,即线性DNA序列的某些部分能够影响同一线性DNA序列其他部分的活性。例如,如果信号肽DNA作为前体表达并参与多肽的分泌,那么信号肽(分泌前导序列)DNA就是可操作地连于多肽DNA;如果启动子控制序列的转录,那么它是可操作地连于编码序列;如果核糖体结合位点被置于能使其翻译的位置时,那么它是可操作地连于编码序列。一般,“可操作地连于”意味着相邻近,而对于分泌前导序列则意味着在阅读框中相邻。在本发明中,术语“宿主细胞”包括原核细胞和真核细胞。常用的原核宿主细胞的例子包括大肠杆菌、枯草杆菌等。常用的真核宿主细胞包括酵母细胞,昆虫细胞、和哺乳动物细胞等。较佳地,该宿主细胞是真核细胞,更佳地是哺乳动物细胞。在获得转化的宿主细胞后,可在适合表达本发明融合蛋白的条件下培养该细胞,从而表达出融合蛋白。然后再分离出表达的融合蛋白。FOXP3人叉头蛋白P3(humanforkheadboxP3,Foxp3)是Treg发育和功能维持的重要转录因子,对调控Treg的发育和功能起重要作用。在人体中,FOXP3功能缺失会引起免疫功能紊乱,引起多种内分泌失调,肠道病及X-性连锁综合征IPEX(Immunodysregulation,Polyendocrinopathy,andEnteropathy,X-linked)。在鼠中,FOXP3功能缺失会发展成淋巴组织增生性疾病(Scurfy),表现为严重皮炎、多器官淋巴细胞浸润及自身免疫溶血性贫血,原因为天然型Treg的缺失。将FOXP3基因人工整合到T细胞中表达可以获得Treg的表型。在小鼠中进行骨髓嵌合实验,发现FOXP3基因敲除的骨髓细胞无法发育成Treg,而野生型骨髓细胞则可以。而FOXP3基因3’非编码区的变更导致的FOXP3表达水平的显著下调,会严重削弱Treg的免疫抑制功能,说明FOXP3的表达水平对Treg的功能有直接影响。综上所述,FOXP3是调节Treg细胞发育和功能的重要转录因子。术语“治疗”是指基于治愈、缓解、改善、减轻、影响治疗对象疾病、症状、疾病体质(predisposition)的目的而给予需要治疗的对象本发明的白介素-17。术语“治疗对象”是指鼠、人及其他哺乳动物。术语“治疗有效量”是指能够在治疗对象体内达到治疗目的的去泛素化酶或其衍生物、去泛素化酶激动剂或拮抗剂的量。本领域的普通技术人员应理解,所述“治疗有效量”可随去泛素化酶或其衍生物、去泛素化酶激动剂或拮抗剂的给药途径、所用药物辅料以及与其他药物联合用药情况的不同而有所不同。药物组合物和施用方法本发明的药物组合物包含安全、有效量范围内的本发明去泛素化酶或其衍生物、去泛素化酶激动剂或拮抗剂(活性成分)及药理上可以接受的赋形剂或载体。其中“安全、有效量”指的是:活性成分的量足以明显改善病情,而不至于产生严重的副作用。通常,药物组合物含有0.001-1000mg的活性成分/剂,较佳地0.05-300mg的活性成分/剂,更佳地,含有0.5-200mg的活性成分/剂。本发明的活性成分及其药理上可接受的盐可制成各种制剂,其中包含安全、有效量范围内的本发明的活性成分或其药理上可接受的盐及药理上可以接受的赋形剂或载体。其中“安全、有效量”指的是:活性成分的量足以明显改善病情,而不至于产生严重的副作用。活性成分的安全、有效量根据治疗对象的年龄、病情、疗程等具体情况来确定。“药理上可以接受的赋形剂或载体”指的是:一种或多种相容性固体或液体填料或凝胶物质,它们适合于人使用,而且必须有足够的纯度和足够低的毒性。“相容性”在此指的是组合物中各组份能与本发明的化合物以及它们之间相互掺和,而不明显降低化合物的药效。药理上可以接受的赋形剂或载体部分例子有纤维素及其衍生物(如羧甲基纤维素钠、乙基纤维素钠、纤维素乙酸酯等)、明胶、滑石、固体润滑剂(如硬脂酸、硬脂酸镁)、硫酸钙、植物油(如豆油、芝麻油、花生油、橄榄油等)、多元醇(如丙二醇、甘油、甘露醇、山梨醇等)、乳化剂(如)、润湿剂(如十二烷基硫酸钠)、着色剂、调味剂、稳定剂、抗氧化剂、防腐剂、无热原水等。施用本发明组合物时,可以口服、直肠、肠胃外(静脉内、肌肉内或皮下)、局部给药。本发明组合物可以单独给药,或者与其他药学上可接受的化合物联合给药。含有本发明的组合物的微胶囊可用于本发明的活性成分的缓释给药。重组蛋白的微囊缓释给药技术已成功应用于重组人生长激素(rhGH)、重组人干扰素(rhIFN)、白介素-2和MNrgp120(Johnsonetal.,Nat.Med.,2:795-799(1996);Yasuda,Biomed.Ther27:1221-1223(1993);WO97/03692,WO96/40072,WO96/07399;U.S.Pat.No.5654010。本发明的活性成分的缓释制剂可用具有良好生物兼容性和宽泛生物可降解性的乳酸羟基乙酸高聚物(PLGA)制备。PLGA的降解产物,乳酸和羟基乙酸可被人体很快清除。而且,该高聚物的降解能力可随其分子量和组成的不同,从几个月延长到几年(Lewis,“Controlledreleaseofbioactiveagentsformlactide/glycolidepolymer,”in:M.ChasinandR.Langer(Eds.),BiodegradablePolymersasDrugDeliverySystems(MarcelDekker:NewYork,1990),pp.1-41))。使用药物组合物时,是将安全有效量的本发明的活性成分适用于需要治疗的哺乳动物(如人),其中施用时剂量为药学上认为的有效给药剂量,对于60kg体重的人而言,每次给药剂量通常为0.01~300mg,优选0.5~100mg。当然,具体剂量还应考虑给药途径、病人健康状况等因素,这些都是熟练医师技能范围之内的。本发明的主要目的之一是提供泛素化途径相关因子及其激动剂或拮抗剂在调节FOXP3、IL-10、IL-2、和TGF-β活性中的用途。本发明的另一目的在于提供这些调节因子在调节FOXP3对其靶基因的转录调控活性,进而调控FOXP3+Treg的免疫抑制活性中的用途。在本发明一方面提供了泛素化途径相关因子、其激动剂或拮抗剂在制备调节FOXP3、IL-10、IL-2、和TGF-β活性的组合物中的用途,其中所述泛素化途径相关因子选自:USP44/USP7、诱导USP44/USP7表达或改变其核质定位的信号因子、和/或它们的编码序列;和/或所述泛素化途径相关因子的激动剂或拮抗剂。在本发明的另一个实施方式中,对FOXP3、IL-10、IL-2、和TGF-β活性的调节可以是正调节或负调节,其中,所述泛素化途径相关因子或其激动剂用于正调节FOXP3、IL-10和TGF-β活性和负调节IL-2活性,所述泛素化途径相关因子的拮抗剂用于负调节FOXP3、IL-10和TGF-β活性和正调节IL-2活性。在一个优选例中,所述拮抗剂为shUSP44,shUSP7。在另一个优选例中,所述拮抗剂为USP44抑制剂(10-hydroxycamptothecin,10-羟基喜树碱)。在本发明的另一个实施方式中,所述促炎症细胞因子选自:IL-17和IFN-γ。在本发明的一个优选实施方式中,所述用途是泛素化途径相关因子在制备正调节FOXP3活性的组合物中的用途,其中所述泛素化途径相关因子选自:USP44/USP7、诱导USP44/USP7表达或改变其核质定位的信号因子、和/或所述泛素化途径相关因子的激动剂或拮抗剂。在本发明的一个优选例中,所述活性失调是活性过高或活性过低。在本发明的另一个实施方式中,所述与FOXP3、IL-10、IL-2、和TGF-β活性相关。USP44/USP7蛋白特异性的shRNA可以抑制FOXP3、IL-10和TGF-βmRNA表达,促进IL-2mRNA表达。在本发明的一个优选例中,所述组合物还包含药学上、保健品学上或免疫学上可接受的载体。在本发明的另一方面,提供了一种调节FOXP3、IL-10、IL-2、和TGF-β活性的组合物,其包含:(a)一种或多种选自下组的泛素化途径相关因子:USP44/USP7,原诱导USP44/USP17表达或改变其核质定位的信号因子、和/或它们的编码序列;和/或所述泛素化途径相关因子的激动剂或拮抗剂。(b)药学上、免疫学上或保健品学上可接受的载体。在一个优选例中,所述组合物用于治疗或预防与FOXP3、IL-10、IL-2、和TGF-β活性失调(即活性过高或活性过低)相关的疾病或症状或用作疫苗佐剂。在一个优选例中,所述组合物还包含一种或多种可调节FOXP3、IL-10、IL-2、和TGF-β的其它活性物质。在另一个优选例中,所述基因蛋白USP44/USP7可减少与FOXP3降解相关的泛素化。在一个优选例中,所述组合物中调节因子的含量为0.05-99.5重量%,优选0.1-95重量%,更优选1-90重量%,更优选5-80重量%。在另一优选例中,所述组合物是注射剂、片剂、颗粒剂、粉剂或胶囊。在本发明的其它方面中,提供了一种调节FOXP3、IL-10、IL-2、和TGF-β活性的方法,所述方法包括给予一种或多种选自下组的泛素化途径相关因子:USP44/USP7,诱导USP44/USP7表达或改变其核质定位的信号因子、和/或它们的编码序列;和/或所述泛素化途径相关因子的激动剂或拮抗剂。在另一优选例中,本发明还进一步提供了治疗或预防与FOXP3、IL-10、IL-2、和TGF-β活性失调相关的疾病或症状的方法,所述方法包括给予需要所述治疗或预防的对象有效量的一种或多种选自下组的泛素化途径相关因子:USP44/USP7,诱导USP44/USP7表达或改变其核质定位的信号因子、和/或它们的编码序列;和/或所述泛素化途径相关因子的激动剂或拮抗剂。在另一优选例中,所述方法进一步用于提高疫苗的免疫原性。本发明的其它方面由于本文的公开内容,对本领域的技术人员而言是显而易见的。本发明的主要优点在于:(1)首次揭示了去泛素化酶USP44在调节FOXP3的稳定性上的作用;(2)首次揭示了TGF-β能够用于促进去泛素化酶USP44的转录。(3)去泛素化酶能够增强FOXP3的稳定性进而提高调节性T细胞活性及其分化。下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。本领域技术人员可对本发明做出适当的修改、变动,这些修改和变动都在本发明的范围之内。下列实施例中未注明具体条件的实验方法,可采用本领域中的常规方法,例如参考《分子克隆实验指南》(第三版,纽约,冷泉港实验室出版社,NewYork:ColdSpringHarborLaboratoryPress,1989)或按照供应商所建议的条件。DNA的测序方法为本领域常规的方法,也可由商业公司提供测试。除非另外说明,否则百分比和份数按重量计算。除非另行定义,文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明方法中。文中所述的较佳实施方法与材料仅作示范之用。材料与方法1.实验材料1.1质粒人USP7,USP44基因克隆自人PBMC。用于承载人源FOXP3a和USP44基因的质粒载体pIPHA2/MYC2/FLAG2,承载含有人Il-2启动子基因的pGL3-basic购自Promega公司。质粒pIPHA2-FOXP3a及其不同突变体和截短体,pIPFLAG2-USP44及其截断体,突变体pIPFLAG2-USP44-C282S,pIPMYC2-USP7-C223S,pIPMYC2-STUB1-H260Q或K30A和pIPHis6-Ub及其K0,K6,K11,K23,K29,K33,K48,K63突变体均通过常规方法构建。慢病毒包装和表达质粒pLVX-IRES-EGFP获自上海巴斯德研究所,FUGW,del8.9和VSV-G获自上海巴斯德研究所。用于构建shRNA质粒的载体pLKO.1购自OpenBiosystems公司并经本实验室改造以适合开放性shRNAs的插入。荧光素酶报告基因载体pGL4-basic获自上海交通大学医学院。USP44启动子区域+17-(-1712)克隆自HEK293T细胞基因组DNA。1.2抗体本发明实施例中所使用的抗体包括:anti-USP44(1:1000,M2,SantaCruz),anti-USP7(1:1000,CellSignaling),anti-Foxy(1:2500,eBioscience),anti-STUB1(H-231,SantaCruz),anti-HA(1:1000,F-7,SantaCruz),anti-FLAG(1:20000,M2,Sigma),anti-MYC(1:1000,9E10,SantaCruz)。anti-β-actin(1:1000,SungeneBiotech)andanti-GAPDH(1:5000,Sungenebiotech),anti-人CD45RA-PerCP/Cy5.5(BioleGend,304121),anti-人CD4-FITC(BioleGend,300506),anti-人CD25-PE(BioleGend,302606),anti-FOXP3-APC(eBioscience,E09946-1633)。实验所用到的FACS抗体均购自BDPharmingen。anti-CD3/CD28Dynabeads(Gibco,1412799)。所用的辣根过氧化物酶标记的二抗购自JacksonLab。1.3酶和试剂分子克隆所需的所有限制性内切酶,DNA聚合酶,T4DNA连接酶均购自TAKARA或者NEB公司。点突变KOD-plus酶及试剂盒购自于Toyobo。cDNA逆转录试剂盒和实时荧光定量PCR试剂盒(SYBRgreen)购自于TaKaRa。重组人细胞因子购自R&Dsystem,TGF-β(R&D,240-B-002),IL-6(R&D,206-IL-010),IL-23(R&D,1290-1L-010)andIL1β(R&D,201-LB-005),IL-2(R&D,202-IL-010),rIL-4(R&D,204-IL-010),α-IL-4(R&D,MAB204),IL-12(R&D,219-IL-005),α-IFN-γ(R&D,285-IF-100)。TRIzol试剂购自于Invitrogen。蛋白酶体抑制剂MG132购自Merck公司。蛋白酶抑制剂Cocktail购自Sigma。蛋白合成抑制剂Cycloheximide(CHX)购自Sigma。ProteinAG-beads购自SantaCruz。淋巴细胞分离液(Ficoll,StemCellTechnologies)。LPS-EK购自Invivogen。1.4引物本课题中所有引物均订购自生工生物工程有限公司(上海)。本课题中用于基因克隆的引物序列为:FOXP3a的各种截断体引物均由陈祚珈博士设计,参考文献(Chen,Barbietal.2013)。用于实时荧光定量PCR的引物序列为:其余实时荧光定量PCR引物,如STUB1,IL-2,CTLA4,CD25,GITR均由陈祚珈博士设计,并在(ZuojiaChen,et.al.Immunity.2013)(ChenZ2013)有描述。用于构建shRNA的引物的基因序列为:用于点突变的引物序列为:引物序列SEQIDNO.USP44-C282S-FGAGAAATTTGGGAAATACTAGCTATATGAATTCTGTTC50USP44-C282S-RGAACAGAATTCATATAGCTAGTATTTCCCAAATTTCTC51USP7-C223S-FGAATCAGGGAGCGACTAGCTACATGAACAGCCTGC52USP7-C223S-RGCAGGCTGTTCATGTAGCTAGTCGCTCCCTGATTC53其余突变体,如FOXP3a的各种突变及STUB1-H206Q,K30A点突变,引物均由陈祚珈博士设计,参考文献(Chen,Barbietal.2013)。2实验方法2.1细胞系的培养本课题中所用到的HEK293T细胞,是人胚肾细胞转化细胞系经转染SV40大T抗原获得的可以体外传代的细胞系,培养在含有10%的胎牛血清(Fetalbovineserum,FBS,购自Excell),100μg/ml青链霉素的DMEM(DulbeccoModifiedEaglemedium)培养基中。培养条件为温度37℃及5%CO2饱和湿度。JurkatT细胞,即人急性T淋巴细胞白血病细胞株JurkatE6.1T细胞系培养在含有10%FBS(购自Hyclone),100μg/ml青链霉素,1×NEAA(Gibco),1×丙酮酸钠(Gibco)的1640培养基中。培养条件为温度37℃及5%CO2饱和湿度。2.2细胞转染HEK293T细胞的转染使用聚乙烯亚胺Polyethylenimine(PEI)试剂并严格按照说明书操作。简而言之,待HEK293T细胞密度长到70-90%开始进行转染,先将4μg质粒与100μl低血清培养基OPTI-MEM(Gibco)充分混合,再加入12μlPEI充分混匀,室温静置10min后,将待转染细胞弃去旧培液换上含10%FBS的新鲜培养基DMEM(完全培养基),缓慢加入以上混合物。在37℃,5%CO2培养箱中培养4h后,弃去旧培液换上完全培养基,继续在37℃,5%CO2培养箱中培养48h左右收样。JurkatT转染使用电穿孔转染仪(Bio-RadLaboratories,USA)。转染前先将JurkatT细胞用50ng/ml佛波酯(PMA)和1μM离子霉素Ionomycin或带有anti-CD3(1μg/ml)和anti-CD28(1μg/ml)的磁柱活化4h,严格按照操作手册上推荐的程序和条件进行电转,之后在37℃,5%CO2培养箱中培养48h左右收样。2.3免疫共沉淀(Immunoprecipitation,IP)和蛋白免疫印记实验(Westernblotting,WB)将收集的细胞用预冷的1×PBS洗涤后,加入含有蛋白酶抑制剂(1:100,P8340,Sigma-Aldrich),PMSF(1mM))和NaF(1mM)的RIPA裂解液(50mMTris-HClpH7.4,150mMNaCl,1%NP-40,0.5%Na-DOC,1mMEDTA)冰上静置30min让细胞充分被裂解,12000rpm,4℃离心10min,弃沉淀将上清转移至新离心管中,加入对应的目的蛋白抗体并于4℃冷库摇床上孵育1h。再依次加入10μl的ProteinA/GAgaroseBeads,继续相同条件下孵育1h,之后1000rpm,4℃离心3min沉降Beads,去除上清后加入1毫升RIPA(没有NP-40)裂解液,反复洗涤4次。最后一次离心去上清后,每管加40μl的2×SDSloadingbuffer,混匀后将样品管于干燥加热器上100℃煮5-10min,冷却后12000rpm常温离心1min,取上清电泳分析。将等量体积的样品上清上样在浓缩胶的样品孔中,恒压进行SDS-PAGE电泳。浓缩胶电泳条件:80V,30min;分离胶电泳条件:120V,90min。用湿转法(100V,90min)将胶上蛋白转至硝酸纤维素膜(NC)上。之后将膜用5%脱脂牛奶室温封闭1h或4℃过夜,随后用目的蛋白对应的一抗室温孵育1h。1×TBST洗涤3次(10min/次)除去多余的一抗,然后用与辣根过氧化物酶偶联的二抗室温孵育1h。1×TBST洗涤3次(10min/次)除去多余的二抗,再加入ECL化学底物溶液A和溶液B按1:1混合与二抗反应(试剂盒购自Millipore),并用显色仪GELAS4000检测并收集图像用于分析。2.4免疫荧光实验Jurkat-HA-FOXP3a稳转株细胞或从人PBMC中分离出的Treg细胞加入用poly-L-lysine包被的板子中,300g离心5min,轻轻弃去上清,轻轻加入4%的PFA(多聚甲醛)室温固定15min;加入含有0.5%Triton-X100,3%的BSA穿膜液室温封闭1h,然后依次加入与目的蛋白对应的一抗(1h)、二抗(驴抗鼠-488,羊抗兔-555和核染料抗体DAPI(1:5000)一起加,0.5h)室温孵育,每次孵育完用1×PBS洗涤(3次,5min/次)除去多余的抗体,加入防淬灭剂后封片,避光保存。最后用LeicaConfocalsystemSP5仪器检测荧光信号并收集图像用于分析。2.5荧光素酶报告基因检测实验人pGL3-IL-2-reporter和pGL4-USP44-reporter荧光素酶报告基因质粒和内参Renilla(pSV40)质粒通过PEI转染至HEK293T或电转至JurkatT细胞中,48h后收集细胞(JurkatT在收集之前用50ng/mlPMA和1μMIonomycin先活化4h)。离心收集下来的细胞先用预冷的1×PBS洗涤,弃去PBS后用报告基因裂解液处理使其充分裂解,12000rpm离心10min,取上清用双报告基因检测试剂盒(购自Promega)与其反应,然后用化学发光仪检测荧光素酶活性,并以Renilla作为转染效率的内参,来分析报告基因的表达。2.6细胞RNA的提取离心收集细胞(1×106)后加入1mlTRIzol试剂(购自Invitrogen)充分混匀后冰上裂解细胞,加入0.2ml氯仿,剧烈振荡15s后放置冰上5min,于12000rpm4℃离心15min使其分层。小心将上层水相转移至新的管中,加入0.5ml异丙醇沉淀RNA,充分混匀后,冰上静置5min。于12000rpm4°C离心15min后弃去上清。加入75%的乙醇溶液洗涤沉淀一次,7500rpm4°C离心5min。弃上清后于室温开盖干燥沉淀5-10min,最后将沉淀溶于RNase-free水(不少于20μl)中。2.7实时荧光定量PCR(QuantitativeReal-timePCR)在进行实时荧光定量PCR之前,先使用SYBRPrimeScriptRT-PCR(reversetranscriptionPCR)Kit(购自TaKaRa)将抽提的RNA进行反转录得到cDNA。两步法反应条件如下:37℃15min(反转录反应)85℃5s(反转录酶的失活反应),即得到用于实时荧光定量PCR的cDNA模板。然后使用SYBRgreenPCRmix试剂盒(12μl体系)制备混合液并分装到PCR板各个孔内,然后在ABIPrism7900HT(购自AppliedBiosystems)仪器上进行实时荧光定量PCR。程序设定:95℃2min;2步PCR程序:95℃15s和60℃60s,以此进行40循环。使用β-actin或GAPDH作为内标基因排除样品中总体RNA的差异。用相对定量法可以由机器计算直接得到样品组相对于对照组的基因表达的倍数。绝对定量则需先计算每组样品三个复孔的平均循环阕值(cyclethreshold,CT),样品CT值与内标基因CT值的差值为ΔCT,样品ΔCT和对照样品ΔCT的差值为ΔΔCT,计算目的基因的相对表达量为2-ΔΔCT,然后依次分析各个基因。2.8人原代细胞的分离、诱导与扩增1.全血中PBMC的分离将健康人献血者白细胞样品(上海市血液中心提供)置于50ml离心管中(每管不超过15ml),1×PBS等体积稀释,然后在新的50ml离心管中分装体积和稀释血液等量的淋巴细胞分离液(Ficoll),沿壁缓缓加入全血稀释液,使液体自然分层,交界面尽量不要出现浑浊。2500rpm不刹车离心20分钟。用1ml移液器小心吸取中间白色PBMC细胞层,尽量不要吸到细胞上层的液体,收集PBMC至新的离心管中,加入1×PBS洗涤细胞,300g离心5分钟,去上清,重复2次。再用1640培养基洗涤一次,根据实验需求直接裂解或者染色分选或者用X-VIVO培养基重悬,置37℃,5%CO2培养箱中培养,以供后续实验使用。2.人T和Treg细胞的分选及iTreg的体外诱导分化将由健康人献血者白细胞样品(上海市血液中心提供)分离的PBMC细胞,用流式抗体孵育染色,使用FACSARIAII细胞分选仪(购自BD)分选获得CD4+CD25hiCD127loTreg细胞(纯度度大于95%),CD4+CD25-CD45RA+T细胞。人Treg细胞用10%人AB血清的X-Vivo培养基(加入500U/mlIL-2和anti-CD3/CD28beads(1:1))扩增培养。使用前先将扩增后的Treg细胞去除beads在含有100U/mlIL-2培养基中静息培养2天,再加入anti-CD3/CD28beads(1:4)和相应的细胞因子刺激。T细胞用10%人AB血清的X-Vivo培养基(加入100U/mlIL-2和5ng/mlTGF-β,及anti-CD3/CD28beads(细胞和磁珠比例为1:1))7d诱导其分化成iTreg,检测FOXP3表达之后再使用。3.人Th细胞亚群的体外诱导分化人Th细胞亚群在相应的诱导条件下分化,简而言之,原始细胞为人细胞,加入anti-CD3/CD28beads(细胞和磁珠比例为1:1),然后对于Th0细胞,α-IL-4(10μg/ml),α-IFN-γ(10μg/ml),IL-2(50u/ml);对于Th1细胞诱导分化条件为,anti-IL-4(10μg/ml),rIL-12(10ng/ml),IL-2(50u/ml);对于Th2细胞诱导分化条件为,rIL-4(20ng/ml),α-IFN-γ(10μg/ml),IL-2(50u/ml);对于Th17细胞诱导分化条件为,TGF-β(1ng/ml),IL-6(1ng/ml),IL-23(100ng/ml)andIL1β(10ng/ml)。诱导7d使其分化成相应Th细胞,检测相应转录因子及细胞因子表达之后再使用。2.9泛素沉淀实验(His-pulldown)本实验参考(JorgvanLoosdregt,et.al.Immunity.2013)(vanLoosdregt,Fleskensetal.2013)。简言之,将带有6个组氨酸标记的泛素质粒和表达目的蛋白的质粒用PEI转染入HEK293T细胞中,收样前4h用MG132(20μM)处理。收集细胞用溶液1(PH8.0尿素溶液,8MUrea,100mMNa2HPO4,10mMTRISPH8.0,0.2%TX-100,10mMimmidazole,1mMN-ethylmaleimide)裂解,超声破碎仪超声1min(30s,停10s,30s),然后12000rpm,20℃,离心30min。取上清依次加入Ni-NTAbeads(5μl),在摇床上室温孵育3h,3000rpm,1.5min沉淀beads,然后分别用溶液1洗两次,溶液2(PH6.3尿素溶液,8MUrea,100mMNa2HPO4,10mMTRISPH6.3,0.2%TX-100,10mMimmidazole))洗两次,溶液3(20mMTRISPH8.0,100mMNaCl,20%glycerol,1mMDTT,10mMimidazole)洗一次,以除去非特异结合的蛋白和杂质。然后离心弃去残留上清,加入2xSDSloading煮样5-10min,并进行蛋白免疫印记实验分析。2.10慢病毒的包装与感染将目的基因的pLKO.1-shRNA质粒和pLKO.1-shCK和慢病毒包装质粒△8.9,VSV-G共转染HEK293T细胞10cm培养皿。48h后收取上清用0.45μM滤膜过滤,分装成1ml一管冻在-80℃备用。人Treg细胞(5×105)用anti-CD3/28beads(1:1)活化后感染病毒。感染过夜后(24h)换成正常培液。48h后观察感染效率。72h后即可收集细胞进行检测或进行筛选。2.11流式细胞技术(FACS)检测收集用于检测的细胞,用预冷的1×PBS离心洗两遍,先染viabilitydye工作液染色排除死细胞,用1×PBS洗去多余的染料,再将细胞重悬至FACS缓冲液中(1%BSAPBS)。加入细胞表面抗体冰上避光孵育30min,用FACS缓冲液洗涤两遍除去多余的抗体,随后加入固定穿膜工作液(eBioscience)混匀,于冰上避光静置45min。加入1×穿膜缓冲液离心洗涤细胞两次。随后用穿膜缓冲液稀释的胞内抗体工作液加入细胞,冰上避光静置1h进行胞内染色。加入1×穿膜缓冲液离心洗涤细胞两次除去多余的抗体,最后将细胞重悬至1×106/ml,调试FACSFortessa仪器(购自BD公司)程序并上机进行检测,收集实验数据用FlowJo软件分析。2.12统计学分析所有定量数据均表示为平均值±标准误差(SEM)。数据差异的显著性分析通过T-test在GraphPadPrism软件中完成,均表示为至少三次独立重复实验。(*p<0.05,**p<0.005)实施例1,USP44在iTreg中特异高表达本发明人首先将从人外周血(若未经特殊说明指健康人)中分离得到的外周血单核细胞(PBMC)进行流式抗体染色,然后用流式细胞技术(FACS)从人外周血PBMC中分离得到幼稚T细胞(T),效应T细胞(Teff)和nTreg,体外诱导T使其分化成iTreg,裂解细胞抽取RNA进行实时荧光定量PCR(QuantitativeReal-timePCR,qRT-PCR)检测相关基因的表达,结果显示USP44在iTreg中特异高表达(图1A)。体外诱导分化不同的T辅助细胞(Th)亚群(Th1,Th2,Th17)和iTreg,同样进行qRT-PCR检测,也证明USP44在iTreg中特异高表达(图1B)。说明在iTreg中USP44和FOXP3的表达具有相关性。实施例2,USP44与FOXP3相互作用由于USP44和FOXP3在iTreg中协同上调,本发明人假设二者可能具有某种相互作用,为了验证USP44是否作用与FOXP3并和其功能具有相关性,本发明人设计实验验证二者的相互作用。首先,在HEK293T细胞中外转表达FLAG-USP44和MYC-FOXP3,进行双向免疫共沉淀和蛋白免疫印记实验,结果显示二者在外转体系中可以相互作用(图2A)。然后收集稳定表达HA-FOXP3的JurkatT细胞,用相应抗体进行双向免疫共沉淀和蛋白免疫印记实验,结果显示二者在稳转细胞系中也可以相互作用(图2B)。再从人外周血PBMC中分离得到T细胞,体外诱导分化成iTreg,用相应抗体进行免疫共沉淀和蛋白免疫印记实验,结果显示二者蛋白在iTreg中相互作用(图2C)。而免疫荧光实验也显示二者在iTreg中共定位(图2D)。以上实验充分证明了USP44和FOXP3蛋白之间存在相互作用,这促使本发明人进一步思考USP44对FOXP3的蛋白及功能的影响。实施例3,USP44稳定FOXP3蛋白为了了解USP44对FOXP3的蛋白的影响,本发明人首先在过表达体系中共同表达MYC-FOXP3和FLAG-USP44(剂量成梯度递增0.5,1,1.5μg),用相应抗标签抗体进行蛋白免疫印记实验,结果显示USP44可以稳定FOXP3蛋白,并且具有剂量依赖(图3A)。由于USP44具有去泛素化酶活性,为了验证其对FOXP3蛋白的稳定是否与其去泛素化酶活性相关,本发明人构建了USP44酶失活突变体(C282S)并设计了蛋白合成抑制剂放线菌酮CHX处理(0,4,8,12h)实验,结果显示共表达野生型(WT)USP44能够显著延长FOXP3蛋白的半衰期,而酶失活突变C282S显著降低了这一作用,这说明USP44对FOXP3蛋白稳定性的影响与其去泛素化酶活性相关,同时也说明USP44对FOXP3的表达的影响是在其翻译后修饰水平,通过抑制其进入蛋白酶体途径降解来实现(图3B)。为进一步证明内源性的USP44对FOXP3蛋白稳定性的影响,本发明人用慢病毒感染(带有shCK、shUSP44-1、shUSP44-2)敲除iTreg中内源的USP44,用相应抗体进行蛋白免疫印记实验和用流式细胞技术FACS分析,结果显示敲低USP44降低了内源FOXP3蛋白的稳定性(图3C,D)。用qRT-PCR实验检测FOXP3下游相关基因的表达,结果显示敲低USP44导致FOXP3下游基因表达量发生变化:即降低FOXP3诱导的下游基因CTLA-4的转录水平,升高了FOXP3抑制的下游基因IL2的转录水平。shCK的序列如下:CAACAAGATGAAGAGCACCAA(SEQIDNO.54)shUSP44-1的序列如下:ACTGAGAATGGACATTCTAAA(SEQIDNO.55)shUSP44-2的序列如下:GAGTATCAAGTTAAAGCAGAA(SEQIDNO.56)实施例4,USP44影响FOXP3对下游Il2基因的转录抑制为了进一步验证USP44对FOXP3蛋白功能的影响,本发明人在HEK293T细胞中外转包含人Il2基因启动子的荧光素酶报告基因质粒,FLAG-USP44(WT和C282S)和MYC-FOXP3,以USP7为阳性对照,STUB1为阴性对照,Renilla为转染效率的内参,收集细胞进行荧光素酶活性测定和用相应抗体进行蛋白免疫印记实验,结果显示USP44能显著增强FOXP3对下游Il2基因的转录抑制作用(图4A)。剂量实验显示USP44对FOXP3介导的Il2基因转录抑制的增强成剂量梯度依赖(图4B)。而用慢病毒(含有shCK、shUSP44-1、shUSP44-2)敲低内源USP44后,这种转录抑制的增强作用显著降低(图4C),进一步验证了USP44对FOXP3蛋白功能的影响具有重要作用。以上实验证明了USP44对FOXP3蛋白的稳定性和功能具有影响,且发生在蛋白翻译后修饰水平,而蛋白泛素化修饰-蛋白酶体降解途径是常见的发生在蛋白翻译后修饰水平并且影响蛋白稳定性和功能的方式之一,USP44具有去泛素化酶活性,这促使本发明人进一步探讨USP44对FOXP3蛋白稳定性和功能影响的机制。实施例5,USP44去除FOXP3与降解相关的K48偶联的多聚泛素化修饰本课题中发现的iTreg特异的去泛素化酶USP44对其重要转录因子FOXP3的稳定性和功能具有重要作用,接下来本发明人想要知道USP44作为一个去泛素化酶是否能够去除FOXP3的泛素化修饰。本发明人首先在HEK293T细胞中共转染表达FLAG-USP44(WT)及酶失活突变体(C282S),MYC-FOXP3和His标签的泛素蛋白(ubiquitin),收样前加入MG132(20μM)处理4h阻止蛋白酶体降解途径,然后用Ni-NTA磁珠以配位键共价结合His标签进行泛素沉淀实验,蛋白免疫印记结果显示USP44(WT)可以显著降低FOXP3蛋白的泛素化水平而酶失活突变体(C282S)不能(图5A)。免疫共沉淀实验也显示即使是酶失活突变体C282S也依然可以和FOXP3相互作用(数据未予列出),显示C282S不能去泛素化FOXP3不是因为不能跟其结合导致,而是依赖于其去泛素化酶活性。为了证明这一泛素化水平降低的过程依赖于USP44,本发明人用慢病毒(带有shCK、shUSP44-1、shUSP44-2)感染来敲低内源USP44,筛选一周后转染表达MYC-FOXP3和His-ubiquitin的质粒,同样进行泛素沉淀,然后用相应抗体检测蛋白表达及FOXP3的泛素化水平,结果显示敲低USP44显著增加FOXP3蛋白的泛素化水平(图5B)。说明FOXP3的泛素化水平的降低依赖于USP44的去泛素化酶活性。与泛素第48位赖氨酸(K48)偶联的泛素化修饰与蛋白的降解直接相关早有报导,而第63位赖氨酸(K63)偶联的泛素化修饰对蛋白的功能发挥具有重要作用。为了了解USP44去除的是哪一种泛素化修饰,本发明人先把泛素上所有的K突变成精氨酸(R),即K0,然后依次对K0进行回复突变,构建泛素不同K的单个保留突变体(K6,K11,K23,K29,K33,K48,K63)。本发明人在过表达中共转染表达USP44,MYC-FOXP3和His标签的泛素蛋白(WT)及其各种突变体的质粒,进行泛素沉淀,然后用相应抗体检测蛋白表达及FOXP3的泛素化水平,结果显示USP44主要催化去除泛素K48偶联的泛素化修饰(图5C),这一结果揭示了USP44稳定FOXP3的机制。实施例6,FOXP3蛋白K179/250/263/268是USP44的去泛素化作用位点由于之前的研究证明FOXP3蛋白上的多个位点都可以被泛素化修饰,所以,除了K179,可能还存在其他位点的泛素化修饰也可以被USP44催化去除。为了找出这些位点,本发明人将上文提到构建的所有的FOXP3单个赖氨酸保留突变体与USP44共转染并进行蛋白免疫印记实验,三次独立实验之后,得到较为稳定的四个单个保留位点(K179/250/263/268)仍然可以被USP44稳定(图6A)。为了验证这四个位点是否是USP44的全部作用位点,本发明人构建了这四个位点赖氨酸的联合突变体4R(K179/250/263/268R),并进行外转共表达和泛素沉淀实验,结果显示跟野生型比起来,加入USP44后FOXP3-4R泛素化水平明显增加,且基本上不能被USP44稳定(图6B,C)。揭示K250,K263,K268是USP44可能的其他去泛素化作用位点。STUB1的作用位点中也包括K250,K263,K268,因此这一结果暗示USP44和STUB1对FOXP3的调节可能具有功能拮抗作用。实施例7,TGF-β信号通过上调USP44转录水平促进iTreg分化本发明人分析了USP44基因的启动子区,发现多个TGF-β下游激酶SMADs的结合位点(图7A),暗示iTreg特异高表达的去泛素化酶USP44可能受TGF-β信号调控。为了验证这一假设,本发明人首先构建了包含USP44基因的启动子序列+17-(-1712)bp的荧光素酶报告基因质粒,并将其转染到JurkatT细胞中,36h后用佛波酯(PMA,50ng/ml)和离子霉素(Ionomycin,1μM)及不同浓度的TGF-β(0,1,5,10μg/ml)刺激不同时间(0,1,2,4,8h),然后进行荧光素酶活性检测,结果显示TGF-β刺激可以显著上调USP44的转录水平(图1-12),磷酸化的SMAD2(p-SMAD2)水平显示TGF-β通路在刺激1h时即被激活。显示USP44基因的表达受TGF-β调控,这也解释了为什么USP44特异在iTreg中高表达。由于TGF-β在iTreg体外诱导分化中具有非常重要的作用,本发明人假设TGF-β通过上调USP44促进iTreg诱导分化。为了证明这一点,本发明人从人PBMC分离细胞进行体外诱导分化0,1,2,3,4,5d得到iTreg,抽提RNA进行qRT-PCR检测相应基因mRNA表达水平,同时通过免疫印记实验用特定抗体检测USP44,USP7,STUB1,Hsp70和FOXP3的蛋白水平,结果显示在iTreg分化过程中,随着TGF-β作用时间的延长,USP44表达水平不断增加,FOXP3表达也不断上调(图7B,C),而STUB1和Hsp70表达水平呈下降趋势,USP7表达水平变化不明显。这一结果证明TGF-β信号通过上调USP44转录水平来稳定FOXP3表达并促进iTreg分化。实施例8,STUB1通过增强USP44多泛素化修饰来降解USP44泛素连接酶STUB1通过修饰FOXP3K48偶联的泛素化促进FOXP3蛋白降解,从而增加Treg的不稳定性是本发明人实验室之前的研究结果(ZuojiaChen,et.al.Immunity.2013)(ChenZ2013)。上面的实验也证明USP44和STUB1具有部分共同作用的位点,且二者在iTreg中的表达水平呈负相关,对FOXP3的调节作用也相反。这些结果促使本发明人思考STUB1和USP44的相互调节作用,想要了解清楚USP44是否能够催化去除STUB1对FOXP3的泛素化修饰,以及USP44表达和功能是否受STUB1的工作条件的影响。本发明人首先设计实验共转STUB1,USP44,FOXP3和泛素,免疫共沉淀结果显示,加入USP44后,被STUB1修饰的FOXP3泛素化水平并没有明显降低,反而USP44本身就被STUB1降解(数据没有列出)。因此本发明人推测,STUB1可以通过降解USP44来维持FOXP3的泛素化修饰。为了验证这一推论,本发明人构建了稳定表达USP44的JurkatT细胞系,取细胞(1×106)先用PMA(50ng/ml)和Ionomycin(1μM)刺激4h,再分别用不同温度(37℃或42℃)刺激不同时间(1h,3h),或用LPS(1μg/ml)刺激不同时间(0,12,24h),然后收集细胞裂解用相应抗体进行蛋白免疫印记实验,结果显示42℃刺激1hUSP44即开始降解,3h大部分USP44已被降解,而LPS刺激12h,大部分USP44已被降解(图8A),说明在STUB1对FOXP3作用的工作条件中,USP44的功能因为本身被降解而受抑制。为了了解在iTreg中,USP44是否受使FOXP3不稳定因素的影响,本发明人取体外诱导分化的iTreg,加入100U/mlIL-2和anti-CD3/CD28beads(1:4,4个细胞一个beads)活化细胞,分别用LPS(1μg/ml),IL-6(20ng/ml),IL-1β(10ng/ml)刺激24h,收集细胞裂解后,用相应抗体进行蛋白免疫印记实验,结果显示,这些不稳定因素可以部分降解USP44水平,相反STUB1表达水平上调(图8B)。这些结果促使本发明人迫切想知道,STUB1是否作用于USP44。首先,本发明人在过表达体系中转染剂量呈梯度递增的MYC-STUB1(0.5,1,1.5μg)和USP44,用相应抗体进行蛋白免疫印记实验,结果显示STUB1能降解USP44,且呈剂量依赖(图8C)。接着共转STUB1(WT,酶失活突变体H260Q或不能与分子伴侣Hsp70结合的突变体K30A)与USP44,进行免疫共沉淀和蛋白免疫印记实验,结果显示STUB1可与USP44相互作用,STUB1酶失活突变体H260Q和不能与分子伴侣Hsp70结合的突变体K30A均不能降解USP44,而STUB1-K30A也不能结合USP44,这说明STUB1对USP44的降解与其泛素化酶活性和分子伴侣的协助相关(图8D,E,F)。泛素沉淀实验显示共转STUB1可以显著增加USP44的泛素化水平,说明STUB1通过增强USP44多泛素化修饰来降解USP44,从而促进FOXP3的不稳定。实施例9,USP44和USP7协同作用稳定FOXP3去泛素化酶USP7通过相互作用并去除泛素化修饰来稳定FOXP3蛋白和Treg功能已有报导(JorgvanLoosdregt,etal.Immunity.2013)(vanLoosdregt,Fleskensetal.2013)。本课题中发现的去泛素化酶USP44同样对FOXP3蛋白具有相互作用和通过去泛素化修饰稳定其蛋白水平,进而增强其功能的作用。同时发现USP44可以被STUB1降解,而USP7也具有和STUB1部分相同的作用位点,也可以被LPS降解,因此,本发明人假设USP44和USP7协同作用于FOXP3。为了证明这一假设,本发明人首先看USP44是否和USP7相互作用。在过表达体系中外转表达MYC-USP44和FLAG-USP7,通过双向免疫共沉淀实验发现二者可以相互作用(图9A)。确定了二者的相互作用,下一步本发明人想了解二者是否可以协同稳定FOXP3蛋白。设计实验共转USP44,MYC-FOXP3和FLAG-USP7(0.5,1,1.5μg)的质粒,并进行免疫共沉淀和蛋白免疫印记实验,结果显示共转USP44和USP7可以稳定更多的FOXP3蛋白,而USP7本身可以稳定USP44,且呈剂量依赖,以上结果证明USP44和USP7协同稳定FOXP3(图9B)。而共转USP44和USP7进行泛素沉淀实验,结果显示外转USP44或USP7均能降低FOXP3泛素化水平,而同时转染二者,FOXP3泛素化水平最低(图9C),显示USP44和USP7协同稳定FOXP3的机制是通过去除FOXP3的泛素化修饰。由于上文中已经证明了STUB1可以降解USP44,而图9B显示USP7本身可以稳定USP44,且呈剂量依赖。因此本发明人想弄清楚这三者之间的关系。在HEK293T细胞中外转带有shCK或shSTUB1的慢病毒包装质粒,1天后,再转入表达USP44和MYC-USP7的质粒,用相应抗体进行蛋白免疫印记实验,结果显示敲低STUB1之后,USP7对USP44蛋白的稳定明显增加(图9D)。而转染FLAG-USP44(WT,C282S)和MYC-STUB1(WT,H260Q)或USP7(WT,酶失活突变体C223S)质粒,并用相应抗体进行蛋白免疫印记实验,本发明人可以看到,共转STUB1(WT)和USP44(泳道6)与转染这二者加上USP7(C223S)(泳道10),USP44水平最低;而共转USP7(WT)和USP44(泳道3)与转染这二者加上STUB1(H260Q)(泳道9),USP44水平最高;USP7共转USP44(WT)蛋白水平明显增多,而共转USP44(C282S)蛋白水平和单转USP7本身接近(图9E)。综上结果,本发明人分析得出USP44和USP7相互作用,相互稳定,而且通过协同增强去泛素化作用来稳定FOXP3蛋白水平。实施例10,USP44基因敲除影响内源性FOXP3的表达和Treg的抑制功能为了在动物体内验证USP44对Treg功能的影响,本发明人首先将1×106CD4+T细胞(CD62LhighCD25-)单独或者与野生型Treg或USP44基因敲除小鼠中分离的Treg细胞4×105打入RAG2-/-免疫缺陷小鼠体内制造肠炎模型,在一定时间(如图)记录其体重并做曲线图(N=6),结果显示USP44基因敲除组Treg小鼠体重下降快于野生型Treg组(图10A)。取图10A中打入细胞8周后的肠炎小鼠模型的远端肠组织进行苏木精-伊红(H/E)染色,并进行组织切片显微镜下白光(100×)分析,并进行疾病评估打分做出柱状图。结果显示USP44基因敲除显著影响Treg抑制炎症的作用(图10B,C)。将与T细胞和野生型Treg和USP44基因敲除小鼠中分离的Treg细胞一同打入免疫缺陷小鼠体内,一定时间后取小鼠的黏膜淋巴结(mLN),外周淋巴结(pLN),脾脏(SPL)进行分离Treg细胞(CD4+/Thy1.1+),用特异抗体进行FACS分析FOXP3的表达,对照组设计如图(图10D)。结果显示USP44基因敲除显著影响Treg的FOXP3表达水平。同时将与不同Treg的一同打入免疫缺陷小鼠体内的T细胞,在一定时间取出并用特异抗体(CD4+/Thy1.2+)进行FACS分析IFN-γ和IL-17的表达,对照组设计如图(图10E)。结果显示与USP44基因敲除Treg一同打入免疫缺陷型小鼠体内的T细胞的IFN-γ和IL-17的表达水平显著上升。实施例11,USP44和FOXP3在HCV阳性的肝癌病人样本的癌组织中共同高表达在HCV阳性的肝癌病人样本的癌组织中用USP44抗体进行免疫组化实验,发现USP44特异表达在肿瘤间质中(图11A)。统计信息显示在17例由HCV感染最终导致肝癌(HCC)的病人的癌组织和癌旁及正常组织中,USP44和FOXP3在其中11例样本的癌组织中共同高表达(图11B)。免疫组化实验结果显示在17例由HCV感染最终导致肝癌(HCC)的病人的癌组织和癌旁及正常组织中,USP44和FOXP3在其中11例样本的癌组织中共同高表达(图11C)。实施例12,10-羟基喜树碱(10-HCPT)可以特异的抑制USP44对FOXP3蛋白的稳定在HEK293T细胞中共转染FLAG标签USP44和MYC标签FOXP3,并用不同浓度的10-羟基喜树碱处理,DMSO作为对照,结果显示,10-羟基喜树碱(10-HCPT)可以特异的抑制USP44对FOXP3蛋白的稳定,且呈剂量依赖(图12)。在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。参考文献:Chen,Z.,J.Barbi,S.Bu,H.Y.Yang,Z.Li,Y.Gao,D.Jinasena,J.Fu,F.Lin,C.Chen,J.Zhang,N.Yu,X.Li,Z.Shan,J.Nie,Z.Gao,H.Tian,Y.Li,Z.Yao,Y.Zheng,B.V.Park,Z.Pan,J.Zhang,E.Dang,Z.Li,H.Wang,W.Luo,L.Li,G.L.Semenza,S.G.Zheng,K.Loser,A.Tsun,M.I.Greene,D.M.Pardoll,F.PanandB.Li(2013)."TheubiquitinligaseStub1negativelymodulatesregulatoryTcellsuppressiveactivitybypromotingdegradationofthetranscriptionfactorFoxp3."Immunity39(2):272-285.ChenZ,B.J.,PanF,LiB,et.al.(2013)."TheubiquitinligaseStub1negativelymodulatesregulatoryTcellsuppressiveactivitybypromotingdegradationofthetranscriptionfactorFOXP3."Immunity39(2):272-285.vanLoosdregt,J.,V.Fleskens,J.Fu,A.B.Brenkman,C.P.Bekker,C.E.Pals,J.Meerding,C.R.Berkers,J.Barbi,A.Grone,A.J.Sijts,M.M.Maurice,E.Kalkhoven,B.J.Prakken,H.Ovaa,F.Pan,D.M.ZaissandP.J.Coffer(2013)."StabilizationofthetranscriptionfactorFoxp3bythedeubiquitinaseUSP7increasesTreg-cell-suppressivecapacity."Immunity39(2):259-271.序列表<110>中国科学院上海巴斯德研究所<120>泛素化途径相关因子在调控调节性T细胞功能中的应用<130>P2016-0882<160>56<170>PatentInversion3.5<210>1<211>2139<212>DNA<213>人工序列<400>1atgctagcaatggatacgtgcaaacatgttgggcagctgcagcttgctcaagaccattcc60agcctcaaccctcagaaatggcactgtgtggactgcaacacgaccgagtccatttgggct120tgccttagctgctcccatgttgcctgtggaagatatattgaagagcatgcactcaagcac180tttcaagaaagcagtcatcctgttgcattggaggtgaatgagatgtacgttttttgttac240ctttgtgatgattatgttctgaatgataacacaactggagacctgaagttactacgacgt300acattaagtgccatcaaaagtcaaaattatcactgcacaactcgtagtgggaggttttta360cggtccatgggtacaggtgatgattcttatttcttacatgacggtgcccaatctctgctt420caaagtgaagatcaactgtatactgctctttggcacaggagaaggatactaatgggtaaa480atctttcgaacatggtttgaacaatcacccattggaagaaaaaagcaagaagaaccattt540caggaaaaaatagtagtaaaaagagaagtaaagaaaagacggcaggaattggagtatcaa600gttaaagcagaattggaaagtatgcctccaagaaagagtttacgtttacaagggctcgct660cagtcgaccataatagaaatagtttctgttcaggtgccagcacaaacgccagcatcacca720gcaaaagataaagtactctctacctcagaaaatgaaatatctcaaaaagtcagtgactcc780tcagttaaacgaaggccaatagtaactcctggtgtaacaggattgagaaatttgggaaat840acttgctatatgaattctgttcttcaggtgttgagtcatttacttatttttcgacaatgt900tttttaaagcttgatctgaaccaatggctggctatgactgctagcgagaagacaagatct960tgtaagcatccaccagtcacagatacagtagtatatcaaatgaatgaatgtcaggaaaaa1020gatacaggttttgtttgctccagacaatcaagtctgtcatcaggactaagtggtggagca1080tcaaaaggtagaaagatggaacttattcagccaaaggagccaacttcacagtacatttct1140ctttgtcatgaattgcatactttgttccaagtcatgtggtctggaaagtgggcgttggtc1200tcaccatttgctatgctacactcagtgtggagactcattcctgcctttcgtggttacgcc1260caacaagacgctcaggaatttctttgtgaacttttagataaaatacaacgtgaattagag1320acaactggtaccagtttaccagctcttatccccacttctcaaaggaaactcatcaaacaa1380gttctgaatgttgtaaataacatttttcatggacaacttcttagtcaggttacatgtctt1440gcatgtgacaacaaatcaaataccatagaacctttctgggacttgtcattggagtttcca1500gaaaggtatcaatgcagtggaaaagatattgcttcccagccatgtctggttactgaaatg1560ttggccaaatttacagaaactgaagctttagaaggaaaaatctacgtatgtgaccagtgt1620aactcaaagcgtagaaggttttcctccaaaccagttgtactcacagaagcccagaaacaa1680cttatgatatgccacctacctcaggttctcagactgcacctcaaacgattcaggtggtca1740ggacgtaataaccgagagaagattggtgttcatgttggctttgaggaaatcttaaacatg1800gagccctattgctgcagggagaccctgaaatccctcagaccagaatgctttatctatgac1860ttgtccgcggtggtgatgcaccatgggaaaggatttggctcagggcactacactgcctac1920tgctataattctgaaggagggttctgggtacactgcaatgattccaaactaagcatgtgc1980actatggatgaagtatgcaaggctcaagcttatatcttgttttatacccaacgagttact2040gagaatggacattctaaacttttgcctccagagctcctgttggggagccaacatcccaat2100gaagacgctgatacctcgtctaatgaaatccttagctga2139<210>2<211>712<212>PRT<213>人工序列<400>2MetLeuAlaMetAspThrCysLysHisValGlyGlnLeuGlnLeuAla151015GlnAspHisSerSerLeuAsnProGlnLysTrpHisCysValAspCys202530AsnThrThrGluSerIleTrpAlaCysLeuSerCysSerHisValAla354045CysGlyArgTyrIleGluGluHisAlaLeuLysHisPheGlnGluSer505560SerHisProValAlaLeuGluValAsnGluMetTyrValPheCysTyr65707580LeuCysAspAspTyrValLeuAsnAspAsnThrThrGlyAspLeuLys859095LeuLeuArgArgThrLeuSerAlaIleLysSerGlnAsnTyrHisCys100105110ThrThrArgSerGlyArgPheLeuArgSerMetGlyThrGlyAspAsp115120125SerTyrPheLeuHisAspGlyAlaGlnSerLeuLeuGlnSerGluAsp130135140GlnLeuTyrThrAlaLeuTrpHisArgArgArgIleLeuMetGlyLys145150155160IlePheArgThrTrpPheGluGlnSerProIleGlyArgLysLysGln165170175GluGluProPheGlnGluLysIleValValLysArgGluValLysLys180185190ArgArgGlnGluLeuGluTyrGlnValLysAlaGluLeuGluSerMet195200205ProProArgLysSerLeuArgLeuGlnGlyLeuAlaGlnSerThrIle210215220IleGluIleValSerValGlnValProAlaGlnThrProAlaSerPro225230235240AlaLysAspLysValLeuSerThrSerGluAsnGluIleSerGlnLys245250255ValSerAspSerSerValLysArgArgProIleValThrProGlyVal260265270ThrGlyLeuArgAsnLeuGlyAsnThrCysTyrMetAsnSerValLeu275280285GlnValLeuSerHisLeuLeuIlePheArgGlnCysPheLeuLysLeu290295300AspLeuAsnGlnTrpLeuAlaMetThrAlaSerGluLysThrArgSer305310315320CysLysHisProProValThrAspThrValValTyrGlnMetAsnGlu325330335CysGlnGluLysAspThrGlyPheValCysSerArgGlnSerSerLeu340345350SerSerGlyLeuSerGlyGlyAlaSerLysGlyArgLysMetGluLeu355360365IleGlnProLysGluProThrSerGlnTyrIleSerLeuCysHisGlu370375380LeuHisThrLeuPheGlnValMetTrpSerGlyLysTrpAlaLeuVal385390395400SerProPheAlaMetLeuHisSerValTrpArgLeuIleProAlaPhe405410415ArgGlyTyrAlaGlnGlnAspAlaGlnGluPheLeuCysGluLeuLeu420425430AspLysIleGlnArgGluLeuGluThrThrGlyThrSerLeuProAla435440445LeuIleProThrSerGlnArgLysLeuIleLysGlnValLeuAsnVal450455460ValAsnAsnIlePheHisGlyGlnLeuLeuSerGlnValThrCysLeu465470475480AlaCysAspAsnLysSerAsnThrIleGluProPheTrpAspLeuSer485490495LeuGluPheProGluArgTyrGlnCysSerGlyLysAspIleAlaSer500505510GlnProCysLeuValThrGluMetLeuAlaLysPheThrGluThrGlu515520525AlaLeuGluGlyLysIleTyrValCysAspGlnCysAsnSerLysArg530535540ArgArgPheSerSerLysProValValLeuThrGluAlaGlnLysGln545550555560LeuMetIleCysHisLeuProGlnValLeuArgLeuHisLeuLysArg565570575PheArgTrpSerGlyArgAsnAsnArgGluLysIleGlyValHisVal580585590GlyPheGluGluIleLeuAsnMetGluProTyrCysCysArgGluThr595600605LeuLysSerLeuArgProGluCysPheIleTyrAspLeuSerAlaVal610615620ValMetHisHisGlyLysGlyPheGlySerGlyHisTyrThrAlaTyr625630635640CysTyrAsnSerGluGlyGlyPheTrpValHisCysAsnAspSerLys645650655LeuSerMetCysThrMetAspGluValCysLysAlaGlnAlaTyrIle660665670LeuPheTyrThrGlnArgValThrGluAsnGlyHisSerLysLeuLeu675680685ProProGluLeuLeuLeuGlySerGlnHisProAsnGluAspAlaAsp690695700ThrSerSerAsnGluIleLeuSer705710<210>3<211>3309<212>DNA<213>人工序列<400>3atgaaccaccagcagcagcagcagcagcagaaagcgggcgagcagcagttgagcgagccc60gaggacatggagatggaagcgggagatacagatgacccaccaagaattactcagaaccct120gtgatcaatgggaatgtggccctgagtgatggacacaacaccgcggaggaggacatggag180gatgacaccagttggcgctccgaggcaacctttcagttcactgtggagcgcttcagcaga240ctgagtgagtcggtccttagccctccgtgttttgtgcgaaatctgccatggaagattatg300gtgatgccacgcttttatccagacagaccacaccaaaaaagcgtaggattctttctccag360tgcaatgctgaatctgattccacgtcatggtcttgccatgcacaagcagtgctgaagata420ataaattacagagatgatgaaaagtcgttcagtcgtcgtattagtcatttgttcttccat480aaagaaaatgattggggattttccaattttatggcctggagtgaagtgaccgatcctgag540aaaggatttatagatgatgacaaagttacctttgaagtctttgtacaggcggatgctccc600catggagttgcgtgggattcaaagaagcacacaggctacgtcggcttaaagaatcaggga660gcgacttgttacatgaacagcctgctacagacgttatttttcacgaatcagctacgaaag720gctgtgtacatgatgccaaccgagggggatgattcgtctaaaagcgtccctttagcatta780caaagagtgttctatgaattacagcatagtgataaacctgtaggaacaaaaaagttaaca840aagtcatttgggtgggaaactttagatagcttcatgcaacatgatgttcaggagctttgt900cgagtgttgctcgataatgtggaaaataagatgaaaggcacctgtgtagagggcaccata960cccaaattattccgcggcaaaatggtgtcctatatccagtgtaaagaagtagactatcgg1020tctgatagaagagaagattattatgatatccagctaagtatcaaaggaaagaaaaatata1080tttgaatcatttgtggattatgtggcagtagaacagctcgatggggacaataaatacgac1140gctggggaacatggcttacaggaagcagagaaaggtgtgaaattcctaacattgccacca1200gtgttacatctacaactgatgagatttatgtatgaccctcagacggaccaaaatatcaag1260atcaatgataggtttgaattcccagagcagttaccacttgatgaatttttgcaaaaaaca1320gatcctaaggaccctgcaaattatattcttcatgcagtcctggttcatagtggagataat1380catggtggacattatgtggtttatctaaaccccaaaggggatggcaaatggtgtaaattt1440gatgacgacgtggtgtcaaggtgtactaaagaggaagcaattgagcacaattatgggggt1500cacgatgacgacctgtctgttcgacactgcactaatgcttacatgttagtctacatcagg1560gaatcaaaactgagtgaagttttacaggcggtcaccgaccatgatattcctcagcagttg1620gtggagcgattacaagaagagaaaaggatcgaggctcagaagcggaaggagcggcaggaa1680gcccatctctatatgcaagtgcagatagtcgcagaggaccagttttgtggccaccaaggg1740aatgacatgtacgatgaagaaaaagtgaaatacactgtgttcaaagtattgaagaactcc1800tcgcttgctgagtttgttcagagcctctctcagaccatgggatttccacaagatcaaatt1860cgattgtggcccatgcaagcaaggagtaatggaacaaaacgaccagcaatgttagataat1920gaagccgacggcaataaaacaatgattgagctcagtgataatgaaaacccttggacaata1980ttcctggaaacagttgatcccgagctggctgctagtggagcgaccttacccaagtttgat2040aaagatcatgatgtaatgttatttttgaagatgtatgatcccaaaacgcggagcttgaat2100tactgtgggcatatctacacaccaatatcctgtaaaatacgtgacttgctcccagttatg2160tgtgacagagcaggatttattcaagatactagccttatcctctatgaggaagttaaaccg2220aatttaacagagagaattcaggactatgacgtgtctcttgataaagcccttgatgaacta2280atggatggtgacatcatagtatttcagaaggatgaccctgaaaatgataacagtgaatta2340cccaccgcaaaggagtatttccgagatctctaccaccgcgttgatgtcattttctgtgat2400aaaacaatccctaatgatcctggatttgtggttacgttatcaaatagaatgaattatttt2460caggttgcaaagacagttgcacagaggctcaacacagatccaatgttgctgcagtttttc2520aagtctcaaggttatagggatggcccaggtaatcctcttagacataattatgaaggtact2580ttaagagatcttctacagttcttcaagcctagacaacctaagaaactttactatcagcag2640cttaagatgaaaatcacagactttgagaacaggcgaagttttaaatgtatatggttaaac2700agccaatttagggaagaggaaataacactatatccagacaagcatgggtgtgtccgggac2760ctgttagaagaatgtaaaaaggccgtggagcttggggagaaagcatcagggaaacttagg2820ctgctagaaattgtaagctacaaaatcattggtgttcatcaagaagatgaactattagaa2880tgtttatctcctgcaacgagccggacgtttcgaatagaggaaatccctttggaccaggtg2940gacatagacaaagagaatgagatgcttgtcacagtggcgcatttccacaaagaggtcttc3000ggaacgttcggaatcccgtttttgctgaggatacaccagggcgagcattttcgagaagtg3060atgaagcgaatccagagcctgctggacatccaggagaaggagtttgagaagtttaaattt3120gcaattgtaatgatgggccgacaccagtacataaatgaagacgagtatgaagtaaatttg3180aaagactttgagccacagcccggtaatatgtctcatcctcggccttggctagggctcgac3240cacttcaacaaagccccaaagaggagtcgctacacttaccttgaaaaggccattaaaatc3300cataactga3309<210>4<211>1102<212>PRT<213>人工序列<400>4MetAsnHisGlnGlnGlnGlnGlnGlnGlnLysAlaGlyGluGlnGln151015LeuSerGluProGluAspMetGluMetGluAlaGlyAspThrAspAsp202530ProProArgIleThrGlnAsnProValIleAsnGlyAsnValAlaLeu354045SerAspGlyHisAsnThrAlaGluGluAspMetGluAspAspThrSer505560TrpArgSerGluAlaThrPheGlnPheThrValGluArgPheSerArg65707580LeuSerGluSerValLeuSerProProCysPheValArgAsnLeuPro859095TrpLysIleMetValMetProArgPheTyrProAspArgProHisGln100105110LysSerValGlyPhePheLeuGlnCysAsnAlaGluSerAspSerThr115120125SerTrpSerCysHisAlaGlnAlaValLeuLysIleIleAsnTyrArg130135140AspAspGluLysSerPheSerArgArgIleSerHisLeuPhePheHis145150155160LysGluAsnAspTrpGlyPheSerAsnPheMetAlaTrpSerGluVal165170175ThrAspProGluLysGlyPheIleAspAspAspLysValThrPheGlu180185190ValPheValGlnAlaAspAlaProHisGlyValAlaTrpAspSerLys195200205LysHisThrGlyTyrValGlyLeuLysAsnGlnGlyAlaThrCysTyr210215220MetAsnSerLeuLeuGlnThrLeuPhePheThrAsnGlnLeuArgLys225230235240AlaValTyrMetMetProThrGluGlyAspAspSerSerLysSerVal245250255ProLeuAlaLeuGlnArgValPheTyrGluLeuGlnHisSerAspLys260265270ProValGlyThrLysLysLeuThrLysSerPheGlyTrpGluThrLeu275280285AspSerPheMetGlnHisAspValGlnGluLeuCysArgValLeuLeu290295300AspAsnValGluAsnLysMetLysGlyThrCysValGluGlyThrIle305310315320ProLysLeuPheArgGlyLysMetValSerTyrIleGlnCysLysGlu325330335ValAspTyrArgSerAspArgArgGluAspTyrTyrAspIleGlnLeu340345350SerIleLysGlyLysLysAsnIlePheGluSerPheValAspTyrVal355360365AlaValGluGlnLeuAspGlyAspAsnLysTyrAspAlaGlyGluHis370375380GlyLeuGlnGluAlaGluLysGlyValLysPheLeuThrLeuProPro385390395400ValLeuHisLeuGlnLeuMetArgPheMetTyrAspProGlnThrAsp405410415GlnAsnIleLysIleAsnAspArgPheGluPheProGluGlnLeuPro420425430LeuAspGluPheLeuGlnLysThrAspProLysAspProAlaAsnTyr435440445IleLeuHisAlaValLeuValHisSerGlyAspAsnHisGlyGlyHis450455460TyrValValTyrLeuAsnProLysGlyAspGlyLysTrpCysLysPhe465470475480AspAspAspValValSerArgCysThrLysGluGluAlaIleGluHis485490495AsnTyrGlyGlyHisAspAspAspLeuSerValArgHisCysThrAsn500505510AlaTyrMetLeuValTyrIleArgGluSerLysLeuSerGluValLeu515520525GlnAlaValThrAspHisAspIleProGlnGlnLeuValGluArgLeu530535540GlnGluGluLysArgIleGluAlaGlnLysArgLysGluArgGlnGlu545550555560AlaHisLeuTyrMetGlnValGlnIleValAlaGluAspGlnPheCys565570575GlyHisGlnGlyAsnAspMetTyrAspGluGluLysValLysTyrThr580585590ValPheLysValLeuLysAsnSerSerLeuAlaGluPheValGlnSer595600605LeuSerGlnThrMetGlyPheProGlnAspGlnIleArgLeuTrpPro610615620MetGlnAlaArgSerAsnGlyThrLysArgProAlaMetLeuAspAsn625630635640GluAlaAspGlyAsnLysThrMetIleGluLeuSerAspAsnGluAsn645650655ProTrpThrIlePheLeuGluThrValAspProGluLeuAlaAlaSer660665670GlyAlaThrLeuProLysPheAspLysAspHisAspValMetLeuPhe675680685LeuLysMetTyrAspProLysThrArgSerLeuAsnTyrCysGlyHis690695700IleTyrThrProIleSerCysLysIleArgAspLeuLeuProValMet705710715720CysAspArgAlaGlyPheIleGlnAspThrSerLeuIleLeuTyrGlu725730735GluValLysProAsnLeuThrGluArgIleGlnAspTyrAspValSer740745750LeuAspLysAlaLeuAspGluLeuMetAspGlyAspIleIleValPhe755760765GlnLysAspAspProGluAsnAspAsnSerGluLeuProThrAlaLys770775780GluTyrPheArgAspLeuTyrHisArgValAspValIlePheCysAsp785790795800LysThrIleProAsnAspProGlyPheValValThrLeuSerAsnArg805810815MetAsnTyrPheGlnValAlaLysThrValAlaGlnArgLeuAsnThr820825830AspProMetLeuLeuGlnPhePheLysSerGlnGlyTyrArgAspGly835840845ProGlyAsnProLeuArgHisAsnTyrGluGlyThrLeuArgAspLeu850855860LeuGlnPhePheLysProArgGlnProLysLysLeuTyrTyrGlnGln865870875880LeuLysMetLysIleThrAspPheGluAsnArgArgSerPheLysCys885890895IleTrpLeuAsnSerGlnPheArgGluGluGluIleThrLeuTyrPro900905910AspLysHisGlyCysValArgAspLeuLeuGluGluCysLysLysAla915920925ValGluLeuGlyGluLysAlaSerGlyLysLeuArgLeuLeuGluIle930935940ValSerTyrLysIleIleGlyValHisGlnGluAspGluLeuLeuGlu945950955960CysLeuSerProAlaThrSerArgThrPheArgIleGluGluIlePro965970975LeuAspGlnValAspIleAspLysGluAsnGluMetLeuValThrVal980985990AlaHisPheHisLysGluValPheGlyThrPheGlyIleProPheLeu99510001005LeuArgIleHisGlnGlyGluHisPheArgGluValMetLysArg101010151020IleGlnSerLeuLeuAspIleGlnGluLysGluPheGluLysPhe102510301035LysPheAlaIleValMetMetGlyArgHisGlnTyrIleAsnGlu104010451050AspGluTyrGluValAsnLeuLysAspPheGluProGlnProGly105510601065AsnMetSerHisProArgProTrpLeuGlyLeuAspHisPheAsn107010751080LysAlaProLysArgSerArgTyrThrTyrLeuGluLysAlaIle108510901095LysIleHisAsn1100<210>5<211>27<212>DNA<213>人工序列<400>5cgggatccatgctagcaatggatacgt27<210>6<211>27<212>DNA<213>人工序列<400>6gatatctcagctaaggatttcattaga27<210>7<211>28<212>DNA<213>人工序列<400>7ccgctcgagatgctagcaatggatacgt28<210>8<211>29<212>DNA<213>人工序列<400>8gctctagatcagctaaggatttcattaga29<210>9<211>24<212>DNA<213>人工序列<400>9gatatcaggttggtgtacctgtcc24<210>10<211>28<212>DNA<213>人工序列<400>10cccaagcttactgctttcctgaagtcac28<210>11<211>28<212>DNA<213>人工序列<400>11cgggatccacaggattgagaaatttggg28<210>12<211>26<212>DNA<213>人工序列<400>12gatatctcatacaccaggagttacta26<210>13<211>26<212>DNA<213>人工序列<400>13gatatctcataacttcaggtctccag26<210>14<211>27<212>DNA<213>人工序列<400>14cgggatcctgtgtggactgcaacacga27<210>15<211>28<212>DNA<213>人工序列<400>15cgggatccctacgacgtacattaagtgc28<210>16<211>28<212>DNA<213>人工序列<400>16cgtcgtagacagtgccatttctgagggt28<210>17<211>28<212>DNA<213>人工序列<400>17ggcactgtctacgacgtacattaagtgc28<210>18<211>20<212>DNA<213>人工序列<400>18tgccacctacctcaggttct20<210>19<211>20<212>DNA<213>人工序列<400>19ctggtctgagggatttcagg20<210>20<211>20<212>DNA<213>人工序列<400>20tcaaacgattcaggtggtca20<210>21<211>20<212>DNA<213>人工序列<400>21accgcggacaagtcatagat20<210>22<211>20<212>DNA<213>人工序列<400>22gaggaggacatggaggatga20<210>23<211>20<212>DNA<213>人工序列<400>23aagcgtggcatcaccataat20<210>24<211>20<212>DNA<213>人工序列<400>24tgtccgggacctgttagaag20<210>25<211>20<212>DNA<213>人工序列<400>25ggctcgttgcaggagataaa20<210>26<211>20<212>DNA<213>人工序列<400>26tgcaaaaggcttcagagaca20<210>27<211>20<212>DNA<213>人工序列<400>27ctctgttggggtgaaaggag20<210>28<211>20<212>DNA<213>人工序列<400>28tcccagagttcctccacaac20<210>29<211>20<212>DNA<213>人工序列<400>29attgagtgtccgctgcttct20<210>30<211>22<212>DNA<213>人工序列<400>30aggccaagcacgacaagtacat22<210>31<211>22<212>DNA<213>人工序列<400>31ctgatcttgccacacaggtagt22<210>32<211>20<212>DNA<213>人工序列<400>32aagcagacgcagatcttcac20<210>33<211>20<212>DNA<213>人工序列<400>33ctcgatctcctccttgctca20<210>34<211>20<212>DNA<213>人工序列<400>34gcaactcctgtcttgcattg20<210>35<211>20<212>DNA<213>人工序列<400>35cagttctgtggccttcttgg20<210>36<211>20<212>DNA<213>人工序列<400>36agtgggactgcatgtgtgtc20<210>37<211>20<212>DNA<213>人工序列<400>37gcagtctgtccaaggtttgc20<210>38<211>20<212>DNA<213>人工序列<400>38tggggaatgagttgaccttc20<210>39<211>20<212>DNA<213>人工序列<400>39gcacggttctggatcaatta20<210>40<211>20<212>DNA<213>人工序列<400>40gagtcaacggatttggtcgt20<210>41<211>20<212>DNA<213>人工序列<400>41gacaagcttcccgttctcag20<210>42<211>21<212>DNA<213>人工序列<400>42caacaagatgaagagcaccaa21<210>43<211>21<212>DNA<213>人工序列<400>43actgagaatggacattctaaa21<210>44<211>21<212>DNA<213>人工序列<400>44gagtatcaagttaaagcagaa21<210>45<211>21<212>DNA<213>人工序列<400>45cggatgatgaacttgtgcaat21<210>46<211>21<212>DNA<213>人工序列<400>46ttgtggttacgttatcaaata21<210>47<211>21<212>DNA<213>人工序列<400>47tcctaaggaccctgcaaatta21<210>48<211>21<212>DNA<213>人工序列<400>48gcacgacaagtacatggcgga21<210>49<211>21<212>DNA<213>人工序列<400>49tgccgccactatctgtgtaat21<210>50<211>38<212>DNA<213>人工序列<400>50gagaaatttgggaaatactagctatatgaattctgttc38<210>51<211>38<212>DNA<213>人工序列<400>51gaacagaattcatatagctagtatttcccaaatttctc38<210>52<211>35<212>DNA<213>人工序列<400>52gaatcagggagcgactagctacatgaacagcctgc35<210>53<211>35<212>DNA<213>人工序列<400>53gcaggctgttcatgtagctagtcgctccctgattc35<210>54<211>21<212>DNA<213>人工序列<400>54caacaagatgaagagcaccaa21<210>55<211>21<212>DNA<213>人工序列<400>55actgagaatggacattctaaa21<210>56<211>21<212>DNA<213>人工序列<400>56gagtatcaagttaaagcagaa21当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1