用于抑制天然心脏瓣膜、被支撑的心脏瓣膜或生物假体的狭窄、阻塞或钙化的装置和方法与流程
本发明涉及用于抑制天然心脏瓣膜和心脏瓣膜生物假体的狭窄、阻塞或钙化的装置和方法。
背景技术:
心脏是通过有节律地收缩来使血液循环贯穿生物体的身体的中空肌肉器官。在哺乳动物中,心脏具有四个腔室,其定位成使得右心房和右心室与左心房和左心室完全分离。通常,血液从全身性静脉流动到右心房,并且然后流动至右心室,经由肺动脉从所述右心室驱动到肺部。在从肺部返回后,血液进入左心房,并且然后流动到左心室,从所述左心室驱动到全身性动脉。
四个主要心脏瓣膜防止血液在有节律的收缩期间回流:三尖瓣、肺动脉瓣、二尖瓣以及主动脉瓣。三尖瓣分开右心房和右心室,肺动脉瓣分开右心房和肺动脉,二尖瓣分开左心房和左心室,并且主动脉瓣分开左心室和主动脉。通常,心脏瓣膜异常的患者的特征为患有瓣膜性心脏病。
心脏瓣膜的故障可以体现为未能适当打开(狭窄)或体现为渗漏(返流)。例如,具有功能障碍的主动脉瓣的患者可能被诊断为患有主动脉瓣狭窄或主动脉瓣反流。在任一情况下,通过手术方式进行瓣膜置换可以是可能的治疗。置换瓣膜可以是自体移植物、异体移植物或异种移植物以及机械瓣膜或者部分由其他动物(诸如猪或牛)的瓣膜制成的瓣膜。不幸的是,随着时间的推移,置换瓣膜本身易于发生问题诸如变性、血栓形成、钙化和/或阻塞。另外,瓣膜置换的过程可能引起周围组织穿孔,从而也导致狭窄、变性、血栓形成、钙化和/或阻塞。
因此,需要用于抑制心脏瓣膜的狭窄、阻塞或钙化的新方法和假体。
发明简述
上述问题通过根据本发明的用于抑制天然瓣膜和瓣膜假体的狭窄、阻塞或钙化的方法来解决。
在本发明的第一方面,所述方法通过经由刻痕基因1(notch1)蛋白裂解和糖原合成酶激酶磷酸化活化wnt路径,所述糖原合成酶激酶进而将β连环蛋白释放到核中以活化心脏瓣膜和/或假体的骨和软骨的形成减慢了二叶主动脉瓣(bav)钙化、三叶主动脉瓣钙化(tav)、经皮主动脉瓣置换(tavr)、手术生物假体主动脉瓣置换(sbavr)、二尖瓣粘液瘤样变性(mvmd)的进展。
在本发明的另一个方面,提供了减慢二尖瓣的狭窄、阻塞、钙化和/或反流的进展的若干治疗性医学疗法。确切地说,在高脂血症存在下,存在一氧化氮减少以及wnt3a被法尼基化以便分泌wnt,其进而结合至lrp5,另外对刻痕基因1进行拼接和灭活以便对细胞增殖细胞外基质蛋白合成进行cbfa1调节,以通过活化成骨程序启动骨形成。
在其他方面,本发明可以列出在以下编号的条款中:
1.一种用于抑制患者中植入的生物假体瓣膜的狭窄、阻塞或钙化的方法,其包括:
将生物假体瓣膜植入患者以置换天然心脏瓣膜;
在植入之后施用有效量的抗高脂血剂与pcsk9抗体的组合;以及
引起对所述生物假体瓣膜或天然瓣膜或二者的狭窄、阻塞或钙化的抑制。
2.根据条款1的方法,其中所述有效量的抗高脂血剂选自10mg至80mg的阿托伐他汀(atorvastatin)、10mg至40mg的辛伐他汀(simvastatin)、5mg至40mg的罗素伐他汀(rosuvastatin)、20mg至80mg的普伐他汀(pravastatin)、1mg至4mg的匹伐他汀(pitavastatin)以及其组合。
3.如条款3的方法,其中pcsk9的初始剂量是0.25mg/kg至约0.5mg/kg。
4.如条款3的方法,其中pcsk9的随后剂量是约1mg/kg至约1.5mg/kg。
5.如条款4的方法,其中所述初始剂量和所述随后剂量的时间间隔约为一周。
6.如条款1的方法,其还包括施用有效量的法尼基转移酶抑制剂。
7.如条款6的方法,其中所述法尼基转移酶抑制剂包括洛那法尼(lonafarnib)并且所述有效量包括115mg/m2至150mg/m2。
8.如条款7的方法,其还包括施用等于10mg的量的依折麦布(zetia)。
9.如条款1的方法,其中所述生物假体瓣膜是生物假体主动脉瓣。
10.如条款1的方法,其中所述生物假体瓣膜是生物假体二尖瓣。
11.如条款1的方法,其中所述生物假体瓣膜是生物假体肺动脉瓣。
12.如条款1的方法,其中所述生物假体瓣膜是生物假体三尖瓣。
13.如条款1的方法,其中所述生物假体瓣膜包括生物来源的一个或更多个尖瓣。
14.如条款13的方法,其中所述一个或更多个尖瓣是猪的、牛的或人类的尖瓣。
15.如条款13的方法,其还包括将编码一氧化氮合成酶的核酸引入到一个或更多个尖瓣。
16.如条款13的方法,其还包括将药物洗脱治疗编码物引入所述一个或更多个具有抗增殖和抗钙化处理的尖瓣的两侧上。
17.如条款1的方法,其还包括施用等于80mg/天的量的阿司匹林。
18.如条款1的方法,其还包括施用有效量的口服p2y12抑制剂。
19.如条款18的方法,其中所述p2y12抑制剂选自氯吡格雷(clopidogrel)、普拉格雷(prasugrel)、替格瑞洛(ticagrelor)以及其组合。
20.如条款19的方法,其中所述氯吡格雷的有效量在植入时是300mg的负荷剂量并且在之后是75mg/天的维持剂量。
21.如条款19的方法,其中所述普拉格雷的有效量在植入时是60mg的负荷剂量并且在之后是10mg/天的维持剂量。
22.如条款19的方法,其中所述替格瑞洛的有效量在植入时是180mg的负荷剂量并且在之后是每天两次90mg的维持剂量。
附图说明
以下详细描述,通过实例的方式给出,但不旨在将本发明仅限制为所述特定实施方式,最好可结合附图来理解。
图1是描绘在高血脂症存在下瓣膜钙化的信号传导机制的图。
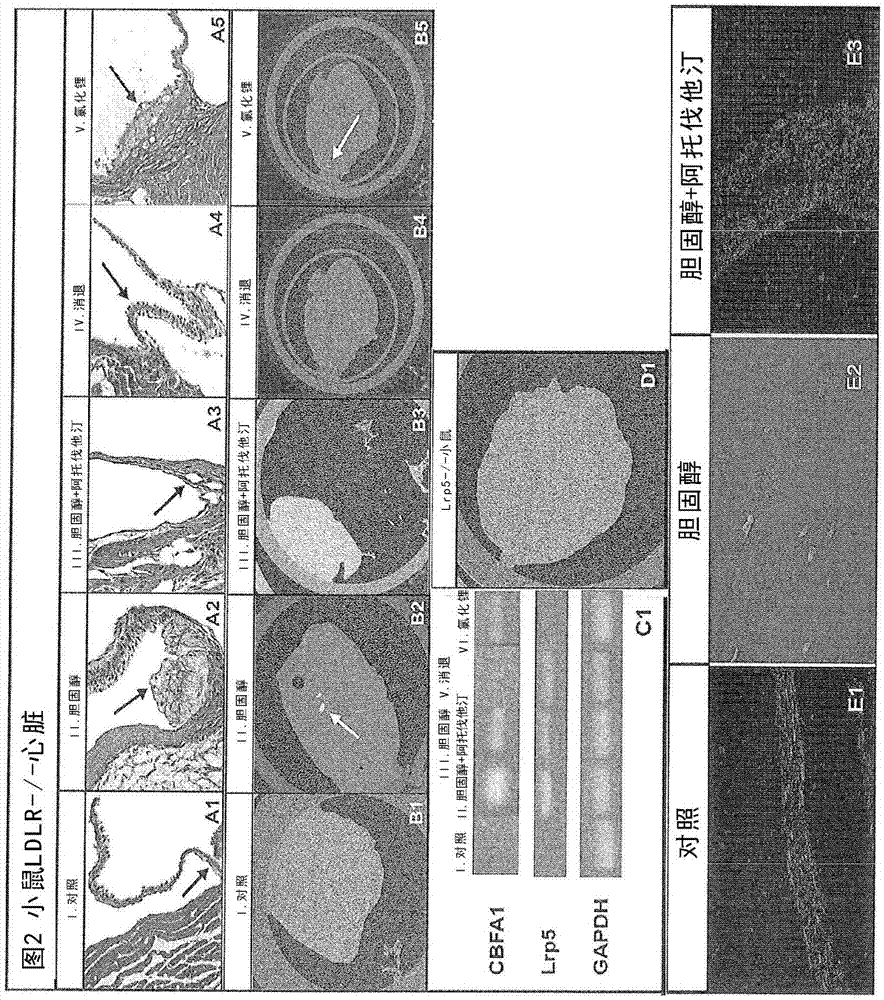
图2是示出在不具有ldl受体的小鼠瓣叶中在胆固醇膳食、氯化锂膳食的存在下天然瓣膜动脉粥样硬化和具有阿托伐他汀处理的瓣叶减弱的初始数据图。
图3的子图a描绘了在逐渐增加的剂量的增加细胞增殖的氯化锂的情况下成肌纤维细胞的直接处理的体外数据。
图3的子图b是使用阿托伐他汀的dkk1抑制和lrp5直接抑制。
图4证明了通过组织形态、rtpcr和超声心动描记术定义的enos表型的特征。
图4的子图a描绘了bav的组织形态。
图4的子图b描绘了来自bavenos-/-小鼠的半定量rtpcr以及二尖瓣对比三尖瓣主动脉瓣的超声心动图数据。
图4的子图c是描绘来自不同膳食的enos无效小鼠的超声心动图的表。
图5是示出在天然瓣叶中在高血脂症存在下经由在内皮细胞至成肌纤维细胞之间的信号传导而发展疾病过程的细胞层的示意图,所述信号传导活化wnt分泌以打开lrp5受体,进而活化天然成肌纤维细胞中的骨形成以及不同抑制剂和口服药剂来减慢疾病的进展。
图6是示出具有主动脉瓣的主动脉的示意图,所述主动脉瓣具有天然瓣膜或生物假体的细胞,其中支架周围的主动脉已部分地被狭窄阻塞,所述狭窄继发于来自主动脉附近的支架的损伤之后的血管平滑肌细胞增殖和骨形成细胞分化,以及继发于炎症的向骨形成细胞的c-kit干细胞或体内成肌纤维细胞的增殖和分化和变成骨形成细胞的c-kit干细胞的归巢;以及药物(包括他汀类、前蛋白转化酶枯草溶菌素克新类型9拮抗剂抗体(“pcsk9抗体”)以及法尼基转移酶(“fti”)抑制剂)的作用。
图7描绘了在失效(failed)生物假体心脏的手术瓣膜置换时在来自人类患者的外植瓣膜中的血管翳(pannus)形成和钙化,所述形成和钙化继发于增殖的间质干细胞附着至瓣膜和支架,其钙化并引起瓣叶和支架破坏。
图8是表明附着至钙化的心脏瓣膜的ckit阳性干细胞的rna表达的图。
图9描绘在生物假体瓣膜钙化的兔模型中测试80mg/天的抗炎药物阿托伐他汀的结果,其中对照膳食显示出较少的动脉粥样硬化,胆固醇膳食证实严重的动脉粥样硬化以及在胆固醇膳食情况下的阿托伐他汀疗法证实动脉粥样硬化减弱。
技术实现要素:
本发明提供了一种用于在有需求的患者中在植入瓣膜假体之后抑制天然瓣膜、被支撑的主动脉和瓣叶或具有或不具有缝合环(sewingring)的生物假体的狭窄、阻塞或钙化的方法,其可以包括一旦部署弹性支架、高泰克斯覆盖件和生物假体就对于具有早期至晚期证据疾病的证据的瓣膜心脏病使用口服药物疗法进行处理,其中单独或组合使用一种或更多种治疗剂的口服疗法改进假体材料(包括支架、瓣膜和高泰克斯覆盖件)的钙化抑制和寿命改善的效率,通过经由刻痕基因1蛋白裂解和糖原合成酶激酶磷酸化活化wnt路径,所述糖原合成酶激酶进而将β连环蛋白释放到核中以活化心脏瓣膜和/或假体的骨和软骨形成以确切地减慢二叶主动脉瓣(bav)钙化、三叶主动脉瓣钙化(tav)、经皮主动脉瓣置换(tavr)、手术生物假体主动脉瓣置换(sbavr)、二尖瓣粘液瘤样变性(mvmd)的进展,并且本发明将包括减慢二尖瓣的狭窄、阻塞、钙化和/或反流的进展。
如本文所公开,本发明人还开发了一种用于抑制天然心脏瓣膜和生物假体瓣膜(在将所述生物假体瓣膜手术植入在具有壁的血管中之后)的狭窄、阻塞或钙化的方法。当天然瓣膜发展瓣膜性疾病时以及在用生物假体瓣膜手术置换天然患病瓣膜时,为患者提供了一系列单独或组合的医学处理。生物假体瓣膜可以包括经由活化天然瓣叶中的成骨和软骨形成的弹性支架和/或间质干细胞附着之后具有成骨形成可能性的生物假体瓣叶(在图2中清晰地可见),在不具有ldl受体的小鼠瓣叶中在阿托伐他汀处理的情况下在胆固醇膳食、氯化锂膳食和瓣叶减弱存在下天然瓣膜动脉粥样硬化的发展。图3表明了在阿托伐他汀存在下在细胞增殖活化和dk1灭活中氯化锂的直接处理对成肌纤维细胞的作用。
本文还提供了一种抑制刻痕基因1受体的拼接的方法,其通过使用降脂药他汀类与将抑制ldl受体以调节脂质水平的pcsk9抗体的组合处理瓣膜来进行。法尼基转移酶(“fti”)抑制剂抑制wnt的法尼基化以抑制wnt3a与lrp5受体的结合,所述受体在高血脂症存在下调节成肌纤维细胞以经由成骨路径进行分化。fti抑制剂是可逆地结合至法尼基转移酶caax结合位点的小分子。fti抑制剂通过减少wnt3a的法尼基化将抑制细胞附着中的wnt3a活化,所述细胞附着中的wnt3a活化形成假体瓣叶中的疾病和/或天然瓣膜细胞增殖和/或骨形成,如图5中表明,所述wnt3a的法尼基化对于wnt3a/lrp5/卷曲蛋白(frizzled)复合物的活化而言是关键的。
抑制细胞增殖和钙化的治疗剂与有效量的他汀和pcsk9抗体组合通过降低高血脂症状态下的炎症来抑制细胞附着和/或天然瓣膜细胞增殖和/或骨形成。pcsk9是血浆脂蛋白胆固醇(ldl-c)的调节剂。前蛋白转化酶枯草溶菌素/克新类型9(pcsk9)蛋白调节低密度脂蛋白(ldl)受体的活性。使用单克隆抗体抑制pcsk9导致ldl受体的增加的循环和ldl胆固醇(ldl-c)的增加的清除率。在肝脏中高度表达的pcsk9在原功能域自动催化裂解之后分泌,所述原功能域保持与如图5中所示的催化结构域非共价缔合,经由pcsk9抗体与他汀药剂组合抑制ldlr受体。这些治疗剂与有效量的法尼基转移酶抑制剂(fti)组合抑制细胞增殖和钙化,所述fti抑制剂通过减少wnt3a的法尼基化来抑制细胞附着中的wnt3a活化和/或天然瓣膜细胞增殖和/或骨形成,所述细胞附着中的wnt3a活化形成假体瓣叶中的疾病,如图5中表明,所述wnt3a的法尼基化对于wnt3a/lrp5/卷曲蛋白复合物的活化而言是关键的。
如图6所示,在患有天然瓣膜疾病和/或具有手术或皮下放置的生物假体瓣膜的患者中,本文所提供的处理和方法与本文所公开的治疗剂的组合将减慢生物假体(植入生物假体瓣膜之后的)或天然瓣膜的或二者的钙化、狭窄、反流和阻塞的进展,抑制和/或减慢生物假体(植入生物假体瓣膜之后的)或天然瓣膜的或二者的狭窄、阻塞和/或钙化的进展。
将安装在弹性支架上的生物假体可收缩的弹性瓣膜固定在患者中的所需位置处,以使得弹性支架与可能已手术去除或未去除的天然瓣膜接触并且任选地使用医学疗法进行治疗以抑制能够在固定生物假体瓣膜的瓣叶、支架或缝合环的两侧上形成钙化的干细胞附着,从而抑制在植入被支撑的瓣膜假体之后,或在有需求的患者中或手术置换置换天然瓣膜的生物假体的患者中,或在具有早期至晚期瓣膜化疾病过程的患者中的被支撑的主动脉的狭窄、阻塞或钙化。
如本文所用的,术语“狭窄”可以是指心脏瓣膜的可以阻断或阻塞血液从心脏流出并引起心脏内的血流和压力积聚(back-up)的缩小(narrowing)。瓣膜狭窄可由各种原因引起,包括但不限于由于疾病诸如风湿热引起的瘢痕形成;经由瓣叶上的骨形成的进行性钙化;进行性磨损和刺破;以及其他原因。
如本文所用的,术语“瓣膜”可以是指防止在有节律的收缩期间血液回流的四个主要心脏瓣膜中的任一个。四个主要心脏瓣膜是三尖瓣、肺动脉瓣、二尖瓣以及主动脉瓣。三尖瓣分开右心房和右心室,肺动脉瓣分开右心房和肺动脉,二尖瓣分开左心房和左心室,并且主动脉瓣分开左心室和主动脉。
在所述方法的一个实施方式中,生物假体瓣膜和患病瓣膜可以是主动脉瓣、肺动脉瓣、三尖瓣或二尖瓣。
如本文所用的,术语“瓣膜假体”可以是指用于置换或补充缺陷的、功能障碍的或损失的心脏瓣膜的装置。瓣膜假体的实例包括但不限于生物假体、机械假体以及类似假体,包括ats
通常,生物假体包括具有一个或更多个尖瓣的瓣膜并且所述瓣膜安装在框架或支架上,二者通常具有弹性。如本文所用的,术语“弹性的”意指装置能够弯曲、折叠、扩展或其组合。瓣膜的尖瓣通常由哺乳动物的组织制成,所述哺乳动物例如但不限于猪(猪的)、牛(牛的)、马、绵羊、山羊、猴以及人类。
根据本发明的方法,瓣膜可以是具有一个或更多个尖瓣的可收缩的弹性瓣膜并且所述可收缩的弹性瓣膜可以安装在弹性支架上。
在一个实施方式中,可收缩的弹性瓣膜可以包括生物来源的一个或更多个尖瓣。
在另一个实施方式中,所述一个或更多个尖瓣是猪的、牛的或人类的尖瓣。
生物假体的实例可以包括具有一个或更多个尖瓣的可收缩的弹性瓣膜并且所述可收缩的弹性瓣膜安装在弹性支架上,所述瓣膜包括但不限于edwardslifesciences制造的sapien经导管心脏瓣膜以及由medtronic制造的
用于本发明中的瓣膜假体的弹性支架部分可以是可自我展开的或通过气球导管的方式可展开的。弹性支架可以包括本领域普通技术人员已知的任何生物相容性材料。生物相容性材料的实例包括但不限于陶瓷类;聚合物类;不锈钢;钛;镍-钛合金,诸如镍钛诺;钽;含有钴的合金,诸如
根据本发明的方法,组合使用一种或更多种治疗剂对患者进行口服治疗以在高血脂症存在下抑制图1中发展的瓣膜钙化的发展,存在一氧化氮降低并且wnt3a被法尼基化以便分泌wnt,其进而结合至lrp5,另外拼接和灭活刻痕基因1以便启动细胞增殖以及经由cbfa1的活化启动细胞增殖以及通过活化表1中列出的成骨程序来启动骨形成。
一旦瓣叶内骨形成活化,在成肌纤维细胞和/或干细胞附着至瓣膜假体和/或弹性支架附着至生物假体时,成肌纤维细胞和/或干细胞向骨形成分化。瓣膜假体的弹性支架部分可以任何圆柱形的形状(最终形状是圆柱形,可以是最初接触瓣膜或瓣膜壁所需要的所有漏斗形),其中在不受理论约束的情况下,治疗剂通过瓣膜或瓣膜壁或主动脉(包括主动脉瓣、二尖瓣、三尖瓣、腔静脉瓣)释放和吸收。
在一个实施方式中,弹性支架部分可以是基本上呈圆柱形的以便能够在固定时接触瓣膜或瓣膜壁。
在另一个实施方式中,弹性支架部分的直径可以是约15mm至约42mm。
根据本发明的一个实施方式,所述方法还可以包括将编码一氧化氮合成酶的核酸引入到瓣膜假体的一个或更多个尖瓣中。在2003年12月9日授予的美国专利号6,660,260中描述了用于将编码一氧化氮合成酶的核酸引入到一个或更多个尖瓣中的方法并且所述专利以引用的方式整体并入本文中。
如图1中清晰可见,若干治疗性医学疗法减慢了二尖瓣的狭窄、阻塞、钙化和/或反流的进展。在高脂血症存在下,存在一氧化氮减少并且wnt3a被法尼基化以便分泌wnt,其进而结合至lrp5,另外对刻痕基因1进行拼接和灭活以便对细胞增殖细胞外基质蛋白合成进行cbfa1调节,通过活化成骨程序启动骨形成。
如图2中清晰可见,向在低密度脂蛋白受体不存在下给予遗传修饰的小鼠实验性高胆固醇膳食,图2的子图a1是对照膳食,图2的子图a2是胆固醇膳食,图2的子图a3是具有动脉粥样硬化改善的胆固醇+阿托伐他汀膳食,图2的子图a4是具有使用胆固醇的处理的消退膳食和半途的(halfway)膳食阿托伐他汀处理,并且图2的子图a5使用氯化锂膳食的处理在胆固醇缺乏下诱导动脉粥样硬化病变,但具有糖原合成酶激酶的抑制以抑制lrp5/β连环蛋白路径。图2的子图b1-b5是图2的子图a中定义的瓣叶中来自相应膳食的显微ct数据,图b1对照膳食没有钙化的证据,图2的子图b2胆固醇膳食表明钙化增加,图2的子图b3和b4阿托伐他汀处理没有钙化的证据并且使用氯化锂膳食的图2的子图b5证实心脏瓣膜中的显微钙化。图2的子图c1证实在胆固醇处理和lrp5基因表达中骨转录因子cbfa1的增加的基因表达。lrp5无效小鼠没有心脏钙化的证据。图2的子图e是β连环蛋白的染色共聚焦显微镜检查,所述连环蛋白转位至核中以活化lrp5下游的骨形成。图2的子图el表明了在胆固醇膳食处理中β-连环蛋白到核中的正平移(positivetranslocation)。
图3的子图a描绘了在逐渐增加剂量的氯化锂增加细胞增殖的情况下成肌纤维细胞的直接处理的体外数据。
图3的子图b是使用阿托伐他汀的dkk1抑制和lrp5的直接抑制。
图4证明了如组织形态、rtpcr和超声心动描记术定义的enos表型的特征。图4的子图a是bav的组织形态,图4的子图b是来自bavenos-/-小鼠的半定量rtpcr,以及二尖瓣对比三尖瓣主动脉瓣的超声心动图数据。参考图4的子图c,为了理解具有bav表型的enos-/-小鼠是否比经由lrp5路径活化的三尖瓣主动脉瓣更早地发展加速的狭窄,向enos-/-小鼠给予胆固醇膳食对比胆固醇和阿托伐他汀。还进行超声心动图血流动力学以确定在食用不同膳食的二尖瓣对比三尖瓣主动脉enos-/-小鼠中的狭窄时间。为了进一步理解二尖瓣主动脉瓣疾病的机制,在大量小鼠中使用对照膳食(n=60)、胆固醇膳食(n=60)和胆固醇+阿托伐他汀膳食(n=60)测试enos无效小鼠。在处死之前,进行二尖瓣主动脉瓣的存在和不存在的超声心动图,并且图4的子图c是来自食用不同膳食的enos无效小鼠的超声心动图。通过蛋白质和rna表达测量经典wnt路径的notchl、wnt3a和下游标记物。减少notchl蛋白质并且rna表达证实了使用脂质处理的类似拼接变体,其在对照和阿托伐他汀处理的情况下是不存在的。胆固醇膳食增加了经典wnt路径的成员并且阿托伐他汀显著减少了这些标记物(p<0.05)。
如图1-图5所示的,示出了lrp5wnt路径的活化在此疾病过程的发展中,尤其是在缺乏ldl受体的遗传小鼠中的作用。还示出了在活化β连环蛋白以启动细胞增殖和额外细胞基质产生的氯化锂膳食存在下的动脉粥样硬化发展。
参考图5,其描绘了显示在天然瓣叶中发展疾病过程的细胞层的示意图。在高血脂症存在下内皮细胞至成肌纤维细胞之间的信号传导活化了wnt的分泌以打开lrp5受体,进而活化天然成肌纤维细胞中的骨形成。表1中列出的不同抑制剂和口服药剂抑制或减慢疾病的进展。
图5进一步描述了pcsk9作为血浆脂蛋白胆固醇(ldl-c)的调节剂的作用以及作为有效减少冠状动脉疾病的风险的药剂的作用。前蛋白转化酶枯草溶菌素/克新类型9(pcsk9)蛋白调节低密度脂蛋白(ldl)受体的活性。使用单克隆抗体抑制pcsk9导致ldl受体的循环增加以及ldl胆固醇(ldl-c)的清除率的增加。在肝脏中高度表达的pcsk9在原功能域自动催化裂解之后分泌,所述原功能域保持与催化结构域非共价缔合。pcsk9的催化结构域结合至低密度脂蛋白受体(ldlr)的表皮生长因子样重复a(egf-a)结构域。需要pcsk9的两种功能性以靶向用于溶酶体降解的ldlr-pcsk9复合物并降低ldl-c,这与连接至功能缺失和功能增加的两种结构域的突变一致1。
本发明提供了用于长期减少血液中的ldl-c水平的治疗方案,其通过与如下表1中列出的对于患有以下疾病的患者的ldl-c血浆水平有作用的他汀药剂的组合抑制pcsk9活性以及pcsk9的相应作用:主动脉瓣疾病、二尖瓣脱垂和/或生物假体瓣膜(包括经皮主动脉瓣)置换。
表1表明了单独的和组合的不同口服疗法通过经由刻痕基因1蛋白裂解和糖原合成酶激酶磷酸化活化wnt路径,所述糖原合成酶激酶进而将β连环蛋白释放到核中以活化心脏瓣膜和/或假体的骨和软骨形成减慢以下的进展:二叶主动脉瓣(bav)钙化、三叶主动脉瓣钙化(tav)、经皮主动脉瓣置换(tavr)、手术生物假体主动脉瓣置换(sbavr)、二尖瓣粘液瘤样变性(mvmd),并且本发明将包括减慢二尖瓣的狭窄、阻塞、钙化和/或反流的进展的若干治疗性医学疗法。抗高脂血剂包括与有效量的10mg至80mg范围内的阿托伐他汀、10mg至40mg范围内的辛伐他汀、5mg至40mg的罗素伐他汀、20mg至80mg的普伐他汀、1mg至4mg的匹伐他汀以及pcsk9抗体的组合,初始剂量可以是约0.25mg/kg、约0.5mg/kg、约1mg/kg或约1.5mg/kg,并且初始剂量和第一随后剂量以及另外的随后剂量的时间可以间隔约一周,或者与fti抑制剂诸如范围为115mg/m2至150mg/m2的115mg/m2剂量的洛那法尼的组合、与10mg有效量的依折麦布组合。其他有效的fti抑制剂包括烷基衣康酸(chaetomellicacid)a、fpt抑制剂i、fpt抑制剂ii、fpt抑制剂iii、ft酶抑制剂i、ft酶抑制剂ii、fti-276三氟乙酸盐、fti-277三氟乙酸盐、ggti-297、姜辣素、胶霉毒素、l-744,832二盐酸盐、手霉素a、替吡法尼、a-羟基法尼基膦酸。
表1
图2表明了定义胆固醇在lrp5受体活化中的作用的数据并且瓣膜钙化实验表明动脉粥样硬化并且在ldlr-/-小鼠的主动脉瓣中发展了钙化。此数据表征了这些小鼠中的心脏,以确定脂质是否影响这些组织中的骨形成以及他汀类是否可以改进骨生物学。来自此研究的结果由以下五个处理组获得:第i组:对照膳食,第ii组:实验性高胆固醇血症0.2%(v/v)膳食,并且第iii组:实验性高胆固醇血症0.2%(v/v)膳食和阿托伐他汀0.1%(v/v),持续12周,第iv组:6周胆固醇膳食并且然后6周单独的阿托伐他汀0.1%(v/v)作为消退治疗组,以及第v组:单独的氯化锂膳食0.12%(v/v)(每个处理组n=20)。对主动脉瓣执行马森三色染色以评定动脉粥样硬化和早期矿物化。
图2是来自5个不同处理组的马森三色光学显微镜(40x)和主动脉瓣的显微ct数据的复合体。图2的子图a1显示对照主动脉瓣不会发展任何动脉粥样硬化的证据。图2的子图a2表明高胆固醇主动脉瓣发展了钙化的动脉粥样硬化病变。所述病变沿着主动脉瓣的主动脉表面发展。图2的子图a3是来自胆固醇加上阿托伐他汀处理组的主动脉瓣,其显示沿着瓣叶的动脉粥样硬化病变的显著改善。图2的子图a4显示第iv组消退处理主动脉瓣不会具有沿着主动脉瓣表面的任何动脉粥样硬化的证据。图2的子图a5表明糖原合成酶激酶的直接抑制剂氯化锂的作用。使用氯化锂的处理增加了细胞内的β连环蛋白水平并且因此经由将β连环蛋白转位至核中并活化lef/tcf转位因子来启动骨形成。此数据表明动脉粥样硬化病变在氯化锂主动脉瓣中的证据。图a5中的箭头指向动脉粥样硬化病变。离体显微ct分析显示钙化是否在来自不同处理组的主动脉瓣中发展。在使用和不使用如上文所列出的阿托伐他汀的情况下使用胆固醇处理ldlr-/-小鼠并且在处死之后在显微ct扫描仪中进行离体扫描。图2的子图b显示来自五个处理组的ldlr-/-小鼠的初步显微ct数据。在每张图中的白色区域指示瓣叶中的钙化证据。灰色区域是每个瓣叶中的未钙化区域。蓝色区域是计算机赋予此数据的背景。图2的子图b1是对照膳食(第i组),其中主动脉瓣不会发展任何钙化证据。胆固醇(第ii组)处理的小鼠发展早期矿物化区域,如图2的子图b2所示的显微ct扫描中存在的两个白色钙化区域所示的。阿托伐他汀(第iii组)处理的心脏不会发展任何钙化,如图2的子图b3所示的。图2的子图b4显示消退处理(第iv组)主动脉瓣也不会发展任何矿物化证据。图2的子图c1表明了不同处理组的rtpcr数据。rtpcr显示在胆固醇膳食(第ii组)的情况下cbfal和lrp5受体基因表达的增加,以及阿托伐他汀处理在主动脉瓣中在使用阿托伐他汀的12周治疗(第iii组)中降低cbfal和lrp5表达,以及在6周阿托伐他汀消退处理(第iv组)中进一步降低cbfal和lrp5基因表达。最终,氯化锂处理表明了在无任何lrp5表达的情况下的cbfal增加。对照膳食(第i组)未显示lrp5表达并且未显示cbfal表达。图2的子图d1是对照lrp5-/-处理的小鼠。在lrp5-/-小鼠中没有钙化的证据2,3。
最终,使用共聚焦显微镜检查主动脉瓣中的β-连环蛋白表达。图2的子图e证实了在三个膳食组中β-连环蛋白表达的共聚焦显微镜检查。子图e1显示了对照瓣膜中的少量细胞质β-连环蛋白表达。子图e2显示了位于核内的β-连环蛋白表达的增加,并且子图e3表明了β-连环蛋白表达的减弱。
图6-图9描绘了在手术瓣膜置换失效的生物假体心脏瓣膜时在来自人类患者的外植瓣膜中的血管翳形成和钙化过程。对照生物假体瓣膜对比来自人类的外植生物假体瓣膜。子图(al)对照瓣膜的心室表面,子图(a2)具有经由干细胞附着至心脏瓣膜的血管翳和钙化过程的患病瓣膜的心室表面。图7是表明附着至钙化的心脏瓣膜从而引起钙化过程发生在瓣膜上的ckit阳性间质干细胞的rna表达的图,如由已熟知的骨转录因子cbfal(核结合因子al)和opn(骨桥蛋白)以及细胞外基质蛋白所表达的。将结果表达为对照的百分比,其中对照对于所有这些标记物为0。gapdh是用作实验的对照的看家基因。图8证实了在患病生物假体瓣膜中与对照相比的ckit基因表达增加。
图9中来自对照动物的植入瓣叶似乎沿着瓣叶表面具有中等量的细胞浸润,如通过图9的子图a1的马森三色染色所表明。高功率放大表明了瓣叶与沿着瓣叶表面发展的细胞浸润之间的界线。在对照生物假体瓣膜中存在少量ckit阳性染色细胞(图9的子图b1),以及中等量的表达骨桥蛋白的增殖细胞,如图9的子图c1和d1所示的。相比之下,在来自胆固醇喂食的兔的瓣膜组织中(图9的子图a2、b2、c2、d2),存在显著的细胞浸润,如马森三色所示的,组织浸润物表达ckit、pcna和opn。最后,如通过半定量目视分析所测量的,在外植时并且在光学显微镜下,在胆固醇处理下,动脉粥样硬化负荷增加四倍。在阿托伐他汀处理的兔中的植入瓣叶表明动脉粥样硬化斑块负荷、增殖、ckit和骨桥蛋白表达的量的显著降低,如图9的子图a3、b3、c3、d3。
图9描绘了来自用于测试减少炎症并且也减少瓣叶上的血管翳形成的阿托伐他汀的剂量的实验动物的结果。实验程序如下,将重2.5-3.0kg的雄性新西兰白兔分配至对照(n=10)或0.5%胆固醇喂食组(n=10)或胆固醇喂食和阿托伐他汀组(n=10)。所有动物均随意进食,持续12周。向对照兔喂食标准膳食。胆固醇喂食动物接受补充有0.5%(w/w)胆固醇(purinamills,woodmont,in)的膳食,并且对于他汀处理组向胆固醇喂食和阿托伐他汀组给予每天口服3.0mg/kg阿托伐他汀。在开始膳食之前,兔经历使用肌内氯胺酮/甲苯噻嗪(40/5mg/kg)进行的牛心包生物假体瓣膜组织(perimount,edwards,irvineca)手术植入。在此12周时段之后,使用肌内氯胺酮/甲苯噻嗪(40/5mg/kg)麻醉兔并且使其经历通过心脏内施用1mlbeuthanasia进行的安乐死。在从皮下植入位点移除之后立即将生物假体瓣膜固定在4%缓冲福尔马林中持续24小时然后包埋在石蜡中。切割石蜡包埋的切片(6μm)并且用马森三色染色进行染色以用于组织病理学检查。
下表2描绘了测试等效于人类剂量的80mg/天的抗炎药阿托伐他汀的结果,并且显示使用阿托伐他汀处理的瓣膜上的干细胞rna表达的百分比减少和干细胞介导的血管翳形成的减少。
表2表明对照、胆固醇和胆固醇加上阿托伐他汀实验测定的rna基因表达。与对照和阿托伐他汀组相比,胆固醇进食动物的瓣叶中存在sox9、成骨细胞转录因子、周期素和ckit的增加(p<0.05)。表1是来自实验模型的rtpcr数据。与对照测定相比,血清胆固醇水平在胆固醇喂食组中显著更高(1846.0±525.3mg/dl对比18.0±7mg/dl,p<0.05)。阿托伐他汀处理的实验组表现出比单独的胆固醇膳食更低的胆固醇水平(824.0±152.1mg/dl,p<0.05)。与对照测定相比,在胆固醇喂食组中存在hscrp血清水平的增加(13.6±19.7对比0.24±0.1,p<0.05),其通过阿托伐他汀减少(7.8±8.7,p<0.05)。在使用和不使用等效于人类的80mg/天的剂量的阿托伐他汀的情况下在实验性高胆固醇血症的兔模型中测试这些测定。执行先前的实验以测试20mg/天和40mg/天的较低剂量范围的阿托伐他汀并且在较低剂量范围内不存在治疗益处。
他汀作为抗炎剂与抗增殖剂和抗钙化剂组合的作用机制将介导钙化和干细胞附着的抑制。阿托伐他汀与抗增殖剂的组合通过活化瓣膜内的内皮一氧化氮合成酶减少ckit干细胞附至瓣膜来减少瓣膜的进一步破坏。在抑制这些组织中的钙化的两种模型中,成肌纤维细胞增殖和细胞外基质的生产减少95%,使用表1中所列出的药物组合可以抑制图1-图9所列出的疾病的各种水平的活化。
另外,处理可以包括使用上述抗高脂血剂和pcsk9抗体与抗血小板疗法诸如阿司匹林和/或p2y12抑制剂(包括氯吡格雷、普拉格雷、替格瑞洛)的组合。在嘌呤信号传导领域,主要地但不是独占性地在血小板表面上发现p2y12蛋白,并且所述蛋白是重要的血液凝结调节剂。p2y12属于g蛋白偶联(gpcr)嘌呤受体组的gi类并且是腺苷二磷酸(adp)的化学受体。
有效地与预防天然和/或生物假体心脏瓣膜钙化的处理组合使用的剂量是:氯吡格雷在植入时是300mg的负荷剂量和之后75mg/天的维持剂量;普拉格雷在植入时是60mg的负荷剂量和之后10mg/天的维持剂量;以及替格瑞洛在植入时是180mg的负荷剂量和之后每天两次90mg的维持剂量。
根据本发明的患者处理进一步抑制一个或更多个尖瓣中的内皮细胞的低密度脂蛋白受体;在一个或更多个尖瓣中的成肌纤维细胞和/或间质干细胞中的lrp5受体和一个或更多个尖瓣中的内皮细胞中的wnt3a分泌。
尽管本发明已参考各个方面和实施方式来描述,但是本领域普通技术人员将认识到,可以在不脱离本发明的精神和范围的情况下对形式和细节作出改变。
- 还没有人留言评论。精彩留言会获得点赞!