HFn包载阿霉素的方法及其产物与流程
本发明涉及hfn(人h铁蛋白,即由人铁蛋白的h亚基自组装形成的铁蛋白)包载阿霉素(dox)的方法及其产物。具体而言,本发明涉及利用脲或盐酸胍解聚、复性hfn并包载阿霉素的方法及产物。
背景技术:
铁蛋白(ferritin)是参与和维持铁代谢平衡的重要功能蛋白,它是一类广泛存在于动植物及微生物细胞中含高铁量的蛋白质。从细菌到人类,尽管不同生物的铁蛋白氨基酸序列具有极大的差别,但其结构相似。典型的铁蛋白结构是由蛋白外壳和铁内核两部分构成,其中蛋白外壳是由24个亚基自组装形成的笼状结构(外径12nm,内径8nm),铁内核的主要成分为水铁矿(5fe2o3·9h2o)。铁蛋白外壳通常是由两种蛋白亚基(h和l)组成。在机体不同组织和器官中,铁蛋白分子中含有h和l亚基的比例有所不同。
人h铁蛋白(hfn)是指由人铁蛋的h亚基自组装形成的铁蛋白。由人铁蛋白的h亚基可以自组装形成笼状蛋白,所包含的人铁蛋白的h亚基数目通常为24。人h铁蛋白的全长氨基酸序列如seqidno:1所示。
mttastsqvrqnyhqdseaainrqinlelyasyvylsmsyyfdrddvalknfakyflhqsheerehaeklmklqnqrggriflqdikkpdcddwesglnamecalhleknvnqsllelhklatdkndphlcdfiethylneqvkaikelgdhvtnlrkmgapesglaeylfdkhtlgdsdnes(seqidno.1)
根据文献报道,不同来源铁蛋白的药物装载,主要依赖于两种方式:1、药物在特定处理条件下,通过铁蛋白上的离子通道或疏水通道,进入蛋白壳内部;2、利用低ph值或高浓度脲,使蛋白壳发生解聚,在随后的复聚过程中加入待包载药物,进而实现药物在蛋白壳内部的装载。上述的包载方法中,尤其以高浓度脲条件下的hfn包载阿霉素效率最高,达到每分子hfn装载33分子阿霉素;该方法的简要步骤为:将人hfn加入终浓度大于6m的脲中,室温下反应30分钟,随后加入适量阿霉素试剂,并避光反应10分钟,然后使用透析的方法,将反应体系中的脲浓度逐级递减至0,从而实现阿霉素在hfn中的包载。相比其他包载方法,虽然高浓度脲法有效地提高了阿霉素在hfn中的装载量,但是距离临床用药需求仍有较大的差距,按照1分子铁蛋白装载33分子的阿霉素计算,临床单次给药所需的蛋白质量就达到了克级水平,显著超出了现有蛋白质药物的最高给药剂量(百毫克级)。为了满足临床用药需求,本领域必须开发载药量更大的hfn药物包载方法。
阿霉素是一种抗肿瘤抗生素,可抑制rna和dna的合成,对rna的抑制作用最强,抗瘤谱较广,对多种肿瘤均有作用,属周期非特异性药物,对各种生长周期的肿瘤细胞都有杀灭作用。主要适用于急性白血病,对急性淋巴细胞白血病及粒细胞白血病均有效,一般作为第二线药物,即在首选药物耐药时可考虑应用此药。对于恶性淋巴瘤,可作为交替使用的首选药物。其对乳腺癌、肉瘤、肺癌、膀胱癌等其他各种癌症都有一定疗效,多与其他抗癌药联合使用。
但是,阿霉素在直接注射使用时,由于随血液全身弥散分布,对机体可产生广泛的生物化学效应,具有强烈的细胞毒性作用。主要的毒性反应有,白细胞和血小板减少,约60%~80%的病人可发生;100%的病人有不同程度的毛发脱落,停药后可以恢复生长;心脏毒性,表现为心律失常,st-t改变,多出现在停药后的1~6个月;恶心、食欲减退;药物溢出血管外可引起组织溃疡及坏死。另外,用药后尿液可出现红色。
因此,本领域存在对hfn高效装载阿霉素的方法及相应产物的需求。
技术实现要素:
本发明的第一方面涉及一种hfn包载阿霉素的方法,其包括步骤:
1)将hfn在30~60℃孵育温度下在含有5~9m的脲、促进阿霉素溶解的添加剂和阿霉素的溶液中解聚8-30h,优选地,孵育温度为35~50℃,更优选地,38~48℃,更优选地,40~45℃;和/或,优选地,孵育时间为8~20h,更优选地,8~16h,更优选地,10~14h;
2)通过去除溶液中的变性剂使hfn复聚并包载阿霉素;
3)任选地,去除溶液中残余的脲、添加剂和阿霉素;
4)任选地,干燥上述溶液获得包载了阿霉素的hfn固体;
其中促进阿霉素溶解的添加剂选自甘油、吐温-20、triton-100、蔗糖、葡萄糖、精氨酸、甜菜碱或其混合物。
在一些实施方案中,组成hfn的h亚基的氨基酸序列如seqidno.1所示。
在一些实施方案中,促进阿霉素溶解的添加剂选自甘油或蔗糖。
在一些实施方案中,溶液中hfn与阿霉素的质量比例为1:2~5:1,优选地,1:1~4:1,更优选地,8:2.5~8:3.5。
在一些实施方案中,去除溶液中的脲、促进阿霉素溶解的添加剂和残余阿霉素采用脱盐方式进行,优选地,采用脱盐柱进行。
在一些实施方案中,hfn包载阿霉素的质量比为5%-60%,优选地,至少8%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%或更高,更优选地,至少20%、25%、30%或35%。
在一些实施方案中,溶液中hfn含量范围为0.1~100mg/ml,优选地,0.2~10mg/ml,更优选地,0.3~5mg/ml,更优选地,0.5~2mg/ml,更优选地,0.7~1.4mg/ml;和/或,阿霉素的含量范围为0.1~50mg/ml,优选地,0.2~10mg/ml,更优选地,0.3~5mg/ml,更优选地,0.5~2mg/ml,更优选地,0.7~1.4mg/ml。
在一些实施方案中,脲的浓度为8m,和/或解聚9~20h,更优选地,10~14h,和/或孵育温度为35℃~48℃,优选地,39℃~45℃。
在一些实施方案中,溶液是tris-hcl缓冲液、柠檬酸-柠檬酸钠缓冲液或乙酸-乙酸钠缓冲液,优选地,溶液的ph值为4~10,更优选地,7~9,更优选地,7.5~8.5;和/或,优选地,溶液的浓度为20~200mm,更优选地,25~100mm,更优选地,25~50mm。
本发明的第二方面涉及一种利用上述第一方面所述的hfn包载阿霉素的方法获得的包载阿霉素的hfn。
本发明的第三方面涉及一种包含利用上述第一方面所述的hfn包载阿霉素的方法获得的包载阿霉素的hfn的药物组合物。
利用本发明的hfn包载阿霉素的方法可以使阿霉素包载量大幅度提高,进而在达到相同治疗效果的前提下,临床给药剂量将会大大减少。
附图说明
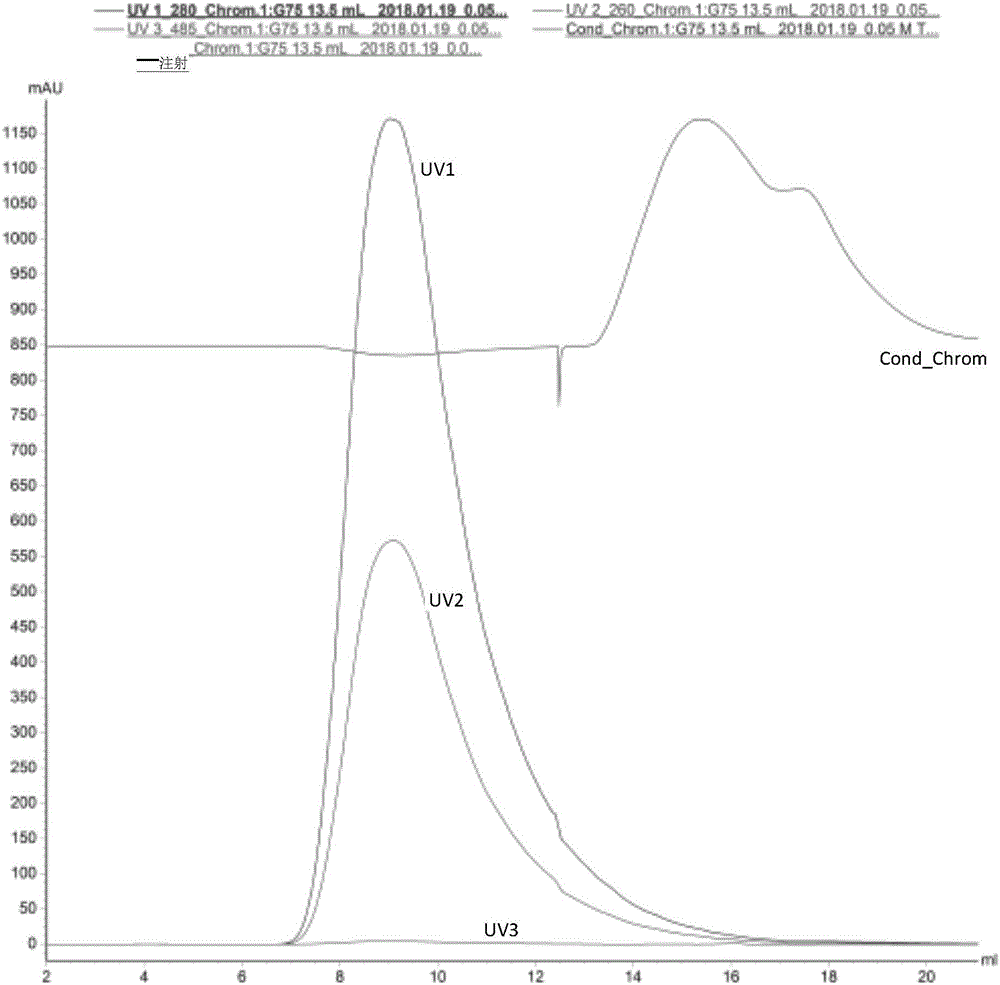
图1.单独的hfn样品的akta图谱。
图2.包载dox的hfn样品的akta图谱。hfn和dox的浓度保持一致。hfn在485nm波长处有没有特殊吸收峰,而dox在485nm波长处有特殊吸收峰,由本图可以明显看到在hfn的出峰位置里面有485nm波长的吸收峰,说明hfn对dox进行了包载。
具体实施方式
定义
本发明的hfn是指全人重链(h亚基)铁蛋白,其氨基酸序列如seqidno.1所示。
本发明的解聚是指铁蛋白天然24聚体的紧密闭合球状结构被打开,直观表现为凝胶排阻柱上的出峰时间被显著延迟,从而解聚蛋白峰与未解聚蛋白峰发生分离。在本发明中解聚比例为至少50%,例如至少55%、60%、65%、70%、80%、90%、95%、96%、97%、98%、99%,最高可达到100%。
复聚是指在引起解聚的物质被去除或降低到足够低浓度后,发生解聚的铁蛋白又恢复到天然24聚体的紧密闭合球状结构,直观表现为凝胶排阻柱上的出峰时间减少至与天然铁蛋白相近的出峰时间。在本发明中,复聚比例为至少50%,例如55%、60%、65%、70%、80%、90%、95%、96%、97%、98%、99%,最高可达100%。
本发明中的hfn包载阿霉素是指阿霉素包载在hfn的笼状结构中的过程,在溶液体系中的hfn解聚和复聚的过程中,处于同一溶液体系中的待包载的阿霉素就会包载在复聚后重新形成的笼状结构中。
本发明中的hfn中包载阿霉素的上限为hfn笼状结构的内部容积所能容纳的药物的最大量,即约268立方纳米的体积内所能容纳的药物的量。在一些实施方案中,以质量比计算,药物包载量为5~60%,优选地,10~50%、20~40%、25~35%,例如至少8%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%或更高。在一些实施方案中,每分子hfn包载50-500个阿霉素分子,例如60、80、90、100、110、120、130、140、150、170、190、200、220、240、260、280、240、260、280、300、350、400、450、500或更多个。
利用本发明的hfn包载阿霉素的方法可以使阿霉素包载量大幅度提高,进而在达到相同治疗效果的前提下,临床给药剂量将会大大减少。
本发明的包载阿霉素的溶液的缓冲体系可以包括但不限于tris-hcl、柠檬酸-柠檬酸钠、乙酸-乙酸钠缓冲液。缓冲液浓度在20mm~200mm的范围,优选地,30mm~150mm,更优选地,40mm~80mm,ph值从6.9.0-9.0的范围,优选地,7.2~8.5,更优选地,7.5~8.3。
本发明的包载阿霉素的缓冲体系中还含有促进阿霉素溶解的添加剂,本领域中已知用于促进阿霉素溶解的任何添加剂都可以用于本发明的方法。在一些实施方案中,所述添加剂选自甘油、吐温-20、triton-100、蔗糖、葡萄糖、精氨酸、甜菜碱或其混合物,在一些实施方案中,所述添加剂选自甘油或蔗糖或甘油和蔗糖的混合物,在一些实施方案中,所述添加剂的体积比或重量比含量为8-40%,优选地,10-25%,更优选地,12-20%。
本发明的包载阿霉素的hfn可以以药物组合物的形式提供,即,除包载阿霉素的hfn外,其还含有药学上可接受的载体。这些药物组合物可以用药学上可接受的载体或稀释剂以及任何其他已知的赋形剂根据常规技术配制,这些常规技术是例如在以下中披露的技术:remington:thescienceandpracticeofpharmacy,第22版,gennaro编,mackpublishingco.,2013。
利用本发明的方法所获得的包载阿霉素的hfn可以用于治疗和/或预防受试者的疾病或状态。本发明的包载阿霉素的hfn所能治疗治疗和/或预防的疾病或状态取决于所包载的阿霉素,即,现有技术中已知可以由阿霉素治疗和/或预防的疾病或状态均可以由本发明的包载阿霉素的hfn治疗和/或预防。不受限于任何理论,本发明的包载阿霉素的hfn可以靶向肿瘤,从而在施用后在肿瘤部位释放所包载的阿霉素,实现对所述肿瘤的预防和/或治疗。在一些实施方案中,所述疾病或状态选自急性白血病(淋巴细胞性和粒细胞性)、恶性淋巴瘤、乳腺癌、支气管肺癌(未分化小细胞性和非小细胞性)、卵巢癌、软组织肉瘤、成骨肉瘤、横纹肌肉瘤、尤文肉瘤、母细胞瘤、神经母细胞瘤、膀胱癌、甲状腺癌、前列腺癌、头颈部鳞癌、睾丸癌、胃癌、肝癌。
本发明的药物组合物可以通过任何适合途径和模式给予,包括都不限于静脉内或皮下注射或输注。
本发明的药物组合物还可以与其他药物组合使用,例如abvd、caf、caop、fam、ac、aop、acp、cy-va-dic、macc,或者与放疗配合使用。
以下结合具体的实施案例对本发明做进一步说明,以下实施例仅用于说明本发明而不意欲限定本发明的范围。对于本领域的技术人员来说,在本发明范围内所做的任何变更、修改或直接采用实施例中的同等条件而实施的例子,都应理解为在本发明的涵盖范围内。
实施例
实施例1hfn包载阿霉素工艺研究
1主要设备
1.1aktaavant(含g75脱盐柱)(gehealthcare)
1.2恒温水浴锅
1.3agilent1260hplc(含agilentsec-5300a凝胶排阻柱)(agilenttechnologies)
2工艺条件研究
2.1ph值对hfn包载阿霉素的影响
2.1.1样品准备
首先将hfn(其亚基序列如seqidno.1所示,为24个亚基组成的笼状结构,naturenanotechnology,2012,7(7),459-464)溶液(50mmtris–hclph7.2)浓缩至25~30mg/ml,使其成为hfn母液备用。使用超纯水配制20mg/ml的dox母液备用。
然后分别用ph值为4、5、6的50mm醋酸-醋酸钠缓冲液溶液和ph值为7、8、9、10的50mmtris-hcl缓冲液溶液,对备用的hfn母液进行1000倍换液。
其次称取7份0.960g脲,每份脲里分别加入换液后的不同ph(4、5、6、7、8、9、10)值的hfn12mg,再分别加入dox母液0.2ml,最后每个样品分别加入和hfnph值一致的缓冲液溶液,定容至2ml。
使用振荡器将每个样品混合30s,然后置于37℃水浴锅中加热30s,连续重复操作,直至样品完全混合均匀,固体脲完全溶解。
最后将样品置于25℃的恒温箱中,孵育18h。
2.1.2样品处理
使用和样品ph值一样的缓冲液分别将每个样品在13.5ml的g75柱子上直接洗脱脲和游离的阿霉素。
2.1.3样品测定
对样品进行sds-page(确定蛋白是否存在)、nanodrop(测量阿霉素的值,厂家genecompanylimited基因有限公司,型号nd2000)、bca蛋白质测定(可以得出hfn的包载量,试剂盒厂家:赛默飞世尔科技(中国)有限公司,货号prod#23227)、hplc(得到hfn包载阿霉素之后的单体情况,厂家:安捷伦科技(中国)有限公司,型号高效液相色谱1260infinity)测定。结果见表1。
表1.ph值对hfn包载dox的影响
小结:由于dox在ph值高于8.0的碱性条件下会发生降解,所以选择最佳的ph值为8.0。
图1和图2分别示出了单独的hfn和包载了dox的hfn的akta图谱,其清楚地表现了确认hfn是否包载dox的情形。
2.2hfn和dox的配比对hfn包载dox的影响
2.2.1样品配制
首先将hfn溶液(50mmtris–hclph8.0)浓缩至25~30mg/ml,使其成为hfn母液备用。使用超纯水配制20mg/ml的dox母液备用。由于需要配置很多样品,所以以表2的形式记录样品的配置。
表2.hfn:dox样品配比表
注:每个样品配制2ml,最终用50mmtris–hclph8.0的缓冲液溶液定容至2ml。
使用振荡器将每个样品混合30s,然后置于37℃水浴锅中加热30s,连续重复操作,直至样品完全混合均匀,固体脲完全溶解。
最后将样品置于25℃的恒温箱中,孵育18h。
2.2.2样品处理
样品使用50mmtris–hclph8.0缓冲液溶液在13.5ml的g75柱子上直接洗脱脲和游离的阿霉素。
2.2.3样品测定
对样品进行sds-page(确定蛋白是否存在)、nanodrop(测量阿霉素的值)、bca蛋白质测定(可以得出hfn的包载量)、hplc(得到hfn包载阿霉素之后的单体情况)测定。结果见表3。
表3.hfn:dox数据表
小结:综合hfn包载dox的结果,同时从dox的利用的角度,最终选择hfn为8mg/ml、dox为3mg/ml。
2.3时间和温度对hfn包载dox的影响
2.3.1样品配制
首先将hfn溶液(50mmtris–hclph8.0)浓缩至25~30mg/ml,使其成为hfn母液备用。使用超纯水配制20mg/ml的dox母液备用。
每份样品均0.960g脲,每份脲里分别加hfn16mg,再分别加入dox母液0.3ml,最后每个样品分别加入缓冲液溶液,定容至2ml。
使用振荡器将每个样品混合30s,然后置于37℃水浴锅中加热30s,连续重复操作,直至样品完全混合均匀,固体脲完全溶解。由于本次所考察的项目的是温度和时间,所以有20个样品,表4提供了这些信息。
表4.温度和时间样品表
2.3.2样品处理
样品使用50mmtris–hclph8.0缓冲液溶液在13.5ml的g75柱子上直接洗脱脲和游离的阿霉素。
2.3.3样品测定
对样品进行sds-page(确定蛋白是否存在)、nanodrop(测量阿霉素的值)、bca蛋白质测定(可以得出hfn的包载量)、hplc(得到hfn包载阿霉素之后的单体情况)测定。结果见表5和表6。
表5.时间和温度数据表
小结:孵育的温度确定为42℃、孵育的时间确定为12h。
表6.时间和温度细化实验数据表
小结:结果表明孵育的温度为42℃,孵育的时间为12h效果最佳。
2.4添加剂对hfn包载dox的影响
本发明还研究了添加剂对hfn包载dox的影响。本发明发现添加剂可能主要解决包载时hfn的聚集问题,当添加剂抑制聚集产生时,减少hfn包载dox的量;而当添加剂促进聚集体产生时,增加hfn包载dox的量。
本发明测试了多种添加剂,包括但不限于,甘油、吐温-20、triton-100、蔗糖、葡萄糖、精氨酸、甜菜碱或其混合物,结果发现效果比较明显的添加剂有甘油和蔗糖。
2.4.1甘油对hfn包载dox的影响
2.4.1.1实验条件
孵育hfn:dox的质量浓度比为8:3。
孵育缓冲液:50mmtris–hclph:8.0(含1%、5%、10%、15%、20%甘油)。
孵育时脲的浓度:8m,孵育的温度:42℃,孵育时间:12h、24h。
2.4.1.2样品配制:
2.4.1.2.1将纯化的hfn蛋白浓缩然后使用50mmtris–hclph:8.0的缓冲液对其进行换液,体积变化1000倍,最终将hfn浓缩至约20mg/ml备用。
2.4.1.2.2分别称取5份0.960g的脲,然后每份脲里加入6.0mg的dox,混合均匀后往每份脲和dox的混合物中加入16mg的hfn,40℃水浴溶解,再往每份样品里面加入20μl、100μl、200μl、300μl、400μl的100%甘油,最后每份样品定溶到2ml。
2.4.1.2.3将样品和空白对照分别放置于42℃孵育12h、24h后将样品分析。
2.4.1.3样品分析:
2.4.1.3.1样品使用50mmtris–hclph:8.0含有与样品同等浓度甘油的缓冲液在g75柱子上直接洗脱脲和多余的dox。
2.4.1.3.2对样品进行sds-page(确定蛋白是否存在)、nanodrop(测量阿霉素的值)、bca蛋白质测定(可以得出hfn的包载量)、hplc(得到hfn包载阿霉素之后的单体情况)测定。结果见表7。
2.4.2蔗糖对hfn包载dox的影响
2.4.2.1实验条件
孵育hfn:dox的质量浓度比为8:3。
孵育缓冲液:50mmtris–hclph:8.0(含1%、3%、5%、10%蔗糖)
孵育时脲的浓度:8m,孵育的温度:42℃,孵育时间:12h、24h。
2.4.2.2样品配制:
2.4.2.2.1将纯化的hfn蛋白浓缩然后使用50mmtris–hclph:8.0的缓冲液对其进行换液,体积变化1000倍,最终将hfn浓缩至约20mg/ml备用。
2.4.2.2.2分别称取4份0.960g的脲,然后每份脲里加入6.0mg的dox,混合均匀后往每份脲和dox的混合物中加入16mg的hfn,40℃水浴溶解,再往每份样品里面加入20mg、60mg、100mg、200mg的蔗糖,最后每份样品定溶到2ml。
2.4.2.2.3将样品和空白对照分别放置于42℃孵育12h、24h后将样品分析。
2.4.2.3样品分析:
2.4.2.3.1样品使用50mmtris–hclph:8.0含有与样品同等浓度蔗糖的缓冲液在g75柱子上直接洗脱脲和多余的dox。
2.4.2.3.2对样品进行sds-page(确定蛋白是否存在)、nanodrop(测量阿霉素的值)、bca蛋白质测定(可以得出hfn的包载量)、hplc(得到hfn包载阿霉素之后的单体情况)测定。结果见表7。
2.4.3吐温-20对hfn包载dox的影响
2.4.3.1实验条件
孵育hfn:dox的质量浓度比为8:3。
孵育缓冲液:50mmtris–hclph:8.0(含0.01%、0.05%、0.10%、0.50%吐温)
孵育时脲的浓度:8m,孵育的温度:42℃,孵育时间:12h、24h。
2.4.3.2样品配制:
2.4.3.2.1将纯化的hfn蛋白浓缩然后使用50mmtris–hclph:8.0的缓冲液对其进行换液,体积变化1000倍,最终将hfn浓缩至约20mg/ml备用。
2.4.3.2.2分别称取4份0.960g的脲,然后每份脲里加入6.0mg的dox,混合均匀后往每份脲和dox的混合物中加入16mg的hfn,40℃水浴溶解,再往每份样品里面加入0.2μl、1μl、2μl、10μl的100%吐温-20,最后每份样品定溶到2ml。
2.4.3.2.3将样品和空白对照分别放置于42℃孵育12h、24h后将样品分析。
2.4.3.3样品分析:
2.4.3.3.1样品使用50mmtris–hclph:8.0含有与样品同等浓度吐温-20的缓冲液在g75柱子上直接洗脱脲和多余的dox。
2.4.3.3.2对样品进行sds-page(确定蛋白是否存在)、nanodrop(测量阿霉素的值)、bca蛋白质测定(可以得出hfn的包载量)、hplc(得到hfn包载阿霉素之后的单体情况)测定。结果见表7。
2.4.4精氨酸对hfn包载dox的影响
2.4.4.1实验条件
孵育hfn:dox的质量浓度比为8:3。
孵育缓冲液:50mmtris–hclph:8.0(含1%、2%、4%精氨酸)
孵育时脲的浓度:8m,孵育的温度:42℃,孵育时间:12h。
2.4.4.2样品配制:
2.4.4.2.1将纯化的hfn蛋白浓缩然后使用50mmtris–hclph:8.0的缓冲液对其进行换液,体积变化1000倍,最终将hfn浓缩至约25-30mg/ml备用。
2.4.4.2.2分别称取3份0.480g的脲,然后每份脲里加入0.1ml浓度为30mg/ml的dox母液,再往每份样品里面分别加入84μl、166.5μl、333μl的12%精氨酸、ph为8.0的母液,混合均匀后往每份脲和dox的混合物中加入8mg的hfn,最后每份样品定溶到1ml。
2.4.4.2.3将样品和空白对照分别放置于42℃孵育12h后将样品分析。
2.4.4.3样品分析:
2.4.4.3.1样品使用50mmtris–hclph:8.0含有与样品同等浓度精氨酸的缓冲液在g75柱子上直接洗脱脲和多余的dox。
2.4.4.3.2对样品进行sds-page(确定蛋白是否存在)、nanodrop(测量阿霉素的值)、bca蛋白质测定(可以得出hfn的包载量)、hplc(得到hfn包载阿霉素之后的单体情况)测定。结果见表7。
表7.甘油、蔗糖、吐温-20、精氨酸对hfn包载dox的影响
2.5离子强度对hfn包载dox的影响
2.5.1样品制备
首先将hfn溶液(50mmtris–hclph8.0)浓缩至25~30mg/ml,使其成为hfn母液备用。
然后称取4份4.800g脲,每份加入60.0mgdox,将两者充分混合均匀后,再每份加入80mg的hfn,最后加入适量的1000mmtris–hclph8.0母液和适量的超纯水,将样品的体积定容至10ml,每份样品的tris–hcl浓度分别为20、30、40、50mm。
使用振荡器将每个样品混合30s,然后置于37℃水浴锅中加热30s,连续重复操作,直至样品完全混合均匀,固体脲完全溶解。
最后将样品置于42℃的恒温箱中,孵育12h。
2.5.2样品处理
使用50mmtris–hclph8.0缓冲液分别将每个样品在13.5ml的g75柱子上直接洗脱脲和游离的阿霉素。
2.5.3样品测定
对样品进行sds-page(确定蛋白是否存在)、nanodrop(测量阿霉素的值)、bca蛋白质测定(可以得出hfn的包载量)、hplc(得到hfn包载阿霉素之后的单体情况)测定。结果见表8。
表8.离子强度对hfn包载dox的影响
小结:为了保证液体的缓冲能力,所以选择体系的离子强度为30mmtris-hcl。
序列表
<110>昆山新蕴达生物科技有限公司
<120>hfn包载阿霉素的方法及其产物
<130>lz1800247cn01
<160>1
<170>siposequencelisting1.0
<210>1
<211>183
<212>prt
<213>智人(homosapiens)
<400>1
metthrthralaserthrserglnvalargglnasntyrhisglnasp
151015
serglualaalaileasnargglnileasnleugluleutyralaser
202530
tyrvaltyrleusermetsertyrtyrpheaspargaspaspvalala
354045
leulysasnphealalystyrpheleuhisglnserhisglugluarg
505560
gluhisalaglulysleumetlysleuglnasnglnargglyglyarg
65707580
ilepheleuglnaspilelyslysproaspcysaspasptrpgluser
859095
glyleuasnalametglucysalaleuhisleuglulysasnvalasn
100105110
glnserleuleugluleuhislysleualathrasplysasnasppro
115120125
hisleucysasppheilegluthrhistyrleuasngluglnvallys
130135140
alailelysgluleuglyasphisvalthrasnleuarglysmetgly
145150155160
alaprogluserglyleualaglutyrleupheasplyshisthrleu
165170175
glyaspseraspasngluser
180
- 还没有人留言评论。精彩留言会获得点赞!