鼠尾草酚作为炎症小体抑制剂的用途的制作方法
本申请涉及药物筛选领域,尤其但不限于涉及鼠尾草酚作为炎症小体抑制剂的用途。
背景技术:
炎症小体是细胞内的一种大型多蛋白复合物,由受体蛋白、凋亡相关斑点样蛋白(apoptosis-associatedspeck-likeprotein,asc)和半胱氨酸天冬氨酸特异蛋白酶1前体(pro-caspase-1)组成,炎症小体通过模式识别受体(patternrecognitionreceptor,prr)识别病原微生物及内源性危险信号,即病原相关分子模式(pathogenassociatedmolecularpattern,pamp)和危险相关分子模式(damageassociatedmolecularpattern,damp),招募并激活caspase-1,剪切il-1β和il-18前体,产生相应的成熟细胞因子,从而促进细胞凋亡,参与机体对病原体的清除及适应性免疫应答的产生。目前发现的炎症小体,根据受体蛋白的不同分别被命名为核苷酸结合寡聚化结构域受体蛋白1(nucleotide-bindingoligomerizationdomain-likereceptorprotein1,nlrp1)、核苷酸结合寡聚化结构域受体蛋白3(nucleotide-bindingoligomerizationdomain-likereceptorprotein3,nlrp3)、核苷酸结合寡聚化结构域受体card结构域蛋白4(nucleotide-bindingoligomerizationdomain-likereceptorcard-domaincontainingprotein4,nlrc4)、黑色素瘤缺乏因子2(absentinmelanoma2,aim2)炎症小体。
炎症小体作为固有免疫的重要组成部分,其异常活化和功能失调与多种获得性炎性疾病和自身免疫病的病理过程密切相关。目前研究发现,溃疡性结肠炎、阿尔茨海默病、2型糖尿病、动脉粥样硬化、痛风和非酒精性脂肪性肝炎等都与炎症小体的异常活化密切相关。但目前在治疗获得性炎性疾病和自身免疫病方面,并未有相关靶向药物的临床应用,因此开发炎症小体抑制剂,抑制炎症小体的异常活化,将有利于上述疾病的治疗并为其提供新的治疗途径。
技术实现要素:
以下是对本文详细描述的主题的概述。本概述并非是为了限制权利要求的保护范围。
近年来,一些小分子化合物已经显示出对nlrp3炎性体激活的潜在抑制作用,例如3,4-亚甲二氧基-硝基苯乙烯,格列本脲,小白菊内酯,萝卜硫素,异甘草素,mcc950,β-羟基丁酸酯,氟芬那酸和甲芬那酸酸等,但对各种炎症小体均有抑制作用的化合物较少。鼠尾草酚(carnosol),cas号5957-80-2,分子式c20h26o4,相对分子质量330.424g/mol。现代研究表明,鼠尾草酚其具有抗炎、抗肿瘤等作用。文献报道,鼠尾草酚通过抑制nf-κb和mapk等,减少肿瘤坏死因子(tnf-α)等促炎细胞因子的释放,但其抗炎作用的潜在机制和直接靶标还是未知的。炎症小体在炎症疾病中发挥核心的作用,因此,研究鼠尾草酚对炎症小体的调控作用以及其在治疗炎症性疾病中的作用具有重要意义。鼠尾草酚来源于唇形科迷迭香属植物迷迭香,无色结晶,溶于dmso,具有抗辐射、抗氧化、抗炎、抗癌等多种功效。
具体地,本申请提供鼠尾草酚作为炎症小体活化抑制剂的用途。
在本申请中,鼠尾草酚在制备治疗炎症小体异常活化相关疾病的药物中的用途。
在本申请中,所述炎症小体可以选自寡聚化结构域样受体家族热蛋白结构域3(nlrp3)炎症小体、寡聚化结构域样受体家族半胱天冬酶激活募集结构域4(nlrc4)、黑色素瘤缺乏因子2(aim2)中的任一种或更多种。
在本申请中,鼠尾草酚可以抑制caspase-1和il-1β的表达。
在本申请中,鼠尾草酚可以抑制感染性休克。
在本申请中,鼠尾草酚可以降低革兰氏阴性菌感染引起的死亡。
在本申请中,所述相关疾病可以选自溃疡性结肠炎、阿尔茨海默病、2型糖尿病、动脉粥样硬化、痛风和非酒精性脂肪性肝炎中的任一种或更多种。
在本申请中,鼠尾草酚的施用剂量可以为20mg/kg-100mg/kg。
在本申请中,鼠尾草酚的施用方式可以为口服或注射。
本发明人发现:1.鼠尾草酚对炎症小体活化具有抑制作用,能抑制nlrp3、nlrc4、aim2等多种炎症小体活化,是广谱的炎症小体抑制剂。
2.目前有多种获得性炎性疾病和自身免疫病与炎症小体相关,例如溃疡性结肠炎、阿尔茨海默病、2型糖尿病、动脉粥样硬化、痛风和非酒精性脂肪性肝炎等,但并没有针对此类疾病的靶向药物。本申请发现鼠尾草酚可抑制炎症小体活化,进而用于开发可治疗获得性炎性疾病和自身免疫病的药物。
3.本申请在lps诱导的小鼠感热休克症模型中发现鼠尾草酚可显著抑制小鼠感热休克症反应及其引起的死亡。
4.目前研究发现,在化学性结肠炎小鼠模型中,抑制caspase-1的基因表达或者抑制il-1β或者il-18均能缓解结肠炎症。2010年英国《gut》胃肠病杂志发表dss诱导的结肠炎的文章研究发现,敲除nlrp3或者asc、caspase-1编码基因的巨噬细胞的il-1β的分泌显著下降,经口给予dss干预后的nlrp3-/-小鼠表现出较野生型小鼠更轻的结肠炎症,和较低的炎症因子表达水平,而药物抑制结肠炎小鼠caspase-1p20后达到与nlrp3-/-小鼠相似的黏膜保护作用,这表明dss是通过nlrp3炎症小体通路激活诱导结肠炎症;小鼠经腹腔注射给药鼠尾草酚后,可显著改善化学性dss诱导的小鼠结肠炎症状。文献报道,mcc950在纳摩尔级别就可以完全抑制nlrp3炎症小体活化,并可体外模拟nlrp3-/-小鼠。本申请在mcc950模拟的nlrp3-/-小鼠中经口给予dss,在此基础上腹腔注射给药鼠尾草酚,从而证明鼠尾草酚通过抑制nlrp3活化起到治疗小鼠结肠炎症的作用。
5.非酒精性脂肪性肝病(nafld)可增加心血管事件、癌症、肝硬化的死亡率和肝细胞癌,而nlrp3炎症小体在非酒精性脂肪性肝病中起到至关重要的作用。本申请发现鼠尾草酚可以通过抑制nlrp3炎症小体,显著降低小鼠非酒精性脂肪性肝炎(nonalcoholicsteatohepatitis,nash)模型中的小鼠肝纤维化程度,有利于临床开发可治疗nash的靶向药物。
本申请的其它特征和优点将在随后的说明书中阐述,并且,部分地从说明书中变得显而易见,或者通过实施本申请而了解。本申请的目的和其他优点可通过在说明书、权利要求书以及附图中所特别指出的结构来实现和获得。
附图说明
附图用来提供对本申请技术方案的进一步理解,并且构成说明书的一部分,与本申请的实施例一起用于解释本申请的技术方案,并不构成对本申请技术方案的限制。
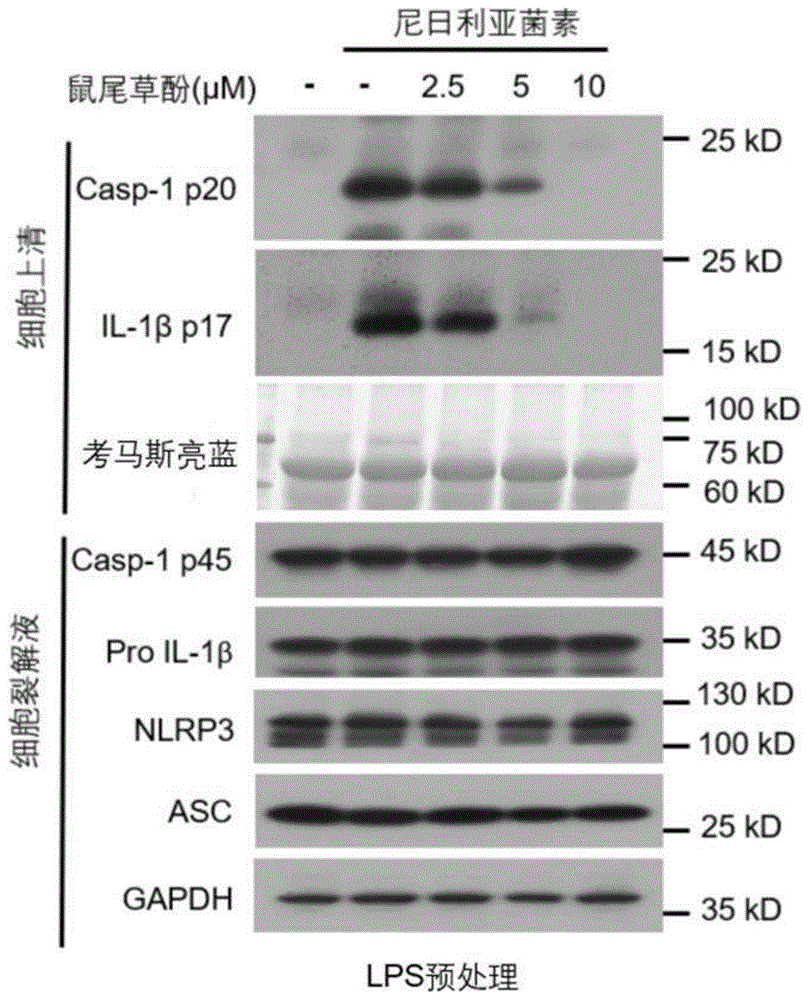
图1示出鼠尾草酚剂量依赖性抑制lps+nigerigin诱导的nlrp3活化。免疫印迹法检测细胞上清中caspase-1p20、il-1βp17的含量以及细胞裂解液中nlrp3、asc、pro-caspase-1、pro-il-1β表达(图1a)。利用caspase-1活性检测试剂盒测定细胞上清中caspase-1活性(图1b),elisa试剂盒检测细胞培养上清中il-1β的含量(图1c)。
图2示出鼠尾草酚显著抑制nlrp3、nlrc4、aim2等炎症小体的活性。图2a和图2b是免疫印迹法检测结果,图2c和图2e是caspase-1活性检测试剂盒检测细胞上清中caspase-1含量结果,图2d和图2f是elisa检测细胞上清中il-1β含量的结果,其中con代表对照组,ns代表没有统计学差异。
图3示出鼠尾草酚治疗lps诱导的感染性休克,并显著降低革兰氏阴性菌感染引起的死亡。图3a是利用elisa法检测小鼠血清中il-1β含量的结果,图3b是小鼠腹腔给药1小时后,腹腔注射lps后小鼠的生存曲线。
图4示出鼠尾草酚治疗dss诱导的小鼠急性溃疡性结肠炎。图4a是小鼠结肠图片,图4b是小鼠结肠长度,图4c是小鼠的体重变化。
图5示出鼠尾草酚通过抑制nlrp3炎症小体的活性治疗小鼠急性溃疡性结肠炎。图5a是小鼠结肠图片,图5b是小鼠结肠长度,图5c是小鼠的体重变化。
图6示出鼠尾草酚治疗非酒精性脂肪型肝炎。图6a是取小鼠血清检测alt的结果,图6b是去小鼠血清检测ast的结果。
具体实施方式
为使本申请的目的、技术方案和优点更加清楚明白,下文中将结合附图对本申请的实施例进行详细说明。需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征可以相互任意组合。
药物:
鼠尾草酚(carnosol)、mcc950均购自targetmol公司;lps购自美国sigma公司。
试剂、材料:
dmem培养基、胎牛血清(美国hyclone公司);opti-mem无血清培养基(美国gibco公司);胰蛋白酶、双抗(青霉素-链霉素溶液)(迈晨科技北京有限公司);三磷酸腺苷(atp)、尼日利亚菌素(nigericin)、脂多糖(lps)、二甲基亚砜(dmso)(美国sigmaaldrich公司);nlrp3、asc、caspase-1、pro-caspase-1、pro-il1β、gapdh抗体(美国cellsignalingtechnology公司);cck-8试剂盒(mce);caspase-1活性测定试剂盒(美国promega公司);tnf-α、il-1βelisa检测试剂盒(北京达科为生物技术有限公司);5×sds蛋白电泳上样缓冲液、pm2510三色预染蛋白marker(北京鼎国昌胜生物技术有限公司);电泳液、转印液、10×tbs-t缓冲液、考马斯亮蓝(北京博迈德基因技术有限公司);甲醇、乙酸(北京化工厂);ripa裂解液(上海碧云天生物技术有限公司);a、b显影液、pvdf膜(美国millipore公司)。
仪器:
二氧化碳培养箱(美国thermoscientific公司);酶标仪(美国promega公司);低温高速离心机(美国sigma公司);电泳槽、转印槽、凝胶电泳分析系统(美国bio-rad公司);细胞培养板振荡仪(德国ika公司)。
1.细胞水平检验在lps分别与三磷酸腺苷(adenosinetriphosphate,atp)、尼日利亚菌素(nigericin)、二氧化硅(sio2)、聚肌苷酸-聚胞苷酸(poly(i:c))、聚(脱氧腺苷-脱氧卵磷脂)(poly(deoxyadenylic-deoxythymidylic),poly(da:dt))、沙门氏杆菌(salmonella)共同刺激下,鼠尾草酚对各种活化的炎症小体的抑制作用;pam3csk4刺激与转染lps激活的非经典炎症小体的抑制作用。
2.鼠尾草酚可显著抑制小鼠感热休克症反应及其引起的死亡。
3.高剂量的lps可以诱导机体免疫应激,导致tnf-α、il-1β等炎症因子分泌增加,本申请发现鼠尾草酚可显著降低lps导致的tnf-α、il-1β等炎症因子的分泌增加,降低腹腔巨噬细胞、中性粒细胞水平。
4.小鼠经腹腔注射给药鼠尾草酚后,可显著改善化学性dss诱导的小鼠结肠炎症状,并在mcc950模拟的nlrp3-/-小鼠中经口给予dss,再腹腔注射给药鼠尾草酚,从而证明鼠尾草酚通过抑制nlrp3炎症小体活化起到治疗小鼠结肠炎症的作用。
5.在非酒精性脂肪性肝炎模型中,小鼠腹腔注射给药鼠尾草酚,可显著降低小鼠转氨酶水平,并明显改善小鼠肝纤维化程度,说明本鼠尾草酚可以治疗非酒精性脂肪性肝炎。
产品制备实施例:
1.鼠尾草酚能显著降低lps与多种因素共同刺激下炎症小体活化而引起的il-1β的分泌
a.小鼠原代骨髓巨噬细胞(bmdm)的制备:取10周龄c57bl/6雌性小鼠,分离肱骨和股骨,用dmem培养基(10%胎牛血清)反复抽取骨髓细胞并按1∶4000加入小鼠集落刺激因子(mcsf)分化5天后,消化细胞并按9×105个/ml孔板(24孔板,0.5ml/孔),过夜贴壁后进行下一步实验。
b.lps刺激:采取换液的方式,以50ng/ml的浓度(0.4ml/孔)加入到bmdm并刺激4h。
c.加药:取dmso溶解的鼠尾草酚单体,用opti-mem培养基配置成10μm,再2倍稀释成5μm,2.5μm共三个浓度,采取换液的方式加入到bmdm(0.4ml/孔)中,刺激1h。
d.nlrp3刺激因子刺激:采取补液的方式,分别加入终浓度为5mmatp(0.02ml/孔)刺激1小时,10μm的nigericin(0.02ml/孔)刺激0.5小时。250μg/ml的sio2(0.02ml/孔),2μg/ml的poly(i:c)和poly(da:dt)(0.02ml/孔),沙门氏杆菌(mol,1:10)刺激6小时。
e.收样:细胞收样,直接加入sds蛋白电泳上样缓冲液裂解(120μl/孔),迅速晃匀,使loading覆盖所有细胞,5min后再如此,反复3次,将loading吸入ep管中。细胞上清样品处理:室温4000rpm离心5min,收上清,加入1/4体积三氯乙酸(tca),4℃静置1h以上后,4℃,12000rpm离心15min;弃上清,加入冰的丙酮(500μl/孔)上下颠倒混匀,4℃,12000rmp离心15min,弃上清,95℃金属浴挥干丙酮,待丙酮挥发后加1×ripaloading35μl振荡混匀,水浴煮沸,冷却后作为上清样品。
f.westernblot:检测上清中il-1βp17、caspase-1p20蛋白表达水平,检测细胞裂解液中nlrp3、asc、pro-caspase-1,pro-il-1β蛋白水平。细胞上清蛋白样品采用12%浓度的sds-聚丙烯酰胺凝胶电泳,细胞裂解液样品采用10%浓度的sds-聚丙烯酰胺凝胶电泳,接通电源,设定恒定电压80v,45min后电压改为135v,溴酚蓝到达分离胶底部时,结束电泳,安装转印装置。细胞上清液结束电泳后,沿marker60kd位置裁胶,60kd以上采用考马斯亮蓝染色30min,脱色液(水:甲醇:乙酸=5:4:1),至背景蓝色脱透明;转移槽的阴极铺4层滤纸,将60kd以下剩余凝胶平铺于滤纸上,并在胶上铺pvdf膜,将5层滤纸铺在膜的上方。接通电源,设定恒定电流,450ma,3h。转膜后,5%脱脂奶室温封闭1h,caspase-1(p20),il-1β,caspase-1(p45),pro-il-1β,asc,nlrp3,gapdh抗体(1:1000)4℃孵育过夜,pvdf膜经1%tbs-t溶液间隔5min洗膜3次,再与相应标记的鼠或兔来源的二抗(1:5000,按照试剂说明书)溶液进行反应1h,弃二抗,用1%tbs-t溶液间隔5min洗膜3次,将显影液a和b两种试剂等体积混合后,立即加到膜上,暗室采用x光胶片压片曝光方式显影。
g.elisa:测定细胞上清液中il-1β、tnf-α的含量,操作步骤按说明书进行。在450nm波长读取od值,根据标准曲线计算样品浓度。
h.caspase-1活性测定:按照caspase-1活性测定试剂盒说明书进行操作。先室温平衡caspase-
i.统计学方法:数据采用graphpadprism6.0(graphpad,sandiego,ca)统计软件进行处理,组间差异分析选用one-wayanova方法进行。p<0.05被认为存在统计学差异。
2.鼠尾草酚可以治疗lps诱导的感染性休克,并显著降低革兰氏阴性菌感染引起的死亡:
a.c57bl/6小鼠,8周,雌性,40只,购自北京斯贝福生物技术有限公司,随机分为5组,分别为空白对照组、模型组、鼠尾草酚组(40mg/kg)、鼠尾草酚+lps组(40mg/kg)、mcc950+lps组(40mg/kg);空白对照组、模型组腹腔注射0.2ml含10%吐温80的pbs溶液,其余各组分别腹腔注射鼠尾草酚和mcc950;1小时后,除空白对照组腹腔注射0.2ml的pbs溶液,其余各组分别注射0.2ml20mg/kg的lps,2小时后眼球取血,取腹腔巨噬细胞,取血后4℃离心取血清,elisa检测血清炎症因子il-1β、tnf-α,腹腔巨噬细胞流式细胞术检测腹腔巨噬细胞和中性粒细胞数,结果表明鼠尾草酚可以治疗lps诱导的感染性休克。
b.小鼠生存率曲线:c57bl/6小鼠,8周,雌性50只,购自北京斯贝福生物技术有限公司,在实验室适应性饲养一周后,随机分为5组,分别为模型组、鼠尾草酚+lps组(给药剂量分别为25mg/kg、50mg/kg、100mg/kg)和mcc950+lps组(50mg/kg)。模型组腹腔注射0.2ml含10%吐温80的pbs溶液,其余组别分别腹腔注射不同给药剂量的鼠尾草酚和mcc950;1小时后,各组均腹腔注射0.2ml20mg/kg的lps,每3小时观察记录小鼠存活情况,并绘制小鼠生存曲线分析存活率;结果显示在lps诱导的小鼠革兰氏阴性菌感染模型中,鼠尾草酚可显著降低小鼠的死亡率。
3.鼠尾草酚治疗dss(右旋葡聚糖硫酸钠)诱导的小鼠急性溃疡性结肠炎。
c57bl/6小鼠,8周,雌性36只,购自北京斯贝福生物技术有限公司,在实验室适应性饲养一周后,随机分为6组(n=6),分别为正常对照组、鼠尾草酚(20mg/kg,40mg/kg)组、dss模型组、dss+鼠尾草酚(20mg/kg,40mg/kg)组。正常对照组和鼠尾草酚组正常饮无菌蒸馏水7天,其他各组饮含2.5%dss的无菌蒸馏水,除正常对照组和dss组每天腹腔注射0.2mlpbs外,其他各组每天腹腔注射0.2ml鼠尾草酚(20mg/kg,40mg/kg)。每天称重记录,观察粪便、是否便血、小鼠活动情况,记录小鼠的dai评分。第8天小鼠眼球取血,取脾称重,取结肠,测量结肠长度,用pbs冲洗干净后末端剪下一段放到-80℃保存,其余结肠放到10%中性福尔马林缓冲液中固定。
4.鼠尾草酚主要通过抑制nlrp3炎症小体的活化来抑制dss诱导的急性溃疡性结肠炎。
c57bl/6小鼠,8周,雌性30只,购自北京斯贝福生物技术有限公司,在实验室适应性饲养一周后,随机分为5组(n=6),分别为正常对照组、dss模型组、dss+鼠尾草酚(40mg/kg)组、dss+mcc950(40mg/kg)组、dss+鼠尾草酚(40mg/kg)+mcc950(40mg/kg)组。正常对照组和鼠尾草酚组正常饮无菌蒸馏水7天,其他各组饮含2.5%dss的无菌蒸馏水,除正常对照组和dss组每天腹腔注射0.2mlpbs外,其他各组每天腹腔注射0.2ml鼠尾草酚(20mg/kg,40mg/kg,含mcc950组提前一天腹腔注射0.2mlmcc950(40mg/kg)。每天称重记录,观察粪便、是否便血、小鼠活动情况,记录小鼠的dai评分。第9天小鼠眼球取血,取脾称重,取结肠,测量结肠长度,用pbs冲洗干净后末端剪下一段放到-80℃保存,其余结肠放到10%中性福尔马林缓冲液中固定。
5.鼠尾草酚治疗对非酒精性脂肪性肝炎。
c57bl/6小鼠,8周,雄性48只,购自北京斯贝福生物技术有限公司,在实验室适应性饲养一周后,随机分为6组(n=8),分为进食缺乏蛋氨酸和胆碱饲料饮食组(mcd饲料)和进食不缺乏蛋氨酸和胆碱饲料饮食组(mcs饲料)。mcd饲料组和mcs饲料组分别分为正常对照组、鼠尾草酚(40mg/kg)组、mcc950(40mg/kg)组。对照组每天灌胃给药0.2mlpbs一周,鼠尾草酚组和mcc950组每天灌胃给药一周,一周后隔一天给药一次,直到6周。6周后小鼠眼球取血,取3500rpm/min离心,测血清中il-1β、tnf-α、alt、ast的含量;解剖小鼠,肝大叶放入10%中性福尔马林缓冲液中固定,he染色检测肝细胞损伤,tunnel染色检测肝细胞凋亡,其余肝组织放到-80℃保存。
结果:
1.从图1中可以看出,在lps预处理的基础上给予鼠尾草酚,然后给予刺激因子nigericin诱导炎症小体活化,收集细胞上清和细胞裂解液。利用免疫印迹法对细胞上清中caspase-1p20和成熟il-1β及细胞裂解液中的nlrp3、asc等炎症小体相关蛋白进行检测,结果显示鼠尾草酚呈剂量依赖性的抑制细胞上清中的caspase-1p20和成熟il-1β的表达,但对细胞裂解液中的nlrp3、asc等炎症小体相关蛋白的表达没有影响(图1a)。进一步通过caspase-
2.从图2中可以看出,在lps预处理的基础上给予鼠尾草酚,然后给予atp、nigericin、sio2、poly(i:c)、poly(da:dt)、沙门氏杆菌等不同的刺激因素诱导炎症小体活化,收集细胞上清和细胞裂解液。利用免疫印迹法对细胞上清中caspase-1p20和成熟il-1β及细胞裂解液中的nlrp3、asc等炎症小体相关蛋白进行检测,结果显示鼠尾草酚显著抑制各种刺激因素活化下细胞上清中的caspase-1p20和成熟il-1β的表达,但对细胞裂解液中的nlrp3、asc等炎症小体相关蛋白的表达没有影响(图2a、b)。进一步通过caspase-
3.从图3a中可以看出,在lps诱导的小鼠感染休克模型中,鼠尾草酚对血清中il-1β的分泌有显著的抑制作用(p<0.05)。
4.从图3b中可以看出,鼠尾草酚显著降低革兰氏阴性菌感染引起的死亡。
5.从图4中可以看出,鼠尾草酚可以改善小鼠疾病症状,模型组小鼠结肠长度变短,鼠尾草酚对小鼠结肠长度有明显的恢复作用。与正常组相比,模型组体重明显降低(p<0.001)鼠尾草酚组无明显变化(p>0.05);而与模型组比较,鼠尾草酚+dss组体重降低情况明显改善(p<0.05)。与正常组比较,模型组炎症因子il-1β显著升高(p<0.05),鼠尾草酚组无明显变化;与模型组比较,鼠尾草酚+dss组il-1β显著降低(p<0.05)。
6.从图5可以看出,与正常对照组比较,模型组小鼠结肠长度变短,小鼠体重明显降低,炎症因子il-1显著升高(p<0.05)。与模型组比较,mcc950+dss组、鼠尾草酚+dss组、鼠尾草酚+mcc950+dss组小鼠结肠长度明显恢复,小鼠体重明显恢复(p<0.05),炎症因子il-1β显著降低(p<0.05)。与鼠尾草酚+dss组比较,mcc950+dss组、鼠尾草酚+mcc950+dss组结肠长度、小鼠体重、炎症因子il-1β无明显差别。说明鼠尾草酚主要通过抑制nlrp3炎症小体的活化来改善dss诱导的急性溃疡性结肠炎。
7.从图6可以看出,喂mcs饲料各组间alt、ast无显著差异;与只喂mcs饲料组比较,只喂mcd组alt、ast显著升高。与只喂mcd的模型组比较,在喂mcd饲料的基础上灌胃给药鼠尾草酚和mcc950,小鼠的alt、ast显著降低。说明鼠尾草酚对非酒精性脂肪肝有显著的治疗作用。
通过以上实施例的结果可以看出,在体外实验中,鼠尾草酚能够抑制atp、尼日利亚菌素、sio2、poly(i:c)、poly(da:dt)、沙门氏杆菌、转染lps等刺激引起的各种炎症小体的活化。在体内实验中,进一步发现鼠尾草酚明显降低lps感染休克症状和感染引起的死亡;显著改善化学性dss诱导的小鼠急性溃疡性结肠炎症状。由此可见,鼠尾草酚可作为预防或治疗与炎症小体异常活化相关疾病的潜在药物。
虽然本申请所揭露的实施方式如上,但所述的内容仅为便于理解本申请而采用的实施方式,并非用以限定本申请。任何本申请所属领域内的技术人员,在不脱离本申请所揭露的精神和范围的前提下,可以在实施的形式及细节上进行任何的修改与变化,但本申请的专利保护范围,仍须以所附的权利要求书所界定的范围为准。
- 还没有人留言评论。精彩留言会获得点赞!