催化剂及其用途的制作方法
发明领域
本发明涉及原样使用的生物催化剂,使用生物催化剂还原底物的方法和包含该生物催化剂的试剂盒。
背景
在有机合成中酶(生物催化剂)的使用为金属催化剂的使用提供了更为生态上可持续的替代方案,以及在催化的反应中允许高程度的化学、区位和/或对映选择性。
已经使用“oldyellowenzyme”家族的烯还原酶描述了用于烯烃衍生物的酶促还原的方法。例如,us2010/0035315描述了在来自枯草芽孢杆菌的酶yqjm和来自番茄植物的酶opr1和opr3的存在下的底物的还原,其中所述底物是浓度为5mm的烯烃衍生物。
发明概述
本发明人已经发现,可以有利地使用本文所述的催化剂进行还原反应,特别是不饱和碳-碳键的还原。具体地,本发明人已经发现,由于其对高底物浓度的耐受性,本文所述的催化剂特别可用于工业反应中的应用。
在一般方面,本发明提供了本文所述的催化剂作为催化剂(例如用于催化还原反应)的用途和使用本文所述的催化剂进行还原反应的方法。
在第一个开发中,本发明提供了本文所述的催化剂用于催化还原反应的用途,其中底物浓度是高的。例如,本发明提供了催化剂用于催化还原反应的用途,其中底物浓度为至少50mm,至少100mm,至少200mm,至少300mm或至少500mm。
在本发明的第一方面,提供了催化剂用于催化还原反应的用途,其中所述催化剂是包含与seqidno:1具有至少50%同一性的氨基酸序列的多肽。
在一个实施方案中,提供了催化剂用于催化还原反应的用途,其中所述催化剂是包含与seqidno:1具有至少50%同一性的氨基酸序列的多肽,并且其中底物浓度为至少10mm,例如至少100mm,例如至少200mm或至少500mm。该用途可以包括使底物与催化剂接触。
在一个实施方案中,提供了催化剂用于催化还原反应的用途,其中所述催化剂是包含与seqidno:1具有至少70%同一性的氨基酸序列的多肽,并且其中底物浓度为至少50mm。该用途可以包括使底物与催化剂接触。
在一个实施方案中,提供了催化剂用于催化还原反应的用途,其中所述催化剂是包含与seqidno:7具有至少70%同一性的氨基酸序列的多肽,并且其中底物浓度为至少50mm。该用途可以包括使底物与催化剂接触。
在一个实施方案中,提供了催化剂用于催化还原反应的用途,其中所述催化剂是包含与seqidno:9具有至少70%同一性的氨基酸序列的多肽,并且其中底物浓度为至少50mm。该用途可以包括使底物与催化剂接触。
在第二个开发中,本发明提供了本文所述的催化剂在还原底物的方法中的用途,其中底物浓度是高的。例如,本发明提供了催化剂在还原底物的方法中的用途,其中底物浓度为至少50mm,至少100mm,至少200mm,至少300mm或至少500mm。
在本发明的第二方面,提供了催化剂在还原底物的方法中的用途,所述方法包括使底物与催化剂接触,其中所述催化剂是包含与seqidno:1具有至少50%同一性的氨基酸序列的多肽。还提供了用于还原底物的方法,所述方法包括使底物与催化剂接触,其中所述催化剂是包含与seqidno:1具有至少50%同一性的氨基酸序列的多肽。还提供了催化剂在还原底物的方法中的用途,所述方法包括使底物与催化剂接触,其中所述催化剂是包含与seqidno:1具有至少70%同一性的氨基酸序列的多肽。还提供了用于还原底物的方法,所述方法包括使底物与催化剂接触,其中所述催化剂是包含与seqidno:1具有至少70%同一性的氨基酸序列的多肽。所述方法可任选地包括在共底物的存在下使底物与催化剂接触,在一个实施方案中,提供了催化剂在还原底物的方法中的用途,所述方法包括使底物与催化剂接触,其中所述催化剂是包含与seqidno:1具有至少70%同一性的氨基酸序列的多肽,并且其中在所述方法中,底物浓度为至少50mm。
在一个实施方案中,提供了催化剂在还原底物的方法中的用途,所述方法包括使底物与催化剂接触,其中所述催化剂是包含与seqidno:7具有至少70%同一性的氨基酸序列的多肽,并且其中在所述方法中,底物浓度为至少50mm。
在一个实施方案中,提供了催化剂在还原底物的方法中的用途,所述方法包括使底物与催化剂接触,其中所述催化剂是包含与seqidno:9具有至少70%同一性的氨基酸序列的多肽,并且其中在所述方法中,底物浓度为至少50mm。
在一个实施方案中,底物包含活化的乙烯基,例如位于酰基、羧基、酰氧基、硝基、酰基氨基或腈基的α、β位的乙烯基。
在一个实施方案中,底物包含活化的乙烯基,例如位于酰基、羧基、酰氧基、硝基或酰基氨基的α、β位的乙烯基。
本发明还提供了本文所述的催化剂、编码该催化剂的核酸、含有编码该催化剂的核酸的宿主细胞、表达该催化剂的宿主细胞、用于产生如本文所述的催化剂的方法、以及包含如本文所述的催化剂的催化剂制剂。本发明还提供了包含任选与一种或多种另外的催化剂一起的催化剂的试剂盒。
附图概述
图1显示了使用根据本发明实施方案的催化剂,一系列底物(示出的)至其还原形式(未示出)的转化百分比随时间(小时)过去的变化。
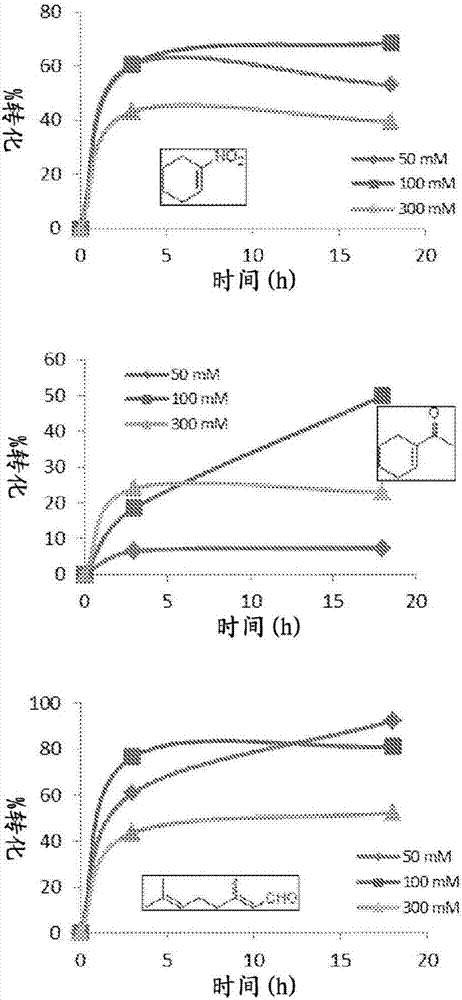
图2显示了使用根据本发明的实施方案的催化剂,在不同的底物浓度下,一系列底物(示出的)至其还原形式(未示出)的转化百分比随时间(小时)过去的变化。每个底物以50mm(菱形)、100mm(正方形)和300mm(三角形)使用。
图3显示了使用根据本发明实施方案的催化剂,随着反应介质的ph变化,催化剂活性(u/mg)的变化。使用底物柠檬醛。
图4显示了使用根据本发明的实施方案的催化剂,随着反应温度(℃)的变化,催化剂活性(u/mg)的变化。使用底物柠檬醛。
图5显示了使用根据本发明实施方案的催化剂,在不同反应温度下残留活性(u/mg)随时间(小时)的变化。反应在30℃(菱形)、40℃(正方形)和50℃(三角形)下进行。
图6显示了使用根据本发明实施方案的催化剂,随着反应介质共溶剂的变化,底物的转化百分比(通过gc测定的峰面积%;浅色阴影)的变化和还原产物的ee(深色阴影)的变化。每种共溶剂以5体积%使用。
图7显示了使用根据本发明实施方案的催化剂,随着添加到反应介质共溶剂中的添加剂的变化,底物的转化百分比(通过gc测定的峰面积%;浅色阴影)的变化和还原产物的ee(深色阴影)的变化。每种表面活性剂以0.1或0.3体积%使用。
图8显示了在不同底物浓度下底物的转化百分比随时间(小时)的变化。底物以750mm(菱形)和1,500mm(正方形)使用。
图9显示了在不同底物浓度下产物浓度(mm)随时间(小时)的变化。底物以750mm(菱形)和1,500mm(正方形)使用。
图10显示了底物的转化百分比随时间(小时)的变化。底物以730mm使用。
图11显示了产物浓度(mm)随时间(小时)的变化。底物以730mm使用。
图12显示了对于不同底物的ene-101(正方形)、ene-102(菱形)和ene-103(三角形)的转化特征谱。
图13a和13b显示了对于不同浓度的不同底物的ene-101、ene-102和ene-103的转化特征谱。
图14显示了对于ene-101、ene-102和ene-103的底物转化百分比随时间(小时)的变化。对于ene-102(圆圈)使用300mm的底物,对于ene-101(实心三角形)、ene-102(正方形)和ene-103(空心三角形)使用750mm,对于ene-101(菱形)使用1.5m。
图15显示了对于ene-101、ene-102和ene-103的产物浓度(mm)随时间(小时)的变化。对于ene102(圆圈)使用300mm的底物,对于ene-101(实心三角形)、ene-102(正方形)和ene-103(空心三角形)使用750mm,对于ene-101(菱形)使用1.5m。
图16显示了对于ene-101(实心三角形)、ene-102(正方形)和ene-103(空心三角形)的底物转化百分比随时间(小时)的变化。底物以730mm使用。
图17显示了对于ene-101(实心三角形)、ene-102(正方形)和ene-103(空心三角形)的产物浓度(mm)随时间(小时)的变化。底物以730mm使用。
图18显示了seqidno:1、7和9的clustalomega(1.2.1)多重序列比对。
序列
用于本发明的催化剂在本文中参考下面列出的序列识别号进行描述。序列公开在序列表中。
seqidno:1:催化剂氨基酸序列(ene-101氨基酸序列)
seqidno:2:编码催化剂的核酸序列(编码seqidno:1)
seqidno:3:编码催化剂的密码子优化的核酸序列(编码seqidno:1)
seqidno:4:催化剂氨基酸序列,包含t7标签
seqidno:5:催化剂氨基酸序列,包含his标签和t7标签
seqidno:6:编码包含his标签和t7标签的催化剂的核酸序列(编码seqidno:5)
seqidno:7:催化剂氨基酸序列(ene-102氨基酸序列)
seqidno:8:编码催化剂的核酸序列(编码seqidno:7)
seqidno:9:催化剂氨基酸序列(ene-103氨基酸序列)
seqidno:10:编码催化剂的核酸序列(编码seqidno:9)
发明详述
本发明提供了催化剂在底物反应中的用途。如下文进一步详细描述的,所述催化剂适合用于还原反应,例如活化的乙烯基的还原。所述催化剂允许以高产率(例如大于90%的转化率)和/或以高的立体选择性(例如大于99%的ee)产生反应产物。所述催化剂可以在高底物浓度(例如50、100和300mm)下使用。实际上,本发明人已经确定,催化剂可以在高达750和1,500mm的底物浓度下使用。
本发明提供了催化剂用于催化还原反应的用途,其中底物浓度是高的。本发明提供了催化剂用于催化还原反应的用途,其中底物浓度是高的,并且其中所述催化剂是包含氨基酸序列的多肽,所述氨基酸序列与图18中所示的氨基酸序列之一具有至少70%的同一性。
本发明提供了催化剂作为还原催化剂的用途,其中所述催化剂是包含与seqidno:1具有至少70%同一性的氨基酸序列的多肽。本发明提供了催化剂作为还原催化剂的用途,其中所述催化剂是包含与seqidno:7具有至少70%同一性的氨基酸序列的多肽。本发明提供了催化剂作为还原催化剂的用途,其中所述催化剂是包含与seqidno:9具有至少70%同一性的氨基酸序列的多肽。该用途可以是用作氢化催化剂。
本发明提供了催化剂作为还原催化剂的用途,其中所述催化剂是包含与seqidno:1具有至少95%同一性的氨基酸序列的多肽。本发明提供了催化剂作为还原催化剂的用途,其中所述催化剂是包含与seqidno:7具有至少95%同一性的氨基酸序列的多肽。本发明提供了催化剂作为还原催化剂的用途,其中所述催化剂是包含与seqidno:9具有至少95%同一性的氨基酸序列的多肽。该用途可以是用作氢化催化剂。
本发明提供了催化剂作为还原催化剂的用途,其中所述催化剂是包含seqidno:1的氨基酸序列或由seqidno:1的氨基酸序列组成的多肽。本发明提供了催化剂作为还原催化剂的用途,其中所述催化剂是包含seqidno:7的氨基酸序列或由seqidno:7的氨基酸序列组成的多肽。本发明提供了催化剂作为还原催化剂的用途,其中所述催化剂是包含seqidno:9的氨基酸序列或由seqidno:9的氨基酸序列组成的多肽。该用途可以是用作氢化催化剂。
本发明人已经显示,本文所述的催化剂能够在高的底物浓度的存在下催化反应。高底物或产物浓度对酶活性的抑制在酶促过程的按比例扩大中通常是一个显著的问题。因此,本文公开的催化剂、用途和方法对于工艺按比例扩大是有利的。
本发明提供了本文所述的催化剂用于催化还原反应的用途,其中底物浓度是高的。例如,本发明提供了催化剂用于催化还原反应的用途,其中底物浓度为至少10mm,至少20mm,至少50mm,至少100mm,至少200mm,至少300mm,至少500mm或至少1500mm。所述催化剂是如本文所述的催化剂,例如催化剂可以是包含与seqidno:1、7或9中任一个具有至少70%序列同一性的氨基酸序列的多肽。所述催化剂可以是包含与seqidno:1、7或9中任一个具有至少80%,至少90%,至少95%,至少98%,至少99%或100%序列同一性的氨基酸序列的多肽。
在一个实施方案中,本发明提供了催化剂用于催化还原反应的用途,其中底物浓度为至少50mm,并且其中所述催化剂是包含与seqidno:1、7或9中任一个具有至少95%序列同一性的氨基酸序列的多肽。
在一个实施方案中,本发明提供了催化剂用于催化还原反应的用途,其中底物浓度为至少100mm,并且其中所述催化剂是包含与seqidno:1、7或9中任一个具有至少95%序列同一性的氨基酸序列的多肽。
在一个实施方案中,本发明提供了催化剂用于催化还原反应的用途,其中底物浓度为至少50mm,并且其中所述催化剂为包含seqidno:1、7或9的氨基酸序列或由seqidno:1、7或9的氨基酸序列组成的多肽。
在一个实施方案中,本发明提供了催化剂用于催化还原反应的用途,其中底物浓度为至少100mm,并且其中所述催化剂是包含seqidno:1、7或9的氨基酸序列或由seqidno:1、7或9的氨基酸序列组成的多肽。
催化剂-结构
催化剂是多肽。多肽催化剂被称为酶,因此催化剂是酶。酶也被称为生物催化剂。更具体地,催化剂是还原酶。特别地,催化剂是能够还原具有2-环-己烯-1-酮或2-环戊烯-1-酮组分的底物的还原酶。催化剂能够使用nadh作为辅因子。催化剂是黄素依赖性酶。
催化剂可以是属于被称为“oldyellowenzymes”的组的酶。通过使用国际生物化学和分子生物学联合会的命名委员会(nc-iubmb)的命名法,催化剂是属于1类的酶(氧化还原酶)。催化剂可以是属于ec1.3的酶(该组包括作用于供体的ch-ch基团的氧化还原酶)。催化剂可以是属于ec1.3.1的酶(该组使用nadh或nadph作为辅因子)。催化剂可以是属于ec1.3.1.42的酶(该组包括12-氧代植物二烯酸(oxophytodienoate)还原酶)。
催化剂可以是重组多肽,即,催化剂可以已经从重组核酸序列表达,如下文更详细讨论的。催化剂可以从本文提供的核酸表达。催化剂可以从seqidno:3所示的核酸序列表达。
或者,催化剂可以是天然存在的多肽。催化剂可以是由细菌中的内源(天然)基因表达的还原酶。
催化剂可以是由植物杆菌属西瓜嗜酸菌(acidovoraxavenae)表达的酶。催化剂可以是由西瓜嗜酸菌(a.avenae)表达的还原酶。具体地,催化剂可以是由保藏为atcc19860的西瓜嗜酸菌(lucas等人,2011)表达的还原酶。由登录号f0q098鉴定的多肽(uniprot数据库中的变型1)是由通过登录号adx43981.1鉴定的西瓜嗜酸菌核酸序列(变型1,embl-ebieuropeannucleotidearchive,lucas等人,2011)编码的还原酶。
seqidno:1所示的氨基酸序列是f0q098的氨基酸序列。seqidno:2所示的核酸序列是adx43981.1的核酸序列。
催化剂可以是由紫色色杆菌(chromobacteriumviolaceum)表达的酶。催化剂可以是由紫色色杆菌(c.violaceum)表达的还原酶。具体地,催化剂可以是由保藏为atcc12472的紫色色杆菌表达的还原酶。由登录号q7nsc5鉴定的多肽是由紫色色杆菌编码的还原酶(变型1,uniprot,2003年12月15日发布)。
seqidno:7所示的氨基酸序列是q7nsc5的氨基酸序列。
催化剂可以是由芽孢杆菌属物种表达的酶。催化剂可以是由芽孢杆菌属物种表达的还原酶。具体地,催化剂可以是由芽孢杆菌属的种nrrlb-14911表达的还原酶。由登录号q2b6d5鉴定的多肽是由芽孢杆菌属的种nrrlb-14911编码的还原酶(变型1,uniprot,2006年4月4日发布)。
seqidno:9所示的氨基酸序列是q2b6d5的氨基酸序列。
图18显示seqidno:1、seqidno:7和seqidno:9的比对。在图18和本申请的其它地方,seqidno:1的氨基酸序列被称为ene-101,seqidno:7的氨基酸序列被称为ene-102,seqidno:9的氨基酸序列被称为ene-103。
催化剂可以是包含与seqidno:1具有至少约50%同一性的氨基酸序列的多肽。催化剂可以是包含与seqidno:1具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%或至少约99%序列同一性的氨基酸序列的多肽。催化剂可以是包含与seqidno:1具有100%同一性的氨基酸序列的多肽,即,催化剂可以是包含如seqidno:1所示的氨基酸序列的多肽。
催化剂可以是包含与seqidno:7具有至少约50%同一性的氨基酸序列的多肽。催化剂可以是包含与seqidno:7具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%或至少约99%序列同一性的氨基酸序列的多肽。催化剂可以是包含与seqidno:7具有100%同一性的氨基酸序列的多肽,即,催化剂可以是包含如seqidno:7所示的氨基酸序列的多肽。
催化剂可以是包含与seqidno:9具有至少约50%同一性的氨基酸序列的多肽。催化剂可以是包含与seqidno:9具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%或至少约99%序列同一性的氨基酸序列的多肽。催化剂可以是包含与seqidno:9具有100%同一性的氨基酸序列的多肽,即,催化剂可以是包含如seqidno:9所示的氨基酸序列的多肽。
催化剂可以是基本上由与seqidno:1具有至少约50%序列同一性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:1具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%,至少约95%或至少约99%序列同一性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:1具有100%序列同一性的氨基酸序列组成的多肽,即催化剂可以是基本上由seqidno:1所示的氨基酸序列组成的多肽。
催化剂可以是基本上由与seqidno:7具有至少约50%序列同一性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:7具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%,至少约95%或至少约99%序列同一性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:7具有100%序列同一性的氨基酸序列组成的多肽,即催化剂可以是基本上由seqidno:7所示的氨基酸序列组成的多肽。
催化剂可以是基本上由与seqidno:9具有至少约50%序列同一性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:9具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%,至少约95%或至少约99%序列同一性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:9具有100%序列同一性的氨基酸序列组成的多肽,即催化剂可以是基本上由seqidno:9所示的氨基酸序列组成的多肽。
催化剂可以是由与seqidno:1具有至少约50%序列同一性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:1具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%或至少约99%序列同一性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:1具有100%序列同一性的氨基酸序列组成的多肽,即,催化剂可以是由seqidno:1所示的氨基酸序列组成的多肽。
催化剂可以是由与seqidno:7具有至少约50%序列同一性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:7具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%或至少约99%序列同一性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:7具有100%序列同一性的氨基酸序列组成的多肽,即,催化剂可以是由seqidno:7所示的氨基酸序列组成的多肽。
催化剂可以是由与seqidno:9具有至少约50%序列同一性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:9具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%或至少约99%序列同一性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:9具有100%序列同一性的氨基酸序列组成的多肽,即,催化剂可以是由seqidno:9所示的氨基酸序列组成的多肽。
催化剂可以是包含与seqidno:1具有至少约50%相似性的氨基酸序列的多肽。序列相似性也被称为序列同源性。催化剂可以是包含与seqidno:1具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%或至少约99%相似性的氨基酸序列的多肽。催化剂可以是包含与seqidno:1具有100%相似性的氨基酸序列的多肽。
催化剂可以是包含与seqidno:7具有至少约50%相似性的氨基酸序列的多肽。序列相似性也被称为序列同源性。催化剂可以是包含与seqidno:7具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%或至少约99%相似性的氨基酸序列的多肽。催化剂可以是包含与seqidno:7具有100%相似性的氨基酸序列的多肽。
催化剂可以是包含与seqidno:9具有至少约50%相似性的氨基酸序列的多肽。序列相似性也被称为序列同源性。催化剂可以是包含与seqidno:9具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%或至少约99%相似性的氨基酸序列的多肽。催化剂可以是包含与seqidno:9具有100%相似性的氨基酸序列的多肽。
催化剂可以是基本上由与seqidno:1具有至少约50%序列相似性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:1具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%,或至少约99%序列相似性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:1具有100%序列相似性的氨基酸序列组成的多肽。
催化剂可以是基本上由与seqidno:7具有至少约50%序列相似性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:7具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%,或至少约99%序列相似性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:7具有100%序列相似性的氨基酸序列组成的多肽。
催化剂可以是基本上由与seqidno:9具有至少约50%序列相似性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:9具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%,或至少约99%序列相似性的氨基酸序列组成的多肽。催化剂可以是基本上由与seqidno:9具有100%序列相似性的氨基酸序列组成的多肽。
催化剂可以是由与seqidno:1具有至少约50%序列相似性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:1具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%,或至少约99%序列相似性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:1具有100%序列相似性的氨基酸序列组成的多肽。
催化剂可以是由与seqidno:7具有至少约50%序列相似性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:7具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%,或至少约99%序列相似性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:7具有100%序列相似性的氨基酸序列组成的多肽。
催化剂可以是由与seqidno:9具有至少约50%序列相似性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:9具有至少约60%,至少约70%,至少约80%,至少约90%,至少约95%,至少约98%,或至少约99%序列相似性的氨基酸序列组成的多肽。催化剂可以是由与seqidno:9具有100%序列相似性的氨基酸序列组成的多肽。
催化剂可以是包含与如上所述的seqidno:1、seqidno:7或seqidno:9具有一定百分比序列同一性和/或相似性的氨基酸序列的多肽。所述多肽可以包含一个或多个另外的氨基酸。例如,多肽可以进一步包含亲和标签。亲和标签可用于纯化催化剂。这样的亲和标签是本领域公知的。例如,亲和标签可以是用于使用镍柱纯化催化剂的多组氨酸标签(“his标签”),其可以是用于使用包含抗-t7标签抗体的柱子纯化蛋白质的t7表位标签(t7标签),或其可以是用于使用谷胱甘肽柱纯化催化剂的谷胱甘肽-s-转移酶标签(“gst标签”)。亲和标签可以位于多肽的n末端或c末端。或者或另外地,多肽还可以在n-末端包含前导序列。前导序列可用于在重组表达系统中指导多肽的分泌和/或细胞内靶向。前导序列也被称为信号肽,并且是本领域熟知的。或者或另外地,多肽可进一步包含标记,例如荧光标记。
催化剂可以是包含与seqidno:1、seqidno:7或seqidno:9具有一定百分比序列同一性和/或相似性的氨基酸序列加上一个或多个另外的氨基酸的多肽,如上文所示的。催化剂可以是包含由seqidno:1、seqidno:7或seqidno:9所示的氨基酸序列组成的氨基酸序列的多肽。特别地,催化剂可以是包含由seqidno:1所示的氨基酸序列加上n端t7标签组成的氨基酸序列的多肽(例如seqidno:4所示的多肽)。催化剂可以是包含由seqidno:1所示的氨基酸序列加上n端his标签和t7标签组成的氨基酸序列的多肽(例如seqidno:5所示的多肽)。
催化剂-功能
所述催化剂是还原酶。所述催化剂能够催化如本文所定义的底物的还原。具体地,所述催化剂能够还原不饱和碳-碳双键。特别地,所述催化剂可以能够催化以下反应图解中所示的反应:
其中-r1至-r4中的每一个如下文进一步详细定义,例如在共底物的存在下。
在本发明的某些实施方案中,催化剂可以能够催化以下反应方案中所示的反应:
其中-r1至-r4中的每一个如下文进一步详细定义,例如在共底物的存在下。
可以通过光度法测量催化剂的活性,例如通过在作为辅因子的nadh的存在下进行反应并测量由nadh的氧化引起的在340nm处的吸光度的降低。
在一个实施方案中,本发明的催化剂是在nadh辅助因子的存在下在底物还原中具有活性的酶。
酶的量可以在其活性方面使用酶单位来表示。一个酶单位(u)是每分钟转化1微摩尔底物的酶的量。通常,使用参考底物测定催化剂制剂中存在的酶单位的数目,例如提供u/mg催化剂制剂。一个u的本发明的催化剂可以被定义为在22℃、ph7下每分钟催化1μmolnadh至nad的催化剂的量,例如当参考底物是1-辛烯-3-酮时。参考底物可以以0.98mm的浓度存在于测定混合物中。可以使用本领域技术人员已知的技术,使用340nm处吸光度的变化来监测nadh至nad的反应。
以酶单元计的催化剂的活性可用于表示存在于催化剂制剂(其可提供如下所述的相对粗制形式的催化剂)中的酶的量。
(开特(katal)表示使用si基本单位的酶活性,其中一个开特是每秒转化1摩尔底物的酶的量,因此1u等于1/60微开特)。
例如,催化剂制剂中存在的酶单位的数目可以根据下面所述的测定程序来确定。
将含有980μl溶液a(1-辛烯-3-酮在ph7.0的0.1m磷酸钾缓冲液中的1mm溶液)的两个比色皿在22℃下孵育至少5分钟,以提供测试比色皿和空白比色皿。通过加入10μl溶液b(h2o中的15mmnadh)和10μl溶液c(h2o中的酶(例如冻干的酶)溶液;0.8mg催化剂制剂/mlh2o)并充分混合来在测试比色皿中起始反应。将10μl溶液b和10μlh2o加入空白比色皿中并充分混合。测定在22℃在340nm处1分钟内的吸光度的降低。(如果降低不是线性的,则酶溶液(溶液c)应用h2o稀释。对于测试比色皿和空白比色皿均使用最大线性速率确定δa340min-1。以u/mg催化剂制剂计的酶活性使用以下公式确定:
(δa340min-1测试-δa340min-1空白)/(6.2x0.01x0.8)
其中6.2x103lmol-1cm-1是nadh在340nm处的摩尔消光系数,0.01是酶溶液的体积(ml),0.8是催化剂制剂的量(mg/ml)(并且可以基于溶液c的任何稀释度进行调整)。
本文公开的催化剂是还原酶。它们可以催化3-甲基环己-2-烯-1-酮(表1的条目4至6中所示的底物)的还原,以产生具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的ee值的产物。这里,催化剂可以用于如本文所述的实验程序1或实验程序2中所示的方法。
其为包含与seqidno:1至少50%相同的氨基酸序列并且相对于seqidno:1的氨基酸序列包含一个或多个氨基酸添加、取代和/或缺失的多肽的催化剂可以催化3-甲基环己-2-烯-1-酮(表1的条目4至6中所示的底物)的还原以产生具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的ee值的产物。这里,催化剂可以用于如本文所述的实验程序1或实验程序2中所示的方法。
其为包含与seqidno:7至少50%相同的氨基酸序列并且相对于seqidno:7的氨基酸序列包含一个或多个氨基酸添加、取代和/或缺失的多肽的催化剂可以催化3-甲基环己-2-烯-1-酮(表1的条目4至6中所示的底物)的还原以产生具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的ee值的产物。这里,催化剂可以用于如本文所述的实验程序1或实验程序2中所示的方法。
本文公开的催化剂是还原酶。它们可以催化2-甲基环戊-2-烯-1-酮(表1的条目7至9中所示的底物)的还原,以得到具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物。这里,催化剂可以用于如本文实验部分所述的实验程序1或实验程序2中所示的方法。
其为包含与seqidno:1至少50%相同的氨基酸序列并且相对于seqidno:1的氨基酸序列包含一个或多个氨基酸添加、取代和/或缺失的多肽的催化剂可以催化2-甲基环戊-2-烯-1-酮(表1的条目7至9所示的底物)的还原,以得到具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物。这里,催化剂可以用于如本文实验部分所述的实验程序1或实验程序2中所示的方法。
其为包含与seqidno:7至少50%相同的氨基酸序列并且相对于seqidno:7的氨基酸序列包含一个或多个氨基酸添加、取代和/或缺失的多肽的催化剂可以催化2-甲基环戊-2-烯-1-酮(表1的条目7至9所示的底物)的还原,以得到具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物。这里,催化剂可以用于如本文实验部分所述的实验程序1或实验程序2中所示的方法。
其为包含与seqidno:9至少50%相同的氨基酸序列并且相对于seqidno:9的氨基酸序列包含一个或多个氨基酸添加、取代和/或缺失的多肽的催化剂可以催化2-甲基环戊-2-烯-1-酮(表1的条目7至9所示的底物)的还原,以得到具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物。这里,催化剂可以用于如本文实验部分所述的实验程序1或实验程序2中所示的方法。
本文所述的催化剂是具有高底物耐受性的还原酶。当底物浓度为50mm时,它们可以催化2-甲基环戊-2-烯-1-酮(表1的条目7至9所示的底物)的还原,以得到具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物。这里,催化剂可以用于如本文实验部分所述的实验程序1或实验程序2中所示的方法。反应时间可以是18小时。在下文示出的“测试反应条件”中催化剂可以能够提供具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物。
本文所述的催化剂是具有高底物耐受性的还原酶。当底物浓度为100mm时,它们可以催化2-甲基环戊-2-烯-1-酮(表1的条目7至9中所示的底物)的还原,以得到具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物。这里,催化剂可以用于如本文实验部分所述的实验程序1或实验程序2中所示的方法。反应时间可以是18小时。在下文示出的“测试反应条件”中催化剂可以能够提供具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物。
本文所述的催化剂是具有高底物耐受性的还原酶。当底物浓度为300mm时,它们可以催化2-甲基环戊-2-烯-1-酮(表1的条目7至9中所示的底物)的还原,以得到具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物。这里,催化剂可以用于如本文实验部分所述的实验程序1或实验程序2中所示的方法。反应时间可以是18小时。在下文示出的“测试反应条件”中催化剂可以能够提供具有70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物。
“测试反应条件”可以是在35℃下的250mm磷酸盐缓冲液ph7、1.1mmnad+、30mmd-葡萄糖、10u/mlgdh。反应时间可以是3、6或18小时。
技术人员能够将不具有高底物耐受性的催化剂与本公开内容的催化剂(其具有高底物耐受性并因此适于本文所述的用途和方法)区分开。具有高底物耐受性的催化剂具有上文所述的功能性能力。相比之下,不具有高底物耐受性的催化剂不具有那些功能性能力。不具有高底物耐受性的催化剂可以在底物浓度为50mm时催化2-甲基环戊-2-烯-1-酮(表1的条目7至9所示的底物)的还原,以得到具有20%或更低、10%或更低、5%或更低或2%或更低的转化率。不具有高底物耐受性的催化剂可以在底物浓度为20mm或更低时催化2-甲基环戊-2-烯-1-酮的还原以得到具有30%或更高、40%或更高、50%或更高、60%或更高、70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物,并且在底物浓度为50mm或更高时,得到具有30%或更低、20%或更低、10%或更低、5%或更低或2%或更低的转化率的产物。不具有高底物耐受性的催化剂可以在底物浓度为20mm或更低时催化2-甲基环戊-2-烯-1-酮的还原,以得到具有30%或更高、40%或更高、50%或更高、60%或更高、70%或更高、80%或更高、90%或更高、95%或更高、98%或更高、99%或更高或99.9%或更高的转化率的产物,并且在底物浓度为300mm或更高时,得到具有30%或更低、20%或更低、10%或更低、5%或更低或2%或更低的转化率的产物。这里,催化剂可以在如本文实验部分所述的实验程序1或实验程序2中所示的方法中或在上述“测试条件”下使用。反应时间可以是18小时。
核酸
本文提供了编码催化剂的核酸序列。核酸可以是dna或rna。核酸可以是单链或双链的。催化剂可以由如seqidno:2中所示的核酸序列编码,所述核酸序列是来自西瓜嗜酸菌基因组(lucas等人,2011)的核酸序列。seqidno:2的核酸序列编码seqidno:1的氨基酸序列。因为遗传密码是简并的(多于一个密码子可以编码一个氨基酸),所以可以改变seqidno:2的核酸序列,以提供也编码seqidno:1的氨基酸序列的其它核酸序列。
催化剂可以由如seqidno:8中所示的核酸序列编码。seqidno:8的核酸序列编码seqidno:7的氨基酸序列。因为遗传密码是简并的(多于一个密码子可以编码一个氨基酸),所以可以改变seqidno:8的核酸序列以提供也编码seqidno:7的氨基酸序列的其它核酸序列。
催化剂可以由如seqidno:10所示的核酸序列编码。seqidno:10的核酸序列编码seqidno:9的氨基酸序列。因为遗传密码是简并的(多于一个密码子可以编码一个氨基酸),所以可以改变seqidno:10的核酸序列,以提供也编码seqidno:9的氨基酸序列的其它核酸序列。
可将编码催化剂的核酸序列引入宿主细胞中,以提供表达催化剂的重组宿主细胞。可以通过提供表达催化剂的宿主细胞在细胞中提供催化剂。可以通过提供表达催化剂的宿主细胞、在宿主细胞中表达催化剂并分离催化剂,来以分离的形式提供催化剂。宿主细胞可以是原核细胞,例如大肠杆菌(escherichiacoli)、枯草芽孢杆菌(bacillussubtilis)或假单胞菌(pseudomonas)物种。宿主细胞可以是真核细胞,例如酵母细胞例如酿酒酵母(saccharomycescerevisiae)或哺乳动物细胞例如hela细胞或cho细胞。
可以优化编码催化剂的核酸序列以在重组宿主细胞中表达。因为遗传密码可以在生物体之间变化(密码子偏好可以在生物体之间变化),所以可以通过根据宿主细胞的密码子偏好改变编码多肽的核酸来改善特定宿主细胞中期望多肽的表达。为了改善催化剂在宿主细胞例如大肠杆菌中的表达,改变了西瓜嗜酸菌核酸序列seqidno:2以提供seqidno:3。因为遗传密码是简并的,所以可以改变seqidno:3的核酸序列,以提供在宿主细胞例如大肠杆菌中也编码催化剂的其它核酸序列。因为密码子使用可以在生物体之间变化,所以可以改变seqidno:2和/或seqidno:3的核酸序列,以提供适于在其它宿主细胞中表达催化剂的其它核酸。因为催化剂可以是seqidno:1的氨基酸序列的变体,所以编码seqidno:1的变体的核酸序列可以适于在宿主细胞中表达催化剂。类似地,可以改变seqidno:8和seqidno:10的核酸序列以提供适于在其它宿主细胞中表达催化剂的其它核酸,并且因为催化剂可以是seqidno:7和seqidno:9的氨基酸序列的变体,所以编码seqidno:7或seqidno:9的变体的核酸序列可适于在宿主细胞中表达催化剂。
编码催化剂的核酸序列可以包含与seqidno:3具有至少50%同一性的核酸序列。编码催化剂的核酸序列可以包含与seqidno:3具有至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约98%或至少约99%同一性的核酸序列。编码催化剂的核酸序列可以包含与seqidno:3具有100%同一性的核酸序列。编码催化剂的核酸序列可以包含如seqidno:3所示的核酸序列。
编码催化剂的核酸序列可以包含与seqidno:8具有至少50%同一性的核酸序列。编码催化剂的核酸序列可以包含与seqidno:8具有至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约98%或至少约99%同一性的核酸序列。编码催化剂的核酸序列可以包含与seqidno:8具有100%同一性的核酸序列。编码催化剂的核酸序列可以包含如seqidno:8中所示的核酸序列。
编码催化剂的核酸序列可以包含与seqidno:10具有至少50%同一性的核酸序列。编码催化剂的核酸序列可以包含与seqidno:10具有至少约60%、至少约70%、至少约80%、至少约90%、至少约95%、至少约98%或至少约99%同一性的核酸序列。编码催化剂的核酸序列可以包含与seqidno:10具有100%同一性的核酸序列。编码催化剂的核酸序列可以包含如seqidno:10所示的核酸序列。
编码催化剂的核酸可以是分离的和/或纯化的形式,或者不含或基本上不含与其天然缔合的物质,例如不含或基本上不含在西瓜嗜酸菌基因组中seqidno:2侧翼的核酸序列。编码催化剂的核酸可以是分离的和/或纯化的形式,或者不含或基本上不含与其天然缔合的物质,例如不含或基本上不含在紫色色杆菌基因组中seqidno:8侧翼的核酸序列。编码催化剂的核酸可以是分离的和/或纯化的形式,或者不含或基本上不含与其天然缔合的物质,例如不含或基本上不含在芽孢杆菌物种基因组中seqidno:10侧翼的核酸序列。
通常,编码催化剂的核酸可以通过修饰seqidno:2或seqidno:3获得。重组技术诸如定点诱变可用于修饰seqidno:2或seqidno:3,以提供编码催化剂的其它核酸序列。这样的其它核酸序列可以编码seqidno:1的变体。编码催化剂的核酸可以通过修饰seqidno:8获得。重组技术诸如定点诱变可用于修饰seqidno:8以提供编码催化剂的其它核酸序列。这样的其它核酸序列可以编码seqidno:7的变体。编码催化剂的核酸可以通过修饰seqidno:10获得。重组技术诸如定点诱变可用于修饰seqidno:10以提供编码催化剂的其它核酸序列。这样的其它核酸序列可以编码seqidno:9的变体。
本发明提供了包含如seqidno:3所示的核酸序列的核酸。本发明还提供了包含与seqidno:3具有至少80%、至少90%、至少95%、至少98%或至少99%同一性的核酸序列的核酸,其中所述核酸编码催化剂。本发明提供了包含与seqidno:3具有至少80%、至少90%、至少95%、至少98%或至少99%同一性的核酸序列的核酸,其中所述核酸编码包含与seqidno:1具有至少50%同一性的氨基酸序列的多肽,所述多肽是还原酶。
本发明提供了包含seqidno:8所示的核酸序列的核酸。本发明还提供了包含与seqidno:8具有至少80%、至少90%、至少95%、至少98%或至少99%同一性的核酸序列的核酸,其中所述核酸编码催化剂。本发明提供了包含与seqidno:8具有至少80%、至少90%、至少95%、至少98%或至少99%同一性的核酸序列的核酸,其中所述核酸编码包含与seqidno:7具有至少50%同一性的氨基酸序列的多肽,所述多肽是还原酶。
本发明提供了包含seqidno:10所示的核酸序列的核酸。本发明还提供了包含与seqidno:10具有至少80%、至少90%、至少95%、至少98%或至少99%同一性的核酸序列的核酸,其中所述核酸编码催化剂。本发明提供了包含与seqidno:10具有至少80%、至少90%、至少95%、至少98%或至少99%同一性的核酸序列的核酸,其中所述核酸编码包含与seqidno:9具有至少50%同一性的氨基酸序列的多肽,所述多肽是还原酶。
用于产生催化剂的载体、宿主细胞和方法
编码催化剂的核酸可以并入可复制的载体中。载体可以用于在相容的宿主细胞中复制核酸。因此,编码催化剂的核酸可以通过将编码催化剂的核酸引入可复制的载体中、将载体引入相容性宿主细胞中并在导致载体复制的条件下生长宿主细胞来产生。
编码催化剂的核酸可以可操作地连接到能够提供催化剂在宿主细胞中的表达的控制序列。例如,编码催化剂的核酸可以在表达载体中。例如,编码催化剂的核酸可以在质粒或染色体中。术语“可操作地连接”是指其中所描述的组分处于允许它们以其预期方式发挥功能的关系中的毗连。“可操作地连接”编码序列的控制序列以这样的方式连接,其使得编码序列的表达在与控制序列相容的条件下实现。
任选地,seqidno:2中的n末端ttg密码子可以用起始密码子如atg替换。
可以选择或构建合适的载体,其包含合适的调节序列,包括启动子序列、终止子片段、多聚腺苷酸化序列、增强子序列、标记基因和其它适当的序列。视情况而定,载体可以是质粒、病毒例如噬菌体噬粒或杆状病毒、粘粒、yac、bac或pac。载体包括基因治疗载体,例如基于腺病毒、腺相关病毒、逆转录病毒(例如hiv或mlv)的载体或α病毒载体。
载体可以具有复制起点、任选地用于表达催化剂的启动子和任选地启动子的调节子。载体可以是低拷贝质粒、中等拷贝质粒或高拷贝质粒。载体可以含有一个或多个选择性标记基因,例如在细菌质粒的情况下的氨苄青霉素抗性基因或用于哺乳动物载体的新霉素抗性基因。载体可以在体外使用,例如用于产生rna或用于转染或转化宿主细胞。用于在多种不同宿主细胞中克隆和表达多肽的系统是公知的。
载体可以包含其它序列例如启动子或增强子以驱动插入的核酸的表达。启动子可以是诱导型启动子,以使得可以通过向宿主细胞生长培养基中加入诱导剂来开始或增强催化剂的表达。例如,启动子可以基于lac操纵子,对于该操纵子iptg(异丙基-β-d-硫代半乳糖苷)是诱导剂。或者,启动子可以是组成型活性启动子。启动子可以是强启动子。
载体可以包含其它核酸序列,以使得催化剂作为融合蛋白(例如包含催化剂和亲和标签的融合蛋白)产生,和/或包含编码前导序列的核酸序列,以使得在宿主细胞中产生的多肽从细胞分泌。
本文提供了宿主细胞,例如上述的宿主细胞,其可在使催化剂表达的条件下培养。催化剂可以在宿主细胞内提供。以这种方式,催化剂可以在还原反应中在体内使用,即,催化剂可以用于细胞内还原反应。或者,在催化剂的表达之后可以从宿主细胞中分离催化剂。可以使用电泳和/或色谱技术分离催化剂。可以例如通过将催化剂表达为包含亲和标签的融合蛋白并使用结合亲和标签的试剂回收融合蛋白来分离催化剂。例如该试剂可以附着至琼脂糖柱。可以在已分离蛋白质后从其切割掉亲和标签。
催化剂制剂
催化剂可以以纯的或基本上纯的形式提供。将纯的或基本上纯的形式的催化剂与天然伴随蛋白质的其它分子或细胞组分(例如核糖体,细胞膜组分)分离。
催化剂可以以相对粗的形式作为催化剂制剂提供,例如催化剂制剂可以是表达催化剂的重组细胞的裂解物或澄清的裂解物。催化剂制剂可以是表达催化剂的重组细胞的匀浆或糊剂。
催化剂可以包含在宿主细胞中。催化剂可以以游离形式或以固定化形式提供。固定化形式的催化剂可以附着至惰性载剂例如纤维素粉末或合成聚合物例如聚乙烯(lalondeandmargolin,2002)。
本文提供了产生催化剂的方法,所述方法包括在宿主细胞中表达编码催化剂的核酸,并从宿主细胞中分离催化剂。该方法可以包括裂解宿主细胞以提供细胞裂解物,并且还可以包括移除宿主细胞碎片(例如通过离心)以提供澄清的细胞裂解物。裂解宿主细胞的步骤可以使用包含黄素单核苷酸(fmn)的裂解缓冲液,例如裂解缓冲液可以包含约1-50μmfmn、或约5-25μmfmn、或约20μmfmn。另外或备选地,裂解宿主细胞的步骤可使用含有mgso4的裂解缓冲液,例如裂解缓冲液可包含约1-50mmmgso4、约1-5mmmgso4或约5mmmgso4。裂解缓冲液可以包含fmn和mgso4。
可以从催化剂或催化剂制剂中除去水,以提供冻干形式的催化剂。催化剂可以作为冻干物提供。催化剂或催化剂制剂可以是冷冻的。
催化剂制剂中的催化剂的量可以表示为酶单位(u)/mg催化剂制剂,例如表示为酶单位/mg冻干物。
催化剂制剂中的催化剂的量可以为至少约0.25u/mg催化剂制剂,至少约1u/mg催化剂制剂或至少约3u/mg催化剂制剂(例如使用上文所述的测定方法测定的)。催化剂制剂中的催化剂的量可以是至多约5u/mg催化剂制剂,至多约10u/mg催化剂制剂,至多约20u/mg催化剂制剂或至多约50u/mg催化剂制剂(例如使用上文所述的测定方法测定的)。催化剂制剂可以是包含至少约0.25u/mg冻干物、至少约1u/mg冻干物或至少约3u/mg冻干物的冻干物(例如使用上文所述的测定方法测定的)。冻干物中的催化剂的量可以是至多约5u/mg冻干物,至多约10u/mg冻干物,至多约20u/mg冻干物或至多约50u/mg冻干物(例如使用上文所述的测定方法测定的)。
制剂中催化剂的量可以在选自上文给出的较高量和较低量的范围内,例如在1-20u/mg催化剂制剂的范围内。
本发明提供了包含如本文所定义的催化剂的催化剂制剂。催化剂制剂可以包含至少一定量的如上所定义的催化剂(以u催化剂/mg催化剂制剂定义的)。例如,催化剂制剂可以包含其为包含与seqidno:1具有至少约70%序列同一性的氨基酸的多肽的催化剂,其中催化剂制剂中的催化剂的量为至少0.25u/mg催化剂制剂。例如,催化剂制剂可以包含其为包含与seqidno:7具有至少约70%序列同一性的氨基酸的多肽的催化剂,其中催化剂制剂中的催化剂的量为至少0.25u/mg催化剂制剂。例如,催化剂制剂可以包含其为包含与seqidno:9具有至少约70%序列同一性的氨基酸的多肽的催化剂,其中催化剂制剂中的催化剂的量为至少0.25u/mg催化剂制剂。
相似性和序列同一性
氨基酸序列同一性和相似性和核酸序列同一性可以使用标准生物信息学软件工具(例如可免费获得的emboss或blast软件工具)测量。通常使用默认参数。例如,embossneedle配对序列比对可用于确定氨基酸序列同一性。使用needleman-wunsch算法(j.mol.biol.(48):444-453(1970))的embossneedle配对序列比对可以用于确定氨基酸序列相似性,例如使用默认参数并使用blosum评分矩阵,例如blosum62评分矩阵。默认参数可以与间隙生成罚分=12和间隙扩展罚分=4一起使用。可以优选使用gap,但是可以使用其它算法,例如blast或tblastn(其使用altschul等人(1990)j.mol.biol.215:405-410的方法),fasta(其使用pearsonandlipman(1988)pnasusa85:2444-2448的方法),或smith-waterman算法(smithandwaterman(1981)j.molbiol.147:195-197),通常采用默认参数。
如上所述,催化剂是与seqidno:1具有至少50%氨基酸序列同一性并且能够催化底物的还原的多肽。与seqidno:1具有小于50%氨基酸序列同一性的催化剂能够催化底物的还原,因此具有至少50%氨基酸序列同一性的许多多肽也能够催化底物的还原。例如,被称为来自枯草芽孢杆菌的yqjm(ec1.6.99.1,uniprot条目p54550)的酶与seqidno:1具有约30%的序列同一性,并且能够还原某些
烯烃衍生物,由番茄oypr1基因编码的酶(ec1.3.1.42,uniprotq9xg54)与seqidno:1具有约42%的序列同一性,并且能够还原某些烯烃衍生物,以及由番茄oypr3基因编码的酶(ec1.3.1.42,uniprotq9few9)与seqidno:1具有约42%序列同一性并且能够还原某些烯烃衍生物(参见us2010/0035315,其通过引用整体并入
本文)。
其为包含与seqidno:1至少50%相同的氨基酸序列的多肽的催化剂可以包含相对于seqidno:1的氨基酸序列的一个或多个氨基酸添加、取代和/或缺失。催化剂可以包含相对于seqidno:1的氨基酸序列的一个或几个氨基酸添加、取代和/或缺失。相对于seqidno:1的氨基酸序列,催化剂可以包含1-150、1-100、1-50、1-20或1-10个氨基酸添加、取代和/或缺失。
其为包含与seqidno:7至少50%相同的氨基酸序列的多肽的催化剂可以包含相对于seqidno:7的氨基酸序列的一个或多个氨基酸添加、取代和/或缺失。相对于seqidno:7的氨基酸序列,催化剂可以包含一个或几个氨基酸添加、取代和/或缺失。相对于seqidno:7的氨基酸序列,催化剂可以包含1-150、1-100、1-50、1-20或1-10个氨基酸添加、取代和/或缺失。
其为包含与seqidno:9至少50%相同的氨基酸序列的多肽的催化剂可以包含相对于seqidno:9的氨基酸序列的一个或多个氨基酸添加、取代和/或缺失。催化剂可以包含相对于seqidno:9的氨基酸序列的一个或几个氨基酸添加、取代和/或缺失。相对于seqidno:9的氨基酸序列,催化剂可以包含1-150、1-100、1-50、1-20或1-10个氨基酸添加、取代和/或缺失。
本发明的催化剂可以是seqidno:1、7和9中任一个所示的多肽的变体。变体可以通过插入、添加、取代或缺失1个氨基酸、2、3、4、5-10、10-20、20-30、30-50、50-100或超过150个氨基酸而不同于seqidno:1、7和9中所示的序列。变体可以使用常规分子克隆方法制备。
技术人员知道如何制备这样的变体并且意识到可能影响催化剂的功能性能力的因素。例如,技术人员理解具有相对少的氨基酸插入、添加、缺失和取代的变体比具有相对多的氨基酸取代的变体相对更可能保留seqidno:1、7和9中所示的催化剂的功能性。技术人员还理解具有一个或多个保守氨基酸取代的变体比具有一个或多个非保守取代的变体更可能保留功能性。
seqidno:1、7和9的比对显示在图18中。关于如图18中所示的seqidno:1、7和9之间的保守氨基酸(由*表示)、强相似氨基酸(由:表示)和弱相似氨基酸(由.表示)表明可能需要避免取代的氨基酸位置。不保守、或不相似或仅微弱相似的氨基酸位置可以更适于取代同时保留功能性。因此,技术人员能够产生seqidno:所示多肽的变体。技术人员能够使用例如本文所述的方法确定变体多肽是否适合用作根据本发明的催化剂。氨基酸取代可以是保守氨基酸取代,其中seqidno:1、seqidno:7或seqidno:9的氨基酸被具有相似特征的氨基酸取代。例如疏水氨基酸(例如leu)被另一疏水氨基酸(例如ile)取代。氨基酸和保守取代显示在下表中。
用途
本发明的催化剂可以原样使用,例如用作离体例如体外反应中的催化剂。在此上下文中,体外反应是指细胞外或无细胞反应。
已经发现本发明的催化剂具有在还原反应中用作催化剂的用途。在一个实施方案中,还原反应是不饱和键例如不饱和碳-碳键、例如乙烯键的还原。催化剂可以被认为具有氢化活性或转移氢化活性。因此,本发明的催化剂通常用于还原含烯基的化合物,例如以得到相应的还原产物。
在一个实施方案中,本发明的催化剂用作还原本文所述的底物例如式(i)化合物的催化剂。本发明的催化剂可以被称为还原酶。因此,催化剂通常用于还原反应并且更特别地用于氢化反应。因此,催化剂可催化还原反应,其形式上导致在碳-碳双键(c=c)上添加氢。通常,本文所述的还原反应中的氢化物源由辅因子例如nadh提供。
在一个实施方案中,如上所述,本发明的催化剂在细胞内提供,用于细胞内反应。
在一个方面,提供了seqidno:1的催化剂用作催化剂的用途,任选地与辅因子一起使用。在另一方面,提供了seqidno:7的催化剂用作催化剂的用途,任选地与辅因子一起使用。在另一方面,提供了seqidno:9的催化剂用作催化剂的用途,任选地与辅因子一起使用。
在一个实施方案中,催化剂具有还原活性,例如氢化活性,例如碳-碳双键(c=c)的氢化。
在一个实施方案中,催化剂具有烯还原酶活性。
在一个实施方案中,本发明的催化剂用于本文所述的方法中。
方法
一方面,本发明提供了一种合成方法,该方法包括在本发明的催化剂的存在下使底物反应从而提供产物的步骤。该方法可以包括使底物与催化剂接触。
该方法可以是还原,并因此在催化剂和还原剂的存在下还原底物。
在一个实施方案中,反应是立体特异性反应。
任选地,该方法还包括分离产物的步骤,例如将产物与催化剂和任何剩余的底物分离。分离步骤可以包括将产物与副产物(例如作为产物的立体异构体(包括对映异构体)的那些产物)分离。分离步骤还可以包括将产物与反应介质分离的步骤。
在一个实施方案中,该方法包括分离催化剂的步骤。根据需要,催化剂随后可以在本发明的另一种方法中重复使用。
本发明的催化剂可以允许以高产率制备产物,例如还原的产物。工作实施例表明,催化剂可用于还原反应,以得到产率为50%或更高,例如60%或更高的产物。
本发明的方法可以在水中进行,通常在另一种溶剂(“共溶剂”)存在的情况下。反应介质可以是单相或双相的。
在一个实施方案中,共溶剂以至多10体积%、至多15体积%或至多25体积%的量存在。
在一个实施方案中,共溶剂以至少0.5体积%,至少1体积%或至少2体积%的量存在。
在一个实施方案中,共溶剂以约5体积%的量存在。
共溶剂可以选自由甲苯,二甲苯,乙醇,异丙醇,乙醚,四氢呋喃,2-甲基四氢呋喃,乙酸乙酯,乙酸异丙酯,乙腈,甲基叔丁基醚(mtbe),异丙醇,二甲基甲酰胺(dmf)和二甲基亚砜(dmso)。
在一个实施方案中,共溶剂是甲苯。
反应可以在其中水以非常低的量(例如相对于溶剂的总体积为5v/v%或更低)存在的反应介质中进行。这是不太优选的。
反应可以在环境温度或升高的温度下进行。
反应可以在至多35℃、至多40℃、至多45℃、至多50℃或至多55℃的温度下进行。如所预期的,非常高和持续的温度与酶活性的丧失相关。
反应可以在至少30℃、至少25℃、至少20℃、至少15℃或至少0℃的温度下进行。
本发明人已经发现,当催化剂在选自上文给出的较高量和较低量的范围内(例如在20至45℃的范围内或在20至35℃的范围内)的温度下使用时,获得最佳结果。
在水性介质中的反应可以在有限范围内的ph下进行。
在一个实施方案中,反应介质的ph为至多8,至多9或至多10。
在一个实施方案中,反应介质的ph为至少5,至少6,至少6.5或至少7。
本发明人已经发现,当催化剂在选自上文给出的较高量和较低量的范围内(例如在ph6.5至8的范围内)的ph下使用时,获得最佳结果。
反应介质的ph可以指反应开始时反应介质的ph。另外或可选择地,ph可以指反应的反应终点的ph。
可以在反应介质中提供缓冲液以将反应介质的ph保持在选自上面给出的较高值和较低值的范围内。
本发明人已经确定,本发明的催化剂可以在高底物浓度下使用。工作实施例证明了催化剂在300mm、750mm和1,500mm的底物浓度下的使用。相反,us2010/0035315中的工作证明生物催化剂仅在至多5mm的底物浓度下使用。
在一个实施方案中,底物以至少0.1mm,至少0.5mm,至少1mm,至少5mm,至少10mm,至少50mm,至少100mm,至少200mm,至少300mm,至少400mm,至少500mm,至少750mm,至少1,000mm,至少1,500mm,至少2,000mm,至少2,500mm或至少3,000mm的浓度存在。
在一个实施方案中,底物以至多50mm,至多100mm,至多200mm,至多300mm,至多500mm,至多1,000mm,至多1,500mm,至多2,000,至多2,500mm,至多3,000mm,至多3,500mm,至多4,000mm,至多4,500mm或至多5,000mm的浓度存在。
本发明人已经发现,当底物以在选自上面给出的较高量和较低量的范围内(例如在5mm至1,500mm的范围内)的浓度使用时,获得最佳结果。
底物浓度可以在50mm至5,000mm,50mm至3,000mm,50mm至1,500mm,50mm至1,000mm,50mm至500mm,100mm至5,000mm,100mm至3,000mm,100mm至1,500mm,100mm至1,000mm,500mm至5,000mm,500mm至3,000mm,500mm至1,500mm或500mm至1,000mm的范围内。
在一个实施方案中,底物以至少10mg/l,至少50mg/l,至少100mg/l,至少500mg/l,至少1,000mg/l,至少5g/l,至少10g/l,至少20g/l,至少30g/l,至少40g/l,至少50g/l,至少75g/l,至少100g/l,至少150g/l,至少200g/l,至少250g/l或至少300g/l的浓度存在。
在一个实施方案中,底物以至多5g/l,至多10g/l,至多20g/l,至多30g/l,至多50g/l,至多100l,至多150g/l,至多200g/l,至多250g/l,至多300g/l,至多350g/l,至多400g/l,至多450g/l,或至多500g/l的浓度存在。
反应中所需的催化剂制剂的量相对于存在的底物量可以是小的,并且就其在反应介质中的浓度而言是低的。例如,可以使用0.4g/l的催化剂制剂。
在一个实施方案中,催化剂制剂可以以至多5g/l,至多10g/l,至多50g/l,至多100g/l的浓度存在。
在一个实施方案中,催化剂制剂可以以至少0.05g/l,至少0.10g/l,至少0.25g/l,至少0.5g/l或至少1.0g/l的浓度存在。
在一个实施方案中,催化剂制剂以约0.4g/l存在。
在一个实施方案中,催化剂制剂以约0.4g/l存在。
如上所述,酶的量可以在其活性方面使用酶单位u来表示。u可以使用上文所述的测定来确定。类似地,酶的浓度可以表示为u/ml。
在一个实施方案中,酶可以以至多500u/ml,至多300u/ml,至多200u/ml或至多150u/ml的浓度存在。在一些实施方案中,酶可以以至多50u/ml的浓度存在。
在一个实施方案中,酶可以以至少1u/ml,至少5u/ml,至少10u/ml或至少20um/l的浓度存在。在一些实施方案中,酶可以以至少50u/ml的浓度存在。
本发明人已经发现,当酶以在选自上文给出的较高量和较低量的范围内的量使用时,获得最佳结果。
反应中所需的酶的量相对于存在的底物的量可以是小的。例如,每mmol底物可存在约70u的酶,或每mmol底物可存在约140u的酶。例如,每mmol底物可存在1250u的酶。
在一个实施方案中,酶以每mmol底物至多5000u,每mmol底物至多2500u,每mmol底物至多2000u,或每mmol底物至多1500u的量存在。在一些实施方案中,酶以每mmol底物至多500u,每mmol底物至多300u,或每mmol底物至多200u的量存在。
在一个实施方案中,酶以每mmol底物至少1u,每mmol底物至少10u,每mmol底物至少20u,每mmol底物至少40u,或每mmol底物至少60u的量存在。
本发明人已经发现,当酶以在选自上文给出的较高量和较低量的范围内的量使用时,获得最佳结果。
反应可以进行足够的时间以允许产生所需量的材料。随后,可以加工(workup)反应混合物以分离产物材料。
在一个实施方案中,反应时间为至少1小时,至少2小时或至少3小时。
在一个实施方案中,反应时间为至多18小时,至多24小时,至多36小时,至多48小时,至多72小时,至多96小时或至多120小时。
反应的结束可以是催化剂和产物的分离时。
当所需产物的产率不随时间显著增加时,可以认为反应完成。
在一个实施方案中,反应在体外进行。
反应可以连续或不连续进行。
底物
本发明的催化剂可以原样用于底物的反应中。底物在催化剂的存在下反应以产生产生。底物可与共底物反应以产生产物。
在一个实施方案中,底物是具有可以被还原的官能性的化合物。因此,反应的产物是还原产物。
在一个实施方案中,底物具有乙烯键(c=c)。反应的产物可以是具有还原的乙烯键的底物,例如-ch-ch-。
在一个实施方案中,乙烯键是活化的乙烯键。因此,乙烯键可以位于活化基团的α、β位。活化基团的实例包括酰基、羧基、酰氧基、硝基、酰基氨基和腈基。因此,底物可以具有α,β-不饱和酰基、酰氧基、硝基、酰基氨基或腈基。
在一个实施方案中,乙烯键是活化的乙烯键。因此,乙烯键可以位于活化基团的α、β位。活化基团的实例包括酰基、羧基、酰氧基、硝基或酰基氨基。因此,底物可以具有α,β-不饱和酰基、酰氧基、硝基或酰基氨基。
在一个实施方案中,底物是式(i)的化合物:
其中:
-r1独立地选自酰基、羧基、酰氧基、硝基、酰基氨基和腈;
-r2独立地选自氢、烷基、烯基、炔基、环烷基、杂环基、芳基、氨基、羟基和氧基,并且-r2任选地进一步选自酰氨基或腈;
-r3是氢、烷基、烯基、炔基、环烷基、杂环基、芳基、氨基、羟基、氧基、羧基、酰氧基、腈和酰基氨基,
或其中-r1是酰基、酰氧基或酰基氨基,-r1和-r2可以形成含有酰基、酰氧基或酰基氨基的环,或者-r1和-r3可以形成含有酰基、酰氧基或酰基氨基的环;和
-r4是氢、烷基、烯基、炔基、环烷基、杂环基、芳基、氨基、羟基、氧基、羧基、酰氧基、腈和酰基氨基,
并且烷基、烯基、炔基、环烷基、杂环基和芳基各自任选被取代;
或者-r2和-r4可一起形成未取代或取代的环。
在一个实施方案中,r1独立地选自酰基、羧基、酰氧基、硝基和酰基氨基。
在一个实施方案中,-r1是酰基或酰氧基。本发明人已经确定,在本发明的催化剂的存在下,具有存在于-r1的这样的基团的底物以良好的产率和/或以高对映体过量还原。
在一个实施方案中,-r1是酰基氨基。
在一个实施方案中,-r2是氢。在该实施方案中,-r3和-r4可以不同。在这种情况下,本发明人已经发现还原反应提供了具有特别高的对映体过量的产物。
在一个实施方案中,-r2是未取代的或取代的烷基,例如未取代的烷基。
在一个实施方案中,-r2与-r4和它们连接的碳原子一起形成未取代的或取代的碳环,例如未取代的或取代的碳环。例如,环可以是环戊烯或环己烯环,例如未取代或取代的环己烯环。该环可以任选地包括杂原子。
在一个实施方案中,-r2是酰氨基,例如当-r1是酰氧基时。
在一个实施方案中,当-r1是酰基、酰氧基或酰基氨基时,-r1和-r2可以形成含有酰基、酰氧基或酰基氨基的环。在该实施方案中,碳-碳双键是在环外的。该环可以具有4-7个环原子,例如5或6个环原子。当-r1是酰氧基时,一个环原子是氧原子,并且当-r1是酰基氨基时,一个环原子是氮原子。
在一个实施方案中,-r1和-r2与它们连接的碳原子(α碳)一起形成环戊烯酮或环己烯酮环。这里,-r1是酰基。
当-r1和-r2形成环时,该环任选被取代。
在一个实施方案中,-r3选自氢,和未取代或取代的烷基、环烷基、烯基和炔基。
在一个实施方案中,-r3是氢。
在一个实施方案中,-r3选自未取代或取代的烷基、环烷基、烯基和炔基。
在一个实施方案中,-r3选自未取代或取代的烷基。
在一个实施方案中,当-r1是酰基、酰氧基或酰基氨基时,-r3和-r1形成含有酰基、酰氧基或酰基氨基的未取代或取代的环。该环可以具有4-7个环原子,例如5或6个环原子。例如,该环可以是环戊烯酮或环己烯酮环。
该环可以任选地包括杂原子。该环可以被提供为具有环碳原子上的氧代(=o)取代基。氧代取代的碳环原子可以与酰基氨基连接以形成环状酰亚胺(-c(o)-nr-c(o)-)。例如在sye-4酶的存在下这样的结构被显示为活性底物(例如参见iqbal等人)。
在一个实施方案中,当-r1包含酰基时,-r3和-r1形成未取代或取代的环。
当烯基或炔基存在于-r2、-r3和-r4中的任一个中时,其优选不与位于基团-r1的α、β位的不饱和键共轭。
在一个实施方案中,-r4选自氢和未取代或取代的烷基、环烷基、烯基和炔基。在一个实施方案中,-r4是氢。
在一个实施方案中,-r2、-r3和-r4之一不是氢。
在一个实施方案中,-r2、-r3和-r4之一是氢。例如,-r2是氢或-r3是氢。
在一个实施方案中,r3和-r4是氢。
在一个实施方案中,底物不是12-氧代-顺式-10,15-植物二烯酸酯(phytodienoate)。
本发明人已经发现ene-103对底物3-甲基-2-环戊烯酮和3-甲基-2-环己烯酮具有小的活性。然而,这种小活性被认为与这些特定的底物相关,并且ene-103表现出与其它结构相关的底物的催化剂活性,如本案的工作实施例所显示的。
在一个实施方案中,底物不是3-甲基-2-环戊烯酮或3-甲基-2-环己烯酮,例如当催化剂是包含与seqidno:9具有至少70%同一性的氨基酸序列的多肽时,例如其中多肽包含seqidno:9的氨基酸序列。
在一个实施方案中,-r4是氢。在一个实施方案中,-r2独立地选自烷基,烯基,炔基,环烷基,杂环基,芳基,氨基,羟基和氧基。
这些实施方案可应用于其中-r1是酰基,且-r1和-r3一起形成含有酰基的环,例如环戊烯酮环时。
在一个实施方案中,底物不含腈(-cn)基团。例如,-r1、-r3和-r4中的每一个不是腈。因此,基团-r1可以独立地选自酰基、羧基、酰氧基、硝基和酰基氨基。基团-r3可独立地选自氢、烷基、烯基、炔基、环烷基、杂环基、芳基、氨基、羟基、氧基、羧基、酰氧基和酰基氨基。基团-r4可以是独立选择的氢、烷基、烯基、炔基、环烷基、杂环基、芳基、氨基、羟基、氧基、羧基、酰氧基和酰基氨基。
烷基可以指直链或支链的c1-20饱和烷基。烷基可以是c1-4、c1-6或c1-10烷基。烷基的实例包括甲基,乙基,丙基和1-甲基乙基(异丙基)。
烯基可以指直链或支链的c2-20烯基。烯基可以是c2-4、c2-6或c2-10烯基。烯基的实例包括乙烯基和丙烯基。当烯基被提供为具有取代基时,该基团的乙烯可以被提供在取代基的α、β位。烯基可以具有一个或多个不饱和键。
炔基可以指直链或支链的c2-20炔基。炔基可以是c2-4、c2-6或c2-10炔基。炔基的实例包括乙炔基和丙炔基。炔基可以具有一个或多个不饱和键。
环烷基可以指c6-10环烷基。烷基的实例包括环己基和环戊基。
在一个实施方案中,环烷基是任选不饱和的。
环烷基可以是稠环体系的一部分。在稠环体系中,环烷基具有包含两个或更多个稠环的环体系,其中稠环体系的一个环可以是芳族环(包括杂芳族环),并且该基团通过非芳族环原子(即作为环体系的一部分的非芳族环的一部分的环原子)连接到分子的其余部分。因此,稠环体系通过环烷基环的环原子连接。稠合体系的实例包括四氢萘基和茚满基。稠环体系可以任选在任何可用的环原子上被取代。
杂环基可以指c5-10杂环基。杂环基可以是c5-7、c5-6或c6杂环基。杂环基含有一个或多个,例如一个或两个选自n、o和s的杂原子。杂环基可以通过环碳原子或环氮原子连接(如果存在的话)。氮环原子可以是基团nh,或者氮环原子可以是取代的。硫环原子可以是基团-s-,-s(o)-或-s(o)2-。
杂环基的实例包括四氢呋喃,四氢噻吩,吡咯烷,1,4-二恶烷,吗啉,硫代吗啉,哌嗪,哌啶和1,4-二氮杂卓(diazepine)。
杂环基可以是稠环体系的一部分。在稠合体系中,杂环基具有包含两个或更多个稠环的环体系,其中稠环体系的一个环可以是芳族环(包括杂芳族环),并且基团通过非芳族环原子(即作为环体系的一部分的非芳族环的一部分的环原子)连接至分子的其余部分。因此,稠环体系通过杂环基环的环原子连接。实例包括二氢吲哚基,吲哚基,二氢苯并呋喃基,苯并二氢吡喃基和2,3-二氢-1,4-苯并二氧杂环己烯基(benzodioxinyl)。稠环体系可以任选在任何可用的环原子上被取代。
芳基可以指c5-14碳芳基(carboaryl)或杂芳基。
碳芳基可以是c6-14或c6-10碳芳基。
碳芳基的实例包括苯基和萘基。
碳芳基可以是稠环体系的一部分。在稠环体系中,碳芳基具有包含两个或更多个稠环的环体系,其中稠环体系的至少一个环是芳族环(包括杂芳族环),并且该基团通过芳族环原子(即,作为环体系的一部分的芳族环的一部分的环原子)连接到分子的其余部分。因此,稠环体系通过芳族环的环原子连接。实例包括萘基,二氢吲哚基,吲哚基和二氢苯并呋喃基,苯并二氢吡喃基和2,3-二氢-1,4-苯并二氧杂环己烯基。稠环体系可以任选在任何可用的环原子上被取代。
杂芳基可以是c5-14、c5-10或c5-6杂芳基。
杂芳基的实例包括呋喃基,吡咯基,咪唑基,恶唑基,噻唑基,吡啶酮基,吡嗪基,喹啉基和异喹啉基。
杂芳基可以是稠环体系的一部分。在稠环体系中,杂芳基具有包含两个或更多个稠环的环体系,其中稠环体系的至少一个环是杂芳族环,并且该基团通过杂芳族环中的环原子(即,作为环体系的一部分的芳族环的一部分的环原子)连接到分子的其余部分。因此,稠环体系通过芳族环的环原子连接。杂芳基可以通过环碳原子或环氮原子连接(如果存在的话)。实例包括吲哚基,苯并呋喃基,异苯并呋喃基,苯并恶唑基,嘌呤基,喹啉基和异喹啉基。
烷基、烯基、炔基环烷基、杂环基和芳基任选被取代。基团可以是单-、二-或三-取代的。
当基团被称为被取代时,其可以被独立地选自卤素、羟基(-oh)、硝基(-no2)、烷基、烯基、炔基、环烷基、杂环基、芳基、氧基、硫基、氨基、酰基、羧基、酰氧基、氧酰基、酰氨基和酰基氨基的取代基取代。这些基团将在下文讨论。
当氮环原子存在于杂环基中时,环原子可以是未取代的(nh)或任选地被烷基、烯基、炔基环烷基、杂环基、芳基、酰基和酰氧基取代,例如本文所述的。
卤素、羟基(-oh)、硝基(-no2)、烷基、烯基、炔基、环烷基、杂环基、芳基、氧基、硫基、氨基、酰基、羧基、酰氧基、氧酰基、酰氨基和酰基氨基可以是如下文所描述的基团。
酰基是基团-c(o)h或-c(o)r,其中r选自取代或未取代的烷基、烯基、炔基、环烷基、杂环基和芳基。
在一个实施方案中,酰基是-c(o)r。
当酰基是氮环原子的取代基时,酰基与氮环原子一起形成酰氨基。
在一个实施方案中,当-r1是酰基时,-r选自取代或未取代的烷基。
在一个实施方案中,其中-r1是酰基,该基团可以是与基团-r3一起形成的环的一部分。例如,-r1和-r3与它们所连接的碳原子一起可以形成环己-2-烯-1-酮或环戊-2-烯-1-酮环。
羧基是c(o)oh或该基团的羧酸盐形式。
酰氧基是基团-c(o)or,其中-r选自取代或未取代的烷基、烯基、炔基、环烷基、杂环基和/或芳基。
当酰基是氮环原子的取代基时,酰氧基与氮环原子一起形成氨基甲酸酯基。
基团-r1可以是酰氧基。在一个实施方案中,-r可以与-r3一起形成环。在一个实施方案中,-r6和-r3以及它们所连接的原子形成未取代或取代的环,其中该环具有4-8个,例如5-7个环原子。该环可以是例如环己烯或环戊烯环。该环任选被取代。
在一个实施方案中,当-r1是酰氧基时,-r选自取代或未取代的烷基。
卤素基团独立地选自-f、-cl、-i和-br。
氧基是基团-or,其中r独立地选自烷基,烯基,炔基,环烷基,杂环基和芳基。
硫基是基团-sh或sr,其中r独立地选自烷基,烯基,炔基,环烷基,杂环基和芳基。
氨基是选自-nh2,-nhr和-n(r)2的基团,其中每个r独立地选自烷基,烯基,炔基,环烷基,杂环基和芳基,例如烷基、环烷基和芳基。
氧酰基是基团-oc(o)r,其中-r独立地选自取代或未取代的烷基,烯基,炔基,环烷基,杂环基和芳基。
酰氨基是基团-nhc(o)r,-nrc(o)r,其中-r独立地选自取代或未取代的烷基,烯基,炔基,环烷基,杂环基和芳基,例如取代或未取代的烷基。
酰基氨基是基团-c(o)nh2,-c(o)nhr或-c(o)n(r)2,其中r独立地选自取代或未取代的烷基,烯基,炔基,环烷基,杂环基和芳基,或两个r基团可以与它们所连接的氮原子一起形成取代或未取代的氮杂环,任选地含有一个另外的环杂原子。杂环任选被烷基,烯基,炔基,环烷基,杂环基和芳基取代。
上文描述的是基团-r,其选自取代或未取代的烷基,烯基,炔基,环烷基,杂环基和芳基。
在一个实施方案中,当存在时,-r选自取代或未取代的烷基,烯基,炔基和环烷基。
在一个实施方案中,当存在时,-r选自取代或未取代的烷基和环烷基,例如烷基。
在一个实施方案中,当存在时,-r选自取代或未取代的烷基,烯基和芳基。
在一个实施方案中,当存在时,-r是取代或未取代的芳基。
烷基、烯基或炔基不被烷基、烯基或炔基取代。
每个取代基可以任选进一步被取代。
在一个实施方案中,-r3和-r4不相同。在一个实施方案中,-r2、-r3和-r4不相同。
在一个实施方案中,-r2、-r3和-r4不含位于活化基团的α、β位(例如酰基、羧基、酰氧基或硝基的α、β位)的乙烯基。这里,底物仅具有一个活化的乙烯基,并且是位于-r1的α、β位的乙烯基。
在一个实施方案中,底物是分子量为至多500,至多750,或至多1,000的化合物。
在一个实施方案中,底物是非手性的。
共底物
在本发明的方法中,底物可与共底物一起反应以产生产物。在还原反应中,共底物可以被认为是还原剂。还原剂可以形式上提供用于还原的氢。还原剂通常是辅因子。
辅因子
催化剂可以使用nad(p)h作为辅因子以提供还原反应的还原当量(reducingequivalent)。例如,在催化不饱和碳-碳双键的还原时,催化剂可以使用来自nad(p)h的还原等价物,从而将其氧化成nad(p)+。还原的辅因子与氧化的辅因子的比率,例如nad(p)h与nad(p)+的比率应当相对较高,以便有利于辅因子氧化和伴随的底物还原。
辅因子也被称为辅酶,也可称为共底物。术语“nad(p)h”用于表示nadh和/或nadph,并且术语和“nad(p)+”用于表示nad+和/或nadp+。例如,使用“nad(p)h”作为辅因子的催化剂可以使用nadh作为辅因子,并且可以额外地或可选择地使用nadph作为辅因子。
在体外反应中,还原的辅因子可以以化学计量的量与底物一起存在。或者,还原的辅因子可以以显著小于化学计量的量与底物存在。可以使用还原辅因子再生系统再生还原的辅因子,所述系统还原在反应期间氧化的辅因子,从而允许辅因子以显著小于化学计量的量与底物存在。还原辅因子再生系统是本领域已知的。这样的系统可以包含还原剂,任选地连同能够将还原当量从还原剂转移到氧化的辅因子的酶。还原剂包括糖,特别是己糖如葡萄糖、甘露糖、果糖,还原剂还包括可氧化的醇如乙醇、丙醇和异丙醇,还原剂还包括甲酸盐、亚磷酸盐和分子氢。这样的系统可以包含糖作为还原剂,任选地具有相容的糖脱氢酶以催化还原当量从糖至氧化的辅因子的转移。对于nadh作为辅因子,还原辅因子再生系统可以包括葡萄糖和葡萄糖脱氢酶(gdh),如方案1所示。对于nadh作为辅因子,还原辅因子再生系统可以包含甲酸盐和甲酸脱氢酶。对于nadph作为辅因子,辅因子再生系统可以包括葡萄糖-6-磷酸盐和葡萄糖-6-磷酸酶。
在体内反应中,当在细胞中提供催化剂时,还原的nad(p)h通过细胞内酶再生。这样的酶可以是内源的或重组的。例如,参与糖酵解的细胞内酶如磷酸甘油醛脱氢酶可将nad+还原为nadh。
催化剂可以是黄素依赖性酶。也就是说,催化剂可以接受来自辅因子的还原当量,以通过黄素单核苷酸(fmn)辅基还原不饱和碳-碳双键。
立体选择性反应
本发明的催化剂可用于产生其中产物中的一个或多个例如两个碳原子具有特定立体化学的产物。因此,本发明的催化剂可有利地用于制备手性化合物。
本发明的催化剂可用于产生具有70%或更高,80%或更高,95%或更高,99%或更高的ee值的产物。
因此,本发明的催化剂可用于制备主要含有一种立体异构体和少量另一种立体异构体如对映异构体的产物。
本发明的催化剂可以与非手性的底物一起使用。因此,底物可以不具有拥有立体中心的原子。本文所述的方法允许在产物中产生一个或两个立体中心。因此,本发明的催化剂可用于从非手性原料赋予手性。
应注意,本文所述的反应方法不限于立体选择性合成方法。如工作实施例所示,本发明的催化剂可用于产生高产率的还原底物。在有或没有高产率的产物的情况下,可发生底物的立体选择性还原。
当底物含有乙烯键时,使用催化剂的该键的还原应理解为在键的相对面(反)上发生氢的形式添加。在式(i)的化合物中,显示了乙烯键,其中基团-r1位于右下方。如图所示,在催化剂的存在下该键的还原可以发生为在与-r3和-r4键合的碳的顶面(纸平面上方)加入氢原子,和在与-r1和-r2键合的碳的底面(在纸平面下方)加入氢原子。
因此,在一个实施方案中,式(i)化合物的还原如此发生:
产物中对映异构体的量或对映异构体的比率可以通过标准光谱技术测定,例如使用手性固定相的hplc。如本文所述,还原反应产物的ee值通过产物混合物的gc分析测定。
本发明人已经发现,当-r3和-r4所连接的碳原子是前手性碳原子(在还原时成为手性碳原子的碳原子)时,可以获得高对映体过量。相反,当-r1和-r2连接的碳原子(α碳)是前手性原子时,在一些情况下不能获得高对映体过量。这被认为是由于在还原后与α碳连接的氢原子的较高的相对不稳定性,这可能在α碳是手性碳原子时导致外消旋化反应(例如当-r1是酰基时通过烯醇化物形式)。因此,当需要高对映体过量时,可优选与-r3和-r4连接的碳原子是前手性碳原子。优选的是,-r1和-r2所连接的碳原子不是前手性碳原子。
特别地,本发明人已经发现,对于其中-r2是氢并且-r3和-r4各自不是氢并且不相同的那些化合物,可以获得高对映体过量。这里,-r3和-r4所连接的碳可以被认为是前手性中心,因为其在还原时将变成手性碳原子。相比之下,-r1的α碳在还原时不会产生四元立体中心,因为反应将导致该碳原子带有两个氢原子。
技术人员将容易地理解本文所用的术语手性碳原子。它包括具有与其连接的四个不同基团的碳原子,其中一个可以是氢原子。
试剂盒
在一个方面,本发明在试剂盒中提供本发明的催化剂。
试剂盒可以包含一种或多种另外的催化剂。另外的催化剂可以用于还原反应,例如本文所述的乙烯基的还原。
另外或可选地,另外的催化剂可以用于不是还原反应或不是乙烯基的还原的反应中。
在一个实施方案中,另外的催化剂是生物催化剂。因此,每种催化剂具有酶活性。
催化剂可以与试剂盒的其它催化剂或其它组分在空间上分离。因此,可以在孔板的孔中,或在单独的小瓶或其它容器中提供催化剂。
本发明的试剂盒可以是具有还原催化剂以及一种或多种其它催化剂的试剂盒,其中还原催化剂是包含与seqidno:1具有至少70%同一性的氨基酸序列的多肽。其可以是具有还原催化剂以及一种或多种其它催化剂的试剂盒,其中所述还原催化剂是包含与seqidno:7具有至少70%同一性的氨基酸序列的多肽。其可以是具有还原催化剂和一种或多种其它催化剂的试剂盒,其中所述还原催化剂是包含与seqidno:9具有至少70%同一性的氨基酸序列的多肽。
试剂盒可以提供有使用试剂盒的说明书。任选地,试剂盒可以提供与催化剂一起使用的另外的试剂。例如,可以提供辅因子,缓冲液,溶剂等。可以以浓缩形式提供缓冲液,用于随后的再水化。
其它催化剂之一或全部可以是酶催化剂。
在一个实施方案中,试剂盒还包含一种或多种具有选自转移酶活性,水解酶活性,裂解酶活性,异构酶活性和连接酶活性的活性的催化剂。
在一个实施方案中,试剂盒还包含一种或多种具有选自以下的活性的催化剂:脂肪酶活性,酯酶活性,酰胺酶活性(包括肽酶活性),糖苷酶活性,乙二醇转移酶活性,环氧酶活性,腈水解酶活性(包括腈水合酶活性),羟化活性,脱氢酶活性(包括醇脱氢酶活性),二羟基化活性,baeyer-villiger氧化活性,醛缩酶活性,氧腈酶活性,氨基转移酶活性和辅因子再生活性。
另外或可选地,试剂盒包含具有作为烯还原酶活性的活性的催化剂。
在一个实施方案中,试剂盒被提供为具有用于试剂盒中的一种或每种催化剂的底物。可以提供底物作为参考底物,例如以确定试剂盒内的催化剂的活性。
在一个实施方案中,试剂盒提供使用每种催化剂的说明书。
其它实施方案
上面描述的实施方案的每一个相容组合在本文中被明确地公开,如同每一个组合被单独地和明确地记载。
考虑到本公开内容,本发明的各种其它方面和实施方案对于本领域技术人员将是明显的。
“和/或”在本文中被用作两个指定特征或部件中的每一个在具有或不具有另一个的情况下的具体公开。例如,“a和/或b”被认为是(i)a、(ii)b和(iii)a和b中的每一个的具体公开,如同每一个在本文中单独示出。
除非上下文另有规定,否则上述特征的描述和定义不限于本发明的任何特定方面或实施方案,并且同样适用于所描述的所有方面和实施方案。
现在将通过实例并参考上文描述的附图来说明本发明的某些方面和实施方案。
实验
催化剂
使用标准表达技术在大肠杆菌中表达ene-101。将针对ene-101在大肠杆菌中的表达而优化的核酸序列(seqidno:3)克隆到用于iptg诱导型表达的标准表达载体中。
在一些实验中,表达并证实具有一个或多个n端标签的编码ene-101的核酸序列(非密码子优化的)(seqidno:5和seqidno:7)具有催化活性。
通过收获细胞、回收生物质并在缓冲液(0.1m磷酸钾,ph7.0)中重悬浮生物质、裂解悬浮液并除去细胞碎片以提供澄清的细胞裂解物来产生ene-101制剂。在一些实验中,裂解缓冲液含有20μmfmn(黄素单核苷酸)和5mmmgso4。在裂解缓冲液中包含20μmfmn和5mmmgso4导致ene-101活性增加10%。澄清的细胞裂解物首先通过0.5μm和0.2μm孔径的过滤器过滤,然后通过超滤进一步浓缩以提供ene-101制剂。这种ene-101制剂可以直接使用或冻干用于随后的重构和使用。ene-101制剂通常包含约5umg-1的催化剂,通过上述测定法测定,使用1-辛烯-3-酮作为参照底物。
对于活性研究,使用表达seqidno:3的载体制备ene-101制剂。
下面描述了seqidno:1的催化剂的用途。这被称为ene-101。
实验程序1
将50μl冻干的ene-101制剂的水溶液(100mg/ml;每次测试5mg酶)加入到含有900μlph7的水性介质(250mm磷酸钾缓冲液ph7,1.1mmnad+,30mmd-葡萄糖,10u/mlgdh)和50μl的在甲苯中的底物溶液(400mm,底物终浓度20mm)的反应小瓶。将小瓶在35℃下振荡3、6和18小时。加入1mletoac后,将反应小瓶涡旋并离心。通过gc分析有机相的样品以测量转化率和ee。
结果示于表1。
在所使用的具体反应条件下,发现一些实验中的转化率值相对较低。然而,没有观察到副产物,并且未反应的底物是剩余的主要组分。假设底物可以回收并在随后的反应中再使用,则产物的产率可以被认为是相对高的。
表1-实验程序1中底物的反应时间、转化率和ee
a产物峰在gc中的积分(未校正的gc面积)。b观察到反应介质中产物ee的减少;这种减少不是酶促催化的。cee尚未确定。c立体化学是指产物的所分配的立体化学。
3-甲基-2-环戊烯酮(条目1、2和3)和3-甲基-2-环己烯酮(条目4、5和6)的还原被证明是缓慢的,并且在这两种情况下仅获得部分转化。这两种底物的对映体选择性都很好。
另一方面,2-甲基-2-环戊烯酮证明非常有活性并且反应快。注意到,相应的产物2-甲基环戊酮在反应条件下外消旋化。
图1显示表1中列出的四种底物的%转化随反应时间(h.)的变化的变化。
浓度研究
随后在三种不同浓度:50、100和300mm下测试那些被证明对ene-101更具活性的底物。对于这些测试,遵循实验程序1。葡萄糖、ene-101、gdh和nad的量根据底物浓度按比例放大,因此当量数保持恒定。如上述实验程序中所述,将250mm磷酸盐缓冲液(ph7.0)用于反应。没有尝试在反应发生时调节ph。这意味着在高底物浓度下,所产生的葡萄糖酸可能不会被完全中和,因此使得培养基的ph对于ene-101来说过于酸性而无法发挥作用。
结果示于表2。
表2-具有浓度变化的底物的反应时间、转化率和ee
a产物峰在gc中的积分(未校正的gc面积)。b观察到反应介质中产物ee的减少;这种减少不是酶促催化的。cee尚未确定。
图2显示了表1中列出的三种底物的%转化随反应时间(h.)的变化和底物浓度的变化的变化。
对于大多数测试的底物,注意到当反应时间从3小时增加到18小时时,转化率没有显著改善。这在高底物浓度下特别显著,并且表明反应介质的ph对于酶起作用过于酸性,从而导致转化停止。这通过在3小时和18小时后测量反应小瓶的ph来证明。
在所测试的实例中,没有一个显示产物或底物抑制的证据,即使在高达300mm的浓度下。这表明以高达300mm(甚至更高)的浓度运行这些还原应当是可能的,并且理想地与反应介质ph的控制一起。
ph研究
在ph研究中,选择柠檬醛(3,7-二甲基-2,6-辛二烯醛)作为进一步研究的测试底物。然后研究缓冲液的ph的影响,结果示于图3中。
鉴于反应时间短(通常约1分钟),假定反应混合物的ph在整个反应过程中保持基本上恒定。
通过光度测定确定反应性,由nadh的氧化引起的340nm处的吸光度的降低是ene-101的催化活性的量度。测定浓度:在1ml反应混合物中,终浓度为0.1m磷酸钾ph7.4,10mm底物,15mmnadh和0.4mgene-101。
测量每个ph值的背景活性(在不存在底物时nadh吸光度的降低)。发现其对于ph6至6.5和对于ph8至9较高。发现ene-101是稳定的并且在ph6.5至8之间更有活性。
温度特征谱和稳定性
还研究了ene-101的温度特征谱,并测量了每个温度的背景活性,并从酶活性测定值中减去。结果示于图4中。
通过如上关于ph研究所述的光度测定法测定反应性。底物是柠檬醛。
在三种不同的温度(30、40和50℃)下研究ene-101的稳定性。如前所述,测量并除去背景活性。残余活性的结果显示在图5中。同样,通过光度测定法测定反应性,底物是柠檬醛。
图5中的结果表明,ene-101在低于40℃的温度下相当稳定,但在50℃下迅速丧失活性
溶剂和添加剂效应
使用相对反应性的底物2-甲基-2-环戊烯酮研究溶剂和添加剂效应。在实验程序1之后比较5体积%的不同共溶剂。来自该比较的关于产物的产率和ee的结果如图6所示。
如前所述,还原产物2-甲基环戊酮在反应条件下外消旋化。在所测试的共溶剂中,它们似乎都不以显著的程度改善转化或防止外消旋作用。
在相同的条件下,评价对反应混合物的表面活性剂添加效应(0.1和0.3体积%)。结果示于图7中。
在指定体积下测试的共溶剂中,它们似乎都不以显著程度改善转化或防止外消旋化。
按比例放大实验
随后进行更大规模的催化反应以显示催化剂在工业上有用的水平上的效用。
按比例放大反应观察还原反应,如以下方案1所示。
方案1
程序1-试剂和方法
在温度控制(40℃)并配备有ph控制计量泵的磁力搅拌(600rpm,蛋形搅拌棒)50ml圆底烧瓶中引入去离子水(36.3ml)、k2hpo4(597mg)和kh2po4(27mg)。这产生0.1mph8.0的磷酸盐缓冲溶液。然后加入d-葡萄糖一水合物(8.2g),使溶液的ph降至7.1。温度稳定后,加入nacl(1.68g),然后加入ene-101(1.0g),gdh(103mg;4.88u/mg;500u),nad(166mg)和1-乙酰基环己烯(4.67g;37.6mmol)。
将反应在40℃下搅拌,直到通过gc分析观察到完全转化。为了保持恒定的ph7.0,将反应用45%naoh溶液计量加入。
为了监测转化,以规律的间隔从反应中取出样品(50μl)。将它们用dcm(1.5ml)处理,涡旋、离心以除去不溶物质,并通过gc分析以测量转化。20小时后,通过gc观察到99.3%转化为产物。反应特征谱可见于图8和9。
程序2-试剂和方法
按照与上述相同的程序,在双倍底物浓度下重复反应。在这种情况下,将d-葡萄糖一水合物(15.4g;77.7mmol)、氯化钠(1.68g)、nad(316mg;0.47mmol)、gdh(103mg;4.88u/mg;500u)和ene-101(1.0g)在ph8.0的0.1m磷酸盐缓冲液(24.8ml)中的溶液在40℃下置于磁力搅拌的圆底烧瓶中,然后用1-乙酰基环己烯(9.34g;75.2mmol)处理。将反应在40℃下搅拌96小时。为了保持恒定的ph7.0,将反应用45%naoh溶液计量加入。
以规律的间隔从反应中取出样品(25μl)以监测转化。将它们用dcm(1.5ml)处理,涡旋、离心以除去不溶物质,并通过gc分析以测量转化。26小时后,通过gc观察到75%转化为产物(1.125m产物浓度)。反应减慢并在95%转化率下停止。反应的特征谱可以在图8和9中找到。
观察还原的进一步按比例放大反应如下面方案2所示。
方案2
程序3-试剂和方法
在温度控制(40℃)且配备有ph控制计量泵的磁力搅拌(600rpm,蛋形搅拌棒)50ml圆底烧瓶中引入去离子水(36.8ml)、k2hpo4(597mg)和kh2po4(27mg)。这产生0.1mph8.0的磷酸盐缓冲溶液。然后加入d-葡萄糖一水合物(8.2g),使溶液的ph降至7.1。温度稳定后,加入nacl(1.68g),然后加入ene-101(1.0g)、gdh(103mg;4.88u/mg;500u)、nad(166mg)和衣康酸二甲酯(5.9g;37.3mmol)。将反应在40℃下搅拌,直到通过gc分析观察到完全转化。为了保持恒定的ph7.0,将反应用45%naoh溶液计量加入。
为了监测转化,以规律的间隔从反应中取出样品(50μl)。将它们用dcm(1.5ml)处理,涡旋、离心以除去不溶物质,并通过gc分析以测量转化。43小时后,通过gc观察到99%转化为产物(>99.9%ee,r对映异构体)。反应特征谱可见于图10和11。
进一步的实验数据
催化剂
ene-102和ene-103被产生为具有标签(例如,具有n末端t7和his标签)或没有标签。
ene-102和ene-103以与上述ene-101类似的方式制备。ene-102和ene-103制剂通常包含使用nadph作为辅因子的约1-2umg-1的催化剂制剂,如通过上述测定一般描述的,使用1-辛烯-3-酮作为参照底物。
这些进一步的实验数据包括上面已经给出的数据,以便于比较。
为了定义酶ene-101、ene-102和ene-103的底物范围,针对许多底物(活化的c=c键)测试它们。反应在相同条件下进行(如“实验程序2”中所述);在3、6和18小时后取样,并通过gc分析以测量转化率和对映体过量。这些反应的结果描述在表3中。
实验程序2:将冻干酶ene-101、ene-102或ene-103制剂的50μl水溶液(100mg/ml;每次测试5mg酶)加入到含有900μlph7的水性介质(250mm磷酸钾缓冲液ph7,1.1mmnad+,30mmd-葡萄糖,10u/mlgdh)和50μl的在甲苯中的底物溶液(400mm,底物终浓度20mm)的反应小瓶。将小瓶在35℃下振荡3、,6和18小时。加入1mletoac后,将反应小瓶涡旋并离心。通过gc分析有机相的样品以测量转化率和ee。
表3
a产物峰在gc中的积分(未校正的gc面积)。b观察到反应介质中产物ee的减少;这种减少不是酶促催化的。cee尚未确定。
3-甲基-2-环戊烯酮和3-甲基-2-环己烯酮的还原被证明是缓慢的,并且使用ene-101和ene-102仅获得部分转化。然而,对于两种底物的对映选择性都是优良的。ene-103对这些底物明显无活性(数据未显示)。这似乎是一个孤立的无活性事件,因为观察到ene-103对结构相关的形式(例如2-甲基-2-环戊烯酮和1-(环己烯-1-基)乙酮(表3中的条目16和17))具有活性。
2-甲基-2-环戊烯酮被三种酶快速还原。不幸的是,相应的产物2-甲基环戊酮在反应条件下外消旋化。
据报道,α-取代的烯酮比β-取代的烯酮更容易被老黄酶还原。例如,参见关于希瓦氏菌属(shewanella)oye(sye-4)(iqbal等人,2012)、来自运动发酵单胞菌(zymomonasmobilis)的烯酸还原酶(enoatereductase)和来自乳酸克鲁维酵母(kluyveromyceslactis)(kye1)和来自伯氏耶尔森氏菌(yersiniabercovieri)(yers-er)的oye的还原的报告(yanto等人,2011;hall等人,2008)。
图12显示了表3中报告的数据。
随后在三种不同浓度:50、100和300mm下测试证明更容易还原的那些底物。对于这些测试,遵循实验程序2。葡萄糖、ene、gdh和nad的量根据底物浓度增加,因此当量数保持恒定。如实验程序中所述,将250mm磷酸盐缓冲液(ph7.0)用于反应。没有尝试在反应发生时调节ph。这意味着在高底物浓度下,所产生的葡萄糖酸可能不会被完全中和,以使得培养基的ph对于ene来说过于酸性而无法发挥作用。
这些测试的结果可以在表4和图13a和13b中找到。
表4
a产物峰在gc中的积分(未校正的gc面积)。b观察到反应介质中产物ee的减少;这种减少不是酶促催化的。cee尚未确定。
对于大多数测试的底物,在3至18小时的反应时间时,转化率没有显著改善。这在高底物浓度下特别显著,并且表明反应介质的ph对于酶起作用过于酸性,从而导致转化停止。这通过在3小时和18小时后测量反应小瓶的ph来证明。
在任何实验中没有发现产物或底物抑制的证据,即使在高达300mm的浓度下。这表明,以高达300mm或高于300mm的浓度运行这些还原是可能的。调节反应介质的ph可以进一步改善使用高底物浓度的反应。
按比例放大实验
1-乙酰基环己烯的还原
方案3.反应方案。
程序a.1(0.75m)
在温度控制(40℃)并配备有ph控制计量泵的磁力搅拌(600rpm,蛋形搅拌棒)50ml圆底烧瓶中引入去离子水(36.3ml)、k2hpo4(597mg)和kh2po4(27mg)。这产生0.1mph8.0的磷酸盐缓冲溶液。然后加入d-葡萄糖一水合物(8.2g),使溶液的ph降至7.1。温度稳定后,加入nacl(1.68g),然后加入ene(-101、-102或-103,1.0g),gdh(103mg;4.88u/mg;500u),nad(166mg)和1-乙酰基环己烯(4.67g;37.6mmol)。
将反应在40℃下搅拌,直到通过gc分析观察到完全转化。为了保持恒定的ph7.0,将反应用45%naoh溶液计量加入。
对于在750mm下获得的ene-102不完全转化(即使在延长的时间后),以300mm重复该反应,导致过夜完全转化。对于ene-101,在双倍浓度1500mm下重复反应。
程序a.2(1.5m)
按照与上述相同的程序,在双倍底物浓度下重复反应。在这种情况下,将d-葡萄糖一水合物(15.4g;77.7mmol)、氯化钠(1.68g)、nad(316mg;0.47mmol)、gdh(103mg;4.88u/mg;500u)和ene-101(1.0g)在ph8.0的0.1m磷酸盐缓冲液(24.8ml)中的溶液在40℃下置于磁力搅拌的圆底烧瓶中,然后用1-乙酰基环己烯(9.34g;75.2mmol)处理。将反应在40℃下搅拌96小时。为了保持恒定的ph7.0,将反应用45%naoh溶液计量加入。
为了监测转化,以规律的间隔从不同的反应中取出样品(50μl)。将它们用dcm(1.5ml)处理,涡旋、离心以除去不溶物质,并通过gc分析以测量转化。不同反应的特征谱可以在图14和15中看到。
衣康酸二甲酯的还原
方案4.反应方案。
程序b.1(0.73m)
在温度控制(40℃)且配备有ph控制计量泵的磁力搅拌(600rpm,蛋形搅拌棒)50ml圆底烧瓶中引入去离子水(36.8ml)、k2hpo4(597mg)和kh2po4(27mg)。这产生0.1mph8.0的磷酸盐缓冲溶液。然后加入d-葡萄糖一水合物(8.2g),使溶液的ph降至7.1。温度稳定后,加入nacl(1.68g),然后加入ene(-101、-102或-103,1.0g),gdh(103mg;4.88u/mg;500u),nad(166mg)和衣康酸二甲酯(5.9g;37.3mmol)。
将反应在40℃下搅拌,直到通过gc分析观察到完全转化。为了保持恒定的ph7.0,将反应用45%naoh溶液计量加入。
为了监测转化,以规律的间隔从反应中取出样品(50μl)。将它们用dcm(1.5ml)处理,涡旋、离心以除去不溶物质,并通过gc分析以测量转化。对于三种酶,通过gc观察到超过95%转化为产物(>99.9%ee,r对映异构体)。反应特征谱可见于图16和17。
参考文献
上文引用了许多出版物以便更充分地描述和公开本发明以及本发明所属领域的现状。这些参考文献的完整引用如下。这些参考文献中的每一个的全部内容并入本文。
对于标准分子生物学和蛋白质表达和分离技术,参见:
sambrook,j.,russel,d.w.molecularcloning,alaboratorymanual.3ed.2001,coldspringharbor,newyork:coldspringharborlaboratorypress
altschul等人(1990)j.mol.biol.215:405-410)
brenna等人(2012)chemcatchem.4:653-659
hall等人(2008)eur.j.org.chem.1511
hirata等人(2009)journalofmolecularcatalysisb:enzymatic.59:158-162.
iqbal等人(2012)tetrahedron.68:7619-7623
lalondeandmargolin(2002)“immobilizationofenzmes”indrauzk.andwaidmannh.,enzymecatalysisinorganicsynthesis,vo.iii,991-1032,wiley-vch,weinheim.
lucass等人,西瓜嗜酸菌亚种avenaeatcc19860的完整序列。递交(feb-2011)至embl/genbank/ddbj数据库。菌株:atcc19860/dsm7227/jcm20985/ncppb1011。
us2010/0035315
needlemanandwunschj.mol.biol.48:444-453(1970)
mangan等人(2012)advsynthcatal.354:2185-2190
mansell等人(2013)catalysis.3:370-379
pearsonandlipman(1988)pnasusa85:2444-2448
peitruszkaj.andscholzelm.,(2012)adv.synth.catal.,354:751-756
smithandwaterman(1981)j.molbiol.147:195-197
winkler等人(2013)thejournaloforganicchemistry.78:1525-1533
yanto等人(2011),org.lett.13:2540
序列表
<110>johnsonmattheyplc
<120>催化剂及其用途
<130>70241/njw
<150>gb1413899.4
<151>2014-08-06
<160>10
<170>patentinversion3.3
<210>1
<211>376
<212>prt
<213>西瓜嗜酸菌
<400>1
metserhisthrleupheaspprovalglnalaglyaspleuglnleu
151015
alaasnargilealametalaproleuthrargasnargserproasn
202530
alavalprolysaspilethralathrtyrtyralaglnargalathr
354045
alaglyleuleuilethrglualathralaileserhisglnglygln
505560
glytyralaaspvalproglyleutyrserthrgluglnleuaspgly
65707580
trplyslysvalthralaalavalhisgluargglyglyargileval
859095
thrglnleutrphisvalglyargileserhisasnaspleuglnpro
100105110
aspglyglyalaprovalalaproseralailealaalalysserlys
115120125
thrtyrleuileasplysalathrglyglnglyhisphealaalathr
130135140
sergluproargalaleuaspalaglugluleuproglyilevalhis
145150155160
asptyralaalaalaalaargasnalavalgluthralaglypheasp
165170175
glyvalgluilehisglyalaasnglytyrleuleuaspglnpheleu
180185190
lysthrglyalaasnargargthraspasptyrglyglyserileglu
195200205
asnargalaargleuleuleuglualathrargalavalvalaspala
210215220
ileglyglyglylysvalglyileargleuserprovalthrproala
225230235240
asnaspilevalaspalaaspproglnproleupheasptyrvalile
245250255
argglnleualaproleuglyleualatyrvalhisvalileglugly
260265270
serthrglyglyproarggluleugluaspargpropheasptyrglu
275280285
alaleulysthralatyrargglualaglyglylysglyalatrpmet
290295300
valasnasnalatyraspargalaleualametglualavalalaser
305310315320
glyargalaaspilevalalapheglylysalapheileserasnpro
325330335
aspleuvalgluargleuargglnaspalaproleuasnprotrpasp
340345350
serlysthrphetyrglyglyglyglulysglytyrthrasptyrpro
355360365
thrleuglygluseralalysgly
370375
<210>2
<211>1131
<212>dna
<213>西瓜嗜酸菌
<400>2
ttgtcccatacgcttttcgatcccgtccaggccggcgacctgcagctcgccaaccgcatc60
gccatggcgccgctcacgcgcaaccgctcgccgaatgcggtgcccaaggacattaccgcc120
acctactacgcccagcgcgccaccgccggcctgctgatcaccgaggccacggccatcagc180
caccagggccagggctatgcggacgtgccgggcctgtacagcaccgaacagctcgatgga240
tggaaaaaggtcaccgcagcggtccatgagcgcggcggcaggatcgtgacccagctctgg300
cacgtgggccgcatttcccacaatgacctgcagcccgacggcggcgcccccgtggccccc360
tccgccatcgccgccaagtccaagacctacctgatcgacaaggccaccggccagggccat420
ttcgcggccacgtccgaaccccgtgcgctggatgccgaagagctgcccggcatcgtgcac480
gactacgccgccgccgcgcgcaacgcggtggagacggccggattcgacggcgtcgagatc540
cacggcgccaacggctacctgctggaccagttcctcaagaccggcgccaaccggcgcacc600
gacgactacggcggcagcatcgagaaccgcgcgcgcctgctgctcgaagccacgcgcgcc660
gtggtggacgcgatcggcggcggcaaggtgggcatccgactctcgcccgtcacgccggcc720
aacgacatcgtcgatgccgatccgcagccgctgttcgactacgtgatccgccagctcgca780
ccgctgggcctggcctacgtgcacgtgatcgaaggctccaccggcggcccgcgcgagctg840
gaagaccgtccgttcgactacgaagccctgaagaccgcctaccgcgaggccggcggcaaa900
ggcgcctggatggtcaacaacgcctatgaccgtgcgttggcgatggaagcggtggccagt960
ggccgcgccgacatcgtcgccttcggcaaggccttcatctccaaccccgacctggtcgag1020
cggctgcgccaggacgcaccgctcaacccctgggactccaagaccttctacggcggcggc1080
gagaagggctacaccgactacccgacgctcggcgaatcggcgaaaggctga1131
<210>3
<211>1134
<212>dna
<213>人工序列
<220>
<223>合成序列:密码子优化的编码催化剂的核酸序列(编码seqidno:1)
<400>3
atgagccataccctgtttgatccggttcaggcaggcgatctgcagctggcaaatcgtatt60
gcaatggcaccgctgacccgtaatcgtagcccgaatgcagttccgaaagatattaccgca120
acctattatgcacagcgtgcaaccgcaggtctgctgattaccgaagcaaccgcaattagc180
catcagggtcagggttatgcagatgttccgggtctgtatagcaccgaacagctggatggt240
tggaaaaaagttaccgcagcagtgcatgaacgtggtggtcgtattgttacccagctgtgg300
catgtgggtcgtattagccataatgatctgcaaccggatggtggtgctccggtggcaccg360
agcgcaattgcagcaaaaagcaaaacctatctgattgataaagcaaccggtcagggtcat420
tttgcagcaaccagcgaaccgcgtgcactggatgcagaagaactgcctggtattgttcat480
gattatgcagcagcagcacgtaatgcagttgaaaccgcaggctttgatggtgttgaaatt540
catggtgcaaatggctatctgctggatcagtttctgaaaaccggtgcaaatcgtcgtacc600
gatgattatggtggtagcattgaaaatcgtgcccgtctgctgctggaagcaacccgtgca660
gttgttgatgcaattggtggtggtaaagttggtattcgtctgagtccggttacaccggca720
aatgatattgtggatgccgatccgcagccgctgtttgattatgttattcgtcagctggct780
ccgctgggtctggcctatgttcatgttattgaaggtagcaccggtggtcctcgtgaactg840
gaagatcgtccgttcgattatgaagcactgaaaacagcatatcgtgaagcaggcggtaaa900
ggtgcatggatggttaataatgcctatgatcgtgccctggcaatggaagcagttgcaagc960
ggtcgtgcagatattgttgcatttggtaaagcctttattagcaatccggatctggttgaa1020
cgtctgcgtcaggatgctccgctgaatccgtgggatagtaaaaccttttatggtggcggt1080
gaaaaaggctataccgattatccgaccctgggtgaaagcgcaaaaggttaataa1134
<210>4
<211>392
<212>prt
<213>人工序列
<220>
<223>合成序列:催化剂氨基酸序列,包含t7标签
<400>4
metalasermetthrglyglyglnglnmetglyargglysergluphe
151015
metserhisthrleupheaspprovalglnalaglyaspleuglnleu
202530
alaasnargilealametalaproleuthrargasnargserproasn
354045
alavalprolysaspilethralathrtyrtyralaglnargalathr
505560
alaglyleuleuilethrglualathralaileserhisglnglygln
65707580
glytyralaaspvalproglyleutyrserthrgluglnleuaspgly
859095
trplyslysvalthralaalavalhisgluargglyglyargileval
100105110
thrglnleutrphisvalglyargileserhisasnaspleuglnpro
115120125
aspglyglyalaprovalalaproseralailealaalalysserlys
130135140
thrtyrleuileasplysalathrglyglnglyhisphealaalathr
145150155160
sergluproargalaleuaspalaglugluleuproglyilevalhis
165170175
asptyralaalaalaalaargasnalavalgluthralaglypheasp
180185190
glyvalgluilehisglyalaasnglytyrleuleuaspglnpheleu
195200205
lysthrglyalaasnargargthraspasptyrglyglyserileglu
210215220
asnargalaargleuleuleuglualathrargalavalvalaspala
225230235240
ileglyglyglylysvalglyileargleuserprovalthrproala
245250255
asnaspilevalaspalaaspproglnproleupheasptyrvalile
260265270
argglnleualaproleuglyleualatyrvalhisvalileglugly
275280285
serthrglyglyproarggluleugluaspargpropheasptyrglu
290295300
alaleulysthralatyrargglualaglyglylysglyalatrpmet
305310315320
valasnasnalatyraspargalaleualametglualavalalaser
325330335
glyargalaaspilevalalapheglylysalapheileserasnpro
340345350
aspleuvalgluargleuargglnaspalaproleuasnprotrpasp
355360365
serlysthrphetyrglyglyglyglulysglytyrthrasptyrpro
370375380
thrleuglygluseralalysgly
385390
<210>5
<211>412
<212>prt
<213>人工序列
<220>
<223>合成序列:催化剂氨基酸序列,包含his标签和t7标签
<400>5
metglyserserhishishishishishisserserglyleuvalpro
151015
argglyserhismetalasermetthrglyglyglnglnmetglyarg
202530
glysergluphemetserhisthrleupheaspprovalglnalagly
354045
aspleuglnleualaasnargilealametalaproleuthrargasn
505560
argserproasnalavalprolysaspilethralathrtyrtyrala
65707580
glnargalathralaglyleuleuilethrglualathralaileser
859095
hisglnglyglnglytyralaaspvalproglyleutyrserthrglu
100105110
glnleuaspglytrplyslysvalthralaalavalhisgluarggly
115120125
glyargilevalthrglnleutrphisvalglyargileserhisasn
130135140
aspleuglnproaspglyglyalaprovalalaproseralaileala
145150155160
alalysserlysthrtyrleuileasplysalathrglyglnglyhis
165170175
phealaalathrsergluproargalaleuaspalaglugluleupro
180185190
glyilevalhisasptyralaalaalaalaargasnalavalgluthr
195200205
alaglypheaspglyvalgluilehisglyalaasnglytyrleuleu
210215220
aspglnpheleulysthrglyalaasnargargthraspasptyrgly
225230235240
glyserilegluasnargalaargleuleuleuglualathrargala
245250255
valvalaspalaileglyglyglylysvalglyileargleuserpro
260265270
valthrproalaasnaspilevalaspalaaspproglnproleuphe
275280285
asptyrvalileargglnleualaproleuglyleualatyrvalhis
290295300
valilegluglyserthrglyglyproarggluleugluaspargpro
305310315320
pheasptyrglualaleulysthralatyrargglualaglyglylys
325330335
glyalatrpmetvalasnasnalatyraspargalaleualametglu
340345350
alavalalaserglyargalaaspilevalalapheglylysalaphe
355360365
ileserasnproaspleuvalgluargleuargglnaspalaproleu
370375380
asnprotrpaspserlysthrphetyrglyglyglyglulysglytyr
385390395400
thrasptyrprothrleuglygluseralalysgly
405410
<210>6
<211>1239
<212>dna
<213>人工序列
<220>
<223>合成序列:编码包含his标签和t7标签的催化剂的核酸序列(编码seqidno:5)
<400>6
atgggcagcagccatcatcatcatcatcacagcagcggcctggtgccgcgcggcagccat60
atggctagcatgactggtggacagcaaatgggtcgcggatccgaattcatgtcccatacg120
cttttcgatcccgtccaggccggcgacctgcagctcgccaaccgcatcgccatggcgccg180
ctcacgcgcaaccgctcgccgaatgcggtgcccaaggacattaccgccacctactacgcc240
cagcgcgccaccgccggcctgctgatcaccgaggccacggccatcagccaccagggccag300
ggctatgcggacgtgccgggcctgtacagcaccgaacagctcgatggatggaaaaaggtc360
accgcagcggtccatgagcgcggcggcaggatcgtgacccagctctggcacgtgggccgc420
atttcccacaatgacctgcagcccgacggcggcgcccccgtggccccctccgccatcgcc480
gccaagtccaagacctacctgatcgacaaggccaccggccagggccatttcgcggccacg540
tccgaaccccgtgcgctggatgccgaagagctgcccggcatcgtgcacgactacgccgcc600
gccgcgcgcaacgcggtggagacggccggattcgacggcgtcgagatccacggcgccaac660
ggctacctgctggaccagttcctcaagaccggcgccaaccggcgcaccgacgactacggc720
ggcagcatcgagaaccgcgcgcgcctgctgctcgaagccacgcgcgccgtggtggacgcg780
atcggcggcggcaaggtgggcatccgactctcgcccgtcacgccggccaacgacatcgtc840
gatgccgatccgcagccgctgttcgactacgtgatccgccagctcgcaccgctgggcctg900
gcctacgtgcacgtgatcgaaggctccaccggcggcccgcgcgagctggaagaccgtccg960
ttcgactacgaagccctgaagaccgcctaccgcgaggccggcggcaaaggcgcctggatg1020
gtcaacaacgcctatgaccgtgcgttggcgatggaagcggtggccagtggccgcgccgac1080
atcgtcgccttcggcaaggccttcatctccaaccccgacctggtcgagcggctgcgccag1140
gacgcaccgctcaacccctgggactccaagaccttctacggcggcggcgagaagggctac1200
accgactacccgacgctcggcgaatcggcgaaaggctga1239
<210>7
<211>364
<212>prt
<213>紫色色杆菌
<400>7
metasnalaasplysleuleuthrproleuthrmetglyalavalala
151015
leuserasnargvalvalmetalaproleuthrargleuargasnile
202530
gluproglyaspvalproglyproleualalysglutyrtyrarggln
354045
argalaseralaglyleuilevalalagluglythrhisileserpro
505560
thralalysglytyralaglyalaproglyiletyrsergluglugln
65707580
valargalatrpsergluvalthrglyalavalhisglnaspglygly
859095
lysilealaleuglnleutrphisthrglyargileserhisargser
100105110
leuglnproasnglyaspalaprovalglyproseralaileglnala
115120125
aspserargthrasnileargalaalaaspglyserleuvalargglu
130135140
glncysaspthrproargalaleugluileglugluilegluaspile
145150155160
ilegluasptyrargargalaalaaspasnalaargargalaglyphe
165170175
aspmetvalgluilehisglyalahisglytyrleuileaspglnphe
180185190
leuserproalaalaasnvalargthraspglntyrglyglyserval
195200205
gluasnargalaargpheleuleugluvalvalaspalavalvalala
210215220
glutrpaspalaasphisvalglyileargileserproleuglyile
225230235240
pheasnglyvalserasnthraspglnleuaspmetalaleutyrleu
245250255
alagluglnleualalysarglysleualapheleuhisileserglu
260265270
proasptrpalaglyglyprothrleuaspaspglypheargalaglu
275280285
leuargglnargtyrproglyvalileileglyalaglyglytyrser
290295300
alaglulysalagluthrleuleulyslysglypheileaspalaala
305310315320
alapheglyargsertyrilealaasnproaspleuvalgluargleu
325330335
lysglnasnalaproleuasnproprolysproaspthrphetyrgly
340345350
glyglyalagluglytyrthrasptyrprothrleu
355360
<210>8
<211>1095
<212>dna
<213>紫色色杆菌
<400>8
atgaacgccgacaaactgctgaccccgctgaccatgggcgccgtcgccctgagcaaccgc60
gtcgtcatggccccgctgacccgcctgcgcaacatcgaaccgggcgacgtgcccggcccg120
ctggccaaggaatactaccgccagcgcgccagcgccggcctgatcgtggccgaaggcacc180
cacatttcccccaccgccaagggctatgccggcgcgcccggcatctacagcgaggaacaa240
gtgcgcgcctggagcgaagtcaccggcgcggtgcatcaagacggcggcaagatcgcgctg300
caactgtggcacaccggccgcatctcgcaccgctcgctgcagccgaacggcgacgcgccg360
gtcggcccgtccgccatccaggccgacagccgcaccaacatccgcgccgccgacggcagc420
ctggtgcgcgaacaatgcgacaccccgcgcgcgctggaaatcgaggaaatcgaggacatc480
atcgaggactaccgccgcgccgccgacaacgcgcgccgcgccggtttcgacatggtggag540
atccacggcgcccacggctatctgatcgaccagttcctgtcgccggccgccaacgtccgc600
accgaccagtacggcggcagcgtggaaaaccgcgcccgcttcctgctggaagtggtggac660
gcggtggtggcggaatgggacgccgatcacgtcggcatccgcatctcgccgctgggcatc720
ttcaacggcgtcagcaacaccgaccagctggacatggcgctgtacctggccgagcagttg780
gccaagcgcaagctggccttcctgcacatctccgagccggactgggccggcggcccgacg840
ctggacgacggcttccgcgccgaactgcgccagcgctatcccggcgtgatcatcggcgcc900
ggcggctactccgcggagaaggccgaaacgctgctgaagaaaggctttatcgacgccgcc960
gccttcggccgcagctacatcgccaacccggatctggtggagcgtctgaagcagaacgct1020
ccgctgaacccgcccaagccggatactttctatggcggcggcgcggaaggctataccgac1080
tacccgacgctgtaa1095
<210>9
<211>338
<212>prt
<213>芽孢杆菌属的种
<400>9
metaspthrlysleuphesersertyrthrvallysaspvalthrleu
151015
lysasnargilevalmetalaprometcysmettyrserserhisasn
202530
gluaspglylysvalgluasntrphisleuthrhistyrthrserarg
354045
alavalglyglnvalglyleuileilevalglualathralavalthr
505560
alaglnglyargileserproglnaspleuglyiletrpseraspasp
65707580
hisilegluglyleuglnglnleuthrglymetmetlysgluhisgly
859095
thrargalaglyileglnleualahisalaglyarglysalavalile
100105110
gluglygluileilealaproseralavalalapheasnglulysmet
115120125
lyslysprolysglumetthrlysglugluilelysgluthrileglu
130135140
alaphelysgluglyalavalargalalyslysalaglyphegluval
145150155160
ilegluilehisalaalahisglytyrleuileasnglupheleuser
165170175
proleuserasnleuarggluaspglutyrglyglyilealagluasn
180185190
argtyrargpheleuarggluvalileaspserileglnservaltrp
195200205
aspglyproleuphevalargvalseralaserasptyrasngluasn
210215220
glyleuaspvalgluasptyrvalthrpheglyargtrpmetlysglu
225230235240
glnglyileaspleuileaspvalserserglyalaleuvalproala
245250255
argilehisalatyrproglytyrglnvallysphealagluthrile
260265270
lysasnglualaaspileprothrglyalavalglyleuilethrser
275280285
glyleuglnalaglugluileleuglnasnaspargalaaspleuile
290295300
pheilealaarggluleuleuargaspprotyrpheprolysthrala
305310315320
alalysglnleuglythrgluilegluproprolysglntyrasparg
325330335
glytrp
<210>10
<211>1017
<212>dna
<213>芽孢杆菌属的种
<400>10
atggacacaaagttattttcttcatacacagtgaaagacgtcacactaaaaaaccgcatc60
gtcatggcgccgatgtgcatgtattccagccataatgaagatggaaaagtagaaaactgg120
catttgacccattatacaagcagagctgttggacaggttggcctgatcattgtggaagcg180
accgctgtaactgcgcagggccgcatttcaccacaggatctggggatctggagcgatgat240
catatcgaggggctgcagcagctgacaggcatgatgaaggagcatggcacccgtgccggc300
atccagcttgcgcatgcaggcagaaaagcggttattgagggcgaaatcattgctccatct360
gccgtggctttcaatgaaaaaatgaaaaagcctaaagagatgacaaaagaagagattaaa420
gaaacgatcgaagcctttaaggaaggcgctgtccgtgctaaaaaagcaggcttcgaggtt480
atagaaatccatgctgcccacggctatctgatcaatgagtttctatccccgctttccaat540
ctgcgggaggatgaatacggcgggatcgcagaaaaccgctaccgcttcctgagggaagtc600
atcgacagcatccagtctgtttgggacggacctctctttgtaagggtatcagcgagcgat660
tataacgaaaacggacttgatgttgaggattatgtcacgttcgggcgctggatgaaagag720
cagggcatcgacctgatcgatgtaagctccggagcactggtgccggcccgcattcacgct780
tatccaggctaccaggtcaaattcgctgaaaccatcaagaatgaggcagacatcccgaca840
ggcgccgtcggcctgattacatccggactgcaggctgaagagatcctgcaaaacgacaga900
gcagaccttatcttcatcgcacgtgagctgctccgcgatccatacttcccaaaaaccgca960
gccaaacagctcggcaccgaaatcgaacccccgaaacaatatgatagagggtggtaa1017
- 还没有人留言评论。精彩留言会获得点赞!
- 一种高性能抗指纹剂的制备方法
- 一种常压下光催化合成苯胺类化合物的方法及其使用的催化剂的制作方法
- 一种底物按次序催化的金属纳米粒子基催化剂的制作方法
- 一种Cu?ZnO?ZrO<sub>2</sub>?NH<sub>2</sub>/SBA?15复合催化剂的制备方法及其应用
- 一种催化气化灰渣中不可溶性碱金属催化剂的回收方法
- 一种催化氧化丙烷制取丙烯酸的催化剂及其制备方法
- 催化氧化丙烷制取丙烯酸的催化剂及其制备方法
- 一种催化合成γ-氯丙基三氯硅烷的方法及其催化剂的制作方法
- 一种高性能氧还原MnO<sub>2</sub>-Mn<sub>3</sub>O<sub>4</sub>/碳纳米管复合催化剂及其制备方法和应用
- 锡类催化剂催化合成聚乳酸共聚改性产物的方法