小分子多肽102aa及其应用的制作方法
本发明涉及生物医药技术领域,具体是小分子多肽102aa及其载体和应用。
背景技术:
周围神经损伤已成为临床上的常见病及多发病,由交通事故、疾病或手术造成,常导致多种并发症,如运动障碍、感觉障碍和神经性疼痛,严重影响患者的生活质量。近年来关于神经再生的理论和临床实践有了长足的进步,尤其是显微外科的产生和发展,但纯粹的显微手术修复神经无法解决周围神经再生中复杂的细胞和分子事件。因此更需要对神经再生的各个方面有更深刻的认识,以提高临床应用的水平。
周围神经损伤后,轴突再生和Schwann细胞迁移、分化是周围神经损伤修复的关键因素。Fyn是非受体酪氨酸激酶Src家族中的一员,分子量为59KD,主要由N端Src同源性的一个独特的乙酰化SH4结构域,以及一个与蛋白结合的SH3和SH2结构域和SH1激酶结合结构域以及C端的调节尾端组成,主要存在于胞质中。Fyn在髓鞘形成起始阶段发挥重要作用。Fyn缺乏小鼠,髓鞘变薄40-50%。Fyn信号通路最后通过激活MBP(myelin basic protein,髓鞘碱性蛋白)基因而在髓鞘形成中发挥重要作用。抑制Fyn的活性引起MAG(mye lin associated glycoprotein,髓鞘相关糖蛋白)、P0(外周髓磷脂P0蛋白)、MBP表达降低,抑制神经轴突的髓鞘化,并且可以阻断ERK、Akt以及p38MAPK的磷酸化,对Schwann细胞的增殖、分化和轴突的髓鞘化产生影响。
近期研究表明,Scyl1bp1(Scyl-binding protein 1,Scyl结合蛋白)因与Scyl发生相互作用而得名,具有多个预测的磷酸化位点。Scyl1bp1一方面转录调节MDM2,影响下游P53的表达从而调节轴突的生长。另一方面,在坐骨神经损伤后修复过程中,Scyl1bp1转录调节RhoA影响下游ROCK的表达,改变了Schwann细胞和轴突的骨架结构,从而调节轴突的再生和髓鞘化以及Schwann细胞的分化、迁移。
技术实现要素:
发明目的:针对现有技术中存在的不足,本发明的目的是提供一种小分子多肽102aa及其应用,具有促进Schwann细胞分化、轴突再生的药物用途。
技术方案:为了实现上述发明目的,本发明采用的技术方案为:
小分子多肽102aa,其氨基酸序列如SEQ ID NO.1所示。
编码所述的小分子多肽102aa的基因,其DNA序列如SEQ ID NO.2所示。
含有所述的小分子多肽102aa的编码基因的DNA序列的载体。
所述的载体,将小分子多肽102aa的DNA序列连接进pCMV-HA真核表达载体,构建出重组表达质粒。
所述的小分子多肽102aa在制备用于治疗周围神经损伤后修复与再生中的药物的应用。
所述的应用,其特征在于:小分子多肽102aa在制备用于促进Schwann细胞分化、轴突再生药物中的应用。
有益效果:与现有技术相比,本发明利用生物工程技术,基因重组一段102个氨基酸多肽对应的DNA序列到pCMV-HA真核表达载体。经酶切和序列分析证明重组成功后,将此真核表达重组多肽转染到神经细胞,免疫印迹证明多肽的蛋白表达,实现了多肽的重组。接着对多肽的促进周围神经再生功能进行了研究,细胞学和大鼠体内实验表明此多肽具有促进Schwann细胞分化、轴突再生及运动功能恢复的效应,在制备用于治疗周围神经损伤后修复与再生中的药物中将有很好的应用。
附图说明
图1是102aa多肽对应DNA序列PCR结果图;
图2是102aa多肽重组真核表达载体酶切鉴定结果图;
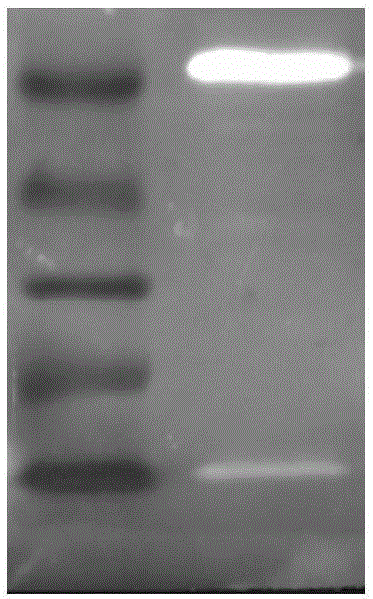
图3是检测35aa多肽的表达图,大小为20KD;
图4是小分子多肽能促进原代Schwann细胞的分化图;
图5是小分子多肽能促进轴突的延伸图;
图6是小分子多肽能促进坐骨神经损伤大鼠运动功能的恢复结果图。
具体实施方式
下面结合具体实施例对本发明作进一步的说明。实施例中未注明具体条件的实验方法,通常按照常规条件,例如分子克隆实验指南(第三版,J.萨姆布鲁克等著,黄培堂等译,科学出版社,2002年)中所述的条件,或按照制造厂商所建议的条件进行。
实施例1重组肽的克隆载体构建
全长Fyn质粒购买于上海吉凯基因,上游引物为5’-CCGGAATTCGGACCATGATCCAGGCAGAAGAGTGGTACTTTG-3’(含EcoRI酶切位点);下游引物为5’-CCGCTCGAGAAACCACAGTTAAGTTAAAACACAAACCATC-3’(含XhoI酶切位点),应用PCR技术成功扩增出102aa对应的306bp的mRNA序列(图1),其DNA序列如SEQ ID NO.2所示,所编码的102aa的氨基酸序列如SEQ ID NO.1所示。扩增得到的片段经ECOR1和XhoI酶切后与pCMV-HA载体连接,将连接产物转入感受态大肠杆菌DH5α中,在含Amp+琼脂平板上挑选克隆,以碱裂解法小提重组质粒后,以ECOR1和XhoI酶切鉴定(图2)。
实施例2重组肽的表达鉴定
将正确连接的102aa多肽真核表达载体转染293T细胞,48小时后搜集样品,RIPA细胞裂解液裂解,免疫印迹结果证明了此多肽的表达(图3)。主要过程如下:
利用lifectamine 2000试剂盒进行转染。用胰酶将处于对数生长期的细胞消化后,以每孔5×105个的细胞密度接种于6孔板;当细胞融合度达到60%时,更换无血清培养基,平衡2h;随后将2μg质粒DNA溶于250μL无血清培养基中并混匀;4μL脂质体混于250μL基培中;将以上两种溶液合并、混匀,室温孵育20min;将500μL含有脂质体和质粒DNA的培养基加至各孔,轻轻混匀后至于37℃,5%CO2的培养箱中培养;待6h后更换完全培养基。待转染48h后,可置于倒置荧光显微镜下观察荧光表达情况,估计转染效率,或提取细胞蛋白进行Western blot检测目的分子的表达。
实施例4Shwann细胞的分化、未分化PC12细胞突起延伸功能的检测
体外证明重组肽细胞水平的促分化、轴突延伸效应:以原代Shwann细胞、未分化PC12细胞为例,cAMP 10uM刺激原代Shwann细胞72h以及NGF 100ng/ml刺激未分化PC12 72h,利用Lipofectamin 2000kit将102aa多肽真核表达载体和对照组瞬时转染,48小时后观察Shwann细胞的分化及未分化PC12细胞形态变化,结果如图4和图5,显示与空载对照相比,102aa多肽真核表达实验组显著促进了Shwann细胞的分化、未分化PC12细胞突起延伸。
大鼠坐骨神经损伤模型足迹实验:以大鼠坐骨神经损伤模型为例,利用微量注射器注射10μl 102aa多肽真核表达载体和对照组至大鼠坐骨神经,分N、2w两个时间点进行足迹实验,结果如图6,显示此多肽具有促进运动功能恢复的作用。
SEQUENCE LISTING
<110> 南通大学
<120> 小分子多肽102aa的应用
<130> 100
<160> 4
<170> PatentIn version 3.3
<210> 1
<211> 102
<212> PRT
<213> Fyn
<400> 1
Ile Gln Ala Glu Glu Trp Tyr Phe Gly Lys Leu Gly Arg Lys Asp Ala
1 5 10 15
Glu Arg Gln Leu Leu Ser Phe Gly Asn Pro Arg Gly Thr Phe Leu Ile
20 25 30
Arg Glu Ser Glu Thr Thr Lys Gly Ala Tyr Ser Leu Ser Ile Arg Asp
35 40 45
Trp Asp Asp Met Lys Gly Asp His Val Lys His Tyr Lys Ile Arg Lys
50 55 60
Leu Asp Asn Gly Gly Tyr Tyr Ile Thr Thr Arg Ala Gln Phe Glu Thr
65 70 75 80
Leu Gln Gln Leu Val Gln His Tyr Ser Glu Lys Ala Asp Gly Leu Cys
85 90 95
Phe Asn Leu Thr Val Val
100
<210> 2
<211> 306
<212> DNA
<213> Fyn
<400> 2
atccaggcag aagagtggta ctttggaaaa cttggccgca aagatgctga gagacagctc 60
ctgtcctttg gaaacccaag aggtaccttt cttatccgcg agagcgaaac caccaaaggt 120
gcctactcac tttccatccg tgattgggat gatatgaaag gggaccacgt caaacattat 180
aaaatccgca agcttgacaa tggtggatac tatatcacaa cgcgggccca gtttgaaaca 240
cttcagcaac tggtacagca ttactcagag aaagctgatg gtttgtgttt taacttaact 300
gtggtt 306
<210> 3
<211> 42
<212> DNA
<213> Artificial
<220>
<223> 上游序列
<400> 3
ccggaattcg gaccatgatc caggcagaag agtggtactt tg 42
<210> 4
<211> 40
<212> DNA
<213> Artificial
<220>
<223> 下游序列
<400> 4
ccgctcgaga aaccacagtt aagttaaaac acaaaccatc 40
- 还没有人留言评论。精彩留言会获得点赞!