三维灌流培养系统及3D打印的组织器官的制作方法
本发明涉及组织工程领域,特别地涉及用于培养生物3D打印组织的心肺模拟三维灌流培养系统及采用该三维灌流培养系统培养的3D打印的组织器官。
背景技术:
生物3D打印技术的兴起,给医学界中组织工程领域的发展带来了巨大影响。通过3D生物打印技术,可以将生物相容性良好的生物材料打印成用于组织和/或器官修复、维持或改善受损组织或器官的组织工程(支架)。另外还可以将含有正常组织细胞(活细胞)的水凝胶打印在生物材料支架上,从而形成具有特定形态、结构和功能的相应组织器官。得到的含有活细胞的组织器官再经过一段时间的培养,细胞在生长增殖同时生物材料的支架逐渐降解被吸收,最终形成真正的活体器官,达到组织再生、修复和重建的功能。
为使3D打印的组织器官能够成功转化为需要的活体组织器官,如何实现组织细胞在三维的支架内长期培养、维持其功能以至于成活,成为一个十分重要的课题。三维灌流培养反应器为此提供了技术支持。
在三维灌流培养的发展过程中,先后出现平板型静态灌流培养和旋转型三维灌流培养等。但人体是一个复杂的活动的个体,需要不断供给营养和排泄废物的血液循环系统,现有的灌流培养系统都无法满足要求。因此,医学研究领域急需具有灌流功能的培养装置用来尽可能地模拟出体内微环境。
技术实现要素:
为了克服上述现有技术的缺陷而实现了本发明。本发明的发明目的在于提供一种三维灌流培养系统,其能够为生物3D打印的含组织细胞的三维组织器官提供心肺模拟环境,进而为组织器官的生长提供接近体内的微观环境。本发明的另一个发明目的在于提供一种通过上述三位灌流培养系统培养的3D打印的组织器官。
为了实现上述的发明目的,本发明采用如下的技术方案。
本发明提供了一种如下的三维灌流培养系统,所述三维灌流培养系统包括:培养液供给部,所述培养液供给部用于存储在所述三维灌流培养系统内流动的培养液;复合动力源,所述复合动力源能够在所述三维灌流培养系统内产生复合动力以模拟人体体内的心脏供给系统;三维培养器,所述三维培养器以使得组织器官能够进行多自由度运动的方式通过所述培养液对该组织器官进行培养;以及氧气/二氧化碳循环供给部,所述氧气/二氧化碳循环供给部用于将所述培养液中的氧气和二氧化碳维持在预定的浓度以模拟人体体内的肺部呼吸系统,在所述三维灌流培养系统中的培养液流动方向上,所述培养液供给部、所述复合动力源、所述三维培养器和所述氧气/二氧化碳循环供给部串联连通。
优选地,所述复合动力源包括彼此并联的蠕动泵和柱塞泵,在所述蠕动泵所在的支路上,所述蠕动泵与至少一个单向阀串联,并且在所述柱塞泵所在的支路上,所述柱塞泵与至少一个单向阀串联。
优选地,所述三维培养器包括:旋转培养组件,所述旋转培养组件用于收纳所述组织器官并对该组织器官进行培养;驱动组件,所述驱动组件能够产生使得所述旋转培养组件产生所述多自由度运动的驱动力;传动组件,所述传动组件用于将所述驱动组件的驱动力传动到所述旋转培养组件;以及支撑组件,所述支撑组件用于支撑所述旋转培养组件、所述驱动组件和所述传动组件。
更优选地,所述驱动组件包括能够至少两个减速电机,并且所述传动组件包括:主轴,所述主轴分别与所述至少两个减速电机连接;以及摇臂,所述摇臂的一端与所述主轴连接并且所述摇臂的另一端与所述旋转培养组件连接。
更优选地,所述旋转培养组件包括:旋转培养箱,所述旋转培养箱与所述摇臂连接;以及培养固定支架,所述培养固定支架收纳于所述旋转培养箱并且在所述培养固定支架上固定有用于培养所述组织器官的容器,所述培养液流经所述容器。
优选地,所述三维灌流培养系统还包括用于过滤所述培养液中的细胞排泄物的杂质过滤部,并且所述杂质过滤部设置于所述三维培养器的在培养液流动方向上的下游侧并与所述三维培养器连通。
更优选地,在所述杂质过滤部的培养液流动方向上的上游侧设置有单向阀。
优选地,所述三维灌流培养系统还包括用于暂时存储通过所述杂质过滤部过滤后的所述培养液的培养液回收存储部、用于对所述培养液进行监控的自动监控部以及用于补充所述培养液的培养液自动补给部,并且所述培养液回收存储部设置于所述杂质过滤部的在培养液流动方向上的下游侧并与所述杂质过滤部连通,所述自动监控部和所述培养液自动补给部均与所述培养液回收存储部连通。
优选地,所述三维灌流培养系统为闭环系统。
本发明还提供了一种如下的3D打印的组织器官,其特征在于,所述3D打印的组织器官以上技术方案中任意一项技术方案所述的三维灌流培养系统进行培养。
通过采用上述的技术方案,本发明提供了一种三维灌流培养系统,其能够为生物3D打印的含组织细胞的三维组织器官提供心肺模拟环境,进而为组织器官的生长提供接近体内的微观环境,该三维灌流培养系统克服静态或其它三维培养方法的缺陷,从而实现3D打印的组织器官的构建,并实现再生细胞在体外的长期培养。本发明还提供了一种通过上述三位灌流培养系统培养的3D打印的组织器官。
附图说明
图1是示出了根据本发明的一实施方式的三维灌流培养系统的连接结构示意图。
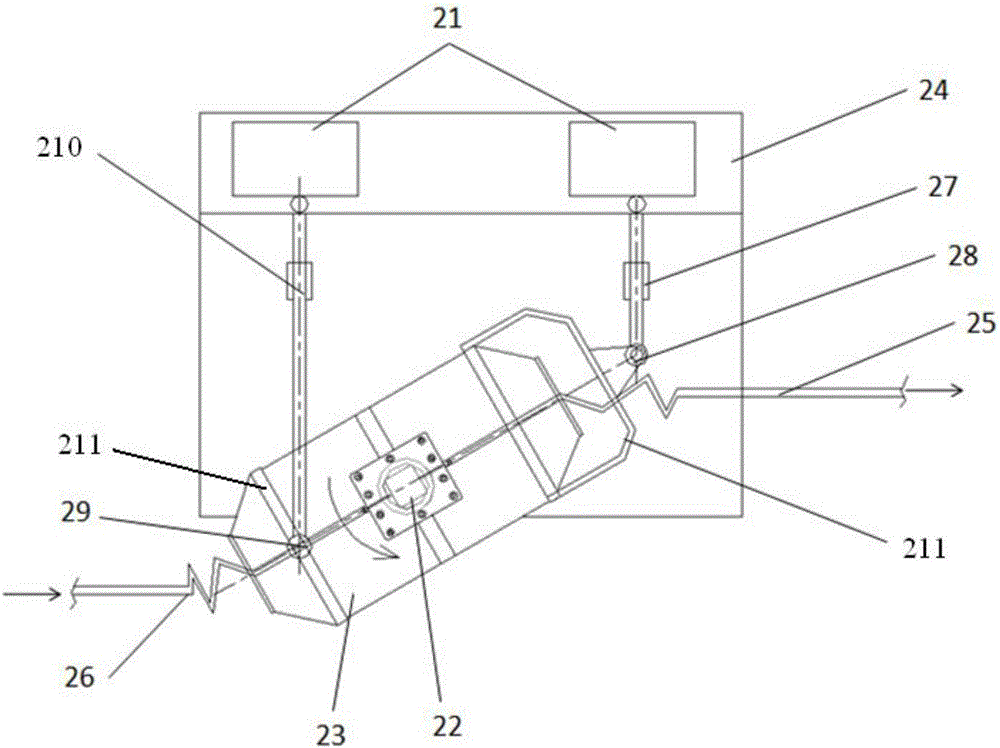
图2是示出了图1的三维灌流培养系统的三维培养器的结构示意图。
图3是用于说明图2中的三维培养器的运动状态的图,其中实线表示三维培养器的旋转培养箱的当前状态,虚线表示旋转培养箱能够从当前状态运动到的状态。
图4是用于说明图2中的三维培养器的运动状态的图,其中实线表示三维培养器的旋转培养箱的当前状态,虚线表示旋转培养箱能够从当前状态运动到的状态。
附图标记说明
1灌流培养装置 11蠕动泵 12单向阀 2三维培养器 21减速马达 22培养固定支架 23旋转培养箱 24机座 25出液管道 26进液管道 27主动轴 28、29万向节 210从动轴 211 Y型摇臂 3心脏供给模拟系统 31柱塞泵 32单向阀 4氧气/二氧化碳循环供给肺部模拟系统 41气体过滤装置 5杂质过滤系统 51单向阀 52过滤除杂装置 6自动监控系统 7培养液自动补给系统 71蠕动泵 72培养液存储罐 8培养液回收存储罐 9培养液供给罐
具体实施方式
以下将参照附图来说明根据本发明的三维灌流培养系统的连接结构。
如图1所示,根据本发明的一实施方式的三维灌流培养系统是闭环系统,图中的箭头表示在三位灌流培养系统中的培养液的流动方向。该三维灌流培养系统为按照如下顺序将各部分彼此串联连通成的闭环系统:培养液供给罐9、复合动力源(灌流培养装置1和心脏供给模拟系统3)、三维培养器2、杂质过滤系统5、培养液回收存储罐8、氧气/二氧化碳循环供给肺部模拟系统4。当该三维培养系统工作时,来自培养液供给罐9的培养液在该闭环系统中循环流动。由于整个三维灌流培养系统是闭环式的三维培养系统,培养液经过循环处理后继续利用,避免了培养液的大量浪费;同时由于是闭环系统,方便实现了对3D打印组织器官的无菌培养。该三维灌流培养系统自动监测、自动调节灌流的速度、灌流量以及灌流压力,因而能够适应不同3D打印的组织器官细胞的生长及构建要求。
在本实施方式中,培养液供给罐9为存储培养的容器并用于供给整个三维灌流培养系统中的培养液。
在本实施方式中,复合动力源设置于培养液供给罐9的在培养液流动方向上的下游侧并且该复合动力源包括彼此并联的灌流培养装置1和心脏供给模拟系统3,通过灌流培养装置1和心脏供给模拟系统3能够为培养液提供复合的动力以模拟人体体内的心脏供给系统。
作为构成复合动力源的一个支路,灌流培养装置1包括彼此串联的蠕动泵11和单向阀12。蠕动泵11增加调速调压功能,根据系统监测反馈,自动调整培养液的进液速度,压力等参数。单向阀则防止培养液倒流。
作为构成复合动力源的另一个支路,心脏供给模拟系统3包括彼此串联的柱塞泵31和两个单向阀32。柱塞泵31模拟人体体内的心脏供给环境,两个单向阀32分别位于柱塞泵31的培养液流动方向上的上游侧和下游侧。在3D打印的组织器官培养过程中,通过该心脏供给模拟系统3以心脏跳动的频率供给培养液。这样避免了蠕动泵11(脉冲方式)由于供给动力不足而无法实现心脏供血模拟的弊端,从而使细胞的生长更接近人体体内的环境。
在本实施方式中,三维培养器2为用于3D打印的组织器官的能够进行多自由度空间全方位旋转的三维培养器2。该三维培养器2设置于复合动力源的在培养液流动方向上的下游侧并且包括支撑组件、驱动组件、传动组件以及旋转培养组件。
作为支撑组件的机座24用于支撑驱动组件、传动组件和旋转培养组件。
驱动组件包括并排设置的两个减速马达21,即步进减速马达21。采用两个步进减速马达21相互配合驱动三维培养器2,使三维培养器2实现多自由度运动(即多自由度空间全方位运动),进而能够使培养液充分的流到3D打印的组织器官的各个部位,实现营养供给完全,提高组织细胞的增长速度及成活率。
传动组件包括主轴(主动轴27和从动轴210)、摇臂以及万向节28、29。主动轴27和从动轴210分别与两个减速马达21连接并且能够在减速马达21的带动下至少进行伸缩和旋转运动。在本实施方式中,设置两个Y型摇臂211,两个Y型摇臂211的一端分别与主动轴27和从动轴210通过万向节28、29连接,两个Y型摇臂211的另一端固定于旋转培养组件的下述旋转培养箱23。每个Y型摇臂211与旋转培养箱23具有两个固定部位,一个Y型摇臂211的两个固定部位的连线与另一个Y型摇臂211的两个固定部位的连线在空间上大致正交。优选地,两个Y型摇臂211分别固定于旋转培养箱23的靠近两端部的部分。
旋转培养组件包括旋转培养箱23、培养固定支架22、出液管道25和进液管道26。旋转培养箱23具有大致圆筒形状并且与上述Y型摇臂211固定在一起。在该旋转培养箱23内部固定培养固定支架22,3D打印的组织器官收纳于固定在该培养固定支架22的培养容器(未示出)。进液管道26和出液管道25从旋转培养箱23的两端分别被导入旋转培养箱23,并且均与上述培养容器连通。培养液通过进液管道26和出液管道25流入该培养容器内。
这样,三维培养器2能够使旋转培养箱23实现多自由度运动,该多自由度运动包括多种转动和/或线性运动的复合动作,使得旋转培养箱23能够实现多自由度空间全方位运动。可以说,通过驱动组件和传动组件的配合动作使得旋转培养箱23几乎可以实现空间内任意姿态(例如,如图3和图4中虚线所示的姿态,图3和图4仅是示例性地示出了旋转培养箱23能够实现的姿态)。通过旋转培养箱23的运动最终加速了培养液在培养过程中的流动和扩散作用,同时避免了一般三维培养器2因离心力等作用所产生的培养液内物质比重偏析和积聚现象。进一步,使得培养液流动无死角,保证培养液在3D打印的组织器官中的均匀度达到99%以上,能够有效确保培养最佳品质。
在本实施方式中,杂质过滤系统5设置于三维培养器2的在培养液流动方向上的下游侧并用于过滤从三维培养器2流出的培养液中的细胞排泄物等。该杂质过滤系统5包括彼此串联的过滤除杂装置52和单向阀51。该过滤除杂装置52采用高分子过滤的方法,去除在3D打印的组织器官培养过程中细胞产生的排泄物等杂质,使培养液可以回收利用,大量减少了培养液的浪费。单向阀51防止培养液产生逆流。
在本实施方式中,培养液回收存储罐8设置于杂质过滤系统5的在培养液流动方向上的下游侧并用于暂时存储通过杂质过滤系统5过滤后的培养液。
在本实施方式中,三维灌流培养系统还包括均与培养液回收存储罐8连通的自动监控系统6和培养液自动补给系统7。培养液自动监控系统6对培养液的pH值等的参数进行实时监控。培养自动补给系统7包括培养液存储罐72和将培养液存储罐72内的培养液供给到三维灌流培养系统的蠕动泵71。根据自动监控系统6监测的结果,培养自动补给系统7能够及时向培养液回收存储罐8提供新鲜的培养液,保证整个三维培养系统的培养液处于一个相对稳定的范围,从而提供了组织细胞的正常生长环境,提高组织细胞的增长速度及成活率。
在本实施方式中,氧气/二氧化碳循环供给肺部模拟系统4设置于培养液回收存储罐8的在培养液流动方向上的下游侧。该氧气/二氧化碳循环供给肺部模拟系统4包括气体过滤装置41,该气体过滤装置41具有进气口和出气口并且三维灌流培养系统的连通通路在该气体过滤装置41中优选地采用波纹形状。
通过该气体过滤装置41能够在三维灌流培养系统的连通通路内不断进行氧气、二氧化碳的交换,模拟人体体内的肺部呼吸系统,不断的给培养液提供所需的氧气,进而保证培养液中的氧气和二氧化碳处于预定的浓度,从而使细胞的生长更接近人体体内的环境。
通过使根据本发明的三位灌流培养系统为全封闭循环系统,并且该系统具有自动监测和自动补给的功能,能够有效地防止培养液的污染,大量节省培养液的浪费。整个三维灌流培养系统模拟心肺循环系统,使整个系统更接近体内的微观环境,从而提高了3D打印组织细胞的成活率及增长速度,促进组织器官的构建。
另外,需要说明的是,在某些条件下,根据本发明的三维灌流培养系统可以是开环系统。在根据本发明的三维灌流培养系统为开环系统的情况下,组成该三位灌流培养系统的各部分的连接顺序应当作出适当的调整,并且可以省略其中部分组成部分。
通过采用上述的技术方案,本发明提供了一种三维灌流培养系统,其能够为生物3D打印的含组织细胞的三维组织器官提供心肺模拟环境,进而为组织器官的生长提供接近体内的微观环境,该三维灌流培养系统克服静态或其它三维培养方法的缺陷,从而实现3D打印的组织器官的构建,并实现再生细胞在体外的长期培养。本发明还提供了一种通过上述三位灌流培养系统培养的3D打印的组织器官。
显然,本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!