一种香豆素类的苯硫酚荧光探针及其制备方法与流程
本发明涉及一种基于香豆素类结构的苯硫酚荧光探针的制备及其对苯硫酚的选择性荧光检测,属于有机小分子荧光探针领域。
背景技术:
苯硫酚属于硫醇类化合物,无色液体,具有特殊臭味,是一种重要的化工原料。但是苯硫酚具有很大的毒性,对鱼类半数致死量为0.01mmol/L~0.4 mmol/L。人体接触苯硫酚液体或者气体都将导致严重的中枢神经系统损害以及其他相关系统的伤害,包括呼吸急促、肌肉虚弱、恶心呕吐、昏迷甚至死亡。苯硫酚遇明火、高热或与氧化剂接触,有引起燃烧爆炸的危险。考虑到苯硫酚对环境及人体健康的危害,发展简单有效的方法检测苯硫酚具有重要意义。
技术实现要素:
一种基于2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素结构的苯硫酚荧光探针,其结构如下:
。
该探针的制备方法如下:
以2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素、2,4-二硝基氟苯为原料,在有机溶剂中经碱催化合成该探针。其中2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素:2,4-二硝基氟苯:碱摩尔比为1:1~1.5:2~3进行反应,碱选用碳酸钾或三乙胺;有机溶剂为二氯甲烷、乙腈或四氢呋喃;反应温度为室温;反应时间6~12小时。反应方程式:
。
本发明的苯硫酚荧光探针具有以下显著优点:(1)具有新颖的结构;(2)可以在缓冲体系中特异性地检测苯硫酚;(3)检测限低(仅为36nmol/L)、Stokes位移较大(128nm);(4)与苯硫酚反应表现为荧光增强,可以对苯硫酚进行定性定量检测;(5)该制备方法原料易得,产品易于分离、纯化。
附图说明
图1为实施例1制得的荧光探针的乙腈/PBS缓冲液(10mmol/L,pH=7.4)溶液(乙腈与PBS缓冲液体积比为3:7, 探针浓度为10µmol/L)及探针溶液与各种分析物混合后的荧光发射图谱(对甲氧基苯硫酚、苯硫酚、对氨基苯硫酚浓度为200µmol/L;其他分析物浓度为500µmol/L,包括氟化钾、氯化钠、溴化钾、碘化钾、碳酸钠、醋酸钠、硝酸钠、硫化钠、亚硫酸钠、硫酸钠、硫氰酸钾、硫代硫酸钠、连二亚硫酸钠、亚硝酸钠、双氧水、巯基乙酸、乙硫醇、丙氨酸、甘氨酸、半胱氨酸、谷胱甘肽、高半胱氨酸),纵坐标表示荧光强度,横坐标表示波长。激发波长为395nm。
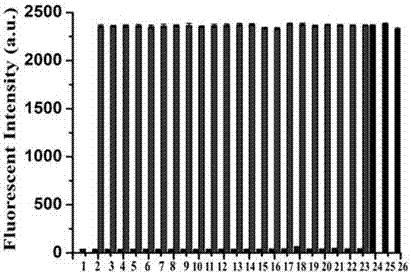
图2为实施例1制得的荧光探针的乙腈/PBS缓冲液(10mmol/L,pH=7.4)溶液(乙腈与PBS缓冲液体积比为3:7, 探针浓度为10µmol/L)对不同分析物(1探针;2氟化钾;3氯化钠;4溴化钾;5碘化钾;6碳酸钠;7醋酸钠;8硝酸钠;9硫化钠;10亚硫酸钠;11硫酸钠;12硫氰酸钾;13硫代硫酸钠;14连二亚硫酸钠;15亚硝酸钠;16双氧水;17巯基乙酸;18乙硫醇;19丙氨酸;20甘氨酸;21半胱氨酸;22谷胱甘肽;23高半胱氨酸;24对甲氧基苯硫酚;25苯硫酚;26对氨基苯硫酚,其中24对甲氧基苯硫酚、25苯硫酚、26对氨基苯硫酚的浓度为200µmol/L,其他分析物浓度为500µmol/L)在519nm处的溶液荧光强度对比图,激发波长为395nm。在图2中,纵坐标表示荧光强度,横坐标表示不同分析物;左起第一个柱1表示不加任何分析物;后面每组柱左边表示只有该被分析物存在下的溶液荧光强度,右边表示500µmol/L该被分析物和200µmol/L苯硫酚同时存在下的溶液荧光强度;最后三个柱表示200µmol/L甲氧基苯硫酚(24)、苯硫酚(25)、对氨基苯硫酚(26)存在时溶液的荧光强度。激发波长为395nm。
图3为不同浓度的苯硫酚加到该荧光探针的乙腈/PBS缓冲液(10mmol/L,pH=7.4)(乙腈与PBS缓冲液体积比为3:7, 探针浓度为10µmol/L)溶液后,溶液在519nm处荧光强度随时间的变化图,纵坐标表示荧光强度,横坐标表示时间。激发波长为395nm。
图4为该荧光探针的乙腈/PBS缓冲液(10mmol/L,pH=7.4)(乙腈与PBS缓冲液体积比为3:7, 探针浓度为10µmol/L)溶液,加入不同浓度的苯硫酚后50分钟时荧光响应光谱图,其中苯硫酚的浓度为0~250µmol/L,纵坐标表示荧光强度,横坐标表示波长。激发波长为395nm。
图5为该荧光探针的乙腈/PBS缓冲液(10mmol/L,pH=7.4)(乙腈与PBS缓冲液体积比为3:7, 探针浓度为10µmol/L)溶液在519nm处的溶液荧光强度随着苯硫酚浓度(0~250µmol/L)变化的散点图,纵坐标表示荧光强度,横坐标表示苯硫酚浓度。激发波长为395nm。
图6为该荧光探针的乙腈/PBS缓冲液(10mmol/L)(乙腈与PBS缓冲液体积比为3:7, 探针浓度为10µmol/L)溶液在不同pH条件与200µmol/L苯硫酚作用50分钟后,在519nm处的荧光强度变化图,纵坐标表示荧光强度,横坐标表示pH。激发波长为395nm。
具体实施方式
2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素结构的苯硫酚荧光探针的合成:
实施例1:探针的合成。将50.0mg(0.20 mmol) 2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素溶于3ml二氯甲烷中,加入58.0mg(0.40 mmol)K2CO3、37.2mg(0.20 mmol) 2,4-二硝基氟苯,室温搅拌反应,TLC跟踪反应,12小时反应完全,乙酸乙酯萃取,有机相用无水硫酸钠干燥,过滤,减压蒸除溶剂,硅胶柱层析分离提纯得62.3深红色固体,收率73.6%。1H NMR (400 MHz, CDCl3): δ 8.86(s, 1 H), 8.32 (d, J = 6.8 Hz, 1 H), 7.53 (s, 1 H), 7.10 (d, J = 9.2 Hz, 1 H), 6.88 (s, 1 H), 3.29-3.33 (m, 4 H), 2.77-2.90 (m, 4 H), 1.99-2.09 (m, 4 H). 13C NMR (100 MHz, CDCl3): δ 157.13, 155.44, 150.25, 146.30, 141.65, 138.64, 133.16, 131.39, 128.69, 125.10, 122.25, 119.76, 117.64, 106.90, 50.05, 49.65, 27.53, 21.25, 20.36. HRMS (ESI) (C13H15NO3) m/z: calculated for [M+H]+: 424.1145. Found [M+H]+: 424.1139.
实施例2:探针的合成。将50.0mg(0.20 mmol) 2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素溶于3mL二氯甲烷中,加入0.06mL(0.40 mmol)Et3N、37.2mg(0.20 mmol) 2,4-二硝基氟苯,室温搅拌反应,TLC跟踪反应,10小时反应完全,乙酸乙酯萃取,有机相用无水硫酸钠干燥,过滤,减压蒸除溶剂,硅胶柱层析分离提纯得73.9mg深红色固体,收率87.4%。
实施例3:探针的合成。将50.0mg(0.20 mmol) 2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素溶于3ml乙腈中,加入0.09mL(0.60mmol)Et3N、37.2mg(0.20mmol) 2,4-二硝基氟苯,室温搅拌反应,TLC跟踪反应,8小时反应完全,乙酸乙酯萃取,有机相用无水硫酸钠干燥,过滤,减压蒸除溶剂,硅胶柱层析分离提纯得69.5mg红棕色固体,收率82.2%。
实施例4:探针的合成。将50.0mg(0.20mmol) 2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素溶于3ml乙腈中,加入0.09mL(0.60mmol)Et3N、55.8mg(0.30mmol) 2,4-二硝基氟苯,室温搅拌反应,TLC跟踪反应,6小时反应完全,乙酸乙酯萃取,有机相用无水硫酸钠干燥,过滤,减压蒸除溶剂,硅胶柱层析分离提纯得74.5mg红棕色固体,收率88.0%。
实施例5:探针的合成。将50.0mg(0.20mmol) 2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素溶于3ml四氢呋喃中,加入0.09mL(0.60mmol)Et3N、55.8mg(0.30mmol) 2,4-二硝基氟苯,室温搅拌反应,TLC跟踪反应,8小时反应完全,乙酸乙酯萃取,有机相用无水硫酸钠干燥,过滤,减压蒸除溶剂,硅胶柱层析分离提纯得69.4mg红棕色固体,收率82.0%。
实施例6:基于2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素结构的荧光探针对苯硫酚的光物理检测应用研究。
将实施例1制备的基于2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素结构的荧光探针溶于3mL乙腈中,配制成浓度为1mmol/L的储备液,然后用乙腈/PBS缓冲液(10mmol/L,pH=7.4)(乙腈与PBS缓冲液体积比为3:7)配制浓度为10µmol/L探针测试溶液。探针溶液在395nm激发下,519nm处有较弱的荧光发射,当向探针溶液中加入苯硫酚或对氨基苯硫酚或对甲氧基苯硫酚时,荧光强度明显增强,Stokes位移达到128nm;苯硫酚加入量在0~50µmol/L内,探针溶液在519nm处的荧光强度与苯硫酚的浓度成较好的线性,且检测限仅为36nmol/L;加入其他常见分析物后,没有引起探针溶液的荧光强度显著变化。
由图1可知,向探针的溶液加入500µmol/L其他分析物后,包括氟化钾、氯化钠、溴化钾、碘化钾、碳酸钠、醋酸钠、硝酸钠、硫化钠、亚硫酸钠、硫酸钠、硫氰酸钾、硫代硫酸钠、连二亚硫酸钠、亚硝酸钠、双氧水、巯基乙酸、乙硫醇、丙氨酸、甘氨酸、半胱氨酸、谷胱甘肽、高半胱氨酸,荧光没有发生明显的增强;而加入苯硫酚或对氨基苯硫酚或对甲氧基苯硫酚后,探针溶液的荧光发射强度明显增强。
由图2可知,当10µmol/L探针的乙腈/PBS缓冲液(10mmol/L,pH=7.4)(乙腈与PBS缓冲液体积比为3:7)溶液中存在500µmol/L其他分析物时,包括氟化钾、氯化钠、溴化钾、碘化钾、碳酸钠、醋酸钠、硝酸钠、硫化钠、亚硫酸钠、硫酸钠、硫氰酸钾、硫代硫酸钠、连二亚硫酸钠、亚硝酸钠、双氧水、巯基乙酸、乙硫醇、丙氨酸、甘氨酸、半胱氨酸、谷胱甘肽、高半胱氨酸,再向该溶液中加200µmol/L苯硫酚,其柱高表明,在其他分析物存在的条件下,并不能干扰该探针对苯硫酚的响应,探针表现出很好的抗干扰能力。
由图3可知,不同浓度的苯硫酚加到探针溶液时,溶液的荧光强度都会随着时间的延长而增加,高浓度的苯硫酚增加的快,低浓度的增加的慢。
由图4、图5可知,探针浓度为10µmol/L时,随着苯硫酚浓度增大,荧光强度逐渐增大;苯硫酚浓度在0~50µmol/L内,探针溶液在519nm处的荧光强度与苯硫酚浓度成较好的线性。
由图6可知,该探针对苯硫酚的检测具有明显的pH依赖性。
由此得出结论,本发明制备的基于2,3,6,7-四氢-10-羟基-1H,5H-喹嗪并(9,1-GH)香豆素结构的荧光探针对苯硫酚具有很高的选择性和灵敏性,且可用于苯硫酚的定性定量检测。
- 还没有人留言评论。精彩留言会获得点赞!