一种原位形成拟胚体的多功能微流控芯片的制备方法与流程
本发明涉及微流控芯片的结构设计和制备技术领域,特别提供了一种原位形成拟胚体的多功能微流控芯片的制备方法。
背景技术:
现有技术中,用于细胞迁移和侵袭实验的微流控芯片即Transwell的相关实验技术,传统方法是将Transwell小室放入培养板中,小室内称上室,培养板内称下室,上室内盛装上层培养液,下室内盛装下层培养液,上下层培养液以聚碳酸酯膜相隔。我们将细胞种在上室内,由于聚碳酸酯膜有通透性,下层培养液中的成分可以影响到上室内的细胞,从而可以研究下层培养液中的成分对细胞生长、运动等的影响。但Transwell实验因为中间膜材料的性质限制,无法直接观察下层的现象,只能通过荧光进行观察,限制了它的应用。
微流控芯片实验室又称芯片实验室或微流控芯片,指的是把生物和化学等领域中所涉及的样品制备、反应、分离、检测、细胞培养、分选、裂解等基本操作单元集成或基本集成到一块几平方厘米(甚至更小)的芯片上,由微通道形成网络,以可控流体贯穿整个系统,用以取代常规化学或生物实验室的各种功能的一种技术。微流控芯片技术作为一门迅速发展起来的科学技术,已经在生物医学领域展现了其独特的优势,更因其同细胞尺寸匹配、环境同生理环境相近、在时间和空间维度上能够提供更为精确的操控,易于通过灵活设计实现多种细胞功能研究等特点而成为新一代生物仿生和细胞研究的重要平台。但传统的Transwell实验无法直接观察下层的现象,只能通过荧光进行观察,限制了它的应用。
人们迫切希望获得一种技术效果优良的原位形成拟胚体的多功能微流控芯片的制备方法。
技术实现要素:
本发明的目的是提供一种技术效果优良的原位形成拟胚体的多功能微流控芯片的制备方法。
本发明提供了一种原位形成拟胚体的多功能微流控芯片的制备方法,所述多功能微流控芯片是用于细胞迁移和侵袭实验的TRANSWELL微流控芯片;其特征在于:该芯片由三层芯片组成,上层芯片为带有防塌陷小柱的细胞培养室,中间层为多孔滤膜,下层为带有微阵列小柱的细胞培养室;所述微流控芯片的顶层芯片的下表面和多孔滤膜为静电吸附,底层芯片的上表面和多孔滤膜为聚二甲基硅氧烷PDMS粘合,同时底层芯片的上表面和顶层芯片的下表面进行聚二甲基硅氧烷PDMS粘合;
所述原位形成拟胚体的多功能微流控芯片的制备方法依次要求如下:
取多孔滤膜在顶层芯片相应观察窗的位置处进行打孔;
将多孔滤膜置于玻璃片上进行紫外活化0.5-3小时,然后,用硅烷化处理10~60分钟;
多孔滤膜与顶层芯片一同进行不可逆的氧等离子封接后,置于70-90°烘箱中加热30分钟;
聚二甲基硅氧烷PDMS粘合方法为:使用单体与引发剂比例为(15~25):1的聚二甲基硅氧烷PDMS聚合物,在玻璃片上甩10um-50um厚的薄膜,将底层芯片的上表面进行氧等离子的处理后,蘸取聚二甲基硅氧烷PDMS聚合物薄膜,与封接有顶层芯片的多孔滤膜对齐封接粘合,置于70~90°烘箱中加热,15-60分钟固化完全;
之后将封接好的芯片从烘箱中拿出后,切成需要的尺寸备用。
所述原位形成拟胚体的多功能微流控芯片的制备方法还满足下述要求之一或其组合:
其一,所述多功能微流控芯片的材料为能透光透气的聚二甲基硅氧烷PDMS聚合物,聚二甲基硅氧烷PDMS单体与引发剂比例为(5~15):1;
其二,多孔滤膜材料为聚碳酸酯膜,聚碳酸酯膜的孔径为0.01um-10um;
其三,顶层芯片培养室内设置有防塌陷小柱,防止顶层芯片塌陷影响液体的流通;
其四,底层芯片内有阵列排布的微柱,其中微柱的直径为200-800μm,微柱之间的距离为50-100μm,微柱的高度为200-900μm;微阵列小柱的高度要求低于底层通道的高度,以保证下层芯片中细胞具有充足的营养;
其五,顶层芯片与底层芯片为十字交叉,多孔滤膜切割成适当尺寸粘合于交叉部位,顶层芯片通道结构延长的部位可以观察顶层细胞,底层芯片通道延长的部位可以观察底层细胞。
本发明中制得的微流控芯片同时具有Transwell小室和微流控芯片的功能,通过视窗可以直接观察底层芯片,底层芯片可直接形成拟胚体,进行向心肌或脑的定向分化,可用于具有代谢依赖性药物的评价。
本发明有以下优点:
(1)可在不同的芯片层根据实验设计接种不同细胞。
(2)可同时观察顶层芯片和底层芯片的细胞培养状况。
(3)底层芯片可高通量的原位形成拟胚体,同时向心肌或脑等进行定向分化,用于进行药物评价。
附图说明
下面结合附图及实施方式对本发明作进一步详细的说明:
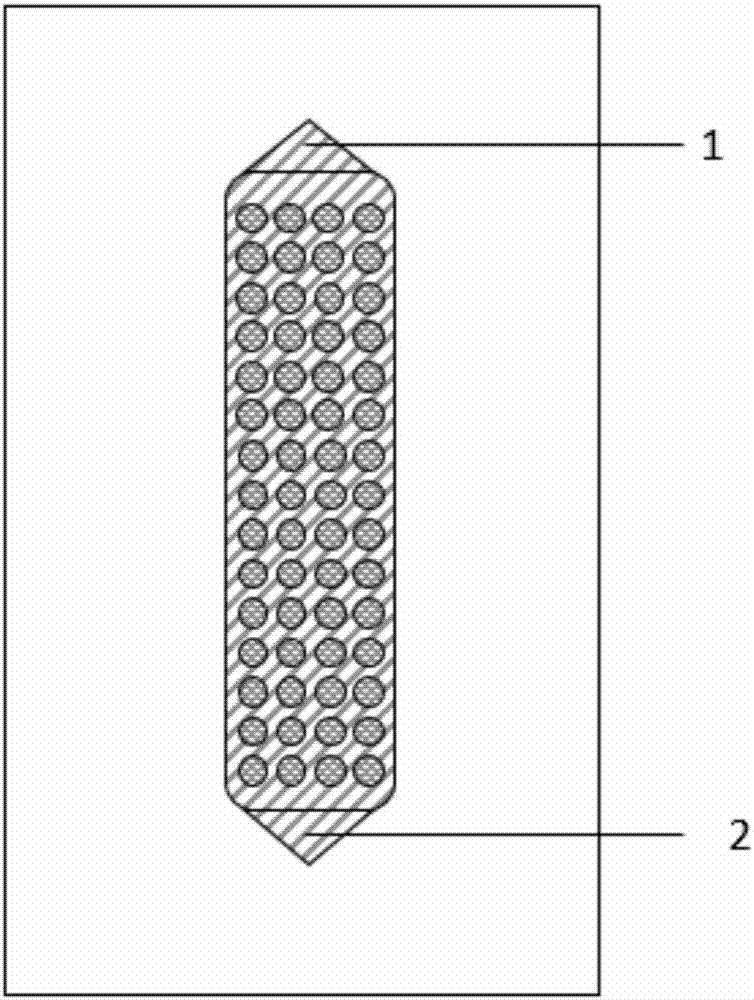
图1为原位形成拟胚体的多功能微流控芯片的制备方法制得的顶层芯片结构示意图;
图2为原位形成拟胚体的多功能微流控芯片的制备方法制得的底层芯片结构示意图;
图3为底层芯片电镜图;
图4为底层芯片拟胚体形成的明场观察图。
具体实施方式
图1中附图标记含义如下:1为液体入口,2为液体出口,3为防塌陷小柱。
实施例1
一种原位形成拟胚体的多功能微流控芯片的制备方法,所述多功能微流控芯片是用于细胞迁移和侵袭实验的TRANSWELL微流控芯片;该芯片由三层芯片组成,上层芯片为带有防塌陷小柱的细胞培养室,中间层为多孔滤膜,下层为带有微阵列小柱的细胞培养室;所述微流控芯片的顶层芯片的下表面和多孔滤膜为静电吸附,底层芯片的上表面和多孔滤膜为聚二甲基硅氧烷PDMS粘合,同时底层芯片的上表面和顶层芯片的下表面进行聚二甲基硅氧烷PDMS粘合;
所述原位形成拟胚体的多功能微流控芯片的制备方法依次要求如下:
取多孔滤膜在顶层芯片相应观察窗的位置处进行打孔;
将多孔滤膜置于玻璃片上进行紫外活化0.5-3小时,然后,用硅烷化处理10~60分钟;
多孔滤膜与顶层芯片一同进行不可逆的氧等离子封接后,置于70-90°烘箱中加热30分钟;
聚二甲基硅氧烷PDMS粘合方法为:使用单体与引发剂比例为(15~25):1的聚二甲基硅氧烷PDMS聚合物,在玻璃片上甩10um-50um厚的薄膜,将底层芯片的上表面进行氧等离子的处理后,蘸取聚二甲基硅氧烷PDMS聚合物薄膜,与封接有顶层芯片的多孔滤膜对齐封接粘合,置于70~90°烘箱中加热,15-60分钟固化完全;
之后将封接好的芯片从烘箱中拿出后,切成需要的尺寸备用。
所述原位形成拟胚体的多功能微流控芯片的制备方法还满足下述要求之一或其组合:
其一,所述多功能微流控芯片的材料为能透光透气的聚二甲基硅氧烷PDMS聚合物,聚二甲基硅氧烷PDMS单体与引发剂比例为(5~15):1;
其二,多孔滤膜材料为聚碳酸酯膜,聚碳酸酯膜的孔径为0.01um-10um;
其三,顶层芯片培养室内设置有防塌陷小柱,防止顶层芯片塌陷影响液体的流通;
其四,底层芯片内有阵列排布的微柱,其中微柱的直径为200-800μm,微柱之间的距离为50-100μm,微柱的高度为200-900μm;微阵列小柱的高度要求低于底层通道的高度,以保证下层芯片中细胞具有充足的营养;
其五,顶层芯片与底层芯片为十字交叉,多孔滤膜切割成适当尺寸粘合于交叉部位,顶层芯片通道结构延长的部位可以观察顶层细胞,底层芯片通道延长的部位可以观察底层细胞。
本实施例中制得的微流控芯片同时具有Transwell小室和微流控芯片的功能,通过视窗可以直接观察底层芯片,底层芯片可直接形成拟胚体,进行向心肌或脑的定向分化,可用于具有代谢依赖性药物的评价。
本实施例有以下优点:(1)可在不同的芯片层根据实验设计接种不同细胞。(2)可同时观察顶层芯片和底层芯片的细胞培养状况。(3)底层芯片可高通量的原位形成拟胚体,同时向心肌或脑等进行定向分化,用于进行药物评价。
实施例2
微流控芯片制作
取多孔滤膜在顶层芯片相应观察窗的位置处进行打孔,将多孔滤膜(2)置于玻璃片上进行紫外活化1小时,然后,用硅烷化处理30分钟,多孔滤膜(2)与顶层芯片一同进行不可逆的氧等离子封接后,置于80度烘箱中加热30分钟。使用单体与引发剂比例为20:1的PDMS聚合物,在玻璃片上甩10um-50um厚的薄膜,将底层芯片的上表面进行氧等离子的处理后,蘸取薄PDMS,与封接有顶层芯片的多孔滤膜对齐粘合,置于80度烘箱中加热,30分钟固化完全。将封接好的芯片从烘箱中拿出后,切成需要的尺寸。
实施例2
细胞接种和诱导
将芯片放在培养皿中,紫外灭菌2h,用移液枪将细胞培养基从芯片入口处加入,使培养基充满整个细胞培养室。放入真空泵中抽真空,除掉细胞培养室中的气泡。将六孔板中的Hips细胞用ReLeSR进行消化,细胞从壁上脱落后,终止消化,将培养瓶中的细胞悬液吸入离心管中进行离心,离心后,吸走上清液扔掉,加入新的培养基使细胞重悬,用移液枪吸取细胞悬液,从芯片下层液体入口处加入,从液体出口处吸走对应体积的培养基,在培养皿中加入培养基,减少芯片中培养基的挥发。将培养皿放在37℃的培养箱中保持静止24h,使细胞形成拟胚体,然后进行心肌细胞的定向分化,即第一天加入12微摩尔的CHIR99021作用24小时,第4天加入12微摩尔IWP2作用2天,前6天使用1640/B27减低胰岛素培养基,第七天开始使用1640/B27培养基。心肌细胞在第十天时开始跳动。
实施例3
心肌跳动一周后,开始接种上层细胞,将培养瓶中的HePG2细胞用胰酶进行消化,细胞从壁上脱落后,终止消化,将培养瓶中的细胞悬液吸入离心管中进行离心,离心后,吸走上清液扔掉,加入新的培养基使细胞重悬,用移液枪吸取细胞悬液,从顶层芯片液体入口1处加入细胞悬液,从液体出口2处吸走对应体积的培养基,进行置换,重复三次后,可认为底层顶层中已充满细胞悬液,放入培养箱中,使细胞贴壁生长。
- 还没有人留言评论。精彩留言会获得点赞!