可完全去疤的可逆末端终止功能核苷酸及其应用的制作方法
本发明属于生物学技术领域,特别涉及一种可完全除疤的可逆末端终止功能核苷酸及其在高通量测序技术上的应用。其中可逆末端终止功能核苷酸的连接臂可以经过两步反应而被完全去除(可完全去疤),从而实现此可逆末端终止功能核苷酸在引物上高效合成延伸和有效终止,进而实现可逆末端终止测序的长读长。
背景技术:
上个世纪七十年代,由Sanger等发明的双脱氧链终止法第一代DNA测序技术,为科学发展做出了重大贡献,成就了“人类基因组计划”。但由于其通量低、成本高等的缺点,所以无法满足多物种大规模基因组测序以及深度和重复测序的需求,于是第二代高通量测序技术应运而生。从2005年至今,二代测序技术发展十分迅猛,各二代测序平台的更新换代速度之快令人目不暇接,其所产生的数据量也呈指数级增长,这极大地推动了几乎所有生物医学领域的研究进展。目前主流二代高通量测序仪所采用的二代测序技术主要有“合成测序法”和“连接测序法”两种。
“可逆末端终止测序法”属于合成测序法(Sequencing By Synthesis,SBS)的一种,由美国哥伦比亚大学的Jing yue Ju教授在2003年首先提出并付诸实践,是目前市场占有率最高、应用前景最被看好的一种二代高通量测序技术(Li Z,Bai X,Ruparel H,et al.Proc Natl AcadSci U S A.2003,100:414-9.)。可逆末端终止法测序反应底物分子是一种具有可逆末端终止功能的核苷酸类似物,称为“可逆末端终止功能核苷酸”(reversible terminator)。与传统Sanger测序法所采用的“双脱氧末端终止功能核苷酸”的最大不同在于,其末端终止基团的引物延伸终止功能是可逆的,可以通过一定的化学转变恢复为正常的、可以再次进行引物延伸的基团。
目前,可逆末端终止功能核苷酸大体可分为两种:(a)第一种在核苷酸戊糖3’端羟基氧上连一个行使可逆末端终止功能的封闭基团。在这种情况下,与碱基上相连的可被切掉的荧光基团仅起到测序指示剂的作用(Guo J,Yu L,Turro NJ,Ju J.Acc Chem Res.2010,43(4),551-63.)。(b)第二种可逆末端终止封闭基团不位于3’端,而连接于碱基上。与碱基相连的荧光基团通常不仅起到测序指示剂的作用,而且也是可逆终止基团的一部分,起到了终止引物延伸的作用(Bowers J,Mitchell J,Beer E,et al.Nat Methods.2009,6(8), 593-5.)。这两种可逆末端终止功能核苷酸各有优劣,第一种由于有专门的可逆末端终止基团,可逆终止的效果可能会更好一点。第二种由于3’端没有修饰基团,更容易合成也更容易被DNA聚合酶所接受。
3’末端带有封闭基团的可逆末端终止功能核苷酸目前发展比较成熟并已经商品化的有三种:(1)Illumina Solexa所使用的3’-O-N3可逆末端终止功能核苷酸(Bentley DR,Balasubramanian S,Swerdlow HP,et al.Nature.2008,456(7218),53-9.)。(2)Steven A Benner团队研发的3’-ONH2可逆末端终止功能核苷酸(Hutter D,Kim MJ,Karalkar N.,et al.Nucleos.Nucleot.Nucl.Acids,2010,29,879-895.)。(3)哥伦比亚大学Jing yue Ju团队研发的3’-O-丙烯基可逆末端终止功能核苷酸(Guo J,Yu L,Turro NJ,Ju J.Acc Chem Res.2010,43(4),551-63.)。单就可逆末端终止功能而言,这三种测序试剂的表现都是不错的,其可逆末端终止基团和荧光基团都可以几乎100%地被切除。对于可逆末端终止封闭基团连接于碱基上的可逆末端终止功能核苷酸,目前已商品化的只有Helicos公司的单分子测序仪所采用的'virtual terminator'。
由于可逆末端终止功能核苷酸采用荧光作为测序指示剂,这极大地增强了测序的灵敏性与准确率,同时降低了上样量;并且由于采用了可逆末端终止测序策略,有效地解决了多聚重复序列(例如PolyA)的准确读取问题。这种测序策略可以准确读出大于18个连续的A。Solexa公司正是充分利用和发挥了可逆末端终止测序法的这些优势(并整合了原Illumina在DNA芯片上的优势),在被Illumina购买后不到5年的时间内,迅速地在二代高通量测序市场上脱颖而出,成为了目前市场上应用最广泛的二代高通量测序仪。其在测序成本和测序通量上都击败了其主要竞争对手Life Tech公司ion系列测序平台,但其在读长上的优势并不明显(Chen F,Dong M,Ge M,et al.Genomics Proteomics Bioinformatics.2013,11(1),34-40)。
影响可逆末端终止测序法读长的原因就在于:每一步切除荧光基团后在碱基上留下的连接臂残余(即疤痕)。每读出一个碱基,在延伸的引物上就加上一个带有疤痕的脱氧核苷酸。并且,随着测序引物的合成延伸,这种带有疤痕的脱氧核苷酸越积越多,这会极大地破坏DNA双螺旋结构的稳定性,从而影响DNA聚合酶与底物的结合;另一方面,这种带有疤痕的脱氧核苷酸也会影响DNA聚合酶对底物的识别。
技术实现要素:
为了解决至少部分上述技术问题,本发明的发明人进行了深入研究,并发现通过由含有C-C糖苷键的核苷酸、连接核苷酸的碱基与荧光基团的邻二醇基可切割连接臂和荧光基团三部分构成的可逆末端终止功能核苷酸可完全去除连接臂残余。基于此完成了本发明。具体地,本发明包括以下内容。
本发明的一方面,提供可完全去疤的可逆末端终止功能核苷酸,此功能核苷酸由含有C-C糖苷键的核苷酸、连接核苷酸的碱基与荧光基团的邻二醇基可切割连接臂和荧光基团三部分构成。
在某些实施方案中,含有C-C糖苷键的核苷酸中的核苷酸为选自由dATP、dTTP、dGTP和dCTP组成的组中的至少之一。
在某些实施方案中,邻二醇基可切割连接臂具有如下所述的结构式:
-(CH2)m(CHOH)2(CH2)n-
其中m和n分别为1至5的整数,例如,1、2、3、4或5。
在某些实施方案中,荧光基团选自由Cy3、Cy5、Cy5.5、Cy7、FITC、Alexa 488、Alexa 568、JOE、ROX、罗丹明6G(Rhodamine 6G)、四甲基罗丹明(Tetramethyl rhodamine)、丽丝胺(Lissamine)、德克萨斯红(Texas Red)、BODIPY 576/589、BODIPY 630/650和BODIPY 650/665组成的组的至少之一。
在优选的实施方式中,本发明的可逆末端终止功能核苷酸具有下式1所示的化学结构式之一。
本发明的另一方面,提供可完全去疤的可逆末端终止功能核苷酸在高通量测序技术上的应用。
在某些实施方案中,可完全去疤的可逆末端终止功能核苷酸在高通量测序技术上的应用包括下述具体步骤:
1)测序DNA模板及引物的固定;
2)引物延伸:向反应体系加入延伸反应混合液开始进行引物聚合延伸,此混合液主要包括DNA聚合酶(或逆转录酶)及四种不同碱基带有不同颜色荧光的可完全去疤可逆末端终止功能核苷酸;
3)延伸终止:去离子水洗涤,清除延伸反应混合液,终止引物延伸反应;
4)碱基读取:CCD拍照,通过荧光颜色来判定所延伸的碱基的种类;
5)切除连接臂及与其相连的荧光基团:先加入高碘酸钠(NaIO4)溶液切断邻二醇基连接臂去除荧光基团,一定温度下反应一段时间后再用去离子水清洗;然后加入胺类催化剂将剩余的丙醛基完全去除,一定温度下反应一段时间后再用去离子水清洗;
6)重复步骤2-5;
7)序列判读:利用图像分析软件,根据荧光与碱基种类的对应关系,对测序DNA模板进行序列判读。
在某些实施方案中,可逆末端终止功能核苷酸在高通量测序技术上的应用中,步骤2)的DNA聚合酶或逆转录酶为以下酶的一种:Taq、REAP 475、EEAP 442、Vent(exo-)、Deep Vent(exo-)、9° Nm、Therminator、Therminator-2、Therminator-3、Bst、Bsu、Klenow、Klenow(exo-)、AffinityScript RT、M-MLV Reverse Transcriptase、ImProm-II Reverse Transcriptase、ThermoScript Reverse Transcriptase、HIV Reverse Transcriptase、Maxima Reverse Transcriptase、ReverAidTM Reverse Transcriptase、SuperScript II Reverse Transcriptase、SuperScript III Reverse Transcriptase、Enhanced Avian Reverse Transcriptase。
在某些实施方案中,可逆末端终止功能核苷酸在高通量测序技术上的应用中,步骤5)的胺类催化剂为选自氨基乙酸、吗啉和吡咯烷的至少一种。
在某些实施方案中,本发明的可逆末端终止功能核苷酸可以完全切除连接臂(本发明中,有时也称作可完全去疤)。
在某些实施方案中,本发明的可逆末端终止功能核苷酸的连接臂较短,引物延伸聚合一个带有大荧光基团的可逆末端终止功能核苷酸后,DNA的双螺旋结构由于大沟构成的改变而改变,便无法再聚合第二个,从而达到“延伸且只延伸一个”的目的。
在某些实施方案中,出于完全去除连接臂的考虑,嘧啶碱基5位和嘌呤碱基的7位C被N所取代。这样,完全消除疤痕以后,DNA双螺旋结构不会因可逆末端终止功能核苷酸在引物上的累积而遭到破坏,从而实现可逆末端终止测序法的长读长。
在某些实施方案中,本发明所述的高通量测序属于可逆末端终止测序法,即合成测序法,其利用DNA聚合酶的链延伸反应,边合成边测序,包括多步引物延伸、终止、切除操作。
附图说明
图1:为本发明某些实施方案中的可完全去疤可逆末端终止功能核苷酸的结构式(Dye:荧光基团)。
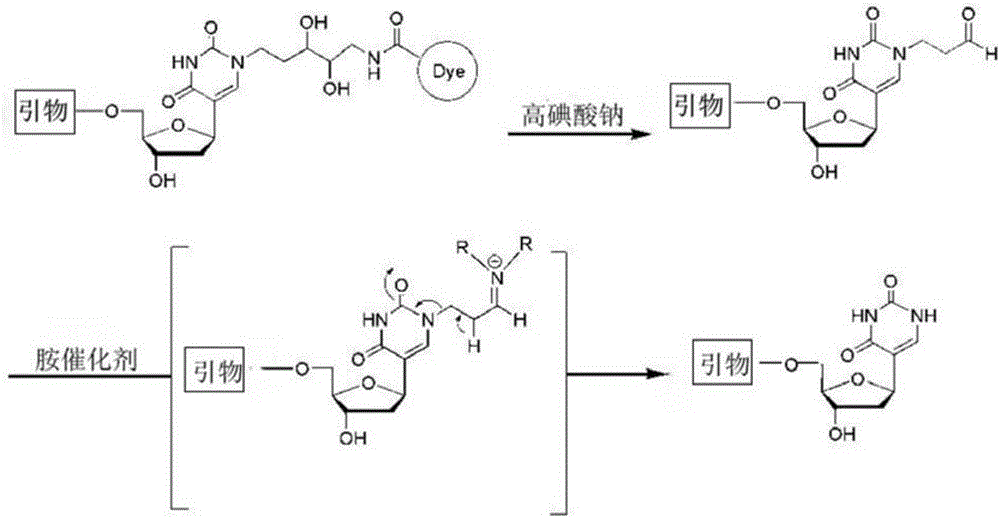
图2:为本发明某些实施方案中的可完全去除连接臂(完全去疤)过程示意图。
图3:为本发明某些实施方案中的可逆末端终止测序法的具体操作步骤(多步引物延伸、终止、切除)。
图4:为本发明某些实施方案的烯糖化合物的合成路线。
图5:为本发明某些实施方案的可完全去疤dT可逆末端终止功能核苷酸的合成路线。
图6:为本发明某些实施方案的甲苯磺基取代的无疤连接臂的合成路线。
图7:为本发明某些实施方案的可完全去疤dC可逆末端终止功能核苷酸的合成路线。
图8:为本发明某些实施方案的可完全去疤dA可逆末端终止功能核苷酸的合成路线。
图9:为本发明某些实施方案的可完全去疤dG可逆末端终止功能核苷酸的合成路线。
图10:为本发明某些实施方案的可完全去疤dT可逆末端终止功能核苷酸完全去疤反应。
图11:为本发明某些实施方案的可完全去疤可逆末端终止功能胞嘧啶核苷酸(BODIPY 576/589Labeled 1-(5-amino-3,4-dihydroxypentyl)-2'-deoxy-pseudouridine-5'-triphosphate)结构式。
图12:为本发明某些实施方案的单侧引物延伸PAGE电泳图。
图13:为本发明某些实施方案的固定到醛基基片上的测序底物及引物。
具体实施方式
通过解释以下本申请的优选实施方案,本发明的其他目的和优点将变得清楚。
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的实验方法、测定或测试方法,但是在本发明的实验、测定或测试中也可以使用与本文所述相似或等同的任何方法。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法或实验。在与任何并入的文献冲突时,以本说明书的内容为准。
本发明中,名词术语既包括单数形式,也包括复数形式,除非上下文另行明确指出。本发明中所述的“至少之一”或“至少一种”不仅仅指包含“一个”或“一种”的情况,更重要的还包含“多个”或“多种”的情况。
本发明中,术语“可完全去疤”是指可逆末端终止功能核苷酸的连接臂可以被完全切除/去除/消除。其被完全去除的过程可例如如图2所示。首先,连接臂中的邻二醇基被高碘酸盐氧化所切断,从而去除荧光基团。随后,剩余的丙醛基经胺类催化剂催化形成亚胺,亚胺基α位的一个电子引发了β-消除反应,从而使碱基杂环上的N原子与丙醛完全分离,达到完全去除连接臂(疤痕)的目的。
本发明中,术语“含有C-C糖苷键的核苷酸”是指核苷酸中的嘧啶碱基5位或者嘌呤碱基的7位C被N所取代的天然核苷酸的衍生物。它是一种具有可逆末端终止功能的核苷酸类似物,称为“可逆末端终止功能核苷酸”(reversible terminator)。优选地,天然核苷酸为由碱基、核糖或脱氧核糖和磷酸组成。优选所述天然核苷酸选自由dATP、dTTP、dGTP和dCTP组成的组中的至少之一。
本发明中,术语“邻二醇基可切割连接臂”为在邻位上具有两个醇基(-OH)的化合物。优选地,其具有如下所述的结构式:-(CH2)m(CHOH)2(CH2)n-,其中m和n分别为1至5的整数,例如,1、2、3、4或5。在优选的实施方案中,m为2,n为1。
本发明中,术语“荧光基团”为本领域内通常使用的任何荧光基团,包括但不限于Cy3、Cy5、Cy5.5、Cy7、FITC、Alexa 488、Alexa 568、JOE、ROX、罗丹明6G(Rhodamine 6G)、四甲基罗丹明(Tetramethyl rhodamine)、丽丝胺(Lissamine)、德克萨斯红(Texas Red)、BODIPY 576/589、BODIPY 630/650和BODIPY 650/665。在某些实施方案中,荧光基团可组合使用两种以上的上述任何基团。
本发明中,优选地,邻二醇基可切割连接臂通过选自由NH-CO、CO-NH、CO-NH-NH、NH-NH-CO、NH-CO-NH和CO-NH-NH-CO组成的组任何之一与荧光基团连接。
本发明中,“测序”优选指可逆末端终止法测序,其末端终止基团的引物延伸终止功能是可逆的,可以通过一定的化学转变恢复为正常的、可以再次进行引物延伸的基团。所述测序包括但不限于高通量测序。
本发明中,“高通量测序”的具体步骤和方法有多种,在此,仅简单提及下述具体步骤:
1)测序DNA模板及引物的固定;
2)引物延伸:向反应体系加入延伸反应混合液开始进行引物聚合延伸,此混合液主要包括DNA聚合酶(或逆转录酶)及四种不同碱基带有不同颜色荧光的可完全去疤可逆末端终止功能核苷酸;
3)延伸终止:去离子水洗涤,清除延伸反应混合液,终止引物延伸反应;
4)碱基读取:CCD拍照,通过荧光颜色来判定所延伸的碱基的种类;
5)切除连接臂及与其相连的荧光基团:先加入NaIO4溶液切断邻二醇基连接臂去除荧光基团,一定温度下反应一段时间后再用去离子水清洗;然后加入胺类催化剂将剩余的丙醛基完全去除,一定温度下反应一段时间后再用去离子水清洗;
6)重复步骤2-5;
7)序列判读:利用图像分析软件,根据荧光与碱基种类的对应关系,对测序DNA模板进行序列判读。
本发明中,所述步骤2)的DNA聚合酶或逆转录酶包括但不限于以下酶:Taq、REAP 475、EEAP 442、Vent(exo-)、Deep Vent(exo-)、9° Nm、Therminator、Therminator-2、Therminator-3、Bst、Bsu、Klenow、Klenow(exo-)、AffinityScript RT、M-MLV ReverseTranscriptase、ImProm-II Reverse Transcriptase、ThermoScript Reverse Transcriptase、HIV Reverse Transcriptase、Maxima Reverse Transcriptase、ReverAidTM Reverse Transcriptase、SuperScript II Reverse Transcriptase、SuperScript III Reverse Transcriptase、Enhanced Avian Reverse Transcriptase。
本发明中,步骤5)的胺类催化剂可为本领域内通常使用的催化剂,包括但不限于氨基乙酸、吗啉和吡咯烷。可选地,本发明的催化剂可以使用两种以上的上述不同类型。
本发明中,优选地邻二醇基连接臂连于嘧啶碱基的5位和嘌呤碱基的7位上,这两个位点位于DNA双螺旋结构的大沟部位,能接受比较大的荧光修饰基团。本发明设计的连接臂较短,引物延伸聚合一个带有大荧光集团的可逆末端终止功能核苷酸后,DNA的双螺旋结构由于大沟构成的改变而改变,便无法再聚合第二个,从而达到“延伸且只延伸一个”的目的。另外,出于完全去除连接臂的考虑,嘧啶碱基5位和嘌呤碱基的7位C被N所取代。这样,完全消除疤痕以后,DNA双螺旋结构不会因可逆末端终止功能核苷酸在引物上的累积而遭到破坏,从而实现可逆末端终止测序法的长读长。
本发明所涉及的可逆末端终止测序法属于合成测序法,是利用DNA聚合酶的链延伸反应,边合成边测序,包括多步引物延伸、终止、切除操作。具体步骤如下(参见图3):
1)引物延伸:加入DNA聚合酶以及四种不同碱基带有不同颜色荧光的可完全去疤可逆末端终止功能核苷酸后,引物开始进行聚合延伸;
2)延伸终止:由于dNTPs碱基上带有可逆末端终止基团,使得延伸反应只能延伸聚合一个可完全去疤可逆末端终止功能核苷酸;
3)读取荧光颜色:通过读取可逆末端终止功能核苷酸的荧光颜色可以判断出新聚合在引物上的碱基种类;
4)洗除多余可完全去疤可逆末端终止功能核苷酸;
5)使用NaIO4和胺类催化剂完全去除带有连接臂的荧光基团(完全去疤);
6)洗除被切除的带有连接臂的荧光基团;
7)开始第二轮引物延伸反应。
实施例
实施例1:四种可完全去疤可逆末端终止功能核苷酸的具体合成路线
1、可完全去疤dT可逆末端终止功能核苷酸的合成路线
1)烯糖化合物的制备方法
首先,化合物1胸腺嘧啶核苷的5'-位的羟基经保护后得到化合物2。然后,再用对3'-位上的羟基经叔丁基二苯基氯硅烷保护和碱性水解后得到化合物3。接着,再用叔丁基二甲基硅烷对5'-位的羟基进行保护得到化合物4。最后,化合物4的糖苷键在六甲基二硅胺作用下断裂并碱性水解得到烯糖化合物5(图4)。
2)完全去疤dT可逆末端终止功能核苷酸的制备方法
2-脱氧-D-核糖经2,2-二甲氧基丙烷的保护、磷叶利德反应和水解后得到烯醇类化合物7。化合物7再与邻苯二甲酰亚胺偶联和水解得到化合物8。接着,经氨基保护和氧化及水解后得到邻二醇衍生物9,化合物9再经高碘酸钠氧化和硼氢化钠还原得到单羟基衍生物10。化合物10再经溴化后与N3-苯甲酰基-5-碘尿嘧啶偶联和水解得到5-碘尿嘧啶衍生物12。化合物12与烯糖化合物5偶联得到尿嘧啶核苷衍生物13。13经水解后得到化合物14。化合物14核糖环的3'-位的羟基经乙酰基保护后得到中间体15,15经焦磷酸化和水解后得到核苷酸16。最后,化合物16侧链上的氨基与活化的荧光基团结合得到最终产物“可完全去疤dT可逆末端终止功能核苷酸”(图5)。
2、可完全去疤dC可逆末端终止功能核苷酸的制备方法
1)甲苯磺基取代的无疤连接臂的制备
首先,2-脱氧-D-核糖经保护、水解、氧化和还原等反应得到醇类化合物1。然后,用对甲苯磺酰氯(MsCl)对化合物1苯磺酰化后得到目标化合物2(图6)。
2)可完全去疤dC可逆末端终止功能核苷酸的制备
首先,异胞嘧啶(2-氨基-4-羟基嘧啶,3)经碘代和乙酰化后得到化合物4。然后,4与化合物2偶联得到N-取代的5-碘异胞嘧啶衍生物5。5与烯糖化合物6偶联得到核苷类衍生物7。化合物7经水解除去核糖3’-位保护基后得到化合物8。接着,8经保护和水解及核糖环的3’-位乙酰化后得到化合物9。再经焦磷酸酸化和水解后得到伪异胞核苷酸10。最后,化合物10嘧啶环侧链末端的氨基与活化的荧光基团结合得到最终产物“可完全去疤dC可逆末端终止功能核苷酸”(图7)。
3.可完全去疤dA可逆末端终止功能核苷酸的制备方法
首先,化合物1与醇类衍生物2偶联得到化合物3。然后,3再与烯糖化合物4发生核苷化反应得到核苷衍生物5,再经水解和6-位氨解得到7。接着,化合物7核糖环上的两个的羟基经1,1,3,3-四异丙基二硅氧烷保护后得到中间体8。然后,对6-位氨基进行乙酰化和水解掉核糖环上的硅烷保护基得到9,化合物9再经乙酰化、焦磷酸化和水解后得到核苷酸11。最后,化合物11的侧链上的氨基与活化的荧光基团结合得到最终产物“可完全去疤dA可逆末端终止功能核苷酸”(图8)。
4.可完全去疤dG可逆末端终止功能核苷酸的制备方法
首先,嘧啶衍生物1经二甲基缩醛对的2-位氨基缩合和新戊酸氯甲酯对1-位上的亚胺保护后得到中间体2。然后,再经二甲基缩醛缩合和闭环反应得到中间体3。中间体3经碘代后得到化合物4。化合物4与醇衍生物5偶联得到化合物6。然后,再与烯糖化合物7反应的得到核苷衍生物8,再经水解得到9。接着,对化合物9核糖环3’-位的羟基进行乙酰化得到中间体10。10再经焦磷酸酸化和水解后得到核苷酸11。最后,化合物11侧链上的氨基活化的荧光基团结合得到最终产物“可完全去疤dG可逆末端终止功能核苷酸”(图9)。
实施例2:可逆末端终止功能核苷酸的完全去疤实验
可逆末端终止功能核苷酸的完全去疤实验(以ScarlessdT Reversible Terminator的切除实验为例说明,图10)采用两步反应。第一步为切断邻二醇基连接臂去除荧光基团:化合物1通过50mM NaIO4(25℃,5min)氧化其碱基侧链上的邻羟基得到侧链醛基衍生物2;第二步为去除丙醛基而完全去疤:侧链含有醛基的衍生物2在胺类催化剂作用下即可完全除疤,得到化合物3。如下表所示,在较温和的反应条件下(55℃),30分钟内即可以完全去除碱基上的丙醛基,完全去疤率可达98-99%。
表1.5’丙醛基胸腺嘧啶核苷酸的完全去疤实验(离子交换HPLC检测)
注:A:100mM氨乙酸基,55℃;B:500mM吗啉,55℃;C:100mM吡咯烷,55℃。
实施例3:酶的筛选及完全去疤可逆末端终止功能核苷酸的单侧引物延伸终止功能实验
通过单侧引物延伸实验,从多种商业化的DNA聚合酶和逆转录酶中筛选获取了多种高效延伸及有效终止(即~100%“延伸且只延伸一个”)完全去疤可逆末端终止功能胸腺嘧啶核苷酸(T)的酶。用于单侧引物延伸的可完全去疤可逆末端终止功能胞嘧啶核苷酸结构式如图11所示。单侧引物延伸PAGE电泳图如图12所示。
反应步骤如下:首先,将5'端32P放射性标记的引物(2.5pmol)与底物(30pmol)经过变性(95℃,5分钟)退火(缓慢降至室温0.1℃/秒)进行杂交反应;然后向反应体系中加入各种DNA聚合酶及逆转录酶(如附图所示),再加入可完全去疤可逆末端终止功能胞嘧啶核苷酸Scarless dT(100μM)启动反应,反应温度如图所示。反应如附图所示时间后,加入等体积的甲酰胺加样缓冲液(2×)终止反应。上样后进行变性聚病烯酰胺凝胶电泳(16%),随后将凝胶干燥并放射自显影。反应底物(Template)与引物(primer)序列顺序如下:
5'-GCG TAA TAC GAC TCA CTA TGG ACG 引物
CGC ATT ATG CTG AGT GAT ACC TGC AAT GTG CTT CTT CTG-5'底物AA(DNA底物)
电泳结果解析:从商业化的11种DNA聚合酶、10种逆转录酶及两种Taq突变体REAP 475、REAP 442(Chen,F.,Gaucher,E.A.,Leal,N.A.,et al.Proc.Natl.Acad.Sci.USA.2010,107,1948-1953)中筛选获取了13高效延伸及有效终止(即~100%“延伸且只延伸一个”,即在胶图上显示~100%“N+1"条带)完全去疤可逆末端终止功能胸腺嘧啶核苷酸(Scarless dT)的酶。REAP 475最终被选为下一步多步“引物延伸-终止-读取-切除”可逆末端终止测序试验。
实施例4:多步“引物延伸-终止-读取-切除”可逆末端终止测序试验
本实验目的是通过进行多步引物延伸、终止、读取、切除实验来验证完全去疤可逆末端终止功能核苷酸及其酶的测序应用性。我们首先合成如下5’端带有氨基修饰的DNA序列(包括底物及引物),然后通过点样的办法将其固定到醛基修饰的基片上(图13)。具体遵循如下步骤操作:
(i)引物延伸:向上述基片上加入延伸反应混合液,包括REAP 475(50μg/ml)、四种不同碱基带有不同颜色荧光的可完全去疤可逆末端终止功能核苷酸(scarless dT-BODIPY 576/589,scarless dC–Cy3.5,scarless dA-Cy 5,scarless dG–Cy3;浓度均为50μM)、1x Thermopol buffer(New EngalndBiolabs,MA),72℃反应15min开始进行引物聚合延伸。
(ii)延伸终止:用去离子水洗涤基片,清除延伸反应混合液,终止引物延伸反应。
(iii)碱基读取:CCD拍照,通过荧光颜色来判定所延伸的碱基的种类。
(iv)切除连接臂及与其相连的荧光基团:先向基片上加入50mM NaIO4溶液,25℃反应5min,去离子水洗涤基片;然后向基片加入500mM吗啉溶液(pH 9),55℃反应20min,去离子水洗涤基片。
(v)重复步骤i-iv。
(vi)序列判读:利用图像分析软件,根据荧光与碱基种类的对应关系,对测序DNA模板进行序列判读。
(vii)结果评估:10次实验,测序准确率超过95%。
参考本申请的优选技术方案详细描述了本申请,然而,需要说明的是,在不脱离本申请的精神的情况下,本领域技术人员可在上述公开内容的基础上做出任何改造、修饰以及变动。本申请包括上述具体实施方案及其任何等同形式。
- 还没有人留言评论。精彩留言会获得点赞!