酶或非酶生物柴油精制方法与流程
本申请含有计算机可读形式的序列表。该计算机可读形式通过引用结合在此。
技术领域
本发明提供了一种降低生物柴油/脂肪酸烷基酯中游离脂肪酸水平的方法。该方法包括通过以下方式降低油相/轻相中游离脂肪酸的量
i)使所述游离脂肪酸和/或所述脂肪酸原料与醇在一种或多种液体脂肪分解酶的存在下进行反应以产生脂肪酸烷基酯;和/或
ii)使所述游离脂肪酸和/或所述脂肪酸原料与醇在一种或多种非酶催化剂的存在下进行反应以产生脂肪酸烷基酯。
背景技术:
可以将脂肪酸烷基酯在标准的柴油发动机中用作燃料,即生物柴油。生物柴油可以单独使用、或者与石化柴油混合使用。目前因为其环境效益,生物柴油已经变得更有吸引力。
虽然目前生物柴油主要是化学产生的(使用例如NaOH和/或甲醇钠作为催化剂),但是有几个相关的问题限制了它的发展,例如由于高含量的游离脂肪酸引起的油的预处理、为了在反应中的高醇盈余的需求将化学催化剂从酯和甘油相中去除、和在甘油回收期间去除无机盐。
通过使用脂肪分解酶作为催化剂,极大地防止了由化学催化剂导致的这些劣势,并且在最近这些年,在生产生物柴油的酯交换中使用脂肪酶引起了人们的兴趣。
通过酶促生物转换产生的生物柴油(与化学转换相比)更加环保。然而,有非常少的例外,目前酶技术未用于商业规模的生物柴油生产。
使用液体酶来进行脂肪酸烷基酯的酶促生产工艺描述于例如,WO 2006/072256,Lv等人(Process Biochemistry[工艺生物化学]45(2010)446-450)和WO 2012/098114中。
在产生脂肪酸烷基酯或生物柴油的方法中,将脂肪酸原料与醇(典型地甲醇)反应以产生脂肪酸烷基酯和甘油。在脂肪酸原料已经与醇反应产生脂肪酸烷基酯之后,油相/轻相含有残留的游离脂肪酸。通常,游离脂肪酸的存在是不希望的,并且游离脂肪酸的水平必须尽可能降低:例如,欧洲生物柴油标准要求游离脂肪酸的水平低于0.25%(w/w)。用于酯化基于甘油酯的油中的游离脂肪酸的树脂的工业用途作为碱性化学生物柴油方法的预处理步骤而众所周知。然而,将甲基酯中的游离脂肪酸酯化成低于0.25%的FFA水平是非常具有挑战性的,这是由于较高的水活度以及甲基酯的吸湿性。据普遍认识,为了去除游离脂肪酸而对脂肪酸甲酯进行额外的纯化或“精制”会导致脂肪酸甲酯的损失。因此,通常在生产产量与游离脂肪酸水平之间进行权衡。
因此,需要更有效的生产具有降低的游离脂肪酸含量的脂肪酸烷基酯或生物柴油的方法。
技术实现要素:
本发明提供了一种降低生物柴油/脂肪酸烷基酯中游离脂肪酸水平的方法,所述方法包括
i)提供一种组合物,该组合物包含
a.含有脂肪酸烷基酯、游离脂肪酸和任选地脂肪酸原料的油相/轻相;和
b.含有醇和水的水相/重相;
ii)减少所述组合物中的水量,例如将该水相/重相的水含量降低至按水相/重相的重量计在0-15%的范围内和/或将该油相/轻相的水含量降低至在200-600ppm的范围内;
并且然后减少该油相/轻相中的游离脂肪酸的量和任选地所述脂肪酸原料的量
iii)使所述游离脂肪酸和/或所述脂肪酸原料与醇在一种或多种液体脂肪分解酶的存在下进行反应以产生脂肪酸烷基酯;和/或
iv)使所述游离脂肪酸和/或所述脂肪酸原料与醇在一种或多种非酶催化剂的存在下进行反应以产生脂肪酸烷基酯。
附图说明
图1:显示通过脂肪酸或脂肪酸原料与醇的酶催化酯交换反应来制造脂肪酸烷基酯的方法的示意图。
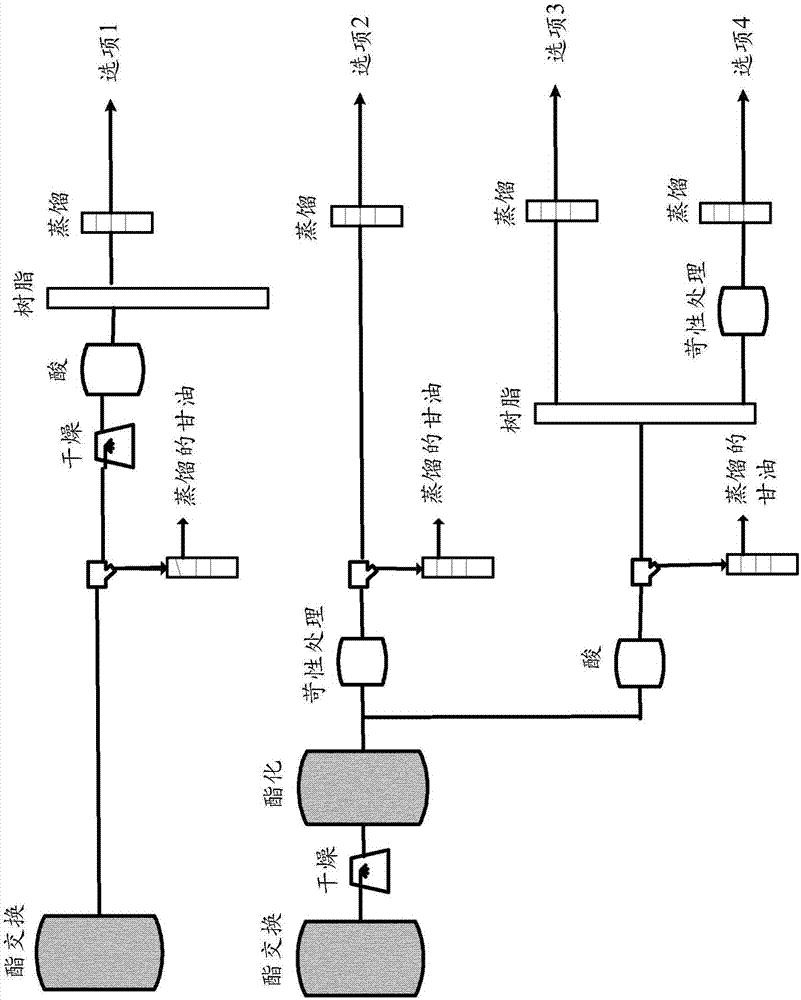
图2显示本发明的四个主要实施例。
图3-9显示当使用根据本发明的方法来产生具有降低的游离脂肪酸含量的脂肪酸甲酯时获得的结果。
将这些图包括在内仅仅出于说明的目的,并且决不应被理解为限制本发明。
具体实施方式
定义
生物柴油:短链醇的脂肪酸烷基酯(FAAE)(如脂肪酸甲酯(FAME)和脂肪酸乙酯(FAEE))也称为生物柴油,因为它们可用作石化柴油的添加剂或替代物。
醇:用于本发明的方法中的醇优选是具有1至5个碳原子(C1、C2、C3、C4、或C5)的短链醇。
脂肪酸原料:术语“脂肪酸原料”在本文中定义为包含任何脂肪酸来源(包括三酸甘油酯、二酸甘油酯、单酸甘油酯或其任何组合)的底物。原则上,任何包含脂肪酸的植物或动物来源的油和脂肪可以在本发明的方法中被用作底物来生产脂肪酸烷基酯。
脂肪分解酶
应用于本发明的方法中的一种或多种脂肪分解酶选自脂肪酶、磷脂酶、角质酶、酰基转移酶、或者脂肪酶、磷脂酶、角质酶和酰基转移酶中一种和多种的混合物。该一种或多种脂肪分解酶选自在EC 3.1.1、EC 3.1.4、和EC 2.3中的酶。该一种或多种脂肪分解酶也可以是一种或多种脂肪酶的混合物。该一种或多种脂肪分解酶可以包括脂肪酶和磷脂酶。该一种或多种脂肪分解酶包括EC 3.1.1.3的脂肪酶。该一种或多种脂肪分解酶包括对三-、二-、和单酸甘油酯具有活性的脂肪酶。
脂肪酶:合适的脂肪分解酶可以是具有脂肪酶活性的多肽,例如,选自如在WO 88/02775中披露的南极假丝酵母(Candida antarctica)脂肪酶A(CALA);如在WO 88/02775中披露并示于WO 2008065060的SEQ ID NO:1中的南极假丝酵母(C.antarctica)脂肪酶B(CALB);在EP 258 068中披露的疏棉状嗜热丝孢菌(Thermomyces lanuginosus)(之前为柔毛腐质霉(Humicola lanuginosus))脂肪酶;在WO 2000/60063或WO 1995/22615中披露的疏棉状嗜热丝孢菌变体(具体地,示于WO 95/22615的SEQ ID NO:2的位置1-269处的脂肪酶)、Hyphozyma属脂肪酶(WO 98/018912)、和米黑根毛霉脂肪酶(在WO 2004/099400中的SEQ ID NO:5));来自产碱假单胞菌或类产碱假单胞菌(EP 218 272)、洋葱假单胞菌(EP 331 376)、施氏假单胞菌(GB 1,372,034)、萤光假单胞菌、假单胞菌属物种菌株SD 705(WO 95/06720和WO 96/27002)、威斯康星假单胞菌(P.wisconsinensis)(WO 96/12012)的脂肪酶;芽孢杆菌属脂肪酶,例如来自枯草芽孢杆菌(Dartois等人(1993),Biochemica et Biophysica Acta[生物化学与生物物理学报],1131,253-360)、嗜热脂肪芽抱杆菌(JP 64/744992)或短小芽孢杆菌(WO 91/16422)。还优选的是来自任何以下生物体的脂肪酶:尖孢镰刀菌、包蜕膜犁头酶(Absidia reflexa)、多枝犁头霉(Absidia corymbefera)、米黑根毛霉、德氏(米)根霉、黑曲霉、塔宾曲霉、异孢镰刀菌、米曲霉、卡门柏青霉菌、臭曲霉、黑曲霉、米曲霉和疏棉状嗜热丝孢菌,例如,选自在WO 2004/099400中的SEQ ID NO:1-15中任一个的脂肪酶。
与本发明相关的有用的脂肪酶是与SEQ ID NO:2的成熟多肽,即与示于WO 95/22615的SEQ ID NO:2的位置1-269处的多肽、或与示于WO 2008/065060的SEQ ID NO:1的多肽具有至少60%,例如至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%、或甚至100%序列同一性的脂肪酶。
适合在本发明的方法中使用的商业脂肪酶制剂包括LIPOZYME CALB L、LIPOZYME(R)TL 100L、CALLERATM TRANS和Transform(全部都可从诺维信公司(Novozymes A/S)获得)。
具体地有用的脂肪酶可以选自下组,该组由以下各项组成
(a)包含SEQ ID NO:1或SEQ ID NO:2中所示的氨基酸序列或由其组成的多肽;
(b)是SEQ ID NO:1或2中所示的氨基酸序列的子序列的多肽;
(c)与在(a)和(b)中定义的多肽中的任一种具有至少60%,如例如至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%序列同一性的多肽。
在(c)中所示的脂肪酶可以是在SEQ ID NO:1中所示的氨基酸序列的变体,其中该多肽包含以下取代T231R和N233R。
在项目(c)中所示的脂肪酶可以具有如下氨基酸序列,该氨基酸序列与SEQ ID NO:1或2的多肽相差多达40个氨基酸,例如,1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、或40个。
该脂肪酶可以是亲本脂肪酶的变体,该变体具有脂肪酶活性并且与SEQ ID NO:1具有至少60%,如至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、如至少96%、至少97%、至少98%、或至少99%、但小于100%的序列同一性,并且包含在对应于SEQ ID NO:1的T231R+N233R的位置处以及D96E、D111A、D254S、G163K、P256T、G91T、G38A、D27R、和N33Q中至少一个或多个(例如,若干个)的位置处的取代。
在进一步的实施例中,该脂肪酶是如下变体,该变体具有脂肪酶活性并且与SEQ ID NO:1具有至少60%,如至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%统一性、至少96%、至少97%、至少98%、或至少99%、但小于100%的序列同一性,并且包含在对应于SEQ ID NO:1的T231R+N233R的位置处以及D96E、D111A、D254S、G163K、P256T、G91T、G38A、D27R、和N33Q中的选自以下组的至少一个或多个(例如,若干个)的位置处的取代:
a)D96E T231R N233R;
b)N33Q D96E T231R N233R;
c)N33Q T231R N233R;
d)N33Q D111A T231R N233R;
e)N33Q T231R N233R P256T;
f)N33Q G38A G91T G163K T231R N233R D254S;
g)N33Q G38A G91T D96E D111A G163K T231R N233R D254S P256T;
h)D27R N33Q G38A D96E D111A G163K T231R N233R D254S P256T;
i)D27R N33Q G38A G91T D96E D111A G163K T231R N233R P256T;
j)D27R N33Q G38A G91T D96E D111A G163K T231R N233R D254S;
k)D27R G38A G91T D96E D111A G163K T231R N233R D254S P256T;
l)D96E T231R N233R D254S;
m)T231R N233R D254S P256T;
n)G163K T231R N233R D254S;
o)D27R N33Q G38A G91T D96E G163K T231R N233R D254S P256T;
p)D27R G91T D96E D111A G163K T231R N233R D254S P256T;
q)D96E G163K T231R N233R D254S;
r)D27R G163K T231R N233R D254S;
s)D27R G38A G91T D96E D111A G163K T231R N233R D254S;
t)D27R G38A G91T D96E G163K T231R N233R D254S P256T;
u)D27R G38A D96E D111A G163K T231R N233R D254S P256T;
v)D27R D96E G163K T231R N233R D254S;
w)D27R D96E D111A G163K T231R N233R D254S P256T;
x)D27R G38A D96E G163K T231R N233R D254S P256T。
例如,在WO 2015/049370中提供了亲本脂肪酶的这样的有用的变体。
脂肪酶活性:
在本发明的上下文中,可以使用三丁酸酯作为底物将该脂解活性确定为脂肪酶单位(LU)。该方法是基于三丁酸甘油酯通过该酶的水解,并且将在水解过程中维持pH恒定的碱性消耗登记为时间的函数
根据本发明,一个脂肪酶单位(LU)可以被定义为,在标准条件(即在30℃;pH 7.0;具有0.1%(w/v)阿拉伯胶作为乳化剂和0.16M三丁酸甘油酯作为底物)下,每分钟释放1微摩尔可滴定丁酸的酶量。
可替代地,脂解活性可以被确定为长链脂肪酶单位(LCLU),使用底物pNP-棕榈酸盐(C:16),当在pH 8.0在30℃下孵育时,该脂肪酶水解该酯键并释放pNP,该pNP是黄色的并且可以在405nm处被检测到。
磷脂酶:
所述一种或多种脂肪分解酶可以包括具有磷脂酶活性、优选地磷脂酶A1、磷脂酶A2、磷脂酶B、磷脂酶C、磷脂酶D、溶血-磷脂酶活性、和/或其任何组合的多肽。在本发明的方法中,所述一种或多种脂肪分解酶可以是磷脂酶,例如,单一磷脂酶,如A1、A2、B、C、或D;两种或更多种磷脂酶,如,两种磷脂酶(包括但不限于,A型和B型两者、A1型和A2型两者、A1型和B型两者、A2型和B型两者、A1型和C型两者、A2型和C型两者);或两种或更多种相同类型的不同磷脂酶。
所述一种或多种脂肪分解酶可以是具有磷脂酶活性以及具有酰基转移酶活性的多肽,例如,选自披露于WO 2003/100044、WO 2004/064537、WO 2005/066347、WO 2008/019069、WO 2009/002480、和WO 2009/081094中的这些多肽中的多肽。例如可以通过在WO 2004/064537中描述的测定确定酰基转移酶活性。
该磷脂酶可以选自披露于WO 2008/036863和WO 20003/2758中的多肽。合适的磷脂酶制剂是PURIFINE(R)(可从范恩尼姆公司(Verenium)获得)和LECITASE(R)ULTRA(可从诺维信公司获得)。具有酰基转移酶活性的酶可作为商业酶制剂LYSOMAX(R)OIL(可从丹尼斯科公司(Danisco A/S)获得)而获得。
角质酶:所述一种或多种脂肪分解酶可以包括具有角质酶活性的多肽。
例如该角质酶可以选自披露于WO 2001/92502中的多肽,具体地是披露于实例2中的特异腐质霉角质酶变体。
优选地,所述一种或多种脂肪分解酶是与上述脂肪酶、磷脂酶、角质酶、和酰基转移酶中的任一种具有至少60%、至少70%、至少80%、至少90%、至少95%、至少96%、至少97%、至少98%、或甚至至少99%同一性的酶。
在一个实施例中,所述一种或多种脂肪分解酶与WO 95/22615的SEQ ID NO:2的位置1-269处示出的氨基酸序列具有至少60%、至少70%、至少80%、至少90%、至少95%、至少96%、至少97%、至少98%、至少或甚至至少99%同一性。
酶来源和配制品:在本发明的方法中使用的一种或多种脂肪分解酶可以源自或可获得自本文提及的来源中的任一种。术语“源自”在本发明的上下文中意指该酶可以从其天然存在的生物体中分离,即该酶的氨基酸序列的身份(identity)与天然的酶相同。术语“源自”还意指这些酶可以在宿主生物体中重组产生,该重组产生的酶具有与天然的酶相同的身份,或具有修饰的氨基酸序列,例如,具有一个或多个缺失、插入和/或取代的氨基酸,即,重组产生的酶是天然的氨基酸序列的突变体和/或片段。天然的酶的含义中包含天然的变体。此外,术语“源自”包括通过例如肽合成而合成产生的酶。术语“源自”还涵盖已经通过例如糖基化、磷酸化等在体内或体外修饰的酶。术语“可获得的”在本发明的上下文中意指该酶与天然的酶具有相同的氨基酸序列。该术语涵盖已经从生物体中分离的酶(在该生物体中该酶天然地存在,或在该生物体中该酶在相同类型的或其他类型的生物体中重组地表达),或通过例如肽合成而合成产生的酶。对于重组产生的酶,术语“可获得的”和“源自”是指酶的身份而不是重组产生该酶的宿主生物体的身份。
因此,可以通过使用任何合适的技术从微生物获得所述一种或多种脂肪分解酶。例如,酶制剂可以通过发酵合适的微生物并且随后通过本领域已知的方法从所得的发酵液或微生物中分离酶制剂而获得。该酶还可以通过使用重组DNA技术而获得。这样的方法通常包括培养用重组DNA载体转化的宿主细胞,该DNA载体包含编码所讨论的酶的DNA序列,并且该DNA序列与适当的表达信号可操作地连接,这样使得该DNA序列能在允许酶表达的条件下在培养基中表达该酶,并且从培养物中回收该酶。还可以将DNA序列掺入宿主细胞的基因组中。DNA序列可以是基因组、cDNA或合成来源的、或它们的任何组合,并且可以按照本领域已知的方法进行分离或合成。
该一种或多种脂肪分解酶可以应用于任何合适的配制品中,例如,呈冻干粉末或在水性溶液中。
序列同一性
两个氨基酸序列之间或两个核苷酸序列之间的关联度通过参数“序列同一性”来描述。
出于本发明的目的,使用如在EMBOSS软件包(EMBOSS:欧洲分子生物学开放软件包(EMBOSS:The European Molecular Biology Open Software Suite),Rice等人,2000,Trends Genet.[遗传学趋势]16:276-277)(优选5.0.0版或更新版)的尼德尔(Needle)程序中所实施的尼德尔曼-翁施算法(Needleman和Wunsch,1970,J.Mol.Biol.[分子生物学杂志]48:443-453)确定两个氨基酸序列之间的序列同一性。使用的参数是缺口开放罚分10、缺口扩展罚分0.5以及EBLOSUM62(BLOSUM62的EMBOSS版本)取代矩阵。将标记为“最长同一性”的尼德尔输出(使用-非简化(nobrief)选项获得)用作百分比同一性并且是如下计算的:
(相同的残基x 100)/(比对的长度-在比对中的空位总数)
方法设计
本发明提供了一种降低生物柴油/脂肪酸烷基酯中游离脂肪酸水平的方法,所述方法包括
i)提供一种组合物,该组合物包含
a.含有脂肪酸烷基酯、游离脂肪酸和任选地脂肪酸原料的油相/轻相;以及
b.含有醇和水的水相/重相;
ii)减少所述组合物中的水量,例如将该水相/重相的水含量降低至按该水相/重相的重量计在0-15%的范围内和/或将该油相/轻相的水含量降低至在200-600ppm的范围内;
并且然后减少该油相/轻相中的游离脂肪酸的量和任选地所述脂肪酸原料的量
iii)使所述游离脂肪酸和/或所述脂肪酸原料与醇在一种或多种液体脂肪分解酶的存在下进行反应以产生脂肪酸烷基酯;和/或
iv)使所述游离脂肪酸和/或所述脂肪酸原料与醇在一种或多种非酶催化剂的存在下进行反应以产生脂肪酸烷基酯。
具体地,根据本发明的方法可以包括
i)提供一种组合物,该组合物包含
a.含有脂肪酸烷基酯、游离脂肪酸和任选地脂肪酸原料的油相/轻相;以及
b.含有醇和水的水相/重相;
ii)减少所述组合物中的水量,例如将该水相/重相的水含量降低至按水相/重相的重量计在0-15%的范围内和/或将该油相/轻相的水含量降低至在200-600ppm的范围内;
iii)通过使游离脂肪酸和/或脂肪酸原料与醇在一种或多种液体脂肪分解酶的存在下进行反应产生脂肪酸烷基酯,减少在该油相/轻相中的所述游离脂肪酸的量和任选地所述脂肪酸原料的量;
并且,任选地
iv)通过使游离脂肪酸和/或脂肪酸原料与醇在一种或多种非酶催化剂的存在下进行反应产生脂肪酸烷基酯,进一步减少在该油相/轻相中的所述游离脂肪酸的量和任选地所述脂肪酸原料的量。
可以通过如下反应来提供i)中的组合物,在该反应中将游离脂肪酸和/或脂肪酸原料与醇反应以产生脂肪酸烷基酯直到该反应已基本达到平衡。具体而言,“平衡”可以被定义为反应混合物中的游离脂肪酸没有进一步净减少的点。因此,出于本发明的目的,可以具体地通过如下反应来提供i)中的组合物,该反应已经被允许进行到游离脂肪酸没有进一步净减少或基本没有进一步净减少的点。
可以具体地通过如下反应来提供i)中的组合物,在该反应中所述脂肪酸原料与醇在对应于按水相/重相的重量计的0-70%的量的甘油、对应于按水相/重相的重量计的10%-70.0%的量的水、以及在按水相/重相的重量计的10%-50%范围内的量的醇(如甲醇)存在下进行反应。
在步骤ii)中,该水相/重相的含水量可以降低至按水相/重相的重量计2%-15%的范围内,如按水相/重相的重量计5%-15%的范围内,如按水相/重相的重量计7%-15%的范围内,如按水相/重相的重量计10%-15%的范围内,如按水相/重相的重量计0-10%的范围内,如按水相/重相的重量计2%-10%的范围内,如按水相/重相的重量计5%-10%的范围内,如按水相/重相的重量计0-9%的范围内,如按水相/重相的重量计2%-9%的范围内,或如按水相/重相的重量计5%-9%的范围内。
该油相/轻相的含水量也可以降低至在200-600ppm的范围内,如在300-600ppm、400-600ppm、200-500ppm、200-400ppm的范围内,或如在300-500ppm的范围内。
甘油含量可以相当于按水相/重相的重量计的0至60%,如0至50%、0至40%、0至30%、0至20%、2%至60%、5%至60%、10%至60%、20%至60%、30%至60%、30%至50%、5%至50%、10%至50%、20%至50%、30%至50%、2%至40%、5%至40%、10%至40%、20%至40%、2%至30%、5%至30%、或如相当于按水相/重相的重量计的10%至30%。
含水量可以相当于按水相/重相的重量计的10%至60%,如10%至50%、10%至40%、10%至30%、10%至20%、12%至60%、15%至60%、20%至60%、30%至60%、30%至50%、10%至50%、20%至50%、30%至50%、10%至40%、20%至40%,或如相当于按水相/重相的重量计的10%至30%。如技术人员将理解的,水相/重相中的水含量取决于所使用的脂肪酸原料:如果主要使用游离脂肪酸作为底物,则水相/重相将主要包含水,然而使用具有较大量的结合的甘油的脂肪酸原料将增加水相/重相中的甘油量并降低水量。
优选地,醇(如甲醇)的量是在按水相/重相的重量计的10%至45%的范围内,如在10%至40%、10%至35%、10%至30%、10%至25%、10%至20%、15%至50%、15%至45%、15%至40%、15%至35%、15%至30%、15%至25%、20%至50%、20%至45%、20%至40%、20%至35%、20%至30%、25%至50%、25%至45%、25%至40%的范围内,或如在按水相/重相的重量计的25%至35%的范围内。
在根据本发明的方法中,可以通过如下反应来提供i)中的组合物,该反应包括使游离脂肪酸和/或脂肪酸原料与醇进行反应直至所述脂肪酸原料中的至少90%(w/w)或例如至少95%(w/w)的脂肪酸酰基基团或游离脂肪酸已转化为脂肪酸烷基酯。
在本发明的一些实施例中,使步骤iii)和/或步骤iv)中的所述脂肪酸和/或所述脂肪酸原料与醇进行反应直至所述脂肪酸原料中的至少80%(w/w)、至少85%(w/w)、至少90%(w/w)或如至少95%(w/w)的所述游离脂肪酸和/或所述脂肪酸酰基基团已转化为脂肪酸烷基酯。
优选地,通过如下反应提供步骤i)中的组合物,在该反应中所述一种或多种脂肪分解酶是脂肪酶。上文提供了优选的脂肪酶。
具体地可以通过如下反应来提供i)中的组合物,在该反应中所述一种或多种脂肪分解酶的总量是在0.005-5g酶蛋白(EP)/kg油相/轻相或脂肪酸原料的范围内,如在0.005-2.5g EP/kg油相/轻相或脂肪酸原料、0.005-1g EP/kg油相/轻相或脂肪酸原料、0.005-0.75g EP/kg油相/轻相或脂肪酸原料、0.005-0.5g EP/kg油相/轻相或脂肪酸原料、0.005-0.25g EP/kg油相/轻相或脂肪酸原料、0.005-0.1g EP/kg油相/轻相或脂肪酸原料、0.005-0.075g EP/kg油相/轻相或脂肪酸原料、0.005-0.05g EP/kg油相/轻相或脂肪酸原料、0.005-0.025g EP/kg油相/轻相或脂肪酸原料、0.005-0.01g EP/kg油相/轻相或脂肪酸原料、0.01-5g EP/kg油相/轻相或脂肪酸原料、0.02-5g EP/kg油相/轻相或脂肪酸原料、0.03-5g EP/kg油相/轻相或脂肪酸原料、0.04-5g EP/kg油相/轻相或脂肪酸原料、0.05-5g EP/kg油相/轻相或脂肪酸原料、0.06-5g EP/kg油相/轻相或脂肪酸原料、0.07-5g EP/kg油相/轻相或脂肪酸原料、0.08-5g EP/kg油相/轻相或脂肪酸原料、0.09-5g EP/kg油相/轻相或脂肪酸原料、0.1-5g EP/kg油相/轻相或脂肪酸原料、0.2-5g EP/kg油相/轻相或脂肪酸原料、0.3-5g EP/kg油相/轻相或脂肪酸原料、0.4-5g EP/kg油相/轻相或脂肪酸原料、0.5-5g EP/kg油相/轻相或脂肪酸原料、0.6-5g EP/kg油相/轻相或脂肪酸原料、0.7-5g EP/kg油相/轻相或脂肪酸原料、0.8-5g EP/kg油相/轻相或脂肪酸原料、0.9-5g EP/kg油相/轻相或脂肪酸原料、1-5g EP/kg油相/轻相或脂肪酸原料、2-5g EP/kg油相/轻相或脂肪酸原料、3-5g EP/kg油相/轻相或脂肪酸原料、4-5g EP/kg油相/轻相或脂肪酸原料、0.01-4g EP/kg油相/轻相或脂肪酸原料、0.02-3g EP/kg油相/轻相或脂肪酸原料、0.03-2g EP/kg油相/轻相或脂肪酸原料、0.04-1g EP/kg油相/轻相或脂肪酸原料、0.05-0.9g EP/kg油相/轻相或脂肪酸原料、0.06-0.8g EP/kg油相/轻相或脂肪酸原料、0.07-0.7g EP/kg油相/轻相或脂肪酸原料、0.08-0.6g EP/kg油相/轻相或脂肪酸原料、0.09-0.5g EP/kg油相/轻相或脂肪酸原料、0.1-0.4g EP/kg油相/轻相或脂肪酸原料、0.1-0.3g EP/kg油相/轻相或脂肪酸原料的范围内,或如在0.1-0.25g EP/kg油相/轻相或脂肪酸原料的范围内。
在该方法的步骤ii)中,可以通过应用热量(如通过对流、传导和/或辐射)减少水的量。
具体地,可以在步骤ii)中使用气流来将所述水作为湿气去除
在替代性实施例中,在步骤ii)中使用真空来将所述水作为湿气去除。
在目前优选的实施例中,在步骤ii)中通过急骤干燥来减少水的量。
在根据本发明的方法中,步骤iii)中的醇的量可以相当于按油相/轻相的重量计的5%-10%,如6%至10%、7%至10%、8%至10%、5%至9%、5%至8%,或如相当于按油相/轻相的重量计的5%至7%。
步骤iv)中的醇的量可以相当于按油相/轻相的重量计的10%至25%,例如11%至25%、12%至25%、13%至25%、14%至25%、15%至25%、16%至25%、17%至25%、18%至25%、19%至25%、20%至25%、10%至24%、10%至23%、10%至22%、10%至21%、10%至20%、10%至19%、10%至18%、10%至17%、10%至16%、10%至15%,或如相当于按油相/轻相的重量计的12%至15%。
在根据本发明的方法中,步骤iv)可以包括在进一步减少游离脂肪酸的量和任选地脂肪酸原料的量之前,将水相/重相与油相/轻相分离。
根据本发明的方法中的步骤iv)的持续时间可以为0.5-7小时,如0.5-6小时、0.5-5小时、0.5-4小时、0.5-3小时、0.5-2小时、0.5-1小时、1-7小时、2-7小时、3-7小时、或如4-7小时。
步骤iii)中的一种或多种脂肪分解酶可以具体地是脂肪酶或者一种或多种脂肪酶,如之前上文所披露的脂肪酶中的任何一种。
步骤iii)中的所述一种或多种脂肪分解酶的总量可以是在0.01-0.10g酶蛋白(EP)/kg油相/轻相的范围内,或如在0.02-0.10g EP/kg油相/轻相、0.03-0.01g EP/kg油相/轻相、0.04-0.10g EP/kg油相/轻相、0.05-0.1g EP/kg油相/轻相、0.06-0.1g EP/kg油相/轻相或脂肪酸原料、0.07-0.1g EP/kg油相/轻相、0.08-0.01g EP/kg油相/轻相、0.01-0.09g EP/kg油相/轻相、0.01-0.08g EP/kg油相/轻相、0.01-0.07g EP/kg油相/轻相、0.01-0.06g EP/kg油相/轻相、0.01-0.05g EP/kg油相/轻相、0.01-0.04g EP/kg油相/轻相、0.01-0.03g EP/kg油相/轻相、0.02-0.08g EP/kg油相/轻相或脂肪酸原料、或如0.03-0.06g EP/kg油相/轻相的范围内。
在根据本发明的方法中,步骤iv)中使用的一种或多种非酶催化剂可以选自下组,该组由以下各项组成:酸催化剂(如磺酸、硫酸、磷酸和盐酸)和碱催化剂(如金属醇盐(例如醇钠或醇钾))。在目前优选的实施例中,该催化剂是磺酸。
在根据本发明的具体实施例中,步骤v)中的一种或多种非酶催化剂被固定在固体树脂如多孔的聚合物基树脂上。可商购获得的这样的树脂的实例是来自朗盛公司(Lanxess)的Lewatit GF 101。
步骤iv)中的反应可以在含有一种或多种固定化非酶催化剂的树脂床或柱、搅拌反应器或连续搅拌反应器中进行。具体地,使用连续搅拌的反应器或者树脂床或柱提供了以下优势:该反应可以作为连续反应进行。
如果选择以分批法运行该反应,则可以使用常规的搅拌反应器。可替代地,可以采用具有集成的除水系统的更复杂的反应器,如气漏式分批反应器(air bobbled batch reactor)。这样的复杂反应器将允许在整个反应过程中连续地去除水。
然而,本发明的一个主要优势是使用一个主要树脂酯化步骤,而不使用任何具有集成除水系统的复杂反应器。在如本申请中阐述的连续搅拌反应器或者树脂床或柱中应用步骤iv)中的一种或多种非酶催化剂,允许在酯化过程期间进行简单的连续过程而不除水,或者至少没有大量的水去除。
将固体树脂优选地填装在至少1米的高度,如至少1.5米、至少2米、至少2.5米、或如至少3米的高度的树脂床或柱中。特别优选的柱具有从1-3米,如从1-2.5米、从1-2米、从1-1.5米的高度。
根据其中将树脂填装在树脂床或柱中的实施例,树脂上的保持时间优选地在1-4小时的范围内,如1.5-4小时、1.5-3小时、2-3小时或者优选地在2.2-2.4小时的范围内。
步骤iv)可以在加压系统中在75℃-95℃范围内的温度下进行,如在80℃-95℃、85℃-95℃、90℃-95℃、75℃-90℃、75℃-85℃、75℃-80℃的范围内,或者如在80℃-90℃的范围内。
在根据本发明的方法的各个步骤中使用的醇优选是C1-C5醇,更优选是乙醇或甲醇。
根据本发明使用的脂肪酸原料可以源自于以下中的一种或多种:海藻油;低芥酸菜籽油(canola oil);椰子油;蓖麻油;椰子油;椰子核油;玉米油;酒糟玉米油;棉花籽油;亚麻油;鱼油;葡萄籽油;大麻油;麻疯果油;荷荷芭油;芥菜油;低芥酸菜籽油;棕榈油;棕榈硬脂;棕榈油精;棕榈仁油;花生油;菜籽油;米糠油;红花油;大豆油;向日葵油;妥尔油;来自盐生植物的油;和/或动物脂肪,包括来自猪、牛和羊的油脂、猪油、鸡脂肪、鱼油;棕榈油游离脂肪酸馏出物;豆油游离脂肪酸馏出物;皂原料脂肪酸材料;黄色油脂;和棕色油脂或其任何组合。
在根据本发明的方法中,步骤iii)或iv)之后可以是如下步骤:在该步骤中在所述醇/所述轻相的存在下,通过用一种或多种碱性试剂处理在该油相/轻相中由剩余的游离脂肪酸形成皂/盐。
所述一种或多种碱性试剂能以以下量添加,该量相当于游离脂肪酸的量的1.0-2.0摩尔当量,如1.2-2.0摩尔当量、1.3-2.0摩尔当量、1.4-2.0摩尔当量、1.5-2.0摩尔当量、1.6-2.0摩尔当量、1.7-2.0摩尔当量、1.8-2.0摩尔当量、1.0-0.9摩尔当量、1.0-0.8摩尔当量、1.0-0.7摩尔当量、1.0-0.6摩尔当量、1.0-0.5摩尔当量、1.0-0.4摩尔当量、1.0-0.3摩尔当量、或者如游离脂肪酸的量的1.3-1.8摩尔当量。
用一种或多种碱性试剂处理可以包括使该油相/轻相和任选的所述水相/亲水相与碱性试剂或碱进行接触,该碱性试剂或碱选自KOH或NaOH或其混合物。
用一种或多种碱性试剂处理可以优选地在35℃至70℃的范围内,如在40℃至70℃的范围内、在45℃至70℃的范围内、在50℃至70℃的范围内、在55℃至70℃的范围内、或如在35℃至65℃的范围内的温度下进行。
该碱性试剂可以具体地是甲醇钠或甲醇钾或这两者的混合物。
根据本发明的方法可以包括如下步骤:通过使该皂/脂肪酸盐进行酸化,如通过用酸化学计量滴定皂/脂肪酸盐以产生游离脂肪酸,如通过使该皂/脂肪酸盐与H3PO4和/或H2SO4接触,降低该组合物中皂/脂肪酸盐的量。
所述减少皂/脂肪酸盐的量的步骤可以具体地在步骤iv)之前进行。
根据本发明的方法可以进一步包括将含有脂肪酸烷基酯的油相/轻相与亲水相/重相分离。
如技术人员将认识到,可以通过重力沉降、倾析和/或离心将油相/轻相与亲水相/重相分离。
根据本发明的方法可以包括干燥所述甘油以从甘油中去除例如水和醇,如甲醇或如本文所披露的任何其他C1-C5醇。
优选地,将该甘油进行纯化,如通过干燥和/或去除醇以产生如下组合物:其中甘油的含量高于95%(w/w),如高于97%(w/w)、高于97.5%(w/w)、高于98%(w/w)、高于98.5%(w/w)、高于99%(w/w)、高于99.5%(w/w)、高于99.75%(w/w)、高于99.8%(w/w)或高于99.9%(w/w)。
具体地,该甘油可以进行热-真空蒸馏。
根据本发明的方法可以包括使脂肪酸烷基酯进行蒸馏,如热-真空蒸馏,其中将脂肪酸烷基酯进行蒸发并随后浓缩。
在具体的实施例中,将脂肪酸烷基酯在240℃-260℃下进行热-真空蒸馏。
根据本发明提供的方法的一个优点是,除了如上所阐述的蒸馏之外,纯化脂肪酸烷基酯(包括在步骤iii)和/或iv)中产生的任何脂肪烷基酯)是不必要的并且可以被避免。然而,如果仍希望的话,脂肪酸烷基酯可以进行进一步纯化。
所述纯化可以通过使脂肪酸烷基酯经受水洗来进行。
具体地,可以通过允许脂肪酸甲酯沉降(如通过重力沉降),并且然后使沉降的脂肪酸烷基酯经受水洗来进行纯化。
根据本发明的方法可以是分批法,如以下方法,在该方法中分批进行步骤i)、ii)和iii)的全部或者步骤i)、ii)和iv)的全部。可替代地,该方法可以是半连续的,如以下方法,其中以连续方式进行步骤i)、ii)和iii)中的一个或多个但不是全部,或其中以连续方式进行步骤i)、ii)和iv)中的一个或多个但不是全部。优选地,该方法是连续方法,其中以连续方式进行步骤i)、ii)和iii)的全部或者步骤i)、ii)和iv)的全部。
在根据本发明的具体实施例中,它们在图2中被示为“选项1”,根据本发明的方法包括
i)提供一种组合物,该组合物包含
a.含有脂肪酸烷基酯、游离脂肪酸和任选地脂肪酸原料的油相/轻相;以及
b.含有醇和水的水相/重相;
ii)将含有该脂肪酸烷基酯的该油相/轻相与该亲水相/重相分离;并且
iii)降低该油相/轻相的含水量至在200-600ppm的范围内;
iv)通过使皂/脂肪酸盐进行酸化来产生游离脂肪酸,如通过使该皂/脂肪酸盐与H3PO4和/或H2SO4接触,任选地减少该组合物中该皂/脂肪酸盐的量;
v)通过使游离脂肪酸和/或脂肪酸原料与醇在一种或多种非酶催化剂的存在下进行反应产生脂肪酸烷基酯,进一步减少在该油相/轻相中的所述游离脂肪酸的量和任选地所述脂肪酸原料的量;并且
vi)纯化和/或蒸馏脂肪酸烷基酯,包括在步骤v)中产生的脂肪酸烷基酯。
在根据本发明的其他具体实施例中,它们在图2中被示为“选项2”,该方法包括
i)提供一种组合物,该组合物包含
a.含有脂肪酸烷基酯、游离脂肪酸和任选地脂肪酸原料的油相/轻相;以及
b.含有醇和水的水相/重相;
ii)将所述组合物中水的量降低例如至按该水相/重相的重量计的0-15%的范围内;
iii)通过使游离脂肪酸和/或所述脂肪酸原料与醇以及一种或多种液体脂肪分解酶进行反应产生脂肪酸烷基酯,减少在该油相/轻相中的所述游离脂肪酸的量和任选地所述脂肪酸原料的量;
iv)在允许从油相/轻相中的剩余游离脂肪酸形成皂/盐的条件下,使该组合物与一种或多种碱性试剂接触;
v)将含有该脂肪酸烷基酯的该油相/轻相与该亲水相/重相分离;并且
vi)纯化和/或蒸馏脂肪酸烷基酯,包括在步骤iii)中产生的脂肪酸烷基酯。
在根据本发明的仍其他具体实施例中,它们在图2中被示为“选项3”,该方法包括
i)提供一种组合物,该组合物包含
a.含有脂肪酸烷基酯、游离脂肪酸和任选地脂肪酸原料的油相/轻相;以及
b.含有醇和水的水相/重相;
ii)将所述组合物中水的量降低例如至按该水相/重相的重量计的0-15%的范围内;
iii)通过使游离脂肪酸和/或所述脂肪酸原料与醇以及一种或多种液体脂肪分解酶进行反应产生脂肪酸烷基酯,减少在该油相/轻相中的所述游离脂肪酸的量和任选地所述脂肪酸原料的量;
iv)通过使皂/脂肪酸盐进行酸化来产生游离脂肪酸,如通过使该皂/脂肪酸盐与H3PO4和/或H2SO4接触,任选地降低该组合物中该皂/脂肪酸盐的量。
v)将含有该脂肪酸烷基酯的该油相/轻相与该亲水相/重相分离;
vi)通过使游离脂肪酸和/或脂肪酸原料与醇在一种或多种非酶催化剂的存在下进行反应产生脂肪酸烷基酯,进一步减少在该油相/轻相中的所述游离脂肪酸的量和任选地所述脂肪酸原料的量;并且
vii)纯化和/或蒸馏脂肪酸烷基酯,包括在步骤iii)和vi)中产生的脂肪酸烷基酯。
在本发明的仍另外的实施例中,它们在图2中被示为“选项4”,该方法包括
i)提供一种组合物,该组合物包含
a.含有脂肪酸烷基酯、游离脂肪酸和任选地脂肪酸原料的油相/轻相;以及
b.含有醇和水的水相/重相;
ii)将所述组合物中水的量降低例如至按该水相/重相的重量计的0-15%的范围内;
iii)通过使游离脂肪酸和/或所述脂肪酸原料与醇以及一种或多种液体脂肪分解酶进行反应产生脂肪酸烷基酯,减少在该油相/轻相中的所述游离脂肪酸的量和任选地所述脂肪酸原料的量;
iv)通过使皂/脂肪酸盐进行酸化来产生游离脂肪酸,如通过使该皂/脂肪酸盐与H3PO4和/或H2SO4接触,任选地减少该组合物中该皂/脂肪酸盐的量;
v)将含有该脂肪酸烷基酯的该油相/轻相与该亲水相/重相分离;
vi)通过使游离脂肪酸和/或脂肪酸原料与醇在一种或多种非酶催化剂的存在下进行反应产生脂肪酸烷基酯,进一步减少在该油相/轻相中的所述游离脂肪酸的量和任选地所述脂肪酸原料的量;
vii)在允许从油相/轻相中的剩余游离脂肪酸形成皂/盐的条件下,使该组合物与一种或多种碱性试剂接触;并且
viii)纯化和/或蒸馏脂肪酸烷基酯,包括在步骤iii)和vi)中产生的脂肪酸烷基酯。
通过以下实例进一步描述本发明,所述实例不应理解为对本发明的范围进行限制。
实例
实例1:混合精制方法,1L规模
目的:
目的是测试并开发一种可以大规模实施的产率>97%的简单的方法。本文开发的方法是基于在苛性洗涤步骤之前通过额外的液体酶步骤提高FFA的转化。
程序:
1.无机酸中和步骤
a.将770g干RBD大豆油加热至35C/95F,并添加20ppm NaOH呈1N溶液≈0.385g苛性溶液。以530rpm混合15分钟。
b.加水:添加总共2%水(包括苛性溶液)≈15,0g水,混合15分钟。
2.酶促反应。
a.将脂肪酶(具有SEQ ID NO:2中所示的氨基酸序列的脂肪酶)添加分为两次剂量:在0h时间处的0.2%w/w以及在23h时间处的0.1%添加,分别约等于1.54ml和0.77ml。
b.总甲醇剂量为1.5当量,从在0h时间添加21ml开始,在第一个20h内连续添加100ml,并在26.5h时添加14ml。反应进行32小时,目标为<0.5%BG。最终的QTA读数:BG=0.38%,FFA(滴定)=1.5%酯交换过程中三酰甘油、游离脂肪酸等的变化如图3所示。
3.加热和干燥
a.将反应混合物加热至105C/220F持续1小时,然后冷却并在真空(终点22毫巴)和45C/113F下干燥1小时。重相测量(QTA):水15%、甲醇3.3%、MONG 4.4%。
b.将混合物加热至80C/180F并干燥(终点20毫巴)1小时。重相测量(QTA):水9.9%、甲醇0.1%、MONG 0.0%。
4.用脂肪酶(具有SEQ ID NO:2所示的氨基酸序列的脂肪酶)进行的酶促精制反应
a.将干燥的混合物冷却至35C/95F并添加0.075%脂肪酶≈0.50ml并以530rpm混合
b.总甲醇为3.5%w/w。将给予分为6个剂量:在t=0和t=1.5h时各10ml,以及在3h、5.5h、6.5h和23.5h时各5ml。反应进行24.5小时。终点FFA(滴定)=0.8%
显示酶促精制过程中FFA降低的QTA分析数据呈现于图4中。
5.苛性洗涤
将混合物加热至60C/140F并且添加1.5当量NaOH(相对于FFA含量)。添加苛性碱为在甲醇(=62%浓度)和水中的3.2%w/w溶液。总共添加在760g混合物中的40g苛性溶液。以530rpm混合2小时。最终FFA(滴定)<0.1%并且BG=0.2%。油相和重相的QTA分析示于图5中。
6.沉降、洗涤和干燥
a.重力沉降30min。
b.通过用4%v/v水喷雾来进行静态水洗涤,然后搅拌30min
c.沉降并倾析。
d.将FAME相在100C/212F下干燥30min。QTA测量(B100):
i.酸值:0.05
ii.MAG:0.4%
iii.DAG:0.27%
iv.TAG:0.01%
v.BG:0.19%
vi.总甘油:0.21%
7.通过酸化估计产量损失
a.将10g清澈的甘油相添加到0,73ml 4N HCl中并伴随摇动加热至100C持续30min。
b.以1500rpm在22C下离心30min。
c.通过移液管吸出甘油相。
d.油相的重量等于0.7g
e.产量损失估计:
i.总重相170g
ii.在重相中的油量:0.7/10X 170=11.9g
iii.总产量损失:11.9g油相对于770g油等于=1.5%
8.通过QTA测量估计产量损失
a.产量损失估计:
i.总重相170g
ii.在重相中的总MONG含量=11%MONG等于11/100*170=18.7g油
iii.总产量损失:18.7g油相对于770g油等于=2.4%
结论:
以上试验成功地提供了97%-99%的总产量。用来自RBD大豆油的干燥的模型底物粗制FAME、0.075%脂肪酶(具有SEQ ID NO:2所示的氨基酸序列)和添加3.5%甲醇的酶促精制反应,在最终一锅法苛性处理之前的24小时内使FFA从1.5%降低至0.8%。
实例2:在粗制棕榈油上进行树脂精制
目的:
为了研究不同的树脂精制参数,如柱高、甲醇剂量、反应温度和在CPO FAME中的FFA,以实现最终FFA为<0.25%。
第1部分:对1.3%原料FFA用0.4m、0.8m和1.2m高度树脂进行精制
a)在80℃下,在15%的无水甲醇和0.4米柱高下,FFA可以从1.3%降低至平均0.54%。
b)在80℃下,在20%的无水甲醇和0.8米柱高下,FFA可以从1.3%降低至平均0.45%,而1.2米柱高能将FFA降低至平均0.37%。
c)在90℃下,在20%的无水甲醇和1.2米柱高下,在流量为4.3床体积/hr下,FFA从1.3%降低至0.24%(平均3kg FAME通过树脂床)。
第2部分:对2%原料FFA用1.2m柱高进行精制
a)在90℃下,在20%的无水甲醇和1.2米柱高下,FFA能够从2%降低至平均0.45%,并且第二次通过后进一步降低至0.28%-0.31%。
b)用更高的柱可以实现目标FFA。
材料
底物:从ELN-14-PSSH-0008累积的CPO FAME(FFA~1.3%)
树脂:来自朗盛公司的Lewatit GF 101(CHT00077)
化学品:无水的甲醇(最大0.005%H2O)(默克公司(Merck)代码:1.06012.2500)
方法学
1.将树脂用80℃去离子水洗涤以去除杂质,之后填充到25mm直径×250mm高度的玻璃柱(总共0.4米树脂高度)。
2.将无水的甲醇在90℃下通过树脂柱进行泵送以将树脂中的水分降至0.1%的水分,之后进行实际的精制试验。
3.将85%的CPO和15%或20%的MeOH的混合物在60℃水浴中进行孵育,之后通过树脂进行泵送。
4.测量收集的样品的水分%,之后蒸发甲醇进行FFA分析。
5.在几个参数上进行进一步的试验,如甲醇剂量(15%和20%)、温度(80℃和90℃)、柱高(0.4m、0.8m和1.2m)和在原料FAME中的不同FFA(1.3%和2%)。
结果与讨论
第1部分:对1.3%的原料FFA用0.4m、0.8m和1.2m柱高进行精制
表1:用0.4米柱高进行树脂精制后的结果
最初,树脂被填装在2个尺寸为25mm直径×250mm柱高的玻璃柱中。这可以填充多达20g树脂/柱并且床高为20cm/柱。在这种情况,1.4升(1.1kg)无水甲醇通过树脂柱,水分在1hr内从35.3%降低至0.065%(目标:<0.1%水分)
将具有1.3%FFA和0.011%水分的CPO FAME与15%无水甲醇混合为85%作为精制试验的原料。尝试了不同的设置,如树脂温度、甲醇%和床体积流量,以使FFA从1.3%降低至0.25%。然而,用如表1所述的参数,FFA只能降低至0.44%。这表明树脂床高度必须是至少1米用于更好的转化高度。
因此,FFA降低的失败可能是由于水族箱中树脂设置的高度不足造成的,因此为了更好的转换,将来自0.4米树脂高度的2个大柱(25mm直径x250mm高度)的预处理树脂转移到分别为0.8米和1.2米高度的4个和6个小柱(10mm直径x 250mm高度)上。
表2:0.8米高的树脂精制后的结果(水族箱在80℃)
表3:1.2米高的树脂精制后的结果(水族箱在80℃)
所有用0.8米和1.2米柱高的试验都是在80℃进行的。参考表2,用0.8米柱高时FFA只能降低至0.36%,而表3显示使用80%CPO FAME和20%甲醇作为原料,1.2米柱高能够将FFA从1.3%降低至0.22%。FAME+甲醇与树脂的比约为4个床体积。
使用1.2米柱高、原料中20%甲醇和流速为4.3个床体积/hr,将水族箱温度升高到最高90℃。如图6所示,FFA从1.3%降低至0.24%(平均3kg FAME通过树脂床)。树脂处理后的FFA范围为(0.17%-0.30)%。干燥FAME样品的原料,之后添加无水甲醇。水分含量为约0.02%。
参考图7,树脂处理后FAME的水分平均为0.24%。在树脂处理后测试水分,之后蒸发甲醇/水分进行FFA分析。通过化学计量计算,1%棕榈酸FFA转化为FAME将产生0.07%的水分。测得的较高水分含量可能是由于生物柴油在周围环境中吸收水分所致。
第2部分:对2%原料FFA用1.2m树脂高度进行精制
使用相同的1.2米树脂高度和90℃水族箱温度,测试原料中更高的原料FFA(2%)和甲醇(80%:20%)。如图8所示,在第一轮树脂精制之后系统能够将FFA从2%降低至0.45%(平均)。从包括18%-19%甲醇的第一轮精制收集的FAME第二次通过树脂。然后,系统能够将FFA从0.45%(平均)降低至0.28%-0.31%。
图9显示当FFA从2%降低至0.45%时,FAME中的水分为0.27%(平均)。FFA进一步从0.45%降低至0.3%导致水分增加至0.36%(平均)。收集的样品中的水分增量可能是由于从湿气吸水。
结论
表4:对FFA精制的简短的总结概述
本文描述和要求保护的本发明不限于本文披露的特定方面的范围,因为这些方面旨在作为本发明若干方面的说明。任何等同方面意欲在本发明的范围之内。实际上,除了本文所示和描述的那些之外,对于本领域的技术人员而言本发明的各种修改将从前述的说明书变得显而易见。此类修改也旨在落入所附权利要求书的范围内。在冲突的情况下,以包括定义的本披露为准。
序列表
<110> 诺维信公司
<120> 酶或非酶生物柴油精制方法
<130> 14004-WO-PCT
<160> 2
<170> PatentIn版本3.5
<210> 1
<211> 269
<212> PRT
<213> 疏棉状嗜热丝孢菌
<400> 1
Glu Val Ser Gln Asp Leu Phe Asn Gln Phe Asn Leu Phe Ala Gln Tyr
1 5 10 15
Ser Ala Ala Ala Tyr Cys Gly Lys Asn Asn Asp Ala Pro Ala Gly Thr
20 25 30
Asn Ile Thr Cys Thr Gly Asn Ala Cys Pro Glu Val Glu Lys Ala Asp
35 40 45
Ala Thr Phe Leu Tyr Ser Phe Glu Asp Ser Gly Val Gly Asp Val Thr
50 55 60
Gly Phe Leu Ala Leu Asp Asn Thr Asn Lys Leu Ile Val Leu Ser Phe
65 70 75 80
Arg Gly Ser Arg Ser Ile Glu Asn Trp Ile Gly Asn Leu Asn Phe Asp
85 90 95
Leu Lys Glu Ile Asn Asp Ile Cys Ser Gly Cys Arg Gly His Asp Gly
100 105 110
Phe Thr Ser Ser Trp Arg Ser Val Ala Asp Thr Leu Arg Gln Lys Val
115 120 125
Glu Asp Ala Val Arg Glu His Pro Asp Tyr Arg Val Val Phe Thr Gly
130 135 140
His Ser Leu Gly Gly Ala Leu Ala Thr Val Ala Gly Ala Asp Leu Arg
145 150 155 160
Gly Asn Gly Tyr Asp Ile Asp Val Phe Ser Tyr Gly Ala Pro Arg Val
165 170 175
Gly Asn Arg Ala Phe Ala Glu Phe Leu Thr Val Gln Thr Gly Gly Thr
180 185 190
Leu Tyr Arg Ile Thr His Thr Asn Asp Ile Val Pro Arg Leu Pro Pro
195 200 205
Arg Glu Phe Gly Tyr Ser His Ser Ser Pro Glu Tyr Trp Ile Lys Ser
210 215 220
Gly Thr Leu Val Pro Val Thr Arg Asn Asp Ile Val Lys Ile Glu Gly
225 230 235 240
Ile Asp Ala Thr Gly Gly Asn Asn Gln Pro Asn Ile Pro Asp Ile Pro
245 250 255
Ala His Leu Trp Tyr Phe Gly Leu Ile Gly Thr Cys Leu
260 265
<210> 2
<211> 269
<212> PRT
<213> 人工序列
<220>
<223> 脂肪酶变体
<400> 2
Glu Val Ser Gln Asp Leu Phe Asn Gln Phe Asn Leu Phe Ala Gln Tyr
1 5 10 15
Ser Ala Ala Ala Tyr Cys Gly Lys Asn Asn Arg Ala Pro Ala Gly Thr
20 25 30
Asn Ile Thr Cys Thr Ala Asn Ala Cys Pro Glu Val Glu Lys Ala Asp
35 40 45
Ala Thr Phe Leu Tyr Ser Phe Glu Asp Ser Gly Val Gly Asp Val Thr
50 55 60
Gly Phe Leu Ala Leu Asp Asn Thr Asn Lys Leu Ile Val Leu Ser Phe
65 70 75 80
Arg Gly Ser Arg Ser Ile Glu Asn Trp Ile Gly Asn Leu Asn Phe Glu
85 90 95
Leu Lys Glu Ile Asn Asp Ile Cys Ser Gly Cys Arg Gly His Ala Gly
100 105 110
Phe Thr Ser Ser Trp Arg Ser Val Ala Asp Thr Leu Arg Gln Lys Val
115 120 125
Glu Asp Ala Val Arg Glu His Pro Asp Tyr Arg Val Val Phe Thr Gly
130 135 140
His Ser Leu Gly Gly Ala Leu Ala Thr Val Ala Gly Ala Asp Leu Arg
145 150 155 160
Gly Asn Lys Tyr Asp Ile Asp Val Phe Ser Tyr Gly Ala Pro Arg Val
165 170 175
Gly Asn Arg Ala Phe Ala Glu Phe Leu Thr Val Gln Thr Gly Gly Thr
180 185 190
Leu Tyr Arg Ile Thr His Thr Asn Asp Ile Val Pro Arg Leu Pro Pro
195 200 205
Arg Glu Phe Gly Tyr Ser His Ser Ser Pro Glu Tyr Trp Ile Lys Ser
210 215 220
Gly Thr Leu Val Pro Val Arg Arg Arg Asp Ile Val Lys Ile Glu Gly
225 230 235 240
Ile Asp Ala Thr Gly Gly Asn Asn Gln Pro Asn Ile Pro Ser Ile Thr
245 250 255
Ala His Leu Trp Tyr Phe Gly Leu Ile Gly Thr Cys Leu
260 265
- 还没有人留言评论。精彩留言会获得点赞!